Psychotherapie
Uitgangsvraag
Wat is de plaats van psychotherapie bij aanhoudende klachten na licht THL?
Aanbeveling
- Pas psychotherapeutische interventies toe bij patiënten met aanhoudende klachten na licht THL en een bijkomende of overlappende psychische stoornis, zoals een angst- of stemmingsstoornis of een post-traumatische stressstoornis, conform de daarvoor geldende richtlijnen.
- Overweeg om middels ‘Diagnostiek volgens het Gevolgenmodel’ de factoren in kaart te brengen die de lichamelijke of cognitieve klachten beïnvloeden en stel een individueel behandelplan op met (psychotherapeutische) interventies om deze factoren op te heffen.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Het doel van deze uitgangsvraag was om te achterhalen wat de toegevoegde waarde van psychotherapeutische interventies bij patiënten met aanhoudende klachten na licht THL. De evidentie bestaat uit een enkele systematische review naar de effecten van CGT waarin slechts twee RCTs een interventie (bestaande uit cognitieve gedragstherapie) onderzochten in de chronische fase. Bewijs voor effect van CGT op de kritieke uitkomstmaten (symptomen en klachten) was laag tot zeer laag, en op de belangrijke uitkomstmaten (angst, stemming, vermoeidheid, participatie en kwaliteit van leven) eveneens zeer laag tot niet aanwezig. Mogelijk kunnen andere studies leiden tot nieuwe inzichten. De werkzaamheid van andere psychotherapeutische methoden zoals ACT (Acceptance and Commitment Theory) is tot nu toe niet systematisch onderzocht in patiënten met licht THL in de chronische fase.
Daarom kunnen er nu op basis van de literatuur geen harde conclusies geformuleerd worden.
Aangezien de interventies op groepsniveau geanalyseerd zijn kan niet worden uitgesloten dat CGT voor individuele patiënten effectief is. Er is geen reden om bijwerkingen te verwachten van deze interventie. Thans bestaan er geen psychotherapeutische alternatieven voor CGT die meer evidence-based zijn binnen deze populatie. Bovendien is CGT effectief bevonden voor de behandeling van angst- en stemmingsstoornissen in de reguliere populatie. Voor individuele patiënten met aanhoudende klachten na licht THL en bijkomende angst- of stemmingsstoornissen kan CGT daarom als interventie worden ingezet. Verder valt te overwegen om als interventie ACT (Acceptance and Commitment Therapy) aan te bieden. Een recente casestudie (Rauwenhoff, 2022) suggereert dat dit effectief kan zijn bij patiënten met aanhoudende klachten na licht THL en een bijkomende depressieve of angststoornis.
Tot slot is traumabehandeling in de vorm van CGT of EMDR (Eye Movement Desensitization Reprosessing) geïndiceerd bij patiënten met licht THL en een bijkomende post-traumatische stress stoornis (PTSS). Onderzoek laat zien dat PTSS in bovengemiddelde mate voorkomt bij mensen met aanhoudende klachten na licht THL en dat een deel van de gerapporteerde klachten met elkaar overlappen. In een recente studie in de acute fase na licht THL worden positieve effecten gevonden van EMDR-therapie, waarbij patiënten 3 maanden later zowel minder LICHT THL-klachten rapporteerden als PTSS-klachten, vergeleken met patiënten die usual care hadden gehad of alleen extra werden gerustgesteld (Gil-Jardiné, 2018). De effectiviteit van EMDR in de chronische fase na licht THL is nog niet onderzocht.
Bij gebrek aan onderzoek voor deze specifieke populatie patiënten met aanhoudende klachten na licht THL kan gebruik gemaakt worden van de richtlijn SOLK en somatoforme stoornissen . Binnen deze zorgstandaard wordt er een onderscheid gemaakt tussen mensen met en zonder comorbide psychische stoornissen. Indien er sprake is van comorbide psychische stoornissen, zoals een angststoornis, een depressie of slaapstoornis (insomnie), kunnen psychotherapeutische behandelingen worden ingezet volgens de daarvoor geldende richtlijnbehandelingen. Indien er geen sprake is van psychische stoornissen en de lichamelijke of cognitieve klachten op de voorgrond staan, is het zinvol om factoren in kaart te brengen die de lichamelijke of cognitieve klacht beïnvloeden of verergeren. Een systematische methode om deze factoren in kaart te brengen bij een individuele patiënt is ‘Diagnostiek volgens het gevolgenmodel’ (van Rood & de Roos, 2017). Deze methode is nog niet onderzocht bij patiënten met aanhoudende klachten na licht THL, maar blijkt in de praktijk goed bruikbaar. Het product van deze methode is een vicieuze cirkel dat weergeeft hoe bepaalde factoren of gedragingen van de patiënt bijdragen aan de lichamelijke of cognitieve klacht. Op basis van de vicieuze cirkel wordt een individueel behandelplan opgesteld, dat afhankelijk van het in standhoudende (gedrags)patroon kan bestaan uit verschillende psychotherapeutische interventies (o.a. CGT, ACT, EMDR). Wanneer een patiënt zich bijvoorbeeld overbelast vanuit perfectionisme en hoge eisen dan kan CGT worden ingezet op het bewerken van disfunctionele cognities en het aanpassen van het gedragspatroon. Indien een patiënt juist veel piekert en catastroferende gedachten heeft over de klachten, dan is het van belang om dit te verminderen middels CGT of ACT. Bij een deel van de patiënten is het vrees-vermijdingsmodel van toepassing en ligt exposure als interventie voor de hand. Hiervoor wordt ook verwezen naar de module over Exposure, waar de effectiviteit van exposure uitgebreider wordt besproken. Het ‘op maat’ behandelen op basis van symptomen en gedragspatronen van patiënten met licht THL wordt onderschreven door een recent review artikel (Mollica, 2022) en de eerste interventiestudies hiernaar worden op dit moment uitgevoerd.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Wanneer patiënten met aanhouende klachten m.b.t. depressie of angst na licht THL ervaren is het wenselijk om patiënten zelf mee te laten beslissen in het kiezen voor een psychotherapeutische interventie (zoals CGT, ACT). Wanneer deze klachten niet op de voorgrond staan maar patiënten wel chronische cognitieve, somatische of vermoeidheidsklachten ervaren is het de vraag of zij de meerwaarde inzien van een psychotherapeutische interventie. In dat geval is het aan de behandelaar hier een patient goed in mee te nemen. Hierbij kan gebruik gemaakt worden van communicatieadviezen binnen de zorgstandaard ALK. Het is met name van belang dat patiënten erkenning krijgen voor hun klachten en dat deze niet als ‘psychisch’ worden gelabeld. Wel kan een psychotherapeutische interventie mogelijk bijdragen ten aanzien van het verminderen van de lijdenslast, danwel het verminderen van de licht THL gerelateerde klachten zelf.
Kosten (middelenbeslag)
Momenteel ontbreekt wetenschappelijk onderzoek naar de effectiviteit en kosteneffectiviteit van psychotherapie, specifiek bij deze doelgroep. Het aantal en de frequentie van de therapiesessies zijn onbekend, waardoor nog geen inschatting gemaakt kan worden van de kosten(effectiviteit). Indien er sprake is van een psychische stoornis (bijv. angststoornis, depressie, PTSS), dan vindt vaak reguliere behandeling binnen de GGZ plaats. Het is onbekend in hoeverre patiënten met licht THL én een psychische stoornis al behandeld worden binnen de GGZ en of de aanbevelingen tot een toename aan kosten zullen leiden.
Aanvaardbaarheid, haalbaarheid en implementatie
Er is geen onderzoek gedaan naar de aanvaardbaarheid en haalbaarheid van psychotherapeutische interventies binnen de chronische fase na licht THL. Binnen de reguliere populatie zijn kortdurende, klachtgerichte psychotherapieën zoals CGT, ACT en EMDR, aanvaardbaar en haalbaar gebleken met relatief weinig drop-outs.
Psychotherapeutische interventies zijn met name onderzocht binnen algemene of psychiatrische populaties met een laaggemiddeld tot hoog opleidingsniveau. Om te profiteren van dergelijke therapieën zijn wel bepaalde taal- en intellectuele vaardigheden en zelfredzaamheid vereist. Hoewel aanpassingen gemaakt kunnen worden voor mensen met een laag intelligentieniveau, is dit in de praktijk niet altijd haalbaar. Ook is een enigszins stabiele thuissituatie/ omgeving wenselijk. Indien sociaal-economische problemen op de voorgrond staan kan worden overwogen hier eerst aandacht aan te besteden.
Een belangrijke belemmerende factor voor de besluitvorming of implementatie is het gebrek aan kennis over deze specifieke doelgroep (patiënten met aanhoudende klachten na licht THL) en hoe en bij wie precies psychotherapeutische behandelingen kunnen bijdragen aan het verminderen van klachten. Er is behoefte aan een netwerk van (neuro)psychologen met expertise op dit gebied en een bijpassend scholingsaanbod. De psychotherapeutische behandelingen zelf zijn niet voorbehouden aan (klinisch) neuropsychologen en kunnen door GZ-psychologen worden uitgevoerd. Echter, kennis van en ervaring met NAH bij GZ-psychologen is vereist om het onderscheid te kunnen maken tussen cognitieve stoornissen passend bij NAH en cognitieve klachten die in stand worden gehouden door andere factoren, en dus om een goede behandeling te indiceren. De patiënten met licht THL hebben meestal geen (ernstige) cognitieve stoornissen, maar klachten van overprikkeling of cognitieve klachten. Psychotherapie hoeft daarom in de basis niet aangepast worden. Bij geheugenklachten kan wel het gebruik van geheugenstrategieën of hulpmiddelen (bijv. agenda, notitieblok) worden aangemoedigd om de uitleg en afspraken omtrent de psychotherapeutische behandeling vast te leggen. Daarnaast is het van belang om psychotherapeutische interventies af te stemmen met andere zorgprofessionals betrokken bij de patiënt, zodat alle betrokkenen een eenduidige klachtenbenadering hanteren. In de multidisciplinaire revalidatiezorg is deze afstemming goed ingebed, maar binnen de eerste lijn is de zorg vaak nog versnipperd met daarbij risico op tegenstrijdige informatie. Zorgverleners die een ander verklaringsmodel aanhouden en een andere benaderingswijze hanteren kunnen de potentiële effecten van psychotherapeutische interventies soms tenietdoen.
Aanbevelingen
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Bij een gebrek aan onderzoek en daarmee bewijs voor de effecten van psychotherapeutische behandelingen bij mensen met aanhoudende klachten na licht THL is gekozen om een parallel te trekken met andere doelgroepen patiënten met Aanhoudende Lichamelijke Klachten (ALK). Psychotherapeutische interventies worden daar voornamelijk ingezet op overlappende psychische stoornissen of op factoren die de lichamelijke klachten beïnvloeden, danwel verergeren. Binnen de licht THL doelgroep is er de laatste jaren steeds meer bekend over het ontwikkelen en in stand houden van klachten in de chronische fase na LICHT THL. Zo zijn er subgroepen bekend van mensen met een hoge lijdensdruk (met vaak een angst- of stemmingsstoornis) en mensen zonder hoge psychische lijdensdruk, met voornamelijk veel lichamelijke en cognitieve klachten (Rakers, 2021). Daarnaast is op basis van eerder onderzoek bekend dat een passieve copingstijl, catastroferen (angst-vermijdingsmodel), emotionele lijdensdruk en psychische klachten van voor het ongeval voorspellend zijn voor het ontwikkelen van aanhoudende klachten na licht THL (van der Naalt, 2017). In de praktijk worden veel individuele verschillen in gedragspatronen gezien die de klachten kunnen verergeren. Waar de ene patiënt heel angstig wordt van klachten en activiteiten die klachten oproepen vermijdt, is een andere patiënt juist gefrustreerd en is er sprake van overbelasting in activiteiten, met een toename van klachten tot gevolg. Vanwege deze subgroepen en individuele verschillen is een ‘one size fits all’ benadering niet op zijn plaats, wat mogelijk verklaart waarom groepstudies naar de effectiviteit van een specifieke psychotherapeutische behandeling (zoals CGT) beperkte effecten laten zien. Een logische vervolgstap is om psychotherapeutische interventies op maat in te zetten, gericht op overlappende psychische stoornissen of op de factoren die de klachten beïnvloeden of verergeren bij een individuele patiënt (Mollica, 2022). Vanzelfsprekend is het van belang om verder onderzoek te doen naar het ‘op maat’ behandelen, eventueel met interventies voor verschillende subgroepen. De eerste studies hiernaar worden op dit moment uitgevoerd of opgestart (Silverberg, 2022; Naess-Schmidt, 2022). Een bruikbare methode om op een systematische manier bij een individuele patiënt factoren in kaart te brengen die bijdragen aan de lichamelijke klacht, is ‘Diagnostiek volgens het Gevolgenmodel’ (van Rood & de Roos, 2017).
Binnen de licht THL-populatie is er onvoldoende evidentie voor de effecten van psychotherapie in de chronische fase, voornamelijk door gebrek aan onderzoek. Wel zijn er op basis van praktijkervaringen en pilotstudies eerste aanwijzingen dat psychotherapie effectief is voor individuele patiënten (o.a. CGT, ACT, EMDR). Er zijn bovendien geen argumenten tegen de toepassing van psychotherapeutische behandelingen bij patiënten met aanhoudende klachten na licht THL. Psychotherapie is effectief bevonden voor veel bekende psychische stoornissen (o.a. angst en depressie) en er is geen reden om aan te nemen dat het behandelen van deze psychische stoornissen binnen de licht THL-populatie niet effectief zou zijn. Er zijn daarnaast geen bijwerkingen bekend en de behandeling kan elk moment worden afgebroken. Het heeft de voorkeur om psychotherapeutische interventies toe te passen boven de standaardzorg of geen interventie. Wel is het van belang om tussentijds goed te evalueren en effecten te monitoren. Daarnaast is het van belang om psychotherapeutische interventies goed af te stemmen met andere zorgprofessionals die betrokken zijn bij de patiënt.
Onderbouwing
Verschillende onderzoeken tonen aan dat psychologische factoren, zoals een passieve copingstijl, catastroferen en psychische problemen vóór het oplopen van het licht traumatisch hersenletsel (licht THL) een rol spelen bij het ontwikkelen van aanhoudende klachten na licht THL. Mede vanwege deze factoren, of in samenhang met het oplopen van een licht THL kunnen patiënten naast licht THL gerelateerde klachten ook angst- en depressieve klachten ontwikkelen, waarvoor psychotherapie geïndiceerd zou kunnen zijn. Veelgebruikte therapievormen zijn cognitieve gedragstherapie (CGT), Acceptance and Commitment Therapy (ACT), Mindfulness Based Cognitive Therapy (MBCT) en Eye-Movement Desensitization and Reprocessing therapie (EMDR). Voor al deze vormen van psychotherapie geldt dat ze evidence based zijn; ze zijn aangetoond werkzaam voor psychische problemen zoals depressie, angst of posttraumatische stress. Tot nu toe ontbreekt echter een duidelijk overzicht van welke vormen van psychotherapie effectief zijn specifiek bij patiënten met aanhoudende klachten na licht THL. Welke therapievormen zijn wetenschappelijk bewezen effectief in deze groep en voor welke klachten precies? Een dergelijk overzicht is van belang voor de dagelijkse klinische praktijk om patiënten met aanhoudende klachten na licht THL gericht door te kunnen verwijzen.
1. Symptoms and complaints (critical)
|
Low GRADE |
Psychotherapy offered in the chronic stage (> 3 months) post mTBI may result in little to no difference in symptoms and complaints when compared with placebo/usual care/no treatment in patients after mTBI.
Sources: Kjeldgaard, 2014 and Storzbach, 2017 |
2. Anxiety (important)
|
Low GRADE |
Psychotherapy offered in the chronic stage (> 3 months) post mTBI may result in little to no difference in anxiety when compared with placebo/usual care/no treatment in patients after mTBI.
Sources: Kjeldgaard, 2014 |
3. Mood (important)
3.1 Immediate effect
|
Low GRADE |
Psychotherapy offered in the chronic stage (> 3 months) post mTBI may result in little to no difference in mood after completing the intervention when compared with placebo/usual care/no treatment in patients after mTBI.
Sources: Kjeldgaard, 2014 and Storzbach, 2017 |
3.2 Short-term effect
|
Low GRADE |
Psychotherapy offered in the chronic stage (> 3 months) post mTBI may result in little to no difference in mood within 3 months after completing the intervention when compared with placebo/usual care/no treatment in patients with mTBI.
Sources: Storzbach, 2017 |
3.3 Long-term effect
|
No GRADE |
No evidence was found regarding the effect of psychotherapy offered in the chronic stage (> 3 months) post mTBI on mood beyond three months after treatment when compared with placebo/usual care/no treatment in patients after mTBI.
Sources: Storzbach, 2017 |
4. Fatigue (important) and
|
No GRADE |
No evidence was found regarding the effect of psychotherapy on fatigue when compared with placebo/usual care/no treatment in patients after mTBI.
Sources: - |
5. Participation (important)
|
Low GRADE |
Psychotherapy may result in little to no difference in participation when compared with placebo/usual care/no treatment, in patients after mTBI.
Sources: Storzbach, 2017 |
6. Quality of life (important)
|
Low GRADE |
Psychotherapy may result in little to no difference of quality of life when compared with placebo/usual care/no treatment, in patients after mTBI.
Sources: Storzbach, 2017 |
Description of studies
Chen (2020) describes a systematic review and meta-analyses of randomized controlled trials (RCTs) about the effects of cognitive behavioral therapy for adults with post-concussion syndrome. A systematic literature search was performed in four English electronic databases (Cochrane Controlled Register of Trials, PubMed, Embase and Medline OVID) from inception to September 15, 2019. RCTs were included if 1) patients were 18 years or older and experienced symptoms of TBI of all severity levels; 2) cognitive behavioral therapy (CBT) was the examined intervention, including a short-term structured process of cognitive reconstruction behavioral therapy and homework assignment; 3) any type of control group was used; 4) primary outcome measures (severity of PCS symptoms, depression, anxiety and social integration) or secondary outcome measures (fatigue, learning ability, executive function, problem solving and quality of life were described). A total of 24 RCT were included in the review of Chen (2020). To answer the PICO of this module, only 2 RCTs were eligible (table 1) since 8 RCTs used other (active) interventions as a comparison and 10 RCTs predominantly included severe TBI patients (Bédard, 2014; Brenner, 2018; Cantor, 2014; Dahlberg, 2007; Fann, 2015; Hsieh, 2012; Mitchell, 2019; Ponsford, 2015; Potter, 2016 and Tiersky, 2005). Furthermore, two trials were excluded due to a sample size <20 (Dawson, 2013 and Simpson, 2011). The evidence of the review was limited due to small treatment effects, publication bias and the small number of studies in the meta-analyses. Furthermore, the included studies had risk of bias, so results should be interpreted with caution.
Tablel 1. Overview of selected RCTs from Chen (2011)
|
Study |
Population |
Interventie type/ duration (n) |
Control (n) |
Outcomes (FU) |
|
Kjeldgaard, 2014 |
Patients with CPTH, attributed to mild head injury, >3 months postinjury |
9 weeks CBT, 2-hour group sessions. (35) |
Inactive, WL (37) |
Symptoms, Mood (immediate) |
|
Storzbach, 2017 |
Veterans, screened positive for mTBI, time postinjury unknown |
10 weeks CCT, 120-minute group-sessions (50) |
Inactive/ usual care (69) |
Symptoms, Mood (immediate, short-term), participation, Quality of life |
|
Abbreviations: CBT; cognitive behavioral therapy, CCT; compensatory cognitive training, CPTH; chronic post-traumatic headache, mTBI; mild traumatic brain injury, WL; wait-list, TAU; treatment as usual. |
||||
Results
1. Symptoms and complaints (critical)
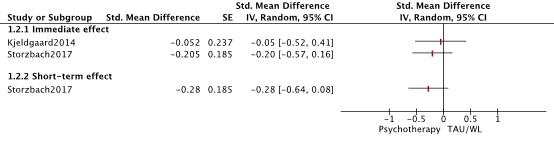
Both RCTs assessed symptom severity (Kjeldgaard, 2014; and Storzbach, 2017; n= 191) . Symptom severity was measured using the Rivermead Post-Concussion Symptoms Questionnaire (RPQ) (Kjeldgaard, 2014) and the Neurobehavioral Symptom Inventory (NSI) (Storzbach, 2017). The analysis by Kjeldgaard (2014) resulted in a standardized mean difference of -0.22 (95%CI -0.68 to 0.24), favoring the psychotherapy group. This difference was not clinically relevant. The analysis by Storzbach (2017) resulted in a standardized mean difference of -0.17 (95%CI -0.53 to 0.20), favoring the psychotherapy group. Results are shown in a forest plot (figure 1).
Figure 1. Forest plot about the effects of psychotherapy on symptoms and complaints.
2. Anxiety (important)
One study assessed the outcome anxiety (Kjeldgaard, 2014). Anxiety was measured using the Symptom Checklist-90-Revised (SCL 90-R) (Kjeldgaard, 2014). The analysis resulted in a standardized mean difference of -0.04 (95%CI -0.50 to 0.43), favoring the psychotherapy group. This difference was not clinically relevant. Results are shown in a forest plot (figure 2).
Figure 2. Forest plot about the effects of psychotherapy on anxiety.
3. Mood (important)
Both RCTs assessed the outcome mood (Kjeldgaard, 2015; and Storzbach, 2017, n=191). Results are shown in a forest plot (figure 3).
3.1 Mood (immediate effect)
Mood after completing the intervention was measured using the BDI-II (Storzbach, 2017) and the Symptom Checklist-90-Revised (SCL-90-R) (Kjeldgaard, 2014). The analysis by Kjeldgaard (2014) resulted in a standardized mean difference of -0.05 (95%CI -0.52 to 0.41), favoring the psychotherapy group. The analysis by Storzbach (2017) resulted in a standardized mean difference of -0.20 (-0.57 to 0.16), favoring the psychotherapy group.
3.2 Mood (short-term effect)
Mood was measured again within 3 months after treatment by Storzbach (2017), using the BDI-II. This analysis resulted in a standardized mean difference of -0.28 (-0.64 to 0.08).
Figure 3. Forest plot about the effects of psychotherapy on mood.
3.3 Mood (long-term effect)
None of the RCTs assessed the effect of psychotherapy on mood on the long term in patients with chronic mTBI.
4. Fatigue (important) and
None of the RCTs assessed the effect of psychotherapy on fatigue in patients with chronic mTBI.
5. Participation (important)
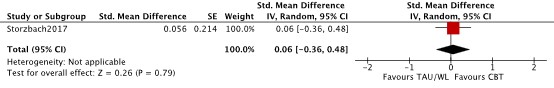
One study measured the outcome participation (Storzbach, 2017). Participation was measured using the University of California, San Diego Performance-Based Skills Assessment-Brief Version (UPSA-B) (Storzbach, 2017). The analysis resulted in a standardized mean difference of 0.06 (95%CI -0.36 to 0.48), favoring the psychotherapy group. This difference was not clinically relevant. Results are shown in a forest plot (figure 4).
Figure 4. Forest plot about the effects of psychotherapy on participation.
6. Quality of life (important)
One study measured measured the outcome quality of life (Storzbach, 2017). Quality of life was measured using the Satisfaction with Life Scale (SLS) (Storzbach, 2017). The analysis resulted in a standardized mean difference of 0.01 (95%CI -0.35 to 0.38), favoring the psychotherapy group. This difference was not clinically relevant. Results are shown in a forest plot (figure 5).
Figure 5. Forest plot about the effects of psychotherapy on quality of life.
Level of evidence of the literature
1. Symptoms and complaints
The level of evidence regarding the outcome symptoms started as high because it was based on an RCT and was downgraded by two levels to low because of high amount of missing data and self-reported outcome without patient blinding (Storzbach, 2017), missing outcome data and deviations from intended interventions in all studies (-1, risk of bias); and the 95% confidence intervals crossed borders of clinical relevance (-1, imprecision).
2. Anxiety
The level of evidence regarding the outcome anxiety started as high because it was based on an RCT and was downgraded by two levels to low because of missing outcome data and deviations from intended interventions (-1, risk of bias) and a low number of included patients (-1, imprecision).
3. Mood
Immediate effects
The level of evidence regarding the outcome mood (immediate effects) started as high because it was based on an RCT and was downgraded by two levels to low because of missing outcome data and deviations from intended interventions (Kjeldgaard, 2014 and Storzbach, 2017) (-1, risk of bias) and a low number of included patients (-1, imprecision).
Short-term effects
The level of evidence regarding the outcome mood (immediate effects) started as high because it was based on an RCT and was downgraded by two levels to low because of missing outcome data and deviations from intended interventions (-1, risk of bias) and the 95% confidence interval crossed a border of clinical relevance (-1, imprecision).
Long-term effects
The level of evidence regarding the outcome measure mood on the long term was not graded because of lack of data.
4. Fatigue
The level of evidence regarding the outcome measures fatigue were not graded because of lack of data.
5. Participation
The level of evidence regarding the outcome participation started as high because it was based on an RCT, and was downgraded by two levels to low because of missing outcome data and deviations from intended interventions (-1, risk of bias) and a low number of included patients (-1, imprecision).
6. Quality of life
The level of evidence regarding the outcome quality of life started as high because it was based on an RCT, and was downgraded by two levels to low because of missing outcome data and deviations from intended interventions (-1, risk of bias); and a low number of included patients (-1, imprecision).
A systematic review of the literature was performed to answer the following question:
What is the effect of psychotherapy after mild traumatic brain injury in patients with remaining complaints after three months on reassurance and insight into the causality of complaints?
P: Patients with remaining complains after mild traumatic brain injury after three months;
I: Psychotherapy;
C: Placebo, usual care, no treatment;
O: Symptoms and complaints, anxiety, mood, fatigue, participation, quality of life.
Relevant outcome measures
The guideline development group considered symptoms and complaints as a critical outcome measure for decision making; and anxiety, mood, fatigue, participation and quality of life as important outcome measures for decision making.
The working group defined the outcome measures as follows:
- Symptoms and complaints: Head Injury Symptom Checklist (HISC), Rivermead Post-Concussion Questionnaire (RPCQ);
- Anxiety: Hospital Anxiety &Depression Scale – Anxiety (HADS-A), Symptom Checklist-Anxiety (SCL-90);
- Mood: Beck Depression Inventory-II (BDI-II), Hospital Anxiety &Depression Scale – Depression (HADS-D), Symptom Checklist-Depression (SCL-20), SCL-90-Revised, Depression Anxiety Stress Scales (DASS), Hamilton Depression Rating Scale (HDRS)
- Fatigue: Fatigue Severity Scale (FSS), Checklist Individual Strength (CIS-20R), Dutch Multifactor Fatigue Scale (DMFS);
- Participation: Social Problem-Solving Inventory-Revised (SPSI-R), Brain Injury Community Rehabilitation Outcome Scales (BICRO-39), Syndney Psychosocial Reintegration Scale (SPRS-2), Community Integration Questionnaire (CIQ), Canadian Occupational Performance Measure (COPM), Participation Objective, Participation Subjective (POPS), University of Californica San Diego Performance-based Skills Assessment (UPSA-B);
- Quality of life: EuroQol 5D (EQ-5D), Life-3, Perceived Quality of Life Scale (PQOL), Satisfaction with Life Scale (SWLS), Quality Of Life after Brain Injury (QOLIBRI), Quality of Life Interview – Brief Version (PQOLI-BV).
The working group defined a standardized mean difference (SMD)/hedge’s G of <-0.5 or >0.5 as a minimal clinically (patient) important difference for each outcome measure.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 1990 until October 12th, 2021.The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 573 hits. Studies were selected based on the following criteria:
- Systematic review and/or meta-analysis, or randomized controlled trial (RCT);
- Included adult patients (18+);
- Described any type of psychotherapy as an intervention;
- Described placebo, usual care or no treatment as a comparison;
- Described at least one of the outcome measures as prescribed in the PICO;
- Included at least 10 patients per treatment arm.
19 studies were initially selected based on title and abstract screening. After reading the full text, 18 studies were excluded (see the table with reasons for exclusion under the tab Methods), and one study was included.
Results
One systematic review was included in the analysis of the literature, from which two RCTs were extracted. Important study characteristics and results are summarized in the evidence table. The assessment of the risk of bias is summarized in the risk of bias table.
- Chen CL, Lin MY, Huda MH, Tsai PS. Effects of cognitive behavioral therapy for adults with post-concussion syndrome: A systematic review and meta-analysis of randomized controlled trials. J Psychosom Res. 2020 Sep;136:110190. doi: 10.1016/j.jpsychores.2020.110190. Epub 2020 Jul 17. PMID: 32712533.
- van der Naalt J, Timmerman ME, de Koning ME, van der Horn HJ, Scheenen ME, Jacobs B, Hageman G, Yilmaz T, Roks G, Spikman JM. Early predictors of outcome after mild traumatic brain injury (UPFRONT): an observational cohort study. Lancet Neurol. 2017 Jul;16(7):532-540. doi: 10.1016/S1474-4422(17)30117-5. Epub 2017 Jun 13. PMID: 28653646.
- Gil-Jardiné C, Al Joboory S, Jammes JTS, et al. Prevention of post-concussion-like symptoms in patients presenting at the emergency room, early single eye movement desensitization, and reprocessing intervention versus usual care: study protocol for a two-center randomized controlled trial. Trials. 2018 Oct;19(1):555. DOI: 10.1186/s13063-018-2902-2. PMID: 30314512; PMCID: PMC6186089.
- Rakers SE, Timmerman ME, Scheenen ME, de Koning ME, van der Horn HJ, van der Naalt J, Spikman JM. Trajectories of Fatigue, Psychological Distress, and Coping Styles After Mild Traumatic Brain Injury: A 6-Month Prospective Cohort Study. Arch Phys Med Rehabil. 2021 Oct;102(10):1965-1971.e2. doi: 10.1016/j.apmr.2021.06.004. Epub 2021 Jul 1. PMID: 34217729.
- Rauwenhoff JCC, Bol Y, Peeters F, van den Hout AJHC, Geusgens CAV, van Heugten CM. Acceptance and commitment therapy for individuals with depressive and anxiety symptoms following acquired brain injury: A non-concurrent multiple baseline design across four cases. Neuropsychol Rehabil. 2022 Mar 25:1-31. doi: 10.1080/09602011.2022.2053169. Epub ahead of print. PMID: 35332849.
- Van Rood YR & De Roos C (2017). Somatisch onvoldoende verklaarde klachten en somatische symptoomstoornissen. In G Keijsers, A Van Minnen, M Verbraak, K Hoogduin & P Emmelkamp (Eds.), Protocollaire behandelingen voor volwassenen met psychische klachten Deel 3(pp 19-61). Amsterdam: Boom.
- Mollica, A., Dey, A., Cairncross, M., Silverberg, N., & Burke, M. J. (2022, February). Neuropsychiatric Treatment for Mild Traumatic Brain Injury: Nonpharmacological Approaches. In Seminars in Neurology. 42(02): 168-181. DOI: 10.1055/s-0041-1742143
- Næss-Schmidt ET, Thastum MM, Stabel HH, Odgaard L, Pedersen AR, Rask CU, Silverberg ND, Schröder A, Nielsen JF. Interdisciplinary intervention (GAIN) for adults with post-concussion symptoms: a study protocol for a stepped-wedge cluster randomised trial. Trials. 2022 Jul 29;23(1):613. doi: 10.1186/s13063-022-06572-7. PMID: 35906645; PMCID: PMC9338593.
- Silverberg ND, Cairncross M, Brasher PMA, Vranceanu AM, Snell DL, Yeates KO, Panenka WJ, Iverson GL, Debert CT, Bayley MT, Hunt C, Baker A, Burke MJ; Canadian Traumatic Brain Injury Research Consortium (CTRC). Feasibility of Concussion Rehabilitation Approaches Tailored to Psychological Coping Styles: A Randomized Controlled Trial. Arch Phys Med Rehabil. 2022 Aug;103(8):1565-1573.e2. doi: 10.1016/j.apmr.2021.12.005. Epub 2021 Dec 28. PMID: 34971596.
Evidence tables
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Chen, 2020 |
SR and meta-analysis of RCTs
Literature search up to September 15th, 2019
A: Kjeldgaard, 2014 B: Storzbach, 2016
Study design: RCT
Setting and Country: Taiwan
Source of funding and conflicts of interest: This research did not receive any specific grant from funding agencies in the public, commercial, or not-for-profit sectors. No competing interests. |
Inclusion criteria SR: Patients 18 years or older who experienced any of the clinically significant symptoms of PCS following TBI of all severity levels were included.
Exclusion criteria SR: Patients with brain injury from any etiology other than trauma were excluded.
2 studies included
Important patient characteristics at baseline:
N, mean age A: 72 patients, age not reported. B: 119 patients, 35.1 yrs.
Sex: A: not reported. B: 5% Female.
Groups comparable at baseline? Yes |
Describe intervention:
A: Cognitive behavioral therapy. B: Cognitive behavioral therapy.
|
Describe control:
A: inactive/ wait-list B: inactive / usual care |
Endpoint of follow-up:
- Short ter (within 3 months) - Mid-term (3-6 months)
For how many participants were no complete outcome data available? (intervention/control) Not reported.
|
Symptoms and complaints Defined as symptom severity measured by the RPQ or the NSI.
Effect measure: standardized mean difference [95% CI]: A: -0.22 [-0.68 – 0.24] in favour of psychotherapy B: -0.17 [-0.53 – 0.20] in favour of psychotherapy.
Anxiety Measured by the SCL 90-R.
Effect measure: standardized mean difference [95% CI]: A: -0.04 [-0.50 – 0.54] in favour of psychotherapy B: not reported
Mood Measured by the BDI-II or the SCL-90-R
Effect measure: standardized mean difference [95% CI]: Immediate effect A: -0.05 [-0.52 – 0.41] in favour of psychotherapy B: -0.20 [-0.57 – 0.16] in favour of psychotherapy.
Short- term A: not reported B: -0.28 [-0.64 – 0.08] in favour of psychotherapy.
Long-term A: not reported B: not reported
Fatigue Not reported.
Participation Measured by the SPSA-B.
Effect measure: standardized mean difference [95% CI]: A: 0.06 [-0.36 – 0.48] in favour of psychotherapy B: not reported
Quality of life Measured by the SLS.
Effect measure: standardized mean difference [95% CI]: A: 0.01 [-0.35 – 0.38] in favour of psychotherapy B: not reported |
Author’s conclusion: integration in patients with TBI. Owing to the small effect sizes in this study, further research is warranted to identify the effective components and optimal mode of delivery of CBT for patients following TBI.
|
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Chen, 2020 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
Yes |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
Arbabi, 2020 |
Absence of meta-analysis |
|
Beedhem, 2020 |
Describes also other interventions (TMS and pharmacotherapy) |
|
Bergersen, 2017 |
Absence of meta-analysis |
|
Cooper, 2015 |
Absence of meta-analysis |
|
Finch, 2016 |
Wrong population (moderate-severe TBI) |
|
Gómez-de-Regil, 2019 |
Wrong study design (descriptive review) |
|
Heslot, 2021 |
Wrong study design (descriptive review) |
|
Jaber, 2019 |
Absence of meta-analysis |
|
Little, 2021 |
Did not include all prescribed outcome measures. |
|
Liu, 2018 |
Wrong population (also moderate-severe TBI patients included) |
|
Minen, 2018 |
Absence of meta-analysis |
|
Möller, 2021 |
Describes also other interventions (interdisciplinary programme, cognitive remediation, cognitive training intervention and supported employment) |
|
Sayegh, 2010 |
Less recent than the other suitable reviews |
|
Snell, 2019 |
Absence of meta-analysis |
|
Sullivan, 2018 |
Study was not up to date (updated in 2020, see below) |
|
Sullivan, 2020 |
Absence of meta-analysis |
|
Teo, 2020 |
Describes also other interventions (cognitive training, psychoeducation) |
|
Xu, 2017 |
Describes also other interventions (cranial electrotherapy, aerobic training, flexyx neurotherapy, Tai Chi, Aquatic physical therapy, combined fitness and strength training, mindfulness-based stress reduction, computerized working memory training, blue light therapy) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 11-03-2024
Beoordeeld op geldigheid : 11-03-2024
Algemene gegevens
In samenwerking met het Nederlands Huisartsen Genootschap.
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Doel en doelgroep
De richtlijn is bestemd voor alle zorgverleners die betrokken zijn bij de diagnostiek, advisering of behandeling bij mensen met langer bestaande klachten (3 maanden) na licht traumatisch hoofd/hersenletsel, met name voor neurologen, revalidatieartsen en paramedici. De NHG-standaard Hoofdtrauma is leidend voor de huisartsen. Naast deze professionals is het van groot belang dat patiënten zelf ook weten waar ze in welk stadium met welke klachten terecht kunnen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten aanhoudende klachten na licht THL.
Werkgroep
- drs. E.W.J. Agterhof, revalidatiearts, VRA
- drs. A. Baars, ergotherapeut, EN
- prof. dr. C.A.M van Bennekom, revalidatiearts/manager, VRA
- dr. N.L. Frankenmolen, i.o. tot klinisch neuropsycholoog, NIP
- drs. P.A.W. Frima-Verhoeven, neuroloog BreinPoli, NVN
- drs. E.A. Goedhart, bondsarts/manager sportgeneeskunde, VSG
- drs. R. Grond, revalidatiearts, VRA
- drs. A. Hansma, huisarts, NHG
- drs. E. Jagersma, revalidatiearts, VRA
- prof. dr. G. Kwakkel, hoogleraar Neurorevalidatie AUMC, KNGF
- drs. S.M. de Lange, bedrijfsarts, NVAB
- mr. M.A.C. Lindhout, Beleidsmedewerker patiëntenvereniging Hersenletstel.nl
- prof. dr. J. van der Naalt, neuroloog, NVN
- prof. dr. R.W.H.M. Ponds, klinisch neuropsycholoog, NIP
- drs. J.M. Schuurman, revalidatiearts, VRA
- prof. dr. J.M. Spikman, klinisch neuropsycholoog, hoogleraar klinische neuropsychologie, NIP
- dr. Melloney Wijenberg, GZ-psycholoog i.o., afdeling neurologie, Adelante, NIP
Met ondersteuning van:
- drs. F. Ham, adviseur Kennisinstituut van de Federatie Medisch Specialisten
- drs. A.A. Lamberts, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Bennekom, van |
Revalidatiearts/ manager R&D, revalidatiecentrum Heliomare te Wijk aan Zee |
Bijzonder hoogleraar revalidatie en arbeid, AUMC te Amsterdam, lid WHR (onbetaald) |
Geen. |
Geen. |
|
Schuurman |
Revalidatiearts Stichting Klimmendaal Revalidatiespecialisten |
Lid WHR (onbetaald) |
Geen. |
Geen. |
|
Jagersma |
Revalidatiearts, Basalt Den Haag |
Voorzitter Werkgroep Hersenletsel Revalidatie (WHR) van de VRA (onbetaalde nevenfunctie) |
Geen. |
Geen. |
|
Agterhof |
Revalidatiearts en medisch manager (0,6 en 0,2) bij de Hoogstraat Revalidatie |
Lid WHR (onbetaald) |
Geen. |
Geen. |
|
Grond |
Revalidatiearts Basalt en HMC (0,4 fte en 0,4 fte). Gedetacheerd vanuit Basalt naar HMC |
Lid stafbestuur Basalt (onbetaald), Lid WHR (onbetaald) |
Geen. |
Geen. |
|
Naalt |
Neuroloog Universitair Medisch Centrum Groningen |
Vanuit expertise in de neurotraumatologie lid van diverse regionale en landelijke commissies, allen onbezoldigd. |
Er is geen financier die belangen heeft bij de uitkomst van de richtlijn. Lopend onderzoek gefinancierd onderzoek door derden betreft:
T-Scemo4all gesubsidieerd door de Hersenstichting: Sociale cognitie en sociaal gedrag verbeteren bij diverse hersenaandoeningen (start 2020). Rol: Medeaanvrager UMCG, nationale multicenter studie.
BRAIN-ReADAPT studie naar het effect van veroudering bij NAH- patienten gesubsidieerd door Zon-MW (start 2021). Rol: PI UMCG, nationale multicenter studie. |
Geen. |
|
Frima-Verhoeven |
Neuroloog bij stichting BreinPoli |
Advies opdrachten bij het CCE, gemiddeld één per anderhalf jaar, betaald. |
Geen. |
Geen. |
|
Goedhart |
Bondarts/ Manager sportgeneeskunde KNVB |
Adviseur Stichting Hersenschudding - onbetaald |
Geen. |
Geen. |
|
Lindhout |
Beleidsmedewerker bij patiëntenvereniging Hersenletstel.nl |
Bestuurslid bij CVA-Kennisnetwerk, onbetaald |
Geen. |
Geen. |
|
Kwakkel |
* Hoogleraar Neurorevalidatie AUMC |
Geen |
Geen. |
Geen. |
|
Hansma |
Huisarts |
Geen |
Geen. |
Geen. |
|
Lange, de |
AIOS bedrijfsgeneeskunde vierde jaar SGBO |
Geen |
Geen. |
|
|
Baars |
Ergotherapeut en mede-eigenaar Plan4 (ergotherapie praktijk in de 1e lijn) |
Voorzitter werkgroep ergotherapie en hersenletsel van Ergotherapie Nederland |
Geen. |
Geen. |
|
Wijenberg |
* Psycholoog, Afdeling Neurologie/ NAH, Adelante Revalidatiecentrum., Hoensbroek 0,8 fte * Docent, Faculty of Psychology and Neuroscience (PFN), Maastrciht University, Maastricht, 0,2 fte |
Bestuurslid Sectie Revalidatie, Nederlands Instituut van Psychologen (NIP), onbetaald
Ik geef les over neuropsychologische onderwerpen vanuit mijn functie als psycholoog bij Adelante (Adelante ontvangt hier een compensatie voor). Dit verricht ik voor meerdere partijen w.o. RINO Zuid, Pro-Education, Maastiricht Univeristy |
Geen. |
Geen. |
|
Frankenmolen |
* GZ-psycholoog in opleiding tot klinisch neuropsycholoog, Klimmendaal Revalidatiespecialisten - 27 uur per week. * Senior onderzoeker, Klimmendaal Revalidatiespecialisten - 8 uur per week |
* Docent Praktijkresearch voor de KP-opleiding bij het RCSW, Nijmegen (betaald) * Gastdocent 'Pain and Psychology' voor de opleiding psychologie van de Radboud Universiteit Nijmegen (betaald) * Lid werkgroep Onderzoek binnen de sectie Revalidatie van het NIP (onbetaald) |
Geen. |
Geen. |
|
Ponds |
* klinisch neuropsycholoog * Hoogleraar Medische Psychologie, VU * Hoofd afdeling Medische Psychologie, Amsterdam UMC |
* Voorzitter Nederlandse Vereniging voor Gezondheidszorgpsychologie (NVGzP), maandvergoeding * Bestuurslid TOP opleidingsplaatse, vacatiegeld * Bestuurslid PAON (post-acad. Opleiding klinisch neuropscycholoog), geen vergoeding * Bestuurslid P3NL, vacatiegeld |
Extern gefinancierd onderzoek: Hersenstichting - PsyMate: e-healicht THL interventue vermoeidheid na hersenletsel – projectleider |
Geen. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de patiëntvereniging Hersenletsel.nl te betrekken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie kop “Waarden en voorkeuren van patiënten”). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en Stichting hersenschudding.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
Module |
Uitkomst raming |
Toelichting |
|
Symptoomclusters en diagnostiek |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Beïnvloedbare factoren |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Psycho-educatie |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Psychotherapie |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
(Graded) physical activity |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Exposure |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Vestibulaire therapie en visuele training |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Sensorische integratie interventies |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Terugkeer naar werk |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Interdisciplinaire revalidatie |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
|
Organisatie van zorg |
Geen financiële gevolgen |
Gebruikmakend van het stroomschema komt de module uit op uitkomst 2 (geen financiele gevolgen). De omvang van de patiëntenpopulatie ligt tussen de 5.000 en 40.000. Er zijn voor de voorgestelde aanpassingen geen substantiële financiele investeringen nodig. |
Implementatie
Inleiding
Dit plan is opgesteld ter bevordering van de implementatie van de richtlijn aanhoudende klacht na licht THL. Voor het opstellen van dit plan is een inventarisatie gedaan van de mogelijk bevorderende en belemmerende factoren voor het toepassen en naleven van de aanbevelingen. Daarbij heeft de richtlijncommissie een advies uitgebracht over het tijdspad voor implementatie, de daarvoor benodigde randvoorwaarden en de acties die voor verschillende partijen ondernomen dienen te worden.
Werkwijze
De werkgroep heeft per aanbeveling geïnventariseerd:
• per wanneer de aanbeveling overal geïmplementeerd moet kunnen zijn;
• de verwachtte impact van implementatie van de aanbeveling op de zorgkosten;
• randvoorwaarden om de aanbeveling te kunnen implementeren;
• mogelijk barrières om de aanbeveling te kunnen implementeren;
• mogelijke acties om de implementatie van de aanbeveling te bevorderen;
• verantwoordelijke partij voor de te ondernemen acties.
Voor iedere aanbevelingen is nagedacht over de hierboven genoemde punten. Echter niet voor iedere aanbeveling kon ieder punt worden beantwoord. Er kan een onderscheid worden gemaakt tussen “sterk geformuleerde aanbevelingen” en “zwak geformuleerde aanbevelingen”. In het eerste geval doet de richtlijncommissie een duidelijke uitspraak over iets dat zeker wel of zeker niet gedaan moet worden. In het tweede geval wordt de aanbeveling minder zeker gesteld (bijvoorbeeld “Overweeg om …”) en wordt dus meer ruimte gelaten voor alternatieve opties. Voor “sterk geformuleerde aanbevelingen” zijn bovengenoemde punten in principe meer uitgewerkt dan voor de “zwak geformuleerde aanbevelingen”. Bij elke module is onderstaande tabel opgenomen.
|
Aanbeveling |
Tijdspad voor implementatie: 1 tot 3 jaar of > 3 jaar |
Verwacht effect op kosten |
Randvoorwaarden voor implementatie (binnen aangegeven tijdspad) |
Mogelijke barrières voor implementatie1 |
Te ondernemen acties voor implementatie2 |
Verantwoordelijken voor acties3 |
Overige opmerkingen |
|
|
|
|
|
|
|
|
|
1 Barrières kunnen zich bevinden op het niveau van de professional, op het niveau van de organisatie (het ziekenhuis) of op het niveau van het systeem (buiten het ziekenhuis). Denk bijvoorbeeld aan onenigheid in het land met betrekking tot de aanbeveling, onvoldoende motivatie of kennis bij de specialist, onvoldoende faciliteiten of personeel, nodige concentratie van zorg, kosten, slechte samenwerking tussen disciplines, nodige taakherschikking, et cetera.
2 Denk aan acties die noodzakelijk zijn voor implementatie, maar ook acties die mogelijk zijn om de implementatie te bevorderen. Denk bijvoorbeeld aan controleren aanbeveling tijdens kwaliteitsvisitatie, publicatie van de richtlijn, ontwikkelen van implementatietools, informeren van ziekenhuisbestuurders, regelen van goede vergoeding voor een bepaald type behandeling, maken van samenwerkingsafspraken.
3 Wie de verantwoordelijkheden draagt voor implementatie van de aanbevelingen, zal tevens afhankelijk zijn van het niveau waarop zich barrières bevinden. Barrières op het niveau van de professional zullen vaak opgelost moeten worden door de beroepsvereniging. Barrières op het niveau van de organisatie zullen vaak onder verantwoordelijkheid van de ziekenhuisbestuurders vallen. Bij het oplossen van barrières op het niveau van het systeem zijn ook andere partijen, zoals de NZA en zorgverzekeraars, van belang. Echter, aangezien de richtlijn vaak enkel wordt geautoriseerd door de (participerende) wetenschappelijke verenigingen is het aan de wetenschappelijke verenigingen om deze problemen bij de andere partijen aan te kaarten.
Implementatietermijnen
Voor “sterk geformuleerde aanbevelingen” geldt dat zij zo spoedig mogelijk geïmplementeerd dienen te worden. Voor de meeste “sterk geformuleerde aanbevelingen” betekent dat dat zij komend jaar direct geïmplementeerd moeten worden en dat per 2023 dus iedereen aan deze aanbevelingen dient te voldoen.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met aanhoudende klachten na licht THL in de chronische fase. Tevens zijn er knelpunten aangedragen door de Nederlandse Vereniging voor Psychiatrie, Inspectie Gezondheidszorg en Jeugd, Koepels van zorginstellingen, Verpleegkundigen & Verzorgenden Nederland, Vereniging Innovatieve Geneesmiddelen, Nederlandse Associate Physician Assistants, Zorginstituut Nederland, Zorgverzekeraars Nederland, Vereniging van Oefentherapeuten Cesar en Mesendieck, CZ en Zilveren Kruis via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healicht THLcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healicht THLcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in healicht THL care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for healicht THL professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Literature search strategy
Algemene informatie
|
Richtlijn: NVN LICHT THL in de chronische fase |
|
|
Uitgangsvraag: Wat is de plaats van psychotherapie na een licht-traumatisch (hoofd)hersenletsel in de chronische fase? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 12-10-2021 |
|
Periode: >1990 |
Talen: Engels, Nederlands |
|
Literatuurspecialist: Linda Niesink |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
→ Voor deze vraag is gezocht op de elementen licht-traumatisch hersenletsel in de chronische fase (in het blauw) en psychotherapie (in het groen).
à De genoemde sleutelartikelen van Teo (2020) en Silverberg (2013) zitten in de zoekopbrengst. Potter (2011) valt buiten de zoekopbrengst vanwege studiedesign (dit is een algemeen review).
à Resultaten staan in Rayyan.
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 12-10-2021 met relevante zoektermen gezocht vanaf 1990 naar systematische reviews en RCT’s over psychotherapie bij patiënten met (chronisch) licht-traumatisch hersenletsel. De literatuurzoekactie leverde 574 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
149 |
143 |
186 |
|
RCTs |
209 |
300 |
388 |
|
Totaal |
358 |
443 |
574 |
Zoekstrategie
|
Database |
Zoektermen |
|||||||||||||||||||||||||||||||||
|
Embase
|
|
|||||||||||||||||||||||||||||||||
|
Medline (OVID)
|
1 exp Brain Injuries, Traumatic/ or exp Brain Concussion/ or exp Head Injuries, Closed/ or exp Chronic Traumatic Encephalopathy/ or exp Post-Concussion Syndrome/ or (traumatic adj2 (brain or cerebral) adj2 (injur* or lesion*)).ti,ab,kf. or 'brain system trauma*'.ti,ab,kf. or ((brain or cerebral or cerebrovascular) adj2 trauma*).ti,ab,kf. or ((traumatic or posttraumatic) adj2 encephalopath*).ti,ab,kf. (57168) 2 exp Psychotherapy/ or exp *Cognitive Behavioral Therapy/ or exp "Acceptance and Commitment Therapy"/ or 'commitment therap*'.ti,ab,kf. or mindfullness.ti,ab,kf. or emdr.ti,ab,kf. or (psychotherap* or neuropsychotherap*).ti,ab,kf. or ((psychotherapeutic or psychological) adj3 (intervention* or treatment*)).ti,ab,kf. or (cognitive adj4 (behavioral or behavioural)).ti,ab,kf. (255166) 3 1 and 2 (1655) 4 limit 3 to ((english or dutch) and yr="1990-Current") (1579) 5 (meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) (522282) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (2173730) 7 4 and 5 (143) – SRs 8 (4 and 6) not 7 (300) - RCTs 9 7 or 8 (443) |