D. Shaver versus koude technieken
Uitgangsvraag
Wat zijn de (on)gunstige effecten van (A)TE door middel van shaver vergeleken met (A)TE door middel van ‘koud/conventioneel instrumentarium’ (sluder, koud staal en blunt dissectie) bij patiënten met indicatie (A)TE?
Aanbeveling
Zie module 'De indicaties voor koude respectievelijk warme operatietechnieken' voor aanbeveling.
Overwegingen
Zie module 'De indicaties voor koude respectievelijk warme operatietechnieken' voor de overwegingen.
Onderbouwing
Conclusies / Summary of Findings
|
- |
Er werden geen studies gevonden die shaver met koude dissectie vergeleken. |
Samenvatting literatuur
Er werden geen studies gevonden die voldeden aan de inclusiecriteria.
Referenties
- Alexiou VG, Salazar-Salvia MS, Jervis PN, et al. Modern technology-assisted vs conventional tonsillectomy: a meta-analysis of randomized controlled trials. Archives of Otolaryngology -- Head & Neck Surgery 2011;137(6):558-70.
- Burton MJ, Doree C. Coblation versus other surgical techniques for tonsillectomy. Cochrane database of systematic reviews 2007.
- Ishlah LW, Fahmi AM, Srinovianti N. Laser versus dissection technique of tonsillectomy. Med J Malaysia 2005;60(1):76-80.
- Kothari P, Patel S, Brown P, et al. A prospective double-blind randomized controlled trial comparing the suitability of KTP laser tonsillectomy with conventional dissection tonsillectomy for day case surgery. Clinical Otolaryngology 2002;27:369-373.
- Leinbach RF, Markwell SJ, Colliver JA, et al. Hot versus cold tonsillectomy: a systematic review of the literature. Otolaryngology - Head & Neck Surgery 2003;129(4):360-4.
- Lowe D, Meulen J van der, Cromwell D, et al. Key Messages From the National Prospective Tonsillectomy Audit. Laryngoscope 2007;117(4):717?724.
- Mosges R, Hellmich M, Allekotte S, et al. Hemorrhage rate after coblation tonsillectomy: a meta-analysis of published trials. Eur Arch Oto-Rhino-Laryngol 2011;268(6):807-16.
- Mowatt G, Cook JA, Fraser C, et al. Systematic review of the safety of electrosurgery for tonsillectomy. Clin Otolaryngol 2006;31(2):95-102.
- Neumann C, Street I, Lowe D, et al. Harmonic scalpel tonsillectomy: a systematic review of evidence for postoperative hemorrhage. Otolaryngology - Head & Neck Surgery 2007;137(3):378-84.
- Omrani M, Barati B, Omidifar N, et al. Coblation versus traditional tonsillectomy: A double blind randomized controlled trial. J Res Med Sci 2012;17(1):45-50.
- Paramasivan VK, Arumugam SV, Kameswaran M. Randomised comparative study of adenotonsillectomy by conventional and coblation method for children with obstructive sleep apnoea. Int J Pediatr Otorhinolaryngol 2012;76(6):816-21.
- Pinder DK, Wilson H, Hilton MP. Dissection versus diathermy for tonsillectomy. Cochrane Database Syst Rev 2001;(3).
- Pinder DK, Wilson H, Hilton MP. Dissection versus diathermy for tonsillectomy. Cochrane database of systematic reviews 2011.
- Sarny S, Ossimitz G, Habermann W, et al. Hemorrhage Following Tonsil Surgery: A Multicenter Prospective Study. Laryngoscope 2011;121(12):2553?2560.
- Shapiro NL, Bhattacharyya N. Cold dissection versus coblation-assisted adenotonsillectomy in children. Laryngoscope 2007;117(3):406-10.
- Tomkinson A, Harrison W, Owens D, et al. Risk Factors for Postoperative Hemorrhage Following Tonsillectomy. Laryngoscope 2011;121(2):279?288.
- Windfuhr JP. Coblation tonsillectomy: a review of the literature. HNO 2007;55(5):337-48.
Evidence tabellen
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
|
Bias due to inadequate blinding of participants to treatment allocation?3
|
Bias due to inadequate blinding of care providers to treatment allocation?3
|
Bias due to inadequate blinding of outcome assessors to treatment allocation?3 |
Bias due to selective outcome reporting on basis of the results?4 |
Bias due to loss to follow-up?5
|
Bias due to violation of intention to treat analysis?6
|
|
|
Coblation vs. Cold dissection |
|||||||||
|
Omrani et al, 2012 |
Random number table |
Unclear * concealment not described |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
Unclear * loss to follow-up not described. Secondary hemorrhage is passively measured (patients need to call), so not very reliable |
Unlikely |
+ Same surgeon with much experience in both techniques. -not all outcome measures are given in absolute numbers; in text some numbers are incorrectly rounded. Overall nog very well structured and written. |
|
Paramasivan et al, 2012 |
Randomly selected |
Unclear* concealment not described |
Unlikely* not blinded, but bias is not likely |
Unlikely |
Unlikely (blinded) |
Unlikely |
Unclear* not reported |
Unclear |
Not very well written, outcomes are grouped without clear explanation |
|
Shapiro et al, 2007 |
Not described |
Unlikely |
Unclear* patients were not blinded, unclear if this caused bias |
Unlikely |
Unclear |
Likely** stratified data without explanation why, data not given in numbers but only in figures, definitions of outcome measures unclear, time in operation room is not reported in results section. |
Unclear |
Unclear |
|
|
Laser vs. Cold dissection |
|||||||||
|
Ishlah et al, 2005 |
Random, not described |
Unclear * not described |
Unlikely ** blinding of participants is not stated, however this is not likely to cause bias (objective outcome measures) |
Unlikely* operator is not blinded, but risk of bias is unlikely |
Unclear * not stated whether outcome assessors are blinded |
Unlikely |
Unlikely * patients who did not come for follow up were contacted, and interviewed by telephone |
Unlikely |
Not very well written English, outcomes reported as means (range), no SD, no critical appraisal of own study. Overall methodology weak. |
|
Kothar et ali, 2002 |
Random by computer |
Unclear * not described |
Unlikely |
Unlikely * operator is not blinded, but since outcome measurement is done by others, risk of bias is unlikely. |
Unlikely |
Unlikely |
Unclear * loss to follow-up is not described |
Unlikely * not described, but since intervention was surgery which was performed right after randomisation risk of bias is low. |
Some outcomes not reported in absolute numbers, which is less transparent. Also, in and exclusion criteria were not described, way of VAS recording was not clearly described. |
Evidence tabellen RCT’s: warme vs. koude technieken
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison/ control (C) 3 |
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Coblation vs. Cold dissection |
|||||||
|
Omran et ali, 2012 |
Type of study: RCT
Setting: Hospital
Country: Iran
Source of funding: None reported |
Inclusion criteria: chronic recurrent tonsillitis, OSAS
Exclusion criteria: history of peritonsillar abscess, ongoing analgesic use for medical conditions, bleeding disorders.
N total at baseline: 94 Intervention: 47 Control: 47
Important prognostic factors2: age ± SD: I: 11.2 C: 11.8
Groups comparable at baseline? unclear
|
AthroCare 2 assisted Evac-70 coblator wand
No antibiotics, topical or local anaesthesia, or other medications were administered before surgery. Aesthetic approach was the same for all patients: IV fentanyl, propofol 2mg/kg, atracurium 0.5mg/kg following intubation. Maintenance achieved by mixture of nitrous oxide, oxygen, propofol.
|
Steel cold dissection |
Length of follow-up: Not described
Loss-to-follow-up: Intervention: N=2
Control: N=1 Reasons: unknown
Incomplete outcome data: Not described.
|
Pain (VAS) No absolute outcomes: exclusion of this outcome measure
Intraoperative blood loss (volume of blood in suction bottle ml) I: 103.4±28.7 C: 161.5±11.8 P<0.001
Primary hemorrhage (bleeding <24h after surgery, patients were asked to call if occurred, n(%)) I: 1 (2.12) C: 2 (4.26) p>0.05
Secondary hemorrhage (bleeding >24h after surgery, patients were asked to call if occurred, n(%)) I: 1 (2.12) C: 5 (10.64) p>0.05
Time to return to normal diet (questionnaire, mean days) I: 6.27±1.07 C: 9.25±1.30 P<0.001
Time to return to normal activities (questionnaire) I: 7.63±1.16 C: 11.70±1.68 P<0.001 |
|
|
Paramasivan et al, 2012 |
Type of study: RCT
Setting: Hospital
Country: India
Source of funding: Not reported |
Inclusion criteria: age 5-12years, tonsillar and adenoid hypertrophy causing obstructive sleep apnoea
Exclusion criteria: septic tonsils, other general contraindications for (A)TE.
N total at baseline: 100 Intervention: 50 Control: 50
Important prognostic factors2: age ± SD: I: 11.2 C: 11.8
Groups comparable at baseline? unclear |
AthroCare 2 assisted Evac-70 coblator wand
|
Adenoid was curetted using St. Clair Thomson adenoid curette and bleeding arrested using postnasal pack, tonsillectomy was performed by blunt dissection and bleeding arrested with ligatures. |
Length of follow-up: 6h and 4days postoperative
Loss-to-follow-up: Not described
Incomplete outcome data: Not described.
|
Pain (Wong Bakers FACES pain rating + questionnaire)
Day 1 (high pain score 5-8) I: 2/50 (4%) C: 12/50 (24%)
Day 4 I: 1/50 (2%) C: 8/50 (16%) p-value: <0.001
Intraoperative blood loss (volume of blood in suction bottle ml) I: 7.4 C: 56.3 P<0.001
Primary hemorrhage (bleeding <24h after surgery, n) I: 1/50 (2%) C: 1/50 (2%)
Secondary hemorrhage (bleeding >24h after surgery, n) I: 0/50 C: 0/50 |
|
|
Shapiro et al, 2007 |
Type of study: RCT
Setting: Hospital
Country: USA
Source of funding: received materials from industry. |
Inclusion criteria: Age 2-16, undergoing outpatient adenotonsillectomy
Exclusion criteria: Severe comorbidities: systemic disease, known bleeding diathesis, craniofacial disorders, chromosomal abnormalities, motor/developmental delays.
N total at baseline: 47 Intervention: 24 Control: 23
Important prognostic factors2: Age mean I: 7.39 C: 6.1
Sex: I: 43.5% M C: 65.2% M
Groups comparable at baseline?
|
Coblatie using EVAC T&A handpiece.
Anaesthesia and recovery room techniques were standardized
|
Cold-dissection tonsillectomy was performed using curved Metzenbaum scissors to enter peritonsillar space, blunt dissection to remove the tonsil from superior to inferior, and wire snare to divide the inferior pole. Hemostasis with bipolar cautery.
Cold dissection adenotonsillectomy with adenoid curette, and hemostasis with suction Bovie cautery.
Anaesthesia and recovery room techniques were standardized
|
Length of follow-up: 12 months
Loss-to-follow-up: None
Incomplete outcome data: Intervention: N=1 Reasons (describe): incomplete postoperative data
Control: N=-
|
Postoperative pain (Wong-Baker Faces pain scale, for 14 days): no difference (no absolute numbers given) P=0.296
Intraoperative bleeding (ml blood loss): Higher in control than the intervention group (no absolute numbers given) P<0.001
Primary hemorrhage, n(%)during hospital stay Not reported
secondary hemorrhage, (n) I: 1 (treated with operative control of bleeding without blood transfusion) C: 0
Time before resumption of normal diet (average day) I: 4 C: 3 P=0.982
Time before resumption of normal activities (average day) I: 2-3 C: 1 P=0.631
Adverse effects; no unscheduled telephone calls, physician office visits or dehydration admissions were recorded |
Indicatie wordt niet vermeld |
|
Laser vs. Cold dissection |
|||||||
|
Ishlah, 2005 |
Type of study: RCT
Setting: hospital
Country: Malaysia
Source of funding: not stated |
Inclusion criteria: - Exclusion criteria: - N total at baseline: 60 Intervention: 30 Control: 30
Important prognostic factors2: age (range): I:15.3 (6-49) C:16.8 (6-42)
Sex: I: 60% M C: 56% M
Indication for tonsillectomy Chr/rec. Tonsillitis (n, %) I: 24 (80%) C: 26 (86.7%)
Groups comparable at baseline? Yes
|
Laser tonsillectomy using the Sharplan model 1080S, power set between 10-15 watts and laser was used to separate the tonsil tissue from tonsillar bed.
Hemostasis was secured by suture ligation or diathermy
Intramuscular and oral Tramal was a standard pain control regimen used in all patients, given every 8 hours. Patients were discharged 1 or 2 days after operation. |
Conventional dissection technique using blunt dissector to dissect tonsillar tissue from tonsillar bed and tonsil snare at the tissue attachment in the inferior pole.
Hemostasis was secured by suture ligation or diathermy
Intramuscular and oral Tramal was a standard pain control regimen used in all patients, given every 8 hours. Patients were discharged 1 or 2 days after operation. |
Length of follow-up: 2 weeks and 1 month after surgery
Loss-to-follow-up: Not stated
Incomplete outcome data: Not stated
|
I vs. C Intraoperative blood loss (measured weighing tonsil swab and the amount in the suction bottle), ml (range) 94.8 (19-256) vs. 151.7 (16-654) p=0.014
Pain scores (VAS, from day 1 to 2 weeks) mean 24.93 vs. 29.17 p=0.43
Readmitted to hospital 2 vs. 2. For: postoperative fever, halitosis and persistent blood-stained saliva. All patients were treated conservatively. |
|
|
Kothari et al, 2002 |
Type of study: RCT
Setting: Hospital
Country: UK
Source of funding: grant from Oxford Regional Health Authority
|
Inclusion criteria: -
Exclusion criteria :-
N total at baseline:151 Intervention:79 Control:72
Important prognostic factors: Mean age : I: 15 C:16.5
Sex: I: % M C: % M
Groups comparable at baseline?
|
Describe intervention (treatment/procedure/test):
KTP 532 (laserscope) laser at 10 W continuous beam for initial dissection and a defocused beam for haemostasis. Laser was delivered via 0.6mm EndostatTM fibre
Standard postoperative care: discharge with dispersible analgesia and mouth washes (10% hydrogen peroxide after food and Difflam mouthwash before food) sufficient for 10 days. |
Describe control (treatment/procedure/test):
Standard cold dissection and snare technique. Haemostasis was achieved with bipolar diathermy of ligation.
Standard postoperative care: discharge with dispersible analgesia and mouth washes (10% hydrogen peroxide after food and Difflam mouthwash before food) sufficient for 10 days. |
Length of follow-up: Reviewed 1 day postoperative and 1 month postoperative.
Loss-to-follow-up: Not stated
Incomplete outcome data: Not stated
|
I vs. C.
Peroperative bleeding (weight of saturated swabs and blood volume in suction bottle), median ml (range): 20 (0-320) vs. 95 (4-400) P<0.001
Postoperative pain (VAS) Day of surgery: not significant (p=0.9)
First postoperative day: larger proportion of patients from laser group had moderate to severe pain (p=0.055)
One month: 30% experiencing pain vs 18% (p=0.056)
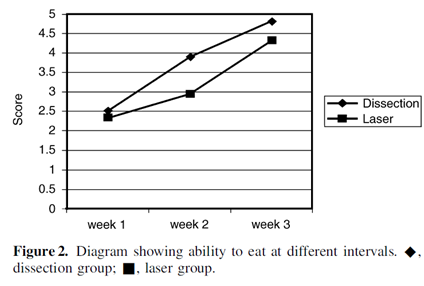
Time to return to normal diet postoperatively (SF-36) 1=not at all, 5=normal See figure 2 below
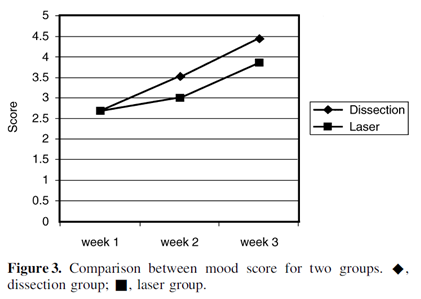
Quality of life (patient comfort and mood (SF-36) 1=silent, 5=cheerful) See Figure 3 below
Haemorrhage (a) primary 11.3% (n=9) vs 5.5 (n=4)P=0.3
(b) secondary (with hospital readmission) 8% (n=6) vs. 4% (n=3) p=0.5 |
|
Evidence tabellen systematische reviews: warme vs. koude technieken
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Coblation vs. Cold dissection |
|||||||
|
Burton and Doree, 2009
PS., study characteristics and results are extracted from the SR only for studies comparing coblation with cold steel dissection. |
SR of RCT’s comparing the effectiveness of coblation tonsillectomy vs. Other surgical methods
Literature search up to December 2006
A: Anthony, 2006 B: Bäck, 2001 C: Jayasinghe, 2005 E: Philpott, 2005
Study design: RCT
Setting and Country: A: hospital, UK B: hospital, Finland C: tertiary referral centre, UK E: hospital, UK
Source of funding: Not stated
|
Inclusion criteria: Randomisation of patients (not tonsils), Adults, Children, Day-case or inpatient setting, adenoidectomy
Exclusion criteria: emergency tonsillectomy in adults and trials in which participants underwent additional procedures other than adenoidectomy
9 studies included
Important patient characteristics at baseline: N, age range A: 27, 3-64 B: 40, 18-65 C: 60, 18-65 E: 92, 18-45
Groups comparable at baseline? yes |
Describe intervention (n) Coblation tonsillectomy (ArthroCare, using Coblator I or II)
A: coblation tonsillectomy (136) B: bipolar radiofrequency thermal ablation tonsillectomy (18) C: coblation tonsillectomy (30) E: coblation tonsillectomy (43) adenotonsillectomy (17)
Perioperative medication: A: participants were issued with analgesics for home use (no information type or dosage) B: premedication (if requested) 10mg oral diazepam and postoperative analgesia as requires (100mg ketoprofen + 500mg acetaminophen and 30mg codeine phosphate) C: post-operative analgesia was standardized (no information type and dosage) E: Co-codamol (2 tabs, 4x day) and diclofenac (50mg 3xday) post discharge |
Describe control (n): Other surgical methods
A: standard cold steel dissection tonsillectomy with clip and tie haemostatis (n=138) B: cold steel dissection tonsillectomy with packs and diathermy haemostasis (n=19) C: cold steel dissection tonsillectomy with packs and diathermy haemostasis (30) E: cold dissection tonsillectomy (49) using a standardized dissection technique, method of haemostasis not stated.
|
End-point of follow-up: A: 14d B: 21d C: 11d E: 14d
For how many participants were no complete outcome data available? (intervention/control) A: 111 (40.5%) B: 3 (7.5%) C: 20 (33%) E: 22 (24%)
|
I vs C Outcome measure: Pain (Validated pain scores (VAS)) A:adults: VAS 0-4; children: unspecified VAS 0-4, daily pain scores during 14 days B: 100mm line, daily during 14 days C: 20 point, daily during 11days, overall mean pain score. E: 10cm line + multiple choice questions on days 1,3,7 and 14
A: no significant differences. B: only graphically. No significant differences. C: 4.43 (sd 1.36) vs 5.14 (sd 1.42) p-value: 0.18 E: no significant differences.
Outcome measure: haemorrhage Intraoperative Blood loss (suction aspirate, ml): A: - B:80 (range5-300) vs 20 (5-100) p= clinically insignificant C: 19.50(SD 18.7) vs 68.95 (64.95), P = 0.0002* E: -
(b) Primary hemorrhage, n(%)during hospital stay A: - B: 5 (28%) vs 3 (16%) p=0.56 C: - E: no incidence
(c) secondary hemorrhage, (%) A: 13.6% vs 2.1% p=0.001 B: 9 (50%) vs 8 (42%) =0.82 C: 1 vs 1 E: 11(31.4%) vs 8 (22.2%) p=0.331
Outcome measure-3 Time before resumption of normal diet A:mean days (95%CI) Adults: 2 (2-3) 2 vs (1-3) Children: 1 (1-2) vs 1 (1-3) B:- C: - E: mean days (sd) 6.59 (3.18) vs. 8.64 (4.47), p-value: 0.032
and/or normal activities A: - B: median days (range): 14 (14-27) vs 14 (14-21) p-value: 0.92 C: - E: (sd) 10.47(4.41) vs 10.20 (4.2) p-value:0.669 |
Anthony 2006 and Jayasinge 2005 are unpublished studies
Brief description of author’s conclusion:
9 trials. All but two studies were of low quality and therefore meta-analysis was not appropriate. In most studies, when considering most outcomes, there was no significant difference between coblation and other tonsillectomy techniques.
Level of evidence: Overall quality Grade (per study as stated in SR) A: C B: C C: C E: C Reasons: >20% loss of follow up, Bäck had quasi randomisation and initial outcome assessment was performed by non-blinded operator
*outcome preoperative hemorrhage in study C (Jayasinghe): student’s T test was used, however not normally distributed so non-parametric test would have been better |
|
Diathermy versus Cold dissection |
|||||||
|
Pinder et al, 2011
Study characteristics and results are extracted from the SR |
SR and meta-analysis of RCT’s comparing tonsillectomy by dissection and diathermy
Literature search up to 31 January 2011
A: Kujawski, 1997 B: Nunez, 2000 Study design: RCT
Setting and Country: -
Source of funding: -
|
Inclusion criteria SR: RCT’s of children and adults undergoing TE or ATE by dissection or diathermy techniques.
Exclusion criteria SR: Trials were tonsils were randomised, where patients underwent additional procedures (except adenoidectomy)
2 studies included
Important patient characteristics at baseline:
N, age range A: 200 patients, 80 children <7 and 120 >7 yrs B: 54 children, 3-12 years
Groups comparable at baseline? yes |
Describe intervention (n) Diathermy
A: Binocular microscope and bipolar dissection (100)
B: diathermy tonsillectomy by monopolar diathermy dissection at 70W and haemostasis at 30W. (24)
Neither protocol included the routine administration of antibiotics
|
Describe control: Dissection
A: dissection by scissors and bipolar haemostasis (100)
B: Cold dissection tonsillectomy was by Gwynne-Evans dissector with an Eves snare to the lower pole. Haemostasis was with monopolar diathermy at 30 W. (26)
|
End-point of follow-up:
Not stated
For how many participants were no complete outcome data available? A: 42 patients (20.5%) were excluded from pain analysis due to loss to follow up or antibiotic use. Therefore pain was excluded from review B: 4 children (7.4%) were excluded (2 withdrew, 2 protocol violations)
|
Outcome measure:
Outcome measure: Haemorrhage
Intraoperative hemorrhage A: suction aspirate, ml : 12 (18) vs 36 (35) B: swab weight and volume suction aspirate. (after adenoidectomy),15.1 (11.7) vs 33.7 (18.4) combined: -21.56 [ -27.26, -15.85 ] (favours intervention)
(a) primary hemorrhage <24h postoperative: No episodes recorded
(b) secondary hemorrhage >24h postoperative. (with/without hospitalisation) Effect measure: mean difference [95% CI]: A: 0.38 [0.11 to 1.29] B: 2.18 [0.22 to 22.03]
Pooled effect (random effects model / fixed effects model): 0.56 [95% CI [0.19 to 1.63] favoring diathermy Heterogeneity (I2): 1.70. Z=1.06 (p=0.29)
Outcome measure: pain control Defined as analgesic requirement (total analgesic doses, mean difference (95%CI)
First 24h B: -0.60 [-1.36 to 0.16] P=0.12
First 12 days B: 7.5 [1.05 to 13.95] P=0.023
Time before resumption of normal activities Days to normal activity (95%CI) B: 7 (5.0-8.0) vs 5.0 (3.0 – 8.0)
Days to normal diet (95%CI) B: 7.5 (5.0-8.0) vs 50 (3.0-7.0)
Operating time A: 36.9 vs 35.9 NS |
Pain data from Kajuwaski (1997) was excluded because of loss to follow up due to antibiotic use.
Both studies assessed intraoperative bleeding by measuring suction aspirate; nut only Nunez weighed the swabs as well. This illustrated the difficulty of comparing data of hemorrhage between studies.
Brief description of author’s conclusion: Data from RCT’s to support one method of tonsillectomy over another are currently lacking, particularly when considering haemorrhage rates. The combined data suggest that there is less intraoperative blood loss using diathermy dissection: this may be relevant for certain patients such as small children and infant. No differences were found in either the primary of secondary haemorrhage rates. This may reflect the fact that the studies were insufficiently powerful to pick up small differences in such rates |
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 01-01-2014
Uiterlijk in 2018 bepaalt het bestuur van de NVKNO of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn om een herzieningstraject te starten.
De NVKNO is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
IN SAMENWERKING MET
in 2012 tot en met 2014
Nederlandse Vereniging voor Anesthesiologie
in 2007
Artsen Jeugdgezondheidszorg Nederland
Nederlands Huisartsen Genootschap
Nederlandse Vereniging voor Anesthesiologie
Nederlandse Vereniging voor Kindergeneeskunde
Nederlandse Vereniging voor Medische Microbiologie
Vereniging Kind en Ziekenhuis
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kims.orde.nl) en werd gefinancierd uit [de Kwaliteitsgelden Medisch Specialisten (SKMS) of andere bron].
Doel en doelgroep
Doel van de richtlijn
De herziening van de richtlijn moet heldere en eenduidige criteria opleveren voor indicatiestelling tot wel of niet operatief ingrijpen en de methode van chirurgie en anesthesie en zo een ondersteuning zijn van de dagelijkse praktijk. Tevens kan de herziene richtlijn gebruikt worden bij voorlichting aan (ouders van) patiënten en in de onderhandelingen met zorgverzekeraars.
Doelgroep
Deze richtlijn is bedoeld voor alle zorgverleners die betrokken zijn bij de behandeling van patiënten met aandoeningen van adenoïd en tonsillen die zich in de tweede lijn hebben gemeld: KNO-artsen, anesthesiologen, kinderartsen, apothekers, medisch microbiologen en verpleegkundigen. Daarnaast heeft deze richtlijn ook consequenties voor de eerste lijn; huisartsen en jeugdartsen.
Samenstelling werkgroep
Voor de beperkte revisie van de richtlijn uit 2007 is in 2012 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alleen die specialismen die inhoudelijk direct gerelateerd zijn aan de te reviseren uitgangsvragen (zie hiervoor de samenstelling van de werkgroep). De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
In 2012 tot en met 2014 hebben de volgende personen deelgenomen aan het updaten en reviseren van de richtlijn:
Werkgroep:
- Dr H.J. Rosingh (voorzitter), KNO-arts, Isala, Zwolle
- Mw Dr C.W.B. Boonacker, epidemioloog, UMC Utrecht
- Dr R.J.H. Ensink, KNO-arts, Gelre Ziekenhuizen, Zutphen
- Drs B. Pullens, KNO-arts, Erasmus MC, Rotterdam
- Mw Drs J.E.M. Samson-Vernooij, anesthesioloog, Rijnstate ziekenhuis, Arnhem
- Mw Dr J.Th. Schmidt, KNO-arts, Ziekenhuis Amstelland, Amstelveen
- Mw Dr E.H. van den Akker, KNO-arts, Meander Medisch Centrum, Amersfoort
- Mw Dr M.C.O. van den Nieuwenhuyzen, anesthesioloog, Ikazia ziekenhuis, Rotterdam
- Drs H.J.A. Visser, KNO-arts, LangeLand Ziekenhuis, Zoetermeer
Meelezers:
- Dr L. Bont, kinderarts infectioloog-immunoloog, Universitair Medisch Centrum Utrecht
- Dr N.J. Smeulers, amesthesioloog, Franciscus Ziekenhuis, Roosendaal
- Dr D.B.M. van der Werff, kinderanesthesioloog, Wilhelmina Kinderziekenhuis, Utrecht
- Mw Dr B.K. van Staaij, huisarts, Amersfoort
Met ondersteuning van:
- Mw B.S. Niël-Weise, arts-microbioloog (n.p.), senior adviseur, Kennisinstituut van Medisch Specialisten
In 2007 hebben de volgende personen deelgenomen aan de ontwikkeling van de richtlijn:
Kernredactie
- Dr H.P. Verschuur, KNO-arts, Medisch Centrum Haaglanden, Den Haag
- Mw Dr E.H. van den Akker, KNO-arts, Meander Medisch Centrum, Amersfoort
- Mw Dr C.J.I. Raats, adviseur, Kwaliteitsinstituut voor de Gezondheidszorg CBO, Utrecht
- Mw Drs C.J.G.M. Rosenbrand, senior-adviseur, Kwaliteitsinstituut voor de Gezondheidszorg CBO, Utrecht
Werkgroep:
- Dr G.J. van Asselt, arts-microbioloog, Medisch Centrum Haaglanden, Den Haag
- Mw M.E.A. van Bergen-Rodts, directeur, Vereniging Kind en Ziekenhuis, Dordrecht
- Mw Drs L.W. Boland, arts jeugdgezondheidszorg, GGD Amstelland-de Meerlanden, Amstelveen
- Dr L. Bont, kinderarts infectioloog-immunoloog, Universitair Medisch Centrum Utrecht
- Dr G.W. van Deelen, KNO-arts, Onze Lieve Vrouwe Gasthuis, Amsterdam
- Dr R.J.H. Ensink, KNO-arts, Gelre Ziekenhuizen, Zutphen
- Drs J.P.C.M. van der Hulst, kinderarts, Zaans Medisch Centrum, Zaandam
- Dr F.W. van der Meulen, KNO-arts, Academisch Medisch Centrum, Universiteit van Amsterdam
- Dr H.J. Rosingh, KNO-arts, Isala, Zwolle
- Drs J.G.H.M. Schlooz, anesthesioloog, VieCuri Medisch Centrum voor Noord-Limburg, Venlo
- Mw Dr E. Sjögren, KNO-arts, Leids Universitair Medisch Centrum, Leiden
- Mw Dr B.K. van Staaij, huisarts, Amersfoort
- Dr E.J.J.M. Theunissen, KNO-arts, VieCuri Medisch Centrum voor Noord-Limburg, Venlo
- Mw Dr M. Wagenaar, KNO-arts, Medisch Centrum Leeuwarden
- Mw Drs D.B.M. van der Werff, anesthesioloog, Universitair Medisch Centrum, Locatie Wilhelmina Kinderziekenhuis, Utrecht
Klankbordgroep:
Nederlandse Vereniging voor Anesthesiologie
- Prof. Dr H.E.M. Kerkkamp
- Mw Dr A.W.M.M. Koopman-van Gemert
- Mw Dr R. Nijholt
Artsen Jeugdgezondheidszorg Nederland
- Mw Dr E. Anten
- Mw Drs B. Carmiggelt
- Mw Drs N. Leeuwenburg
- Mw Dr C. Scheenstra
Nederlandse Vereniging voor KNO-kunde en Heelkunde van het Hoofd-Halsgebied
- Dr P.P.G. van Benthem
- Mw Drs E.M. Bolhuis
- Drs J.A.M. Engel
- Dr L.J. Hoeve
- Dr F.J.A. van den Hoogen
- Drs J.M. Kruijt
- Dr H.F. Nijdam
- Dr M.G.A.C.C. Tilanus
Nederlandse Vereniging voor Kindergeneeskunde
- Drs P.F. Eskes
- Dr N. van der Lelij
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Een overzicht van deze belangenverklaringen ligt ter inzage bij het Kennisinstituut van Medisch Specialisten (KiMS).
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn is alleen beschikbaar in een digitale versie en is verspreid onder alle relevante beroepsgroepen en ziekenhuizen. Ook is de richtlijn te downloaden vanaf de website van de Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (www.kno.nl) en via de website van de Kwaliteitskoepel (www.kwaliteitskoepel.nl).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen in het rapport ‘Richtlijnen 2.0’ van de adviescommissie Richtlijnen van de Raad WOK. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; www.agreecollaboration.org). Dit is een internationaal breed geaccepteerd instrument voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter en de adviseur van de werkgroep de knelpunten en stelden zij concept uitgangsvragen op. Dit concept werd met de werkgroep besproken en vervolgens per mail aan de volgende organisaties voorgelegd met de vraag om input: Zorgverzekeraars Nederland (ZN); Nederlandse Zorgautoriteit (NZA); College voor Zorgverzekeringen (CvZ); Inspectie voor de Gezondheidszorg (IGZ); Achmea; CZ; Menzis; VGZ en de Patiëntenvereniging ‘Kind en Ziekenhuis’.
Uitgangsvragen en uitkomstmaten
De werkgroep stelde de definitieve uitgangsvragen vast. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Tevens definieerde de werkgroep, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en systematische reviews. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in elektronische databases (zie paragraaf ‘zoeken en selecteren van literatuur’ van de individuele modules). Voor uitgangsvragen uit de ZATT-richtlijn 2007, die gereviseerd werden, werd de search beperkt tot de afgelopen vijf jaar, i.e. van 2007 tot 2013. Voor nieuwe uitgangsvragen werd geen beperking in publicatiedatum toegepast. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van op voorhand opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in het hoofdstuk van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidencetabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij voldoende overeenkomsten tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
Bij gereviseerde interventievragen werd de kracht van het wetenschappelijke bewijs bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/) (Atkins et al, 2004). Bij niet gereviseerde interventievragen is het niveau van de bewijskracht beoordeeld met de gebruikelijke EBRO-methode.
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (van Everdingen et al, 2004).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer individuele artikelen, maar wordt deze getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie. Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie, waarbij het niveau van het meest relevante bewijs is weergegeven.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiënten voorkeur, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
