Male-sling postprostatectomie
Uitgangsvraag
Wat is de waarde van een male sling bij mannen met post-prostatectomie SUI?
Aanbeveling
Bied BFT aan direct postoperatief prostatectomie
Bied bij incontinentie primair conservatieve behandeling aan.
Indien na 6-12 maanden aanhoudende incontinentie en significante impact op QoL, kan chirurgische behandeling worden overwogen.
Shared decision making en verwachtingsmanagement lijken essentieel in de keuze voor de behandeling
Overweeg bij lichte en matige incontinentie een sling wanneer conservatieve behandeling heeft gefaald, monitor complicaties.
Overweeg bij behandeling van zware incontinentie AUS
Kies voor een AUS bij een patiënt die behandeld wil worden na bestraling.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In de literatuuranalyse is onderzocht wat de waarde van het plaatsen van een male sling bij patiënten met post prostatectomie stress urine-incontinentie is, in vergelijking verschillende alternatieven (AUS, bulking agents, PRO-ACT). Er is één trial beschreven (Abrams, 2021) waarin de male sling vergeleken werd met AUS. Daarnaast is er één systematische review met vijf observationele studies gevonden (Lin, 2022) waarin male sling vergeleken werden met AUS. Ten slotte werd evidentie aangevuld met enkele individuele observationeel vergelijkende studies (Alwaal, 2016; Chughtai, 2016; Kretschmer, 2017). Naast methodologische beperkingen waren de studiepopulaties relatief klein en waren effectschattingen vaak onvoldoende nauwkeurig. Bewijskracht voor de kritieke uitkomstmaten (verbeteren/verhelpen SUI-klachten en subjectieve verbetering) was zeer laag. Dit betekent dat andere studies kunnen leiden tot nieuwe inzichten. Er kunnen op basis van alleen de literatuur geen sterke aanbevelingen geformuleerd worden over de waarde van de male sling vergeleken met AUS, bulking agents of PRO-ACT voor patiënten met SUI post-prostatectomie.
Salvage radiotherapie wordt toegepast bij patiënten waarbij de postoperatief de prostatectomie niet radicaal bleek of bij hen met (kans op) recidief. Deze bestraling kan ook bijdragen aan de mate van incontinentie door schade aan de sfincter. Daarnaast zijn stenose van de urethra of blaashals gekende complicaties (Queissert, 2023)
Patiënten die een AUS ontvangen na prostatectomie en salvage radiotherapie, hebben een kleinere kans volledig continent te worden vergeleken met patiënten die geen salvage radiotherapie ondergaan. Daarnaast hebben patiënten na salvage radiotherapie een grotere kans op revisie en is de tijd van implantatie tot revisie vaak korter (Zhang, 2022; Queissert, 2023). Opvallend is er geen verschil in AUS gerelateerde kwaliteit van leven tussen patiënten met en zonder salvage bestraling (Joseph, 2019)
In de patiënten die salvage radiotherapie ondergaan na AUS plaatsing, is de kans op revisie evident groter dan de patiënten die salvage radiotherapie ontvingen alvorens de AUS plaatsing.
Alle genoemde interventies voor de behandeling van mannelijke stress-incontinentie bestaan uit het plaatsen van een lichaamsvreemd materiaal. Infectie van dit lichaamsvreemde materiaal is het belangrijkste risico van deze behandelingen, en veelal een indicatie voor explantatie. Daarnaast kan bij de ingreep ook iatrogene schade bestaan aan blaas (retropubische sling) en urethra (sling en AUS). Indien een blaas- of urethradefect peroperatief wordt opgemerkt is dit een reden om de procedure af te breken en het implantaat niet te plaatsen. Het risico op secundaire infectie en nood voor explantatie is dan simpelweg te groot. Naast chirurgische componenten, dient er ook aandacht te zijn voor de co morbiditeit, zoals bij immuun gecompromitteerde patiënten of patiënten met diabetes mellitus en roken?.
Postoperatieve pijnklachten worden gerapporteerd bij zowel slings als de AUS. Indien pijn blijft bestaan op de langere termijn, kan explantatie worden overwogen. De behandelingen kennen beide een aanzienlijke kans op revisie. Revisie wordt verricht indien er afname van effect van de behandeling is. Bij de (gefixeerde) slings is de oorzaak veelal spanningsverlies. Bij de AUS staat mechanisch falen voorop. Ook atrofie van de bulbocavernosus ter plaatse van de manchet, is voor de AUS een revisie indicatie.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
De enige conservatieve behandeling voor post prostatectomie stress urine-incontinentie is bekkenfysiotherapie. Deze behandeling wordt vaak gestart al voor of kort na de prostatectomie. Patiënten wordt veelal geadviseerd zo’n 6 tot 12 maanden na prostatectomie de verbetering van de incontinentie af te wachten. Indien geen of subjectief onvoldoende verbetering, worden patiënten vaak verwezen voor invasieve behandeling.
Indien er geen andere afwijkingen worden gevonden op cystoscopie en eventueel urodynamisch onderzoek, zal patiënt een behandelvoorstel worden gedaan. De keuze voor de chirurgische incontinentiebehandeling wordt met name gebaseerd op de mate van de incontinentie en de conditie van de patiënt. Daar de AUS als gouden standaard wordt gezien voor de behandeling van post prostatectomie wordt deze veelal ingezet voor matig tot ernstige incontinentie. Incontinentie bij patiënten met eerdere behandeling met radiotherapie, hypo-contractiele blaas of veranderde anatomie (bijv. urethrastricturen) wordt bij voorkeur ook met AUS behandeld. Een voorwaarde voor de AUS is een goede handfunctie van de patiënt, aangezien het pompje bediend moet worden voor de mictie. De sling wordt veelal ingezet voor de behandeling van milde tot matige incontinentie, daar waar de behandeling met bulk en proACT in de praktijk voornamelijk gericht is op de milde incontinentie en is gecontra-indiceerd bij patiënten met status na radiotherapie.
Het doel van de behandeling is verbetering van de kwaliteit van leven. Volledige continentie wordt zeker niet altijd bereikt. Daarnaast resulteert significante afname van de incontinentie niet altijd in die verbetering van de kwaliteit van leven. Naast het advies voor een behandeling op basis van de patiënt-karakteristieken en de mogelijk specifieke voorkeur van de patiënt, is er dus ook een belangrijke rol voor verwachtingsmanagement.
Kosten (middelenbeslag)
De kosten van de verschillende behandelingen worden bepaald door nationale vergoedingssystemen voor zorg. Omdat in elk land de vergoedingssystemen anders zijn, zijn internationale studies hiernaar niet goed te vertalen naar de Nederlandse situatie.
Het Zorginstituut stelde in 2016 dat de behandelkosten van een sling operatie 35% bedragen van de kosten van een AUS (Zorginstituut Nederland, 2016).
Het vergelijken van de verschillende behandelingen wordt bemoeilijkt, door het feit doordat ze voor verschillende maten van incontinentie worden toegepast.
Naast de kosten van de behandeling dienen in een lange termijnevaluatie ook de kosten van chirurgische revisies, omwille van pijnklachten en mechanisch falen, te worden opgenomen. Patiënten die geen chirurgische behandeling ondergaan voor hun stress urine-incontinentie, gebruiken veelal incontinentiemateriaal. De kosten van incontinentiemateriaal hebben een grote invloed op de zorgkosten. Een behandeling van de incontinentie zou volgens de werkgroep dus indirect ook tot een reductie van de kosten voor het opvangmateriaal leiden.
Aanvaardbaarheid, haalbaarheid en implementatie
De zorg voor PPSUI behoort tot de verzekerde zorg. Voor de behandeling van PPSUI worden patiënten door de hoofdbehandelaar van het prostaatcarcinoom of door de huisarts verwezen naar een centrum met functionele expertise. Het volledige pallet van behandeling wordt niet in elk centrum aangeboden. Dit wordt veroorzaakt door de hoge kosten, intensiviteit van de behandeling en follow up en ook de expertise en mogelijkheid om revisie chirurgie te verrichten.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Ondanks dat de verschillende maten van incontinentie niet eenduidig zijn gedefinieerd, blijkt er uit de literatuur wel een duidelijke correlatie tussen de mate van verlies en de voorgestelde behandeling. De rol voor de sling in de behandeling voor mannelijke stress-incontinentie wordt met name gelegd in de lichte tot matige incontinentie. De waarde van de AUS lijkt evident bij de zware incontinentie. En de minder invasieve opties als bulking en proACT wordt veelal toegepast in de lichte incontinentie. Conservatieve therapie middels bekkenfysiotherapie wordt erkend.
Gezien de behandeling de verbetering van de kwaliteit van leven na prostatectomie beoogt, is het bespreken van de verschillende opties met voor- en nadelen en verwachtingsmanagement de sleutel tot optimale behandeling van PPSUI.
Onderbouwing
Achtergrond
Stress urine-incontinentie (SUI) is een gekende complicatie van radicale prostatectomie, als gevolg van de denervatie van het sfinctercomplex. Post prostatectomie SUI heeft een significante invloed op de kwaliteit van leven.
De artificiële sfincter wordt al tientallen jaren beschouwd als de gouden standaard in de behandeling van post-prostatectomie SUI, bij patiënten waarbij postoperatief natuurlijk herstel niet optreedt en waarbij bekkenfysiotherapie geen of onvoldoende resultaat heeft gehad. De artificiële sfincter bestaat uit een hydraulisch systeem welke compressie geeft rondom de urethra. In principe kan de sfincterprothese gebruikt worden voor alle vormen van post-prostatectomie SUI, ongeacht de ernst.
Tegenwoordig zijn er ook andere chirurgische behandelingen van SUI bij de man beschikbaar, die elk berusten op een ander chirurgisch principe. Het gaat dan om slings (al dan niet gefixeerd), bulkmateriaal en compressieballonnen. Al deze behandelingen hebben een meer minimaal invasief karakter wanneer vergeleken met de sfincter.
In deze module beperken we ons tot de waarde van de sling in vergelijk met de andere behandelingen van post-prostatectomie SUI.
De sling wordt gepositioneerd op het niveau van de bulbaire urethra, middels een retropubische of transobturatoire benadering. Er zijn slings op de markt die peroperatief worden gefixeerd en slings waar bij de spanning postoperatief nog aanpasbaar is.
Met de gefixeerde slings wordt de urethra gepositioneerd naar een meer proximale positie, zonder dat daarbij het sfinctermechanisme wordt beïnvloed.
De aanpasbare slings bieden de mogelijkheid om postoperatief de uiteinden van de sling aan te trekken of een kussen onder de urethra in meer of mindere mate op te blazen. De druk op de urethra is dus aanpasbaar.
In de praktijk wordt de artificiële sfincter toegepast voor matige tot ernstige SUI, daar waar de slings meestal worden gereserveerd voor milde tot matige SUI. Bulkmateriaal en ook plaatsing van compressieve ballonnen wordt met name verricht voor milde SUI. Echter de definities van milde en matige incontinentie lopen sterk uiteen.
Conclusies / Summary of Findings
1. Effect/recovery of SUI-complaints (critical)
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on effect/recovery of SUI-complaints when compared with AUS in patients with post-prostatectomy SUI.
Source: Abrams, 2021 and Lin, 2022 |
2. Subjective improvement (critical)
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on subjective improvement of SUI-complaints when compared with AUS in patients with post-prostatectomy SUI.
Source: Abrams (2021) |
3. Quality of life (important)
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on quality of life when compared with AUS in patients with post-prostatectomy SUI.
Source: Abrams (2021) |
4.1 Adverse events - infection
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on infection rates when compared with AUS in patients with post-prostatectomy SUI.
Source: Abrams, 2021; Chughtai (2016) and Lin, 2022 |
4.2 Adverse events - erosion
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on erosion rates when compared with AUS in patients with post-prostatectomy SUI.
Source: Lin, 2022 |
4.3 Adverse events - retention
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on retention rates when compared with AUS in patients with post-prostatectomy SUI.
Source: Lin, 2022 |
Male sling versus bulking agents; PRO-ACT
5.1 Adverse events - infection
|
Very low GRADE |
The evidence is very uncertain about the effect of male slings on infection rates when compared with bulking agents in patients with post-prostatectomy SUI.
Source: Chughtai (2016) |
|
No GRADE |
No evidence was found regarding the effect of male slings on any outcome when compared to bulking agents or PRO-ACT in patients with post-prostatectomy SUI.
Source: - |
Samenvatting literatuur
Description of studies
- Male sling versus artificial urinary sphincter
Abrams (2021) performed a multicenter noninferiority randomized trial at 27 sites in the United Kingdom. The study aimed to compare outcomes between male transobturator sling (n= 190) and the artificial urinary sphincter (AUS) (n= 190) in men with bothersome post prostate surgery stress urine incontinence (SUI). Eligible patients had urodynamic confirmed SUI, failed conservative treatment and had prostate surgery at least 12 months prior to inclusion. At randomization, 190 participants (of which 180 post-prostatectomy) were randomized to receive a male transobturator sling, and 190 (of which 181 post-prostatectomy) participants were randomized to AUS. In the male sling group, 178 participants received the intended treatment. In the AUS group, 164 participants received intended treatment. After 12 months, 157 patients in the male sling group, and 161 patients in the AUS group responded. Due to the nature of the intervention, patients could not be blinded to the allocated intervention. Outcomes included intention to treat analyses on effect/recovery of SUI-complaints (pad-test), quality of life (EQ-5D), subjective improvement (ICIQ-UI SF) and revision within 12 months. Men reporting to be dry at 12 months did not need to complete the pad test. Complications rates for retention, complicated infections (material-related) and erosion were not reported.
In the observational study by Alwaal (2016), charts of 1205 patients receiving slings (n= 597) or AUS (n= 608) in the United States were reviewed. Type of incontinence was not stated, neither was the proportion of post-prostatectomy participants. Reported outcomes were 30-day procedure-specific complications.
In the observational study by Chughtai (2016), 1246 patients in the United States, ≥65 years receiving AUS (n= 436), slings (n= 453) or injection with bulking material (n= 357) were identified. Patients were mainly diagnosed with SUI (n= 1189) and 994 participants had a prostate cancer history. Complications after 90 days including infectious complications (including Kidney infection, UTI or cystitis, post-operative infections and wound infections) were reported.
In the observational study by Kretschmer (2017) of patients receiving slings (n= 113) and AUS (n= 120). Perioperative complications (retention, infection, erosion) and explantation rates were reported.
For the systematic review by Lin (2022), a search was performed in February 2021. Five observational studies comparing slings (n= 295) with AUS (n= 214) were included (Hoy, 2014; Lim, 2014; Kim, 2018; Khouri, 2020; and Sacco, 2020), and all outcomes were combined in meta-analysis. Participants were male patients with post prostatectomy SUI using five pads or less per day. Furthermore, surgical success rate had to be assessed using pad-tests, and patients were followed for at least 12 months. All included studies were retrospective chart reviews.
Table 1. Description of included studies
|
Studie |
Male sling characteristics |
AUS characteristics |
Bulking material characteristics |
Follow-up |
Outcomes |
||||
|
|
N |
Mean age |
N |
Mean age |
N |
Mean age |
|
|
|
|
Abrams, 2021 |
190 |
68 |
190 |
69 |
- |
- |
12 months |
Effect/recovery of SUI-complaints (24-hour pad test), Subjective improvement (ICIQ-UI SF), quality of life (EQ-5D) and complications (infection, erosion, and retention) |
|
|
Alwaal, 2016 |
597 |
Aged 18-65: 160 Aged ≥65: 437 |
608 |
Aged 18-65: 165 Aged ≥65: 443 |
- |
- |
30 days |
Surgical site infection (adverse events, complicated infection) |
|
|
Chughtai, 2016 |
453 |
Aged 65-74: 298 Aged ≥75: 155
|
436 |
Aged 65-74: 298 Aged ≥75: 155
|
357 |
Aged 65-74: 211 Aged ≥75: 146
|
90 days |
Adverse events (infection) |
|
|
Kretschmer, 2017 |
113 |
70.0 (6.9)* |
120 |
69.7 (9.4)* |
- |
- |
- |
Adverse events (postoperative infection, postoperative urinary retention) |
|
|
Lin, 2022 |
- |
- |
- |
- |
- |
- |
- |
- |
|
|
|
Hoy, 2014 |
76 |
66.2 |
48 |
68.1 |
- |
- |
12 months |
Effect/recovery of SUI-complaints (yes/no by pad-test) and complications (infection, erosion, and retention) |
|
|
Lim, 2014 |
20 |
70.9 |
13 |
73.5 |
||||
|
|
Kim, 2018 |
50 |
70.8 |
53 |
69.1 |
||||
|
|
Khouri, 2020 |
114 |
66.5 |
65 |
70.8 |
||||
|
|
Sacco, 2020 |
35 |
69.64 |
35 |
70.64 |
||||
|
|
Abbreviations: AE, Adverse events; UTI, urinary tract infection * mean age was reported per group for the total cohort, complications were reported for subgroup in high-volume centers (>20 implantations) |
||||||||
Results
1. Effect/recovery of SUI-complaints (critical)
Abrams (2021) reported on effect/recovery of SUI-complaints using the 24-hour pad-test, reporting on pad weight in grams. In the male sling-group (n= 50), mean pad weight after 24 hours was 30.0 gram (SD[1] 85.3). In the AUS group (n= 44), mean pad weight after 24 hours was 73.7 gram (SD 451.6). Analysis resulted in a mean difference of -43.70 gram (95% CI -179.22 to 91.82).
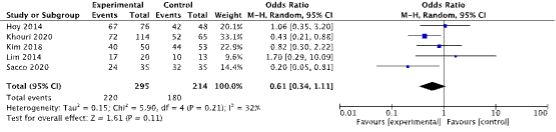
Lin (2022) reported on effect/recovery of SUI-complaints using the number of pads as indication for success (success, yes/no defined by ≤1 pad per day at follow-up). Five studies contributed to this outcome (Hoy, 2014; Lim, 2014; Kim, 2018; Khouri, 2020; and Sacco, 2020). In the groups receiving slings, 220 out of 295 patients were cured of their SUI-complaints. In the groups receiving AUS, 180 out of 214 participants were cured. Pooling the results using a random effect model led to an odds ratio of 0.61 (95% CI 0.34 to 1.11). Results are depicted in figure 1.
Figure 1: The effect of male-sling on number of pads.
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval.
2. Subjective improvement (critical)
Abrams (2021) reported on subjective improvement using the International
Consultation of Incontinence Questionnaire (ICIQ, range 0-21, higher scores indicate more severe UI). In the male sling-group (n= 151), the mean difference at 12 months was 8.7 (SD 0.6.1). In the AUS-group (n= 153), the mean difference was 7.5 (SD? 5.3). The adjusted mean difference was 1.4 (95% CI 0.2 to 2.6). This difference was not clinically relevant.
3. Quality of life (important)
Abrams (2021) reported on quality of life using the EQ-5D (range 0-100, higher scores indicate higher quality of life). In the male sling-group (n= 151), the mean difference at 12 months was 0.809 (SD 0.260). In the AUS-group (n= 158), the mean difference was 0.813 (SD 0.274). The adjusted mean difference was -0.019 (95% CI -0.062 to 0.024). This difference was not clinically relevant.
4. Adverse events (important)
4.1 Infection
In the study by Abrams (2021), one participant in the sling-group developed urosepsis, and three participants in the AUS group developed an infection.
In the study by Alwaal 2016), 30-day complications including separate amounts of surgical site infections were reported. In the patients receiving sling (n= 597), 6 (1%) developed a surgical site infection. In the patients receiving AUS (n= 608), 7 (1.2%) developed a surgical site infection. Comparing sling to AUS, this resulted in an odds ratio of 0.87 (95% CI 0.29 to 2.61).
In the study by Chughtai (2016), infection after 90 days including kidney infection, UTI or cystitis, post-operative infections and wound infections were reported. In the patients receiving sling (n= 453), 26 (5.7%) developed an infection. In the patients receiving AUS, n= 436), 40 (9.2%) developed an infection, and in the patients receiving injections with bulking material (n= 357), 19 (5.3%) developed an infection. Comparing slings to AUS, odds ratio for infection was 0.60 (95% CI 0.36 to 1.01). Comparing slings to bulking material, odds ratio for infection was 1.08 (95% CI 0.59 to 1.99).
In the study by Kretschmer (2017), adverse events including postoperative infections within the first 6 months were reported. In the patients receiving sling (n=113), 4 (3.5%) developed postoperative infection. In the patients receiving AUS (n= 120), 8 (6.7%) developed postoperative infection. Comparing sling to AUS, this resulted in an odds ratio of 0.51 (95% CI 0.15 to 1.76).
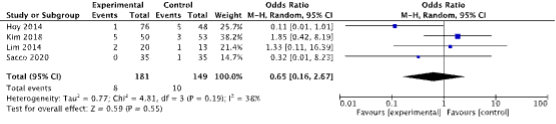
Lin (2022) reported on infection pooling the results of four studies (Hoy, 2014; Lim, 2014; Kim, 2018; and Sacco, 2020). In the groups receiving slings, in 8 out of 181 patients infection was reported. In the groups receiving AUS, in 10 out of 149 patients infection was reported. Pooling the results using a random effect model led to an odds ratio of 0.65 (95% CI 0.16 to 2.67). Results are depicted in figure 2.
Figure 2: The odds ratio on infection for sling versus AUS
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval.
4.2 Erosion
In the study by Abrams (2021), one participant in the sling-group developed mesh erosion, and in three participants in the AUS group erosion of the device was reported.
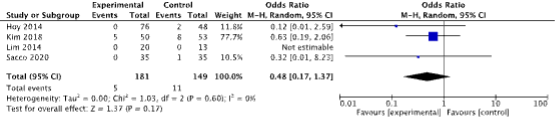
Lin (2022) reported on erosion pooling the results of four studies (Hoy, 2014; Lim, 2014; Kim, 2018; and Sacco, 2020). In the groups receiving slings, in 5 out of 181 patients infection was reported. In the groups receiving AUS, in 11 out of 149
patients infection was reported. Pooling the results using a random effect model led to an odds ratio of 0.48 (95% CI 0.17 to 1.37). Results are depicted in figure 3.
Figure 3: The odds ratio on erosion for slings versus AUS
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval.
4.3 Retention
In the study by Abrams (2021), one participant in the AUS group reported urinary retention.
In the study by Kretschmer (2017), adverse events including postoperative urinary retention within the first 6 months was reported. In the group receiving sling (n= 113), 11 (9.7%) participants developed urinary retention post-surgery. In the group receiving AUS (n= 120), 13 (10.8%) developed urinary retention post-surgery. Comparing sling to AUS, this resulted in an odds ratio of 0.89 (95% CI 0.38 to 2.07).
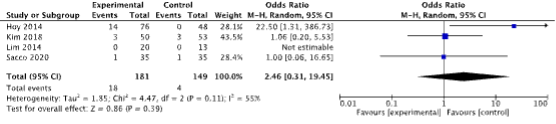
Lin (2022) reported on retention pooling the results of four studies (Hoy, 2014; Lim, 2014; Kim, 2018; and Sacco, 2020). In the groups receiving slings, in 18 out of 181 patients infection was reported. In the groups receiving AUS, in 4 out of 149 patients infection was reported. Pooling the results using a random effect model led to an odds ratio of 2.46 (95% CI 0.31 to 19.45). Results are depicted in figure 4.
Figure 4: The odds ratio on retention for slings versus AUS
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval.
Level of evidence of the literature
1. Effect/recovery of SUI-complaints (critical)
The level of evidence regarding the outcome measure effect/recovery of SUI-complaints started as low because it was partly based on observational studies and was downgraded by one level to very low because of the confidence interval crossing a border of clinical decision making (-1, imprecision).
2. Subjective improvement (critical)
The level of evidence regarding the outcome measure incontinence episodes started as high because it was based on an RCT and was downgraded by two levels to low because of lack of blinding and patient reported outcome (-2, risk of bias); and a small number of participants (-1, imprecision).
3. Quality of life (important)
The level of evidence regarding the outcome measure incontinence episodes started as high because it was based on an RCT and was downgraded by two levels to low because of and lack of blinding and patient reported outcome (-2, risk of bias); and a small number of participants (-1, imprecision).
4. Adverse events/complications (important)
4.1 Infection
The level of evidence regarding the outcome measure infection started as low because it was based on observational studies and was downgraded by one level to very low because of the confidence interval crossing borders of clinical decision making (-1, imprecision).
4.2 Erosion
The level of evidence regarding the outcome measure erosion started as low because it was based on observational studies and was downgraded by one level to very low because of the confidence interval crossing a border of clinical decision making (-1, imprecision).
4.3 Retention
The level of evidence regarding the outcome measure retention started as low because it was based on observational studies and was downgraded by one level to very low because of the confidence interval crossing a border of clinical decision making (-1, imprecision).
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question: What is the effectiveness and safety of male sling in men with post-prostatectomy stress urine incontinence, compared with bulking material, artificial urinary sphincter (AUS) or PRO-ACT?
P: Men with stress urine incontinence after radical prostatectomy.
I: Male sling.
C: Bulking agents; PRO-ACT; artificial urinary sphincter (AUS).
O: Effect/recovery of SUI-complaints (objective, e.g. pads) subjective improvement, quality of life, adverse events, long term results (explantation/revision).
Relevant outcome measures
The guideline development group considered effect/recovery of SUI-complaints and subjective improvement as a critical outcome measure for decision making; and as an important outcome measure for decision making.
A priori, the working group defined adverse events as retention, complicated infections (material-related) and erosion. For other outcomes, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The working group defined the following minimal clinically (patient) important differences:
Subjective improvement:
-
- Urinary Distress Inventory (UDI-6, 0-100): ≥ 33.33 (Skorupska, 2021)
- International Consultation on Incontinence Questionnaire - Urinary Incontinence Short Form (ICIQ-UI SF, 0-21): ≥ 5 at 12 months, ≥ 4 at 24 months (Sirls, 2013)
- The overactive bladder questionnaire (OAB-q, 0-100): ≥ 10 points (Coyne, 2006)
- The overactive bladder quality of life short-form questionnaire (OAB-q SF, 0-100): ≥ 11 points (Blanker, 2019)
In all other cases, the working group defined the GRADE-standard limit of 25% difference for dichotomous outcomes (RR < 0.8 or > 1.25), and 0.5 SD for continuous outcomes as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2010 until June 6th 2022. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 285 hits. Studies were selected based on the following criteria:
- Systematic review (searched in at least two databases, and detailed search strategy, risk of bias assessment and results of individual studies available), randomized controlled trial or observational study comparing male sling with bulking agents; PRO-ACT; artificial urinary sphincter (AUS);
- Patients aged ≥ 18 years;
- Full-text English language publication;
- Studies including ≥ 20 (ten in each study arm) patients; and
- Studies according to PICO.
A total of 27 studies were initially selected based on title and abstract screening. After reading the full text, 22 studies were excluded (see the table with reasons for exclusion under the tab Methods), and five studies were included (Abrams, 2021, Alwaal, 2016; Chughtai, 2016; Kretschmer, 2017 and Lin, 2022).
Results
Five studies were included in the analysis of the literature (Abrams, 2021; Alwaal, 2016; Chughtai, 2016; Kretschmer, 2017; Lin, 2022). Important study characteristics and results are summarized in table 1 and the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
Referenties
- 1 - Abrams P, Constable LD, Cooper D, MacLennan G, Drake MJ, Harding C, Mundy A, McCormack K, McDonald A, Norrie J, Ramsay C, Smith R, Cotterill N, Kilonzo M, Glazener C; MASTER Trial Team. Outcomes of a Noninferiority Randomised Controlled Trial of Surgery for Men with Urodynamic Stress Incontinence After Prostate Surgery (MASTER). Eur Urol. 2021 Jun;79(6):812-823. doi: 10.1016/j.eururo.2021.01.024. Epub 2021 Feb 4. PMID: 33551297; PMCID: PMC8175331.
- 2 - Alwaal A, Harris CR, Awad MA, Allen IE, Breyer BN. Comparison of complication rates related to male urethral slings and artificial urinary sphincters for urinary incontinence: national multi-institutional analysis of ACS-NSQIP database. Int Urol Nephrol. 2016 Oct;48(10):1571-6. doi: 10.1007/s11255-016-1347-3. Epub 2016 Jul 14. PMID: 27417131.
- 3 - Berger, A., Szymaniak, J., & Kathrins, M. (2020). Post-Artificial Urinary Sphincter Prostate Radiation is a Predictor of Urethral Atrophy with Recurrent Incontinence. Neurourology and Urodynamics. https://www.ics.org/2020/abstract/4
- 4 - Chughtai B, Sedrakyan A, Isaacs AJ, Mao J, Lee R, Te A, Kaplan S. National study of utilization of male incontinence procedures. Neurourol Urodyn. 2016 Jan;35(1):74-80. doi: 10.1002/nau.22683. Epub 2014 Oct 18. PMID: 25327701.
- 5 - Joseph, J. P., Rivera, M. E., Linder, B. J., Viers, B. R., & Elliott, D. S. (2019). Evaluating the impact of radiation therapy on patient quality of life following primary artificial urinary sphincter placement. Translational Andrology and Urology, 8(Suppl 1), S31ÐS37. https://doi.org/10.21037/TAU.2018.11.12
- 6 - Kretschmer A, Hsch T, Thomsen F, Kronlachner D, Obaje A, Anding R, Pottek T, Rose A, Olianas R, Friedl A, Hbner W, Homberg R, Pfitzenmaier J, Queissert F, Naumann CM, Wotzka C, Hofmann T, Seiler R, Haferkamp A, Bauer RM; Debates On Male Incontinence (DOMINO)-Project. Targeting Moderate and Severe Male Stress Urinary Incontinence With Adjustable Male Slings and the Perineal Artificial Urinary Sphincter: Focus on Perioperative Complications and Device Explantations. Int Neurourol J. 2017 Jun;21(2):109-115. doi: 10.5213/inj.1632626.313. Epub 2017 Jun 21. PMID: 28673058; PMCID: PMC5497191.
- 7 - Lin L, Sun W, Guo X, Zhou L. Artificial Urinary Sphincter Is Better Than Slings for Moderate Male Stress Urinary Incontinence With Acceptable Complication Rate: A Systematic Review and Meta-Analysis. Front Surg. 2022 Feb 9;9:841555. doi: 10.3389/fsurg.2022.841555. PMID: 35223981; PMCID: PMC8863861.
- 8 - Queissert, F., Huesch, T., Kretschmer, A., Kirschner-Hermanns, R., Pottek, T., Olianas, R., Friedl, A., Homberg, R., Pfitzenmaier, J., Naumann, C. M., Nyarangi-Dix, J., Hofmann, T., Rose, A., Weidemann, C., Wotzka, C., Hbner, W., Loertzer, H., Abdunnur, R., Grabbert, M., É Schrader, A. J. (2023). Is the Standard Artificial Urinary Sphincter AMS 800 Still a Treatment Option for the Irradiated Male Patient Presenting with a Devastated Bladder Outlet? Journal of Clinical Medicine, 12(12), 4002. https://doi.org/10.3390/JCM12124002
- 9 - Zhang, L., & Xu, Y. (2022). Impact of Radiation Therapy on Outcomes of Artificial Urinary Sphincter: A Systematic Review and Meta-Analysis. Frontiers in Surgery, 9. https://doi.org/10.3389/FSURG.2022.825239
- 10 - ZIN: https://www.zorginstituutnederland.nl/binaries/zinl/documenten/standpunten/2016/08/15/male-sling-bij-stress-urine-incontinentie/Male+sling+bij+stress+urine+incontinentie.pdf
Evidence tabellen
Risk of bias table
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
|
Was the allocation adequately concealed?
|
Blinding: Was knowledge of the allocated interventions adequately prevented? Were patients/healthcare providers/data collectors/outcome assessors/data analysts blinded? |
Was loss to follow-up (missing outcome data) infrequent?
|
Are reports of the study free of selective outcome reporting?
|
Was the study apparently free of other problems that could put it at a risk of bias?
|
Overall risk of bias If applicable/necessary, per outcome measure
|
|
Abrams, 2020 |
Probably yes
probabilistic algorithm to either a male sling or an AUS in a 1:1 ratio |
Probably yes
remote automated computer-allocated randomisation system |
Defenitely no
Reason: Patients were not blinded. Blinding of other staff not mentioned. |
Defenitely no
In the sling-group, 157 (83%) participant responded, in the AUS-group, 161 (85%) responded. “ appropriate imputation methods according to protocol. Objective improvement was measured in only 94/312 participants.
|
Probably no
Trial protocol published, SF-12 described but not reported on. Pad-test alternatively reported |
Unknown
|
HIGH (all outcomes) |
Table of excluded studies
|
Deruyver 2021 |
compared characteristics for patients receiving sling/AUS, no postoperative outcomes compared (wrong outcome) |
|
Chonière 2021 |
SR with MA but no comparative results presented (wrong study design) |
|
Ginsburg 2020 |
patients were given AUS or sling, but no comparison between the two interventions (wrong study design) |
|
Averbeck 2019 |
non-systematic review (wrong study design) |
|
Shamout 2018 |
Cost effectiveness study without clinical outcomes (wrong outcome) |
|
Barski 2017 |
SR but no comparative results presented (wrong study design) |
|
Bach 2020 |
study in women (wrong population) |
|
MacDonald 2017 |
no postoperative outcomes compared (wrong outcome) |
|
Chen 2017 |
SR with MA but only pre-post outcomes presented, no comparison (wrong study design) |
|
Liu 2016 |
no postoperative outcomes compared (wrong outcome) |
|
Kretschmer 2016 |
narrative review (wrong study design) |
|
Bauer 2011 |
nonsystematic review (wrong study design) |
|
Trost 2012 |
nonsystematic review (wrong study design) |
|
Bruwaene 2015 |
narrative review (wrong study design) |
|
Angulo 2019 |
no comparative studies included (wrong study design) |
|
Grabbert 2019 |
outcomes measured for unknown duration until max. follow up (wrong study design) |
|
Grabbert 2020 |
outcomes measured for unknown duration until max. follow up (wrong study design) |
|
Ajay 2015 |
patients were included for receiving sling, but were then either receiving secondary sling or AUS (wrong design) |
|
Sacco 2012 |
Included in Lin (2022) |
|
Khouri 2022 |
Included in Lin (2022) |
|
Bretterbauer 2016 |
measurement of follow-up differed between 0.24 and 88 months (wrong outcome) |
|
Tran 2014 |
large variation in follow-up time between two groups (wrong outcome) |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-04-2024
Beoordeeld op geldigheid : 11-04-2024
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met urine-incontinentie in de 2e- en 3e-lijnszorg.
Werkgroep
- Dhr. dr. M.R. (Michael) van Balken, uroloog, NVU (voorzitter)
- Dhr. dr. L.P.W. (Bart) Witte, uroloog, NVU
- Dhr. drs. M.A.C. (Martijn) Smits, uroloog, NVU
- Mevr. dr. M.K. (Marian) Engberts, urogynaecoloog, NVOG
- Mevr. dr. P. (Pieternel) Steures, urogynaecoloog, NVOG
- Mevr. drs. A.C. (Rianne) van der Meer, klinisch geriater, NVKG
- Mevr. C.W.L. (Tine) van den Bos, Bekkenbodem4All
Meelezers:
- Mevr. dr. T.A.M. (Doreth) Teunissen, huisarts, NHG
- Dhr. H.J. (Henk Jan) Mulder, urologie verpleegkundige, V&VN
- Mevr. drs. A. (Ana) Dos Santos, bekkenfysiotherapeut, NVFB
- Mevr. drs. C. (Corine) Adamse, bekkenfysiotherapeut, NVFB
- Dhr. dr. R.S. (Ramon) Dekker, internist, NIV
Met ondersteuning van:
- Mevr. dr. I.M. (Irina) Mostovaya, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten, Utrecht
- Mevr. drs. B. (Beatrix) Vogelaar, adviseur, Kennisinstituut van de Federatie Medisch Specialisten, Utrecht
- Mevr. drs. D.A.M. (Danique) Middelhuis, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten, Utrecht
- Mevr. drs. L. (Laura) van Wijngaarden, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten, Utrecht
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroep |
||||
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Van Balken (voorzitter) |
Uroloog, Rijnstate Ziekenhuis, Arnhem |
Bestuurslid NVU (vacatie)
Presentatie gehouden op de Post ICS IUGA congres in 2021 waarvoor vergoeding van Astellas |
Transparantieregister 2018:
Deelname als onderzoeker aan Renova-trial (OASIS). Bedrijf: Bluewind. Alleen tegemoetkoming onkosten te maken voor ziekenhuiskosten e.d.
|
geen dienstverlening bedrijven tijdens Richtlijn- ontwikkeling
Extra kritisch commentaar gevraagd van onafhankelijke reviewers tijdens de commentaarfase
|
|
Engberts |
Urogynaecoloog bij Isala |
Trainer Altis Sling Coloplast -> tegen vergoeding
Presentatie gehouden op de Post ICS IUGA congres in 2021 waarvoor vergoeding van Astellas |
Trainer bij Coloplast SIMS Altis tegen SUI om die reden bij herziening richtlijn UI NVOG met name medicatie bij OAB in combinatie/PTNS beoordeeld
Ik doe ook onderzoek naar Bulkamid & Altis sling maar hier is tot op heden nog geen vergoeding voor.
|
Extra kritisch commentaar gevraagd van onafhankelijke reviewers tijdens de commentaarfase |
|
Witte |
Uroloog, Isala Klinieken, Zwolle, Nederland |
Secretaris Werkgroep Functionele en Reconstructieve Urologie van de Nederlandse Vereniging van Urologie, onbetaald.
|
In 2018 heb ik een vergoeding gekregen als spreker in opdracht van Pierre Fabre.
In ons ziekenhuis lopen verschillende studies die extern gefinancierd worden. Van de OASIS studie is de inclusie net gesloten. Het gaat om een implanteerbaar device voor de behandeling van aandrangsincontinentie. Wij hebben 4 patiënten geïncludeerd. Follow up is 12 maanden. |
Geen actie |
|
Van den Bos |
Bekkenfysiotherapeut zzp bij paramedisch centrum AdFysio te De Lier 0.5 fte |
Voorzitter Bekkenbodem4All - vrijwilligers vergoeding
|
Geen |
Geen actie |
|
Van der Meer |
Klinische geriater, Groene Hart Ziekenhuis Gouda, 0,7 fte
|
Geen |
Geen |
Geen actie |
|
Smits |
Uroloog, Maastricht UMC+ |
Lid Werkgroep Functionele en Reconstructieve urologie NVU (-)
Presentatie gehouden op de Post ICS IUGA congres in 2021 waarvoor vergoeding van Astellas |
Diensteverlening honorarium Medtronic 2020 665euro = Deelname advisory board Medtronic
Deelname als onderzoeker aan:
Enkel support financiële support voor onkosten ziekenhuis
geen dienstverlening bedrijven tijdens Richtlijn- ontwikkeling |
Extra kritisch commentaar gevraagd van onafhankelijke reviewers tijdens de commentaarfase |
|
Steures |
Urogynaecoloog, Jeroen Bosch Ziekenhuis, ’s Hertogenbosch |
Lid van landerlijke werkgroep bekkenbodem
Lid commissie Actualisatie en revisie gynaecologische richtlijnmodules. Modules: urine-incontinentie |
Geen |
Geen actie |
|
Klankbordgroep |
||||
|
Achternaam klankbordgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Teunissen |
Huisarts, zelfstandig 0,6 fte
|
Geen |
Geen |
Geen |
|
Adamse |
Bekkenfysiotherapeut en Klinisch Epidemioloog, Antonius Ziekenhuis Sneek
|
Commissielid Wetenschapscommissie NVFB
|
Mogelijk positie bekkenfysiotherapie
|
Geen |
|
Dekker |
Internist ouderengeneeskunde bij Ziekenhuis Rivierenland
|
2021 – heden Commissielid NIV kerngroep Ouderengeneeskunde – Kwaliteit & Richtlijnen - onbetaald
|
Geen |
Geen |
|
Dos Santos |
Geregistreerd bekkenfysiotherapeut MSc bij Pelvicentrum centrum voor bekkenfysiotherapie Leiden
|
Lid van NVFB wetenschappelijke commissie vergoeding voor reiskosten en bijwonen vergaderingen
|
Deelname aan het ontwikkelen kan ervoor zorgen dat collega gaan verwijzen naar mijn praktijk vanwege meer bekendheid.
|
Geen |
|
Mulder |
Verpleegkundig specialist Martini Ziekenhuis Groningen
|
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afvaardiging van Stichting Bekkenbodem4All in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie per module ook “Waarden en voorkeuren van patiënten”). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Bekkenbodem4All en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
Module |
Uitkomst raming |
Toelichting |
|
Module male sling post-prostatectomie |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat [het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet OF het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft]. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met urine-incontinentie in de 2e en 3e lijnszorg. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodule (NVU, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door de Nederlandse Vereniging voor Klinische Geriatrie (NVKG), Nederlandse Vereniging voor Obstetrie & Gynaecologie (NVOG), Nederlandse Vereniging voor Urologie (NVU), Bekkenbodem4All (B4A), Inspectie voor de Gezondheidszorg en Jeugd (IGJ), Nederlands Huisartsen Genootschap (NHG), Nederlandse Vereniging voor Bekkenfysiotherapie (NVFB (in afstemming met de Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF)), Nederlandse Vereniging van Ziekenhuizen (NVZ), Patiëntenfederatie, Verpleegkundigen & Verzorgenden Nederland (V&VN), Zorginstituut Nederland (ZiNL), Zelfstandige Klinieken Nederland (ZKN) en Zorgverzekeraars Nederland (ZN) via een schriftelijke knelpunteninventarisatie.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Module Male-sling postprostatectomie
Literature search strategy
Zoekverantwoording
Algemene informatie
|
Richtlijn: NVU Urine-incontinentie 2e en 3e lijn |
|
|
Uitgangsvraag: Wat is de waarde van een male sling bij mannen met post-prostatectomie SUI? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 07-06-2022 |
|
Periode: >2010 |
Talen: Geen beperking |
|
Literatuurspecialist: Linda Niesink |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
→ Voor deze vraag is gezocht op de elementen (stress) urine incontinentie (in het blauw), (male) sling (in het groen) en mannen óf prostatectomie (in het oranje).
De genoemde sleutelartikelen van Abrams (2021) en Meisterhofer (2020) zitten in de zoekopbrengst. Wenjin (2022) is een conference abstract/supplement en Silva (2014) gaat niet over male sling.
Eventueel zijn er nog 157 observationele studiedesigns beschikbaar.
Resultaten staan in Rayyan.
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 07-06-2022 met relevante zoektermen gezocht vanaf 2010 naar systematische reviews en RCT’s over male slings bij mannen met (stress) urine incontinentie. De literatuurzoekactie leverde 130 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
26 |
36 |
39 |
|
RCTs |
80 |
19 |
91 |
|
Observationele studies |
(87) |
(168) |
(157) |
|
Totaal |
106 (193) |
55 (223) |
130 (287) |
Zoekstrategie
|
Database |
Zoektermen |
||||||||||||||||||||||||||||||||||||||||||
|
Embase
|
|
||||||||||||||||||||||||||||||||||||||||||
|
Medline (OVID)
|
1 exp Urinary Incontinence, Stress/ or 'stress urge incontinence'.ti,ab,kf. or 'stress urgency incontinence'.ti,ab,kf. or 'stress urinary incontinence'.ti,ab,kf. or 'stress urine incontinence'.ti,ab,kf. or 'stress incontinence'.ti,ab,kf. or 'postprostatectomy incontinence'.ti,ab,kf. or ((urge or urgency or urinary or urine) adj3 incontinence*).ti,kf. (24835) 2 exp Suburethral Slings/ or ((male or transobturator or retropubic or quadratic or bulbourethral) adj4 sling*).ti,ab,kf. (3913) 3 exp Prostatectomy/ or Male/ or ((prostate adj3 surger*) or prostatectom* or (male or men)).ti,ab,kf. (9488409) 4 1 and 2 and 3 (579) 5 limit 4 to yr="2010-Current" (474) 6 5 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) (421) 7 (meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) (569795) 8 (exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf.) not (animals/ not humans/) (1381879) 9 Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) (5172605) 10 6 and 7 (36) – SRs 11 (6 and 8) not 10 (19) - RCTs 12 (6 and 9) not (10 or 11) (168) - observationeel 13 10 or 11 or 12 (223) 14 10 or 11 (55)
|