Kinderbekkenfysiotherapie (exclusief neuromodulatie)
Uitgangsvraag
Wat is de rol van fysiotherapie voor kinderen met functionele urine-incontinentie?
Aanbeveling
Overweeg gerichte bekkenbodemspiertraining door de kinderbekkenfysiotherapeut, bij kinderen met persisterend onvermogen tot bewust aan/ontspannen of paradoxaal gebruik van de bekkenbodemspieren.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Urotherapie is een multidisciplinaire benadering waarbij psychologische, fysiotherapeutische en (kinder)verpleegkundige/therapeutische elementen worden geïntegreerd. Het psychologische aspect, een essentieel element van urotherapie, richt zich op cognitieve en gedragsmatige training om gezond mictiegedrag aan te leren en zelfredzaamheid te vergroten.
Het kinderbekkenfysiotherapeutische aspect omvat een trainingsprogramma met name gericht op bewustwording van de bekkenbodemspieren en zo nodig spierversterkende en/of ontspanningsoefeningen toepassen. Biofeedback en myofeedback versterken dit leerproces door directe feedback te geven over het plaspatroon en het gebruik van bekkenbodemspieren. Biofeedback omvat technieken zoals real-time uroflowmetrie en echografie voor het herkennen en corrigeren van onjuiste mictiepatronen en residu. Myofeedback maakt gebruik van elektromyografie (EMG) om informatie te verstrekken over het gebruik van bekkenbodemspieren, waardoor het kind leert op de juise manier gebruik te maken van de spieren betrokken bij mictie en defeatie.
Het verpleegkundige/therapeutische onderdeel omvat instructies over mictiegedrag, toilethouding en vocht- en voedingsadviezen.
De behandeling vereist gecertificeerde zorgverleners, zoals urotherapeuten of kinderbekkenfysiotherapeuten, met uitgebreide kennis en vaardigheden om succesvolle behandelplannen te implementeren en kinderen effectief te begeleiden.
De werkgroep heeft een literatuurstudie verricht naar de effectiviteit van urotherapie en kinderbekkenfysiotherapie in de behandeling van kinderen met functionele urine-incontinentie.
Er zijn drie studies gevonden die rapporteren over de uitkomstmaat effect van de behandeling. Op basis van de beschikbare literatuur is het onzeker wat het effect is van urotherapie en/of alleen kinderbekkenfysiotherapie op de cruciale uitkomstmaat van de behandeling. De bewijskracht werd beoordeeld als zeer laag vanwege risico op bias en indirectheid wegens het gebruik van een controlegroep afkomstig van een andere populatie.
Ondanks het ontbreken van directe literatuur die antwoord geeft op de zoekvraag, kan er toch worden verwezen naar verschillende studies over diverse vormen van urotherapie. Deze studies tonen vaak een hoog succespercentage aan bij het verminderen van LUT-symptomen door middel van urotherapie en/of kinderbekkenfysiotherapie. Het betreft veelal niet-gecontroleerde studies die zich richten op verschillende subtypen van LUTD, zoals overactieve blaas, dysfunctioneel plassen, of hypoactieve blaas, zonder specifieke protocollen. Diverse combinaties van cognitieve training, biofeedback, centrale inhibitietraining, kinderbekkenfysiotherapie en klokplassen worden beschreven, al dan niet ondersteund met farmacotherapie. In de meeste studies worden cohorten beschreven of worden urotherapie-elementen onderling vergeleken.
Er is weinig literatuur die specifiek gericht is op alleen (bekkenbodem)-fysiotherapie. Er bestaan beschrijvingen van niet-gecontroleerde studies met succesvolle programma's waarbij kinderbekkenfysiotherapie is opgenomen als onderdeel van specifieke urotherapie zoals biofeedback- en cognitieve trainingsprogramma's.
Hieronder volgt een beschrijving van studies naar de effecten van urotherapie en kinderbekkenfysiotherapie.
Urotherapie: bekkenfysiotherapie
Een cochrane review (Buckley, 2019) analyseerde 27 studies RCT met 1803 kinderen (5-16 jaar) waarin diverse onderdelen van urotherapie werden geëvalueerd. Echter vanwege de heterogeniteit in interventies, uitkomsten en metingen, kon er weinig zekerheid gegeven worden over de effectiviteit van de verschillende behandelingen. Wat betreft urotherapie alleen of in combinatie met bekkenfysiotherapie, educatie en instructie, biofeedback met flowmetrie of timed voiding blijft het onzeker of en welke combinaties effectiever zijn,
Urotherapie: timedvoiding-alarmbehandeling
In een onderzoek uit 2010 door Hagstroem werden 58 kinderen (5-14 jaar) met een overactieve blaas en minstens één episode van functionele urine-incontinentie per week verdeeld in twee groepen. Gedurende 12 weken kreeg de ene groep standaard urotherapie, terwijl de andere groep dezelfde behandeling kreeg met toevoeging van een timerwatch. Standaard urotherapie omvatte advies over vochtinname, elke twee uur plassen tot aan bedtijd, en het bijhouden van plasdagboeken. Vóór de interventie vertoonden kinderen in de timer-groep iets meer incontinentie-episodes. Na 12 weken vertoonden kinderen in de timer-groep significant minder incontinentie-episodes dan de groep met alleen standaard urotherapie. De timer-groep toonde een opvallende verbetering, met 60% van de kinderen die een afname van meer dan 50% van het aantal incontinentie-episodes bereikten, vergeleken met 18% in de groep zonder timer. Opmerkelijk was dat 30% van de kinderen in de timergroep volledige continentie overdag bereikte, terwijl dit niet het geval was in de standaard urotherapiegroep. Bij de follow-up na 7 maanden was 60% van de kinderen in de timergroep overdag nog steeds continent.
Urotherapie: medicatie en biofeedbacktraining
Van Gool (2014) vergeleek drie interventies (urotherapie plus anticholinergica, urotherapie plus placebo, en specifieke urotherapie met uroflowmeting en biofeedback) bij 202 kinderen (6 tot 12 jaar), van wie 97 een overactieve blaas hadden met aandrangincontinentie (groep 1) en 105 kinderen gediagnosticeerd met dysfunctional voiding (groep 2).
Alle kinderen kregen standaard urotherapie (uitleg instructies, plasdagboek) tijdens drie polikiliniek bezoeken, gedurende zes maanden. Daarnaast ontvingen ze zes maanden lang begeleiding van een urotherapeut met 6 tot 12 sessies. De kinderen werden gerandomiseerd aan verschillende interventiegroepen.
In groep 1 (OAB) ontvingen de kinderen ofwel standaard urotherapie plus anticholinergica, ofwel standaard urotherapie plus placebo, of specifieke urotherapie (blaastraining).
In groep 2 (DV) ontvingen de kinderen ofwel standaardurotherapie ofwel specifieke urotherapie (blaastraining) met uroflowmeting als biofeedback.
De resultaten toonden aan dat de percentages van kinderen die volledige continentie bereikten vergelijkbaar waren tussen de groepen: 15% in groep 1 en 25% in groep 2.
In groep 1 bereikte 44% continentie met alleen standaard urotherapie, 39% in de placebogroep, en 43% in de anticholinergica-groep.
In groep 2 waren de resultaten 52% en 49% met uroflowmetrie en biofeedback respectievelijk.
In een systematische review door Qi (2021) over de effectiviteit van biofeedback training voor kinderen (leeftijd van 5- 16 jaar) met LUTD werden 15 studies geanalyseerd, met in totaal 1274 patiënten. Daarnaast omvatte een meta-analyse zeven gerandomiseerde gecontroleerde onderzoeken met 539 patiënten. De review concludeerde dat de biofeedback training effectief was voor het verminderen van urineweginfecties, het minimaliseren van residu na het plassen, het verbeteren van de flowpatronen en het verminderen van obstipatie. Bovendien vertoonde de biofeedback een gunstiger effect op urineweginfecties (UTI) in vergelijking met standaard urotherapie. Dit effect was na 12 maanden nog aanwezig. Er werd geen significant verschil gevonden tussen biofeedbacktraining en standaard urotherapie voor incontinentie overdag en nachtelijke incontinentie.
In een retrospectieve studie van Donmez (2022) rapporteerde de lange termijn resultaten van biofeedbacktherapie bij 64 kinderen (gemiddelde leeftijd 8,8 jaar) met dysfunctional voiding Zij benadrukten de noodzaak van voortdurende biofeedbacktherapie vanwege klinische recidieven bij deze kinderen. De resultaten lieten zien dat ondanks een initieel klinisch succespercentage van 75% na een mediane reeks van 6 biofeedbacksessies, ongeveer 20% van de patiënten binnen 2 jaar een terugval vertoont.
Een recente meta-analyse en systematische review van Li (2024), waarvan de onderzoekspopulatie voor een groot deel overlapt met de studie van Qi (2021), onderzocht het effect van biofeedback bij kinderen met dysfunctional voiding (DV). De studie toonde aan dat biofeedback als aanvullende therapie geen duidelijk effect had op het verbeteren van continentie overdag en 's nachts, noch op obstipatie. Echter, het had wel een significant effect op het ontspannen van de bekkenbodemspieren tijdens mictie, het normaliseren van plaspatronen en een afname van urineweginfecties effecten die bleven bestaan in de follow-up periode.
Urotherapie: klinische urotherapie en alarmtherapie
In een andere retrospectieve studie Meijer (2015), werden de resultaten gerapporteerd van klinische urotherapie bij kinderen met een overactieve blaas (OAB). De effectiviteit van de klinische training werd onderzocht bij 70 kinderen met therapieresistente OAB. Zes maanden na de behandeling voltooide 74,3% van de kinderen de training met succes. Twee jaar na de behandeling bleek dat bij 70,5% van de kinderen de symptomen verdwenen waren of verbeterd waren. Leeftijd van het kind bleek de uitkomst van de training te voorspellen, hoe ouder het kind, hoe beter de uitkomst.
Bovenstaande literatuur laten zien dat er ondanks mogelijk positieve effecten van urotherapie vrijwel geen betrouwbare gecontroleerde studies bestaan. Veel studies zijn moeilijk met elkaar te vergelijken door de diversiteit in interventies, resultaten en meetmethoden.
Ondanks deze beperkingen, wordt internationaal (ESPU/ICCS) urotherapie als de eerste keuze behandeling voor kinderen met incontinentie aanbevolen. Dit komt doordat de behandeling van functionele incontinentie complex kan zijn vanwege de onderlinge verwevenheid van de oorzaken en de verscheidenheid aan behandelmogelijkheden. Voor een succesvolle behandeling is echter een nauwkeurige diagnose van essentieel belang. Incontinentie kan worden onderverdeeld in verschillende subtypen, gebaseerd op problemen met blaasopslag en blaaslediging. Urotherapie wordt specifiek aangepast aan deze subtypen, evenals aan de individuele omstandigheden en het type kind. Hierbij wordt rekening gehouden met factoren zoals de ervaren gezondheid en het zelfmanagement.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Er zijn geen studies naar waarden en voorkeuren t.a.v. behandeling van patiënten en ouders/verzorgers. Er is wel één studie gedaan naar de verwachtingen van ouders/ verzorgers ten aanzien van de behandeling van hun kind. Uit dit Nederlands onderzoek (Linde, 2021) is gebleken dat ouders en hun kind vaak verschillende perspectieven hebben op functionele urine-incontinentie, wat invloed kan hebben op de gezinsdynamiek, de aanpak van de behandeling en het succes ervan. De perceptie van functionele urine-incontinentie door ouders beïnvloedt ook hun neiging om medische hulp te zoeken, waarbij ouders van kinderen met urineverlies andere opvattingen kunnen hebben dan behandelaren. Het blijkt zinvol te zijn om bij het eerste polikliniekbezoek de verwachtingen van ouders en kinderen te bespreken en rekening te houden met factoren zoals de ervaren gezondheid, zelfmanagement en sociale impact van functionele urine-incontinentie. Sommige ouders willen een medische verklaring voor functionele urine-incontinentie, terwijl anderen tevreden zijn als er geen onderliggende aandoening wordt vastgesteld. Voor veel ouders is het belangrijker om hun kind copingstrategieën aan te leren dan om volledig droog te worden. Het begrijpen van hoe ouders omgaan met tegenslagen en welke benadering zij prefereren, is ook bepalend voor de keuze van de behandelmethode voor hun kind.
Het bereiken van continentie hoeft geen doel op zich te zijn. Tevredenheid en acceptatie kunnen ook als behandeluitkomsten gelden. Het is belangrijk om te beseffen dat behandelsucces en genezing niet hetzelfde zijn.
Klinische ervaring benadrukt het belang van het voorkomen dat training te lang wordt voortgezet zonder voldoende resultaat, aangezien dit zowel demotiverend als frustrerend kan zijn voor zowel het kind als de ouders. Daarnaast heeft klinische ervaring aangetoond dat een duidelijke uitleg aan zowel het kind als de ouders over het verschil tussen behandeling/trainen enerzijds en begeleiding en ondersteuning anderzijds, kan helpen bij het voorkomen van frustratie over langdurige zorg.
Onderzoek suggereert dat training op te jonge leeftijd minder effectief kan zijn, omdat leeftijd een voorspeller is van trainingsresultaten. Studies, zoals die van Meijer (2015), Vijverberg (2011) en Bachman (2007), hebben aangetoond dat kinderen ouder dan 8 jaar betere en snellere trainingsresultaten behalen.
Wanneer een kind bekend is met neurobiologische ontwikkelingsstoornissen, kan het behandelresultaat langer op zich laten wachten. Inzicht en begrip van de problematiek, behandelduur en opties bij zowel ouders als het kind kunnen helpend zijn bij het hanteren van de incontinentieproblemen en het maken van keuzes.
Kosten (middelenbeslag)
Er zijn geen degelijke studies uitgevoerd naar de kosten van urotherapie voor zowel de kind/ouders als de maatschappij. Bovendien ontbreken studies die de verandering in kosten-effectiviteit of bruikbaarheid door richtlijnen, zorgplanning of zorgverschuiving onderzoeken.
Er is nog geen onderzoek gedaan naar de optimale duur van de behandeling. De werkgroep benadrukt echter dat het essentieel is om zorg op maat te bieden, waarbij zorgvuldig wordt afgewogen wat de voordelen en nadelen van een behandeling zijn op het niveau van het kind. Hierbij worden voornamelijk de klinische aspecten van de zorg in overweging genomen. Als de verwachte voordelen, zoals verlichting van klachten, aanzienlijk opwegen tegen de verwachte nadelen, zoals bijwerkingen, wordt de behandeling als 'passend' beschouwd. Bij het aanpassen van de zorg aan het kind en sociale omgeving en gezin worden ook factoren zoals comorbiditeit en de voorkeuren van het kind en ouders meegenomen.
Internationaal wordt over het algemeen een trainingsduur van minimaal 4 tot maximaal 12 weken voor standaard urotherapie aanbevolen. Als er geen verbetering optreedt, is verdere evaluatie, diagnostiek en overweging van medicatie, herbeoordeling en specifieke urotherapie gerechtvaardigd.
Een onderzoek (Ergun, 2022) vergeleek het aantal biofeedbacksessies voor kinderen met dysfunctional voiding. De kinderen werden verdeeld in twee groepen, één met dagelijkse sessies en één met wekelijkse sessies. Het gemiddelde aantal sessies bij de dagelijkse sessies was 5, terwijl het bij de wekelijkse sessies gemiddeld 10 sessies waren. Beide benaderingen bleken even effectief te zijn. De duur kan worden bepaald op basis van de geschiktheid van de patiënt en het apparaat.
Rationale van aanbeveling: weging van argumenten voor en tegen de interventie
Er is beperkt onderzoek verricht naar de functie en dysfunctie van de bekkenbodemspieren bij kinderen. Met uitzondering van dysfunctional voiding is er geen documentatie over of specifieke dysfunctie van deze spieren bijdraagt aan de andere vormen van functionele incontinentie bij kinderen. Specifieke literatuur over bekkenbodemspiertraining bij kinderen met OAB bestaat summier. De studies met een hoog succespercentage kunnen worden verklaard door het feit dat de diagnose van dysfunctioneel voiding niet strikt is vastgesteld en dat een mix van diagnoses wordt behandeld.
Het overwegen van specifieke kinderbekkenfysiotherapie lijkt alleen zinvol wanneer er een duidelijke behoefte is aan fysiotherapeutische interventie, zoals bij het onvermogen om bewust de bekkenbodemspier te ontspannen en aan te spannen of het herkennen en afleren van paradoxale gebruik van de bekkenbodemspieren.
Hoewel de praktijkgebieden van incontinentie bij volwassenen en kinderen aanzienlijk verschillen, zou mogelijk inzicht kunnen worden verkregen uit het uitgebreide werk dat is uitgevoerd op het gebied van bekkenbodemfunctiestoornissen en behandeling bij volwassenen. Bekkenbodemspierbewustzijn, gericht op samentrekking en ontspanning, wordt voornamelijk toegepast om defecatie te vergemakkelijken en dysfunctional voiding te behandelen, met als doel een ontspannen mictie en volledige blaaslediging te bereiken.
Onderbouwing
Achtergrond
Urotherapy is the first treatment option for children and adolescents with Lower Urinary Tract Dysfunction (LUTD) such as urinary incontinence. It is a collective name for all non-surgical and non-pharmacological interventions for LUTD and includes cognitive, behavioral and physical training. Urotherapy can be divided into standard and specific urotherapy. Standard urotherapy consists of recording symptoms, providing information, instructions, lifestyle advice and counselling. Specific urotherapy is tailored towards specific conditions and includes alarm treatment, biofeedback training, pelvic floor training, neuromodulation and other interventions. It includes specific interventions such as psychological support and behavioral modification, biofeedback through the use of a uroflow meter, ultrasound, and/or physiotherapy. It can be combined with pharmacotherapy.
Urotherapy aims to normalize voiding patterns through repetitive training. The ultimate goal is to achieve continence, improve quality of life and prevent further functional deterioration This is achieved by making the child aware of regular micturition and drinking frequency, relaxation during micturition and ultimately a complete emptying of the bladder and intestines. Urotherapy involves targeted coaching and guidance until the desired result is achieved.
Conclusies / Summary of Findings
Comparison urotherapy vs expectant policy/no treatment
|
Very low GRADE |
Urotherapy/physiotherapy compared to monitoring/no treatment might improve treatment effect in children with functional urinary incontinence, however the evidence is very uncertain. Source: Schäfer, 2018; Bachmann, 2006; Hoebeke, 2011 |
Samenvatting literatuur
Description of studies
The SR and meta-analysis by Schäfer (2018) aimed to provide an evaluation of standard urotherapeutic interventions for daytime urinary incontinence (DUI) in children and adolescents. The authors state that a meta-analytical evaluation of the effectiveness of standard urotherapy for DUI is missing due to lack of RCTs, which are needed for such analyses. As a solution, the current meta-analysis did not focus on RCTs and calculated mean spontaneous remission rates based on other samples. Thereafter, an effect size of urotherapy in each study was calculated based on the expected spontaneous remissions within the same period of time. These effects were then pooled. Random effects models were used for the analysis.
To identify relevant publications on spontaneous remission rate and the effectiveness of standard urotherapy, a literature search was conducted in databases ISI Web of Knowledge, PubMed and PsychINFO. The search date was not reported. In addition, relevant review papers and guidelines were assessed to identify studies. Also, all board members of ICCS were requested to share unpublished data on clinical trials evaluating standard urotherapy for the treatment of DUI.
The spontaneous remission rate was based on three population-based studies (Fergusson, 1986; Hellström, 1995 and Swithinbank, 2010) that included 12.270 patients aged 4.5 to 17 years old. On average 54% of the patients were boys and follow-up time ranged from three to ten years.
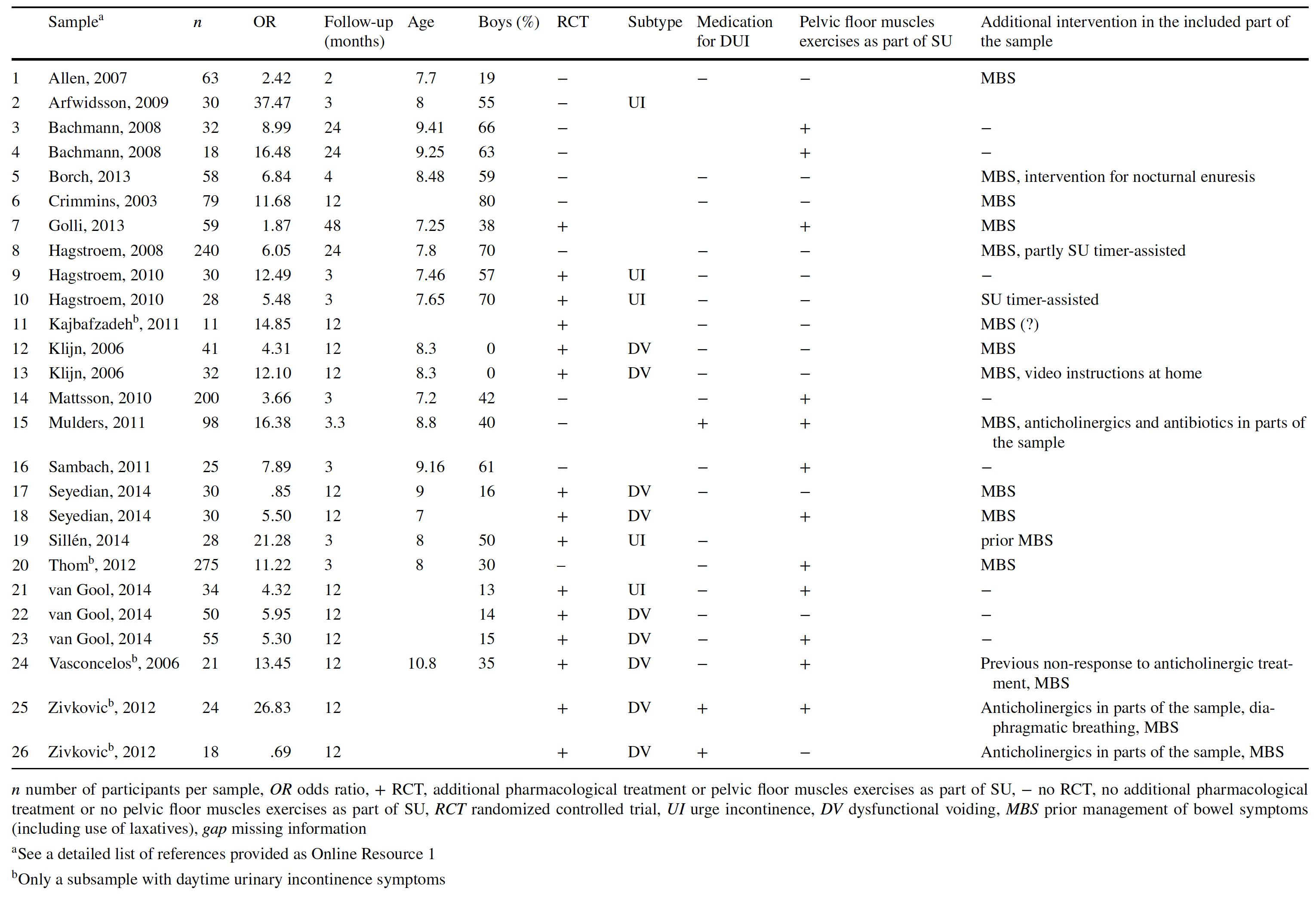
The effectiveness of standard urotherapy was based on twenty-six studies that included 1609 patients. Fifteen of these studies were RCTs, the remaining eleven were not. The mean age of the sample was eight years and 32.23% were boys. Follow-up time ranged from two months to two years. Table 1 provides an overview of all included samples.
Table 1. Overview of included studies in the SR and meta-analysis by Schäfer (2018) to determine the effectiveness of standard urotherapy (derived from Schäfer 2018).
The study conducted by Bachmann (2006) aimed to evaluate a bladder training program (both inpatient and outpatient). Sixty patients with urge incontinence or dysfunctional voiding were evaluated. Children were eligible for inclusion if they were between eight and twelve years old and had been referred to a pediatric-nephrologic outpatient clinic between July 2001 and June 2003 with complaints of urinary incontinence.
Parents decided whether their child participated in the inpatient or outpatient training. After a six-month control period (no treatment) the training commenced. Therefore, the children were under their control.
Inpatient training consisted of a six-day course of four hours a day, and the outpatient training consisted of six single interventions (also four hours a day) every two weeks. The training consisted of eleven sessions, given to child duos of the same age and sex. Topics discussed were: the anatomy and physiology of the urinary tract, keeping a voiding diary (frequency, volume, urge), scheduled drinking, uroflowmetry, and discussion of the curve and pelvic floor training (including biofeedback). Clinical assessment was performed at the beginning of the control period, at the start of bladder training, at training completion and after one, three and six months. In total, forty-three children completed the inpatient program. The mean age of the children was 9.21 years ± SD 1.44. The other seventeen children completed the outpatient bladder training. Their mean age was 9.18 years ± SD 1.29. Baseline clinical and demographic data were equal at baseline.
Outcome measures included day- and nighttime incontinence, mean bladder capacity, dysfunctional voiding and urge incontinence.
The study conducted by Hoebeke (2011) evaluated the results of a clinical voiding re-education program for treatment of lower urinary tract conditions in children and compared the results to a group of children without treatment (waitlist). Thirty-eight children with functional lower urinary tract conditions were included in the study. In the study group, 66% were boys. Mean age was 9 ± SD 1 year and 10 months. The training consisted of a two-week inpatient training program, followed by a two-week break, and then another two-week inpatient program. Children were evaluated before the program (T1), between the training sessions, at the end of training, and after six months (T4). Voiding school consisted of correction of eating and drinking habits, use of a voiding and drinking chart, biofeedback training, uroflowmetry and alarm systems. The control group consisted of fifteen children who were on a waitlist for the voiding school, 73% were boys. Mean age was 8 years and 7 months ± SD 1 year and 11 months. The controls were evaluated when they were put on the waitlist (T1), and six months later (T4). At baseline, there was no difference between the study and control group, except for comorbidities (e.g., ADHD).
Outcome measures included daytime incontinence, enuresis, pelvic floor control and voided volume. Outcome measures were compared between the study and control group at T1 and T4.
Comparison urotherapy/physiotherapy vs monitoring/no treatment
Results
1. Treatment effect
The SR and meta-analysis (Schäfer, 2018) reported a spontaneous remission rate based on three studies (Fergusson, 1986; Hellström, 1995 and Swithinbank, 2010) and a treatment effect based on 26 studies (Table 1).
The meta-analysis of the spontaneous remission rate resulted in a mean remission rate of 15.4% per year (95% CI 9.00% to 21.7%). The authors state that this remission rate cannot be generalized due to significant residual heterogeneity of effect sizes (Q(2) = 60.10, p < .001; I2= 96.66%).
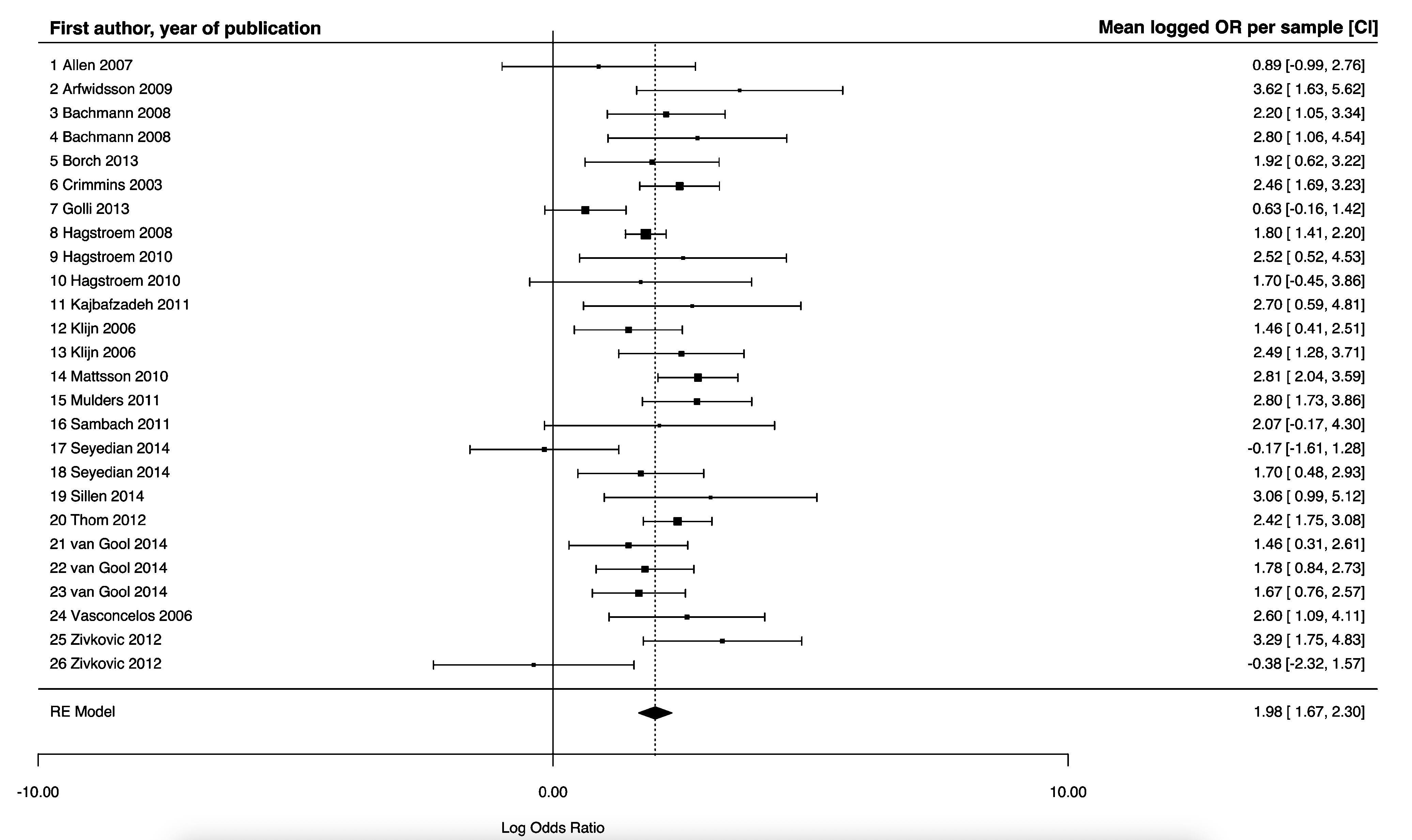
The pooled results for the treatment effect of standard urotherapy were presented in a forest plot (figure 1) mean logged OR 1.98 (95% CI 1.67 to 2.30). Due to a lack of data about the individual studies, it was not possible to construct a forest plot and calculate a risk ratio. The mean weighted odds ratio (OR) was 7.27 (95% CI 5.29 to 9.99) when accounting for the mean spontaneous remission rate of 15%.
Figure 1. Forest plot of the meta-analysis by Schäfer (2018) on the effect of standard urotherapy including all outliers.
Standard urotherapy seems to be an effective intervention in comparison to expected cure rates based on spontaneous remission in children with urinary incontinence.
The prospective trials by Bachmann (2006) and Hoebeke (2011) also reported treatment effects. Due to different study designs and training programs, the results were not pooled.
Bachmann (2006) reported the effects of in- and outpatient bladder training six months after completion.
At 6 months after inpatient training completion, 16 out of 39 children (41%) were cured of daytime wetting, 9 (23%) improved and 14 (36%) remained the same. Compared to zero cured, 8 (20%) improved and 31 (80%) remained the same during the control period. This outcome was significant (p < 0.001). Incontinence rates also showed a significant decrease during the control period (p< 0.005).
Functional bladder capacity increased 14% from training entry to six months after completion (from 163ml to 186ml) compared to 3% (5ml) in the control period (p=0.012).
At 6 months after outpatient training completion 6 out of 17 children (35%) were cured of daytime wetting, 5 (30%) had improved and 6 (35%) remained the same. Compared to zero cured, 3 (18%) improved and 14 (82%) remained the same during the control period (p<0.01).
The bladder training program showed greater improvement in day- and nighttime wetting and functional bladder capacity compared to the no-treatment control period. The more intensive inpatient program (six days, four hours daily) had better results than the outpatient program (six sessions of four hours every two weeks).
Hoebeke (2011) reported treatment effect six months after an inpatient voiding school (n=38) compared to controls (n=15) who were placed on a waitlist.
The results showed greater rates of improvement from daytime incontinence and daytime incontinence plus enuresis in the treatment group compared to the control group. 27% (n=10) of the patients in the treatment group compared to 68% (n=10) in the control group experienced daytime incontinence after voiding school (p = 0.07). For daytime incontinence plus enuresis, this was 21% (n=8) compared to 46% (n=7) (p = 0.05) in the treatment and control group respectively. None of the patients in the treatment group had post-void residual after six months, compared to 23% in the control group (p= 0.023). In the treatment group, 92% (n=35) reported normal frequency compared to 67% (n=10) in the control group (p= 0.033). Pelvic floor activity was adequate in 85% (n=32) of the treatment group and 21% (n=3) in the control group (p < 0.001). Finally, concerning uroflow, this was normal for 91%, dysfunctional for 3% and obstructive for 6% of the patients in the treatment group. Compared to 23% normal, 46% dysfunctional and 31% obstructive in the control group (p= <0.001).
Overall, when comparing the results of voiding school to no treatment in children with urinary incontinence, voiding school seems to have better results.
Level of evidence of the literature
Systematic reviews and (quasi-) RCTs start at GRADE high.
The level of evidence regarding the outcome measure treatment effect was downgraded to very low GRADE. Two levels because of study limitations (risk of bias; non-randomized trials, use of self-reports for assessment of remission rates, blinding of outcome assessors unknown); and two levels for applicability (bias due to indirectness, the control group is from a different study population).
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question:
What is the efficacy of urotherapy/physiotherapy in the treatment of children with functional urinary incontinence?
| Patients: | Children with functional urinary incontinence |
| Intervention: | Urotherapy/physiotherapy |
| Control: | Monitoring/no treatment |
| Outcome measures: | Treatment effect (subjective improvement, objective improvement, among which improvement of uroflometry (with post-void residuals), severity of urinary incontinence, voiding frequency, urgency, quality of life, bladder volume) |
Relevant outcome measures
The guideline development group considered treatment effect as a critical outcome measure for decision making.
The working group defined the outcome measure as follows:
- Effect treatment:
- Subjective improvement
- Objective improvement: improvement of uroflowmetry values with post-void residuals, degree of urinary incontinence (according to ICCS criteria) micturition frequency, frequency voiding charts/voiding diary, urgency complaints, quality of life, bladder volume
The working group defined the following minimal clinically (patient) important differences:
- Effect of treatment: >50% difference (according to ICCS criteria)
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched on 11-07-2023 with relevant search terms from the year 2000. Originally, the current question consisted of two separate PICOs about urotherapy and physiotherapy, for which two separate searches were carried out. When reviewing the literature, the guideline development group concluded that the definitions used for urotherapy and physiotherapy were often inconsistent in between publications and overlapping. It was therefore decided to combine these two modalities into one PICO resulting in one review of the literature using the search from both original questions.
The detailed search strategies are depicted under the tab Methods. The systematic literature searches resulted in 910 hits (292 for the urotherapy and 618 hits for physiotherapy search). Studies were selected based on the following criteria: systematic reviews, RCTs, and observational studies reporting on use of urotherapy and/or physiotherapy for treatment of children with functional urinary incontinence. Studies were initially selected based on title and abstract screening. After reading the full text, twenty-eight studies were excluded (see the table with reasons for exclusion under the tab Methods), and three studies were included.
Results
One systematic review (SR) and meta-analysis and two prospective quasi randomized controlled trials (RCTs) were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
Referenties
- 1 - Bachmann, C., Heilenkötter, K., Janhsen, E., Ackmann, C., Stauber, T., Lax, H., & Bachmann, H. (2007). Prospective evaluation of inpatient and outpatient bladder training in children with functional urinary incontinence: A prospective study. Monatsschrift Kinderheilkunde, 155, 831-837.
- 2 - Bachmann, C., Lehr, D., Janhsen, E., Sambach, H., Muehlan, H., Von Gontard, A., & Bachmann, H. (2009). Health related quality of life of a tertiary referral center population with urinary incontinence using the DCGM-10 questionnaire. The Journal of Urology, 182, 2000-2006. doi:10.1016/j.juro.2009.03.065
- 3 - Bower, W. F. (2008). Self-reported effect of childhood incontinence on quality of life. Journal of Wound Ostomy and Continence Nursing, 35, 617-621.
- 4 - Buckley BS, Sanders CD, Spineli L, Deng Q, Kwong JS. Conservative interventions for treating functional daytime urinary incontinence in children. Cochrane Database Syst Rev. 2019 Sep 18;9(9):CD012367. doi: 10.1002/14651858.CD012367.pub2. PMID: 31532563; PMCID: PMC6749940.
- 5 - Deshpande, A. V., Craig, J. C., Smith, G. H. H., & Caldwell, P. H. Y. (2011). Factors influencing quality of life in children with urinary incontinence. The Journal of Urology, 186, 1048-1052. doi:10.1016/j.juro.2011.04.104
- 6 - Dönmez Mİ, Selvi I, Dereli E, Özgür K, Oktar T, Ziylan O. Maintenance biofeedback therapy for dysfunctional voiding: Does every child need it? Int J Urol. 2023 Jan;30(1):83-90. doi: 10.1111/iju.15065. Epub 2022 Oct 28. PMID: 36305569.
- 7 - Ergun R, Ozturk NI, Sekerci CA. The effect of duration between sessions on biofeedback treatment in children with dysfunctional voiding. Lower Urinary Tract Symptoms. 2022; 14(5): 387-392. doi:10.1111/luts.12456
- 8 - Gordon K, Warne N, Heron J, von Gontard A, Joinson C. Continence Problems and Mental Health in Adolescents from a UK Cohort. Eur Urol. 2023 Nov;84(5):463-470. doi: 10.1016/j.eururo.2023.05.013. Epub 2023 May 27. PMID: 37248139.
- 9 - Hagstroem S, Rittig S, Kamperis K, Djurhuus JC. Timer watch assisted urotherapy in children: a randomized controlled trial. J Urol. 2010 Oct;184(4):1482-8. doi: 10.1016/j.juro.2010.06.024. Epub 2010 Aug 19. PMID: 20727552.
- 10 - Hoebeke P, Renson C, De Schryver M, De Schrijver L, Leenaerts E, Schoenaers A, Deschepper E, Vande Walle J, Van den Broeck C. Prospective evaluation of clinical voiding reeducation or voiding school for lower urinary tract conditions in children. J Urol. 2011 Aug;186(2):648-54. doi: 10.1016/j.juro.2011.03.148. Epub 2011 Jun 17. PMID: 21683382.
- 11 - Joinson C, Heron J, von Gontard A. Psychological problems in children with daytime wetting. Pediatrics. 2006 Nov;118(5):1985-93. doi: 10.1542/peds.2006-0894. PMID: 17079570.
- 12 - Kubik, K., Blackwell, L., & Heit, M. (2004). Does socioeconomic status explain racial differences in urinary incontinence knowledge? American Journal of Obstetrics and Gynecology, 191, 188-193. doi:10.1016/j.ajog.2004.03.084
- 14 - Li, F., Feng, L., Yang, Y., Ma, X., Kang, T., & Huang, W. (2024). The effect of biofeedback on nonneurological dysfunctional voiding in children: A meta-analysis and systematic review. Journal of pediatric urology, S1477-5131(24)00351-6. Advance online publication. https://doi.org/10.1016/j.jpurol.2024.06.042
- 15 - Linde JM, Ekelmans-Hogenkamp JLA, Hofmeester I, Kroes-van Hattem G, Steffens MG, Kloosterman-Eijgenraam FJ, Nijman RJM, Blanker MH. Parents' expectations of the outpatient care for daytime urinary incontinence in children: A qualitative study. J Pediatr Urol. 2021 Aug;17(4):473.e1-473.e7. doi: 10.1016/j.jpurol.2021.05.026. Epub 2021 Jun 4. PMID: 34176751.
- 16 - Meijer EF, Nieuwhof-Leppink AJ, Dekker-Vasse E, de Joode-Smink GC, de Jong TP. Central inhibition of refractory overactive bladder complaints, results of an inpatient training program. J Pediatr Urol. 2015 Feb;11(1):21.e1-5. doi: 10.1016/j.jpurol.2014.06.024. Epub 2014 Aug 11. PMID: 25205144.
- 17 - Natale, N., Kuhn, S., Siemer, S., Stöckle, M., & Von Gontard, A. (2009). Quality of life and self-esteem for children with urinary urge incontinence and voiding postponement. The Journal of Urology, 182, 692-698. doi:10.1016/j.juro.2009.04.033
- 19 - Nieuwhof-Leppink AJ, Hussong J, Chase J, Larsson J, Renson C, Hoebeke P, Yang S, von Gontard A. Definitions, indications and practice of urotherapy in children and adolescents: - A standardization document of the International Children's Continence Society (ICCS). J Pediatr Urol. 2021 Apr;17(2):172-181. doi: 10.1016/j.jpurol.2020.11.006. Epub 2020 Nov 5. PMID: 33478902.
- 20 - Qi W, Zhou Y, Zhong M, Lv G, Li R, Wang W, Li Y, Shi B, Guo H, Zhang Q. The effect of biofeedback treatment for children with non-neurogenic voiding dysfunction: A systematic review and meta-analysis. Neurourol Urodyn. 2022 Apr;41(4):868-883. doi: 10.1002/nau.24886. Epub 2022 Feb 22. PMID: 35191548.
- 21 - Schäfer SK, Niemczyk J, von Gontard A, Pospeschill M, Becker N, Equit M. Standard urotherapy as first-line intervention for daytime incontinence: a meta-analysis. Eur Child Adolesc Psychiatry. 2018 Aug;27(8):949-964. doi: 10.1007/s00787-017-1051-6. Epub 2017 Sep 25. PMID: 28948380.
- 22 - Theunis, M., Van Hoecke, E., Paesbrugge, S., Hoebeke, P., & Vande Walle, J. (2002). Self-image and performance in children with nocturnal enuresis. European Urology, 41,
- 25 - Thibodeau, B. A., Metcalfe, P., Koop, P., & Moore, K. (2013). Urinary incontinence and quality of life in children. Journal of Pediatric Urology, 9, 78-83. doi:10.1016/j.jpurol.2011.12.005
- 27 - van Gool JD, de Jong TP, Winkler-Seinstra P, Tamminen-Möbius T, Lax H, Hirche H, Nijman RJ, Hjälmås K, Jodal U, Bachmann H, Hoebeke P, Walle JV, Misselwitz J, John U, Bael A; European Bladder Dysfunction Study (EU BMH1-CT94-1006). Multi-center randomized controlled trial of cognitive treatment, placebo, oxybutynin, bladder training, and pelvic floor training in children with functional urinary incontinence. Neurourol Urodyn. 2014 Jun;33(5):482-7. doi: 10.1002/nau.22446. Epub 2013 Jun 15. PMID: 23775924.
- 28 - Vijverberg MA, Stortelder E, de Kort LM, Kok ET, de Jong TP. Long-term follow-up of incontinence and urge complaints after intensive urotherapy in childhood (75 patients followed up for 16.2-21.8 years). Urology. 2011 Dec;78(6):1391-6. doi: 10.1016/j.urology.2011.08.055. Epub 2011 Oct 19. PMID: 22014960.
- 29 - von Gontard A, Baeyens D, Van Hoecke E, Warzak WJ, Bachmann C. Psychological and psychiatric issues in urinary and fecal incontinence. J Urol. 2011 Apr;185(4):1432-6. doi: 10.1016/j.juro.2010.11.051. Epub 2011 Feb 23. PMID: 21349549.
- 30 - von Gontard A, Mattheus H, Anagnostakou A, Sambach H, Breuer M, Kiefer K, Holländer T, Hussong J. Behavioral comorbidity, overweight, and obesity in children with incontinence: An analysis of 1638 cases. Neurourol Urodyn. 2020 Sep;39(7):1985-1993. doi: 10.1002/nau.24451. Epub 2020 Jul 20. PMID: 32806882.
Evidence tabellen
Research question: What is the efficacy of urotherapy/physiotherapy in the treatment of children with urinary incontinence?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Schäfer, 2018
Individual study characteristics deduced from Schäfer, 2018
|
SR and meta-analysis of [RCTs and cohort studies]
Search date not reported
Spontaneous remission rate Effectiveness of standard urotherapy A: Allen, 2007 B: Arfwidsson, 2009 C: Bachmann, 2008 D: Borch, 2013 E: Crimmins, 2003 F: Golli, 2013 G: Hagstroem, 2008 H: Hagstroem, 2010 I: Kajbafzadeh, 2011 J: Klijn, 2006 L: Mulders, 2011 M: Sambach, 2011 N: Seyedian, 2014 O: Sillen, 2014 P: Thom, 2012 Q: van Gool, 2014 R: Vasconcelos, 2006 S: Zivkovic, 2012 Study design: A: cohort
A: no RCT* B: no RCT C: no RCT D: no RCT E: no RCT F: RCT G: no RCT H: RCT I: RCT J: RCT O: RCT R: RCT S: RCT
Setting and Country: Germany
Source of funding and conflicts of interest: Funding not reported. The authors report no conflicts of intrest.
|
Inclusion criteria SR:
Effectiveness of standard urotherapy (SU) 6) Published in English or German language. Exclusion criteria SR:
3 studies included for spontaneous remission rate and 19 studies included for effectiveness of urotherapy.
Important patient characteristics at baseline:
N, age range (years) Spontaneous remission rate
Effectiveness of standard urotherapy (SU) A: 63, 7.7 B: 30, 8 C: 32, 9.1 D: 58, 8.48 E: 79, not reported F: 59, 7.25 G: 240, 7.8 H: 30, 7.46 I: 11, not reported J: 41, 8.3 O: 28, 8 R: 21, 10.8 S: 24, not reported
Sex: A: 51 % Male B: 58 % Male C: 52 % Male
A: 19 % Male B: 55 % Male C: 66 % Male D: 59 % Male E: 80 % Male F: 38 % Male G: 70 % Male H: 57 % Male I: not reported J: 0 % Male O: 50 % Male R: 35 % Male S: not reported
Groups comparable at baseline? |
Describe intervention:
|
Describe control:
No further details reported about the included studies on which spontaneous remission rate was determined. |
Endpoint of follow-up (months):
A: 2 B: 3 C: 24 D: 4 E: 12 F: 48 G: 24 H: 3 I: 12 J: 12 O: 3 R: 12 S: 12
For how many participants were no complete outcome data available? Not reported
|
Outcome measure-1 Treatment effect
Spontaneous remission rate - A: 23.33
Effect measure: mean logged OR [95% CI]: A: 0.89 [-0.99 to 2.76] B: 3.62 [1.63 to 5.62] C: 2.22 [1.05 to 3.34] D: 1.92 [0.62 to 3.22] E: 2.46 [1.69 to 3.23] F: 0.63 [-0.16 to 1.42] G: 1.80 [1.41 to 2.20] H: 2.52 [0.52 to 4.53] I: 2.70 [0.59 to 4.81] J: 1.46 [0.41 to 2.51] O: 3.06 [0.99 to 5.12] R: 2.60 [1.09 to 4.11] S: 3.29 [1.75 to 4.83] Pooled effect (random effects model) mean logged OR [95% CI]: 1.98 [95% CI 1.67 to 2.30] favoring standard urotherapy 7.27 [95% CI 5.29 to 9.99] Heterogeneity (I2): 48.67
|
Risk of bias (high, some concerns or low): Tool used by authors: Newcastle Ottawa Scale
A: High B: High C: Some concerns D: High E: High F: Some concerns G: Some concerns H: Low I: Some concerns J: Low O: Low R: Low S: Low The authors conclude: Use of control group from a different study population (=indirectness). Outcome measure-1 Treatment effect
Downgraded to very low GRADE: Two levels because of study limitations (risk of bias; non-randomized trials, use of self-reports for assessment of remission rates, blinding of outcome assessors unknown); and two levels for applicability (bias due to indirectness, control group is from a different study population). Sensitivity analyses (excluding small studies; excluding studies with short follow-up; excluding low quality studies; relevant subgroup-analyses); mention only analyses which are of potential importance to the research question: No sensitivity analyses included in the analysis of literature.
|
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Bachmann, 2006 |
Type of study: Prospective study
Setting and country: Monocentre, outpatient clinic in Germany Funding and conflicts of interest: |
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: 72 (12 dropouts) (patients were their own control) Inpatient program: 43 Outpatient program: 17
Important prognostic factors2: age ± SD: Outpatient program: 9.18 ± 1.29
Sex: Overall: 63% M Outpatient program: 58.8% M
Groups comparable at baseline?
|
Describe intervention (treatment/procedure/test): Outpatient program:
|
Describe control (treatment/procedure/test):
Patients were their own control. After a no-treatment control period of 6 months all patients underwent a 6-day bladder training course. This course was offered as inpatient or outpatient training. |
Length of follow-up: 6 months
Loss-to-follow-up: N (%) 12 (5,56) Reasons (describe) N=2 due to urinary tract infection N=10 due to loss of follow-up
Incomplete outcome data: Inpatient program: N (%) 4 (9.3) for outcome daytime incontinence Reasons (describe) Incomplete data and incomplete micturition protocols. Outpatient program: No incomplete outcome data
|
Outcome measures and effect size (include 95%CI and p-value if available):
Outcome measure 1: Treatment effect after 6 months Daytime wetting N (%) The same 14 (36) p < 0.005 Nighttime wetting (N=33) The same 16 (49) p < 0.003
Functional bladder capacity At training entry 163 ml Daytime wetting The same 6 (35) The same 14 (82) p < 0.005 Functional bladder capacity |
Parents decided which course their child participated in (in- or outpatient). The authors conclude: Compared with the no-treatment control period, the bladder training program evaluated in this study showed considerably greater success rates. These results lead to the assumption that children with nighttime wetting treated in the inpatient training program succeeded better than those in the outpatient bladder training group. The cure and improvement rates in daytime wetting were greater than those for nighttime wetting. Age influ- enced the results in the inpatient training program. Older children had greater success rates. In patients with urge incontinence, who took part in the inpatient training program, the functional bladder capacity increased significantly.
|
|
Hoebeke, 2011 |
Type of study: Prospective controlled study
Setting and country: Monocentre, hospital in Belgium Funding and conflicts of interest: |
Inclusion criteria:
Exclusion criteria: Not reported
N total at baseline: I: 38 C: 15
Important prognostic factors2: Mean age: C: 8 years, 7 months
Sex: I: 65.7% M C: 80% M
Groups comparable at baseline?
|
Describe intervention (treatment/procedure/test):
|
Describe control (treatment/procedure/test):
|
Length of follow-up: 6 months
Loss-to-follow-up: Not reported.
Incomplete outcome data: Not reported.
|
Outcome measures and effect size (include 95%CI and p-value if available):
Outcome measure 1: Treatment effect after 6 months Daytime wetting N (%) C: 10 (68) Daytime wetting plus enuresis N (%) I: 8 (21) C: 7 (46) Post-void residual (N) I: 0 (0) C: 3,5 (23) Normal frequency (N) I: 35 (92) C: 10 (67) Pelvic floor activity I: 32 (85) C: 3 (21) Uroflow I: Dysfunctional 3% Obstructive 6% C: Normal 23% Dysfunctional 46% Obstructive 31% p < 0.001 |
The authors conclude:
|
Table of excluded studies
|
Study |
Reason for exclusion |
|
Altunkol A, Abat D, Sener NC, Gulum M, Ciftci H, Savas M, Yeni E. Is urotherapy alone as effective as a combination of urotherapy and biofeedback in children with dysfunctional voiding? Int Braz J Urol. 2018 Sep-Oct;44(5):987-995. doi: 10.1590/S1677-5538.IBJU.2018.0194. PMID: 30130020; PMCID: PMC6237517. |
Wrong comparison |
|
Amira PA, Dušan P, Gordana ML, Sandra T, Ivaniševic I. Bladder control training in girls with lower urinary tract dysfunction. Int Braz J Urol. 2013 Jan-Feb;39(1):118-26; discussion 127. doi: 10.1590/S1677-5538.IBJU.2013.01.15. PMID: 23489504. |
No comparison |
|
Ansari MS, Srivastava A, Kapoor R, Dubey D, Mandani A, Kumar A. Biofeedback therapy and home pelvic floor exercises for lower urinary tract dysfunction after posterior urethral valve ablation. J Urol. 2008 Feb;179(2):708-11. doi: 10.1016/j.juro.2007.09.091. Epub 2007 Dec 20. PMID: 18082204. |
No comparison |
|
Assis GM, Silva CPCD, Martins G. Urotherapy in the treatment of children and adolescents with bladder and bowel dysfunction: a systematic review. J Pediatr (Rio J). 2019 Nov-Dec;95(6):628-641. doi: 10.1016/j.jped.2019.02.007. Epub 2019 Apr 19. PMID: 31009619. |
Wrong comparison |
|
Ayan S, Kaya K, Topsakal K, Kilicarslan H, Gokce G, Gultekin Y. Efficacy of tolterodine as a first-line treatment for non-neurogenic voiding dysfunction in children. BJU Int. 2005 Aug;96(3):411-4. doi: 10.1111/j.1464-410X.2005.05641.x. PMID: 16042740. |
No comparison |
|
Bachmann CJ, Heilenkötter K, Janhsen E, Ackmann C, Thomä M, Lax H, Bachmann H. Long-term effects of a urotherapy training program in children with functional urinary incontinence: a 2-year follow-up. Scand J Urol Nephrol. 2008;42(4):337-43. doi: 10.1080/00365590801933226. PMID: 19230166. |
No comparison |
|
Bael A, Lax H, de Jong TP, Hoebeke P, Nijman RJ, Sixt R, Verhulst J, Hirche H, van Gool JD; European Bladder Dysfunction Study (European Union BMH1-CT94-1006). The relevance of urodynamic studies for Urge syndrome and dysfunctional voiding: a multicenter controlled trial in children. J Urol. 2008 Oct;180(4):1486-93; discussion 1494-5. doi: 10.1016/j.juro.2008.06.054. Epub 2008 Aug 16. PMID: 18710726. |
Wrong comparison |
|
Ballek NK, McKenna PH. Lower urinary tract dysfunction in childhood. Urol Clin North Am. 2010 May;37(2):215-28. doi: 10.1016/j.ucl.2010.03.001. PMID: 20569800. |
Wrong study design |
|
Barroso U Jr, Lordêlo P, Lopes AA, Andrade J, Macedo A Jr, Ortiz V. Nonpharmacological treatment of lower urinary tract dysfunction using biofeedback and transcutaneous electrical stimulation: a pilot study. BJU Int. 2006 Jul;98(1):166-71. doi: 10.1111/j.1464-410X.2006.06264.x. PMID: 16831163. |
Wrong intervention |
|
Blanco JL, Oliver FJ, De Celis R, Joao CM. Tratamiento de los trastornos miccionales en niños mediante biofeedback [Biofeedback therapy for urinary incontinence in children]. Cir Pediatr. 2006 Apr;19(2):61-5. Spanish. PMID: 16846125. |
No comparison |
|
Brownrigg N, Braga LH, Rickard M, Farrokhyar F, Easterbrook B, Dekirmendjian A, Jegatheeswaran K, DeMaria J, Lorenzo AJ. The impact of a bladder training video versus standard urotherapy on quality of life of children with bladder and bowel dysfunction: A randomized controlled trial. J Pediatr Urol. 2017 Aug;13(4):374.e1-374.e8. doi: 10.1016/j.jpurol.2017.06.005. Epub 2017 Jul 4. PMID: 28733159. |
Wrong comparison |
|
Brownrigg N, Pemberton J, Jegatheeswaran K, DeMaria J, Braga LH. A pilot randomized controlled trial evaluating the effectiveness of group vs individual urotherapy in decreasing symptoms associated with bladder-bowel dysfunction. J Urol. 2015 Apr;193(4):1347-52. doi: 10.1016/j.juro.2014.10.049. Epub 2014 Oct 16. PMID: 25444961. |
Wrong comparison |
|
Buckley BS, Sanders CD, Spineli L, Deng Q, Kwong JS. Conservative interventions for treating functional daytime urinary incontinence in children. Cochrane Database Syst Rev. 2019 Sep 18;9(9):CD012367. doi: 10.1002/14651858.CD012367.pub2. PMID: 31532563; PMCID: PMC6749940. |
Wrong comparison |
|
Bulum B, Özçakar ZB, Kavaz A, Hüseynova M, Ekim M, Yalçinkaya F. Lower urinary tract dysfunction is frequently seen in urinary tract infections in children and is often associated with reduced quality of life. Acta Paediatr. 2014 Oct;103(10):e454-8. doi: 10.1111/apa.12732. Epub 2014 Jul 18. PMID: 24974882. |
No comparison |
|
Chin-Peuckert L, Salle JL. A modified biofeedback program for children with detrusor-sphincter dyssynergia: 5-year experience. J Urol. 2001 Oct;166(4):1470-5. PMID: 11547115. |
No comparison |
|
Chua ME, Rickard M, Kim JK, Brownrigg N, Dos Santos J, Aba LK, Lorenzo A, Mistry N. Use of timed alarm device for pediatric daytime urinary incontinence Meta-analysis of comparative studies. Can Urol Assoc J. 2023 Apr;17(4):129-136. doi: 10.5489/cuaj.8113. PMID: 36486180; PMCID: PMC10073526. |
Wrong comparison |
|
Dönmez Mİ, Selvi I, Dereli E, Özgür K, Oktar T, Ziylan O. Maintenance biofeedback therapy for dysfunctional voiding: Does every child need it? Int J Urol. 2023 Jan;30(1):83-90. doi: 10.1111/iju.15065. Epub 2022 Oct 28. PMID: 36305569. |
Wrong intervention |
|
Das A, O'Kelly F, Wolf J, Hermes G, Wang M, Nemr C, Truscott S, Finnup J, Farhat W, Su R. Biofeedback therapy for children: What is the maximum number of sessions we should offer? J Pediatr Urol. 2023 Jun;19(3):240.e1-240.e6. doi: 10.1016/j.jpurol.2022.11.022. Epub 2022 Nov 26. PMID: 36944560. |
Wrong intervention |
|
de Azevedo RV, Oliveira EA, Vasconcelos MM, de Castro BA, Pereira FR, Duarte NF, de Jesus PM, Vaz GT, Lima EM. Impact of an interdisciplinary approach in children and adolescents with lower urinary tract dysfunction (LUTD). J Bras Nefrol. 2014 Oct-Dec;36(4):451-9. English, Portuguese. doi: 10.5935/0101-2800.20140065. PMID: 25517273. |
No comparison |
|
De Paepe H, Renson C, Hoebeke P, Raes A, Van Laecke E, Vande Walle J. The role of pelvic-floor therapy in the treatment of lower urinary tract dysfunctions in children. Scand J Urol Nephrol. 2002;36(4):260-7. doi: 10.1080/003655902320248218. PMID: 12201917. |
No comparison |
|
Wall LL, Nieuwhof-Leppink AJ, Schappin R. Alarm-assisted urotherapy for daytime urinary incontinence in children: A meta-analysis. PLoS One. 2023 Feb 3;18(2):e0275958. doi: 10.1371/journal.pone.0275958. PMID: 36735674; PMCID: PMC9897563. |
Wrong intervention |
|
Desantis DJ, Leonard MP, Preston MA, Barrowman NJ, Guerra LA. Effectiveness of biofeedback for dysfunctional elimination syndrome in pediatrics: a systematic review. J Pediatr Urol. 2011 Jun;7(3):342-8. doi: 10.1016/j.jpurol.2011.02.019. Epub 2011 Apr 27. PMID: 21527216. |
Wrong intervention |
|
Dos Reis JN, Mello MF, Cabral BH, Mello LF, Saiovici S, Rocha FET. EMG biofeedback or parasacral transcutaneous electrical nerve stimulation in children with lower urinary tract dysfunction: A prospective and randomized trial. Neurourol Urodyn. 2019 Aug;38(6):1588-1594. doi: 10.1002/nau.24009. Epub 2019 Apr 25. PMID: 31025397. |
Wrong comparison |
|
Dossche L, Snauwaert E, Renson C, Van Daele J, Raes A, Dehoorne J, Roels SP, Van Laecke E, Van Herzeele C, Hoebeke P, Vande Walle J. The long-term added value of voiding school for children with refractory non-neurogenic overactive bladder: an inpatient bladder rehabilitation program. J Pediatr Urol. 2020 Jun;16(3):350.e1-350.e8. doi: 10.1016/j.jpurol.2020.01.019. Epub 2020 Feb 12. PMID: 32147348. |
No comparison |
|
Drzewiecki BA, Kelly PR, Marinaccio B, Borer JG, Estrada CR, Lee RS, Bauer SB. Biofeedback training for lower urinary tract symptoms: factors affecting efficacy. J Urol. 2009 Oct;182(4 Suppl):2050-5. doi: 10.1016/j.juro.2009.06.003. Epub 2009 Aug 20. PMID: 19695584. |
Wrong intervention |
|
Ebiloglu T, Kaya E, Köprü B, Topuz B, Irkilata HC, Kibar Y. Biofeedback as a first-line treatment for overactive bladder syndrome refractory to standard urotherapy in children. J Pediatr Urol. 2016 Oct;12(5):290.e1-290.e7. doi: 10.1016/j.jpurol.2016.02.018. Epub 2016 Mar 31. PMID: 27102986. |
No comparison |
|
Fazeli MS, Lin Y, Nikoo N, Jaggumantri S, Collet JP, Afshar K. Biofeedback for nonneuropathic daytime voiding disorders in children: a systematic review and meta-analysis of randomized controlled trials. J Urol. 2015 Jan;193(1):274-9. doi: 10.1016/j.juro.2014.07.097. Epub 2014 Jul 27. PMID: 25072179. |
Wrong intervention |
|
Glazier DB, Ankem MK, Ferlise V, Gazi M, Barone JG. Utility of biofeedback for the daytime syndrome of urinary frequency and urgency of childhood. Urology. 2001 Apr;57(4):791-3; discussion 793-4. doi: 10.1016/s0090-4295(01)00927-x. PMID: 11306409. |
No comparison |
|
Golli T, Meglič A, Kenda RB. Long-term prospective evaluation of an inpatient voiding reeducation program for lower urinary tract conditions in children. Int Urol Nephrol. 2013 Apr;45(2):299-306. doi: 10.1007/s11255-012-0348-0. Epub 2013 Feb 5. PMID: 23381501. |
No comparison |
|
Hagstroem S, Rittig N, Kamperis K, Mikkelsen MM, Rittig S, Djurhuus JC. Treatment outcome of day-time urinary incontinence in children. Scand J Urol Nephrol. 2008;42(6):528-33. doi: 10.1080/00365590802098367. PMID: 18609267. |
No comparison |
|
Hagstroem S, Rittig S, Kamperis K, Djurhuus JC. Timer watch assisted urotherapy in children: a randomized controlled trial. J Urol. 2010 Oct;184(4):1482-8. doi: 10.1016/j.juro.2010.06.024. Epub 2010 Aug 19. PMID: 20727552. |
Wrong comparison |
|
Heilenkötter K, Bachmann C, Janhsen E, Stauber T, Lax H, Petermann F, Bachmann H. Prospective evaluation of inpatient and outpatient bladder training in children with functional urinary incontinence. Urology. 2006 Jan;67(1):176-80. doi: 10.1016/j.urology.2005.07.032. PMID: 16413359. |
Duplicate |
|
ISIYEL, E., ÇOMAK, E., & İlkay, E. R. (2022). The Role of Biofeedback Treatment in Children with Lower Urinary Tract Dysfunction. Türkiye Çocuk Hastalıkları Dergisi, 16(2), 117-120. |
Wrong intervention |
|
Jabaji R, Palazzi K, Finley AM, Nguyen Q, Kaplan G, Chiang G. Two Sessions of Behavioral Urotherapy for Bowel and Bladder Dysfunction: Does It Get Any Better? Urol Nurs. 2014 Nov-Dec;34(6):312-7. PMID: 26298927. |
No abstract |
|
Jessen AS, Hagstroem S, Borch L. Comparison and characteristics of children successfully treated for daytime urinary incontinence. J Pediatr Urol. 2022 Feb;18(1):24.e1-24.e9. doi: 10.1016/j.jpurol.2021.11.013. Epub 2021 Nov 29. PMID: 34930690.
|
Wrong comparison |
|
Kajbafzadeh AM, Sharifi-Rad L, Ghahestani SM, Ahmadi H, Kajbafzadeh M, Mahboubi AH. Animated biofeedback: an ideal treatment for children with dysfunctional elimination syndrome. J Urol. 2011 Dec;186(6):2379-84. doi: 10.1016/j.juro.2011.07.118. Epub 2011 Oct 22. PMID: 22019033. |
Wrong comparison |
|
Kaye JD, Palmer LS. Characterization and management of voiding dysfunction in children with attention deficit hyperactivity disorder. Urology. 2010 Jul;76(1):220-4. doi: 10.1016/j.urology.2010.01.026. Epub 2010 Mar 29. PMID: 20350758. |
No comparison |
|
Khen-Dunlop N, Van Egroo A, Bouteiller C, Biserte J, Besson R. Biofeedback therapy in the treatment of bladder overactivity, vesico-ureteral reflux and urinary tract infection. J Pediatr Urol. 2006 Oct;2(5):424-9. doi: 10.1016/j.jpurol.2005.09.004. Epub 2005 Oct 25. PMID: 18947650. |
Wrong intervention |
|
Kibar Y, Piskin M, Irkilata HC, Aydur E, Gok F, Dayanc M. Management of abnormal postvoid residual urine in children with dysfunctional voiding. Urology. 2010 Jun;75(6):1472-5. doi: 10.1016/j.urology.2009.09.008. Epub 2009 Nov 6. PMID: 19896172. |
Wrong comparison |
|
Kilcik MH, Ozdemir F, Elmas AT. Effectiveness of game-based core exercise in children with non-neuropathic bladder dysfunction and comparison to biofeedback therapy. Low Urin Tract Symptoms. 2023 Jan;15(1):16-23. doi: 10.1111/luts.12467. Epub 2022 Nov 11. PMID: 36366947. |
Wrong comparison |
|
Kopru B, Ergin G, Ebiloglu T, Kibar Y. Does biofeedback therapy improve quality of life in children with lower urinary tract dysfunction: parents' perspective. J Pediatr Urol. 2020 Feb;16(1):38.e1-38.e7. doi: 10.1016/j.jpurol.2019.11.014. Epub 2019 Nov 30. PMID: 31928898. |
Wrong intervention |
|
Krzemińska K, Maternik M, Drożyńska-Duklas M, Szcześniak P, Czarniak P, Gołębiewski A, Zurowska A. High efficacy of biofeedback therapy for treatment of dysfunctional voiding in children. Cent European J Urol. 2012;65(4):212-5. doi: 10.5173/ceju.2012.04.art6. Epub 2012 Dec 11. PMID: 24578964; PMCID: PMC3921803. |
Wrong intervention |
|
Glad Mattsson G, Brännström M, Eldh M, Mattsson S. Voiding school for children with idiopathic urinary incontinence and/or bladder dysfunction. J Pediatr Urol. 2010 Oct;6(5):490-5. doi: 10.1016/j.jpurol.2009.11.004. Epub 2009 Nov 27. PMID: 19945349. |
No comparison |
|
Ladi Seyedian SS, Sharifi-Rad L, Ebadi M, Kajbafzadeh AM. Combined functional pelvic floor muscle exercises with Swiss ball and urotherapy for management of dysfunctional voiding in children: a randomized clinical trial. Eur J Pediatr. 2014 Oct;173(10):1347-53. doi: 10.1007/s00431-014-2336-0. Epub 2014 May 21. PMID: 24844352. |
Wrong comparison |
|
Ladi-Seyedian S, Kajbafzadeh AM, Sharifi-Rad L, Shadgan B, Fan E. Management of non-neuropathic underactive bladder in children with voiding dysfunction by animated biofeedback: a randomized clinical trial. Urology. 2015 Jan;85(1):205-10. doi: 10.1016/j.urology.2014.09.025. Epub 2014 Nov 11. PMID: 25444633. |
Wrong comparison |
|
Ladi-Seyedian SS, Sharifi-Rad L, Kajbafzadeh AM. Pelvic floor electrical stimulation and muscles training: a combined rehabilitative approach for management of non-neuropathic urinary incontinence in children. J Pediatr Surg. 2019 Apr;54(4):825-830. doi: 10.1016/j.jpedsurg.2018.06.007. Epub 2018 Jun 11. PMID: 29960741. |
Wrong comparison |
|
Ladi-Seyedian SS, Sharifi-Rad L, Amini E, Kajbafzadeh AM. Resolution of Hydronephrosis in Children with Dysfunctional Voiding After Biofeedback Therapy: A Randomized Clinical Trial. Appl Psychophysiol Biofeedback. 2020 Dec;45(4):259-266. doi: 10.1007/s10484-020-09474-z. PMID: 32556710. |
Wrong comparison |
|
Ladi-Seyedian SS, Sharifi-Rad L, Kajbafzadeh AM. Management of Bladder Bowel Dysfunction in Children by Pelvic Floor Interferential Electrical Stimulation and Muscle Exercises: A Randomized Clinical Trial. Urology. 2020 Oct;144:182-187. doi: 10.1016/j.urology.2020.07.015. Epub 2020 Jul 25. PMID: 32717244. |
Wrong comparison |
|
Meijer EF, Nieuwhof-Leppink AJ, Dekker-Vasse E, de Joode-Smink GC, de Jong TP. Central inhibition of refractory overactive bladder complaints, results of an inpatient training program. J Pediatr Urol. 2015 Feb;11(1):21.e1-5. doi: 10.1016/j.jpurol.2014.06.024. Epub 2014 Aug 11. PMID: 25205144. |
Wrong intervention |
|
Mulders MM, Cobussen-Boekhorst H, de Gier RP, Feitz WF, Kortmann BB. Urotherapy in children: quantitative measurements of daytime urinary incontinence before and after treatment according to the new definitions of the International Children's Continence Society. J Pediatr Urol. 2011 Apr;7(2):213-8. doi: 10.1016/j.jpurol.2010.03.010. Epub 2010 Jun 11. PMID: 20541978. |
No comparison |
|
Palmer LS. Pediatrics: Clock-watching: timer-assisted urotherapy improves continence. Nat Rev Urol. 2011 Jan;8(1):13-4. doi: 10.1038/nrurol.2010.204. Epub 2010 Nov 30. PMID: 21116301. |
No abstract |
|
Peng CH, Chen SF, Kuo HC. Long-Term Follow-Up of Lower Urinary Tract Outcome in Children with Dysfunctional Voiding. J Clin Med. 2022 Dec 13;11(24):7395. doi: 10.3390/jcm11247395. PMID: 36556011; PMCID: PMC9781924. |
No comparison |
|
Qi W, Zhou Y, Zhong M, Lv G, Li R, Wang W, Li Y, Shi B, Guo H, Zhang Q. The effect of biofeedback treatment for children with non-neurogenic voiding dysfunction: A systematic review and meta-analysis. Neurourol Urodyn. 2022 Apr;41(4):868-883. doi: 10.1002/nau.24886. Epub 2022 Feb 22. PMID: 35191548. |
Wrong intervention |
|
Qiu S, Bi S, Lin T, Wu Z, Jiang Q, Geng J, Liu L, Bao Y, Tu X, He M, Yang L, Wei Q. Comparative assessment of efficacy and safety of different treatment for de novo overactive bladder children: A systematic review and network meta-analysis. Asian J Urol. 2019 Oct;6(4):330-338. doi: 10.1016/j.ajur.2019.04.001. Epub 2019 Apr 13. PMID: 31768318; PMCID: PMC6872791. |
Wrong comparison |
|
Rhodes C. Effective management of daytime wetting. Paediatr Nurs. 2000 Mar;12(2):14-7. PMID: 11220839. |
No comparison |
|
Saarikoski A, Koppeli R, Taskinen S, Axelin A. Voiding school as a treatment for daytime incontinence or enuresis: Assessing the effectiveness of intervention by measuring changes in wetting episodes. J Pediatr Urol. 2018 Jun;14(3):256.e1-256.e7. doi: 10.1016/j.jpurol.2017.12.015. Epub 2018 Feb 5. PMID: 29452905. |
No comparison |
|
Sumboonnanonda A, Sawangsuk P, Sungkabuth P, Muangsampao J, Farhat WA, Piyaphanee N. Screening and management of bladder and bowel dysfunction in general pediatric outpatient clinic: a prospective observational study. BMC Pediatr. 2022 May 17;22(1):288. doi: 10.1186/s12887-022-03360-9. PMID: 35581653; PMCID: PMC9110931. |
No comparison |
|
Tremback-Ball A, Gherghel E, Hegge A, Kindig K, Marsico H, Scanlon R. The effectiveness of biofeedback therapy in managing Bladder Bowel Dysfunction in children: A systematic review. J Pediatr Rehabil Med. 2018;11(3):161-173. doi: 10.3233/PRM-170527. PMID: 30223405. |
Wrong intervention |
|
Tugtepe H, Thomas DT, Ergun R, Abdullayev T, Kastarli C, Kaynak A, Dagli TE. Comparison of biofeedback therapy in children with treatment-refractory dysfunctional voiding and overactive bladder. Urology. 2015 Apr;85(4):900-4. doi: 10.1016/j.urology.2014.12.031. Epub 2015 Feb 7. PMID: 25669732. |
No comparison |
|
Van den Broeck C, Roman de Mettelinge T, Deschepper E, Van Laecke E, Renson C, Samijn B, Hoebeke P. Prospective evaluation of the long-term effects of clinical voiding reeducation or voiding school for lower urinary tract conditions in children. J Pediatr Urol. 2016 Feb;12(1):37.e1-6. doi: 10.1016/j.jpurol.2015.04.045. Epub 2015 Jul 30. PMID: 26302828. |
No comparison |
|
van Gool JD, de Jong TP, Winkler-Seinstra P, Tamminen-Möbius T, Lax H, Hirche H, Nijman RJ, Hjälmås K, Jodal U, Bachmann H, Hoebeke P, Walle JV, Misselwitz J, John U, Bael A; European Bladder Dysfunction Study (EU BMH1-CT94-1006). Multi-center randomized controlled trial of cognitive treatment, placebo, oxybutynin, bladder training, and pelvic floor training in children with functional urinary incontinence. Neurourol Urodyn. 2014 Jun;33(5):482-7. doi: 10.1002/nau.22446. Epub 2013 Jun 15. PMID: 23775924. |
Wrong comparison |
|
Vasconcelos, M., Lima, E., Caiafa, L., Noronha, A., Cangussu, R., Gomes, S., ... & Colozimo, E. (2006). Voiding dysfunction in children. Pelvic-floor exercises or biofeedback therapy: a randomized study. Pediatric nephrology, 21, 1858-1864. |
Wrong comparison |
|
Vesna ZD, Milica L, Stanković I, Marina V, Andjelka S. The evaluation of combined standard urotherapy, abdominal and pelvic floor retraining in children with dysfunctional voiding. J Pediatr Urol. 2011 Jun;7(3):336-41. doi: 10.1016/j.jpurol.2011.02.028. Epub 2011 Apr 27. PMID: 21527231. |
Wrong comparison |
|
Vijverberg MA, Stortelder E, de Kort LM, Kok ET, de Jong TP. Long-term follow-up of incontinence and urge complaints after intensive urotherapy in childhood (75 patients followed up for 16.2-21.8 years). Urology. 2011 Dec;78(6):1391-6. doi: 10.1016/j.urology.2011.08.055. Epub 2011 Oct 19. PMID: 22014960. |
No comparison |
|
Wiener JS, Scales MT, Hampton J, King LR, Surwit R, Edwards CL. Long-term efficacy of simple behavioral therapy for daytime wetting in children. J Urol. 2000 Sep;164(3 Pt 1):786-90. doi: 10.1097/00005392-200009010-00048. PMID: 10953156. |
No comparison |
|
Yagci S, Kibar Y, Akay O, Kilic S, Erdemir F, Gok F, Dayanc M. The effect of biofeedback treatment on voiding and urodynamic parameters in children with voiding dysfunction. J Urol. 2005 Nov;174(5):1994-7; discussion 1997-8. doi: 10.1097/01.ju.0000176487.64283.36. PMID: 16217376. |
No comparison |
|
Zivkovic VD, Stankovic I, Dimitrijevic L, Kocic M, Colovic H, Vlajkovic M, Slavkovic A, Lazovic M. Are Interferential Electrical Stimulation and Diaphragmatic Breathing Exercises Beneficial in Children With Bladder and Bowel Dysfunction? Urology. 2017 Apr;102:207-212. doi: 10.1016/j.urology.2016.12.038. Epub 2016 Dec 28. PMID: 28040503. |
Wrong comparison |
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 17-07-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS) en/of andere bron. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Belangrijkste wijzigingen t.o.v. vorige versie: Er zijn veertien modules herzien/ontwikkeld:
- Anamnese
- Registratielijsten
- Uroflowmetrie en residubepaling
- Urineonderzoek (urine-incontinentie)
- Urethrocystoscopie
- Echo urinewegen
- Urodynamisch onderzoek
- Urotherapie
- Kinderbekkenfysiotherapie
- Antimuscarinica en mirabegron
- Botuline toxine A
- Methylfenidaat
- Neuromodulatie
- Organisatie van zorg
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor kinderen met functionele urine-incontinentie.
Werkgroep
- Dr. L.L. (Liesbeth) de Wall, kinderuroloog, NVU
- Drs. M.M.C. (Marleen) van den Heijkant, kinderuroloog, NVU
- Drs. M. (Marleen) Trompetter, uroloog (met aantekening voor kinderen), NVU
- Drs. J. (Hans) van der Deure, kinderarts, NVK
- Dr. E. (Ester) de Kleijn, kinderarts, NVK
- Drs. L. (Lieke) Langendonck, kinderarts, NVK
- Dr. A.J. (Anka) Nieuwhof – Leppink, urotherapeut, NVCK
- S. (Saskia) Bruijn, MSc, verpleegkundig specialist kinderurologie, urotherapeut NVCK
- Drs. A.E.H. (Rianne) Stollenga, kinderfysiotherapeut, KNGF/NVFK
- Drs. A. (Astrid) Huijpen, bekkenfysiotherapeut, KNGF/NVFB
- Drs. F.E. (Femke) de Bok, jeugdarts KNMG en arts Maatschappij en Gezondheid in opleiding, AJN
- Drs. E.C. (Esen) Doganer, beleidsadviseur, Stichting Kind en Ziekenhuis
- Drs. A. (Anne) Swinkels, junior projectmanager en beleidsmedewerker Stichting Kind en Ziekenhuis (vervanger van Esen tijdens haar zwangerschapsverlof)
Klankbordgroep
- Drs. B.J.M. (Bernadette) Berendes- van Dijk, bekkenfysiotherapeut, Stichting Bekkenbodem4All
- Dr. H. (Hanny) Cobussen-Boekhorst, verpleegkundig specialist kinderurologie, V&VN
- Drs. V.A.C.T. (Vera) Janssen, verpleegkundig specialist kinderurologie, V&VN
- Drs. W.J.P. (Wies) van Aalst, kinderfysiotherapeut, KNGF/NVKF
Met ondersteuning van
- Drs. D.A.M. (Danique) Middelhuis, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. I.M. (Irina) Mostovaya, senior adviseur en teamleider, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. M. (Janneke) Schultink, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- L.H.M. (Linda) Niesink-Boerboom, Medisch informatiespecialist, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroep |
||||
|
Achternaam werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
De Wall (voorzitter) |
Kinderuroloog Radboudumc Amalia kinderziekenhuis |
Geen |
ZonMw studie: SENS-U studie
Mijn promotie onderzoek bevat diverse artikelen aangaande het onderwerp. Ik kan niet inschatten of dit meer bekendheid zal krijgen door de herziening van de richtlijn. De SENS-U studie betreft een ZonMw gesubsidieerde studie naar de bijdrage van echografische monitoring van de blaas bij ongewild urine verlies. De resultaten van deze studie zullen naar verwachting eind 2024/ begin 2025 op zijn vroegst gepubliceerd worden. Dit zal geen invloed hebben op de huidige revisie. |
Geen restricties |
|
Van den Heijkant |
(kinder)uroloog in van Weel Bethesda Ziekenhuis |
Geen |
Geen |
Geen restricties |
|
Trompetter |
Uroloog Isala |
Commissiewerk binnen het ziekenhuis |
Participeert in de SENS-U studie. Geen persoonlijk belang. |
Geen restricties |
|
Van der Deure |
Kinderarts, Deventer Ziekenhuis |
Geen |
Geen |
Geen restricties |
|
De Kleijn |
Kinderarts (Albert Schweitzer Ziekenhuis) |
Voorzitter centrale Opleidingscommissie, (Albert Schweitzer Ziekenhuis) onbetaald Opleider kindergeneeskunde, (Albert Schweitzer Ziekenhuis) onbetaald |
Geen |
Geen restricties |
|
Langendonck |
Kinderarts in Langeland Ziekenhuis Zoetermeer |
Geen |
Geen |
Geen restricties |
|
Nieuwhof-Leppink |
Coordinator Urotherapie Wilhelmina kinderziekenhuis UMC Utrecht |
-International children's continence society: board member -European society pediatric urology research commissie lid beide zijn onbetaalde functies
Gedetacheerd van uit het UMCU voor 2 uur in de week bij hogeschool utrecht HU als coordinator Urotherapie cursus. |
Studie naar de SENSU als evt toegevoegde waarde in de behandeling van kinderen met incontinentie. |
Geen restricties |
|
Bruijn |
Verpleegkundig specialist kinderurologie / urotherapeut AmsterdamUMC/ Emma Kinderziekenhuis |
Geen |
Geen |
Geen restricties |
|
Stollenga |
Kinderfysiotherapeut en kinderbekkenfysiotherapeut bij Jan van Rijn Kinderfysiotherapie (betaald)
|
Penningmeester NVCK (onbetaald) Lid specialistenregistratie bij NVFK (betaald) |
Geen |
Geen restricties |
|
Huijpen |
Fysiotherapeut, Bekkenfysiotherapeut MSc, specialisatie in kinderen met problemen met de zindelijkheid Eigenaar praktijk Fysio Centrum Zaanland betaalde functie |
Werkzaam in eigen praktijk als algemeen- bekken- en kinderbekkenfysiotherapeut Leidinggevende taken (personeel en planning) Werkzaan in het Zaans Medisch Centrum in de kliniek en op de gezamenlijk poli in samenwerking met kinderarts, Urotherapeut, kinderpsycholoog, uroloog en gynaecoloog betaalde functie |
Onze fysiotherapie praktijk werkt zelfstandig en we hebben productie afspraken met het Zaans Medisch Centrum, er is geen direct verband met de richtlijn. |
Geen restricties |
|
De Bok |
Jeugdarts KNMG, arts Maatschappij en Gezondheid in opleiding, AJN |
Promotie-onderzoek naast specialistenopleiding (betaald, in dienstverband als aios bij SBOH) Bestuurslid regio-bestuur AJN Jeugdartsen Noord Nederland (onbetaald) |
Betreft mijn eigen promotie-onderzoek, het onderwerp is ongerelateerd aan dat van deze richtlijn en commissie |
Geen restricties |
|
Doganer |
Junior projectmanager/beleidsmedewerker bij Stichting Kind en ZIekenhuis |
Geen |
Geen |
Geen restricties |
|
Swinkels |
Junior Projectmanager en beleidsmedewerker Stichting Kind en Ziekenhuis |
Geen |
Geen |
Geen restricties |
|
Klankbordgroep |
||||
|
Achternaam klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Berendes – van Dijk |
Geen, gepensioneerd |
Geen |
Geen |
Geen restricties |
|
Cobussen – Boekhorst |
Verpleegkundig specialist kinderurologie en functionele urologie Amalia kinderziekenhuis, Radboudumc Postbus 9101 , 6500 HB Nijmegen huispost 723 |
Verzorgen van scholingen en presentaties (betaald of in werktijd) bij diverse groepen en verenigingen. -lid van Female LUTS werkgroep van de EAU
Lid project van Astellas voor eerste lijn over volwassenen met klachten van OAB. |
Lid van ICEF (International Clinical Education Forum) van Hollister inc. (stoma en katheter materiaal) = betaalde functie |
Geen restricties |
|
Janssen |
Verpleegkundig specialist (kinder)urologie (betaald) parttime, en functionele urologie radboud UMC Amalia Ziekenhuis |
Presentaties voor oa. V&vn urologie (betaald), webinair Gag spoelingen (betaald via goodlife) |
Lid CAB Hollister: adviescommissie stoma en katheter materiaal, betaald |
Geen restricties |
|
Van Aalst |
Kinderbekkenfysiotherapeut in Radboudumc |
Geen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door Stichting Bekkenbodem4All, Stichting Kind en Ziekenhuis, Patiëntenfederatie Nederland, Stichting Bedplassen en Vereniging Samenwerkende Ouder- en Patiëntenorganisaties uit te nodigen voor de schriftelijke knelpuntenanalyse en was Stichting Kind en Ziekenhuis afgevaardigd in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie per module ook “Waarden en voorkeuren van patiënten”). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Bekkenbodem4All, Stichting Kind en Ziekenhuis, Patiëntenfederatie Nederland, Stichting Bedplassen en Vereniging Samenwerkende Ouder- en Patiëntenorganisaties en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Urotherapie & kinderbekken-fysiotherapie (exclusief neuromodulatie) |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat [het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet OF het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft]. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor kinderen met functionele urine-incontinentie. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodule (NVU, 2008) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door Stichting Bekkenbodem4All, Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF) en AJN Jeugdartsen Nederland via een schriftelijke knelpuntenanalyse. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder het kopje ‘Onderbouwing’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.