Zelfdilatatie na urethrastrictuur
Uitgangsvraag
Wat is de plaats van en het beleid rond postoperatieve zelfdilatatie na een endoscopische behandeling van een urethrastrictuur?
Aanbeveling
Na een endoscopische behandeling van een urethrastrictuur
De commissie kan vanwege onvoldoende wetenschappelijk bewijs geen advies geven over het verrichten van postoperatieve zelfkatheterisatie, de wenselijke duur van postoperatieve zelf-dilatatie en evenmin over de te gebruiken dilatator.
Zelfdilatatie is alleen een palliatieve optie voor patiënten die niet in aanmerking kunnen of willen komen voor een urethraplastiek.
Samengevat (zie de module ‘Indicaties kijkoperatie & urethradilatatie’, ‘Zelfdilatatie na urethrastrictuur’ en ‘Criteria voor urethraplastiek’):
De commissie adviseert in geval van een primaire urethrastrictuur korter dan 2 cm een Sachse-procedure of een dilatatie te verrichten zonder postoperatieve zelfdilatatie.
In geval van een recidief strictuur is de urethraplastiek de behandeling van keuze.
Indien patient niet geschikt is voor een urethraplastiek kan een Sachse-procedure of dilatatie worden gecombineerd met postoperatieve zelfdilatatie.
Overwegingen
Kwaliteit van bewijs
Wat de gewenste en ongewenste effecten betreft van zelf-dilatatie per se, de duur ervan, de gebruikte typen katheters en gels is er zeer lage kwaliteit van bewijs.
Waarden en voorkeuren
Niet van toepassing omdat geen concreet advies wordt gegeven met betrekking tot postoperatieve zelf-dilatatie na een endoscopische ingreep.
Kosten en middelen
Niet van toepassing omdat geen concreet advies wordt gegeven met betrekking tot postoperatieve zelf-dilatatie na een endoscopische ingreep.
Professioneel perspectief
De richtlijncommissie beschouwt postoperatieve zelfdilatatie na een endoscopische behandeling als een palliatieve optie. Deze opvatting is gebaseerd op onderzoek van Steenkamp en Heyns dat laat zien dat herhalen van een endoscopische behandeling in versneld tempo tot recidieven leidt (zie de module ‘Criteria voor urethraplastiek’, overwegingen). Daarbij komt dat er een zeer grote mate van onzekerheid bestaat over de effectiviteit van zelf-dilatatie na een endoscopische ingreep.
Voor patienten die niet geschikt zijn voor een urethraplastiek of hiervoor bewust niet kiezen, is intermitterende dilatatie een optie.
Rationale van de aanbeveling(en)
De richtlijncommissie beschouwt postoperatieve zelfdilatatie na een endoscopische behandeling als een palliatieve optie. Deze opvatting is gebaseerd op onderzoek van Steenkamp en Heyns dat laat zien dat herhalen van een endoscopische behandeling in versneld tempo tot recidieven leidt. Daarbij komt dat er een zeer grote mate van onzekerheid bestaat over de effectiviteit van zelf-dilatatie na een endoscopische ingreep.
Onderbouwing
Intermitterende zelf-dilatatie is een techniek met het doel de terugkeer van een urethrastrictuur te voorkomen dan wel het risico hierop te verminderen. Bij deze techniek brengt de man regelmatig een dunne katheter (doorgaans een disposable) in de urinebuis in. Verondersteld wordt dat de snijranden van een strictuur hierdoor niet of minder snel aan elkaar plakken.
Er zijn echter neveneffecten, zoals risico op een infectie en een kleine kans op beschadiging van de urethra.
De commissie heeft ten behoeve van de afweging van de pro’s en contra’s van intermitterende zelf-dilatatie de literatuur hierover op een rij gezet.
Definities
Endoscopische behandeling: interne urethrotomia interna (Sachse) en endoscopische dilatatie met filiforme bougies en followers.
Postoperatieve dilatatie:
- sondes met beperkte lengte, bijvoorbeeld WycathR Meatal Dilators, of varianten van een antieke dilatator, zoals die van Cook;

- katheters met lengte om tot in de blaas te gaan maar stomp op het uiteinde (dus zonder gaatjes; de blaas kan hier niet mee geledigd worden);
- een ‘’gewone’’ katheter waarmee de patiënt tot in de blaas gaat: op deze manier weet je zeker dat de patiënt voldoende diep is gegaan;
- diverse andere vormen van de tip van de catheter, waardoor passage door de urethra wordt vergemakkelijkt
1. Vergelijking zelf-dilatatie versus geen zelf-dilatatie
|
Zeer laag GRADE |
Recidief urethrastrictuur Zelf-dilatatie zou het optreden van een recidief urethrastrictuur enigszins kunnen verminderen bij patiënten met een eerste of recidief strictuur van de urethra anterior van variabele grootte (1-4 cm) die een urethrotomia interna hebben ondergaan. Bron Afridi 2010; Bodker 1992; Husmann 2006; Khan 2011; Kjaergaard 1994; Matanhelia 1995 |
|
Zeer laag GRADE |
Urineweginfecties Zelf-dilatatie zou het optreden urineweginfecties kunnen verminderen bij patiënten met een eerste of recidief strictuur van de urethra anterior (van onbekende grootte) die een urethrotomia interna hebben ondergaan, maar we zijn hier zeer onzeker over Bron Khan 2011; Kjaergaard 1994 |
|
Onbepaald GRADE |
Aanvaardbaarheid Zelf-dilatatie zou voor vrijwel alle patiënten met een eerste of recidief strictuur van de urethra anterior (van onbekende grootte) die een urethrotomia interna hebben ondergaan, aanvaardbaar zijn maar we zijn hier zeer onzeker over. Bron Khan 2011; Matanhelia 1995; Kjaergaard 1994 |
2. vergelijking verschillende duur voor zelf-dilatatie (6 maanden en 12 maanden of langer)
|
Zeer laag GRADE |
Recidief urethrastrictuur Zelf-dilatatie gedurende 12 maanden of langer zou bij patiënten met een eerste of recidief strictuur van de urethra (onbekende grootte) die een urethrotomia interna hebben ondergaan, het optreden van een recidief urethrastrictuur kunnen verminderen maar we zijn hier zeer onzeker over. Bron Harriss 1994; Tammela 1993 |
|
Onbepaald GRADE |
Aanvaardbaarheid Zelf-dilatatie gedurende 12 maanden of langer zou voor vrijwel alle patiënten met een eerste of recidief strictuur van de urethra (onbekende grootte) die een urethrotomia interna hebben ondergaan, aanvaardbaar zijn maar we zijn hier zeer onzeker over. Bron Harriss 1994 |
3. Vergelijking van verschillende gels voor gebruik van de katheter
|
Zeer laag GRADE |
Recidief urethrastrictuur Een gel met triamcinolon 1% zou in vergelijking met een op water gebaseerde gel het risico op een eerste recidief bij patiënten met een strictuur < 1,5 cm die een urethrotomia interne hebben ondergaan, kunnen verminderen, maar we zijn hier zeer onzeker over. Bron Hosseini 2008 |
4. Vergelijking van verschillende type katheters (lage frictie hydrofiele katheter en Nelaton polyvinylchloride katheter)
|
Zeer laag
GRADE |
Recidief urethrastrictuur Lage frictie hydrofiele katheters zouden in vergelijking met een PVC-katheter het risico van een eerste recidief urethrastrictuur bij patiënten met een strictuur < 2 cm die een urethrotomia interna hebben ondergaan, kunnen verminderen maar we zijn hier zeer onzeker. Bron Sallami 2011 |
|
Zeer laag
GRADE |
Urineweginfectie, klachten & symptomen lagere urinewegen (prostatis, bloeding urethra) Lage frictie hydrofiele katheters zouden in vergelijking met een PVC-katheter het risico van genoemde ongewenste effecten bij patiënten met een strictuur < 2 cm die een urethrotomia interna hebben ondergaan, kunnen verminderen maar we zijn hier zeer onzeker over. Bron Sallami 2011 |
|
Onbepaald
|
Aanvaardbaarheid Lage frictie hydrofiele katheters zouden in vergelijking met een PVC-katheter meer aanvaardbaar zijn voor patiënten met een strictuur < 2 cm die een urethrotomia interna hebben ondergaan, maar we zijn hier zeer onzeker over. Bron Sallami 2011 |
In de systematische review van Jackson et al. (2014) werden 11 trials geïncludeerd met in totaal 776 mannen.
In 6 trials werd intermitterende zelf-dilatatie na optische urethrotomie vergeleken met een controlegroep die geen zelf-dilatatie verrichtte, en eveneens optische urethrotomie had ondergaan (Afridi 2010; Bodker 1992; Husmann 2006; Khan 2011; Kjaergaard 1994; Matanhelia 1995). In drie trials was de leeftijd van de studiedeelnemers onbekend (Afridi 2010; Husmann 2006; Matanhelia 1995). In de andere studies varieerde de leeftijd van 18-87 jaar. De studieomvang varieerde van 51 (Matanhelia 1995) tot 146 mannen (Afridi 2010). In alle studies behalve die van Husmann 2006 (betrof specifiek de peniele urethra) werd de plaats van de strictuur als anterieur omschreven. In één studie (Bodker 1992) werd expliciet vermeld dat het mannen met recidiverende urethrastricturen betrof.
Twee trials vergeleken programma’s van intermitterende zelf-dilatatie met een verschillende duur met elkaar (Harriss 1994; Tammela 1993). Alle studiedeelnemers ondergingen optische urethrotomie. Hun leeftijd was gemiddeld 60-70 jaar. In beide studies betrof het mannen met recidiverende urethrastricturen.
Twee trials vergeleken verschillende middelen van zelf-dilatatie met elkaar (Hosseini 2008; Sallami 2011). Beide studies vermelden niet of het patiënten met recidiverende urethrastricturen betrof. In de studie van Sallami 2011 betrof het mannen met een strictuur van de urethra anterior of posterior. In de andere studie werd dit niet vermeld. De leeftijd in de studies varieerde van 10 tot 86 jaar.
1. Vergelijking zelf-dilatatie versus geen zelf-dilatatie
Risico op een recidiverende urethrastrictuur
Zes trials (Afridi 2010; Bodker 1992; Husmann 2006; Khan 2011; Kjaergaard 1994; Matanhelia 1995) met in totaal 404 studiedeelnemers konden worden gecombineerd. Let wel: de diverse onderzoekers hanteerden verschillende definities voor de aanwezigheid van een recidief. Bijvoorbeeld op basis van beeldvorming (urethrografie, cytoscopie) of van de maximale urinestroom. Alleen Husmann 2006 definieerde een recidief als de noodzaak tot een heringreep.
Combineren van de zes trials laat zien dat zelf-dilatatie het relatief risico op een recidief met 30% vermindert (figuur 1). Het absolute risico vermindert met bijna 19%. Dit komt overeen met een number needed to treat van 5: er wordt 1 extra recidief voorkomen bij postoperatieve zelf-dilatatie door vijf patiënten. De studies laten echter sterk wisselende effectgroottes zien. Deze variëren van vermindering van het risico met meer dan 70% (Kjaergaard 1994) tot 0% (Husmann 2006).
Figuur 1. Risico op een recidief urethrastructuur

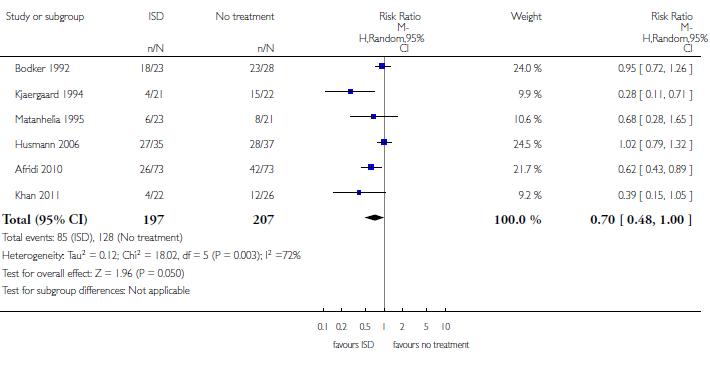
Bron: Jackson et al. (2014)
Urethratrauma, urineweginfectie, klachten & symptomen lage urinewegen
Bodker 1992 rapporteerde dat 2 van de 28 patiënten (7,1%) in de interventiegroep urethrabloedingen hadden. Bij de overige 92,9% kwamen geen hematurie of infecties voor. Percentage ongewenste effecten in de controlegroep werd niet vermeld.
Khan 2011 rapporteerde dat 4 van de 22 patiënten (18,1%) in de interventiegroep urineweginfecties hadden, gedefinieerd als een of meer positieve urinekweken of epididymitis, hadden, en 4 van de 26 patiënten (15,3%) in de controlegroep.
Kjaergaard 1994 rapporteerde minder bacteriurie en epididymitis bij patiënten uit de zelf-dilatatie groep dan uit de groep zonder zelf-dilatatie, namelijk 1 op de 21 (4,7%) versus 5 op de 22 patiënten (22,7%) (p = 0.4).
Matanhelia 1995 rapporteerde dat er geen urineweginfecties optraden bij patiënten uit de zelf-dilatatie groep.
Een meta-analyse van de ongewenste uitkomsten (urineweginfecties) die werden gerapporteerd in Khan 2011 en Kjaergaard 1994, wijst op een kleiner risico hierop in de zelf-dilatatiegroep (RR=0,60; 95% BI: 0,11-3,21); zie figuur 2. Voorzichtigheid is echter geboden: de uitkomst is niet statistisch significant, en de groottes van de risico’s in beide studies verschillen nogal (1,18 versus 0,21).
Figuur 2. Ongewenste effecten
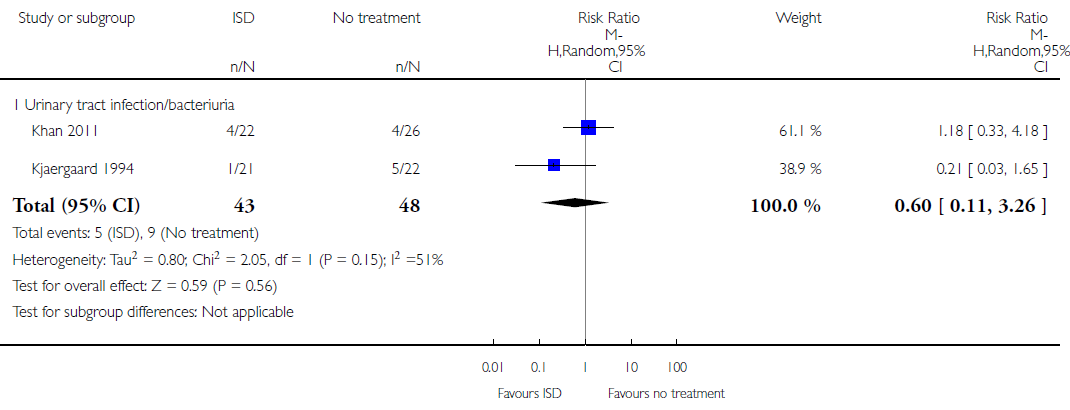
 Bron: Jackson et al. (2014)
Bron: Jackson et al. (2014)
Aanvaardbaarheid/drop-outs
Drie studies (Khan 2011; Matanhelia 1995; Kjaergaard 1994) rapporteerden over de aanvaardbaarheid van (de methode van) zelf-dilatatie, zonder aan te geven hoe de aanvaardbaarheid hiervan werd vastgesteld. In deze drie studies vonden patiënten (de methode van) zelf-dilatatie – in het algemeen – aanvaardbaar.
Kosten, hospitalisatie, patiënttevredenheid of kwaliteit van leven
In geen van de trials werd over deze uitkomstmaten gerapporteerd.
Kwaliteit van bewijs
Voor de uitkomstmaten recidief urethrastrictuur en urineweginfectie is de kwaliteit van bewijs zeer laag: de methodologische kwaliteit van de studies laat sterk te wensen over vanwege inadequate blindering van de toewijzing aan interventie- en controlegroep, en ontbreken van blindering van de uitkomstenbeoordelaar, en er is grote variatie in de recidiefpercentages tussen de studies (inconsistentie).
Voor de overige uitkomstmaten kon de kwaliteit van bewijs niet worden bepaald: ofwel getalsmatige informatie ontbrak ofwel er werd over deze uitkomstmaten niet gerapporteerd.
2. vergelijking verschillende duur voor zelf-dilatatie (6 maanden en 12 maanden of langer)
Risico op een recidiverende urethrastrictuur
De 2 trials waarin specifieke programma’s van intermitterende zelf-dilatatie met elkaar vergeleken werden (Harriss 1994; Tammela 1993) konden niet worden gecombineerd vanwege verschillende wijzen van rapporteren. Harriss 1994 stelde een recidief vast op basis van cystoscopie. Tammela 1993 deed dit op basis van de noodzaak tot verdere behandeling.
Tammela 1992 vergeleek intermitterende zelf-dilatatie gedurende 6 maanden met intermitterende zelf-dilatatie gedurende 12 maanden. Na 12 maanden follow-up hadden 3 van de 24 patiënten (12,5%) een recidief. In de groep die 6 maanden zelf-dilatatie verrichtten hadden 2 van de 24 patiënten (8,3%) een recidief. Dit zou betekenen dat de groep die het kortste zelf-dilatatie verrichtte een kleinere kans op een recidief had (RR 0,67; 95% BI: 0,12- 3,64).
In de studie van Harriss 1994 verrichtte een groep zelf-dilatatie gedurende 6 maanden, de andere groep minimaal 12 maanden. In de laatste groep waren er 28 die langer dan 12 en minder dan 36 maanden zelf-dilatatie verrichtten, en 10 die dit tot 78 maanden volhielden. In de laatste groep had 0% [0/10] een recidief, in de ’12-36-maanden’ groep was dit 14% (4 op de 28 patiënten), en in de groep die tot 6 maanden zelf-dilatatie verrichtte was dit 40% [19 van de 49 patiënten). Minimaal 12 maanden zelf-dilatatie verrichten zou helpen om de strictuur te ‘stabiliseren’.
Urethratrauma, urineweginfectie, klachten & symptomen lage urinewegen, kosten, hospitalisatie, patiënttevredenheid of kwaliteit van leven
In deze trials werd ofwel niet over deze uitkomstmaten gerapporteerd of werd nagelaten de uitkomsten voor sommige uitkomstmaten (sterfte, [a-]symptomatische bacteriurie) gescheiden voor interventie- en controlegroep te rapporteren.
Aanvaardbaarheid
In beide trials werd de aanvaardbaarheid niet formeel onderzocht. Harriss 1994 merkte op dat ‘de meeste patiënten, de kwetsbare ouderen inbegrepen, zelf-dilatatie erg gemakkelijk vonden om toe te passen’.
Kwaliteit van bewijs
Voor de uitkomstmaat recidief urethrastrictuur is de kwaliteit van bewijs zeer laag: de methodologische kwaliteit van de studies laat sterk te wensen over vanwege inadequate blindering van de toewijzing aan interventie- en controlegroep, en ontbreken van blindering van de uitkomstenbeoordelaar, en de twee studies laten tegenstrijdige resultaten zien (inconsistentie).
Voor de overige uitkomstmaten kon de kwaliteit van bewijs niet worden bepaald: er werd over deze uitkomstmaten niet (apart voor interventie- en controlegroep) gerapporteerd of getalsmatige informatie ontbrak.
3. Vergelijking van verschillende gels voor gebruik van de katheter
Hosseini 2008 onderzocht het effect van verschillende soorten gels om de katheter voor intermitterende zelf-dilatatie mee in te smeren, namelijk een gel of zalf met triamcinolon 1% (een synthetisch corticosteroïd) en een op water gebaseerde gel.
Risico op een recidiverende urethrastrictuur
Met katheters waarvoor triamcinolon 1% gel werd gebruikt, kwamen minder recidiverende urethrastricturen voor dan met katheters waarvoor een op water gebaseerde gel werd gebruikt: 30% (9 van de 20 patiënten) versus 44% (15 van de 34 patiënten) (RR: 0,68; 95% BI 0,35 – 1,32). Dit verschil van 14% is niet statistisch significant.
Urineweginfectie, klachten & symptomen lage urinewegen, kosten, hospitalisatie, patiënttevredenheid of kwaliteit van leven, aanvaardbaarheid
Hierover werd niet gerapporteerd.
Kwaliteit van bewijs
Voor de uitkomstmaat recidief urethrastrictuur is de kwaliteit van bewijs zeer laag: de methodologische kwaliteit van de studie laat sterk te wensen over vanwege inadequate blindering van de toewijzing aan interventie- en controlegroep, en ontbreken van blindering van de uitkomstenbeoordelaar, en het betrouwbaarheidsinterval is zeer breed vanwege de kleine studieomvang (onnauwkeurigheid). Voor de overige uitkomstmaten kon de kwaliteit van bewijs niet worden bepaald: er werd over deze uitkomstmaten niet gerapporteerd.
4. Vergelijking van verschillende type katheters (lage frictie hydrofiele katheter en Nelaton polyvinylchloride katheter)
Sallami 2011 vergeleek het effect van een lage frictie hydrofiele katheter met een standaard Nelaton polyvinylchloride (PVC) katheter.
Risico op een recidiverende urethrastrictuur
Met lage frictie hydrofiele katheters kwamen minder recidieven van de urethrastricturen voor dan met een PVC-katheter: 6% (2 van de 21 patiënten) versus 25% (7 van de 28 patiënten) (RR: 0,26; 95% BI: 0,06 – 1,14). Dit verschil van 19% is niet statistisch significant.[1]
Urineweginfectie, klachten & symptomen lage urinewegen
Met lage frictie hydrofiele katheters traden minder bijwerkingen (prostatitis, bloeding van de urethra, bacteriurie) op dan met een PVC-katheter: 3% (1 van de 21 patiënten) versus 25% (7 van de 28 patiënten) (RR: 0,13; 95% BI: 0,02 –0,98). Dit verschil van 22% is statistisch significant.
Kosten, hospitalisatie, patiënttevredenheid of kwaliteit van leven
Hierover werd niet gerapporteerd.
Aanvaardbaarheid
De aanvaardbaarheid werd niet formeel onderzocht. Sallami 2011 merkte op dat 30 van de 31 mannen die intermitterende zelfdilatatie verrichtten met lage frictie hydrofiele katheter de katheter volledig aanvaardbaar vonden. In de PVC-groep vonden 7 op de 28 mannen de gebruikte katheter volledig aanvaardbaar.
Kwaliteit van bewijs
Voor de uitkomstmaten recidief urethrastrictuur en neveneffecten (prostatitis, bacteriurie, bloeding van de urethra) is de kwaliteit van bewijs zeer laag: de methodologische kwaliteit van de studie laat sterk te wensen over vanwege inadequate blindering van de toewijzing aan interventie- en controlegroep, en ontbreken van blindering van de uitkomstenbeoordelaar, en het betrouwbaarheidsinterval is zeer breed vanwege de kleine studieomvang (onnauwkeurigheid).
Voor de overige uitkomstmaten kon de kwaliteit van bewijs niet worden bepaald: ofwel getalsmatige informatie ontbrak ofwel er werd over deze uitkomstmaten niet gerapporteerd.
[1] In de review van Jackson et al (2014) zijn de totalen van interventie- en controlegroep verwisseld, en is daarom het relatieve risico opnieuw berekend.
Om de uitgangsvraag te kunnen beantwoorden heeft de werkgroep drie systematische literatuuranalyses gepland met de volgende PICO-vraagstelling:
- Wat is het effect van postoperatieve zelfdilatatie (m.b.v. Dilacath of dilatatie in het kader van clean intermittent self catheterisation) versus geen postoperatieve zelfdilatatie bij mannen met een eerste of recidief urethrastrictuur (elke locatie) die een optische urethrotomia interna (Sachse) of endoscopische dilatatie met filiforme bougies en followers hebben ondergaan?
- Wat is het effect van de duur van postoperatieve zelfdilatatie?
- Wat is het effect van verschillende gels voor postoperatieve dilatatie?
- Wat is het effect van verschillende typen katheters (lage frictie hydrofiele katheter en Nelaton polyvinylchloride katheter) voor postoperatieve dilatatie?
|
Selectie- en exclusiecriteria |
|
|
Type studies |
|
|
Type patiënten |
|
|
Type interventies |
|
|
Type uitkomstmaten |
|
|
Follow-up duur |
|
|
Type setting |
|
|
Exclusiecriteria |
|
In de databases Medline (OVID) en CDSR/Central is met relevante zoektermen vanaf 2014 gezocht naar relevante studies. Uitgangspunt voor de zoekactie is een de Cochrane Review van Jackson et al. (2014). De zoekstrategie van deze review werd gebruikt voor een update van deze review. De literatuurzoekactie leverde 107 treffers op. Studies werden geselecteerd op grond van de hiervoor vermelde selectie- en exclusiecriteria. Op basis van titel, abstract en zo nodig de fulltext werden geen recente studies geïdentificeerd om te kunnen toevoegen aan de hiervoor genoemde Cochrane review.
- Afridi NG, Khan M, Nazeem S, Hussain A, Ahmad S, Aman Z. Intermittent urethral self dilatation for prevention of recurrent stricture. Journal of Postgraduate Medical Institute 2010;24(3):23943.
- Bodker A, Ostri P, Rye-Andersen J, Edvardsen L, Struckmann J. Treatment of recurrent urethral stricture by internal urethrotomy and intermittent self-catheterization: a controlled study of a new therapy. Journal of Urology 1992;148(2 Pt 1):30810.
- Harriss DR, Beckingham IJ, Lemberger RJ, Lawrence WT. Long-term results of intermittent low-friction selfcatheterization in patients with recurrent urethral strictures. British Journal of Urology 1994;74(6):7902.
- Hosseini J, Kaviani A, Golshan AR. Clean intermittent catheterization with triamcinolone ointment following internal urethrotomy. Urology Journal 2008;5(4):2658.
- Husmann DA, Rathbun SR. Long-term followup of visual internal urethrotomy for management of short (less than 1 cm) penile urethral strictures following hypospadias repair. Journal of Urology 2006;176(4 Pt 2):173841.
- Jackson MJ, Veeratterapillay R, Harding CK, Dorkin TJ. Intermittent self-dilatation for urethral stricture disease in males. Cochrane Database of Systematic Reviews 2014, Issue 12.
- Khan S, Khan RA,Ullah A, ul Haq F, ur Rahman A, Durrani SN, et al.Role of clean intermittent self catheterisation (CISC) in the prevention of recurrent urethral strictures after internal optical ure-throtomy. Journal of Ayub Medical College, Abbottabad : JAMC 2011;23(2):225.
- Kjaergaard B, Walter S, Bartholin J, Andersen JT, Nohr S, Beck H, et al.Prevention of urethral stricture recurrence using clean intermittent self-catheterization. British Journal of Urology 1994;73(6):6925.
- Matanhelia SS, Salaman R, John A, Matthews PN. A prospective randomized study of self-dilatation in the management of urethral strictures. Journal of the Royal College of Surgeons of Edinburgh 1995;40(5):2957.
- Tammela TL, Permi J, Ruutu M, Talja M. Clean intermittent self-catheterization after urethrotomy for recurrent urethral strictures. Annales Chirurgiae et Gynaecologiae - Supplementum 1993;206:803.
GRADE summary of findings tables
|
Self dilatation compared to no self-dilatation for prevention recurrence urethral stricture |
|||||
|
Bibliography: Jackson MJ, Veeratterapillay R, Harding CK, Dorkin TJ. Intermittent self-dilatation for urethral stricture disease in males. Cochrane Database of Systematic Reviews 2014, Issue 12. |
|||||
|
Outcomes |
№ of participants |
Quality of the evidence |
Relative effect |
Anticipated absolute effects |
|
|
Risk with no self-dilatation |
Risk difference with self dilatation |
||||
|
recurrence urethral stricture (recurrence) |
404 |
⨁◯◯◯ |
RR 0.70 |
618 per 1.000 |
186 fewer per 1.000 |
|
Urinary Tract Infection / Bacteruria (UTI) |
91 |
⨁◯◯◯ |
RR 0.60 |
188 per 1.000 |
75 fewer per 1.000 |
|
*The risk in the intervention group (and its 95% confidence interval) is based on the assumed risk in the comparison group and the relative effect of the intervention (and its 95% CI). |
|||||
|
GRADE Working Group grades of evidence |
|||||
- Downgraded by two levels for risk of bias: all six trials comprising the quantitative synthesis were judged high risk of bias in two or more domains, i.e. concealment of allocation and blinding were inadequate or absent.
- Downgraded by two levels because of large I2 and huge variation of effect sizes
- Not downgraded because imprecision partly results from inconsistency
Author(s): JJA de Beer; BS Niel-Weise
Date:
Question: Short term self-dilatation compared to long term dilatation for prevention of recurrence of urethral stricture
Setting:
Bibliography: Jackson MJ, Veeratterapillay R, Harding CK, Dorkin TJ. Intermittent self-dilatation for urethral stricture disease in males. Cochrane Database of Systematic Reviews 2014, Issue 12.
|
Quality assessment |
№ of patients |
Effect |
Quality |
Importance |
||||||||
|
№ of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
short term self-dilatation |
long term dilatation |
Relative |
Absolute |
||
|
Recurrence urethral stricture (follow up: range 6 months to 78 months; assessed with: different methods) |
||||||||||||
|
2 |
randomised trials |
very serious 1 |
serious 2 |
not serious |
not serious |
none |
22/73 (30.1%) |
6/62 (9.7%) |
not estimable |
not estimable |
⨁◯◯◯ |
CRITICAL |
CI: Confidence interval
- downgraded by two levels because of inadequate / absent concealment of allocation and blinding
- 2 studies have contradictory results
|
Self-dilatation triamcinolon gel compared to self-dilatation water-based gel for prevention of recurrence of urethral stricture |
|||||
|
Bibliography: Jackson MJ, Veeratterapillay R, Harding CK, Dorkin TJ. Intermittent self-dilatation for urethral stricture disease in males. Cochrane Database of Systematic Reviews 2014, Issue 12. |
|||||
|
Outcomes |
№ of participants |
Quality of the evidence |
Relative effect |
Anticipated absolute effects |
|
|
Risk with self-dilatation water-based gel |
Risk difference with self-dilatation triamcinolon gel |
||||
|
recurrence urethral stricture (recurrence) |
64 |
⨁◯◯◯ |
RR 0.68 |
441 per 1.000 |
141 fewer per 1.000 |
|
*The risk in the intervention group (and its 95% confidence interval) is based on the assumed risk in the comparison group and the relative effect of the intervention (and its 95% CI). |
|||||
|
GRADE Working Group grades of evidence |
|||||
- Downgraded by two levels because of serious attrition bias and inadequate concealment of allocation
- Not applicable; 1 study
- Less than 300 events and confidence interval crosses thresholds for appreciabele benefit (0.75) and harm (1.25).
Self-dilatation low friction hydrophilic catheter compared to self-dilatation standard Nelaton polyvinyl chloride catheter be used for prevention of recurrence of urethral stricture |
|||||
|
Bibliography: Jackson MJ, Veeratterapillay R, Harding CK, Dorkin TJ. Intermittent self-dilatation for urethral stricture disease in males. Cochrane Database of Systematic Reviews 2014, Issue 12. |
|||||
|
Outcomes |
№ of participants |
Quality of the evidence |
Relative effect |
Anticipated absolute effects |
|
|
Risk with self-dilatation standard Nelaton polyvinyl chloride catheter |
Risk difference with self-dilatation low friction hydrophilic catheter |
||||
|
recurrence urethral stricture (recurrence) |
59 |
⨁◯◯◯ |
RR 0.26 |
250 per 1.000 |
185 fewer per 1.000 |
|
Adverse effects (prostatis, bacteriruria, urtethral bleeding) (AE) |
59 |
⨁◯◯◯ |
RR 0.13 |
250 per 1.000 |
218 fewer per 1.000 |
|
*The risk in the intervention group (and its 95% confidence interval) is based on the assumed risk in the comparison group and the relative effect of the intervention (and its 95% CI). |
|||||
|
GRADE Working Group grades of evidence |
|||||
- Downgraded by two levels because of inadequate / absent concealment of allocation and blinding
- Not applicable; 1 study
- Much less than 300 events
Beoordelingsdatum en geldigheid
Publicatiedatum : 16-01-2018
Beoordeeld op geldigheid : 02-01-2018
Uiterlijk in 2022 bepaalt het bestuur van de Nederlandse Vereniging voor Urologie of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Urologie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door J.J.A. de Beer, zelfstandig richtlijnmethodoloog en B.S. Niël-Weise, zelfstandig richtlijnmethodoloog, en werd gefinancierd uit [de Kwaliteitsgelden Medisch Specialisten (SKMS) of andere bron].
Doel en doelgroep
Doel
Het doel van het project is het ontwikkelen van een up-to-date multidisciplinaire richtlijn voor de behandeling van volwassen, mannelijke patiënten met verdenking op een urethrastrictuur die een uroloog consulteren, onder meer verwezen via de huisarts, via intercollegiale consulten van andere specialismen, en tertiaire verwijzingen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met urethrastricturen: urologen, radiologen en dermatologen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met urethrastrictuur (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende 2 jaar aan de totstandkoming van de richtlijn.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. R. I. Nooter (voorzitter), uroloog, Franciscus Gasthuis, Rotterdam
- Dr A. de Vylder, uroloog, Jeroen Bosch ziekenhuis ‘s Hertogenbosch
- Drs. G. Pigot, uroloog, VU Medisch Centrum, Amsterdam
- Drs. F.M.J.A. Froeling, uroloog, HagaZiekenhuis, Den Haag
- Dr. K. D'Hauwers, uroloog, Radboud Universitair Medisch Centrum, Nijmegen.
- Prof. dr. J.L.HR. Bosch, uroloog, Universitair Medisch Centrum Utrecht, Utrecht.
- Dr. G.R. Dohle, uroloog, Erasmus Medisch Centrum, Rotterdam
- Dr. E. Taubert, uroloog, Slingeland ziekenhuis, Doetinchem
- Dr. R. L. Miclea, radioloog, Maastricht Universitair Medisch Centrum, Maastricht
Meelezers:
- Dr. E.M. van der Snoek, dermatoloog, Erasmus Medisch Centrum, Rotterdam
Met ondersteuning van:
- Mw. B.S. Niël-Weise, arts-microbioloog (n.p.), zelfstandig richtlijnmethodoloog,
- Deventer
- Dr. ir. J.J.A. de Beer, zelfstandig richtlijnmethodoloog, Utrecht
- Mw. Drs. H. Deurenberg, SIROSS, informatiespecialist, Oss
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Tevens is navraag gedaan naar persoonlijke financiële belangen, belangen door persoonlijke relaties, belangen d.m.v. reputatiemanagement, belangen vanwege extern gefinancierd onderzoek, en belangen door kennisvalorisatie. De belangenverklaringen zijn op te vragen bij de Nederlandse Vereniging voor Urologie, een overzicht vindt u hieronder:
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis Valorisatie |
Overige belangen |
|
Ronald Nooter |
uroloog |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Ann de Veylder |
uroloog |
Werkgroep kinderurologie (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
|
Garry Pigot |
uroloog |
|
|
|
|
|
|
|
|
Frank Froeling |
uroloog |
geen |
geen |
geen |
Lid commissie externe betrekkingen van de NVU. |
geen |
geen |
geen |
|
Kathleen WM d'Hauwers |
uroloog |
Lesgever SOMT Fysiotherapie-opleiding: betaald |
geen |
geen |
Klinefelter patiënten organisatie: geen boegbeeldfunctie, wel contactpunt als mensen met Klinefelter vragen hebben over urologische gerelateerde onderwerpen. Zie ook Cyberpoli - Klinefelter [internet]. |
geen |
geen |
geen |
|
Ruud Bosch |
uroloog |
geen |
Adviseur en Signatory Investigator Ferring AG, Kopenhagen, DK; adviseur Astellas-NL; spreker-faculty lid Update in Urology (AstraZeneca). |
geen |
Lid van EAU richtlijncommissie Urine-incontinentie; voorzitter Continentie Stichting Nederland (CSN). |
geen |
geen |
geen |
|
Gert Dohle |
uroloog |
Medisch adviseur |
Invited speaker astra zeneca en bayer |
geen |
Voorzitter EAU guideline on male hypogonadism |
geen |
geen |
geen |
|
Erich Taubert |
uroloog |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Eric van der Vorm |
arts-microbioloog |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Razvan Miclea |
radioloog |
n.v.t. |
geen |
geen |
geen |
geen |
geen |
geen |
|
Hans de Beer |
richtlijnmethodoloog
|
Lid GRADE Working Group. Lid Guidance committee GRADE network Netherlands. Alle onbetaald. |
geen |
geen |
geen |
geen |
geen |
geen |
|
Barbara Niël-Weise |
richtlijnmethodoloog |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door in de voorbereidende fase de Patiëntenfederatie Nederland te vragen om schriftelijke input omtrent knelpunten en aandachtspunten. Omdat er geen specifieke patiëntenorganisatie voor urethrastrictuur bestaat, heeft de Patiëntenfederatie Nederland de Nederlandse Federatie van Kankerpatiënten organisaties (Leven met blaas- of nierkanker) hiervoor benaderd. Er werden geen knelpunten aangedragen. Tevens heeft de werkgroep een focusgroep bijeenkomst gehouden, waaraan 22 patiënten hebben deelgenomen. Een verslag van de focusgroep is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Het verslag is te vinden bij de aanverwante producten. De conceptrichtlijn is tevens voor commentaar voorgelegd aan deelnemers van de focusgroep en de Patiëntenfederatie Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren (zie ook het implementatieplan bij de aanverwante producten).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwalitieit (www.kwaliteitskoepel.nl). Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreecollaboration.org), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (www.cvz.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Deze werden met de werkgroep besproken. Tevens werd aan de volgende organisaties gevraagd om knelpunten aan te dragen: het Zorginstituut Nederland, Inspectie voor de Gezondheidszorg, Patiëntenfederatie Nederland, Nederlands Huisartsen Genootschap en Zorgverzekeraars Nederland. Er werden geen additionele knelpunten geïdentificeerd.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur conceptuitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews. Voor (internationale) richtlijnen is gezocht op de website van de European Association of Urology en in de databases van National guideline clearinghouse, UpToDate, Guidelines International Network en PubMed. Voor bestaande systematic reviews is gezocht in databases Ovid Medline, Cochrane database of systematic reviews en Epistemonikos.
Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de methodologische checklijsten.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kwaliteit van bewijs (‘quality of evidence’ of ‘certainty of evidence’) werd beoordeeld met behulp van GRADE (Guyatt et al., 2008). GRADE is een methode die per uitkomstmaat van een interventie, of voor een risico- of prognostische factor, een gradering aan de kwaliteit van bewijs toekent op basis van de mate van vertrouwen in de schatting van de effectgrootte (tabel 1 en 2).
Tabel 1 Indeling van de kwaliteit van bewijs (Eng: quality / certainty of evidence) volgens GRADE
|
Hoog |
Er is veel vertrouwen dat het werkelijke effect dicht in de buurt ligt van het geschatte effect. |
|
|
|
|
Matig |
Er is matig vertrouwen in het geschatte effect: het werkelijk effect ligt waarschijnlijk dicht bij het geschatte effect, maar er is een mogelijkheid dat het hiervan substantieel afwijkt. |
|
|
|
|
Laag |
Er is beperkt vertrouwen in het geschatte effect: het werkelijke effect kan substantieel verschillen van het geschatte effect. |
|
|
|
|
Zeer laag |
Er is weinig vertrouwen in het geschatte effect: het werkelijke effect wijkt waarschijnlijk substantieel af van het geschatte effect. |
Tabel 2 De kwaliteit van bewijs (Eng: quality / certainty of evidence) wordt bepaald op basis van de volgende criteria
|
Type bewijs |
Voor studies over interventies: RCT start in de categorie ‘hoog’. Observationele studie start in de categorie ‘laag’. Alle overige studietypen starten in de categorie ‘zeer laag’.
Voor studies over een risico- of prognostische factor: Prospectieve of retrospectieve cohortstudie start in de categorie ‘hoog’. Voor andere studieontwerpen wordt afgewaardeerd via ‘risk of bias’. |
|
|
|
|
|
|
Afwaarderen |
‘Risk of bias’ |
- 1 ernstig - 2 zeer ernstig |
|
|
|
|
|
|
Inconsistentie |
- 1 ernstig - 2 zeer ernstig |
|
|
|
|
|
|
Indirect bewijs |
- 1 ernstig - 2 zeer ernstig |
|
|
|
|
|
|
Onnauwkeurigheid |
- 1 ernstig - 2 zeer ernstig |
|
|
|
|
|
|
Publicatiebias |
- 1 waarschijnlijk - 2 zeer waarschijnlijk |
|
|
|
|
|
|
|
|
|
Opwaarderen |
Groot effect |
+ 1 groot + 2 zeer groot |
|
|
|
|
|
|
Dosis-respons relatie |
+ 1 bewijs voor gradiënt |
|
|
|
|
|
|
Alle plausibele residuele ‘confounding’[1] |
+ 1 zou een effect kunnen reduceren + 1 zou een tegengesteld effect kunnen suggereren terwijl de resultaten geen effect laten zien. |
Formuleren van de conclusies
Een conclusie verwijst niet naar één of meer artikelen, maar wordt getrokken op basis van alle onderzoeken samen (body of evidence).
Overwegingen
Om tot een aanbeveling te komen zijn naast de kwaliteit van het wetenschappelijk bewijs over de gewenste en ongewenste effecten van een interventie, of over de effectgrootte van een risico- of prognostische factor, vaak nog andere aspecten van belang.
Naast de afweging van gunstige en ongunstige effecten kunnen genoemd worden:
- kosten,
- waarden, voorkeuren en ervaringen van patiënten en behandelaars met betrekking tot interventies en uitkomsten van zorg,
- aanvaardbaarheid van interventies,
- haalbaarheid van een aanbeveling.
Bij voorkeur wordt ook voor deze aspecten naar wetenschappelijk bewijs gezocht. De werkgroep die deze richtlijn heeft opgesteld, heeft hiervan afgezien omdat de hiervoor benodigde tijd in geen enkele verhouding zou staan tot de verwachte opbrengst. De werkgroep heeft, daar waar dit noodzakelijk werd geacht, op basis van eigen ervaring en expertise de hiervoor genoemde aspecten geïnventariseerd.
Deze aspecten worden besproken na de ‘conclusie’ onder het kopje ‘overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beste beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in module 9.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Hiervoor werd gebruik gemaakt van de methodiek zoals beschreven in Programm für Nationale VersorgungsLeitlinien von BÄK, KBV und AWMF Qualitätsindikatoren. Manual für Autoren: 6. Qualitätsindikatoren für Nationale VersorgungsLeitlinien (2009).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek staat in de Kennislacunes onder aanverwante producten.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken wetenschappelijke verenigingen voorgelegd voor commentaar. Tevens werd de richtlijn voorgelegd aan alle deelnemers van de focusgroep bijeenkomst en de volgende organisaties ter becommentariëring: het Zorginstituut Nederland, Inspectie voor de Gezondheidszorg, Patiëntenfederatie Nederland, Nederlands Huisartsen Genootschap en Zorgverzekeraars Nederland. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Literatuurlijst
Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, Schünemann HJ; GRADE Working Group. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 336: 924-6. 2008
Programm für Nationale VersorgungsLeitlinien von BÄK, KBV und AWMF Qualitätsindikatoren. Manual für Autoren: 6. Qualitätsindikatoren für Nationale VersorgungsLeitlinien (2009).
[1] Dit criterium wordt sporadisch toegepast. Soms doet zich de situatie voor dat alle plausibele ‘confounders’ (variabelen die vertekening van resultaten veroorzaken) waarvoor in ‘high-quality’ observationele studies niet is gecorrigeerd (residuele ‘confounders’) zouden resulteren in een onderschatting van een ogenschijnlijk behandeleffect. Als bijvoorbeeld alleen ziekere patienten een experimentele behandeling ondergaan, en ze toch beter af zijn, dan is het waarschijnlijk dat het werkelijke behandeleffect zelfs groter is dan de data suggereren. Een analoge situatie doet zich voor wanneer observationele studies geen behandeleffect laten zien.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline
Limitations: Dutch or English
Year of publication: ≥2014
|
1 controlled clinical trial.pt. (91243) 2 randomized controlled trial.pt. (424517) 3 randomized controlled trials/ (108274) 4 random allocation/ (87820) 5 double blind method/ (137644) 6 single blind method/ (22386) 7 clinical trial.pt. (503461) 8 exp clinical trial/ (749084) 9 placebos/ (33502) 10 placebo$.tw. (182199) 11 random$.tw. (870037) 12 research design/ (90320) 13 volunteer$.tw. (165424) 14 (clin$ adj25 trial$).tw. (336081) 15 ((singl$ or doubl$ or trebl$ or tripl$) adj25 (blind$ or mask$)).tw. (151845) 16 factorial.tw. (22029) 17 cross-over studies/ (38948) 18 crossover.tw. (51016) 19 latin square.tw. (4012) 20 (balance$ adj2 block$).tw. (294) 21 (animals not humans).sh. (4244832) 22 or/1-20 (1811080) 23 22 not 21 (1655447) 24 exp clinical trial/ (749084) 25 clinical trials as topic/ or clinical trials, phase i as topic/ or clinical trials, phase ii as topic/ or clinical trials, phase iii as topic/ or clinical trials, phase iv as topic/ or controlled clinical trials as topic/ or randomized controlled trials as topic/ or multicenter studies as topic/ (304076) 26 or/1-20,24-25 (1878011) 27 26 not 21 (1722161) 28 urethrotom$.tw. (1263) 29 (dilatat$ adj25 urethra$).tw. (665) 30 self dilatat$.tw. (49) 31 urethroplast$.tw. (2555) 32 urethral stricture/ (4457) 33 (urethra$ adj5 (stricture$ or stenos$)).tw. (4657) 34 urethral dilatation.kf. (7) 35 urethrotom$.kf. (22) 36 self dilatat$.kf. (3) 37 (urethra$ adj5 (stricture$ or stenos$)).kf. (533) 38 or/28-37 (8247) 39 27 and 38 (553) 40 39 (553) 41 limit 40 to yr="2014 -Current" (83) |
59 RCTs/CCTs 18 systematische of narratieve reviews |
|
Cochrane CDSR en CENTRAL |
#1 MeSH descriptor: [Urethral Stricture] explode all trees #2 (urethra* near/5 (stricture* or stenos*)):ti,ab #3 (urethra* near/5 narrow*):ti,ab #4 #1 or #2 or #3 #5 (urethroplast* or urethrom*):ti,ab #6 dilatat*:ti,ab #7 intermittent near/5 catheteri*:ti,ab #8 MeSH descriptor: [Urinary Catheterization] explode all trees #9 catheter*:ti,ab #10 #5 or #6 or #7 or #8 or #9 #11 #4 and #10 |
3 SRs 27 RCTs/CCTs |
