Rol FeNO diagnostiek
Uitgangsvraag
Wat is de plaats van FeNO in het diagnostisch traject van patiënten verdacht van niet-ernstig astma?
Aanbeveling
Overweeg een FeNO (afkapwaarde >50 ppb) als diagnosticum in de tweede lijn bij patiënten met een hoge verdenking op astma zonder reversibiliteit of variabiliteit in de spirometrie.
- Bij een afkapwaarde van >50 ppb kan met een redelijke bewijskracht worden aangenomen dat de patiënt astma heeft, echter ongeveer 8% zal een onterechte diagnose krijgen.
- Bij elke andere lagere afkapwaarde kan niet met zekerheid gesteld worden of een patiënt astma heeft, danwel astma kan worden uitgesloten.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek uitgevoerd naar de plaats van FeNO in het diagnosetraject van astma bij volwassenen. Sensitiviteit en specificiteit werden gedefinieerd als cruciale uitkomstmaten.
Uit de analyse kwam een Cochrane rapport (Damen 2021), na update van de search werd daar nog 1 meta-analyse aan toe gevoegd (Nekoee, 2020). In deze studies werd de diagnostische accuratesse onderzocht van het gebruik van exhaled nitric oxide (FENO) voor het stellen van de diagnose astma vergeleken met de provocatietest. In de studies werden verschillende afkappunten gebruikt om de sensitiviteit en specificiteit te bepalen.
De gepoolde sensitiviteit bedroeg ongeveer 0.66 (95%; BI) en de gepoolde specificiteit 0.77 (95% BI) met een bijbehorende AUC van 0.786. De meeste van 27 verschillende onderzoeken hanteerden verschillende afkapwaarden (totaal 171), variërend van 1-20 afkapwaarden per onderzoek. Uit de analyse waarin de resultaten van alle 171 gerapporteerde waarden werd meegenomen kwam 26ppb als optimale afkapwaarden, derhalve is dat in de huidige richtlijn overgenomen. Daarbij werden nog naar additionele afkapwaarden gekeken.
Afkapwaarde tot 26
Bij een afkapwaarden van 26 (range 7 – 48) is de bewijskracht voor de sensitiviteit zeer laag en de specificiteit laag. Gemiddeld genomen wordt 32% van de patiënten ten onrechte niet gediagnosticeerd en 23% ten onrechte wel. Daarbij zijn er in de studies een aantal bias gevonden.
Afkapwaarden 15-25
Bij een afkaprange van 15-25 is de bewijskracht voor zowel de sensitiviteit als de specificiteit zeer laag. Gemiddeld genomen wordt 47% van de patiënten ten onrechte niet gediagnosticeerd en 26% ten onrechte wel. Daarbij is ook hier veel bias rondom deze afkapwaarde.
Afkapwaarde boven de 50
Als definitie voor astma wordt aangehouden bij een FeNO van 50-60 is de bewijskracht voor de sensitiviteit wederom zeer laag, 70% van de patiënten met astma worden ten onrechte niet gediagnosticeerd. De bewijskracht voor de specificiteit ligt echter een stuk hoger, de bewijskracht is redelijk. Bij het afkappunt boven de 50 werden 8% van de patiënten ten onrechte gediagnosticeerd met de diagnose astma.
Het voordeel van FeNO is dat een vrij eenvoudig onderzoek betreft. Snel, makkelijke en patiëntvriendelijk uit te voeren vergeleken met de provocatietest. Daarbij zijn er geen nadelige effecten. De kosten voor een sensor zijn relatief duur, maar als de meting goed gaat zijn de overall kosten lager dan een metacholine provocatietest. In de kliniek wordt een normaalwaarden van 20-21ppb aangehouden, echter weten we dat er tussen patiënten en binnen patiënten een variatie kan zijn. Ook zijn er patiënten met altijd een laag FeNO. De studies laten zien dat deze variatie het lastig maakt om FeNO als diagnosticum te gebruiken. Echter, bij een FeNO boven de 50 is er evidence van redelijk niveau dat de diagnose gesteld kan worden, daarbij moet de arts zich bewust zijn dat 8% van de patiënten ten onrechte de diagnose astma krijgen.
De bewijskracht voor FeNO als diagnosticum is met meerdere niveaus verlaagd. Dit heeft te maken met verschillende vormen van bias die op de studies van toepassing zijn, onder andere betreffende de onderzoeksopzet (risk of bias), tegenstrijdige resultaten (inconsistentie) en kleine onderzoekspopulaties (imprecisie). Er is sprake van selectiebias, omdat alleen een vergelijking is gemaakt met patiënten met een indicatie voor een provocatietest, de groep patiënten met diagnose op basis van reversibiliteit zijn niet meegenomen. Meer onderzoek in grotere populaties zijn nodig om de bewijskracht te versterken.
Naast de analyses van onderzoeken in een algemene populatie van mensen met klachten passend bij astma, waren we ook geïnteresseerd in het nut van FeNO bij de diagnostiek van astma in specifieke subpopulaties. Overeenkomstig de resultaten voor de algemene astmapopulatie heeft FeNO ook in subgroepen (roken, atopie, gebruik van inhalatiecorticosteroïden, setting, duur van hoestklachten) onvoldoende accuratesse voor het aantonen danwel uitsluiten van astma om de bestaande diagnostische zorg te vervangen. We identificeerden een aantal onderzoeken specifiek in de populatie niet-rokers. Voor het diagnosticeren van astma zagen we een iets hogere sensitiviteit bij de optimale threshold. Een vergelijking tussen onderzoeken met niet-rokers en onderzoeken met een volledig rokende populatie kon niet worden gemaakt.
Met betrekking tot atopie zagen we dat bij de optimale threshold de sensitiviteit hoger en de specificiteit van FeNO lager was voor atopische vs. niet-atopische deelnemers, maar het verschil was niet statistisch significant. Voor de FeNO-bepaling op basis van chemiluminescentie vonden we een hogere sensitiviteit ten op zichte van elektrochemische detectie, maar met uitzondering van één analyse (diagnosticeren van astma) was dit verschil niet statistisch significant. Voor de overige subgroepen (wel/niet gebruik van inhalatiecorticosteroïden; setting; duur van hoestklachten) werden geen verschillen gevonden.
Analyses in specifieke subpopulaties op basis van ziekte-ernst of mate van astmacontrole konden niet worden uitgevoerd. De meeste ingesloten onderzoeken waren in een algemene populatie met verdenking op astma, zonder gegevens over uiteindelijke ziekte-ernst.
In conclusie, de systematische review van Cochrane (2021) naar diagnostiek van astma bij volwassenen werden 24 onderzoeken (27 onderzoekspopulaties; 4627 deelnemers) geïncludeerd naar de accuratesse van FeNO voor het diagnosticeren van astma bij volwassenen met verdenking op astma. Op basis van de resultaten van de systematische review bleek, overeenkomstig de aanbevelingen in de huidige richtlijnen, dat FeNO over het algemeen onvoldoende accuratesse heeft voor het aantonen danwel uitsluiten van astma om de bestaande diagnostische zorg te vervangen. Ook subgroep populaties werd onvoldoende accuratesse gevonden voor het gebruik van FeNO als diagnosticum.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het belangrijkste doel bij een patiënt met een hulpvraag is het stellen van de juiste diagnose. Een onterechte diagnose astma kan leiden tot overbodig inhalatiemedicatie gebruik, met mogelijke bijwerkingen van dien. Het onterecht uitsluiten van de diagnose kan leiden tot toename van klachten en longaanvallen. Het doel van de interventie is het stellen van de juiste diagnose. De studies laten zien dat dit doel niet gehaald wordt, ook niet bij bepaalde subgroepen. De keuze om de beslissing over te laten aan de patiënt lijkt dan ook niet de correcte methode, gezien er een duidelijke voorkeur is om de FeNO niet te gebruiken als diagnosticum. Bij patiënten met een evident klachtenpatroon en een FeNO boven de 50 kan samen met de patiënt overwogen worden om een (proef)behandeling te starten gezien de redelijke kans op de juiste diagnose. Hiermee kan de patiënt een meer belastende provocatietest bespaard blijven, maar de patiënt moet zich bewust zijn dat hij/zij mogelijk een periode onterecht inhalatiemedicatie gebruikt. Mocht hiervoor gekozen worden moeten resultaten wel duidelijk geëvalueerd worden omdat 8% van de patiënten toch ten onrechte de diagnose astma krijgen.
Kosten (middelenbeslag)
De kosten van een FeNO meting zijn ongeveer de helft ten opzichte van die van een provocatietest. Gezien een deel van de patiënten soms meerdere metingen nodig heeft voor een correcte meting zal het qua kosten in de praktijk weinig verschil maken.
Wat betreft tijdsbestek is het zeker gunstiger om een FeNO uit te voeren gezien het minder tijd en middelen kost. Een goed uitgevoerde FeNO meting duurt met uitleg enkele minuten, een provocatietest al vrij snel 60 minuten.
Aanvaardbaarheid, haalbaarheid en implementatie
De FeNO-meting is een snel en makkelijk onderzoek is om te verrichten. Het heeft geen invloed op de gezondheid en is ook makkelijk uitvoerbaar bij patiënten met geringere gezondheidsvaardigheden. Echter wordt de meting huidig vooral gebruikt voor het bepalen voor inflammatie in de luchtwegen bij patiënten met al diagnosticeert astma. Dit komt omdat er meer factoren zijn dan astma die een FeNO kunnen verhogen, en daarnaast heeft niet elke patiënt met astma een verhoogd FeNO. Hier zullen ook de bezwaren liggen voor het gebruik van FeNO als diagnosticum. Dit wordt met de huidige studies onderbouwd met de lage sensitiviteit en specificiteit die wordt gevonden. Het doel van een analyse is het stellen van de correcte diagnose met juiste behandeling. Bij alleen het gebruik van FeNO wordt hier veel onzekerheid ingebracht. Daarbij hebben in Nederland niet alle ziekenhuizen de beschikbaarheid om een FeNO-meting uit te voeren.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventie
FeNO heeft over het algemeen onvoldoende accuratesse voor het aantonen danwel uitsluiten van astma om de bestaande diagnostische zorg te vervangen. Bij patiënten met een evident klachtenpatroon en een FeNO boven de 50 kan samen met de patiënt overwogen worden om een (proef)behandeling te starten gezien de redelijke kans op de juiste diagnose en de besparing van een meer belastende provocatietest. Wel moet de patiënt ervan bewust gesteld worden dat hij/zij mogelijk een periode onterecht inhalatiemedicatie gebruikt.
Onderbouwing
In internationale en nationale richtlijnen worden verschillende adviezen gegeven met betrekking tot het gebruik van FeNO (fractional exhaled nitric oxide, of uitgeademende stikstofoxide) meting in het diagnostisch traject van patiënten welke worden verdacht van astma. In de meeste richtlijnen wordt beschreven dat het gebruik van FeNO in het diagnostisch traject in de ‘algemene astmapopulatie’ wordt afgeraden, maar dat meer inzicht nodig is m.b.t. het gebruik van FeNO bij specifieke subgroepen. In 2016 zijn twee Cochrane reviews verschenen over kinderen en volwassenen (Petsky, 2016), over de rol van FeNO-levels bij de behandeling van astma. Hierin werd gesteld dat algemeen gebruik van FeNO om de behandeling af te stemmen niet kan worden aangeraden bij kinderen en volwassenen. Mogelijk dat het voor bepaalde subgroepen wel klinisch nuttig is om FeNO in te zetten bij de diagnosestelling of om de behandeling op af te stemmen. Er zijn sinds de publicatie van eerdergenoemde Cochrane reviews nieuwe wetenschappelijke artikelen gepubliceerd over het onderwerp. De vraagstelling in deze module is wat de rol is van FeNO in het diagnostisch traject van volwassenen verdacht van niet-ernstig astma.
De conclusies zijn, met toestemming van de auteurs, overgenomen uit het Cochrane rapport (2021).
FeNO afkapwaarde 26 ppb
Sensitiviteit
|
Zeer laag GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO (mediane afkapwaarde van 26 ppb (range 7 tot 48 ppb) in de ingesloten studies) 32% van de patiënten met astma ten onrechte niet worden gediagnosticeerd.
Bronnen: Arora, 2006; Berkman, 2005; Chen, 2016b; Cordeiro, 2011; Dupont, 2003; Fortuna, 2007; Fukuhara, 2011; He, 2018; Heffler, 2006; Kanemitsu, 2020; Kostikas, 2008; Malinovschi, 2012; Martin, 2016; Munnik, 2010; Pedrosa, 2010; Sato, 2008; Schneider, 2009; Schneider, 2013; Schneider, 2014; Schneider, 2015; Smith, 2004; Tilemann, 2011; Tomita, 2013; Voutilainen, 2013; Wang, 2015; Yang, 2018 |
Specificiteit
|
Laag GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO (mediane afkapwaarde van 26 ppb (range 7 tot 48 ppb) in de ingesloten studies) 23% van de patiënten zonder astma ten onrechte worden geclassificeerd als hebbende astma.
Bronnen: Arora, 2006; Berkman, 2005; Chen, 2016b; Cordeiro, 2011; Dupont, 2003; Fortuna, 2007; Fukuhara, 2011; He, 2018; Heffler, 2006; Kanemitsu, 2020; Kostikas, 2008; Malinovschi, 2012; Martin, 2016; Munnik, 2010; Pedrosa, 2010; Sato, 2008; Schneider, 2009; Schneider, 2013; Schneider, 2014; Schneider, 2015; Smith, 2004; Tilemann, 2011; Tomita, 2013; Voutilainen, 2013; Wang, 2015; Yang, 2018 |
FeNO afkapwaarde tussen 15 en 25 ppb
Sensitiviteit
|
Zeer laag GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO, wanneer een afkapwaarde tussen 15 en 25 ppb als definitie voor astma wordt aangehouden, 47% van de patiënten met astma ten onrechte niet gediagnosticeerd worden.
Bronnen: Arora, 2006; Chen, 2016b; Dupont, 2003; Fortuna, 2007; He, 2018; Heffler, 2006; Kostikas, 2008; Malinovschi, 2012; Sato, 2008; Schneider, 2009; Schneider, 2013; Schneider, 2014; Schneider, 2015; Smith, 2004 |
Specificiteit
|
Zeer laag GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO, wanneer een afkapwaarde tussen 15 en 25 ppb als definitie voor astma wordt aangehouden, 26% van de patiënten zonder astma ten onrechte worden geclassificeerd als hebbende astma.
Bronnen: Arora, 2006; Chen, 2016b; Dupont, 2003; Fortuna, 2007; He, 2018; Heffler, 2006; Kostikas, 2008; Malinovschi, 2012; Sato, 2008; Schneider, 2009; Schneider, 2013; Schneider, 2014; Schneider, 2015; Smith, 2004 |
FeNO afkapwaarde tussen 50 en 60 ppb
Sensitiviteit
|
Zeer laag GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO, wanneer een afkapwaarde tussen 50 en 60 ppb als definitie voor astma wordt aangehouden, 70% van de patiënten met astma ten onrechte niet worden gediagnosticeerd.
Bronnen: Heffler, 2006; Malinovschi, 2012; Sato, 2008; Schneider, 2008; Schneider, 2015 |
Specificiteit
|
Redelijk GRADE |
Bij volwassen patiënten met verdenking op astma zijn er aanwijzingen dat bij het gebruik van FeNO, wanneer een afkapwaarde tussen 50 en 60 ppb als definitie voor astma wordt aangehouden, 8% van de patiënten zonder astma ten onrechte worden geclassificeerd als hebbende astma.
Bronnen: Heffler, 2006; Malinovschi, 2012; Sato, 2008; Schneider, 2008; Schneider, 2015 |
Beschrijving studies
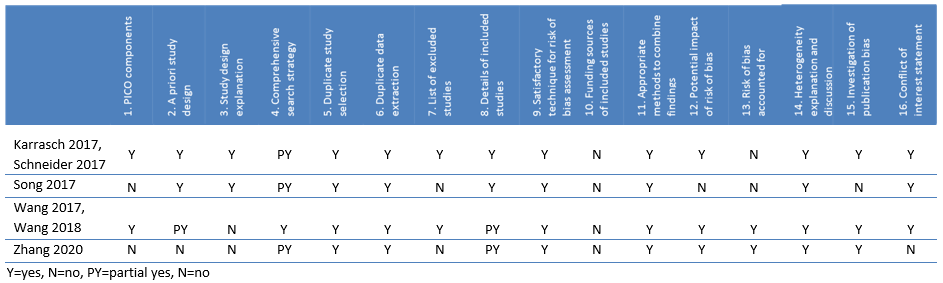
Van de vier ingesloten SR’s richtten twee zich op FeNO bij de diagnostiek van astma in het algemeen (Schneider, 2017; Wang, 2017; Wang, 2018; Karrasch, 2017) en de andere twee keken specifiek naar de rol van FeNO bij de diagnostiek van cough variant asthma (Zhang, 2019; Song, 2017).
De publicatie van Karrasch (2017) beschrijft een SR die de diagnostische testaccuratesse van FeNO bij astma heeft onderzocht. Een heranalyse van de data van deze SR werd beschreven in de publicatie van Schneider (2017), waarbij een nieuw statistisch model werd toegepast dat gebruik maakt van alle beschikbare afkapwaarden om de accuratesse van FeNO voor de diagnose astma te bepalen. In november 2015 werd gezocht naar onderzoeken die FeNO vergeleken met een referentiestandaard om astma te diagnosticeren. Zesentwintig onderzoeken (4.518 deelnemers; kinderen en volwassenen) werden geïncludeerd. Behalve een meta-analyse van alle ingesloten onderzoeken, werd de subgroep ‘ideale onderzoeksopzet’ geanalyseerd (gedefinieerd als: prospectieve onderzoeken met consecutieve inclusie van ongediagnosticeerde, voornamelijk steroïdnaïeve patiënten met symptomen die passen bij astma (niet beperkt tot een specifieke groep) bij wie FeNO metingen gedaan worden volgens de huidige richtlijnen met gebruik van goed gedefinieerde afkapwaarden en adequate referentiestandaarden). Daarnaast werd een overzicht gegeven van de sensitiviteit en specificiteit voor alle beschikbare afkapwaarden. De SR voldeed aan alle AMSTAR 2-criteria, alleen ontbrak informatie over bronnen van financiering van geïncludeerde onderzoeken (item 10) en werd potentiële invloed van vertekening niet meegenomen in de interpretatie van de resultaten (item 13).
Wang en collega’s (publicaties in 2017 en 2018) zochten in april 2017 naar onderzoeken die FeNO vergeleken met een referentiestandaard (klinische diagnose, bronchodilatatie en/of bronchoprovocatie) bij deelnemers vanaf de leeftijd van vijf jaar. Er werden 43 onderzoeken met in totaal 13.747 deelnemers ingesloten. Voor verschillende gebieden van FeNO-afkapwaarden (<20 ppb, 20-29 ppb, 30-39 ppb en >40 ppb) werden sensitiviteit en specificiteit, diagnostische odds ratio’s en likelihoodratio’s berekend voor volwassenen, voor kinderen en voor alle leeftijden. Daarnaast werden analyses uitgevoerd voor de volgende subgroepen: atopische patiënten, niet-rokers, rokers en onderzoeken met positieve bronchoprovocatie als referentiestandaard. Met uitzondering van de onderbouwing voor de keuze voor bepaalde onderzoeksdesigns (item 3) en informatie over bronnen van financiering van geïncludeerde onderzoeken (item 10), werd aan alle criteria van AMSTAR 2 voldaan (Tabel 1).
De SR van Song (2017) richtte zich op de rol van FeNO bij het diagnosticeren van cough variant asthma. De zoekactie werd uitgevoerd in januari 2016 en er werden 13 cross-sectionele onderzoeken ingesloten met in totaal 2019 deelnemers met chronische hoest als voornaamste of enige symptoom. In de meta-analyse werd onderscheid gemaakt tussen een duur van de hoestklachten van drie weken of meer (drie onderzoeken) en acht weken of meer (10 onderzoeken). Als subgroepen werden regio, taal van de publicatie, prospectieve of retrospectieve onderzoeksopzet, type FeNO-meetapparatuur, type referentiestandaard en normale longfoto als selectiecriterium onderzocht. Wat betreft AMSTAR 2 kon de review niet voldoen aan de criteria over de PICO-componenten (item 1), een lijst van uitgesloten onderzoeken (item 7), informatie over bronnen van financiering van geïncludeerde onderzoeken (item 10), potentiële invloed van vertekening op de resultaten en interpretatie daarvan (items 12 en 13) en formeel onderzoek naar publicatiebias (item 15).
Zhang (2020) en collega’s voerden ook een SR uit naar de diagnostische waarde van FeNO bij cough variant asthma. De zoekactie van augustus 2018 resulteerde in inclusie van twaalf onderzoeken (1968 deelnemers) waarin deelnemers drie weken of langer hoestklachten hadden, deels overlappend met de set ingesloten onderzoeken in de SR van Song (2017). Alle twaalf de onderzoeken werden in de meta-analyse opgenomen en er werden geen specifieke subgroepen geanalyseerd. De SR voldeed niet aan de AMSTAR 2 criteria betreffende de PICO-componenten (item 1), de beschikbaarheid van een onderzoeksprotocol (item 2), onderbouwing voor de keuze voor bepaalde onderzoeksdesigns (item 3), lijst van uitgesloten onderzoeken (item 7) en informatie over bronnen van financiering van geïncludeerde onderzoeken en de SR zelf (items 10 en 16).
De prevalentie van astma varieerde bij de volwassenen van 20% tot 80%.
Van de 27 onderzoeken werden er vijf in Duitsland uitgevoerd (Schneider, 2015; Schneider, 2014; Schneider, 2013; Schneider, 2015; Tilemann, 2011), vier in Japan (Kanemitsu, 2020; Tomita, 2013; Fukuhara, 2011; Sato, 2008; Asano, 2017), drie in China (Chen, 2016; He, 2018; Wang, 2015), twee in Nederland (Cordeiro, 2011; Munnik, 2010), twee in Spanje (Fortuna, 2007; Pedrosa, 2010), twee in België (Dupont, 2003; Nekoee, 2020) en steeds één onderzoek in Denemarken (Malinovschi, 2012), Finland (Voutilainen, 2013), Griekenland (Kostikas, 2008), Israël (Berkman, 2005), Italië (Heffler, 2006), Nieuw Zeeland (Smith, 2004), Republiek Korea (Yang, 2018), Verenigd Koninkrijk (Martin, 2016) en de Verenigde Staten (Arora, 2006). De grootte van de onderzoekspopulaties varieerde van 40 tot 923. In de meeste onderzoeken werden deelnemers geïncludeerd met klachten passend bij astma die een (poli)kliniek longziekten bezochten en twee onderzoeken vonden specifiek in huisartsenpraktijken plaats (Schneider, 2015; Schneider 2009). In twee onderzoeken werd eerst een willekeurige steekproef genomen uit een bepaalde populatie waarbij op basis van een vragenlijst deelnemers met klachten suggestief voor astma werden geselecteerd (Kostikas, 2008; Malinovschi, 2012). De gemiddelde leeftijd van de deelnemers liep uiteen van 22 jaar tot 64 jaar. In drie onderzoeken werden rokers expliciet uitgesloten van deelname (Kanemitsu, 2020; Dupont, 2003; Heffler, 2006) en in vijf onderzoeken was recent gebruik van inhalatiecorticosteroïden een exclusiecriterium (Dupont, 2003; Fortuna, 2007; Fukuhara, 2011; Kostikas, 2008; Wang, 2015). De apparaten waarmee de FeNO-waarde werd bepaald, maakten voornamelijk gebruik van chemoluminescentie of elektrochemische detectie. De referentiestandaard was in de meeste onderzoeken overeenkomstig met de geldende richtlijnen of bevatte in ieder geval elementen van zowel bronchodilatatie als bronchoprovocatie, behalve in twee waarin de diagnose astma werd gesteld op basis van enkel bronchoprovocatie (Pedrosa, 2010; Wang, 2015), dan wel enkel bronchodilatatie (Wang, 2015).
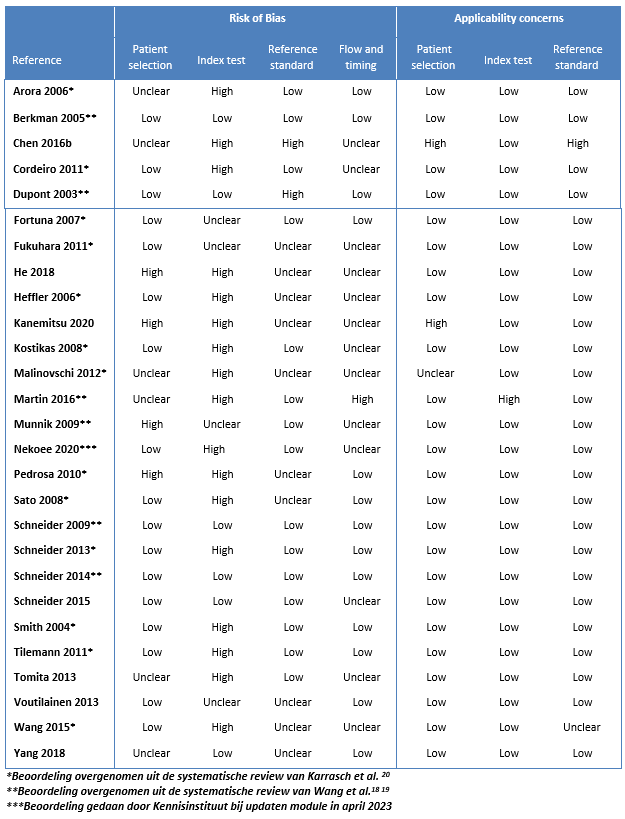
Tabel 3 geeft een overzicht van de kans op vertekening in de onderzoeken en applicability concerns (QUADAS-2). Vier onderzoeken scoorden een hoge kans op vertekening voor de selectie van patiënten, omdat patiënten niet consecutief geïncludeerd werden of omdat enkel niet-rokers werden geïncludeerd of deelnemers die alle diagnostische tests hadden ondergaan (He, 2018; Kanemitsu, 2020; Munnik, 2010; Pedrosa, 2010). Vanwege een selecte onderzoekspopulatie werd in twee gevallen de toepasbaarheid als laag beoordeeld (Chen, 2016; Kanemitsu, 2020). De kans op vertekening betreffende de indextest werd als hoog ingeschat voor zestien onderzoekendoor het ontbreken van een vooraf gedefinieerde FeNO afkapwaarde en/of vanwege de interpretatie van FeNO-waarde met kennis van de uitslag van de referentiestandaard. Vanwege een suboptimale referentiestandaard (bronchoprovocatie of bronchodilatatie) in één onderzoek (Chen, 2016) en het feit dat de FeNO-waarde bekend was bij de interpretatie van de referentiestandaard in een ander onderzoek (Dupont, 2003) werd een hoge kans op vertekening betreffende de referentiestandaard gescoord en in één van de twee onderzoeken ook een verminderde toepasbaarheid31. Geen van de onderzoeken scoorde een hoge kans op vertekening voor het QUADAS-2-domein Flow and timing.
Resultaten
Vijfentwintig onderzoeken konden worden opgenomen in een meta-analyse, waarvan het onderzoek van Schneider (2015) voor twee populaties apart gegevens leverde (huisartsen- en longartsenpraktijken) en Malinovschi (2012) voor drie populaties (rokers, niet-rokers en nooit-rokers). In totaal werden dus 28 onderzoekspopulaties (n=5.329 deelnemers) geanalyseerd. De mediane prevalentie van astma in deze onderzoeken was 39,4% (range 20% tot 80%).
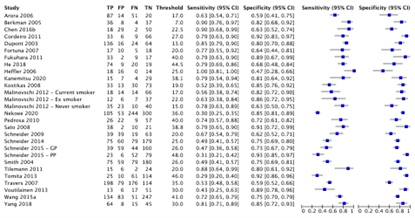
Uitgaande van de optimale FeNO-afkapwaarden in de onderzoeken (mediaan 26 ppb, range 7 ppb tot 48 ppb), zoals gerapporteerd door de auteurs of bij meerdere afkapwaarden per onderzoek bepaald op basis van Youden’s index, liep de sensitiviteit uiteen van 0,29 tot 1,00 (mediaan 0,74) en de specificiteit van 0,47 tot 0,93 (mediaan 0,80) (Figuur 1). De gepoolde sensitiviteit bedroeg 0,66 (95% BI; 0,58 tot 0,73) en de gepoolde specificiteit 0,77 (95% BI; 0,72 tot 0,81), met een bijbehorende area under the curve (AUC) van 0,786 (Tabel 1). Bij een mediane astmaprevalentie van 40% bedragen de bijbehorende voorspellende waarden voor de aanwezigheid van astma 65% (95% BI; 58% tot 71%) voor een positieve testuitslag en 21% (95% BI; 17% tot 26%) voor een negatieve testuitslag. In een hypothetische populatie met 1000 patiënten bij wie de FeNO-waarde wordt bepaald, zouden 138 patiënten (95% BI; 114 tot 168) ten onrechte geclassificeerd worden als hebbende astma (fout-positieven) en bij 136 patiënten met astma (95% BI; 108 tot 168) zou de diagnose gemist zijn (fout-negatieven).
Figuur 1. Gepaarde forestplot van sensitiviteit en specificiteit van FeNO voor het aantonen van astma bij volwassenen (28 onderzoeken)
Gepoolde sensitiviteit 0,66 (95% BI; 0,58 tot 0,73); gepoolde specificiteit 0,77 (95% BI; 0,72 tot 0,81)
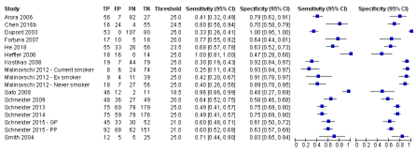
Figuur 2. Gepaarde forestplot van sensitiviteit en specificiteit van FeNO voor het aantonen van astma bij volwassenen bij een FeNO-afkapwaarde tussen 15 en 25 ppb (17 onderzoeken)
Gepoolde sensitiviteit 0,53 (95% BI; 0,44 to 0,62); gepoolde specificiteit 0,74 (95% BI; 0,65 tot 0,81)
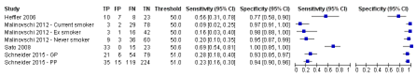
In de onderzoeken die resultaten voor een FeNO-afkapwaarde tussen de 50 en 60 ppb rapporteerden (n=7; 954 deelnemers), liep bij een mediane prevalentie van 39% (range 29% tot 68%) de sensitiviteit uiteen van 0,09 tot 0,69 (mediaan 0,23) en de specificiteit van 0,77 tot 1,00 (mediaan 0,95) (Figuur 3). De gepoolde sensitiviteit bedroeg 0,30 (95% BI; 0,16 tot 0,48) en de gepoolde specificiteit 0,92 (95% BI; 0,85 tot 0,96), met een bijbehorende AUC van 0.788 (Tabel 1). Bij een mediane astmaprevalentie van 39% bedragen de bijbehorende voorspellende waarden voor de aanwezigheid van astma 70% (95% BI; 41% tot 89%) voor een positieve testuitslag en 33% (95% BI; 26% tot 39%) voor een negatieve testuitslag. In een hypothetische populatie met 1000 patiënten bij wie de FeNO-waarde wordt bepaald, zouden 49 patiënten (95% BI; 24 tot 91) ten onrechte geclassificeerd worden als hebbende astma (fout-positieven) en bij 273 patiënten met astma (95% BI; 203 tot 328) zou de diagnose gemist zijn (fout-negatieven).
Figuur 3. Gepaarde forestplot van sensitiviteit en specificiteit van FeNO voor het aantonen van astma bij volwassenen bij een FeNO-afkapwaarde tussen 50 en 60 ppb (7 onderzoeken)
Gepoolde sensitiviteit 0,30 (95% BI; 0,16 tot 0,48); gepoolde specificiteit 0,92 (95% BI; 0,85 tot 0,96)
Tabel 1. Gepoolde sensitiviteit en specificiteit van FeNO voor het aantonen van astma bij volwassenen (bivariate analyse)
|
Analysis |
Number of studies (participants) |
Prevalence median (range) |
Sensitivity (95% CI) |
Specificity (95% CI) |
AUC |
|
Optimal threshold |
28 (5329) |
0.40 (0.20 to 0.80) |
0.66 (0.58 to 0.73) |
0.77 (0.72 to 0.81) |
0.786 |
|
Non-smoking |
6 (623) |
0.36 (0.22 to 0.67) |
0.82 (0.72 to 0.89) |
0.69 (0.55 to 0.81) |
0.833 |
|
Non-ICS |
5 (1015) |
0.44 (0.36 to 0.69) |
0.74 (0.62 to 0.84) |
0.78 (0.71 to 0.83) |
0.822 |
|
General practice |
2 (320) |
0.42 (0.36 to 0.47) |
0.49 (0.17 to 0.81) |
0.82 (0.36 to 0.97) |
0.688 |
|
Atopy |
1 (122) |
0.77 |
0.79 (0.69 tot 0.86) |
0.68 (0.48 to 0.84) |
- |
|
Non-atopy |
1 (170) |
0.48 |
0.68 (0.57 to 0.78) |
0.63 (0.52 to 0.73) |
- |
|
Chemiluminescence |
12 (1546) |
0.46 (0.34 to 0.77) |
0.76 (0.68 to 0.83) |
0.77 (0.69 to 0.84) |
0.834 |
|
Electrochemical |
13 (2394) |
0.39 (0.20 to 0.60) |
0.58 (0.47 to 0.69) |
0.78 (0.71 to 0.83) |
0.756 |
|
Cutoff 15-25 |
17 (2829) |
0.41 (0.20 to 0.80) |
0.53 (0.44 to 0.62) |
0.74 (0.65 to 0.81) |
0.674 |
|
Cutoff 50-60 |
7 (954) |
0.39 (0.29 to 0.68) |
0.30 (0.16 to 0.48) |
0.92 (0.85 to 0.96) |
0.788 |
CI: confidence interval; AUC: area under the curve; ICS: inhalation corticosteroids
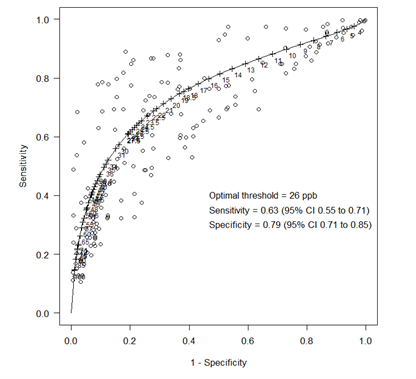
De 27 onderzoeken rapporteerden resultaten voor in totaal 171 afkapwaarden, variërend van 1 tot 20 afkapwaarden per onderzoek (mediaan: 4), en er konden 61 unieke afkapwaarden worden onderscheiden. De FeNO-afkapwaarde waarvoor het vaakst resultaten werden gerapporteerd, was 20 ppb (11 keer), gevolgd door 15 ppb en 30 ppb (beide 10 keer) en 26 (9 keer). Uit een analyse waarin de resultaten voor alle 171 gerapporteerde FeNO-afkapwaarden werden meegenomen, kwam 26 ppb als optimale afkapwaarde voor FeNO (Figuur 4).
Figuur 4. sROC-curve van FeNO voor het aantonen van astma bij volwassenen (multiple thresholds analyse)
Elke cirkel geeft een combinatie van sensitiviteit en specificiteit weer die in de individuele onderzoeken gevonden werd bij een bepaalde afkapwaarde. De getallen geven de FeNO-afkapwaarden weer (ppb)
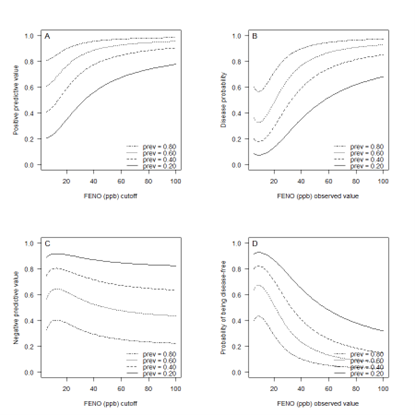
In Figuur 5 zijn voor prevalenties van 20%, 40%, 60% en 80%, en voor diverse (afkap- of geobserveerde) waardes van FeNO A) de positief voorspellende waarde (positive predictive value, PPV), B) de kans op astma, C) de negatief voorspellende waarde (negative predictive value, NPV) en D) de kans op afwezigheid van astma af te lezen. In Tabel 2 staat de informatie uit Figuur 5 uitgewerkt voor een astmaprevalentie van 40%. Opgemerkt moet worden dat voor sommige afkapwaarden in deze tabel de betrouwbaarheidsintervallen rondom de geschatte voorspellende waarden en kans op astma breed zijn. Dit komt doordat het lastig is voor het model om absolute kansen te schatten op basis van (meta-)gegevens over sensitiviteit en specificiteit, wat leidt tot een onzekere schatting.
Figuur 5.
Positief voorspellende waarde (A), kans op op astma (B), negatief voorspellende waarde (C) en kans op afwezigheid van astma (D) voor diverse (afkap- of geobserveerde) waardes van FeNO (ppb) bij astmaprevalenties van 20%, 40%, 60% en 80% bij volwassenen (multiple thresholds analyse)
Tabel 2. Sensitiviteit, specificiteit, voorspellende waarden en kans op het hebben van astma bij een bepaalde FeNO-(afkap)waarde en een prevalentie van 40% bij volwassenen (multiple thresholds analyse)
|
FeNO (cutoff) value |
Sensitivity (95% CI) |
Specificity (95% CI) |
PPV |
NPV |
Probability of asthma |
|
15 |
0.81 (0.77 to 0.85) |
0.49 (0.40 to 0.59) |
0.52 (0.15 to 0.87) |
0.80 (0.31 to 0.97) |
0.22 (0.10 to 0.43) |
|
20 |
0.73 (0.67 to 0.78) |
0.66 (0.57 to 0.74) |
0.59 (0.12 to 0.94) |
0.79 (0.41 to 0.95) |
0.30 (0.10 to 0.62) |
|
25 |
0.65 (0.57 to 0.72) |
0.77 (0.69 to 0.83) |
0.65 (0.10 to 0.97) |
0.77 (0.47 to 0.92) |
0.38 (0.08 to 0.82) |
|
30 |
0.57 (0.48 to 0.66) |
0.84 (0.77 to 0.89) |
0.70 (0.10 to 0.98) |
0.75 (0.51 to 0.89) |
0.46 (0.07 to 0.91) |
|
45 |
0.40 (0.30 to 0.51) |
0.93 (0.89 to 0.96) |
0.80 (0.11 to 0.99) |
0.70 (0.54 to 0.82) |
0.64 (0.08 to 0.98) |
|
50 |
0.36 (0.26 to 0.48) |
0.95 (0.91 to 0.97) |
0.82 (0.12 to 0.99) |
0.69 (0.55 to 0.80) |
0.68 (0.08 to 0.98) |
|
55 |
0.32 (0.22 to 0.44) |
0.96 (0.92 to 0.98) |
0.83 (0.12 to 0.99) |
0.68 (0.56 to 0.78) |
0.72 (0.09 to 0.99) |
|
60 |
0.29 (0.19 to 0.41) |
0.96 (0.93 to 0.98) |
0.85 (0.13 to 1.00) |
0.67 (0.56 to 0.77) |
0.74 (0.09 to 0.99) |
CI: confidence interval; PPV: positive predictive value; NPV: negative predictive value
Van de twee onderzoeken die hun resultaten in onvoldoende detail rapporteerden om in de meta-analyses te worden opgenomen, presenteerden Martin en collega’s (Martin, 2016) een AUC van 0,62 voor FeNO als diagnostische test voor astma en Munnik en collega’s (Munnik, 2010) een AUC van 0,826.
Subgroepen
Een aantal onderzoeken werd uitgevoerd in of rapporteerde resultaten apart voor een specifieke populatie of setting: 1) niet-rokers in zes onderzoekspopulaties (vijf onderzoeken (Kanemitsu, 2020; Dupont, 2003; Heffler, 2006; Malinovschi, 2012; Schneider, 2009), 2) deelnemers zonder inhalatiecorticosteroïden in vijf onderzoeken (Dupont, 2003; Fortuna, 2007; Fukuhara, 2011), 3) huisartsenpraktijken in twee onderzoeken (Schneider, 2015; Schneider, 2009) en 4) deelnemers met of zonder atopie (en rhinitis) in één onderzoek (He, 2018). Daarnaast werd een subgroepanalyse uitgevoerd naar 5) type apparaat voor de FeNO-bepaling: chemiluminescentie (12 onderzoeken: He, 2018; Kanemitsu, 2020; Tomita, 2013; Berkman, 2005; Corrdeiro, 2011; Dupont, 2003; Fortuna, 2007; Fukuhara, 2011; Heffler, 2006; Sato, 2008; Smith, 2004; Voutilainen, 2013) of elektrochemische detectie (13 populaties uit 10 onderzoeken: Chen, 2016; Schneider, 2015; Yang, 2018; Kostikas, 2008; Malinovschi, 2012; Pedrosa, 2010; Schneider, 2014; Schneider, 2014; Schneider, 2009; Tilemann, 2011).
- Op basis van onderzoeken met een niet-rokende populatie was de gepoolde sensitiviteit (0,82; 95% BI; 0,72 tot 0,80) hoger dan op basis van alle onderzoeken, bij een vergelijkbare gepoolde specificiteit (0,69; 95% BI; 0,55 tot 0,81) (Tabel 1).
- De meta-analyse van onderzoeken met een populatie zonder inhalatiecorticosteroïdengebruik leverde dezelfde gepoolde effectschattingen als die van alle onderzoeken.
- Hetzelfde geldt voor de meta-analyse van de twee onderzoeken in de eerstelijnssetting. Ook deze meta-analyse leverde dezelfde gepoolde effectschattingen als die van alle onderzoeken.
- Het onderzoek onder atopische deelnemers vond een sensitiviteit van 0,79 (95% BI; 0,69 tot 0,86 en een specificiteit van 0,68 (95% BI; 0,48 tot 0,84). De prevalentie van astma in deze populatie was 77%. In hetzelfde onderzoek werd voor niet-atopische deelnemers een vergelijkbare sensitiviteit en specificiteit gevonden (van respectievelijk 0,68 [95% BI; 0,57 tot 0,78] en 0,63 [0,52 tot 0,73]); de astmaprevalentie in deze groep was 48%.
- Voor onderzoeken met een FeNO-bepaling op basis van chemiluminescentie werd een hogere sensitiviteit gevonden dan die in de subgroep onderzoeken die gebruik maakten van elektrochemische detectie om de FeNO-waarde te bepalen (respectievelijk 0,76 [95% BI; 0,68 tot 0.83] en 0,58 [0,47 tot 0,69]). De specificiteit verschilde niet tussen de twee subgroepen.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat sensitiviteit bij een FeNO mediane afkapwaarde van 26 ppb is met 3 niveaus verlaagd naar GRADE Zeer laag gezien beperkingen in de onderzoeksopzet (risk of bias); tegenstrijdige resultaten (inconsistentie); het geringe aantal patiënten (imprecisie).
De bewijskracht voor de uitkomstmaat specificiteit bij een FeNO mediane afkapwaarde van 26 ppb is met 2 niveaus verlaagd naar GRADE Laag gezien beperkingen in de onderzoeksopzet (risk of bias) en tegenstrijdige resultaten (inconsistentie).
De bewijskracht voor de uitkomstmaten sensitiviteit en specificiteit bij een FeNO afkapwaarde tussen de 15 en 25 ppb is met 3 niveaus verlaagd naar GRADE Zeer laag gezien beperkingen in de onderzoeksopzet (risk of bias); tegenstrijdige resultaten (inconsistentie); het geringe aantal patiënten (imprecisie).
De bewijskracht voor de uitkomstmaat sensitiviteit bij een FeNO afkapwaarde tussen de 50 en 60 ppb is met 3 niveaus verlaagd naar GRADE Zeer laag gezien beperkingen in de onderzoeksopzet (risk of bias); tegenstrijdige resultaten (inconsistentie); het geringe aantal patiënten (imprecisie).
De bewijskracht voor de uitkomstmaat specificiteit bij een FeNO afkapwaarde tussen de 50 en 60 ppb is met 1 niveau verlaagd naar GRADE Redelijk gezien beperkingen in de onderzoeksopzet (risk of bias).
A systematic review of the literature was performed to answer the following question:
What is the diagnostic accuracy of fractional exhaled nitric oxide (FeNO) compared to usual diagnostic care in adults suspected of non-severe asthma?
| P: | Adults suspected of non-severe asthma |
| I: | Fractional exhaled nitric oxide (FeNO) as triage or add-on (in addition to usual diagnostic care) and as a replacement (e.g. for parts of usual diagnostic care, such as spirometry or provocation test) |
| C: | Usual diagnostic care |
| R: | - |
| O: | Diagnostic accuracy for diagnosis asthma (sensitivity, specificity, predictive value) |
| T/S: | FeNO prior to or at diagnosis |
Relevant outcome measures
The guideline development group considered sensitivity and specificity as critical outcome measures for decision making; and predictive value as an important outcome measure for decision making.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until January 3rd 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 98 hits. Studies were selected based on the following criteria: systematic review or meta-analysis investigating the diagnostic accuracy of fractional exhaled nitric oxide (FeNO) compared to provocation test in adults (>18 y) suspected of asthma. Eleven studies were initially selected based on title and abstract screening. After reading the full text, six studies were excluded (see the table with reasons for exclusion under the tab Methods), and five studies were included. After the search strategy and study selection was performed, a Cochrane report was found concerning the exact PICO as defined by the working group (Damen, 2021). Therefore, the literature analysis of this report was copied to this module. For the Cochrane report, the databases Medline and Embase were searched with relevant search terms until September 22nd 2020. The detailed search strategy is also depicted under the tab Methods. The meta-analyses were updated with an additional study included in our fulltext selection (Nekoee, 2020). The literature analysis was published in Dutch and therefore reported in Dutch in this module.
Resultaten
In het Cochrane rapport (Damen, 2021) werden 26 onderzoeken afkomstig uit vier verschillende systematische reviews (SR) (Karrasch, 2017; Wang, 2018; Song, 2017; Zhang, 2020) geïncludeerd voor de literatuuranalyse over het nut van FeNO bij de diagnostiek van astma bij volwassenen. Na update van de search werd nog één onderzoek toegevoegd aan de meta-analyse (Nekoee, 2020). De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- Arora R, Thornblade CE, Dauby P-AL, et al. Exhaled nitric oxide levels in military recruits with new onset asthma. Allergy and Asthma Proceedings 2006;27(6):493-98. doi: 10.2500/aap.2006.27.2904.
- Asano T, Takemura M, Fukumitsu K, et al. Diagnostic utility of fractional exhaled nitric oxide in prolonged and chronic cough according to atopic status. Allergol Int 2017;66(2):344-50. doi: 10.1016/j.alit.2016.08.015 [published Online First: 2016/10/04].
- Berkman N, Avital A, Breuer R, et al. Exhaled nitric oxide in the diagnosis of asthma: comparison with bronchial provocation tests. Thorax 2005;60(5):383-8. doi: 10.1136/thx.2004.031104 [published Online First: 2005/04/30].
- Chen FJ, Liao H, Huang XY, et al. Importance of fractional exhaled nitric oxide in diagnosis of bronchiectasis accompanied with bronchial asthma. Journal of Thoracic Disease 2016;8(5):992-99. doi: https://doi.org/10.21037/jtd.2016.03.72.
- Cordeiro D, Rudolphus A, Snoey E, et al. Utility of nitric oxide for the diagnosis of asthma in an allergy clinic population. Allergy and Asthma Proceedings 2011;32(2):119-26. doi: 10.2500/aap.2011.32.3419.
- Damen J, Heus P, Spijker R, Jenniskens K, Kamm I, Nijman S, Vernooij R, Ghannad M, Korevaar D, Hooft L. Nut van FeNO bij de diagnostiek en behandeling van specifieke groepen astmapatiënten. Cochrane Netherlands 2021.
- Dupont LJ, Demedts MG, Verleden GM. Prospective evaluation of the validity of exhaled nitric oxide for the diagnosis of asthma. Chest 2003;123(3):751-6. doi: 10.1378/chest.123.3.751 [published Online First: 2003/03/12].
- Fortuna AM, Feixas T, Gonzalez M, et al. Diagnostic utility of Inflammatory biomarkers in asthma: Exhaled nitric oxide and induced sputum eosonophil count. Respiratory Medicine 2007;101(11):2416-21. doi: 10.1016/j.rmed.2007.05.019.
- Fukuhara A, Saito J, Sato S, et al. Validation study of asthma screening criteria based on subjective symptoms and fractional exhaled nitric oxide. Annals of Allergy Asthma & Immunology 2011;107(6):480-86. doi: 10.1016/j.anai.2011.09.002.
- He L, Wei M, Luo J, et al. Re-evaluation of the diagnostic value of fractional exhaled nitric oxide & its impact in patients with asthma. Indian Journal of Medical Research 2018;148(4):441-48. doi: https://doi.org/10.4103/ijmr.ijmr_1478_16.
- Heffler E, Guida G, Marsico P, et al. Exhaled nitric oxide as a diagnostic test for asthma in rhinitic patients with asthmatic symptoms. Respiratory Medicine 2006;100(11):1981-87. doi: 10.1016/j.rmed.2006.02.019.
- Kanemitsu Y, Kurokawa R, Ono J, et al. Increased Serum Periostin Levels and Eosinophils in Nasal Polyps Are Associated with the Preventive Effect of Endoscopic Sinus Surgery for Asthma Exacerbations in Chronic Rhinosinusitis Patients. International Archives of Allergy & Immunology 2020:1-9. doi: https://doi.org/10.1159/000509253.
- Karrasch S, Linde K, Rücker G, et al. Accuracy of FENO for diagnosing asthma: a systematic review. Thorax 2017;72(2):109-16. doi: 10.1136/thoraxjnl-2016-208704.
- Kostikas K, Papaioannou AI, Tanou K, et al. Portable exhaled nitric oxide as a screening tool for asthma in young adults during pollen season. Chest 2008;133(4):906-13. doi: 10.1378/chest.07-1561.
- Malinovschi A, Backer V, Harving H, et al. The value of exhaled nitric oxide to identify asthma in smoking patients with asthma-like symptoms. Respiratory Medicine 2012;106(6):794-801. doi: 10.1016/j.rmed.2012.02.009.
- Martin MJ, Wilson E, Gerrard-Tarpey W, et al. The utility of exhaled nitric oxide in patients with suspected asthma. Thorax 2016;71(6):562-4. doi: 10.1136/thoraxjnl-2015-208014 [published Online First: 2016/02/24].
- Munnik P, van der Lee I, Fijn J, et al. Comparison of eNO and histamine hyperresponsiveness in diagnosing asthma in new referrals. Respir Med 2010;104(6):801-7. doi: 10.1016/j.rmed.2009.12.002 [published Online First: 2009/12/29].
- Pedrosa M, Cancelliere N, Barranco P, et al. Usefulness of Exhaled Nitric Oxide for Diagnosing Asthma. Journal of Asthma 2010;47(7):817-21. doi: 10.3109/02770903.2010.491147.
- Petsky HL, Kew KM, Turner C, Chang AB. Exhaled nitric oxide levels to guide treatment for adults with asthma. Cochrane Database Syst Rev. 2016 Sep 1;9(9):CD011440. doi: 10.1002/14651858.CD011440.pub2. PMID: 27580628; PMCID: PMC6457753.
- Sato S, Saito J, Sato Y, et al. Clinical usefulness of fractional exhaled nitric oxide for diagnosing prolonged cough. Respiratory Medicine 2008;102(10):1452-59. doi: 10.1016/j.rmed.2008.04.018.
- Schneider A, Wagenpfeil G, Jorres RA, et al. Influence of the practice setting on diagnostic prediction rules using FENO measurement in combination with clinical signs and symptoms 108.
- Schneider A, Faderl B, Schwarzbach J, et al. Prognostic value of bronchial provocation and FENO measurement for asthma diagnosis--results of a delayed type of diagnostic study. Respir Med 2014;108(1):34-40. doi: 10.1016/j.rmed.2013.11.008 [published Online First: 2013/12/10].
- Schneider A, Schwarzbach J, Faderl B, et al. FENO measurement and sputum analysis for diagnosing asthma in clinical practice. Respiratory Medicine 2013;107(2):209-16. doi: 10.1016/j.rmed.2012.10.003.
- Schneider A, Tilemann L, Schermer T, et al. Diagnosing asthma in general practice with portable exhaled nitric oxide measurement--results of a prospective diagnostic study: FENO < or = 16 ppb better than FENO < or =12 ppb to rule out mild and moderate to severe asthma [added]. Respir Res 2009;10(1):15. doi: 10.1186/1465-9921-10-15 [published Online First: 2009/03/04] of asthma. BMJ Open 2015;5(11):e009676. doi: https://doi.org/10.1136/bmjopen-2015-009676.
- Smith AD, Cowan JO, Filsell S, et al. Diagnosing asthma - Comparisons between exhaled nitric oxide measurements and conventional tests. American Journal of Respiratory and Critical Care Medicine 2004;169(4):473-78. doi: 10.1164/rccm.200310-1376OC.
- Song WJ, Kim HJ, Shim JS, et al. Diagnostic accuracy of fractional exhaled nitric oxide measurement in predicting cough-variant asthma and eosinophilic bronchitis in adults with chronic cough: A systematic review and meta-analysis. J Allergy Clin Immunol 2017;140(3):701-09. doi: 10.1016/j.jaci.2016.11.037 [published Online First: 2017/01/16].
- Tilemann L, Gindner L, Meyer F, et al. Differences in local and systemic inflammatory markers in patients with obstructive airways disease. Primary Care Respiratory Journal 2011;20(4):407-14. doi: 10.4104/pcrj.2011.00069.
- Tomita K, Sano H, Chiba Y, et al. A scoring algorithm for predicting the presence of adult asthma: a prospective derivation study. Prim Care Respir J 2013;22(1):51-8. doi: 10.4104/pcrj.2013.00005 [published Online First: 2013/01/26].
- Voutilainen M, Malmberg LP, Vasankari T, et al. Exhaled nitric oxide indicates poorly athlete's asthma. Clinical Respiratory Journal 2013;7(4):347-53. doi: 10.1111/crj.12014.
- Wang Y, Li L, Han R, et al. Diagnostic value and influencing factors of fractional exhaled nitric oxide in suspected asthma patients. International Journal of Clinical and Experimental Pathology 2015;8(5):5570-76.
- Wang Z, Pianosi P, Keogh K, et al. The Clinical Utility of Fractional Exhaled Nitric Oxide (FeNO) in Asthma Management2017.
- Wang Z, Pianosi PT, Keogh KA, et al. The Diagnostic Accuracy of Fractional Exhaled Nitric Oxide Testing in Asthma: A Systematic Review and Meta-analyses. Mayo Clinic proceedings 2018;93(2):191-98. doi: 10.1016/j.mayocp.2017.11.012.
- Yang SY, Kim YH, Byun MK, et al. Repeated Measurement of Fractional Exhaled Nitric Oxide Is Not Essential for Asthma Screening. Journal of Investigational Allergology & Clinical Immunology 2018;28(2):98-105. doi: https://doi.org/10.18176/jiaci.0215.
- Zhang L, Liu S, Li M, et al. Diagnostic value of fractional exhaled nitric oxide in cough-variant asthma: an updated meta-analysis. The Journal of asthma: official journal of the Association for the Care of Asthma 2020;57(3):1-8. doi: 10.1080/02770903.2019.1568452.
Tabel 3. Table of quality assessment for systematic reviews of diagnostic studies (uit Cochrane, 2021)
Tabel 4. Kans op vertekening en applicability concerns voor onderzoeken betreffende FeNO voor het aantonen van astma bij volwassenen (n=26)
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Schneider A, Linde K, Reitsma JB, Steinhauser S, Rücker G. A novel statistical model for analyzing data of a systematic review generates optimal cutoff values for fractional exhaled nitric oxide for asthma diagnosis. J Clin Epidemiol. 2017 Dec;92:69-78. doi: 10.1016/j.jclinepi.2017.09.001. Epub 2017 Sep 12. PMID: 28916487. |
Wrong study design: secondary analysis of SR Karrash to define optimal threshold FeNO |
|
Li Z, Qin W, Li L, Wu Q, Wang Y. Diagnostic accuracy of exhaled nitric oxide in asthma: a meta-analysis of 4,691 participants. Int J Clin Exp Med. 2015 Jun 15;8(6):8516-24. PMID: 26309503; PMCID: PMC4538098. |
Wrong study design: case control studies included |
|
Wang Z, Pianosi PT, Keogh KA, Zaiem F, Alsawas M, Alahdab F, Almasri J, Mohammed K, Larrea-Mantilla L, Farah W, Daraz L, Barrionuevo P, Morrow AS, Prokop LJ, Murad MH. The Diagnostic Accuracy of Fractional Exhaled Nitric Oxide Testing in Asthma: A Systematic Review and Meta-analyses. Mayo Clin Proc. 2018 Feb;93(2):191-198. doi: 10.1016/j.mayocp.2017.11.012. Epub 2017 Dec 20. PMID: 29275031. |
Wrong O: no separate results for adults reported (only summary) |
|
Zhong, A, Yang, R, Du, H, Zhang, H, Qiu, C, Niu, Y. A meta-analysis: the efficacy of asthma diagnosis based on exhaled nitric oxide. Int J Clin Exp Med. 2016, 9(7), 13053-13058. |
Wrong study design: insufficient quality assessment of included studies, limited reported outcomes |
|
Korevaar DA, Westerhof GA, Wang J, Cohen JF, Spijker R, Sterk PJ, Bel EH, Bossuyt PM. Diagnostic accuracy of minimally invasive markers for detection of airway eosinophilia in asthma: a systematic review and meta-analysis. Lancet Respir Med. 2015 Apr;3(4):290-300. doi: 10.1016/S2213-2600(15)00050-8. Epub 2015 Mar 20. PMID: 25801413. |
Wrong study design: 3 different markers studied, limited reporting of study results |
|
Dweik RA, Boggs PB, Erzurum SC, Irvin CG, Leigh MW, Lundberg JO, Olin AC, Plummer AL, Taylor DR; American Thoracic Society Committee on Interpretation of Exhaled Nitric Oxide Levels (FENO) for Clinical Applications. An official ATS clinical practice guideline: interpretation of exhaled nitric oxide levels (FENO) for clinical applications. Am J Respir Crit Care Med. 2011 Sep 1;184(5):602-15. doi: 10.1164/rccm.9120-11ST. PMID: 21885636; PMCID: PMC4408724. |
Wrong study design: develop ATS guideline for interpretation of FeNO |
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-11-2025
Beoordeeld op geldigheid : 12-09-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met niet-acute astma in de tweedelijn.
Werkgroep
- Dr. B. (Bas) Langeveld, longarts, werkzaam in het Deventer ziekenhuis te Deventer, NVALT (voorzitter)
- Dr. A. (Astrid) Aardenburg – van Huisstede, longarts, werkzaam in Noordwest Ziekenhuisgroep
- Dr. M (Marijke) Amelink, longarts, werkzaam in het Spaarne Gasthuis te Haarlem, NVALT
- Drs. L.M. (Leonie) Imming, longarts, werkzaam in Medisch Spectrum Twente te Enschede, NVALT
- Dr. B. (Bart) Hilvering, longarts, werkzaam in het Amsterdam UMC te Amsterdam, NVALT
- Dr. J.N.G. (Hanneke) Oude Elberink, allergoloog, werkzaam in het Universitair Medisch Centrum Groningen te Groningen, NIV/NVvAKI
- Dr. M.E. (Marjolein) Cornet, KNO-arts, werkzaam in het Alrijne ziekenhuis te Leiden, NVKNO
- Prof. dr. J.W.M. (Jean) Muris, huisarts en hoogleraar Huisartsgeneeskunde, NHG
- Drs. M.H.A. (Mariëtte) Scholma-Bronsema, verpleegkundige specialist Astma/COPD/OSA, werkzaam in het Wilhelmina Ziekenhuis te Assen, V&VN
- Drs. Y. (Yvonne) Kappe, senior beleidsadviseur, Longfonds & VND
- Drs. E.M. (Esther) van der Roest, ervaringsdeskundige, VND
- S.T. (Saskia) van Dorst M, ervaringsdeskundige, Longfonds
Klankbordgroep
- Wendy Bokxem, Verpleegkundig specialist longgeneeskunde i.o, werkzaam in Ziekenhuisgroep Twente te Hengelo, V&VN
Met ondersteuning van
- M. (Mark) van Eck, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (Janneke) Hoogervorst-Schilp, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.N. (Nynke) Kampstra, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Werkgroep
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. B. (Bas) Langeveld, (voorzitter) |
Longarts, Deventer ziekenhuis |
Incidenteel deelname adviesraad industrie (AstraZeneca, Novartis, GSK) over biologicals (betreft ernstig astma, dit valt buiten scope van de richtlijn) |
Deelname Studies: AstraZeneca: ANDHI, tot 2019 GSK: NIMBLE, start 2e kwartaal 2022 (PI) Studies betreffen middelen voor de behandeling van ernstig astma, dit valt buiten de inhoud van deze richtlijn. Opbrengst komt ten goede van de onderzoeksafdeling longziekten van het Deventer ziekenhuis |
Geen restricties (ernstig astma valt buiten deze richtlijn). Deelname adviesraad wordt neergelegd gedurende richltijnontwikkeling. |
|
Dr. A. (Astrid) Aardenburg – van Huisstede |
Longarts, Noordwest Ziekenhuisgroep |
Bijscholing huisartsen CASPIR (betaald) Principal Investigator diverse onderzoeken opgezet door farmacie (betaald) |
Voor alle genoemde studies lokale projectleider: * UMCG - High-flow therapie bij COPD * Astra Zeneca - Oberon studie (COPD) * Franciscus Gasthuis - Tricolon studie (COPD) * Rapsodie database ernstig astma - Geen projectleider |
Geen restricties |
|
Dr. M (Marijke) Amelink |
Longarts, Spaarne ziekenhuis |
Research waarbij unrestricted grant van teva (onbetaald voor mij) mbt ernstig astma. - spreker caspir cursus (betaald via caspir) - verschillende keren een adviesraad gedaan voor pharmacie (eenmalige vergoeding voor astra Z, GSK, Sanofi) - mede voorzitter noord NL symposium met Els Weersink (sponsor chiesi, onbetaald). Staat los van astma. Ik heb geen aandelen, opties of financiële belangen bij een bedrijf. Geen lopend betaald adviseurschap. |
1 unrestricted grand mbt ernstig astma |
Geen restricties |
|
Drs. L.M. (Leonie) Imming |
Longarts, MST |
Geen |
GSK: NIMBLE, start 2e kwartaal 2022. Studie betreft middelen voor de behandeling van ernstig astma, dit valt buiten de inhoud van deze richtlijn. |
Geen restricties |
|
Dr. B. (Bart) Hilvering |
Longarts, Amsterdam UMC |
Incidenteel advisory boards en voordrachten over ernstig astma door GSK, AstraZeneca, Sanofi, dit valt buiten de scope van de richtlijn |
Lokale PI voor de AIRLEAF en CLAIRLEAF studie, geïnitieerd door Boehringer Ingelheim, medicatie voor bronchiectasieen, dit valt buiten de scope van de richtlijn |
Geen restricties |
|
Dr. J.N.G. (Hanneke) Oude Elberink |
Internist-allergoloog, UMCG |
Geen |
Geen |
Geen restricties |
|
Dr. M.E. (Marjolein) Cornet |
KNO-arts, Alrijne ziekenhuis |
Geen |
Geen |
Geen restricties |
|
Prof. dr. J.W.M. (Jean) Muris |
Geen |
Geen |
Geen |
Geen restricties |
|
M.H.A. (Mariëtte) Scholma-Bronsema |
Verpleegkundig specialist longziekten Wilhelmina Ziekenhuis Assen |
Vrijwilliger longfonds voorzitter kwaliteitsteam Assen van de Huisartsen Zorg Drenthe. Lid van transmurale zorg aanpak astma-COPD (landelijke commissie). |
Geen |
Geen restricties |
|
Drs. Y. (Yvonne) Kappe |
Projectleider Longfonds en astmaVereniging Nederland en Davos
|
Geen |
Geen |
Geen restricties |
|
Drs. E.M. (Esther) van der Roest |
ErvaringsdeskundigeastmaVereniging Nederland en Davos |
Geen |
Geen |
Geen restricties |
|
S.T.M. (Saskia) van Dorst |
Ervaringsdeskundige Longfonds |
Geen |
Geen |
Geen restricties |
Klankbordgroep
|
Klankbordgroep lid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Drs. W. (Wendy) Bokxem |
Verpleegkundig specialist longgeneeskunde, ZGT Hengelo |
Geen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afvaardiging van astmaVereniging Nederland en Davos en Longfonds in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie kopje waarden en voorkeuren van patiënten). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patientenfederatie Nederland en de aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz. Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
| Module |
Uitkomst raming |
Toelichting |
|
Rol FeNO diagnostiek |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met niet-acute astma. Tevens zijn er (aanvullende) knelpunten aangedragen door de Nederlandse Associatie Physician Assistants, Longfonds en Astma Vereniging Nederland en Davos, NVALT-sectie astma & allergie, COPD & Astma Huisartsen Advies Groep en de Nederlandse Vereniging van Ziekenhuizen via een schriftelijke knelpuntenanalyse. Een verslag hiervan is opgenomen onder aanverwante producten. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#21 |
#18 NOT #19 Artikel Fahy niet gevonden |
1 |
|
#20 |
#18 AND #19 Sleutelartikelen gevonden |
2 |
|
#19 |
#12 OR #13 OR #14 |
1305 |
|
#18 |
#15 OR #16 OR #17 |
3 |
|
#17 |
'type 2 inflammation in asthma--present in most, absent in many' AND fahy |
1 |
|
#16 |
'diagnosing asthma' AND smith AND 2004 |
1 |
|
#15 |
'diagnostic accuracy of minimally invasive markers for detection of airway eosinophilia in asthma: a systematic review and meta-analysis' |
1 |
|
#14 |
#7 AND (#10 OR #11) Observationele studies |
1203 |
|
#13 |
#7 AND #9 Clinical trial, RCT |
474 |
|
#12 |
#7 AND #8 SR |
98 |
|
#11 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
13738438 |
|
#10 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
6767914 |
|
#9 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3699598 |
|
#8 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
889513 |
|
#7 |
#5 AND #6 |
1646 |
|
#6 |
'sensitivity and specificity'/de OR sensitiv*:ab,ti OR specific*:ab,ti OR predict*:ab,ti OR 'roc curve':ab,ti OR 'receiver operator':ab,ti OR 'receiver operators':ab,ti OR likelihood:ab,ti OR 'diagnostic error'/exp OR 'diagnostic accuracy'/exp OR 'diagnostic test accuracy study'/exp OR 'inter observer':ab,ti OR 'intra observer':ab,ti OR interobserver:ab,ti OR intraobserver:ab,ti OR validity:ab,ti OR kappa:ab,ti OR reliability:ab,ti OR reproducibility:ab,ti OR ((test NEAR/2 're-test'):ab,ti) OR ((test NEAR/2 'retest'):ab,ti) OR 'reproducibility'/exp OR accuracy:ab,ti OR 'differential diagnosis'/exp OR 'validation study'/de OR 'measurement precision'/exp OR 'diagnostic value'/exp OR 'reliability'/exp OR 'predictive value'/exp OR ppv:ti,ab,kw OR npv:ti,ab,kw |
9559472 |
|
#5 |
#4 AND [1-1-2000]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
3464 |
|
#4 |
#3 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
6510 |
|
#3 |
#1 AND #2 |
8669 |
|
#2 |
'asthma'/exp OR 'bronchus hyperreactivity'/exp OR 'airway obstruction'/exp OR (((airway OR airflow OR repirator*) NEAR/2 (obstruct* OR occlusion* OR closure)):ti,ab,kw) OR ((bronch* NEAR/2 (hyperreactiv* OR 'hyper reactiv*' OR hyperrespons* OR 'hyper respons*')):ti,ab,kw) OR asthma*:ti,ab,kw OR wheez*:ti,ab,kw OR breathles*:ti,ab,kw |
413954 |
|
#1 |
'fractional exhaled nitric oxide'/exp OR 'fractional exhaled nitric oxide test'/exp OR 'feno':ti,ab,kw OR ((exhaled NEAR/3 (no OR 'nitric oxide*')):ti,ab,kw) |
11317 |
Ovid/Medline
|
# |
Searches |
Results |
|
16 |
14 not 13 not 12 Observationele stuies |
531 |
|
15 |
13 not 12 Clinical trial, RCT |
318 |
|
14 |
7 and (10 or 11) |
805 |
|
13 |
7 and 9 |
339 |
|
12 |
7 and 8 SR |
52 |
|
11 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5320871 |
|
10 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4323436 |
|
9 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2536907 |
|
8 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
635341 |
|
7 |
5 and 6 |
1340 |
|
6 |
exp "Sensitivity and Specificity"/ or (Sensitiv* or Specific*).ti,ab. or (predict* or ROC-curve or receiver-operator*).ti,ab. or (likelihood or LR*).ti,ab. or exp Diagnostic Errors/ or (inter-observer or intra-observer or interobserver or intraobserver or validity or kappa or reliability).ti,ab. or reproducibility.ti,ab. or (test adj2 (re-test or retest)).ti,ab. or "Reproducibility of Results"/ or accuracy.ti,ab. or Diagnosis, Differential/ or Validation Study/ |
7648880 |
|
5 |
limit 4 to yr="2000 -Current" |
2830 |
|
4 |
3 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
2967 |
|
3 |
1 and 2 |
4233 |
|
2 |
Fractional Exhaled Nitric Oxide Testing/ or feno.ti,ab,kf. or (exhaled adj3 ("NO" or nitric oxide*)).ti,ab,kf. |
5996 |
|
1 |
exp Asthma/ or Bronchial Hyperreactivity/ or Airway Obstruction/ or ((airway or airflow or repirator*) adj2 (obstruct* or occlusion* or closure)).ti,ab,kf. or (bronch* adj2 (hyperreactiv* or hyper reactiv* or hyperrespons* or hyper respons*)).ti,ab,kf. or asthma*.ti,ab,kf. or wheez*.ti,ab,kf. or breathles*.ti,ab,kf. |
242639 |