Behandeling EUG
Uitgangsvraag
Welke plaats heeft een afwachtend of medicamenteus beleid (MTX) versus chirurgisch beleid in de behandeling van de EUG?
Aanbeveling
PICO 1 Afwachten vs. Medicamenteuze behandeling
Voer een expectatief beleid (1 week) bij vrouwen met een persisterende ZOL (serum-hCG < 2000 IE/L) of een EUG met een plateau in serum-hCG-waarde (serum-hCG < 1500 IE/L) die weinig symptomen hebben en goed te instrueren zijn.
PICO 2 Medicamenteuze behandeling MTX vs. Chirurgie
Weeg samen met de patiënt de voor en nadelen van niet invasieve en invasieve behandelingen af voordat de behandeling in gang wordt gezet.
Geef bij voorkeur als niet-invasie therapie systemisch MTX bij vrouwen met een persisterende ZOL (T96 serum-hCG > 2000 IE/L) of EUG (serum-hCG >1500 IE/L) die weinig symptomen hebben en goed te instrueren zijn en niet in aanmerking komen voor afwachtend beleid op grond van serum- hCG.
Voer chirurgie uit bij vrouwen met een EUG met een serum-hCG > 5000 IE/L of bij een echoscopisch bewezen EUG met omvang > 4cm of een vitale EUG.
Overweeg chirurgie bij vrouwen waarbij het niet mogelijk is om instructies te volgen/ die niet terug kunnen komen voor follow-up met een persisterende ZOL (T96 serum-hCG < 2000 IE/L) en klachten.
Overwegingen
PICO 1 Afwachten vs. Medicamenteuze behandeling
Voor de behandeling van een buitenbaarmoederlijke zwangerschap met een lage en een plateau in serum-hCG waarde is een expectatief beleid een alternatief voor behandeling met een enkele (single) dosis systemisch methotrexaat. Zestig procent van de vrouwen met een zichtbare buitenbaarmoederlijke zwangerschap en serum-hCG <1500 IE/L of vrouwen met een ZOL en serum- hCG <2000 IE/L heeft een ongecompliceerd klinisch beloop met een spontane daling van het serum- hCG na expectatief beleid. Dit betekent dat methotrexaat, een potentieel schadelijk medicijn, niet primair hoeft te worden gegeven aan deze vrouwen. Zie de module ‘Behandeling EUG: MTX’ voor details over MTX behandeling.
PICO 2 Medicamenteuze behandeling MTX vs. Chirurgie
Een belangrijke verandering van deze huidige richtlijn ten opzichte van de voorgaande is de nieuwe evidence om bij patiënten met een EUG tot hogere serum-hCG-waarden MTX te geven in een variabel schema, zie de module ‘Behandeling EUG: MTX’. Het variabele schema bestaat uit een enkele (single) dosis MTX, waar bij onvoldoende daling (< 15%) van het serum-hCG na een week een herhaalde dosis MTX wordt gegeven tot maximaal 4 dosis in totaal (variabele dosis). Klinische symptomen verdacht voor een tubaruptuur zijn altijd een indicatie voor een chirurgische interventie, zie de module ‘Behandeling EUG: Chirurgie’. Hetzelfde geldt voor vrouwen met een contra-indicatie voor MTX of die lastig te instrueren zijn voor strikte follow-up.
De NICE richtlijn adviseert een bovengrens voor de behandeling met een variabele dosis MTX van 5000 IE/L op basis van het inclusiecriterium (max. hCG 5000 IE/L) van de studie van Sowter (Sowter, 2001). De overige vier studies hadden 10.000 IE/L of geen bovenste serum-hCG limit. De gemiddelde hCG of mediane hCG van de geïncludeerde patiënten in deze studies was tussen de 2.000 IE/L en 3.200 IE/L. Voor een beschrijving van de hCG-profielen van de geïncludeerde patiënten, zie de evidencetabel. De werkgroep neemt deze bovengrens van de NICE over als advies op basis van bovenstaande gepoolde data. Bij vrouwen met een contra-indicatie voor een operatie is MTX bij hogere hCG-waarden ook effectief gebleken; dan gaat de voorkeur uit naar multipele dosis schema (zie ook de module ‘Behandeling EUG: MTX’).
Onderbouwing
In de huidige situatie in Nederland zijn drie behandelopties voor vrouwen met een tubaire EUG of persisterende zwangerschap met onbekende locatie (ZOL): 1) chirurgie 2) medicamenteuze behandeling met systemisch MTX of 3) een afwachtend beleid. Deze module evalueert de effectiviteit en de veiligheid van deze drie behandelopties en beschrijft de patiëntenpopulatie waarin deze uitkomstmaten zijn onderzocht.
PICO 1 Afwachten vs. Medicamenteuze behandeling
|
Laag GRADE |
Een week expectatief beleid is even effectief als een systemisch MTX in patiënten met een verdenking EUG en hCG-waarden < 1500 IE/L of bij een persisterende ZOL en hCG- waarden < 2000 IE/L. Bronnen: Van Mello, 2013; Silva, 2015 |
|
Laag GRADE |
Er is geen verschil in kwaliteit van leven tussen een expectatief beleid en een systemisch MTX als behandeling van vrouwen met een tubaire EUG. Bron: Van Mello, 2013 |
PICO 2 Medicamenteuze behandeling MTX vs. Chirurgie
|
Laag GRADE |
Systemisch MTX is effectiever dan een tubotomie als behandeling van vrouwen met een tubaire EUG met hCG waarden < 5000 -15.000 IE/L. Bronnen: El-Sherbiny, 2003; Fernandez, 1998; Krag Muller, 2009; Saraj, 2008; Sowter, 2001a |
|
Laag GRADE |
Kwaliteit van leven is hoger na een tubotomie in vergelijking met systemisch MTX bij vrouwen met een EUG. Bron: Nieuwkerk, 1998 |
|
Laag GRADE |
Systemisch MTX geeft een beter fysiek functioneren dan een tubotomie bij vrouwen met een EUG. Bron: Sowter, 2001 |
|
Laag GRADE |
Er is geen verschil in toekomstige fecunditeit tussen systemisch MTX en tubotomie bij vrouwen met een EUG. Bronnen: Dias Pereira, 1999; Fernandez, 2013 |
PICO 1 Afwachten vs. Medicamenteuze behandeling
Beschrijving studies
Er waren drie RCTs (Khorhonen, 1996; Van Mello, 2013; Silva, 2015) die een afwachtend beleid vergeleken met een medicamenteuze behandeling. De eerste vergelijking ging tussen afwachtend beleid en oraal MTX (n=60, Khorhonen, 1996). Dit was een single centre placebogecontroleerde studie. De gemiddelde serum-hCG concentraties waren laag, i.e. 211 IE/l (range 20–1343) in de afwachtend beleid groep en 395 IE/l (range 61–4279) in de orale MTX groep. De tweede vergelijking ging tussen afwachtend beleid en systemisch enkele (single) dosis MTX (Van Mello, 2013; Silva, 2015). De patiënten waren hemodynamisch stabiel en hadden geen contra-indicatie voor MTX. De RCT uit Nederland (Van Mello, 2013) hanteerde geen maximale grootte van de EUG en de bovenste limiet van het serum-hCG gehalte varieerde tussen 1500 bij een echoscopische afwijking verdacht voor EUG en 2000 IE/L bij een ZOL. De studie van Silva, 2015 includeerde alleen vrouwen met een echoscopisch zichtbare EUG en vergelijkbare hCG waarde. Verdere details staan in de evidencetabel.
Resultaten
Toekomstige fecunditeit
Geen van de drie studies heeft de uitkomstmaat toekomstige fecunditeit gerapporteerd.
Behandelsucces (ongecompliceerde daling hCG)
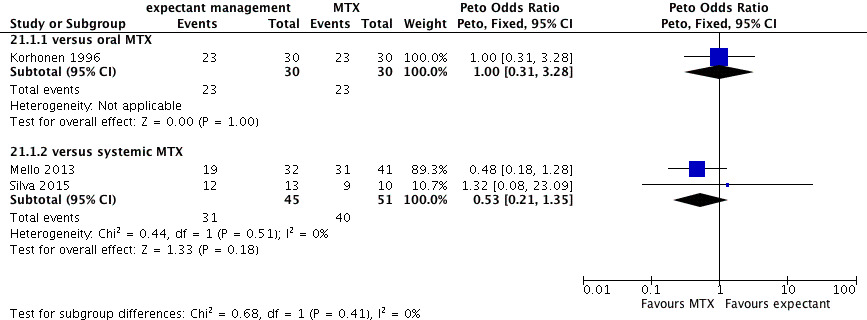
De studie van Korhonen, 1996 waarbij een afwachtend beleid werd vergeleken met orale MTX vond geen significant verschil in behandelsucces (OR 1,00; 95% BI 0,31–3,28). In beide groepen was in 23% een chirurgische interventie nodig zonder gespecificeerde reden.
Het gepoolde resultaat van de twee studies die een afwachtend beleid vergeleken met systemisch MTX in een enkele (single) dosis lieten zien dat het succes van een afwachtend beleid in 68,9% succesvol was en enkele (single) dosis MTX in 78,4% van de vrouwen (twee RCTs, n=91, OR 0,53; 95% BI 0,21 – 1,35) (Van Mello, 2013; Silva, 2015).
Bijwerkingen van MTX
Bekende bijwerkingen van MTX werden in een lage frequentie en milde vorm gemeld door 22% van de vrouwen in de MTX groep en 9% in de afwachtend beleid groep (Van Mello, 2013). Follow up van serumwaarden (bloedbeeld, lever en nierfuncties) lieten geen verschil zien (Korhonen, 1996, Silva, 2015) of een minimale transaminase stijging (Van Mello, 2013).
Kwaliteit van leven
In de studie van Van Mello werd geen verschil gevonden in de kwaliteit van leven op psychologisch en fysiek vlak (Van Mello, 2015). De studie van Silva, 2015 en Korhonen, 1996 hebben geen kwaliteit van leven onderzoek gedaan.
Recidief EUG
Deze uitkomstmaat is (nog) niet gerapporteerd door de geïncludeerde RCTs (Van Mello, 2015; Silva, 2015).
Afwachten vs. chirurgie
Er waren geen RCTs die een afwachtend beleid vergeleken met chirurgie.
Bewijskracht van de literatuur
De studies zijn interventiestudies en werden beoordeeld met behulp van GRADE. Omdat het RCTs zijn start de bewijskracht op een hoog niveau.
De bewijskracht voor de uitkomstmaat behandelsucces is met twee niveaus verlaagd gezien tegenstrijdige resultaten (inconsistentie, zie meta-analyse) en het geringe aantal patiënten (imprecisie).
De bewijskracht voor de uitkomstmaat kwaliteit van leven is ook met twee niveaus verlaagd omdat het één studie betreft (Van Mello, 2013) en deze studie een gering aantal patiënten heeft.
PICO 2 Medicamenteuze behandeling MTX vs. Chirurgie
Beschrijving van de studies
Er waren zeven RCTs die een medicamenteuze behandeling met systemisch MTX vergeleken met chirurgische behandeling. De eerste vergelijking ging tussen systemisch MTX en tubotomie per laparoscopie (El-Sherbiny, 2003; Fernandez, 1998, Hajenius, 1997; Krag Moeller, 2009; Saraj, 1998; Sowter, 2001a; systemisch MTX werd hierbij gebruikt in een fixed multipele dosis afgewisseld met folinezuur (Hajenius, 1997), een enkele (single) dosis of een variabele dosis schema zonder folinezuur. De tweede vergelijking ging tussen enkele (single) dosis systemisch MTX versus tubotomie per laparoscopie gecombineerd met een preventieve enkele (single) dosis systemisch MTX binnen 24 uur postoperatief (Fernandez, 2013).
De patiëntengroepen betroffen vrouwen met een evidente EUG of een persisterende ZOL. Zij waren hemodynamisch stabiel en hadden geen contra-indicatie voor MTX. In de meeste RCTs was de maximale grootte van de EUG 3-4 cm en de bovenste limiet van het serum-hCG gehalte varieerde tussen 5000 en 15.000 IE/L en was er geen cardiale activiteit van de eventuele foetus. Verdere details staan in de evidencetabel.
Resultaten
Toekomstige fecunditeit
Er werd geen verschil gevonden in spontane intra-uteriene zwangerschap na het fixed multipele dosis schema (36%) in vergelijking met tubotomie (40%) (n=74; RR 0,88; 95% BI 0,49–1,60) (Dias Pereira, 1999). In het variabele dosis schema werden ook geen verschillen gevonden in de kans op een intra-uteriene zwangerschap (n=202; OR 1,33; 95% BI 0,73–2,40) in vergelijking met een tubotomie (gepoolde data). De RCT die enkele (single) dosis systemisch MTX vergeleek met tubotomie per laparoscopie gecombineerd met een preventieve enkele (single) dosis systemisch MTX binnen 24 uur postoperatief liet geen verschil gezien in de kans op een intra-uteriene zwangerschap (n=207; OR 0,83; 95% BI 0,43-1,58) (Fernandez, 2013).
Behandelsucces (ongecompliceerde daling hCG)
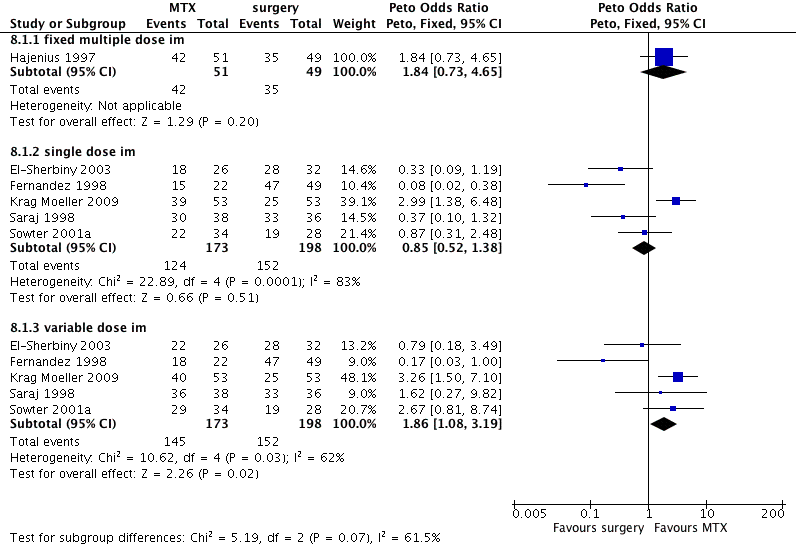
Er was een niet significante trend naar een grotere kans op het verdwijnen van de EUG met systemisch MTX in een fixed multipele dosis schema in vergelijking met laparoscopische tubotomie (RR 1,15; 95% BI 0,93–1,43) (Hajenius, 1997). Het gepoolde resultaat van vijf RCTs (n=371) liet geen verschil zien in behandelsucces tussen een enkele (single) dosis systemisch MTX (50 mg/m2 of 1 mg/kg i.m.) of laparoscopische tubotomie (OR 0,85; 95% BI 0,52–1,38) (El-Sherbiny, 2003; Fernandez, 1998, Krag Muller, 2009; Saraj, 2008; Sowter, 2001a). Met een variabele dosis MTX steeg het behandelsucces en liet het een significant verschil zien met laparoscopische tubotomie (RR 1,86; 95% BI 1,08–3,19) in het voordeel van variabele dosis MTX. Uit de RCT die de enkele (single) dosis systemisch MTX vergeleek met tubotomie per laparoscopie gecombineerd met een preventieve enkele (single) dosis systemisch MTX binnen 24 uur postoperatief blijkt dat een enkele (single) dosis MTX minder effectief is (OR 0,43; 95% BI 0,21-0,91) (Fernandez, 2013).
Bijwerkingen van MTX of van laparoscopische tubotomie
De bijwerkingen werden in de studies niet eenduidig geclassificeerd. Zie evidencetabel.
Kwaliteit van leven
Vrouwen hadden na een fixed multipele dosis MTX schema een significant slechtere kwaliteit van leven (psychologische en fysieke aspecten) dan vrouwen die behandeld werden met laparoscopische tubotomie (p <0,05) (Nieuwkerk, 1998a).
Vrouwen hadden na een enkele (single) dosis MTX een betere kwaliteit van leven dan na laparoscopische tubotomie (p<0,01) (Sowter, 2001). In een variabele dosis schema is de kwaliteit van leven niet onderzocht. De RCT die een enkele (single) dosis systemisch MTX vergeleek met tubotomie per laparoscopie gecombineerd met een preventieve enkele (single) dosis systemisch MTX binnen 24 uur postoperatief rapporteerde geen kwaliteit van leven (Fernandez, 2013).
Recidief EUG
De kans op een recidief EUG werd gerapporteerd door dezelfde zes RCTs in drie vergelijkingen. Deze kans was niet verschillend tussen een fixed multipele dosis MTX en tubotomie (OR 0,88; 95% BI 0,21– 3,67) (Dias Pereira, 1999); een variabele dosis MTX en tubotomie (OR 0,39; 95% BI 0,10–1,48) (gepoolde data) of een enkele (single) dosis MTX en tubotomie met een preventieve enkele (single) dosis MTX (OR 1,19; 95% BI 0,40-3,51) (Fernandez, 2013).
Bewijskracht van de literatuur
De studies zijn interventiestudies en werden beoordeeld met behulp van GRADE. Omdat het RCTs zijn start de bewijskracht op een hoog niveau.
De bewijskracht voor de uitkomstmaat behandelsucces is met twee niveaus verlaagd gezien heterogeniteit in de resultaten (uiteenlopende 95% BI) en het geringe aantal patiënten (imprecisie). Daarnaast zijn de studies Krag Muller, 2009 en Sowter, 2001 vroegtijdig gestopt vanwege inclusie en fundingproblemen.
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met twee niveaus verlaagd omdat het twee studies betreft (Nieuwkerk, 1998 en Sowter, 2001) die niet gepoold konden worden. De studie van Nieuwkerk betrof multipele dosis MTX inclusief een diagnostische laparoscopie en de studie van Sowter betrof variabele dosis MTX. Daarnaast hadden deze studies een gering aantal patiënten.
De bewijskracht voor de uitkomstmaat toekomstige fecunditeit is met twee niveaus verlaagd omdat het twee studies betreft (Dias Pereira, 1999 en Fernandez, 2013) die niet gepoold konden worden. De studie van Dias Pereira betrof multipele dosis MTX en de studie van Fernandez betrof variabele dosis MTX. Daarnaast hadden deze studies een gering aantal patiënten.
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht naar de volgende wetenschappelijke vraagstellingen:
Wat is de effectiviteit en veiligheid van afwachtend beleid ten opzichte van medicamenteus beleid of chirurgie?
PICO 1
P waarschijnlijk bewezen EUG
I expectatief beleid
C ander behandeling (medicamenteus of chirurgisch)
O effectiviteit: toekomstige fecunditeit (spontane intra-uteriene zwangerschap), ongecompliceerde daling hCG (verdwijnen EUG) veiligheid: kwaliteit van leven, patiënttevredenheid, recidief EUG
Wat is de effectiviteit en veiligheid van medicamenteus beleid ten opzichte van chirurgie?
PICO 2
P hoogstwaarschijnlijk bewezen/bewezen EUG
I MTX
C chirurgisch beleid
O effectiviteit: toekomstige fecunditeit (spontane intra-uteriene zwangerschap), ongecompliceerde daling hCG (verdwijnen EUG) veiligheid: kwaliteit van leven, patiënttevredenheid, recidief EUG
Relevante interventies
Voor deze richtlijn hebben we alleen de vergelijkingen geselecteerd die ook werkelijk in de klinische praktijk worden gebruikt:
1) Afwachten/expectatief beleid gedurende een week waarbij evaluatie met serum-hCG. Indien het serum-hCG minder dan 15% daalt wordt er alsnog een enkele (single) dosis MTX toegediend.
2) Systemisch MTX:
a. In een enkele (single) dosis waarna evaluatie na 1 week. Indien minder dan 15% daling ten opzichte van serum-hCG op dag 0 van MTX een tweede dosis (etc. met een maximum van 4 doses). Indien er een tweede of meer enkele (single) dosis nodig zijn heet dit ook wel een variabele dosis.b. In een multipele dosis schema (dag 0, 2, 4, 6) afgewisseld met folinezuur (dag 1, 3, 5, 7). Voor MTX-behandeling wordt u verwezen naar de module ‘Behandeling EUG: MTX’.
3) Of een laparoscopische tubectomie of tubotomie.
Interventies waarbij lokale injecties in de vruchtzak worden gegeven worden niet besproken omdat dit visualisatie van de ectopische vruchtzak vereist en de benodigde technische vaardigheden van de behandelaar.
Relevante uitkomstmaten
De werkgroep achtte toekomstige fecunditeit (spontane intra-uteriene zwangerschap) en een ongecompliceerde daling hCG (verdwijnen EUG) voor de besluitvorming kritieke uitkomstmaten (benefits). Belangrijke veiligheidsuitkomstmaten zijn kwaliteit van leven, patiënttevredenheid en recidief EUG. Een Health Technology Assessment (HTA) valt buiten de scoop van deze richtlijn en expertise van de werkgroep. Om deze reden zijn kosten niet als uitkomstmaat opgenomen en worden deze niet afgewogen tegen de effectiviteit en veiligheid.
Methode
Hiervoor is gebruik gemaakt van de systematische search en selectie uitgevoerd door de Cochrane Collaboration tot juli 2015 (Medline, Embase, CINAHL). In de databases is met relevante zoektermen gezocht naar RCT’s die de effectiviteit van EUG-behandelingen onderzochten. Er wordt volgens de Cochrane criteria niet met een uitkomstmaat gezocht, derhalve is er geen rangorde in verschillende uitkomstmaten.
De zoekverantwoording is weergegeven onder het tabblad Verantwoording. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- RCT én
- Interventies voor (tubaire) EUG.
Op basis van titel en abstract werden in eerste instantie 87 studies voorgeselecteerd. Na raadpleging van de volledige tekst werden vervolgens 25 studies geëxcludeerd (zie exclusietabel). De overgebleven 56 studies werden geselecteerd. Van deze 56 studies sluiten 14 RCTs aan bij de uitgangsvragen van deze module omdat ze interventies vergeleken tussen behandelopties afwachten, medicamenteuze behandeling of chirurgie. Vier RCTs werden alsnog geëxcludeerd omdat deze niet in de klinisch praktijk worden gebruikt: één RCT die afwachten vergeleek met lokale prostaglandine injecties (Egarter, 1991) en drie RCTs die lokale MTX-injectie onder echogeleide of per laparoscopie vergeleken met tubotomie per laparoscopie (Fernandez, 1998; Mottla, 1992; Zilber, 1996). Zes publicaties rapporteren over secundaire uitkomstmaten van de originele studies (Dias Pereira, 1999; Mol, 1999; Van Mello, 2015; Nieuwkerk, 1998a; Sowter, 1991).
Resultaten
Tien RCTs en zes publicaties over secundaire uitkomstmaten van deze RCTs zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Dias Pereira G., Hajenius PJ, Mol BWJ, Ankum WM, Hemrika DJ, Bossuyt-PMM ea. Fertility outcome after systemic methotrexate and laparoscopic salpingostomy for tubal pregnancy. Lancet 1999;353:724-5.
- Elmoghazy-DAM-and-Nour-El-Dine-NM. Prevention of persistent ectopic pregnancy with single dose methotrexate after surgical conservation of the tube. Abstracts of the XVI FIGO World Congress of Obstetrics & Gynecology 2000;57.
- El-Sherbiny MT, El G, I, Mera IM. Methotrexate verus laparoscopic surgery for the management of unruptured tubal pregnancy. Middle east Fertility Society Journal 2003;8:256-62.
- Fernandez H, Pauthier S, Sitbon D, Vincent Y, Doumerc S. Role of conservative therapy and medical treatment in ectopic pregnancy: literature review and clinical trial comparing medical treatment and conservative laparoscopic treatment. Contraception Fertilite Sexualite 1996;24:297-302.
- Fernandez H, Yves Vincent SC, Pauthier S, Audibert F, Frydman R. Randomized trial of conservative laparoscopic treatment and methotrexate administration in ectopic pregnancy and subsequent fertility. Hum Reprod 1998;13:3239-43.
- Hajenius PJ, Engelsbel S, Mol BW, van der Veen F, Ankum WM, Bossuyt PM, Hemrika DJ, Lammes FB. Randomised trial of systemic methotrexate versus laparoscopic salpingostomy in tubal pregnancy. Lancet 13-9-1997;350:774-9.
- Hajenius P, Mol F, Mol B, Bossuyt P, Ankum W, Van d, V. Interventions for tubal ectopic pregnancy. Cochrane Database Syst Rev 2007;CD000324.
- Korhonen J, Stenman U, Ylostalo P. Low-dose oral methotrexate with expectant management of ectopic pregnancy. Obstetrics & Gynecology 1996;88:775-8.
- Krag Moeller LBK, Moeller C, Thomsen SG, Andersen LF, Lundvall L, Lidegaard O, Kjer JJ, Ingemanssen JL, Zobbe V, Floridon C, Petersen J, Ottesen B. Success and spontaneous pregnancy rates following systemic methotrexate versus laparoscopic surgery for tubal pregnancies: A randomized trial. Acta Obstetricia et Gynecologica 2009;88:13311337.
- Mol BWJ, Hajenius PJ, Engelsbel S, Ankum WM, Hemrika DJ, Van d, V. The treatment of tubal pregnancy in The Netherlands: an economic evaluation of systemic methotrexate and laparoscopic salpingostomy. American Journal of Obstetrics & Gynecology 1999;181:945-51.
- Nieuwkerk PT, Hajenius PJ, Ankum WM, van d, V, Wijker W, Bossuyt PM. Systemic methotrexate therapy versus laparoscopic salpingostomy in patients with tubal pregnancy. Part I. Impact on patients' health-related quality of life. Fertil Steril 1998;70:511-7.
- Nieuwkerk PT, Hajenius PJ, van d, V, Ankum WM, Wijker W, Bossuyt PM. Systemic methotrexate therapy versus laparoscopic salpingostomy in tubal pregnancy. Part II. Patient preferences for systemic methotrexate. Fertil Steril 1998;70:518-22.
- Saraj AJ, Wilcox JG, Najmabadi S, Stein SM, Johnson MB, Paulson RJ. Resolution of hormonal markers of ectopic gestation: a randomized trial comparing single dose intramuscular methotrexate with salpingostomy. Obstetrics & Gynecology 1998;92:989-94.
- Silva PM, Araujo Júnior E, Cecchino GN, Elito Júnior J, Camano L. Effectiveness of expectant management versus methotrexate in tubal ectopic pregnancy: a double-blind randomized trial.. Arch Gynecol Obstet 2015;291(4):939-43.
- Sowter MC, Farquhar CM, Petrie KJ, Gudex G. A randomised trial comparing single dose systemic methotrexate and laparoscopic surgery for the treatment of unruptured ectopic pregnancy. British Journal of Obstetrics & Gynaecology 2001;108:192-203.
- Sowter MC, Farquhar CM, Gudex G. An economic evaluation of single dose systemic methotrexate and laparoscopic surgery for the treatment of unruptured ectopic pregnancy. BJOG 2001;108:204-12.
- Su Y, Sun Y, Ma M. Observation on treatment of ectopic pregnancy by combination therapy of Chinese herbal medicine with Mifepristone or Methotrexate. Zhongguo Zhong Xi Yi Jie He Za zhi Zhongguo Zhongxiyi Jiehe Zazhi 2002;22:417-9.
- Van Mello NM, Mol F, Verhoeve HR, van Wely M, Adriaanse AH, Boss EA, Dijkman AB, Bayram N, Emanuel MH, Friederich J, van der Leeuw-Harmsen L, Lips JP, van Kessel MA, Ankum WM, van der Veen F, Mol BW, Hajenius PJ. Methotrexate or expectant management in women with ectopic pregnancy or pregnancy of unknown location and low serum hCG concentrations? A randomised comparison. Hum Reprod 2013;28:60-7.
- Van Mello NM, Mol F, Hajenius PJ, Ankum WM, Mol BW, van der Veen F, van Wely M. Randomized comparison of health-related quality of life in women with ectopic pregnancy or pregnancy of unknown location treated with systemic methotrexate or expectant management. Eur J Obstet Gynecol Reprod Biol. 2015;Sep(192):1-5.
- Wang J, Yang Q, Yu Z. Clinical study of tubal pregnancy treated with integrated traditional Chinese and Western medicine. Zhongguuo Zhong Xi Yi Jie Z Zhi 1998;18:531-3.
- Wei FY, Chen HF. [Clinical analysis of 82 cases of ectopic pregnancy treated by methotrexate combined with traditional Chinese recipe]. Zhong Xi Yi Jie He Xue Bao 2003;1:267, 292.
Exclusie (25)
|
Auteur en jaartal |
Redenen van exclusie |
|
Akira 2008 Colacurci 1998 Fernandez 1990 Fernandez 1996 Garbin 2004 Kaya 2002 Koninckx 1991 Laatikainen 1993 Lindblom 1997 Lund 1955 Lundorf 1993a Lundorff 1993b Lundorff 1997 Mello 2008 Mol 2008a Mol 2008b Murphy 1992 O'Shea 1994 Porpora 1996 Song 2006 Su 2002 Wang 1998 Wei 2003 Yang 2011 Zargar 2008 |
(verwijzen naar cochrane PH281 22.07.15). |
Tabel Exclusie na Cochrane selectie (38+4) (na het lezen van het volledige artikel)
| Auteur en jaartal | Redenen van exclusie |
| Alleyassin 2006 | Sluit niet aan op de uitgangsvraag |
| Cohen 1996 | |
| Elmoghazy 2000 | |
| Fedele 1998 | |
| Fernandez 1991 | |
| Fernandez 1994 | |
| Fernandez 1995 Fujishita 1995b Fujishita 2004 | |
| Gazvani 1998 | |
| Gjelland 1995 | |
| Graczykowski 1997 | |
| Gray 1995 | |
| GuvendagGuven 2010 | |
| Hamed 2012 | |
| Hordnes 1997 | |
| Klauser 2005 | |
| Landstrom 1998 | |
| Lang 1990 | |
| Lim 2007 | |
| Lundorff 1991a Lundorff 1991b Lundorff 1992 | |
| Mol 2014 | |
| Mol 2015 | |
| Rozenberg 2003 | |
| Sadan 2001 | |
| Sharma 2003 | |
| Shulman 1992 | |
| Tabatabaii 2012 Tulandi 1991a Tzafettas 1994 | |
| Ugur 1996 | |
| Vermesh 1989 | |
| Vermesh 1992 | |
| Xu 2014 | |
| Yalcinkaya 1996 | |
| Yalcinkaya 2000 | |
| Egarter 1991 | Lokale injectie prostaglandines of MTX-> geen gangbare behandeling |
| Fernandez 1998 | |
| Mottla 1992 | |
| Zilber 1996 |
| Table I. Main characteristics of included trials. | |||||
| Author (year), sample size, country | |||||
| Participants | Intervention | Comparison | Main outcomes | Quality features | |
| El-Sherbiny et al. (2003) n =55, | <4 cm No fetal cardiac activity; Serum hCG <10 000 IU/l | Single-dose MTX (50 mg/m2 i.m.) | Laparoscopic salpingotomy | Treatment success; Fertility outcome | Randomization by computer; Allocation unclear; No power calculation; Multi centre; Full paper |
| Egypt | |||||
| Fernandez et al. (1998) n =100, | EP by TVS/TAS;Pre- therapeutic score <13; Size nr; Fetal cardiac activity nr; Upper limit serum hCG nr | Single-dose MTX (1 mg/kg i.m.) | Laparoscopic salpingotomy | Treatment success; Fertility outcome | Randomization with a random number table; Allocation unclear; No power calculation; Single centre; Full paper |
| France | |||||
| Fernandez et al. (2013) n=207, | EP by TVS (mass, sac or fetal pole outside the uterus). Hemodynamically stable; Fernandez score < 13 | Single dose MTX (1 mg/kg i.m.) | Laparoscopic salpingotomy with preventive dose of MTX (1 mg/kg i.m.) within 24 hours postoperatively | Treatment success; Fertility outcome | Randomization by computer program; allocation adequeate; power calculation performed; premature ending of trial; intention to treat analysis. |
| France | Multiple Centre; full paper. | ||||
| Hajenius et al. (1997), n =100, | Laparoscopically confirmed; No fetal cardiac activity; No limit in EP size; No upper limit serum hCG | Multiple dose MTX | Laparoscopic salpingotomy | Treatment success; HRQL (Nieuwkerk et al., 1998a, b); Costs (Mol et al., 1998a,b); Fertility outcome (Dias Pereira et al., 1999) | (Block) randomization by a computer program; Allocation adequate; Power calculation performed; Intention-to- treat analysis; Multi centre; Full paper |
| The Netherlands | (1.0 mg/kg im on Days 0, 2, 4, | ||||
| 6; alternated folinic acid 0.1 | |||||
| mg/kg oral on Days 1, 3, 5, 7) | |||||
| Krag Moeller et al. (2009), n=106 | rise in plasma-hCG levels by three consecutive measurements or with an extrauterine location of a live conception with a gestational sac < 3.6 cm were eligible. Women with plasma-hCG < 2,000 IU/L were eligible for randomization only if the rate of increase was< 20%/24 hours and with no ultrasonographic sign of intrauterine pregnancy. | Systemic single dose MTX 1.0 mg/kg IM | laparoscopic salpingotomy | Treatment success Side effects Fertility | Randomization by computer program; allocation adequeate; power calculation performed; premature ending of trial; intention to treat analysis. |
| Denmark | Multiple Centre; full paper. | ||||
| Korhonen et al. (1996), n =60, | <4 cm; Fetal cardiac activity nr; Serum hCG <5000 IU/l | Expectant management | MTX 2.5 mg/day orally for 5 days | Treatment success | Randomization by table of random numbers; Allocation adequate by hospital pharmacy: double blind, placebo controlled; Power calculation performed; Single centre; Full paper |
| Finland | |||||
| Mello et al. (2013), n=73 | hemodynamically stable women with either an ectopic pregnancy visible on transvaginal sonography (an ectopic ring or an ectopic mass and/or fluid in the pouch of Douglas) and a plateauing serum hCG concentration < 1,500 IU/L or with a persisting PUL and a plateauing serum hCG concentration < 2,000 IU/L. A plateauing serum hCG was defined as a < 50% hCG increase or decrease between day 0 and day 4. Women with a viable ectopic pregnancy, signs of tubal rupture and/or active intra-abdominal bleeding, and a contraindication for MTX were not eligible. | Expectant management for one week | Single-dose MTX (1 mg/kg i.m.) | Treatment success | Randomization by computer; allocation adequate; not blinded, not placebo controlled; intention to treat analysis; Multi centre; Full paper |
| The Netherlands | Side effects and HRQL (Mello et al, 2015) | ||||
| Saraj et al. (1998), n =75, USA | <3.5 cm on TVS; No fetal cardiac activity; Upper limit serum hCG nr | Single-dose MTX (1 mg/kg i.m.) | Laparoscopic salpingotomy | Treatment success; Fertility outcome | Randomization nr; Allocation unclear, although sealed envelopes; No power calculation; Multi centre; Full paper |
| Silva et al. (2015), n=23 | confirmed tubal pregnancy (visible tubal pregnancy on transvaginal ultrasound characterized by an inhomogeneous adnexal mass or a tubal ring with or without a yolk sac, a tubal mass <5.0 cm), fertility desire, an initial serum hCG concentration < 2,000 | Expectant management (placebo) | Single dose MTX 50 mg/m2 IM | Treatment success; Side effects | Double blind |
| Brazil | Method of randomization not stated Single centre | ||||
| No power calculation | |||||
| No source of funding stated Ethical committee approval Published as full paper | |||||
| mIU/mL, declining titers of serum hCG 48 h prior to treatment, Exclusion criteria were: embryonic cardiac activity on transvaginal ultrasound, signs of tubal rupture, and contraindication for MTX. Pregnancies of unknown location were not included. | |||||
| Sowter et al. (2001a, b), | <3.5 cm; No fetal cardiac activity; Serum hCG <5000 IU/l | Single-dose MTX (50 mg/m2 i.m.) | Laparoscopic salpingotomy | Treatment success; HQRL; Costs (Sowter et al., 1991); Fertility outcome | Unblocked randomization procedure by a computer program; Allocation adequate by sequentially numbered opaque envelopes sealed by a third party; Power calculation performed; Intention-to-treat analysis; Multi centre; Full paper |
| n =62, | |||||
| New Zealand | |||||
| Evidence table for intervention studies PICO 1 | |||||||||||||
| Study reference | Study characteristics | Patient characteristics 2 | Intervention (I) | Comparison / control (C) 3 | Follow-up | Outcome measures and effect size 4 | Comments | ||||||
| Korhonen et al. | RCT, single centre, university hospital, Finland, no | Inclusion criteria: | Expectant management | MTX 2.5 mg/day orally for 5 days | Length of follow- up: | Fertility (IUG) : not reported | Initial median hCG (range) IU/L Afwachten: 211 | ||||||
| -1996 | source of funding stated | <4 cm; Fetal cardiac activity nr; Serum hCG | Treatment success: hCG < 5 IU/L | (20-1343) | |||||||||
| <5000 IU/l | Treatment success | MTX: 395 (61- | |||||||||||
| N total at baseline: | Loss-to-follow- up: | 4279) | |||||||||||
| n=60 | Not reported | afwachten: 23/30 MTX: 23/30 | |||||||||||
| Peto OR: 1.00 (0.31, 3.28) | Costs: not reported | ||||||||||||
| Incomplete outcome data: Not reported | |||||||||||||
| Fertility (ectopic): not reported HRQL: not reported | |||||||||||||
| Side effects | |||||||||||||
| geen verschil in bloodcount, lever en nierfunctie na behandeling in beide groepen. | |||||||||||||
| Mello et al. (2013) | RCT, multi | Inclusion criteria: hemodynamically stable women with either an ectopic pregnancy visible on transvaginal sonography (an ectopic ring or an ectopic mass | Expectant management for one week | Single-dose MTX (1 mg/kg i.m.) | Length of follow- up: | Fertility (IUG): not reported | Initial median hCG (SD) IU/L | ||||||
| centre, The Netherlands, non- commercially funded | Treatment success: hCG < 2 IU/L | Afwachten: 708 | |||||||||||
| HRQL: 3 maanden | Treatment success Afwachten: 19/32 Single dose MTX: 31/41 | -376 | |||||||||||
| Peto OR 0.48 (0.18, 1.28) | MTX: 535 (500) | ||||||||||||
| Loss-to-follow- up: | |||||||||||||
| Not reported | HRQL (Mello et al, 2015). | Costs: not reported | |||||||||||
| and/or fluid in the pouch of Douglas) and a plateauing serum hCG concentration < 1,500 IU/L or with a persisting PUL and a plateauing serum hCG concentration < 2,000 IU/L. A | Baseline, 1 week, 4 weken en 12 weken. | ||||||||||||
| plateauing serum hCG was defined as a < 50% hCG increase or decrease between day 0 | Incomplete outcome data: HRQL: 16 of 73 | Treatment effect p- | Time effect p- | Success effect p- | |||||||||
| and day 4. Exclusion criteria: Women with a viable ectopic pregnancy, signs of tubal rupture and/or active intra-abdominal bleeding, and a contraindication for MTX were not eligible. | (22%) incomplete | SF-36 | |||||||||||
| N total at baseline: | Physical- component scale | 0.49 | 0.02 | 0.96 | |||||||||
| n=73 | SF-36 | ||||||||||||
| Mental component scale | 0.71 | 0.001 | 0.54 | ||||||||||
| RSCL | |||||||||||||
| physical symptoms | 0.14 | 0.001 | 0.13 | ||||||||||
| HADS | |||||||||||||
| depression | 0.98 | 0.012 | 0.32 | ||||||||||
| HADS | |||||||||||||
| anxiety | 0.3 | 0.02 | 0.94 | ||||||||||
| Other outcomes: | |||||||||||||
| Side effects systemic MTX | |||||||||||||
| MTX | afwachten | ||||||||||||
| Nausea | 9 | 3 (20) | |||||||||||
| -30 | |||||||||||||
| Vomiting | 5 | 0 | |||||||||||
| -16 | |||||||||||||
| Diarrhoea | 3 | 0 | |||||||||||
| (10 | |||||||||||||
| Bucositis | 2 (7) | 0 | |||||||||||
| Conjunctivitis | 4 | 0 | |||||||||||
| -13 | |||||||||||||
| Photosensitivity | 2 (7) | 0 | |||||||||||
| RR (95% CI) 1.5 (0.5–4.6) | |||||||||||||
| HRQL: not reported | |||||||||||||
| Fertility (ectopic): not reported | |||||||||||||
| Silva et al. | RCT, Single | Inclusion criteria: | Expectant | Single dose MTX | Length of follow- | Fertility (IUG): not reported | Initial median | ||||||
| -2015 | Centre, | confirmed tubal | management | 50 mg/m2 IM | up: | hCG (SD) IU/L | |||||||
| University | pregnancy | (placebo, saline | Treatment | Treatment success | Afwachten: 794 | ||||||||
| hospital, | (visible tubal | injection) | success: hCG < 5 | afwachten: 12/13 | -868 | ||||||||
| Brazil, No | pregnancy on | mIU/mL | MTX: 9/10 | MTX: 883 (729) | |||||||||
| source of | transvaginal | Loss-to-follow- | Peto OR 1.32 (0.08,23.09) | ||||||||||
| funding stated | ultrasound | up: | Costs: not | ||||||||||
| characterized by | Not reported | HRQL: not reported | reported | ||||||||||
| an | |||||||||||||
| inhomogeneous | Incomplete | Fertility (ectopic): not reported | |||||||||||
| adnexal mass or a | outcome data: | ||||||||||||
| tubal ring with or | Not reported | Side effects | |||||||||||
| without a yolk | geen verschil in bloodcount, lever en | ||||||||||||
| sac, a tubal mass | nierfunctie na behandeling in beide | ||||||||||||
| <5.0 cm), fertility | groepen. | ||||||||||||
| desire, an initial | |||||||||||||
| serum hCG | |||||||||||||
| concentration < | |||||||||||||
| 2,000 mIU/mL, | |||||||||||||
| declining titers of | |||||||||||||
| serum hCG 48 h | |||||||||||||
| prior to | |||||||||||||
| treatment, | |||||||||||||
| Exclusion criteria: | |||||||||||||
| were: embryonic | |||||||||||||
| cardiac activity | |||||||||||||
| on transvaginal | |||||||||||||
| ultrasound, signs of tubal rupture, and contraindication for MTX. Pregnancies of unknown location were not included. | |||||||||||||
| N total at baseline: | |||||||||||||
| n=23 | |||||||||||||
| Risk of bias table for intervention studies (randomized controlled trials) PICO 1 | |||||||||
| Study reference | Describe method of randomisation1 | Bias due to inadequate concealmen t of | Bias due to inadequate blinding of | Bias due to inadequate blinding of care providers to treatment allocation?3 | Bias due to inadequate blinding of outcome assessors to treatment allocation?3 | Bias due to selective outcome reporting on basis of the results?4 | Bias due to loss to follow-up?5 | Bias due to violation of intention to treat analysis?6 | Other |
| allocation?2 | participants to treatment allocation?3 | ||||||||
| (first author, publication year) | (unlikely/likely/uncle ar) | (unlikely/likely/un clear) | |||||||
| (unlikely/likely/uncl ear) | (unlikely/likely/un clear) | (unlikely/likely | |||||||
| (unlikely/like ly/unclear) | (unlikely/likely/un clear) | /unclear) | |||||||
| Korhonen et al. | Randomization by table of random numbers | Unlikely. (Allocation adequate by hospital pharmacy) | Unlikely (double | Appearance of placebo tablet not reported. | idem | Unclear. No trial protocol or trial registration | Unclear | Unclear | Power calculation performed |
| -1996 | blind, placebo controlled with placebo tablet) | ||||||||
| Mello et al. (2013) | Randomization by computer | Unlikely | Unclear (not | n.a. | idem | Unlikely | Unlikely | Unlikely (Intention-to- treat analysis) | Power calculation performed |
| blinded, not placebo controlled) | |||||||||
| Silva et al. (2015) | Method of randomization not stated | Unclear | Unlikely (doubled blind, placebo | Colour of | idem | No trial protocol or trial | Unclear | Unclear (Intention-to- | No power calculation. |
| methotrexate is yellow. Similarity of | registration | ||||||||
| controlled with saline injection). | colour of placebo saline injection not reported. | treat principle not reported) | |||||||
| Evidence table for intervention studies: PICO 2 | |||||||||||||
| Study reference | Study characteristics | Patient characteristics 2 | Intervention (I) | Comparison / control (C) 3 | Follow-up | Outcome measures and effect size 4 | Comments | ||||||
| El-Sherbiny et al. (2003) | RCT, Multi centre, Egypt, no source of funding stated | Inclusion criteria: | Single-dose MTX | Laparoscopic salpingotomy | Length of follow- up: | Fertility outcome | Initial hCG mean (SD) IU/L | ||||||
| <4 cm No fetal cardiac activity; Serum hCG <10 | (50 mg/m2 i.m.) | hCCG < 5IU/L | IUG | MTX 2274 (815) | |||||||||
| 000 IU/l | Fertility 1 year | MTX: 8/13 | Salpingotomy 2258 | ||||||||||
| N total at baseline: | Chirurgie: 9/15 | -720 | |||||||||||
| n =55 | Loss-to-follow-up: Not reported | Peto OR: 1.07 [0.23, 4.89] | |||||||||||
| Other outcome: Side- effects | |||||||||||||
| Incomplete outcome data: Not reported | Treatment success single dose; | MTX: n=3 (mild neutropenia or elevated SGOT) Salpingotomy: n=3 (portsite hematoma or infection, subcutaneous emphysema) | |||||||||||
| MTX: 18/26 | |||||||||||||
| chirurgie: 28/32 | Costs: not reported | ||||||||||||
| peto-OR 0.33 (0.09, 1.19) | |||||||||||||
| Treatment success variable dose; MTX 22/26 | |||||||||||||
| Chirurgie: 28/32 | |||||||||||||
| Peto OR: 0.79 [0.18, 3.49] | |||||||||||||
| Fertility outcome | |||||||||||||
| EUG | |||||||||||||
| MTX: 2/13 | |||||||||||||
| Chirurgie: 2/15 | |||||||||||||
| Peto OR: 1.18 (0.15, 9.45) | |||||||||||||
| HRQoL: not reported | |||||||||||||
| Fernandez et al. (1998) | RCT, single centre, university hospital, France, no | Inclusion criteria: EP by | Single-dose MTX | Laparoscopic salpingotomy | Length of follow- up: | Fertility outcome | Initial hCG mean (SD) mIU/ml | ||||||
| TVS/TAS;Pre- | (1 mg/kg i.m.) | hCG < 10mI/ml fertility follow up > | IUG | MTX: 3120 (5280) | |||||||||
| therapeutic score | MTX: 5/9 | Salpingotomy: 2592 | |||||||||||
| Chirurgie: 16/29 | -3269 | ||||||||||||
| Peto OR: 1.02 [0.23, 4.57] | |||||||||||||
| source of funding stated. | <13; | 1 year (not further specified) | |||||||||||
| Exclusion criteria: Size nr; Fetal cardiac activity nr; Upper limit serum hCG nr | Treatment success single dose; | Costs: not reported | |||||||||||
| N total at baseline: | Loss-to-follow-up: Intervention: n=10 of 51 (19.6%) | MTX: 15/22 | |||||||||||
| n =100, | Reasons: unknown | chirurgie: 47/49 | |||||||||||
| peto-OR 0.08 (0.02, 0.38) | |||||||||||||
| Control: n=8 of 49 (16.3%) | |||||||||||||
| Reasons: unknown | Treatment success variable dose; MTX: 18/22 | ||||||||||||
| Chirurgie: 47/49 | |||||||||||||
| Incomplete outcome data: Not reported | Peto OR: 0.17 [0.03, 1.00] | ||||||||||||
| Fertility outcome | |||||||||||||
| EUG | |||||||||||||
| MTX: 0/9 | |||||||||||||
| Chirurgie: 5/29 | |||||||||||||
| peto OR: 0.23 (0.03, 2.04) | |||||||||||||
| HRQoL: not reported | |||||||||||||
| Fernandez et al. (2013) | RCT, multiple centre, France, non- commercially funded. | Inclusion criteria: EP by TVS (mass, sac or fetal pole outside the uterus). | Single dose MTX | Laparoscopic salpingotomy with preventive dose of MTX (1 mg/kg i.m.) within 24 hours postoperativel y | Length of follow- up: | Fertility outcome | Initial hCG not reported | ||||||
| Hemodynamically stable; Fernandez score < 13. n=207 | (1 mg/kg i.m.) | unclear | IUG | ||||||||||
| MTX: 58/87 | Costs: not reported | ||||||||||||
| Loss-to-follow-up: Intervention: n=7 of 110 (6%) | chirurgie: 58/82 | ||||||||||||
| Reasons: not stated | peto OR: 0.83 (0.43, 1.58) | ||||||||||||
| Control: n= 8 of 97 | Treatment success; MTX: 86/110 | ||||||||||||
| -8% | Chirurgie: 87/97 | ||||||||||||
| Reasons: not stated | Peto OR: 0.43 (0.21, 0.91) | ||||||||||||
| Incomplete outcome data: Not reported | Fertility outcome | ||||||||||||
| EUG | |||||||||||||
| MTX 8/110 | |||||||||||||
| chirurgie: 6/97 | |||||||||||||
| peto OR: 1.19 (0.40, 3.51) | |||||||||||||
| HRQoL: not reported | |||||||||||||
| Hajenius et al. | RCT, multi | Inclusion criteria: Laparoscopically confirmed; No fetal cardiac activity; No limit in EP size; No upper limit serum hCG | Multiple dose MTX (1.0 mg/kg im on Days 0, 2, 4, 6; | Laparoscopic salpingotomy | Length of follow- up: | Fertility outcome (Dias Pereira et al., 1999) | Initial hCG median (range IU/L) | ||||||
| -1997 | centre, The Netherlands, non- commercially funded. | N total at baseline: | alternated folinic acid | hCG < 2 IU/L | IUG | MTX: 1950 (110–19 | |||||||
| n=100, | 0.1 mg/kg oral on Days 1, 3, 5, 7) | HRQL: 4 weeks | MTX: 12/34 | 500) | |||||||||
| Fertility: 18 months | Chirurgie: 16/40 | Salpingotomy: 2100 | |||||||||||
| Costs: 4 weeks | Peto OR: 0.82 (0.32, 2.11) | (228–18 400) | |||||||||||
| Loss-to-follow-up: | Treatment success MTX: 42/51 | Costs Mol 1999 | |||||||||||
| · Treatment success: not reported | chirurgie: 35/49 | ||||||||||||
| · HRQL: MTX group: n=9 of 51 (18%). Salpingotomty: n= 12 of 50 (24%). Because of language problems (n=11) or not stated (n=10) | peto OR: 1.84 (0.73, 4.65) | ||||||||||||
| · Fertility: n=10 of 100 (10%), not specified per group. | |||||||||||||
| · Costs: n=30 of 100 (30%) to assess indirect costs, not specified per group. | HRQL (Nieuwkerk et al., 1998a) (mean ± SD) | ||||||||||||
| Incomplete outcome data: Not reported | |||||||||||||
| 2 | ns | ns | Me dic al: 50 | Me dic al: 45 | |||||||||
| wk n | ± 22 | ± 29 | |||||||||||
| Sur gic al: 38 | Sur gic al: 68 | ||||||||||||
| ± 24 | ± 32 | ||||||||||||
| P | P < 0.0 | ||||||||||||
| <0. | 5 | ||||||||||||
| 5 | |||||||||||||
| 4 | Ns | No t rep ort ed | No t rep ort ed | ns | |||||||||
| wk n | |||||||||||||
| 16 | ns | ns | ns | ns | |||||||||
| wk n | |||||||||||||
| Fertility outcome (Dias Pereira et al., 1999) | |||||||||||||
| EUG | |||||||||||||
| MTX 3/34 | |||||||||||||
| Chirurgie: 4/40 | |||||||||||||
| Petor OR 0.87 (0.19, 4.12) | |||||||||||||
| Other outcomes: Side-effects | |||||||||||||
| MTX | Salp ingo | ||||||||||||
| tom y | |||||||||||||
| non e | 20 | 38 | |||||||||||
| (39 | (78 | ||||||||||||
| %) | %) | ||||||||||||
| Nau sea/ vom iting | 13 | 3 | |||||||||||
| (25 | -8% | ||||||||||||
| %) | |||||||||||||
| Diar rho ea | 6 | 1 | |||||||||||
| (12 | -2% | ||||||||||||
| %) | |||||||||||||
| Sto mati tis | 12 | 3 | |||||||||||
| (24 | -6% | ||||||||||||
| %) | |||||||||||||
| Conj unct ivitis | 18 | 3 | |||||||||||
| (35 | -6% | ||||||||||||
| %) | |||||||||||||
| Abd omi nal pain | 19 | 3 | |||||||||||
| (37 | (14 | ||||||||||||
| %) | %) | ||||||||||||
| Cyst itis | 2 | 0 | |||||||||||
| -4% | |||||||||||||
| Oth er maj or com plic atio ns | 2 | 0 | |||||||||||
| -4% | |||||||||||||
| Bon e- mar row | 0 | 0 | |||||||||||
| dep ressi on | |||||||||||||
| Rais ed liver enz yme s | 3 | 0 | |||||||||||
| -6% | |||||||||||||
| Krag | RCT, multi | Inclusion criteria: | Systemic | laparoscopic | Length of follow- | Fertility | Initial median hCG | ||||||
| Moeller | et | centre, | rise in plasma- | single | dose | salpingotomy | up: | IUG | (range) IU/L | ||||
| al. (2009), | Denmark, no | hCG levels by | MTX | 1.0 | Until hCG < 5IU/L | MTX: 38/52 | MTX: 2,259 [176– | ||||||
| source of | three consecutive | mg/kg IM | Fertility: the | Chirurgie: 32/52 | 41,000] | ||||||||
| funding stated | measurements or | median follow-up | Peto O: 1.70 [0.74, 3.89] | Salpingotomy: 3,200 | |||||||||
| with an | period was 8.6 | [72–42,859] | |||||||||||
| extrauterine | years (range | Treatment success single dose; | |||||||||||
| location of a live | 6.9–10.3 years). | MTX 39/53 | Remarks | ||||||||||
| conception with a | Chirurgie: 25/53 | Study was | |||||||||||
| gestational sac < | Loss-to-follow-up: | Peto OR: 2.99 (1.38-6.48) | prematurely ended | ||||||||||
| 3.6 cm were | n (%): 2 (1.9%) not | after 3 years due to | |||||||||||
| eligible. Women | stated which group | Treatment success variable dose; | recruitment | ||||||||||
| with plasma-hCG | and no reason | MTX: 40/53 | problems. Sample | ||||||||||
| < 2,000 IU/L were | given. | Chirurgie: 25/53 | size calculation was | ||||||||||
| eligible for | Peto OR: 3.26 [1.50, 7.10] | 422 women to detect | |||||||||||
| randomization | Incomplete | a 10% difference in | |||||||||||
| only if the rate of | outcome data: | pregnancy rates | |||||||||||
| increase was< | Not reported | Fertility | between the two | ||||||||||
| 20%/24 hours | EUG: | arms. | |||||||||||
| and with no | MTX: 0/52 | ||||||||||||
| ultrasonographic | Chirurgie: 2/52 | In the MTX group: | |||||||||||
| sign of | Peto OR: 0.13 (0.01, 2.15) | n=1 had viable IUP. In | |||||||||||
| intrauterine | the salpingotomy | ||||||||||||
| pregnancy. | HRQoL: not reported | group: n=1 had a | |||||||||||
| viable IUP, n=1 had | |||||||||||||
| N total at baseline: | Other outcome: side effects | no diagnosis (failing PUL). | |||||||||||
| n=106 | Nausea | ||||||||||||
| MTX: n=5 | |||||||||||||
| salpingotomy: n=1 | Costs: not reported. | ||||||||||||
| Other less common side effects | |||||||||||||
| MTX: vomiting, diarrhea, constipation, dizziness, loss of hair, and sleeping problems occurred | |||||||||||||
| Salpingotomy: tooth broken during induction of anesthesia, one bladder perforation, one urinary tract infection, and one esophageal lesion necessitating transfusion. | |||||||||||||
| Saraj et al. (1998) | RCT, Multi centre, USA, No source of funding stated | Inclusion criteria: | Single-dose MTX | Laparoscopic salpingotomy | Length of follow- up: | Fertility outcome | Initial mean hCG (SD) IU/L | ||||||
| <3.5 cm on TVS; No fetal cardiac activity; Upper limit serum hCG nr, | (1 mg/kg i.m.) | Until hCG < 15 mIU/mL | IUG | MTX: 3162 (772) | |||||||||
| N total at baseline: | MTX: 5/18 | salpingotomy: 3357 | |||||||||||
| n=75 | Loss-to-follow-up: Not reported | Chirurgie: 4/14 | -766 | ||||||||||
| Peto OR: 0.96 [0.20, 4.54] | |||||||||||||
| Incomplete outcome data: Not reported | Remarks | ||||||||||||
| Treatment success single dose; MTX: 30/38 | 1 woman had no ectopic pregnancy in the salpingotomy group. | ||||||||||||
| Chirurgie: 33/36 | |||||||||||||
| Peto OR: 0.37 (0.10, 1.32) | |||||||||||||
| Costs: not reported. | |||||||||||||
| Treatment success variable dose; MTX: 36/38 | |||||||||||||
| Chirurgie: 33/36 | |||||||||||||
| Peto OR: 1.62 [0.27, 9.82] | |||||||||||||
| Fertility outcome | |||||||||||||
| EUG | |||||||||||||
| MTX: 0/18 | |||||||||||||
| chirurgie: 0/14 Peto OR: n.e. | |||||||||||||
| HRQoL: not reported | |||||||||||||
| Sowter et | RCT, multi | Inclusion criteria: | Single-dose | Laparoscopic | Length of follow- | Fertility (IUG): not reported | Initial median hCG | ||||||
| al. (2001a) | centre, New | <3.5 cm; No fetal | MTX | salpingotomy | up: | (range) IU/L | |||||||
| Zealand. | cardiac activity; | (50 mg/m2 | Until hCG < 5 IU/L | Treatment success single dose; | MTX: 927 {137 - | ||||||||
| Funded, but | Serum hCG <5000 | i.m.) | MTX: 22/34 | 4866} | |||||||||
| type of | IU/l | Loss-to-follow-up: | chirurgie: 19/28 | Laparoscopy: 775 {89 | |||||||||
| funding not | N total at | Not reported | Peto OR: 0.87 (0.31, 2.48) | - 4800} | |||||||||
| stated | baseline: | ||||||||||||
| n=62 | Incomplete | Treatment success variable dose; | Remarks | ||||||||||
| outcome data: | MTX: 29/34 | Unblocked | |||||||||||
| Not reported | Chirurgie: 19/28 | randomization | |||||||||||
| Peto-OR: 2.67 [0.81, 8.74] | procedure by a | ||||||||||||
| computer program; | |||||||||||||
| HQRL; | Allocation adequate | ||||||||||||
| by sequentially | |||||||||||||
| numbered opaque | |||||||||||||
| envelopes sealed by | |||||||||||||
| a third party; Power | |||||||||||||
| calculation | |||||||||||||
| performed (n=98); | |||||||||||||
| Intention-to-treat | |||||||||||||
| analysis; Multi | |||||||||||||
| centre; Full paper. | |||||||||||||
| Trial prematurely | |||||||||||||
| ended (62/98) | |||||||||||||
| because of fewer | |||||||||||||
| women were eligible | |||||||||||||
| for the trial and | |||||||||||||
| uncertainty of | |||||||||||||
| funding. | |||||||||||||
| Costs (Sowter et al., | |||||||||||||
| 2001b) | |||||||||||||
| D | N S | NS | Laproscopy | ||||||||||
| ag 10 | : 70 [53 to | ||||||||||||
| 95], | |||||||||||||
| methotrexa te: 93 [85 to | |||||||||||||
| 89] p = | |||||||||||||
| 0.006) | |||||||||||||
| D | N S | NS | NS | ||||||||||
| ag 28 | |||||||||||||
| Fertility (ectopic): not reported | |||||||||||||
| Risk of bias table for intervention studies (randomized controlled trials) PICO 2 | |||||||||
| Study reference | Describe method of randomisation1 | Bias due to inadequate concealment of allocation?2 | Bias due to inadequate blinding of | Bias due to inadequate blinding of care providers to treatment allocation?3 | Bias due to inadequate blinding of outcome assessors to treatment allocation?3 | Bias due to selective outcome reporting on basis of the results?4 | Bias due to loss to follow-up?5 | Bias due to violation of intention to treat analysis?6 | Other |
| participants to treatment allocation?3 | |||||||||
| (first author, publication year) | (unlikely/likely/ unclear) | (unlikely/likely/ unclear) | |||||||
| (unlikely/likely/ unclear) | (unlikely/likely/ unclear) | (unlikely/like ly/ | |||||||
| unclear) | |||||||||
| (unlikely/likely/uncl ear) | (unlikely/likely/ unclear) | ||||||||
| Fernandez 1998 | Randomization with a random number table | Unclear | Unclear | Unlikely | Unclear | Unlikely | Unlikely | Unclear | No power calculation |
| El Shirbiny 2003 | Not reported | Unclear | Unclear | Unclear | Unclear | Unlikely | Unlikely | Unclear | |
| Krag Moeler 2009 | Individual randomization in block of 6-8 attached was | Unlikely | Unlikely | Unlikely | Unclear | Unlikely | Unlikely | Unclear | Study was prematurely ended after 3 years due to recruitment problems. |
| executed by | Sample size calculation was 422 | ||||||||
| phoning a computer program. | women to detect a 10% difference in pregnancy rates between the two arms. | ||||||||
| Saraj 1998 | Randomization was done through use of | Unlikely | Unlikely | Unclear | Unclear | Unlikely | Unlikely | Unclear | |
| sealed enveloppes. | |||||||||
| Sowter 2001 | Unblocked randomization procedure by a computer program; Allocation adequate by sequentially numbered opaque envelopes sealed by a third party | Unlikely | Trial prematurely ended (62/98) because of fewer women were eligible for the trial and uncertainty of funding | ||||||
Beoordelingsdatum en geldigheid
Publicatiedatum : 05-04-2017
Beoordeeld op geldigheid : 01-12-2016
Deze richtlijn dient te worden herzien binnen een termijn van maximaal 5 jaar na publicatie in het NTOG en op de website van de NVOG en op de Richtlijnendatabase (www.richtlijnendatabase.nl).
Verder moet herziening overwogen worden wanneer nieuwe wetenschappelijk verantwoord vastgestelde inzichten belangrijke wijzigingen in de gegeven aanbevelingen en conclusies van deze richtlijn noodzakelijk maken. Daarnaast is het van belang de belangrijke andere bestaande richtlijnen te volgen en bij herziening van de inhoud daarvan herziening van deze richtlijn te overwegen. Tenslotte dient herziening ook overwogen te worden wanneer op de geformuleerde kennishiaten een afdoend wetenschappelijk verantwoord antwoord is gegeven.
De NVOG is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De NVOG is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Doel en doelgroep
Doel van de richtlijn
Een vrouw met een extra-uteriene graviditeit (EUG) kan zich presenteren zonder of met klachten. Klassieke klachten zijn buikpijn en/of bloedverlies bij een positieve zwangerschapstest. De echoscopische bevindingen kunnen daarbij direct bevestigend zijn voor de diagnose waarbij een zwangerschapsweefsel wel of niet intra/extra-uterien wordt gezien. Een minderheid van deze patiënten zal een EUG hebben. In deze situatie van Zwangerschap met Onbekende Lokalisatie (ZOL; pregnancy with unknown location (PUL)) is het van belang om de diagnose EUG of vroege vitale of niet vitale intra-uteriene zwangerschap accuraat en in een vroeg stadium rond te krijgen. Het serum- hCG in combinatie met een transvaginale echoscopie speelt hierbij een grote rol.
Er zijn verschillende behandelingsopties voor een EUG: een afwachtend beleid (monitoren), een niet- invasieve methotrexaat (MTX) behandeling of een operatieve behandeling. Geprobeerd moet worden de meest effectieve behandeling te kiezen die aansluit bij een (eventueel toekomstige) kinderwens. In deze richtlijn wordt besproken hoe de diagnose EUG te stellen en worden aanbevelingen gedaan ten aanzien van de behandelingsmogelijkheden. Deze richtlijn moet ertoe bijdragen dat elke hulpverlener die een patiënte met een mogelijke ZOL/EUG ziet deze zo effectief en veilig mogelijk kan onderzoeken en behandelen, dan wel verwijzen (zie multidisciplinaire richtlijn “Diagnostiek acute buikpijn bij volwassenen”). Hierdoor kan zwangerschap gerelateerde morbiditeit en mortaliteit worden gereduceerd (Van Mello, 2012).
De NVOG richtlijn “Tubaire EUG, diagnostiek en behandeling” werd in 2001 goedgekeurd. Inmiddels zijn er relevante studies verricht op het gebied van diagnostiek en de niet-invasieve en chirurgische interventies die patiënten met een EUG mogelijk een betere behandeling kunnen bieden.
Beoogde gebruikers van de richtlijn
Deze richtlijn is primair geschreven voor gynaecologen maar kan gebruikt worden door andere beroepsgroepen die betrokken zijn bij de zorg voor patiënten met een zwangerschap en ZOL/EUG, zoals huisartsen, verloskundigen, SEH-artsen (en andere specialisten die betrokken zijn bij een acute buik), echoscopisten en abortusartsen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2013 een Monodisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van de NVOG. De werkgroepleden zijn door de NVOG gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Namens de NVOG
Dr. M.H. van der Gaast, gynaecoloog, Havenziekenhuis, Rotterdam (voorzitter) Dr. W.M. Ankum, gynaecoloog, AMC, Amsterdam
Dr. S.F.P.J. Coppus, gynaecoloog, Radboudumc, Nijmegen Dr. F. Mol, gynaecoloog, AMC, Amsterdam
Dr. A. J.C.M. van Dongen, gynaecoloog, Radboudumc, Nijmegen Dr. N. M. van Mello, gynaecoloog, Radboudumc, Nijmegen
Dr. I. A.J. van Rooij, gynaecoloog, ETZ, Tilburg
Dr. S. J. Tanahatoe, gynaecoloog, UMCU, Utrecht
Drs. H. Visser, gynaecoloog, Ter-Gooi Ziekenhuis, Hilversum
Methodologische begeleiding van de werkgroep
Mw. A. Rozeboom MSc, junior adviseur Kennisinstituut van Medisch Specialisten te Utrecht Drs. E.M.E. den Breejen, senior adviseur, Kennisinstituut van Medisch Specialisten te Utrecht Dr. M.A. Pols, senior adviseur, Kennisinstituut van Medisch Specialisten te Utrecht
Belangenverklaringen
De “KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling” is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met evt. belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroep-lid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie- management |
Extern gefinancierd onderzoek |
Kennis-valorisatie |
Overige belangen |
Getekend |
|
Van der Gaast |
Voorzitter, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Ankum |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Coppus |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Mol |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Van Dongen |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Van Mello |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Van Rooij |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Tanahatoe |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Visser |
Lid, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Rozeboom |
Junior adviseur Kennisinstituut van Medisch Specialisten |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Den Breejen |
Adviseur Kennis- instituut van Medisch Specialisten |
Promovendus, Radboudumc, Nijmegen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
|
Pols |
Senior adviseur Kennisinstituut van Medisch Specialisten |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Ja |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het vragen van input op het raamwerk van de richtlijn en de daaruit voortvloeiende belangrijkste knelpunten zijn verwerkt in de richtlijn. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. Daarnaast werden indicatoren ontwikkeld om de implementatie van de richtlijn in de praktijk te bevorderen. Deze zijn ook te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreetrust.org), een internationaal breed geaccepteerd instrument, en op de ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (www.zorginstituutnederland.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door vertegenwoordigers namens de NVOG, NHG, NPCF, KNOV, IGZ en ZN via een enquête. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen:(AHRQ, NICE, CBO, SUMsearch en SIGN) en naar systematische reviews in de Cochrane Library en via SUMsearch. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld op basis van op voorhand opgestelde methodologische kwaliteitscriteria om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
|
|
|
Zeer laag |
|
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE- methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende of bijkomende aspecten van de organisatie van zorg worden behandeld in de module 'Organisatie van zorg bij EUG en ZOL'.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek staat in de Kennislacunes (zie aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd of geaccordeerd.
Literatuur
Bouyer J, Coste J, Fernandez H, Pouly JL, Job-Spira N. Sites of ectopic pregnancy: a 10 year population-based study of 1800 cases. Hum Reprod. 2002 Dec;17(12):3224-30.
Farmacotherapeutisch Kompas. https://www.farmacotherapeutischkompas.nl/
Jauniaux E, Farquharson RG, Christiansen OB, Exalto N. Evidence-based guidelines for the investigation and medical treatment of recurrent miscarriage. Hum Reprod. 2006;21:2216-22.
Jurkovic D, Mavrelos D. Catch me if you scan: ultrasound diagnosis of ectopic pregnancy. Ultrasound Obstet Gynecol 2007; 30: 1–7.
Kirk E, Bottomley C, Bourne T. Diagnosing ectopic pregnancy and current concepts in the management of pregnancy of unknown location. Hum Reprod. Update 2014 20 (2): 250 – 61.
RCOG Green-top Guideline No 21. Diagnosis and Management of Ectopic Pregnancy. July 2015.
Schutte JM, Steegers EA, Schuitemaker NW, Santema JG, de Boer K, Pel M, Vermeulen G, Visser W, van Roosmalen J. Netherlands Maternal Mortality Committee. Rise in maternal mortality in the Netherlands. BJOG. 2010 Mar;117(4):399-406.
Van Mello NM, Zietse CS, Mol F, Zwart JJ, van Roosmalen J, Bloemenkamp KW, Ankum WM, van der Veen F, Mol BW, Hajenius PJ. Severe maternal morbidity in ectopic pregnancy is not associated with maternal factors but may be associated with quality of care. Fertil Steril. 2012 Mar;97(3):623-9.
Van Oppenraaij RHF, Goddijn M, Lok CAR Exalto N. Ned Tijdschr Geneeskd. 2008;152:20-4.
Wilkinson H; Trustees and Medical Advisers. Saving mothers' lives. Reviewing maternal deaths to make motherhood safer: 2006-2008. BJOG. 2011 Oct;118(11):1402-3; 1403-4.
Zoekverantwoording
|
Uitgangsvraag: Welke plaats heeft een afwachtend of medicamenteus beleid (MTX) versus chirurgisch beleid in de behandeling van de EUG? |
|
|
Database(s): Medline |
Datum: 30-12-2014 |
|
Periode: 2011-heden |
Talen: geen beperking |
|
Database |
Zoektermen Aansluitend op Cochrane |
Totaal |
|
Medline (OVID) 2011- heden Engels
Embase (Elsevier) |
Keywords CONTAINS "ectopic pregnancies"or "ectopic pregnancy"or"ectopic rate"or"tubal pregnancy" or Title CONTAINS "ectopic pregnancies"or "ectopic pregnancy"or"ectopic rate"or"tubal pregnancy"
CINAHL search strategy for PH281 22.07.15
'ectopic pregnancy'/exp OR (pregnanc*:ti AND ((unknown OR uncertain OR undetermined) NEAR/3 (loca* OR site* OR origin)):ti) OR (pregnanc*:ab AND ((unknown OR uncertain OR undetermined) NEAR/3 (loca* OR site* OR origin)):ab) OR ((pathologic* OR ectopic OR tubal OR ovarian OR abdominal) NEAR/6 (pregnan* OR gestation*)):ab,ti AND ('uterine tube surgery'/exp OR 'tubectomy'/exp OR 'tubostomy'/exp OR ((fallopian OR salpinx OR tub* OR oviduct*) NEAR/3 surg*):ab,ti OR tubectom*:ab,ti OR tubectom*:ab,ti OR (radical NEAR/3 surg$):ab,ti OR tubotom*:ab,ti OR tubotom*:ab,ti OR tubostom*:ab,ti OR tubostom*:ab,ti OR (conserv* NEAR/3 surg*):ab,ti) AND [english]/lim AND [embase]/lim AND [2011-2015]/py
AND 'meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp)) (24) – 16 uniek
AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it (33) - 29 uniek |
87 |
