Minimal aortic injury
Uitgangsvraag
Wat is de plaats van conservatief beleid ten opzichte van een endovasculaire stentplaatsing bij patiënten met minimaal letsel aan de aorta?
Aanbeveling
Kies voor een conservatief beleid met follow-up door middel van beeldvorming bij minimale letsels aan de thoracale aorta na trauma (SVS Grade I & II) zonder hoog-risico kenmerken op de CT.
Overweeg een aorta-interventie middels TEVAR bij minimale letsels aan de thoracale aorta na trauma met hoog-risico kenmerken op CT.
Voer beeldvormende follow-up uit met voldoende resolutie bij voorkeur door middel van een CT-scan (of MRI) met de volgende frequentie (tot aan volledige herstel van het aortaletsel):
- Vroege scan binnen twee weken;
- Na zes maanden;
- Jaarlijkse scans bij persisterende afwijkingen (tenzij resolutie van letsel).
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In totaal werden er vier studies beschreven die een conservatieve of niet-operatieve behandeling vergeleken met een endovasculaire aorta-interventie middels TEVAR. Vanwege het observationele studie design van alle geïncludeerde studies werd de bewijskracht voor alle gerapporteerde uitkomstmaten beoordeeld als zeer laag.
Traditioneel worden letsels van de thoracale aorta na trauma gestratificeerd volgens de classificatie gebruikt door de Society of Vascular Surgery (SVS) in de richtlijn uit 2011 (Lee, 2011) over dit onderwerp. Deze letsels worden onderverdeeld in “intimal tear” (grade I), “intramural hematoma” (grade II), “pseudoaneurysm” (grade III) en “aortic rupture” (grade IV) (Lee, 2011; Mazzolai, 2024; Isselbacher, 2022). Oorspronkelijk werden alleen SVS grade I aortaletsels als MAI gestratificeerd, waarvoor altijd een conservatief beleid werd geadviseerd (Lee, 2011; Isselbacher, 2022). Conservatief beleid wordt echter wisselend gedefinieerd in de verschillende studies, maar bestaat in ieder geval altijd uit een vorm een bloeddrukregulatie (dikwijls door middel van intraveneuze betablokkade danwel vasodilatoren)(Isselbacher, 2022). Bijvoorbeeld met een streef mean arterial pressure <80mmHg (Mazzolai, 2024). Voor alle overige traumatische aortaletsels (SVS grade II-IV) werd traditioneel een interventie geadviseerd, met voorkeur voor een endovasculaire behandeling (TEVAR) boven een open chirurgische behandeling (Lee, 2011; Mazzolai, 2024). Sindsdien is er echter voor SVS grade II aortaletsels toenemende literatuur welke onderbouwt dat een conservatief beleid net zo veilig is als bij SVS grade I letsels. Een meta-analyse uit 2024 met data over 204 patiënten met SVS grade II letsels toonde een lage aorta-gerelateerde mortaliteit van 2.9% na conservatief beleid (de Freitas, 2024). Hierbij moet zeker ook worden meegewogen dat een TEVAR gepaard gaat met een relevante kans op complicaties. Systematische overzichten over TEVAR tonen zowel risico’s op korte termijn (zoals 2-10% kans op paraplegie (Awad, 2016)) alsook lange termijn risico’s op endoleak en reinterventies (Karaolanis, 2024).
In het huidige literatuuronderzoek werden vergelijkbare uitkomsten gevonden voor patiënten met een SVS grade II aortaletsel na conservatief beleid danwel na TEVAR wat betreft de cruciale uitkomsten aorta-gerelateerde mortaliteit en progressie van het aortaletsel bij controle beeldvorming, alsook wat betreft de belangrijke uitkomstmaten complicaties en ligduur in het ziekenhuis. Hoewel geen onderdeel van de statistische analyses binnen dit literatuuronderzoek, lijken de uitkomsten tussen patiënten met een SVS grade I en grade II letsels vergelijkbaar. Bijvoorbeeld een systematisch overzicht met 2897 patiënten uit 35 studies van Soong (2019) toonde dat SVS grade II letsels gerelateerd is met een vergelijkbare aorta-gerelateerde mortaliteit als SVS grade I letsels (<1%).
Vanwege de vergelijkbare uitkomsten tussen SVS grade I en grade II aortaletsels na conservatieve behandeling, suggereren recentere studies dat het klassieke SVS 4-categorieënsysteem kan worden vereenvoudigd naar een 3- of zelfs een 2-categorieënsysteem (Lamarche, 2012; Heneghan, 2016). Het 2-categorieënsysteem stratificeert traumatische aortaletsels in MAI danwel significante/ernstige aortaletsels (Kapoor, 2020). MAI wordt dan gedefinieerd als een “subcentimeter intima-media afwijking zonder externe contour veranderingen van de aorta” (Kapoor, 2020). Hier vallen SVS grade I aortaletsels (intimascheur) alsook potentieel SVS grade II letsels (intramuraal hematoom) onder. Ook letsels met een intraluminaal trombus vallen in deze laaggradige categorie. Onder significant of ernstig letsel vallen de overige letsels: intramurale hematomen met contour veranderingen, pseudoaneurysmata, en aortarupturen of transecties (Lamarche, 2012; Heneghan, 2016). In een recente Amerikaanse richtlijn van de American College of Cardiology / American Heart Association (ACC/AHA) over verscheidene aorta-aandoeningen (Isselbacher, 2022). wordt melding gemaakt van enkele hoog-risico kenmerken van aorta-letsels welke op beeldvorming kan worden vastgesteld, maar niet zijn opgenomen in de eerdergenoemde classificaties. Hierdoor kan een interventie voor laaggradige MAI letsels alsnog worden overwogen. In de literatuur genoemde hoog-risico kenmerken van traumatisch aortaletsels zijn: mediastinaal hematoom van meer dan tien millimeter of massawerking door dit mediastinaal hematoom, een ratio van meer dan 1.4 van de grootte van het aortaletsel in relatie tot de normale aortadiameter, pseudocoarctatie van de aorta, betrokkenheid van de aorta ascendens of aortaboog, en/of de aanwezigheid van een grote hematothorax links (Isselbacher, 2022) (zie onderstaande tabel).
|
Posterior mediastinal hematoma > 10 mm |
|
Lesion to normal aortic diameter ratio > 1.4 |
|
Mediastinal hematoma causing mass effect |
|
Pseudocoarctation of the aorta |
|
Large left hemothorax |
|
Ascending aortic, aortic arch, or great vessel involvement |
|
Aortic arch hematoma |
Bron: Isselbacher (2022)
Het voordeel van de nieuwere classificatiesystemen, zoals het 2-categorieënsysteem, is meer eenvoudig, en meer directe correlatie met een behandeladvies (wel of niet conservatief). Daarentegen is het zwaarwegende voordeel van de SVS-classificatie dat het wordt gebruikt in alle studies over dit onderwerp. De werkgroep heeft daarom besloten om deze SVS-classificatie te blijven gebruiken voor deze richtlijn. Daarentegen adviseert de werkgroep dat het waarschijnlijk wel zinvol is om een versimpeld categorieënsysteem te hanteren voor de klinische praktijk. Een indeling op basis van CT in MAI en significant aortaletsel zal wellicht de interbeoordelaars variatie ten goede komen. Het radiologisch verslag dient hiertoe melding te maken van de aan- of afwezigheid van de factoren die deze classificatie bepalen: dus de aanwezigheid, locatie, en grootte van zowel intimo-media afwijkingen, intramuraal hematoom, intraluminaal trombus, contourveranderingen, pseudoaneurysmata, ruptuur, transectie, mediastinaal hematoom en hematothorax. Op basis hiervan kan worden bepaald in welke classificatie het aortaletsel valt en of er aanvullende hoog-risico kenmerken zijn (ACC/AHA guidelines, 2022 - tabel). Daarnaast dient de leeftijd, comorbiditeit, hemodynamische en metabole toestand, de mate van geassocieerd overig letsel, de mogelijkheid om de patiënt te vervolgen in de overweging voor conservatieve beleid danwel operatieve behandeling meegewogen te worden.
Bovenstaande nuances meewegende, is de werkgroep van mening dat bij patiënten met een minimaal letsel aan de aorta na thoraxtrauma, conform de eerdergenoemde definitie van MAI (een “subcentimeter intima-media afwijking zonder externe contour veranderingen van de aorta”), een conservatief beleid kan worden geadviseerd. Bij patiënten met een MAI met hoog-risico kenmerken (ACC/AHA guidelines, 2022– tabel) kan een interventie nog steeds worden overwogen, waarbij traditioneel een voorkeur wordt gegeven voor een endovasculaire interventie (TEVAR) boven een open chirurgische behandeling.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Voor patiënten is het belangrijk om de voor hen meest passende behandeling te krijgen. Dit kan afwachten zijn indien de voordelen van een conservatief beleid voor de patiënt opwegen tegenover de nadelen. De beslissing voor een afwachtend beleid moet goed overwogen worden met afweging van voor- en nadelen. Om latere negatieve gevolgen voor de patiënt te voorkomen, is het belangrijk dat wordt afgestemd met een level 1 traumacentrum.
Kosten (middelenbeslag)
Een endovasculaire interventie is duur (met name de kosten van een prothese) en geeft kans op zowel korte alsook lange termijn complicaties. Complicaties op zeer lange termijn (> 30 jaar) zijn nog onbekend. Een stent geeft artefacten op CT en MRI. Patiënten met TEVAR krijgen langdurigere follow-up (vaak levenslang) vergeleken met patiënten met conservatieve behandeling. Dit alles maakt de zorg duurder en minder duurzaam dan conservatieve therapie.
Aanvaardbaarheid, haalbaarheid en implementatie
De AHA/ACC richtlijn beveelt aan dat patiënten met aortaletsel in een level 1 traumacentrum behandeld worden (ACC/AHA guidelines, 2022). Voor de Nederlandse situatie is de werkgroep van mening dat de beslissing voor conservatieve behandeling multidisciplinair genomen dient te worden, bij voorkeur in, of in overleg met een level 1 traumacentrum. Het advies van de werkgroep is om afspraken te maken binnen het regionale netwerk acute zorg ten aanzien van overleg, beelduitwisseling en indien nodig overplaatsing met als doel om de patiënt op de juiste plek te behandelen. Een ECG getriggerde CT-scan is in principe niet nodig maar kan eventueel gebruikt worden bij twijfel over de aanwezigheid of het type aorta letsel, of voor follow-up (ESER-guideline, 2021).
Gezien de aanbeveling van de werkgroep om MAI te classificeren volgens aangepaste criteria (tabel), is het voor een geslaagde implementatie van belang dat radiologen hiervan op de hoogte worden gebracht. Momenteel worden de criteria niet standaard gerapporteerd bij de verslaglegging van de beeldvorming. Om de interbeoordelaarsbetrouwbaarheid variatie te verkleinen kan het zijn dat bij- en nascholing hiervoor nodig zal zijn.
Indien er sprake is van een indicatie voor een TEVAR bij patiënten met MAI na thoraxtrauma, is de locatie waar dit wordt uitgevoerd afhankelijk van de beschikbare lokale expertise alsook de regionale afspraken binnen bestaande netwerken en samenwerkingsverbanden. Hiervoor verwijzen wij naar de voorwaarden en normeringen zoals bijvoorbeeld beschreven in het Aortadocument (versie 2021) van de Nederlandse Vereniging voor Vaatchirurgie (Aortachirurgie in Nederland).
Follow-up na conservatief beleid
Follow-up beeldvorming op CT bij conservatieve behandeling lijkt niet altijd noodzakelijk. Er zijn artikelen die beschrijven dat follow-up beeldvorming bij SVS Grade I aortaletsels niet zinvol is omdat nagenoeg alle patiënten bij follow-up een stabiel beeld danwel volledige resolutie van het letsel laten zien (Gharai, 2022; Jinadasa, 2022), met een kans op een late interventie van minder dan één procent (Jacob-Brassard 2019). Bij alle andere typen aortaletsels die conservatief behandeld worden, lijkt follow-up CT gerechtvaardigd. Bij progressie, zoals groei van intimamedia afwijkingen, het ontstaan van trombi, of snelle groei van de contour van de aorta op vervolgonderzoek, valt een endovasculaire behandeling alsnog te overwegen (Lozano, 2023). De bestaande richtlijnen (SVS guidelines, 2011; ESC guidelines 2014; ACC/AHA guidelines, 2022) maken bovenstaande onderscheid echter niet, en adviseren altijd follow-up beeldvorming bij een conservatief beleid. De werkgroep heeft besloten om deze aanbevelingen op te volgen, in ieder geval tot resolutie van het aortaletsel op CT, met de kanttekening dat de waarde beperkt zal zijn bij patiënten met een SVS grade I aortaletsel.
Voor het interval en de frequentie van een follow-up CT-scan zijn er geen harde aanbevelingen in de literatuur te vinden. De eerdere genoemde Amerikaanse guidelines adviseren CT follow-up op twee weken, zes maanden en twaalf maanden na de diagnose (ACC/AHA guidelines, 2022).
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Een conservatieve behandeling van MAI leidt bij patiënten tot vergelijkbare uitkomsten op korte termijn wat betreft aorta-gerelateerde mortaliteit, complicaties en ziekenhuisopname. Daarbij is er een zeer lage kans op progressie van het aortaletsel bij follow-up. Verder is een behandeling met TEVAR ook geassocieerd met relevante korte- en lange termijn complicaties, en uiteraard verhoogde kosten.
De werkgroep is daarom van mening dat een conservatief beleid met adequate follow-up kan worden aanbevolen.
Onderbouwing
Letsels van de thoracale aorta na trauma zijn in vele gevallen prehospitaal lethaal. De behandeling van patiënten met deze letsels die wel het ziekenhuis halen, is met name afhankelijk van de uitgebreidheid en ernst van het aortaletsel. Voor ernstige aortaletsels, welke buiten het domein vallen van deze specifieke module, wordt interventie geadviseerd. Hierbij geniet een endovasculaire behandeling (middels thoracic endovascular aortic repair (TEVAR)) de voorkeur boven een open chirurgische behandeling (Lee, 2011; Mazzolai, 2024; Isselbacher, 2022). Voor minimaal aortaletsel (“minimal aortic injury”, MAI) wordt van oudsher een conservatief beleid geadviseerd (in de literatuur veelal aangeduid als “niet-operatieve behandeling”), waarbij bloeddrukregulatie en follow-up centraal staan (Lee, 2011; Mazzolai, 2024; Isselbacher, 2022). Er is echter discussie welke typen aortaletsels in deze conservatieve behandelcategorie kunnen vallen. Daarnaast is de vraag hoe de exacte follow-up van dit type letsel moet plaatsvinden (hoe vaak en welke controlerende beeldvorming). Dit zorgt voor grote praktijkvariatie met als risico over- of onderbehandeling en derhalve mogelijk verhoogd risico voor de patiënt.
Aortic-related mortality (critical)
|
Very low GRADE |
The level of evidence is very uncertain about the effect of observation and follow-up (blood pressure regulation) on aortic-related mortality rates when compared with endovascular repair in patients with minimal aortic injuries.
Sources: DuBose, 2015; DuBose, 2021; Spencer, 2018 |
Progression of minimal aortic injury on a control scan (critical)
|
No GRADE |
It was not possible to formulate a GRADE-conclusion on progression of minimal aortic injury on a control scan due to a lack of comparative data between the two treatment groups.
Source: Spencer, 2018 |
Complications (important)
|
Very low GRADE |
The level of evidence is very uncertain about the effect of observation and follow-up (blood pressure regulation) on complications when compared with endovascular repair in patients with minimal aortic injuries.
Sources: DuBose, 2015; DuBose, 2021; Spencer, 2018 |
Hospital length of stay (important)
|
Very low GRADE |
The evidence is very uncertain about the effect of observation and follow-up (blood pressure regulation) on the length of stay in the hospital when compared with endovascular repair in patients with minimal aortic injuries.
Sources: DuBose, 2015; DuBose, 2021; Sandhu, 2018; Spencer, 2018 |
Description of studies
The retrospective study of DuBose (2021) compared the effect of thoracic endovascular aortic repair (TEVAR) with non-operative management, described as medical management, in patients with blunt thoracic aortic injury (BTAI). Minimal aortic injury was defined as SVS Grade I & II injury types. DeBose (2021) divided the included patients in two groups. The method of thoracic endovascular aortic repair and the non-operative management intervention were not described in detail. In total, 119 patients were included. Forty-eight patients received TEVAR. Seventy-one patients received non-operative management. Length of follow-up was not reported. The reported outcomes in DuBose (2021) were aortic-related mortality, complications, and length of hospital stay.
The retrospective observational study of DuBose (2015) investigated the effect of thoracic endovascular aortic repair (TEVAR) with non-operative management in patients with blunt thoracic aortic injury (BTAI). Minimal aortic injury was defined according to the SVS grade. In total, 91 patients underwent non-operative management, compared to 61 patients who underwent TEVAR. Length of follow-up was not reported. The reported outcomes in DuBose (2015) were aortic-related mortality, complications, and hospital length of stay.
The observational study of Sandhu (2018) investigated the effect of thoracic endovascular aortic repair (TEVAR) with non-operative management in patients with Grade I and II blunt thoracic aortic injury (BTAI). Minimal aortic injury was defined according to the SVS grade. In total, 22 patients with Grade I or II BTAI underwent non-operative management, compared to 23 patients who underwent TEVAR. The length of follow-up was not reported. The reported outcome in Sandhu (2018) was hospital length of stay.
The retrospective cohort study of Spencer (2018) compared the effect of thoracic endovascular aortic repair (TEVAR) with non-operative management in patients with blunt traumatic aortic injury (BTAI). Severity of blunt traumatic aortic injury was classified according to the Society for Vascular Surgery (SVS) classification system (Lee, 2011). Spencer (2018) included the records of patients with SVS grade I to IV BTAIs who were divided into two groups. Minimal aortic injuries were defined as SVS grade I and II injuries. The method or repair was determined based on the patient’s hemodynamic status, associated injuries, and aortic anatomy in a joint effect by the interventional radiologist and vascular surgery team. Non-operative management consisted of short-acting intravenous beta-blocker infusion titrated to maintain systolic blood pressure less than 140 mmHg and heart rate less than 80 beats per minute. Additional agents such as calcium channel blockers or vasodilator were added as needed. In total, 30 patients were included. Fourteen patients received TEVAR, while the remaining sixteen patients underwent non-operative management. Length of follow-up was not reported. The reported outcomes in Spencer (2018) were mortality, complications, and length of hospital stay.
Results
Aortic-related mortality (critical)
Aortic-related mortality was reported in three studies (DuBose, 2021; DuBose, 2015; Spencer, 2018). The results were pooled in a meta-analysis. The pooled mortality rate in the non-operative management group was 0/178 (0%), compared to 4/123 (3.3%) in the TEVAR group. This resulted in a pooled risk difference of -0.03 (95% CI -0.07 to 0.01), in favor of non-operative management (see figure 1). This difference was not considered clinically relevant.
Figure 1. Forest plot showing the comparison between non-operative management and TEVAR for aortic-related mortality in patients with minimal aortic injuries
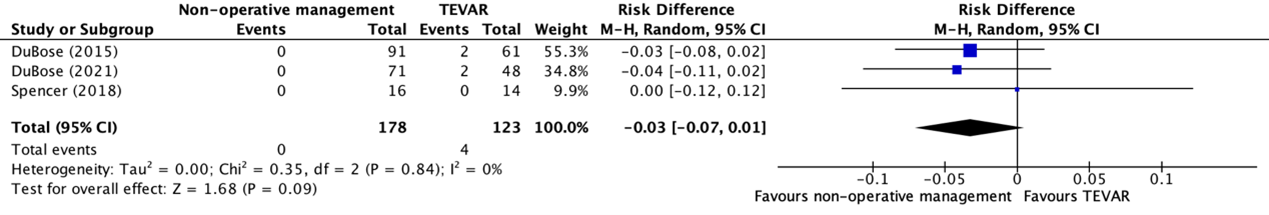
Pooled risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; statistical heterogeneity
Progression of minimal aortic injury on a control scan (critical)
Progression of minimal aortic injury was reported in one study (Spencer, 2018). Spencer (2018) reported resolution of injury, no change in injury, progression of injury, and stable stent with no leak. The results were presented in table 1.
Table 1. Progression of minimal aortic injury
|
Category |
TEVAR |
Non-operative management |
|
Resolution of injury |
Not applicable |
3/16 (18.8%) |
|
No change in injury |
Not applicable |
11/16 (68.8%) |
|
Progression of injury |
Not applicable |
2/16 (12.5%) |
|
Stable stent with no leak |
14/14 (100%) |
Not applicable |
Complications (important)
Complications* were reported in three studies (DuBose, 2021; DuBose, 2015; Spencer, 2018). The results were pooled in a meta-analysis. The pooled complication rate in the non-operative management group was 116/178 (65.2%), compared to 79/123 (64.2%) in the TEVAR group. This resulted in a pooled relative risk ratio (RR) of 0.98 (95% CI 0.81 to 1.18), in favor of non-operative management (see figure 2).
Figure 2. Forest plot showing the comparison between non-operative management and TEVAR for complications in patients with minimal aortic injuries
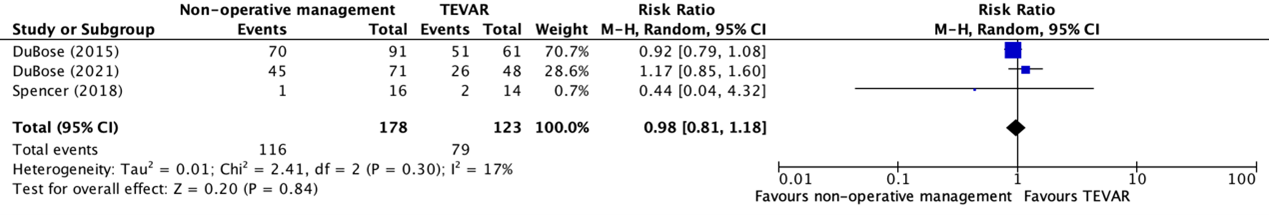
Pooled risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; statistical heterogeneity
*Table 2. Overview of type of complications per included study
|
Author |
Type of complication non-operative management group (N) |
Type of complication TEVAR group (N) |
|
DuBose (2021) |
Delayed stroke – ischemic (N = 1)
Acute renal failure (N = 5)
Pulmonary embolism (N = 3)
Mechanical ventilation > 48 hours (N = 22)
Ventilator -associated pneumonia (N = 5)
Acute lung injury/acute respiratory distress syndrome (N = 2)
Sepsis (N = 7)
|
Delayed stroke – ischemic (N = 1)
Acute renal failure (N = 2)
Pulmonary embolism (N = 3)
Mechanical ventilation > 48 hours (N = 10)
Ventilator -associated pneumonia (N = 4)
Acute lung injury/acute respiratory distress syndrome (N = 3)
Sepsis (N = 3)
|
|
DuBose (2015) |
Stroke (N = 4)
Acute renal failure (N = 8)
Deep venous thrombosis (N = 4)
Pulmonary embolism (N = 4)
Catheter-related urinary tract infection (N = 6)
Blood stream infection (N = 12)
Hospital-acquired pneumonia (N = 4)
Ventilator-associated pneumonia (N = 8)
Acute lung injury/adult respiratory distress syndrome (N = 11)
Sepsis (N = 9)
|
Paralysis (N = 1)
Stroke (N = 1)
Acute renal failure (N = 3)
Deep venous thrombosis (N = 6)
Pulmonary embolism (N = 6)
Catheter-related urinary tract infection (N = 5)
Blood stream infection (N = 6)
Hospital-acquired pneumonia (N = 5)
Ventilator-associated pneumonia (N = 7)
Acute lung injury/adult respiratory distress syndrome (N = 9)
Sepsis (N = 11)
|
|
Spencer (2018) |
Pulmonary embolism (N = 1)
Myocardial infarction (N = 1) |
Atrial fibrillation (N = 1)
Collapsed stent (N = 1) |
Hospital length of stay (important)
Hospital length of stay was reported in four studies (DuBose, 2021; DuBose, 2015; Sandhu, 2018; Spencer, 2018). All studies reported the median (IQR) length of hospital stay in days. The results could not be pooled in a meta-analysis and were therefore described separately.
The median (IQR) length of hospital stay in the study of DuBose (2021) in the non-operative management group (n=71) was 13 (IQR 12) days, compared to 11 (IQR 16) days in the TEVAR group (n=45). This was considered as a clinically relevant difference in favor of TEVAR.
The median (IQR) length of hospital stay in the study of DuBose (2015) in the non-operative management group (n=91) was 12 (IQR 12) days, compared to 16 (IQR 22) days in the TEVAR group (n=61). This was considered as a clinically relevant difference in favor of non-operative management.
The median (IQR) length of hospital stay in the study of Sandhu (2018) in the non-operative management group (n=22) was 5.5 (IQR 3 to 15) days, compared to 4 (IQR 3 to 12) days in the TEVAR group (n=23). This was considered as a clinically relevant difference in favor of non-operative management.
The median (IQR) length of hospital stay in the study of Spencer (2018) in the non-operative management group (n=16) was 11 (IQR 5 to 24) days, compared to 20 (IQR 9 to 33) days in the TEVAR group (n=14). This was considered as a clinically relevant difference in favor of non-operative management.
Level of evidence of the literature
Aortic-related mortality (critical)
The level of evidence regarding the outcome aortic-related mortality was derived from observational studies and therefore started low. The level of evidence was downgraded by one level because of the small number of events (imprecision, -1) and heterogeneity in the control interventions (inconsistency, -1). The level of evidence was considered as very low.
Progression of minimal aortic injury on a control scan (critical)
Due to a lack of comparative data between the two groups, no level of evidence could be determined for the outcome progression of minimal aortic injury on a control scan in patients with minimal aortic injuries.
Complications (important)
The level of evidence regarding the outcome complications was derived from observational studies and therefore started low. The level of evidence was downgraded by one level because of the wide confidence level crossing the lower threshold of clinical relevance (imprecision, -1) and heterogeneity in the control interventions between the included studies (inconsistency, -1). The level of evidence was considered as very low.
Hospital length of stay (important)
The level of evidence regarding the outcome hospital length of stay was derived from an observational study and therefore started low. The level of evidence was downgraded by one level because of the small number of included patients (imprecision, -1). The level of evidence was considered as very low.
A systematic review of the literature was performed to answer the following question: What is the outcome of “non-operative management” (usually observation, blood pressure regulation and follow-up) in comparison with endovascular stent placement in patients with minimal aortic injuries?
| P: |
Patients with minimal aortic injuries |
| I: |
Conservative or “non-operative” management |
| C: |
Endovascular repair |
| O: |
Aortic-related mortality, progression of minimal aortic injury on control scan; TEVAR-related complications; hospital length of stay |
Relevant outcome measures
The guideline development group considered aortic-related mortality and progression of minimal aortic injury on control scan as critical outcomes for decision making; and complications of stent placement and length of hospital stay as important outcomes for decision making.
The working group defined a threshold of 10% for continuous outcomes, a relative risk (RR) for mortality of <0.95 and >1.05 and a relative risk ratio (RR) for other dichotomous outcomes of <0.80 and >1.25 as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until the 19th of September 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 157 hits. Studies were selected based on the following criteria: systematic reviews, randomized controlled trials, and observational study designs on observation and minimally invasive intervention (stent) in patients with minimal aortic injury. Twelve studies were initially selected based on title and abstract screening. After reading the full text, eight studies were excluded (see the table with reasons for exclusion under the tab Methods) and four studies were included.
Results
Four studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Awad H, Ramadan ME, El Sayed HF, Tolpin DA, Tili E, Collard CD. Spinal cord injury after thoracic endovascular aortic aneurysm repair. Can J Anaesth. 2017 Dec;64(12):1218-1235. doi: 10.1007/s12630-017-0974-1. Epub 2017 Oct 10. PMID: 29019146; PMCID: PMC5954412.
- De Freitas S, Joyce D, Yang Y, Dunphy K, Walsh S, Fatima J. Systematic Review and Meta-Analysis of Nonoperative Management for SVS Grade II Blunt Traumatic Aortic Injury. Ann Vasc Surg. 2024 Jan;98:220-227. doi: 10.1016/j.avsg.2023.07.106. Epub 2023 Oct 6. PMID: 37806657.
- DuBose JJ, Leake SS, Brenner M, Pasley J, O'Callaghan T, Luo-Owen X, Trust MD, Mooney J, Zhao FZ, Azizzadeh A; Aortic Trauma Foundation. Contemporary management and outcomes of blunt thoracic aortic injury: a multicenter retrospective study. J Trauma Acute Care Surg. 2015 Feb;78(2):360-9. doi: 10.1097/TA.0000000000000521. Erratum in: J Trauma Acute Care Surg. 2015 Mar;78(3):656. PMID: 25757123.
- DuBose JJ, Charlton-Ouw K, Starnes B, Saqib N, Quiroga E, Morrison J, Gewertz B, Azizzadeh A; AAST/Aortic Trauma Foundation Study Group. Do patients with minimal blunt thoracic aortic injury require thoracic endovascular repair? J Trauma Acute Care Surg. 2021 Feb 1;90(2):384-387. doi: 10.1097/TA.0000000000002995. PMID: 33075025.
- Gandhi SS, Blas JV, Lee S, Eidt JF, Carsten CG 3rd. Nonoperative management of grade III blunt thoracic aortic injuries. J Vasc Surg. 2016 Dec;64(6):1580-1586. doi: 10.1016/j.jvs.2016.05.070. Epub 2016 Jul 25. PMID: 27461999.
- Gharai LR, Ovanez C, Goodman WC, Deng X, Bandyopadhyay D, Aboutanos MB, Parker MS. Minimal Aortic Injury Detected on Computed Tomography Angiography during Initial Trauma Imaging: Single Academic Level 1 Trauma Center Experience. Aorta (Stamford). 2022 Dec;10(6):265-273. doi: 10.1055/s-0042-1757793. Epub 2022 Dec 20. PMID: 36539143; PMCID: PMC9767788.
- Harris DG, Rabin J, Bhardwaj A, June AS, Oates CP, Garrido D, Toursavadkohi S, Khoynezhad A, Crawford RS. Nonoperative Management of Traumatic Aortic Pseudoaneurysms. Ann Vasc Surg. 2016 Aug;35:75-81. doi: 10.1016/j.avsg.2016.02.021. Epub 2016 Jun 3. PMID: 27263820.
- Heneghan RE, Aarabi S, Quiroga E, Gunn ML, Singh N, Starnes BW. Call for a new classification system and treatment strategy in blunt aortic injury. J Vasc Surg. 2016 Jul;64(1):171-6. doi: 10.1016/j.jvs.2016.02.047. Epub 2016 Apr 27. PMID: 27131924.
- Isselbacher, E, Preventza, O. et al. 2022 ACC/AHA Guideline for the Diagnosis and Management of Aortic Disease: A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2022 Dec, 80 (24) e223–e393. https://doi.org/10.1016/j.jacc.2022.08.004.
- Jacob-Brassard J, Salata K, Kayssi A, Hussain MA, Forbes TL, Al-Omran M, de Mestral C. A systematic review of nonoperative management in blunt thoracic aortic injury. J Vasc Surg. 2019 Nov;70(5):1675-1681.e6. doi: 10.1016/j.jvs.2019.02.023. Epub 2019 May 21. PMID: 31126762.
- Jinadasa SP, Mueller AL, Apffel A, Cave B, DuBose JJ, Scalea TM, Kundi R. Close surveillance imaging is unnecessary for patients with grade I blunt thoracic aortic injury. Am J Surg. 2022 Nov;224(5):1324-1328. doi: 10.1016/j.amjsurg.2022.06.007. Epub 2022 Jun 9. PMID: 35728986.
- Kapoor H, Lee JT, Orr NT, Nisiewicz MJ, Pawley BK, Zagurovskaya M. Minimal Aortic Injury: Mechanisms, Imaging Manifestations, Natural History, and Management. Radiographics. 2020 Nov-Dec;40(7):1834-1847. doi: 10.1148/rg.2020200066. Epub 2020 Oct 2. PMID: 33006921.
- Karaolanis Lamarche Y, Berger FH, Nicolaou S, Bilawich AM, Louis L, Inacio JR, Janusz MT, Evans D. Vancouver simplified grading system with computed tomographic angiography for blunt aortic injury. J Thorac Cardiovasc Surg. 2012 Aug;144(2):347-54, 354.e1. doi: 10.1016/j.jtcvs.2011.10.011. Epub 2011 Nov 8. PMID: 22070925.
- Lee WA, Matsumura JS, Mitchell RS, Farber MA, Greenberg RK, Azizzadeh A, Murad MH, Fairman RM. Endovascular repair of traumatic thoracic aortic injury: clinical practice guidelines of the Society for Vascular Surgery. J Vasc Surg. 2011 Jan;53(1):187-92.
- Lozano R, DiLosa K, Schneck M, Maximus S, Callcut R, Shatz D, Mell M. Comparison of treatment and outcomes in blunt thoracic aortic injury based on different vascular surgery guidelines. J Vasc Surg. 2023 Jul;78(1):48-52. doi: 10.1016/j.jvs.2023.03.018. Epub 2023 Apr 22. PMID: 37088445.
- Mazzolai L, Teixido-Tura G, Lanzi S, Boc V, Bossone E, Brodmann M, Bura-Rivière A, De Backer J, Deglise S, Della Corte A, Heiss C, Kałużna-Oleksy M, Kurpas D, McEniery CM, Mirault T, Pasquet AA, Pitcher A, Schaubroeck HAI, Schlager O, Sirnes PA, Sprynger MG, Stabile E, Steinbach F, Thielmann M, van Kimmenade RRJ, Venermo M, Rodriguez-Palomares JF; ESC Scientific Document Group. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J. 2024 Sep 29;45(36):3538-3700.
- Sandhu HK, Leonard SD, Perlick A, Saqib NU, Miller CC 3rd, Charlton-Ouw KM, Safi HJ, Azizzadeh A. Determinants and outcomes of nonoperative management for blunt traumatic aortic injuries. J Vasc Surg. 2018 Feb;67(2):389-398. doi: 10.1016/j.jvs.2017.07.111. Epub 2017 Sep 22. PMID: 28947225.
- Soong TK, Wee IJY, Tseng FS, Syn N, Choong AMTL. A systematic review and meta-regression analysis of nonoperative management of blunt traumatic thoracic aortic injury in 2897 patients. J Vasc Surg. 2019 Sep;70(3):941-953.e13. doi: 10.1016/j.jvs.2018.12.045. PMID: 31445650.
- Spencer SM, Safcsak K, Smith CP, Cheatham ML, Bhullar IS. Nonoperative management rather than endovascular repair may be safe for grade II blunt traumatic aortic injuries: An 11-year retrospective analysis. J Trauma Acute Care Surg. 2018 Jan;84(1):133-138. doi: 10.1097/TA.0000000000001630. PMID: 28640779.
- Tanizaki S, Maeda S, Matano H, Sera M, Nagai H, Nakanishi T, Ishida H. Blunt thoracic aortic injury with small pseudoaneurysm may be managed by nonoperative treatment. J Vasc Surg. 2016 Feb;63(2):341-4. doi: 10.1016/j.jvs.2015.08.107. Epub 2015 Oct 23. PMID: 26506935.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Dubose (2021) |
Type of study: Retrospective study.
Setting and country: Level 1 trauma centers.
Funding and conflicts of interest: The authors declare no conflicts of interest.
|
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: N = 61 Control: N = 91
Important prognostic factors2: age ± SD: I: 40.6 (IQR: 15.9) years C: 42.3 (IQR: 16.5) years
Sex: I: 41/61 (67.2%) M C: 64/91 (66.7%) M
Groups comparable at baseline? Yes.
|
Describe intervention (treatment/procedure/test): Thoracic endovascular aortic repair
|
Describe control (treatment/procedure/test): Non-operative management. |
Length of follow-up: No information.
Loss-to-follow-up: No information.
|
Progression of minimal aortic injury on control scan Not reported.
Aortic-related mortality I: 2/61 (3.3%) C: 0/91 (0%)
Hospital length of stay (median; IQR) I: 16.0 (22.0) days C: 12.0 (12.0) days
Complications I: 51/61 (83.6%) C: 70/91 (76.9%)
|
Author’s conclusion: Our study is the largest contemporary examination of BTAI in the literature. Our findings suggest that optimal BTAI care remains an ongoing challenge of trauma care in the endovascular era. In the context of contemporary practice, NOM failures for SVS Grade I to III injuries are rare, but TEVAR use seems independently protective against aortic-related mortality. TEVAR-specific complication rates have declined compared with previous reports. There remains a persistent need to examine the optimal treatment of BTAI, particularly lower-grade injuries. Long-term studies are required to determine the natural history of both untreated and treated BTAI. |
|
Dubose (2021) |
Type of study: Retrospective cohort study.
Setting and country: 28 international centers.
Funding and conflicts of interest: The authors declare no conflicts of interest.
|
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: N = 48 Control: N = 71
Important prognostic factors2: age ± SD: I: 52.0 (IQR: 26) years C: 41.0 (IQR: 29) years
Sex: I: 35/48 (72.9%) M C: 49/71 (69.0%) M
Groups comparable at baseline? Yes.
|
Describe intervention (treatment/procedure/test): Thoracic endovascular aortic repair
|
Describe control (treatment/procedure/test): Non-operative management. |
Length of follow-up: No information.
Loss-to-follow-up: No information.
|
Progression of minimal aortic injury on control scan Not reported.
Aortic-related mortality I: 2/48 (4.2%) C: 0/71 (0%)
Hospital length of stay (median; IQR) I: 11.0 (16.0) days C: 13.0 (12.0) days
Complications I: 26*/48 (54.2%) C: 45**/71 (63.4%)
*Complications were: - Delayed stroke – ischemic N = 1; - Acute renal failure N = 2 - Pulmonary embolism N = 3; - Mechanical ventilation > 48h N = 10; - Ventilator associated pneumonia N = 4; - Acute lung injury/acute respiratory distress syndrome N = 3; - Sepsis N = 3
** Complications were: - Delayed stroke – ischemic N = 1; - Acute renal failure N = 5 - Pulmonary embolism N = 3; - Mechanical ventilation > 48h N = 22; - Ventilator associated pneumonia N = 5; - Acute lung injury/acute respiratory distress syndrome N = 2; - Sepsis N = 7. |
Author’s conclusion: Minimal aortic injuries (SVS Grade 1 and 2) undergo TEVAR in 40% of patients. When compared with those patients managed medically, however, there appear to be no difference in subsequent outcomes except an increase in complications related to the conduct of TEVAR itself. These findings suggest that the current SVS guidelines for BTAI management warrant revision and greater emphasis should be used to highlight the safety of an MM first strategy for MAIs.
|
|
Sandhu (2018) |
Type of study: Retrospective study.
Setting and country: Prospective institutional trauma registry.
Funding and conflicts of interest: The authors declare no conflicts of interest and no funding.
|
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: N = 22 Control: N = 23
Important prognostic factors2: age ± SD: I: 38.5 (15.8) years C: 40.2 (14.3) years
Sex: I: 16/22 (72.7%) M C: 19/23 (82.6%) M
Groups comparable at baseline? Yes. |
Describe intervention (treatment/procedure/test): Thoracic endovascular aortic repair
|
Describe control (treatment/procedure/test): Non-operative management |
Length of follow-up: No information.
Loss-to-follow-up: None.
|
Hospital length of stay C: 4 (3 to 12) days
|
Author’s conclusion: Based on these limited data, it appears that patients with minimal aortic injuries (grades I and II) may be managed medically, with the majority resolving within 8 weeks. Minimal aortic injury is associated with low mortality and excellent intermediate-term outcomes. Further prospective studies are required to validate these findings.
|
|
Spencer (2018) |
Type of study: Retrospective cohort study.
Setting and country: Level 1 trauma center.
Funding and conflicts of interest: The authors declare no conflicts of interest.
The present work did not receive any specific grant from funding agencies in the public, commercial, or not-for-profit sectors.
|
Exclusion criteria:
N total at baseline: Intervention: N = 14 Control: N = 16
Important prognostic factors2: age ± SD: I: 52 (32 to 65) years C: 43 (37 to 66) years
Sex: I: 11/14 (79%) M C: 8/16 (50%) M
Groups comparable at baseline? Yes. |
Describe intervention (treatment/procedure/test): Thoracic endovascular aortic repair
|
Describe control (treatment/procedure/test): Non-operative management with short-acting intravenous beta-blocker infusion titrated to maintain systolic blood pressure less than 140 mmHg and heart rate less than 80 bpm. Additional agents such as calcium channel blockers or vasodilators were added as needed. |
Length of follow-up: No information.
Loss-to-follow-up: None.
|
Mortality (related to their aortic lesion) I: 0/14 (0%) C: 0/16 (0%)
Mortality (due to devastating thoracic blunt injury) I: 2/14 (14.3%) C: 1/16 (6.3%)
Hospital length of stay C: 11 (5 to 24) days
Complications I: 2*/14 (14.3%) C: 2**/16 (12.5%)
*Atrial fibrillation (n=1) and a collapsing stent (n=1)
**Pulmonary embolism (n=1) and myocardial infarction (n=1). |
Author’s conclusion: Although the SVS guidelines suggest TEVAR for grade II–IV and NOM for grade I BTAI, NOM may be safely used in grade II BTAI. |
Risk of bias tabel
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population? |
Exposure
Can we be confident in the assessment of exposure? |
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study? |
Confounding-assessment
Can we be confident in the assessment of confounding factors? |
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome? |
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed? |
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias |
|
|
|
|
|
|
|
|
|
|
|
|
Dubose (2021) |
Definitely yes
Reason: Participants were selected from a registry.
|
Definitely yes
After institutional review board approval, the American Association for the Surgery of Trauma/Aortic Trauma Founda- tion (ATF) BTAI registry was used to identify patients enrolled from December 2016 to November 2019. Management and outcomes were recorded and compared. Patients with MAI, defined as SVS Grades I and II injury types, were then isolated for comparison. Demographics, admission physiology, severity of associated injuries, complications and outcomes were compared between MAI patients treated with TEVAR versus MM. A priori definitions established for use in the ATF registry were used for comparison. Among these, aortic-related mortality (ARM) was defined as death directly contributed to by either aortic in- jury itself or subsequent treatment of BTAI as determined by the individual site primary investigator. |
No information.
|
No information.
|
No information.
|
Probably yes.
Reason: no missing data. |
No information.
|
No information.
|
Some concerns |
|
DuBose (2015) |
Definitely yes
Reason: Participants were selected from a registry.
|
Probably yes
BTAI patients treated at the respective facilities from January 2008 to December 2013 were identified using trauma registries, with retrospective imaging and chart review used to complete data collection. Patients dying before imaging or transferred from outside hospitals were excluded. Demographic variables examined included age, sex, mechanism of injury, and admission physiologic data. Trauma registry data provided Injury Severity Scores (ISSs), body region specific Abbreviated Injury Scale (AIS) scores, and Glasgow Coma Scale (GCS) scores on arrival. |
No information.
|
No information.
|
No information.
|
Probably yes.
Reason: no missing data. |
No information.
|
No information.
|
Some concerns |
|
Sandhu (2018) |
Definitely yes
Reason: Participants were selected from a registry |
Probably yes
|
No information.
|
No information.
|
No information.
|
Probably yes.
Reason: no missing data. |
No information.
|
No information.
|
Some concerns |
|
Spencer (2018) |
Definitely yes
Reason: Participants were selected from a registry |
Probably yes
Reason: All patients with BTAI were evaluated in a multidisciplinary approach with the initial evaluation completed by the trauma team. |
No information.
|
No information.
|
No information.
|
Probably yes.
Reason: no missing data. |
No information.
|
No information.
|
Some concerns |
Exclusie tabel
|
Author and year |
Reason for exclusion |
|
Al-Thani |
Only included patients with Grade I or II who underwent non-operative management. The study did not include patients with Grade I or II who were treated with TEVAR. Therefore, it was not possible to compare both groups for the predefined outcomes. |
|
Arbabi (2022) |
Compared non-operative management with a mixed group of patients who underwent open repair and endovascular treatment. This did not meet the PICO-criteria of this guideline. |
|
Gaffey (2020) |
Wrong comparison of interventions. |
|
Jacob-Brassard (2019) |
Compared non-operative management with a mixed group of patients who underwent open repair and endovascular treatment. This did not meet the PICO-criteria of this guideline. |
|
Madigan (2022) |
The study reported patients with Grade II BTAI but did not report the predefined outcomes for this specific patient category. |
|
Mosquera (2018) |
Wrong study population. The study included Grade III and IV BTAI patients. |
|
Shackford (2017) |
Wrong study population. The study included Grade III and IV BTAI patients. |
|
Soong (2019 |
Non-comparative study. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-05-2025
Beoordeeld op geldigheid : 28-05-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) en/of andere bron. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met thoracale letsels na trauma.
Werkgroep
- Dr. M.M.E. (Mathieu) Wijffels, traumachirurg, NVvH (voorzitter)
- Drs. P.J. (Pieter Jan) van Huijstee, longchirurg, NVvH (voorzitter)
- Dr. D. (Doeke) Boersma, chirurg, NVvH
- Dr. W.P. (Wietse) Zuidema, chirurg, NVvH
- Drs. W.W.L. (Wilson) Li, cardiothoracaal chirurg, NVT
- Drs. A.W.M. (Antoinette) Stolwijk, chirurg-intensivist, NVIC
- Drs. V.P.M. (Vincent) Rietveld, SEG, NVSHA
- Dr. M. (Monique) Brink, radioloog, NVvR
- Drs. S.A.S. (Sandra) van den Heuvel, anesthesioloog, NVA
- L. (Lydia) Köster MSc, fysiotherapeut, KNGF
Klankbordgroep
- T. (Thomas) Jonkergouw, adviseur patiëntbelang, Patiëntenfederatie Nederland
- Dr. H. (Hendrik-Jan) Dieker, cardioloog, NVVC
Met ondersteuning van
- Dr. R. (Romy) Zwarts – van de Putte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Mitchel) Griekspoor MSc., adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. E.R.L. (Evie) Verweg, junior adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Wijffels |
Traumachirurg, Erasmus MC |
Geen |
Onderzoeksbeurzen van ZonMw (prospectieve ribfixatie studie), Johnson en Johnson DePuy Synthes, OTC/Stryker, Stichting Coolsingel, KLS Martin (onderzoek naar ribplaten) |
Gedeeltelijke restrictie. Het werkgroeplid zal niet meebeslissen over ribfixatie en/of ribplaten. Wanneer deze onderwerpen worden besproken zal Monique Brink de vergadering voorzitten. |
|
Van Huijstee |
Algemeen Thoracaal en Trauma-Chirurg, Medische Specialistische Co-operatie HAGA Ziekenhuis, Den Haag
|
Voorzitter Ned. Ver. Voor Longchirurgie (Onbetaald), Bestuurslid Ned. Ver. Voor Heelkunde (Onbetaald), ATLS-instructeur bij stichting ALSG.
Executive Board Member of Chest Wall International Group (onbezoldigd) |
Ad Hoc, Betaald adviseurschap bij Distrimed voor ontwikkeling van nieuwe implantaten voor congenitale borstkasafwijkingen en onkostenvergoeding bij proctoring van collega-chirurgen in het gebruik van deze implantaten. |
Gedeeltelijk restrictie. Het werkgroeplid zal niet meebeslissen over ribfixatie en/of ribplaten. Wanneer deze onderwerpen worden besproken zal Monique Brink de vergadering voorzitten. |
|
Stolwijk |
Traumachirurg, intensivist, MUMC+ |
Lid klankbordgroep richtlijn abdominale letsels na trauma medisch Manager Acute Zorg Limburg (NAZL) |
Geen.
|
Geen restrictie |
|
Boersma |
Chirurg |
Geen |
Geen |
Geen restrictie |
|
Köster |
Fysiotherapeut projectleider/ adviseur Traumazorg bij het traumacentrum Zuid West Nederland. |
Geen. Penningmeester geworden van Stichting Netwerk Traumarevalidatie Nederland (onbetaald). |
Geen |
Geen restrictie |
|
Brink |
Radioloog, Radboud UMC |
Sprekersbureau Canon Medical Systems |
Research Grant Canon Medical Systems 2016-2020 |
Geen restrictie |
|
Rietveld |
SEH-arts, Rijnstate |
Partner en course director DEUS |
Ontwikkeling point-of-care echografie |
Geen restrictie |
|
Zuidema |
Traumachirurg, Amsterdam UMC |
Secretaris NVT, Lid Geschillencommisie Ziekenhuizen |
Unrestricted grant (Mendela) voor studie over digitale pneumothorax zuigsystemen |
Geen restrictie |
|
Van den Heuvel |
Anesthesioloog 50%, pijnspecialist 50%, Radboud UMC |
Geen |
Regiehouder pijn Radboudumc, Editor pijn.nl Co-secretaris World Institute of Pain Benelux, onbetaald Educational committee web-based learning World Institute of Pain, onbetaald |
Geen restrictie |
|
Li |
Cardiothoracaal chirurg, Radboudumc |
Secretaris NVT |
Geen |
Geen restrictie |
|
Jonkergouw |
Adviseur Patiëntbelang Patiëntenfederatie Nederland |
Vrijwilliger Diabetes Vereniging Nederland |
Geen |
Geen restrictie |
|
Dieker |
Cardioloog, Radboudumc |
Geen |
Geen |
Geen restrictie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname aan de schriftelijke knelpunteninventarisatie en een afgevaardigde patiëntenvereniging in de klankbordgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Module Minimal aortic injury |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met thoracale letsels. Tevens zijn er knelpunten aangedragen door wetenschappelijke verenigingen via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nul effect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), duurzaamheid, aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: NVvH Thoracale letsels na trauma |
|
|
Uitgangsvraag: Wat is de plaats van observatie ten opzichte van een endovasculaire stent plaatsing bij patiënten met een minimal aortic injury? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 19-09-2023 |
|
Periode: Geen beperking |
Talen: Geen beperking |
|
Literatuurspecialist: Linda Niesink en Esther van der Bijl |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
→ Voor deze vraag is gezocht op de elementen minimal aortic injury (in het blauw) en observatie (afwachtend beleid / bloeddrukregulatie etc.) (in het groen) en minimaal invasieve ingreep (stent) (in het oranje).
→ De genoemde sleutelartikelen van Stephen (2018), Shackford (2017), Sandhu (2018) en ook de richtlijn van Isselbacher (2002) zitten in de zoekopbrengst.
→ Resultaten staan in Rayyan.
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 19-09-2023 met relevante zoektermen gezocht naar systematische reviews, RCT’s en observationele studiedesigns over observatie en minimaal invasieve ingreep (stent) bij patiënten met een minimal aortic inury. De literatuurzoekactie leverde 157 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
18 |
11 |
21 |
|
RCTs |
13 |
5 |
18 |
|
Observationele studies |
97 |
82 |
118 |
|
Totaal |
128 |
98 |
157 |
Zoekstrategie
Embase
|
Database |
Zoektermen |
||||||||||||||||||||||||||||||||||||
|
Embase
|
|
Medline (OVID)
|
# |
Searches |
Results |
|
1 |
((Aorta, Thoracic/ or Aorta, Abdominal/) and (Wounds, Nonpenetrating/ or blunt.ti,ab,kf. or nonpenetrat*.ti,ab,kf. or non-penetrat*.ti,ab,kf. or trauma.ti,ab,kf. or injur*.ti,ab,kf.)) or (aort* adj3 (trauma* or injur*)).ti,ab,kf. |
7990 |
|
2 |
exp Conservative Treatment/ or exp Watchful Waiting/ or nonoperative*.ti,ab,kf. or non-operative*.ti,ab,kf. or non operative.ti,ab,kf. or ((conservative or observative) adj2 (management or treatment)).ti,ab,kf. or noninvasive.ti,ab,kf. or non-invasive.ti,ab,kf. or expectative*.ti,ab,kf. or expectantly.ti,ab,kf. or 'watchful waiting'.ti,ab,kf. or (wait adj2 see).ti,ab,kf. or 'no treatment'.ti,ab,kf. or 'no intervention'.ti,ab,kf. or 'natural course'.ti,ab,kf. or observation.ti,ab,kf. or (blood pressure adj3 (control or regulation)).ti,ab,kf. or repetitive radiology.ti,ab,kf. |
744544 |
|
3 |
exp Stents/ or stent*.ti,ab,kf. or Endovascular Procedures/ or endovascular.ti,ab,kf. or 'aortic device*'.ti,ab,kf. or 'open repair'.ti,ab,kf. or surgery.ti,ab,kf. |
1654605 |
|
4 |
1 and 2 and 3 |
234 |
|
5 |
4 not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
221 |
|
6 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
694486 |
|
7 |
exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf. |
1646768 |
|
8 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5513717 |
|
9 |
5 and 6 – SR’s |
11 |
|
10 |
(5 and 7) not 9 – RCT’S |
5 |
|
11 |
(5 and 8) not (9 or 10) – observationele studies |
82 |
|
12 |
9 or 10 or 11 |
98 |
