Het voorspellen van complicaties
Uitgangsvraag
Wat is de waarde van het gebruik van voorspellende factoren voor de identificatie van patiënten met complicaties vanwege thoracale letsels?
Aanbeveling
Overweeg het gebruik van het predictiemodel van Battle met hierin factoren leeftijd, aantal ribfracturen, chronische longaandoeningen, pre-trauma gebruik van bloedverdunners en zuurstof voor het voorspellen van het risico op complicaties bij patiënten met een thorax letsel.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is een literatuuronderzoek verricht naar de prestatie van predictiemodellen, welke de kans op complicaties bij patiënten met bewezen thoracaal letsel voorspellen. Er werd één gevalideerd predictiemodel gevonden die complicaties na een thoracaal letsel voorspelt. Dit predictiemodel heeft een sensitiviteit van 80%, specificiteit van 96%, een positief voorspellende waarde van 93% en een negatief voorspellende waarde van 86%. Ondanks de lage bewijskracht van de geïncludeerde studie lijkt het raadzaam om de risico-score te gebruiken in de dagelijkse praktijk. Door de score die dit oplevert kan de behandeling zo nodig aangepast worden en kan het mogelijk de oplettendheid voor het optreden van complicaties verhogen bij het behandelteam.
Wat de invloed is van het invoeren van een predictiemodel, in afwezigheid van sterk bewijs, is niet te voorspellen. Het klinkt aannemelijk dat een hoge kans op complicaties ervoor zorgt dat het behandelteam scherper is op de aanwezigheid van complicaties bij individuele patiënten, echter het omgekeerde kan waar zijn bij een kleine voorspelde kans op complicaties. Dit laatste is wellicht minder aan de orde vanwege een hoge negatief voorspellende waarde van dit scoringssysteem. De accuratesse van de beschreven score zou afgezet moeten worden tegen de voorspellende waarde van clinici. Tot op heden is die niet bekend en derhalve niet te vergelijken. Het lijkt echter niet aannemelijk dat een clinicus een positief voorspellende waarde van 93% haalt voor het voorspellen van complicaties in de doelgroep. Wanneer het beloop van een patiënt betrouwbaar voorspeld kan worden kan dit voordeel opleveren voor de patiënt als individu en de samenleving als geheel. Het opnameverloop en -duur kan beter inzichtelijk worden gemaakt door gebruik te maken van zo’n score. Echter staat ertegenover dat het tijd kost voor de clinicus om een dergelijke score te berekenen.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het belangrijkste doel van de onderzochte predictiemodellen is het voorspellen van complicaties. Hiermee kan, voor zover mogelijk, geanticipeerd worden op hetgeen al dan niet komen gaat. Eventuele preventieve maatregelen voor het optreden van complicaties kunnen in een vroeg stadium ingezet worden, en ontslagtrajecten kunnen vervroegd gestart worden bij een kleine kans op complicaties. Hierdoor zal de opnameduur van patiënten verkorten en mogelijk zal het aantal complicaties afnemen omdat er eerder kan worden ingegrepen. Hiervoor is geen extra inspanning nodig van de patiënt. De patiënt specifieke factoren die invloed hebben op het optreden van complicaties zijn in het beschreven predictiemodel meegenomen, derhalve is het niet te verwachten dat er specifieke patiëntgroepen zijn waarbij het predictiemodel meer of minder accuraat zal voorspellen.
Verder is het aantal ribfracturen één van de factoren die in de vragenlijst is opgenomen. Hiervoor zal een CT gemaakt moeten worden, daar we weten dat de sensitiviteit van een CT groter is dan van een conventionele foto (Murphy, 2017). Slechts een deel van de trauma patiënten in Nederland ondergaat een CT-scan van de thorax. Wanneer het aantal ribfracturen vastgesteld wordt op slechts een conventionele foto of echografie, valt de score wellicht te laag uit met het risico op onderbehandeling. Een CT-scan kost geld, stelt de patiënt bloot aan meer röntgenstraling dan conventioneel onderzoek, verhoogt de kans op het vinden van nevenbevindingen en medicalisatie, vergt extra geschoold personeel, kost tijd en kan schaars zijn buiten kantoortijden. Voorts is nog niet gedefinieerd welk type ribfracturen bijdragen aan de score; elke knik in de cortex of bicorticaal verplaatste fracturen. Ondanks dat een predictiemodel zinvol kan zijn voor patiënten, is de werkgroep van mening dat er geen CT van de thorax gemaakt moet worden met als enige doel om een predictie score te bepalen (zie de richtlijn ‘Initiële radiodiagnostiek bij traumapatiënten’). De stralenbelasting en mogelijk extra ongemak en pijn als gevolg van het maken van een CT kunnen op dit moment niet verantwoord worden met de opbrengst van een predictie.
Kosten (middelenbeslag)
De kosten van het predictiemodel zijn nihil. Het kost alleen tijd voor de behandelaar om een dergelijke score te berekenen. Derhalve is alle gezondheidswinst, ook al is deze minimaal, op individueel en maatschappelijk niveau acceptabel (zie bovenstaande alinea’s). Daarnaast kan het voorspellen van complicaties resulteren in eventuele preventieve maatregelen om complicaties in een vroeg stadium te voorkomen. Hierdoor wordt wellicht de opnameduur van patiënten verkort, wat kan resulteren in een significante afname van zorgkosten.
Aanvaardbaarheid, haalbaarheid en implementatie
Er is tot op heden geen onderzoek gedaan naar de aanvaardbaarheid, haalbaarheid en implementatie van een voorspellend model. Derhalve kan er op basis van wetenschappelijke evidentie geen antwoord worden gegeven op de vraag wat het voordeel is van implementatie van een voorspellend model. De afwezigheid van significante kosten maakt dat er een lage drempel zou kunnen bestaan voor implementatie van een dergelijk model. Elke winst kan derhalve verantwoord worden. Eventuele aanpassingen van het elektronisch patiëntendossier zou hierop een uitzondering kunnen zijn. Het risico van een predictiemodel is dat gebruikers er blind op gaan vertrouwen. Dit noopt tot expertise van de gebruiker hoe het predictiemodel te gebruiken en te interpreteren. Dit zou implementatie en succes van een dergelijk predictiemodel kunnen bemoeilijken.
Iedereen in Nederland heeft in acute posttraumatische setting recht op zorg, waarbij de gezondheidsgelijkheid is geborgd. In het geval van gebroken ribben kan de vragenlijst uit het geïncludeerde artikel van Battle (2014) gebruikt worden. Een aantal van de factoren die de uiteindelijk score uit de vragenlijst vormen (leeftijd, chronische longziekte en gebruik van antistolling) zijn alleen (hetero-) anamnestisch af te nemen. Taalbarrière zou hierbij een obstakel kunnen vormen.
De implementatie van deze vragenlijst vergt iets of iemand die de score berekent. Dit is weinig arbeids- en tijdsintensief, maar is wel noodzakelijk. Omdat de score een voorspellende waarde heeft zou de behandelend clinicus als eindverantwoordelijke dit moeten doen of delegeren. Door de toenemende vergrijzing van de populatie in Nederland, die gepaard gaat met toename van incidentie van chronische longziekten zullen steeds meer patiënten een hoge Battlescore behalen. Dit lijdt mogelijk tot meer opnames in het ziekenhuis. Bij een beperkte beddencapaciteit zou dit voor implementatie-problemen kunnen zorgen. Helaas is het moeilijk te voorspellen of dit daadwerkelijk zal gaan gebeuren.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is één studie geïncludeerd in de literatuuranalyse met een lage bewijskracht waaruit blijkt dat een predictiemodel met de factoren leeftijd, aantal ribfracturen, chronische longaandoeningen, pre-trauma gebruik van bloedverdunners en zuurstof saturatie kan helpen bij het voorspellen van complicaties in patiënten met bewezen thorax letsel. De scorelijst is makkelijk te implementeren omdat de afzonderlijke parameters veelal bekend zijn bij patiënten die reeds een CT ondergaan hebben. De werkgroep is van mening dat er geen CT van de thorax gemaakt moet worden met als enige doel om een predictie score te bepalen (zie de richtlijn ‘Initiële radiodiagnostiek bij traumapatiënten’). De belasting voor de zorgverlener en de patiënt is beperkt met betrekking tot extra kosten en tijdsinvestering.
Onderbouwing
Stomp thoraxtrauma komt veel voor en is een belangrijke oorzaak van morbiditeit. Dit type trauma resulteert in 4-60% zelfs in mortaliteit (Battle, 2013; Brasel, 2006; Bergeron, 2003; Martinez Casas, 2016). Inschatten van de ernst van het thoraxtrauma is belangrijk om de juiste behandeling te starten, het opname beleid te bepalen (ontslag, verpleegafdeling, medium care en/of intensive care) en de prognose van de patiënt vast te stellen.
Verschillende prognosticerende scores bestaan voor stomp thoraxletsel. Deze richten zich echter vooral op de multitraumatisé, zijn niet extern gevalideerd of direct klinisch toepasbaar (Ahmad, 2010; Moon, 2017). Verder is het evalueren van de veranderingen in klinische presentatie belangrijk om complicaties op te sporen of om het ontslagtraject veilig te kunnen starten. Het is dus belangrijk de bekende factoren en bestaande scoresystemen op validiteit te beoordelen en hieruit de meest betrouwbare scoresystemen aan te bevelen.
|
Low GRADE |
A prediction model including agea, number of rib fracturesb, chronic lung disease, pre-injury anticoagulants, and oxygen saturationc may be suitable for the prediction of complications in patients with proven thoracic trauma.
Source: Battle, 2014 |
a Per one year increase; b per one fracture increase; c per 1% decrease of oxygen saturations
Description of studies
The study of Battle (2014) developed and validated a prognostic model that can be used to assist in the management of blunt chest wall trauma. The prognostic model was developed on a sample of 276 patients who presented to the emergency department of a large regional trauma center in South Wales between 2009 and 2011, with a primary diagnosis of blunt chest-wall trauma. The final prognostic model was based on prognostic variables which were significant at the p<0.05 level following multivariable logistic regression analysis. The model’s accuracy and predictive capabilities were assessed. In the second study phase, external validation of the model was completed in a multicenter prospective study based on 237 patients. Battle (2014) developed a simple clinical score based on the regression coefficients from the final model. The final model includes five relevant factors (age, number of rib fractures confirmed on CT, chronic lung disease, pre-injury anticoagulants, and oxygen saturations) to predict complications in patients with blunt chest-wall trauma. The model was validated by comparing predicted versus observed outcomes and the model performance was assessed using calibration and discrimination analyses.
Results
Model performance for the prediction of complications
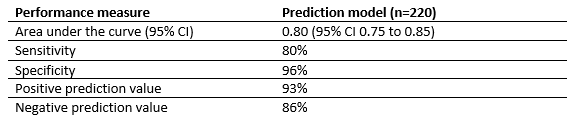
Battle (2014) presented a model including five relevant factors (age, number of rib fractures, chronic lung disease, pre-injury anticoagulants, and oxygen saturations) to predict complications in patients with blunt chest-wall trauma. To calculate the risk score for the individual predictors, the coefficient of each predictor was multiplied by a factor so that the smallest coefficient was transformed into a value close to one. These individual scores were then added together to provide an overall risk score for each patient. Using the validation sample, each patient’s final overall risk score was compared to their probability of developing complications initially calculated using the final logistic regression equation. The individual final risk scores were categorized into groups (0 to 10, 11 to 15, 16 to 20, 21 to 25, 26 to 30 and ≥30) and the mean and standard deviation of all the corresponding probabilities were calculated. This would provide the clinician with a probability of the development of complications for each possible final risk score. The performance scores of the prediction model are presented in Table 1. The model was classified as excellent.
Table 1. Performance of prediction model predicting complications in patients with proven thoracic trauma
Level of evidence
Prediction model performance for the prediction of complications
The level of evidence regarding the outcome prediction model performance for the prediction of complications was derived from an observational (prospective) study and therefore started high. The level of evidence was downgraded by two levels because of a risk of bias (one level, see table of quality assessment) and imprecision (one level, small number of events). The level of evidence was considered as low.
A systematic review of the literature was performed to answer the following question: Which combination of patient characteristics predicts complications in patients with proven thoracic trauma?
| P: |
Patients with proven thoracic trauma |
| I: |
Prediction model for complications |
| C: |
Other prediction model or no comparison |
| O: | Model performance (discrimination parameters, e.g.: area under the curve (AUC), sensitivity, specificity, predictive values) |
| T: | - |
| S: |
Emergency department |
Relevant outcome measures
The guideline development group considered sensitivity as a critical outcome for decision making; and AUC, specificity, and (positive and negative) predictive values as important outcomes for decision making.
The guideline development group defined the performance of the included models as follows:
- AUC between 0.7 and 0.79 is considered as ‘acceptable’.
- AUC between 0.8 and 0.89 is considered as ‘good’.
- AUC equal or greater than 0.9 is considered as ‘excellent’.
Prognostic research: Study design and hierarchy
When reviewing the literature, there is a hierarchy in quality of individual studies. Preferably, the effectiveness of a clinical decision model is evaluated in a clinical trial. Unfortunately, these studies are very rare. If not available, studies in which prediction models are developed and validated in other samples of the target population (external validation) are preferred as there is more confidence in the results of these studies compared to studies that are not externally validated. Most samples do not completely reflect the characteristics of the total population, resulting in deviated associations, possibly having consequences for conclusions. Studies validating prediction models internally (e.g. bootstrapping or cross validation) can be used to answer the first research question as well, but downgrading the level of evidence is obvious due to risk of bias and/or indirectness as it is not clear whether models perform sufficiently in target populations. The confidence in the results of unvalidated prediction models is very low. Therefore, such models will not be graded.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until the 4th of May, 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 1.183 hits. Studies were selected based on the following criteria: systematic reviews, randomized controlled trials, and observational studies on prediction models for patients with thoracic trauma. Five studies were initially selected based on title and abstract screening. After reading the full text, four studies were excluded (see the table with reasons for exclusion under the tab Methods) and one study was included.
Results
One study (Battle, 2014) was included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Ahmad MA, Sante ED, Giannoudis PV: Assessment of severity of chest trauma: is there an ideal scoring system? Injury 2010, 41:981–983.2003;54:478–85.
- Battle C, Hutchings H, Lovett S, Bouamra O, Jones S, Sen A, Gagg J, Robinson D, Hartford-Beynon J, Williams J, Evans A. Predicting outcomes after blunt chest wall trauma: development and external validation of a new prognostic model. Crit Care. 2014 May 14;18(3):R98. doi: 10.1186/cc13873. PMID: 24887537; PMCID: PMC4095687.
- Battle CE, Hutchings H, Evans PA. Risk factors that predict mortality in patients with blunt chest wall trauma: a systematic review and meta-analysis. Injury. 2012 Jan;43(1):8-17. doi: 10.1016/j.injury.2011.01.004. Epub 2011 Jan 22. PMID: 21256488.
- Battle CE, Hutchings H, James K, Evans PA. The risk factors for the development of complications during the recovery phase following blunt chest wall trauma: a retrospective study. Injury. 2013 Sep;44(9):1171-6. doi: 10.1016/j.injury.2012.05.019. Epub 2012 Jun 12.
- Battle CE, Hutchings H, Evans PA. Expert opinion of the risk factors for morbidity and mortality in blunt chest wall trauma: results of a national postal questionnaire survey of Emergency Departments in the United Kingdom. Injury. 2013 Jan;44(1):56-9. doi: 10.1016/j.injury.2011.12.012. Epub 2012 Jan 9. PMID: 22227106.
- Brasel KJ, Guse CE, Layde P, Weigelt JA. Rib fractures: relationship with pneumonia and mortality. Crit Care Med. 2006 Jun;34(6):1642-6.
- Bergeron E, Lavoie A, Clas D, Moore L, Ratte S, Tetreault S, Lemaire J, Martin M. Elderly trauma patients with rib fractures are at greater risk of death and pneumonia. J Trauma. 2003 Mar;54(3):478-85.
- Martinez Casas I, Amador Marchante MA, Paduraru M, et al. Thorax trauma severity score: is it reliable for patient's evaluation in a secondary level hospital? Bull Emerg Trauma 2016;4:150–5.
- Moon, S. H., Kim, J. W., Byun, J. H., Kim, S. H., Choi, J. Y., Jang, I. S., … Park, H. O. The thorax trauma severity score and the trauma and injury severity score: Do they predict in-hospital mortality in patients with severe thoracic trauma?: A retrospective cohort study. Medicine. 2017, 96(42), e8317.
- Murphy CE 4th, Raja AS, Baumann BM, Medak AJ, Langdorf MI, Nishijima DK, Hendey GW, Mower WR, Rodriguez RM. Rib Fracture Diagnosis in the Panscan Era. Ann Emerg Med. 2017 Dec;70(6):904-909. doi: 10.1016/j.annemergmed.2017.04.011. Epub 2017 May 27. PMID: 28559032.
|
Study reference |
Study characteristics |
Patient characteristics |
Candidate predictors |
Model development, performance and evaluation
|
Outcome measures and results |
Comments Interpretation of model |
|
Battle (2014) |
Source of data1 and date: Data were collected retrospectively from the medical notes of each patient.
Setting/ number of centres and country: The ED of a large regional trauma centre in South Wales between 2009 and 2011.
Funding and conflicts of interest: No funding was received for this study.
The authors declare that they have no competing interests. |
Recruitment method2: Data were collected retrospectively from the medical notes of each patient. If there was no record in the patient’s notes of chronic lung disease, cardiovascular disease, use of pre- injury anticoagulants or current smoking status, then it was assumed that these predictors were absent. The number of rib fractures was determined from the chest radiograph if not documented in the medical notes.
Inclusion criteria:
Exclusion criteria:
Participants: N = 274
Mean age ± SD: No information.
Sex: % M / % F 64% was male.
Most common injury
Other important characteristics: None. |
Describe candidate predictors3 and method and timing of measurement:
Predictor 1: Age
Predictor 2: Number of rib fractures
Predictor 3: Chronic lung disease
Predictor 4: Cardiovascular disease
Predictor 5: Use of pre-injury anti-coagulants
Predictor 6: smoking status
Predictor 7: oxygen saturations
Predictor 8: respiratory rate on initial assessment in the ED.
Number of participants with any missing value4? N (%): 0 (0%)
How were missing data handled5? Not applicable.
|
Development Modelling method6: Logistic regression.
Performance Calibration measures7 and 95%CI: Calibration was assessed graphically and with the Hosmer-Lemeshow test.
Discrimination measures8 and 95%CI: Discrimination was assessed with the c-statistic (equivalent to the area under the receiver operator curve)
Classification measures9: Sensitivity, specificity, positive and negative predictive values were calculated for the final model.
Evaluation Method for testing model performance10: external
|
Type of outcome: single/combined? Single
Definition and method for measurement of outcome:
Endpoint or duration of follow-up: No information.
Number of events/outcomes:
RESULTS Multivariable model11: Agea: OR 1.0 (95% CI 1.0 to 1.0) Z-score 1.80
Number of rib fracturesb: OR 1.5 (95% CI 1.3 to 1.9) Z-score 4.21
Chronic lung disease: OR 2.2 (95% CI 1.2 to 4.1) Z-score 2.50
Pre-injury anticoagulants: OR 1.9 (95% CI 1.0 to 3.7) Z-score 1.91
Oxygen saturationsc: OR 0.9 (95% CI 0.9 to 1.0) Z-score -1.55
a: per one year increase b: per one fracture increase c: per 1% decrease of oxygen satursations
Alternative presentation of final model12: |
Interpretation: As a result the reliability and applicability is sufficient that the model could be safely and effectively used in the clinical setting. The external validation results also confirm the clinical usefulness of the model in blunt chest-wall trauma management throughout England and Wales. It is important to emphasise, however, that the validation model c-statistic is a very unusual result and should be interpreted with caution. It is more common for the c- statistic to decrease in the validation study, rather than to increase as we found.
Comparison with other studies? No.
Generalizability? The overall results of this study suggest that the final validation model could be safely and effectively used in the clinical setting in England and Wales for assisting in the management of blunt chest-wall trauma patients. |
1 Cohort, case-control, randomised trial participants, registry data
2 Consecutive participants?
3 Or describe number and type of candidate predictors, e.g. demographics, patient history, physical examination, additional testing, disease characteristics.
4 Include predictors and outcome
5 Complete-case analysis, imputation, other method
6 Logistic, survival, neural networks, machine learning technique
7 Calibration plot, calibration slope, Hosmer-Lemeshow test
8 C-statistic, D-statistic, log-rank
9 Sensitivity, specificity, predictive values, net reclassification improvement and a priori cut points
10 Development dataset only (internal) or separate external validation
11 Including predictor weights or regression coefficients, intercept, baseline survival, model performance measures
12 E.g. sum score, nomogram, score chart, predictions of specific risk subgroups
Risk of bias tabel
|
Study reference (first author, year of publication)
Classification1
|
Participant selection 1) Appropriate data sources?2 2) Appropriate in- and exclusion?
Risk of bias: low/high/unclear |
Predictors 1) Assessed similar for all participants? 2) Assessed without knowledge of outcome? 3) Available at time the model is intended to be used?
Risk of bias: low/high/unclear |
Outcome 1) Pre-specified or standard outcome definition? 2) Predictors excluded from definition? 3) Assessed similar for all participants? 4) Assessed without knowledge of predictors? 5) Time interval between predictor and outcome measurement appropriate?
Risk of bias: low/high/unclear |
Analysis 1) Reasonable number of participants with event/outcome? 2) All enrolled participants included in analysis? 3) Missing data handled appropriately? 4) No selection of predictors based on univariate analysis? 5) Relevant model performance measures evaluated appropriately?3 6) Accounted for model overfitting4 and optimism? 7) Predictors and weights correspond to results from multivariate analysis?
Risk of bias: low/high/unclear |
Overall judgment
High risk of bias: at least one domain judged to be at high risk of bias.
Model development only: high risk of bias.
Risk of bias: low/high/unclear |
|
Battle (2014) |
Low
(Retrospective study with data of patients who presented to the ED of a large regional trauma centre in South Wales between 2009 and 2011, with a primary diagnosis of blunt chest-wall trauma with clear in- and exclusion criteria.) |
Low
(Data were collected retrospectively from the medical notes of each patient. If there was no record in the patient’s notes of chronic lung disease, cardiovascular disease, use of preinjury anticoagulants or current smoking status, then it was assumed that these predictors were absent. The number of rib fractures was determined from the chest radiograph if not documented in the medical notes). |
Low
(Methods were clearly defined).
|
High
(relatively low number of patients with event/outcome). |
Low risk of bias |
Exclusie tabel
|
Author and year |
Reason for exclusion |
|
Buchholz (2022) |
No prognostic study. |
|
Casas (2016) |
The study investigated the prognostic value of the Thorax Trauma Severity Score. |
|
Chen (2014) |
The study compared outcomes for CTS-scores <5 or >5. |
|
Pressley (2012) |
The study compared outcomes for CTS-scores <5 or >5. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-05-2025
Beoordeeld op geldigheid : 28-05-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) en/of andere bron. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met thoracale letsels na trauma.
Werkgroep
- Dr. M.M.E. (Mathieu) Wijffels, traumachirurg, NVvH (voorzitter)
- Drs. P.J. (Pieter Jan) van Huijstee, longchirurg, NVvH (voorzitter)
- Dr. D. (Doeke) Boersma, chirurg, NVvH
- Dr. W.P. (Wietse) Zuidema, chirurg, NVvH
- Drs. W.W.L. (Wilson) Li, cardiothoracaal chirurg, NVT
- Drs. A.W.M. (Antoinette) Stolwijk, chirurg-intensivist, NVIC
- Drs. V.P.M. (Vincent) Rietveld, SEG, NVSHA
- Dr. M. (Monique) Brink, radioloog, NVvR
- Drs. S.A.S. (Sandra) van den Heuvel, anesthesioloog, NVA
- L. (Lydia) Köster MSc, fysiotherapeut, KNGF
Klankbordgroep
- T. (Thomas) Jonkergouw, adviseur patiëntbelang, Patiëntenfederatie Nederland
- Dr. H. (Hendrik-Jan) Dieker, cardioloog, NVVC
Met ondersteuning van
- Dr. R. (Romy) Zwarts – van de Putte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Mitchel) Griekspoor MSc., adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. E.R.L. (Evie) Verweg, junior adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Wijffels |
Traumachirurg, Erasmus MC |
Geen |
Onderzoeksbeurzen van ZonMw (prospectieve ribfixatie studie), Johnson en Johnson DePuy Synthes, OTC/Stryker, Stichting Coolsingel, KLS Martin (onderzoek naar ribplaten) |
Gedeeltelijke restrictie. Het werkgroeplid zal niet meebeslissen over ribfixatie en/of ribplaten. Wanneer deze onderwerpen worden besproken zal Monique Brink de vergadering voorzitten. |
|
Van Huijstee |
Algemeen Thoracaal en Trauma-Chirurg, Medische Specialistische Co-operatie HAGA Ziekenhuis, Den Haag
|
Voorzitter Ned. Ver. Voor Longchirurgie (Onbetaald), Bestuurslid Ned. Ver. Voor Heelkunde (Onbetaald), ATLS-instructeur bij stichting ALSG.
Executive Board Member of Chest Wall International Group (onbezoldigd) |
Ad Hoc, Betaald adviseurschap bij Distrimed voor ontwikkeling van nieuwe implantaten voor congenitale borstkasafwijkingen en onkostenvergoeding bij proctoring van collega-chirurgen in het gebruik van deze implantaten. |
Gedeeltelijk restrictie. Het werkgroeplid zal niet meebeslissen over ribfixatie en/of ribplaten. Wanneer deze onderwerpen worden besproken zal Monique Brink de vergadering voorzitten. |
|
Stolwijk |
Traumachirurg, intensivist, MUMC+ |
Lid klankbordgroep richtlijn abdominale letsels na trauma medisch Manager Acute Zorg Limburg (NAZL) |
Geen.
|
Geen restrictie |
|
Boersma |
Chirurg |
Geen |
Geen |
Geen restrictie |
|
Köster |
Fysiotherapeut projectleider/ adviseur Traumazorg bij het traumacentrum Zuid West Nederland. |
Geen. Penningmeester geworden van Stichting Netwerk Traumarevalidatie Nederland (onbetaald). |
Geen |
Geen restrictie |
|
Brink |
Radioloog, Radboud UMC |
Sprekersbureau Canon Medical Systems |
Research Grant Canon Medical Systems 2016-2020 |
Geen restrictie |
|
Rietveld |
SEH-arts, Rijnstate |
Partner en course director DEUS |
Ontwikkeling point-of-care echografie |
Geen restrictie |
|
Zuidema |
Traumachirurg, Amsterdam UMC |
Secretaris NVT, Lid Geschillencommisie Ziekenhuizen |
Unrestricted grant (Mendela) voor studie over digitale pneumothorax zuigsystemen |
Geen restrictie |
|
Van den Heuvel |
Anesthesioloog 50%, pijnspecialist 50%, Radboud UMC |
Geen |
Regiehouder pijn Radboudumc, Editor pijn.nl Co-secretaris World Institute of Pain Benelux, onbetaald Educational committee web-based learning World Institute of Pain, onbetaald |
Geen restrictie |
|
Li |
Cardiothoracaal chirurg, Radboudumc |
Secretaris NVT |
Geen |
Geen restrictie |
|
Jonkergouw |
Adviseur Patiëntbelang Patiëntenfederatie Nederland |
Vrijwilliger Diabetes Vereniging Nederland |
Geen |
Geen restrictie |
|
Dieker |
Cardioloog, Radboudumc |
Geen |
Geen |
Geen restrictie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname aan de schriftelijke knelpunteninventarisatie en een afgevaardigde patiëntenvereniging in de klankbordgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Module Het voorspellen van complicaties |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met thoracale letsels. Tevens zijn er knelpunten aangedragen door wetenschappelijke verenigingen via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nul effect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), duurzaamheid, aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: NVvH Thoracale letsels na trauma |
|
|
Uitgangsvraag: Welke factoren zijn voorspellend voor het optreden van complicaties bij patiënten met een bewezen thoraxtrauma/ wanneer kan een patiënt veilig naar huis na een bewezen thoraxtrauma? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 04-05-2023 |
|
Periode: >2000 |
Talen: Geen beperking |
|
Literatuurspecialist: Linda Niesink |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
→ Voor deze vraag is gezocht op de elementen thorax trauma (in het blauw) en een prognostisch zoekfilter (in het groen).
→ Alle genoemde sleutelartikelen van Martinez Casas (2016), Battle (2013), Giamello (2023), Battle (2014), Hardin (2019), Brasel (2006), Bergeron (2003) en Moon (2017) zitten in de zoekopbrengst.
→ Resultaten staan in Rayyan. |
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 04-05-2023 met relevante zoektermen gezocht vanaf 2000 naar systematische reviews, RCT’s en observationele studiedesigns over predictiemodellen voor patiënten met een thorax trauma. De literatuurzoekactie leverde 1.183 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
19 |
35 |
36 |
|
RCTs |
154 |
185 |
256 |
|
Observationele studies |
518 |
725 |
891 |
|
Totaal |
691 |
945 |
1183 |
Zoekstrategie
|
Database |
Zoektermen |
|||||||||||||||||||||||||||||||||
|
Embase
|
|
|||||||||||||||||||||||||||||||||
|
Medline (OVID)
|
1 exp *Thoracic Injuries/ or "Sternum"/in or (((blunt OR severity) adj3 (chest OR thorax OR thoracic OR cardiac OR pericardial) adj3 (trauma* OR injur*)).ti,ab,kf.) OR ((pulmonary adj2 (contusion* OR laceration*)).ti,ab,kf.) OR 'broken rib*'.ti,ab,kf. OR 'costa fracture*'.ti,ab,kf. OR 'costal fracture*'.ti,ab,kf. OR 'fractured rib*'.ti,ab,kf. OR 'fractured ribcage'.ti,ab,kf. OR 'rib cage fracture'.ti,ab,kf. OR 'rib fracture*'.ti,ab,kf. OR 'ribcage fracture*'.ti,ab,kf. (28767) 2 Area Under Curve/ or exp Forecasting/ or "Predictive Value of Tests"/ or exp Multivariate Analysis/ or exp Regression Analysis/ or exp Models, Statistical/ or area under the curve.ti,ab,kf. or brier score*.ti,ab,kf. or c statistic*.ti,ab,kf. or computer prediction.ti,ab,kf. or decision curve anal*.ti,ab,kf. or (net reclassification adj2 (improvement or index)).ti,ab,kf. or ((predict* or statistical*) adj3 (model* or validity or value)).ti,ab,kf. or proportional hazards model*.ti,ab,kf. or r square*.ti,ab,kf. or regression.ti,ab,kf. or predict*.ti. or multivaria*.ti,ab,kf. (2395950) 3 1 and 2 (1666) 4 limit 3 to yr="2000 -Current" (1509) 5 4 not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) (1417) 6 meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. (665635) 7 exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. (2583455) 8 Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) (5414257) 9 5 and 6 (35) – SRs 10 (5 and 7) not 9 (185) - RCTs 11 (5 and 8) not (9 or 10) (725) – observationele studies 12 9 or 10 or 11 (945) |
