Signaleren afwijkend voedingsgedrag
Uitgangsvraag
Welke afkappunten worden gebruikt om een afwijkende voedingstoestand te signaleren?
Aanbeveling
Verwijzing naar de kinderarts van kinderen jonger dan 6 jaar met afwijkend voedingsgedrag hoeft niet plaats te vinden indien voldaan wordt aan alle onderstaande criteria:
1. Langdurige voedselweigering (> 1 maand)
2. a. Afwezigheid van duidelijke somatische ziekten die kunnen leiden tot voedselweigering of gebrek aan verbetering van eetgedrag na medische behandeling van een somatische ziekte
b. Afwezigheid van een alarmsymptoom
3. Begin van de klachten voor de leeftijd van 2 jaar, presentatie < 6 jaar
4. Aanwezigheid van ten minste één van de volgende symptomen:
a. Pathologisch/disfunctioneel voeden (’s nachts voeden (bij leeftijd > 6 maanden), ‘stalken’ met voeden, dwingend voeden, mechanisch voeden, afleidingsmanoeuvres bij het voeden)
b. Anticiperend kokhalzen
Voor kinderen met afwijkend voedingsgedrag vanaf de leeftijd van 6 jaar zijn er geen specifieke verwijzingscriteria maar wordt aanbevolen om kinderen naar de kinderarts door te verwijzen indien er een combinatie is van:
- anamnestische alarmsymptomen
- afwijkende groei of voedingstoestand
- afwijkingen bij het lichamelijk onderzoek
Voor oudere kinderen en adolescenten waarbij er verdenking bestaat op de typische eetstoornissen anorexia nervosa en boulimia nervosa wordt verwezen naar de DSM IV criteria en de richtlijn eetstoornissen uit 2006. Het wordt aanbevolen dat de huisarts of jeugdgezondheidsarts bij twijfel over de diagnose eetstoornis bij lichamelijke oorzaak van de klachten dient te verwijzen naar de kinderarts.
Bij een kind met een afwijkend voedingsgedrag dient anamnestisch naar de volgende alarmsymptomen gevraagd te worden: orale en mondmotorische afwijkingen zoals ongecoördineerd slikken, dysfagie, odynofagie (=pijn bij slikken), spugen, recidiverende KNO- en luchtweg problematiek, afwijkende defaecatie zoals diarree, obstipatie, ontkleurde ontlasting, bloedbijmenging en neurologische symptomen.
Bij kinderen met een afwijkend voedingsgedrag dient bij het lichamelijk onderzoek in het bijzonder gelet te worden op: de groei en voedingstoestand, micro-/hydrocefalie, dysmorfieën, dyspnoe, stridor, cardiale souffle, huidafwijkingen/eczeem, bleekzien, hepato-/splenomegalie, hypotonie, neurologische symptomen en een ontwikkelingsachterstand.
Overwegingen
De symptomen die gerelateerd zijn aan afwijkend voedingsgedrag die kunnen wijzen op somatische problematiek worden in de volgende modules van de richtlijn beschreven. Deze worden onderverdeeld in het beoordelen van de
- anamnestische alarmsymptomen
- de groei en voedingstoestand
- afwijkingen bij lichamelijk onderzoek
Anamnestische alarmsymptomen zijn: orale en mondmotorische afwijkingen zoals ongecoördineerd slikken, dysfagie, odynofagie (=pijn bij slikken), spugen, recidiverende KNO- en luchtweg problematiek, afwijkende defecatie zoals diarree, obstipatie, ontkleurde ontlasting, bloedbijmenging, en neurologische symptomen.
Afwijkingen bij lichamelijk onderzoek zijn: micro-/hydrocefalie, dysmorfieën, dyspnoe, stridor, cardiale souffle, huidafwijkingen/eczeem/bleekzien, hepato-/splenomegalie, hypotonie, neurologische symptomen en een ontwikkelingsachterstand.
Symptomen gerelateerd aan afwijkend voedingsgedrag die juist kunnen wijzen op niet-somatische problematiek worden in de modules ‘afwijkend voedingsgedrag’ beschreven.
Onderbouwing
Onderzoek naar de oorzaak van afwijkend voedingsgedrag is gecompliceerd door de verschillende factoren die een rol kunnen spelen. Specifieke cognitieve of psychologische factoren spelen een rol als mede de omgeving van het kind. Bij meer dan 80% van de patiënten met voedingsproblemen die verwezen worden naar een kinderarts speelt gedrag een significante rol (Bryant-Waugh 2010). Daarnaast kan een voedingsprobleem ontstaan door een onderliggende somatische oorzaak. Verschillende studies suggereren dat een somatische oorzaak bij 16-30% van de kinderen met een voedingsprobleem worden gevonden (Bryant-Waugh 2010). Veel symptomen als uiting van afwijkend voedingsgedrag komen frequent voor, kunnen aspecifiek zijn of worden bij veel onderliggende ziektes gezien.
Burklow et al (1998) stelt dat afwijkend voedingsgedrag een gevolg kan zijn van wat hij noemt een “Complex Bio-Behavioral Pediatric Feeding Disorder” waarin 5 categorieën te onderscheiden zijn:
- Structurele afwijkingen
- Neurologische condities
- Gedrags- en psychosociale problemen
- Cardio-respiratoire problemen
- Metabole dysfunctie
In een groep van 103 kinderen van 4 maanden tot 17 jaar die waren verwezen in verband met een beperkte orale inname van voedsel en groeiproblemen vond hij de volgende combinatie van bovenstaande categorieën: 30% structureel/neurologisch/gedrag, 27% neurologisch en gedrag, 12% gedrag, 9% structureel en gedrag en 8% structureel en neurologisch. Alles bij elkaar werden gedragsproblemen het meest frequent gerapporteerd (85%) vergeleken met neurologische condities (73%), structurele afwijkingen (57%), cardio-respiratoire afwijkingen (7%) of metabole dysfunctie (5%).
Om een onderscheid te kunnen maken tussen somatische en niet-somatische oorzaken van afwijkend voedingsgedrag zijn er een aantal classificaties ontwikkeld zowel door de kinderarts MDL (Wolfson-critertia: Levy 2009) als door de kinder- en jeugdpsychiatrie (DC 0-3-R criteria (Chatoor 2002) DSM-IV-R criteria (Bryant-Waught 2010).
|
Niveau 3 |
Het lijkt waarschijnlijk dat afwijkend voedingsgedrag frequent wordt veroorzaakt door een complex van factoren die zowel somatisch als niet-somatisch kunnen zijn.
C Burklow 1998 |
|
Niveau 3 |
Het lijkt waarschijnlijk dat voor het vaststellen van afwijkend voedingsgedrag de Wolfson-criteria beter differentieert dan de DC:0-3-R en DSM-IV-R voor het verschil tussen een somatische en niet-somatische oorzaak.
B Levine 2011 |
Bespreking van de classificaties
De DSM-IV-R criteria benadrukken dat er sprake is van afwijkend voedingsgedrag zonder somatische oorzaak indien de symptomen langer dan 1 maand duren waarbij er gewichtsverlies of een significant tekort is aan gewichtstoename die niet gerelateerd is aan een onderliggende medische ziekte of mentale afwijking met het begin van de problemen voor de leeftijd van 6 jaar.
De DC:0-3-R criteria onderscheiden eetstoornissen bij jonge kinderen in een regulatiestoornis, relationele voedingsstoornis (interactie ouder-kind), sensorische voedingsstoornis, posttraumatische voedingsstoornis, eetstoornis als gevolg van een somatische aandoening en infantiele anorexia. Infantiele anorexia wordt gedefinieerd als kinderen die langdurig zonder duidelijke oorzaak een adequate hoeveelheid voeding weigeren, waardoor een groeiachterstand ontstaat.
De meest praktische en eenvoudige screeningsmethode op eetstoornissen zijn de Wolfsoncriteria. Levine et al. (2011) tonen aan dat de Wolfson criteria (Levy et al, 2009) eetstoornissen goed kunnen identificeren, accurater en eenvoudiger toepasbaar zijn dan de DC: 0-3-R en de DSM-IV-R en onderscheid maken tussen somatische en niet somatische oorzaken van voedselweigering. Deze duidelijke criteria verminderen het ‘dokters-delay’. Belangrijk is ook dat het criterium gewichtsverlies niet is opgenomen. Hierdoor worden kinderen die hun gewicht behouden door niet leeftijdsadequaat eetgedrag of pathologisch voedingsgedrag van de ouders of verzorgers ook herkend worden als kinderen met een eetstoornis.
Wolfson criteria:
1. Langdurige voedselweigering (>1 maand)
2. Afwezigheid van duidelijke somatische ziekten die kunnen leiden tot voedselweigering of gebrek aan verbetering van het eetgedrag na medische behandeling van een somatische ziekte
3. Begin van de klachten voor de leeftijd 2 jaar, presentatie < 6 jaar
4. Aanwezigheid van ten minste één van de volgende symptomen:
a. Pathologisch/disfunctioneel voeden (’s nachts voeden (bij leeftijd > 6 maanden), ‘stalken’ met voeden, dwingend voeden, mechanisch voeden, afleidingsmanoeuvres bij het voeden)
b. Anticiperend kokhalzen
Indien aan alle criteria wordt voldaan is er naar alle waarschijnlijkheid sprake van een eetstoornis met niet-somatische oorzaak.
Criteria per leeftijdscategorie
Kinderen 0-6 jaar
Aangaande het 2e item van de Wolfson criteria, afwezigheid van duidelijk somatische ziekte die kan leiden tot voedselweigering of gebrek aan verbetering op medische behandeling van een somatische ziekte, kan dit naar mening van de werkgroep ingevuld worden door te screenen op alarmsymptomen. De werkgroep heeft derhalve de Wolfson criteria aangepast en in de richtlijn wordt verder gesproken van de term gebaseerd op Wolfson-criteria. Indien er geen alarmsymptomen zijn dan hoeft er ook geen doorverwijzing plaats te vinden naar de kinderarts bij een kind jonger dan 6 jaar.
Kinderen > 6 jaar
Wat betreft de criteria voor eetstoornissen voor kinderen in de basisschoolleeftijd zijn er criteria ontwikkeld door specialisten van Great Ormond Street Hospital in Londen. Deze criteria worden gebruikt in het kenniscentrum kinder- en jeugdpsychiatrie.
- Selectieve eters consumeren slechts enkele producten. De stoornis heeft niet zozeer invloed op de ontwikkeling, maar wel op het sociaal functioneren van de kinderen.
- Restrictieve eters hebben een normaal gevarieerd eetpatroon, maar geven weinig om eten (dit zegt niets over de kwantiteit en inname van voedsel die veelal verlaagd is). Deze kinderen bevinden zich onderaan de groeicurven.
- Kinderen met emotioneel bepaalde eetproblemen eten te veel of te weinig uit spanning of onbehagen, als gevolg van angstgevoelens na een traumatische ervaring. Voedselweigering als gevolg van een verstoorde interactie valt hier ook onder.
- Kinderen met een compleet of atypisch beeld van anorexia of boulimia nervosa. Deze kinderen zijn in tegenstelling tot de andere drie categorieën erg gericht op hun voeding en lichaam.
Wat betreft de somatische problematiek zijn er voor kinderen vanaf de leeftijd van 6 jaar geen specifieke criteria ontwikkeld. Voor kinderen vanaf de leeftijd van 6 jaar zijn naar mening van de werkgroep de criteria voor doorverwijzing naar de kinderarts gebaseerd op een combinatie van:
- anamnestische alarmsymptomen
- afwijkende voedingstoestand
- afwijkingen bij het lichamelijk onderzoek
Deze items worden in de volgende modules van de richtlijn besproken.
Oudere kinderen en adolescenten
Bij oudere kinderen en adolescenten worden de typische eetstoornissen anorexia nervosa en boulimia nervosa gekarakteriseerd door dezelfde basis van psychopathologie: een pre-occupatie met eten, gewicht en lichaamsvorm. Voor de diagnose anorexia nervosa worden de DSM-IV-R criteria gebruikt. In de in 2006 verschenen multidisciplinaire richtlijn eetstoornissen wordt uitgebreid ingegaan op de risiciofactoren en diagnostiek van de diverse eetstoornissen (CBO 2006).
In deze richtlijn wordt gesteld dat voor vroegtijdige onderkenning van eetstoornissen het gewenst is dat hulpverleners in de eerste lijn niet alleen alert zijn op de symptomen en diagnostische criteria voor eetstoornissen, maar ook op bijkomende kenmerken en symptomen.
Een op eetstoornis gerichte anamnese dient de volgende elementen dient te bevatten:
- eetpatroon en braken
- lichaamsbeeld van de patiënt zelf
- stemming van de patiënt
- minimum- en maximumgewicht in de laatste jaren
- andere klachten, in het bijzonder betreffende de menstruatie
- gebruik van medicijnen, laxeermiddelen, diuretica, slankpillen
- gebruik van alcohol en/of drugs
- lichaamsbeweging/sporten
- familieanamnese
- compensatoir gedrag zoals hyperactiviteit, braken en purgeren
Opgemerkt dient te worden dat jonge kinderen zich vaak niet presenteren met hele evidente anorectische cognities.
Vanuit de multidisciplinaire richtlijn Eetstoornissen van CBO/Trimbos-instituut uit 2006 is onderstaand diagram opgenomen wat betreft indicaties voor acute beoordeling bij verdenking anorexia nervosa. Naast de genoemde symptomen voor acute beoordeling kan bij lichamelijk onderzoek bij BMI < 16-17 kg/m2 lanugo beharing zichtbaar zijn en dient verder gekeken te worden naar ander huidafwijkingen, xerosis, vergrote parotiden en tekenen van purgeren zoals het teken van Russell (dit zijn eeltige plekken aan de handrug van de dominante hand die ontstaan door herhaalde lichte beschadiging van de huid als gevolg van het in de mond steken van de vingers om braken op te wekken).
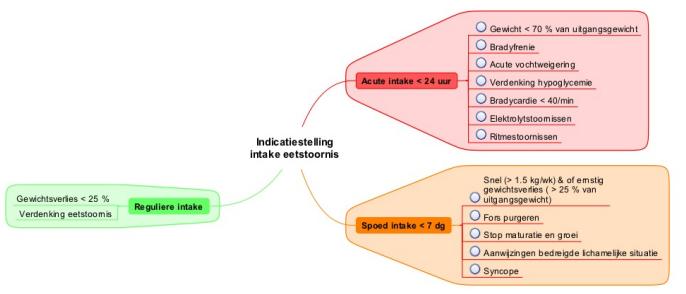
Tevens wordt in deze CBO/Trimbos-instituut richtlijn eetstoornissen 2006 gesteld dat de huisarts bij twijfel over de diagnose eetstoornis dient te verwijzen naar de 2e lijn.
Momenteel werkt het landelijk kenniscentrum kind- en jeugdpsychiatrie aan een nieuwe richtlijn eetstoornissen bij kinderen in de leeftijd 0-10 jaar en voor adolescenten (http://www.kenniscentrum-kjp.nl, 2012). Gezien de specifieke diagnostiek en behandeling wordt verwezen naar deze richtlijn en de CBO richtlijn uit 2006.
Bij een lichamelijke oorzaak van de klachten dient verwezen te worden naar de kinderarts, internist, of gynaecoloog. Bij een psychiatrische oorzaak van de klachten dient verwijzing plaats te vinden naar de GGZ (met voorkeur voor expertise op het gebied van eetstoornissen).
Wanneer de typische psychologische kernsymptomen aanwezig zijn, is de diagnose duidelijk. Anorexia nervosa en boulimia nervosa kunnen gecombineerd voorkomen met een somatische aandoening als diabetes mellitus type I, coeliakie en schildklierziekten. Bij een atypisch klinisch beeld dient gedacht te worden aan onder meer hyperthyriodie, chronische infecties, maligniteit, ziekte van Crohn, malabsorptie, ziekte van Addison, diabetes mellitus, cardiale aandoeningen en verwaarlozing.
- Allen KJ, Heine RG. Eosinophilic esophagitis: trials and tribulations. J Clin Gastroenterol. 2011 Aug;45(7):574-82.
- Arvedson JC. Assessment of pediatric dysphagia and feeding disorders: clinical and instrumental approaches. Dev Disabil Res Rev. 2008;14(2):118-27.
- Berlin KS, Lobato DJ, Pinkos B, Cerezo CS, LeLeiko NS. Patterns of medical and developmental comorbidities among children presenting with feeding problems: a latent class analysis. J Dev Behav Pediatr. 2011 Jan;32(1):41-7.
- Bonuck K, Parikh S, Bassila M. Growth failure and sleep disordered breathing: a review of the literature. Int J Pediatr Otorhinolaryngol. 2006 May;70(5):769-78.
- Brouilette R, Hanson D, David R, Klemka L, Szatkowski A, Fernbach S, et al. A diagnostic approach to suspected obstructive sleep apnea in children. J Pediatr. 1984 Jul;105(1):10-4.
- Bryant-Waugh R, Markham L, Kreipe RE, Walsh BT. Feeding and eating disorders in childhood. Int J Eat Disord. 2010 Mar;43(2):98-111.
- Bulk-Bunschoten AMW, Renders CM, van Leerdam FJM, HiraSing RA. Signaleringsprotocol Overgewicht in de Jeugdgezondheidszorg, VUmc Amsterdam, 2004.
- Burklow KA, Phelps AN, Schultz JR, McConnell K, Rudolph C. Classifying complex pediatric feeding disorders. J Pediatr Gastroenterol Nutr. 1998 Aug;27(2):143-7.
- CBO. Multidisciplinaire richtlijn eetstoornissen. Diagnostiek en behandeling van eetstoornissen: Trimbos- instituut, 2006.
- Chatoor I. Feeding disorders in infants and toddlers: diagnosis and treatment. Child Adolesc Psychiatr Clin N Am. 2002 Apr;11(2):163-83.
- Clark M, Harris R, Jolleff N, Price K, Neville BG. Worster-Drought syndrome: poorly recognized despite severe and persistent difficulties with feeding and speech. Dev Med Child Neurol. 2010 Jan;52(1):27-32.
- Cremers MJ, van der Tweel I, Boersma B, Wit JM, Zonderland M. Growth curves of Dutch children with Down's syndrome. J Intellect Disabil Res. 1996 Oct;40 ( Pt 5):412-20.
- Dabritz J, Domagk D, Monninger M, Foell D. Achalasia mistaken as eating disorders: report of two children and review of the literature. Eur J Gastroenterol Hepatol. 2010 Jul;22(7):775-8.
- Daniel M, Kleis L, Cemeroglu AP. Etiology of failure to thrive in infants and toddlers referred to a pediatric endocrinology outpatient clinic. Clin Pediatr (Phila). 2008 Oct;47(8):762-5.
- Davidson M, Waserman R. The iritable colon of childhood (chronic nonspecific diarrhea syndrome). J Pediatr. 1966 Dec;69(6):1027-38.
- de Bruijn AJM, Kroesbergen HT. Project psychosociale preventie JGZ 4-19 jarigen: eindrapport. Breda: GGD Stadsgewest Breda 1997.
- Detsky AS, McLaughlin JR, Baker JP, Johnston N, Whittaker S, Mendelson RA, et al. What is subjective global assessment of nutritional status? JPEN J Parenter Enteral Nutr. 1987 Jan-Feb;11(1):8-13.
- Dogan Y, Erkan T, Yalvac S, Altay S, Cokugras FC, Aydin A, et al. Nutritional status of patients hospitalized in pediatric clinic. Turk J Gastroenterol. 2005 Dec;16(4):212-6.
- Erkin G, Culha C, Ozel S, Kirbiyik EG. Feeding and gastrointestinal problems in children with cerebral palsy. Int J Rehabil Res. 2010 Sep;33(3):218-24.
- Falconer J. GOR and GORD in infants. Community Pract. 2009 Oct;82(10):42-3.
- Ficicioglu C, An Haack K. Failure to thrive: when to suspect inborn errors of metabolism. Pediatrics. 2009 Sep;124(3):972-9.
- Field D, Garland M, Williams K. Correlates of specific childhood feeding problems. J Paediatr Child Health. 2003 May-Jun;39(4):299-304.
- Frydrych AM, Davies GR, McDermott BM. Eating disorders and oral health: a review of the literature. Aust Dent J. 2005 Mar;50(1):6-15; quiz 56.
- Gezondheidsraad. Voedingsnormen energie, eiwitten, vetten en verteerbare koolhydraten. Den Haag: Gezondheidsraad; 2001.
- Groner ML, Wollmann HA, Schulz V, Rauke MB. Reference values for height and weight in Prader-Willi syndrome based on 315 patients. Horm Res 1997;46 (suppl.2):54.40.
- Haas AM, Maune NC. Clinical presentation of feeding dysfunction in children with eosinophilic gastrointestinal disease. Immunol Allergy Clin North Am. 2009 Feb;29(1):65-75, ix.
- Hager ER, McGill AE, Black MM. Development and validation of a toddler silhouette scale. Obesity (Silver Spring). 2010 Feb;18(2):397-401.
- Heerdink-Obenhuijsen N, Klein Ikkink AJ, Boere-Boonekamp MM, De Vries L, Graat-Wolff C, Grote FK, et al. Landelijke Eerstelijns Samenwerkings Afspraak Kleine lichaamslengte bij kinderen. Huisarts Wet. 2011;54(2):S1-S4.
- Heerdink-Obenhuijsen N, van Dommelen P, Kamphuis M, van Buuren S, Coenen-van Vroonhoven EjC, Verkerk PH. JGZ-richtlijn Signalering van en verwijscriteria bij kleine lichaamslengte. Bilthoven: RIVM2010 Contract No.: 295001011/2010.
- Hemmi MH, Wolke D, Schneider S. Associations between problems with crying, sleeping and/or feeding in infancy and long-term behavioural outcomes in childhood: a meta-analysis. Arch Dis Child. 2011 Jul;96(7):622-9.
- Hendrikse WH, Reilly JJ, Weaver LT. Malnutrition in a children's hospital. Clin Nutr. 1997;16:13-8.
- Hulst J, Joosten K, Zimmermann L, Hop W, van Buuren S, Buller H, et al. Malnutrition in critically ill children: from admission to 6 months after discharge. Clin Nutr. 2004 Apr;23(2):223-32.
- Hulst JM, Zwart H, Hop WC, Joosten KFM. Dutch national survey to test the STRONGkids nutritional risk screening tool in hospitalized children. Clin Nutr. 2010 Feb;29(1):106-111. Epub 2009 Aug 13.
- Hyman PE, Milla PJ, Benninga MA, Davidson GP, Fleisher DF, Taminiau J. Childhood functional gastrointestinal disorders: neonate/toddler. Gastroenterology. 2006 Apr;130(5):1519-26.
- Jacobi C, Hayward C, de Zwaan M, Kraemer HC, Agras WS. Coming to terms with risk factors for eating disorders: application of risk terminology and suggestions for a general taxonomy. Psychol Bull. 2004 Jan;130(1):19-65.
- Landelijk kenniscentrum kinder- en jeugdpsychiatrie. Richtlijn Eetstoornissen bij jonge kinderen (0-10 jaar), 2011, in ontwikkeling.
- Jonkman A, Hermanns J. De psychologie van de sociaal-emotionele ontwikkeling in de eerste levensjaren. Bijblijven. 1997;13(1):83-90.
- Joosten KF, Hulst JM. Prevalence of malnutrition in pediatric hospital patients. Curr Opin Pediatr. 2008 Oct;20(5):590-6.
- Joosten KF, Hulst JM. Malnutrition in pediatric hospital patients: current issues. Nutrition. 2011 Feb;27(2):133-7.
- Joosten KF, Zwart H, Hop WC, Hulst JM. National malnutrition screening days in hospitalised children in The Netherlands. Arch Dis Child. 2010 Feb;95(2):141-5.
- Kamphuis M, Obenhuijsen NH, van Dommelen P, van Buuren S, Verkerk PH. JGZ-richtlijn: 'Signalering van en verwijscriteria bij kleine lichaamslengte'. Ned Tijdschr Geneeskd. 2010;154(18):A2366.
- Kindermann A, Kneepkens CMF. Voedings- en eetproblemen bij jonge kinderen. Praktische Pediatrie. 2010(3):174-9.
- Kliegman R. Nelson Essential of Pediatrics: Elsevier Saunders; 2006.
- Kneepkens CM, Hoekstra JH. Peuterdiarree. Ned Tijdschr Geneeskd. 1996 Oct 12;140(41):2026-8.
- Kneepkens CMF. Werkboek Kindergastro-enterologie. tweede druk ed. Kneepkens CMF, Taminiau JAJM, Polman HA, editors. Amsterdam: VU Uitgeverij; 2002.
- Kotler LA, Cohen P, Davies M, Pine DS, Walsh BT. Longitudinal relationships between childhood, adolescent, and adult eating disorders. J Am Acad Child Adolesc Psychiatry. 2001 Dec;40(12):1434-40.
- Levine A, Bachar L, Tsangen Z, Mizrachi A, Levy A, Dalal I, et al. Screening criteria for diagnosis of infantile feeding disorders as a cause of poor feeding or food refusal. J Pediatr Gastroenterol Nutr. 2011 May;52(5):563-8.
- Levy Y, Levy A, Zangen T, Kornfeld L, Dalal I, Samuel E, et al. Diagnostic clues for identification of nonorganic vs organic causes of food refusal and poor feeding. J Pediatr Gastroenterol Nutr. 2009 Mar;48(3):355-62.
- Malakounides G, Thomas L, Lakhoo K. Just another case of diarrhea and vomiting? Pediatr Emerg Care. 2009 Jun;25(6):407-10.
- Manikam R, Perman JA. Pediatric feeding disorders. J Clin Gastroenterol. 2000 Jan;30(1):34-46.
- Marchi M, Cohen P. Early childhood eating behaviors and adolescent eating disorders. J Am Acad Child Adolesc Psychiatry. 1990 Jan;29(1):112-7.
- Arteletti O, Caldari D, Guimber D, Mention K, Michaud L, Gottrand F. Malnutrition screening in hospitalized children: influence of the hospital unit on its management. Arch Pediatr. 2005 Aug;12(8):1226-31.
- Martucciello G, Lombardi L, Savasta S, Gibbons RJ. Gastrointestinal phenotype of ATR-X syndrome. Am J Med Genet A. 2006 Jun 1;140(11):1172-6.
- Mathisen B, Worrall L, Masel J, Wall C, Shepherd RW. Feeding problems in infants with gastro-oesophageal reflux disease: a controlled study. J Paediatr Child Health. 1999 Apr;35(2):163-9.
- Meer K de, Taminiau JAJM. Definitie van ondervoeding. In: Taminiau JAJM, Meer Kd, Kneepkens CMF, Verheul-Koot MA, Lafeber HN, editors. Werkboek enterale voeding bij kinderen. Amsterdam: VU Boekhandel/Uitgeverij BV.; 1997. p. 9-18.
- Messer A, de Vos I, Wolters W. Eetproblemen bij kinderen en adolescenten. Baarn: Ambo; 1994.
- Miller CK. Updates on pediatric feeding and swallowing problems. Curr Opin Otolaryngol Head Neck Surg. 2009 Jun;17(3):194-9.
- Miller-Loncar C, Bigsby R, High P, Wallach M, Lester B. Infant colic and feeding difficulties. Arch Dis Child. 2004 Oct;89(10):908-12.
- Moy RJD, Smallman S, Booth IW. Malnutrition in a UK children hospital. J Hum Nutr Diet. 1990;3:93-100.
- NVK Richtlijn gastro-oesofageale reflux(ziekte) bij kinderen van 0-18 jaar (concept), 2012.
- NVK, NHG. Richtlijn Obstipatie bij kinderen 0-18 jaar. Utrecht: CBO, 2009.
- NVK richtlijn Richtlijn Diagnostiek van Koemelkallergie in Nederland (concept), 2012.
- Olsen EM, Petersen J, Skovgaard AM, Weile B, Jorgensen T, Wright CM. Failure to thrive: the prevalence and concurrence of anthropometric criteria in a general infant population. Arch Dis Child. 2007 Feb;92(2):109-14.
- Oostdijk W, Grote FK, Wit JM, de Muinck Keizer-Schrama SMPF. NVK Richtlijn Kleine Lengte. Leiden 2008.
- Pankau R, Partsch CJ, Gosch A, Oppermann HC, Wessel A. Statural growth in Williams-Beuren syndrome. Eur J Pediatr. 1992 Oct;151(10):751-5.
- Park RJ, Senior R, Stein A. The offspring of mothers with eating disorders. Eur Child Adolesc Psychiatry. 2003;12 Suppl 1:I110-19.
- Ranke MB, Heidemann P, Knupfer C, Enders H, Schmaltz AA, Bierich JR. Noonan syndrome: growth and clinical manifestations in 144 cases. Eur J Pediatr. 1988 Dec;148(3):220-7.
- Reba-Harrelson L, Von Holle A, Hamer RM, Torgersen L, Reichborn-Kjennerud T, Bulik CM. Patterns of maternal feeding and child eating associated with eating disorders in the Norwegian Mother and Cild Cohort Study (MoBa). Eat Behav. 2010;11(1):54-61.
- Rexwinkel M, Schmeets M, Pannevis C, Derkx B. Handboek Infant Mental Health, 2011, 1e druk, Van Gorcum uitgeverij..
- Richards CA, Andrews PL. Food refusal: a sign of nausea? J Pediatr Gastroenterol Nutr. 2004 Feb;38(2):227-8.
- Rocha GA, Rocha EJ, Martins CV. The effects of hospitalization on the nutritional status of children. J Pediatr (Rio J). 2006 Jan-Feb;82(1):70-4.
- Rongen-Westerlaken C, Corel L, van den Broeck J, Massa G, Karlberg J, Albertsson-Wikland K, et al. Reference values for height, height velocity and weight in Turner's syndrome. Swedish Study Group for GH treatment. Acta Paediatr. 1997 Sep;86(9):937-42.
- Schönbeck Y, Talma H, van Dommelen P, Bakker B, Buitendijk SE, Hirasing RA, et al. Increase in prevalence of overweight in Dutch children and adolescents: a comparison of nationwide growth studies in 1980, 1997 and 2009. PLoS One. 2011;6(11):e27608.
- Schwarz SM, Corredor J, Fisher-Medina J, Cohen J, Rabinowitz S. Diagnosis and treatment of feeding disorders in children with developmental disabilities. Pediatrics. 2001 Sep;108(3):671-6.
- Secker DJ, Jeejeebhoy KN. Subjective Global Nutritional Assessment for children. Am J Clin Nutr. 2007 Apr;85(4):1083-9.
- Semeniuk, J., Kaczmarski, M. (2008). Acid gastroesophageal reflux and intensity of symptoms in children with gastroesophageal reflux disease. Comparison of primary gastroesophageal reflux and gastroesophageal reflux secondary to food allergy. Adv Med Sci 53;2;293-9.
- Schwarz SM, Corredor J, Fisher-Medina J, Cohen J, Rabinowitz S. Diagnosis and treatment of feeding disorders in children with developmental disabilities. Pediatrics. 2001 Sep;108(3):671-6.
- Sylvestre LC, Fonseca KP, Stinghen AE, Pereira AM, Meneses RP, Pecoits-Filho R. The malnutrition and inflammation axis in pediatric patients with chronic kidney disease. Pediatr Nephrol. 2007 Jun;22(6):864-73.
- Swenne I, Thurfjell B. Clinical onset and diagnosis of eating disorders in premenarcheal girls is preceded by inadequate weight gain and growth retardation.Acta Pediatrica: 92:1133-1137, 2003
- Tolboom JJM. Classificatie en epidemiologie van voedingsproblemen. In: Seys DM, Rensen JHM, Obbink MHJ, editors. Behandelingsstratergieen bij jonge kinderen met voedings- en eetproblemen. Houten/Diegem: Bohn Stafleu Van Loghum; 2000.
- Van Buuren S, Bonnemaijer-Kerckhoffs DJ, Grote FK, Wit JM, Verkerk PH. Many referrals under Dutch short stature guidelines. Arch Dis Child. 2004 Apr;89(4):351-2.
- Van den Elzen APM, Sibbles BJ, Nieuwenhuis EES. Failure tot thrive: van symptoom naar diagnose. Praktische Pediatrie. 2007;2:48-52.
- Venugopalan P, Akinbami FO, Al-Hinai KM, Agarwal AK. Malnutrition in children with congenital heart defects. Saudi Med J. 2001 Nov;22(11):964-7.
- WHO. Management of servere malnutrition: a manual for physicians and other senior health workers. Geneva: World Health Organization, 1999.
- Walkers Pediatric Gastrointestinal Disease. Kleinman RE, Sanderson IR, Goulet O, Sherman PM, Mieli-Vergani G, Shneider BL (Ed), 2008.
- Wilne S, Collier J, Kennedy C, Koller K, Grundy R, Walker D. Presentation of childhood CNS tumours: a systematic review and meta-analysis. Lancet Oncol. 2007 Aug;8(8):685-95.
- Wilne S, Koller K, Collier J, Kennedy C, Grundy R, Walker D. The diagnosis of brain tumours in children: a guideline to assist healthcare professionals in the assessment of children who may have a brain tumour. Arch Dis Child. 2010 Jul;95(7):534-9.
- Wollmann HA, Kirchner T, Enders H, Preece MA, Ranke MB. Growth and symptoms in Silver-Russell syndrome: review on the basis of 386 patients. Eur J Pediatr. 1995 Dec;154(12):958-68.
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-07-2014
Beoordeeld op geldigheid : 21-06-2012
In 2013 zal herziening van de richtlijn plaatsvinden door de Nederlandse Vereniging voor Kindergeneeskunde na de commentaarronde en implementatie van de richtlijn Voeding en eetgedrag (0-23 jaar) van de JGZ waarmee de huidige richtlijn verband houdt. Voor de (gedeeltelijke) herziening zal zo nodig een nieuwe werkgroep geïnstalleerd worden. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
Doel en doelgroep
Doel
Met de richtlijn beoogt de Nederlandse Vereniging voor Kindergeneeskunde (NVK) gezamenlijk met de richtlijn “Voeding en eetgedrag (0-23 jaar)” die in hetzelfde traject wordt ontwikkeld door de JGZ te komen tot uniforme verwijzingscriteria en behandelcriteria voor kinderen met afwijkend voedingsgedrag en/of eetstoornissen. Tevens wordt er gerefereerd aan de richtlijn “Eetstoornis bij jonge kinderen” die momenteel door de kinder- en jeugdpsychiatrie wordt ontwikkeld en de CBO richtlijn ”eetstoornissen” uit 2006. De richtlijn van de NVK richt zich met name op indicatoren die gebruikt kunnen worden om vast te stellen wanneer er sprake is van afwijkend voedingsgedrag en doorverwijzing dient plaats te vinden naar de kinderarts. Daarnaast zullen alarmsymptomen worden benoemd voor afwijkend voedingsgedrag die kunnen wijzen op somatische problematiek en waaraan differentiaal diagnostisch gedacht moet worden.
De richtlijn richt zich op vroege diagnostiek van somatische oorzaken van afwijkend voedingsgedrag, waarbij tijdige behandeling gezondheidswinst oplevert voor het kind en tevens kan leiden tot gezond voedingsgedrag. De richtlijn richt zich niet op afwijkend voedingsgedrag in de vorm van overvoeden, het ontstaan van overgewicht, en de somatische oorzaken hiervan. Hiervoor wordt verwezen naar het Signaleringsprotocol Overgewicht in de Jeugdgezondheidszorg (Bulk-Bunschoten 2004).
Doelgroep
0e- en 1e-lijns gezondheidszorg.
Samenstelling werkgroep
Werkgroep
Dr. K.F.M. Joosten, kinderarts-intensivist, Erasmus MC-Sophia Kinderziekenhuis Rotterdam, voorzitter
Dr. R.H.T. v. Beek, kinderarts-neonatoloog, Amphia Ziekenhuis, Breda
Mw. ir. B.S. Glas, voedingskundige/kinderdiëtist, Brenda Glas, Consultancy in kindervoeding
Mw. dr. J.M. Hulst, kinderarts MDL, Erasmus MC-Sophia Kinderziekenhuis Rotterdam
Mw. dr. A. Kindermann, kinderarts MDL, Emma Kinderziekenhuis/AMC Amsterdam
Dr. J.P. van Wouwe, kinderarts en onderzoeker, TNO Leiden
Klankbordgroep
Commissie Voeding NVK
Belangenverklaringen
De werkgroepleden hebben in volledige onafhankelijkheid deze richtlijn geschreven en derhalve is er geen ‘conflict of interest’.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de ontwikkeling van het concept van de richtlijn is zoveel mogelijk rekening gehouden met de implementeerbaarheid van de richtlijn en de daadwerkelijke uitvoerbaarheid van de aanbevelingen. De richtlijn wordt verspreid onder alle relevante beroepsgroepen en ziekenhuizen. Ook wordt een samenvatting van de richtlijn ter publicatie aangeboden aan het Nederlands Tijdschrift voor Geneeskunde en zal er in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn.
Werkwijze
De werkgroep werkte gedurende één jaar aan een conceptrichtlijntekst. De werkgroep formuleerde uitgangsvragen op basis van relevantie en dagelijkse praktijk. De werkgroepleden hebben de literatuur beoordeeld op inhoud en kwaliteit. Vervolgens werden teksten geschreven waarin de beoordeelde literatuur werd verwerkt. De teksten werden in vergaderingen besproken en na verwerking van de commentaren geaccordeerd. Voor het komen tot een aanbeveling zijn er, naast het wetenschappelijk bewijs vaak andere aspecten van belang, bijvoorbeeld: specifieke expertise organisatorische aspecten of maatschappelijke consequenties. Deze aspecten worden besproken na de ‘Conclusie' in de ‘Overige overwegingen'. Hierin wordt de conclusie op basis van de literatuur in de context van de dagelijkse praktijk geplaatst en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen. Het volgen van deze procedure en het opstellen van de richtlijn in dit ‘format' heeft als doel de transparantie van de richtlijn te verhogen. Het biedt ruimte voor een efficiënte discussie tijdens de werkgroepvergaderingen en vergroot bovendien de helderheid voor de gebruiker van de richtlijn.
De uiteindelijke teksten vormen samen de conceptrichtlijn die in februari 2012 is aangeboden aan de commissie Voeding van de NVK, JGZ- werkgroep en hierna aan de leden van de NVK. De commentaren uit deze commentaarronde zijn in de definitieve versie van de richtlijn verwerkt.
Tabel 1: Indeling van de literatuur naar de mate van bewijskracht (CBO 2007)
|
|
Voor artikelen betreffende: interventie (therapie of preventie) |
|
A1 |
Systematische reviews die ten minste enkele onderzoeken van A2-niveau betreffen, waarbij de resultaten van afzonderlijke onderzoeken consistent zijn. |
|
A2 |
Gerandomiseerd vergelijkend klinisch onderzoek van goede kwaliteit (gerandomiseerde, dubbelblind gecontroleerde trials) van voldoende omvang en consistentie. |
|
B |
Gerandomiseerde klinische trials van matige kwaliteit of onvoldoende omvang of ander vergelijkend onderzoek (niet-gerandomiseerd, vergelijkend cohortonderzoek, patiënt-controle-onderzoek). |
|
C |
Niet-vergelijkend onderzoek. |
|
D |
Mening van deskundigen, bijvoorbeeld werkgroepleden. |
Tabel 2: Indeling van de literatuur naar de mate van bewijskracht (CBO 2007)
|
|
Voor artikelen betreffende: diagnostiek |
|
A1 |
Onderzoek naar de effecten van diagnostiek op klinische uitkomsten bij een prospectief gevolgde goed gedefinieerde patiëntengroep met een tevoren gedefinieerd beleid op grond van de te onderzoekentestuitslagen, of besliskundig onderzoek naar de effecten van diagnostiek op klinische uitkomsten, waarbij resultaten van onderzoek van A2-niveau als basis worden gebruikt en voldoende rekening wordt gehouden met onderlinge afhankelijkheid van diagnostische tests; |
|
A2 |
Onderzoek ten opzichte van een referentietest, waarbij van tevoren criteria zijn gedefinieerd voor de te onderzoeken test en voor een referentietest, met een goede beschrijving van de test en de onderzochte klinische populatie; het moet een voldoende grote serie van opeenvolgende patiënten betreffen, er moet gebruikgemaakt zijn van tevoren gedefinieerde afkapwaarden en de resultaten van de test en de ‘gouden standaard’ moeten onafhankelijk zijn beoordeeld. Bij situaties waarbij multipele, diagnostische tests een rol spelen, is er in principe een onderlinge afhankelijkheid en dient de analyse hierop te zijn aangepast, bijvoorbeeld met logistische regressie. |
|
B |
Vergelijking met een referentietest, beschrijving van de onderzochte test en populatie, maar niet de kenmerken die verder onder niveau A staan genoemd. |
|
C |
Niet-vergelijkend onderzoek. |
|
D |
Mening van deskundigen, bijvoorbeeld werkgroepleden. |
Tabel 3: Niveau van bewijs van de conclusies
|
|
Conclusie gebaseerd op |
|
1 |
Één systematische review (A1) of ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A1 of A2. |
|
2 |
Tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B. |
|
3 |
Één onderzoek van niveau A2 of B of onderzoek van niveau C. |
|
4 |
Mening van deskundigen, bijvoorbeeld de werkgroepleden. |
Zoekverantwoording
De aanbevelingen uit deze richtlijn zijn voor zover mogelijk gebaseerd op conclusies getrokken in gepubliceerd wetenschappelijk onderzoek. Naar relevante artikelen is door de informatiespecialist van TNO gezocht via systematische zoekacties in de Cochrane Database of Systematic Reviews (CDSR, via Wiley InterScience),in Medline en Embase (beiden via OvidSP). Gebruikt zijn de zoektermen (Mesh terms, medical subject headings) ´feeding and eating disorders of childhood´, ´failure to thrive´ and child nutrition disorders´ in combinatie met nadere specificeringen (´subheadings) zoals ´diagnoses´ of ‘differential diagnoses’. Daarnaast is gezocht op de trefwoorden: failure to thrive, food refusal, (pediatric) feeding problem(s), feeding difficulty(ies). Voor de somatische aandoeningen is ook gezocht door gebruik te maken van de standaard Mesh terms: gastroesophageal reflux, celiac disease, food hypersensitivity, cardiac output, urinary tract infections lung diseases, genetic diseases, inborn, pharyngitis otitis, respiratory tract infections, nervous system diseases, inflammatory bowel diseases, swallowing or swallow, deglutition disorders, nose diseases, pharynx, ear diseases, heartburn, abdominal pain, pneumonia, constipation, diarrhea, encopresis, fecal incontinence and intestinal obstruction. Hierbij werd de taal gelimiteerd tot Nederlands, Engels en Duits en werden artikelen uitsluitend over dierstudies uitgesloten. Er werd gezocht vanaf publicatiejaar 2000 tot en met de datum van de zoekactie (tussen april en juli 2011). Tevens werden er relevante artikelen aangedragen door werkgroepleden die dateren voor het publicatiejaar 2000.
Belangrijke selectiecriteria hierbij waren: vergelijkend onderzoek met hoge bewijskracht, zoals meta-analyses, systematische reviews, randomised controlled trials (RCT's) en controlled trials (CT's). Waar deze niet voorhanden waren, werd verder gezocht naar vergelijkend cohortonderzoek, vergelijkend patiëntcontrole onderzoek of niet-vergelijkend onderzoek.
De kwaliteit van deze artikelen werd door de werkgroepleden beoordeeld aan de hand van ‘evidence-based richtlijnontwikkeling' (EBRO)-beoordelingsformulieren. Artikelen van matige of slechte kwaliteit werden uitgesloten. Na deze selectie bleven de artikelen over die als onderbouwing bij de verschillende conclusies in de richtlijn staan vermeld. De geselecteerde artikelen zijn vervolgens gegradeerd naar de mate van bewijs, waarbij de volgende indeling is gebruikt (Tabel 1, 2 en 3). De mate van bewijskracht en niveau van bewijs zijn in de conclusies van de verschillende modules weergegeven. De belangrijkste literatuur waarop de conclusies zijn gebaseerd is daarbij vermeld.
