Interventies verpleeghuisopname slaapprobleem
Uitgangsvraag
- Welke niet-farmacologische interventies zijn zinvol voor tijdelijk in het verpleeghuis opgenomen oudere patiënten met nieuwe of verergerende slaapproblemen?
- Welke farmacologische interventies zijn zinvol voor tijdelijk in het verpleeghuis opgenomen oudere patiënten met nieuwe of verergerende slaapproblemen?
Aanbeveling
(voor het verpleeghuis)
|
STERK |
Bij een vastgesteld nieuw of verergerend slaapprobleem bij oudere opgenomen patiënten dient de oorzaak hiervan zo mogelijk te worden achterhaald en weggenomen (zie ook aanverwant Standaardvragen anamnese slaapproblemen bij opname en verblijf). Overweeg de eventuele aanwezigheid van een chronisch slaapprobleem. |
|
STERK |
Een nieuw of verergerend slaapprobleem wordt in eerste instantie niet-medicamenteus behandeld. Hierbij is aandacht voor slaaphygiëne (zie voor maatregelen die hieronder verstaand worden, aanverwant Slaaphygiëne bij acuut opgenomen ouderen) en psycho-educatie. De effectiviteit hiervan wordt dagelijks geëvalueerd (bijvoorbeeld middels een VAS-schaal). Met name aandacht voor lichaamsbeweging en veel (dag)licht overdag is hierbij nuttig. Slaap belemmerende medicatie wordt zo mogelijk gestaakt. |
|
STERK |
Het wordt aanbevolen dat verpleeghuizen een beleid hebben voor het bevorderen van een goede nachtrust (bijvoorbeeld ten aanzien van het lopen van nachtrondes en de beschikbaarheid van extra dekens). Ook behoren er mogelijkheden te zijn om de temperatuur van de ruimtes te beïnvloeden (zie ook aanverwant Slaaphygiëne bij acuut opgenomen ouderen). Slaapstoornissen dienen te worden opgenomen in het zorgleefplan. |
|
STERK |
Bij patiënten die vanwege een slaapprobleem bij opname reeds medicatie gebruiken, wordt het gebruik geëvalueerd en zonodig gecontinueerd. Het gebruik van meerdere soorten benzodiazepines wordt afgeraden. |
|
CONDITI-ONEEL |
Bij een vastgesteld nieuw of verergerend slaapprobleem bij oudere opgenomen patiënten worden gedurende de eerste twee nachten geen medicamenteuze maatregelen gericht op de slaap genomen. Indien het slaapprobleem na adequate niet-medicamenteuze maatregelen na twee nachten persisteert, kunnen medicamenteuze maatregelen worden genomen. |
|
STERK |
Het gebruik van langwerkende benzodiazepines (met een halfwaardetijd van langer dan 12 uur (zie aanverwant Farmacokinetische eigenschappen) wordt afgeraden, vanwege de hiermee gepaard gaande risico’s. Het gebruik van benzodiazepines wordt niet aanbevolen; bij patiënten met ernstige longproblematiek worden benzodiazepines afgeraden, vanwege het risico van ademdepressie. |
|
CONDITI-ONEEL |
Indien medicatie ter behandeling van het slaapprobleem wordt voorgeschreven, dient de voorschrijftermijn hiervan beperkt te zijn en het effect dagelijks te worden geëvalueerd (bijvoorbeeld middels een VAS-schaal). |
|
CONDITI-ONEEL |
Indien medicatie ter behandeling van het slaapprobleem wordt overwogen, is melatonine het middel van eerste keus (dagelijks op hetzelfde tijdstip). Een combinatie van melatonine, magnesium en zink wordt in één studie als alternatief genoemd. Medicatie dient slechts eenmaal per nacht gegeven te worden. |
|
STERK |
In de overdracht bij ontslag/overplaatsing wordt het slaapprobleem en de gekozen aanpak vermeld. |
Overwegingen
Een slaapprobleem is slecht voor de gezondheid en kan gepaard gaan met (verergering van) pijn, hoofdpijn, depressie, geheugenstoornissen, vermoeidheid, emotionaliteit, hypertensie en diabetes. Bovendien is een slaapprobleem gerelateerd aan een slecht herstel van acute ziekte. Adequate behandeling van een acuut slaapprobleem is daarom volgens de werkgroep nuttig voor het herstel (of behoud) van de algemene gezondheid.
Er zijn geen direct vergelijkende onderzoeken waarin de effectiviteit van benzodiazepines wordt vergeleken met melatonine voor de behandeling van acute slaapproblemen bij oudere opgenomen patiënten. Er is geen onderzoek van goede kwaliteit dat een positief effect van benzodiazepines laat zien voor de behandeling van acute slaapproblemen bij oudere opgenomen patiënten. Ook in buitenlandse richtlijnen is geen evidence gevonden. Des te opvallender is het dat benzodiazepines op grote schaal voorgeschreven worden.(99) Wel is er onderzoek voorhanden vanuit de chronische slaapstoornissen ten aanzien het gebruik van benzodiazepines.
Het gebruik van slaapmedicatie (met name bij gebruik van (langwerkende) benzodiazepines) is geassocieerd met veiligheidsrisico’s (met name vallen) en problemen gedurende gebruik tijdens een langere periode dan enkele dagen (gewenning met als gevolg een verminderde effectiviteit bij gelijkblijvende dosis, en verslaving). De werkgroep is dan ook van mening dat met het voorschrijven van slaap bevorderende medicatie uiterst terughoudend moet worden omgegaan. Er wordt daarom in de aanbevelingen voorrang gegeven aan het achterhalen van de oorzaak van het ervaren slaapprobleem (en het zo mogelijk verhelpen daarvan) en niet-medicamenteuze (slaaphygiëne) maatregelen.
Onderbouwing
Niet-farmacologische interventies
|
LAAG |
Er zijn aanwijzingen dat aanpassingen in lichtexpositie (bijvoorbeeld blootstelling aan zonlicht of daglichtlampen overdag of minder lichtexpositie ’s avonds en ‘s nachts) bij patiënten opgenomen in het verpleeghuis de slaapkwaliteit ’s nachts verbeteren en slaap overdag verminderen (onderzocht bij patiënten met een chronisch slaapprobleem). Maar, deze resultaten zijn niet consistent en zijn mogelijk ook te verklaren door andere interventies (bijvoorbeeld meer activiteiten overdag).
Alessi, Anconi-Israel, Dowling, Fetveit, Riemersma, Sloane (54, 100, 101, 103, 104, 108, 109) |
|
LAAG |
De combinatie van aanpassingen in lichtexpositie en het toedienen van melatonine is mogelijk effectief ter verbetering van de slaapkwaliteit bij patiënten opgenomen in het verpleeghuis, maar niet op de hoeveelheid slaap.
Dowling, Riemersma (54, 108) |
|
MATIG |
Een multidimensionele interventie (stimulans overdag uit bed te blijven, zonlichtexpositie, activiteitenprogramma en vermindering van prikkels ’s avonds en ‘s nachts) is mogelijk effectief in het verbeteren van de slaap bij patiënten opgenomen in een verpleeghuis met slaapproblemen.
Alessi (100) |
|
ZEER LAAG |
Passieve lichaamsverwarming lijkt niet effectief in het verbeteren van de slaap bij patiënten opgenomen in een verpleeghuis.
Mishima (105) |
|
Algehele kwaliteit van bewijs = LAAG |
Farmacologische interventies
|
LAAG |
De combinatie van aanpassingen in lichtexpositie en het toedienen van 2,5-5mg melatonine is mogelijk effectief ter verbetering van de slaapkwaliteit bij patiënten opgenomen in het verpleeghuis, maar niet op de hoeveelheid slaap. Het is niet bekend of dit ook geldt bij nieuwe of verergerende slaapproblemenstoornissen.
Dowling, Riemersma (54, 108) |
|
LAAG |
Melatonine (5 mg 1dd ‘s avonds) is mogelijk effectief ter bevordering van de slaapkwaliteit bij bewoners van verpleeghuizen. Het is niet bekend of dit ook geldt bij nieuwe of verergerende slaapproblemen.
Garzan (111) |
|
MATIG |
Een combinatie van 1 dd ’s avonds melatonine5 mg, magnesium 225 mg en zink 11,25 mg verbetert de slaapkwaliteit bij oudere patiënten, opgenomen in het verpleeghuis, met klachten van insomnia. Het is niet bekend of dit ook geldt bij nieuwe of verergerende slaapproblemenstoornissen.
Rondanelli (114) |
|
Algehele kwaliteit van bewijs = LAAG |
Overall kwaliteit
Er is sprake van een grote diversiteit aan studies, die niet gecombineerd kunnen worden vanwege de heterogeniteit in populaties en inhoud van interventies. De algehele kwaliteit van het bewijs is laag en de gevonden evidence is maar zeer beperkt toepasbaar op onze populatie met nieuwe of verergerende slaapstoornissen. Het verder doorvoeren van de GRADE systematiek (met behulp van evidence profielen en summary of findings) is derhalve niet zinvol.
Niet-farmacologische interventies
Twaalf onderzoeken richtten zicht op niet-farmacologische interventies in de verpleeghuis setting.(54, 100-110)
Alessi et al. onderzochten de effecten van een multidimensionele interventie gericht op verschillende factoren voor verstoorde slaap in een verpleeghuis.(100) De studie betreft een RCT onder bewoners van vier verpleeghuizen in de USA van mensen met een verstoorde slaap (≥15% slaap overdag, ≤80% slaap ‘s nachts). De studie is van matige kwaliteit, omdat er geen sprake is van blindering. Patiënten in de interventiegroep werden overdag gestimuleerd om uit bed te blijven, kregen ten minste 30 minuten per dag buiten zonlichtexpositie en namen drie maal per dag aan een (fysiek) activiteitenprogramma. In de avond kregen zij minder geluid, minder licht en persoonlijke zorg. ’s Nachts was er sprake van minimaal licht en geluid en werden patiënten verzorgd als de patiënt wakker was en niet op gezette tijden. Patiënten in de controlegroep kregen ‘usual care’. De effectiviteit werd geëvalueerd aan de hand van actigrafie, pulsoximetrie en observatie van het gedrag. In het onderzoek namen 118 patiënten deel; de gemiddelde leeftijd was 86 jaar (sd 9). Een groot deel van de patiënten was dement of had een delirium. Er was niet specifiek sprake van een nieuw of verergerend slaapprobleem. Er werden geen significante verschillen gevonden in slaaptijd ’s nachts, het aantal keren dat een patiënt ontwaakte ’s nachts en het percentage slaap ’s nachts. Gemiddeld waren patiënten in de controlegroep langer wakker ’s nachts als ze wakker waren (13,8 versus 9,8 minuten; p=0,042) en sliepen patiënten overdag in de interventiegroep minder (21% versus 30%; p<0,001).
In het onderzoek van Ancoli-Israel et al. werd onderzocht of vergroten van de daglichtexpositie de slaap ’s nachts verbetert en het circadiane ritme normaliseert bij bewoners van een verpleeghuis.(101) Het onderzoek is een RCT onder bewoners van een verpleeghuis waarbij ‘te zieke’ mensen, en patiënten die bedlegerig waren, een visuele beperking hadden of niet in staat waren tot communicatie, werden geëxcludeerd. Er is geen sprake van blindering en er is maar een beperkt aantal patiënten per behandelarm van de studie. De studiekwaliteit is daarom als laag gegradeerd. Daarnaast is er geen sprake van nieuwe of verergerende slaapstoornissen. In het onderzoek namen 77 patiënten deel, de gemiddelde leeftijd was 86 jaar (sd 7), 71% had een score op de MMSE <20 (dementie). De patiënten werden gerandomiseerd in vier groepen:daglichtlampen ’s avonds, daglichtlampen ’s ochtends, gedimd rood licht ’s avonds met als controlegroep slaaprestrictie overdag. Als uitkomsten werden de slaaptijden geëvalueerd en werd met actigrafie gemeten. Er werden geen significante verschillen gevonden in slaap ’s nachts of activiteiten overdag, wel werd een beperkte verbetering van het circadiane ritme gevonden in de groep met lichtexpositie ’s ochtends.
Dowling et al. onderzochten het effect van lichttherapie en melatonine op het circadiane ritme en het slaapritme bij patiënten met M. Alzheimer.(54) In deze RCT werden bewoners van twee verpleeghuizen met M. Alzheimer en een verstoord rust-activiteitenritme geïncludeerd. De studie is van lage kwaliteit, omdat er geen sprake is van blindering, het om een beperkt aantal patiënten gaat en het niet duidelijk wordt welk resultaat van welke interventie komt. Ook is er geen sprake van een nieuw of verergerend slaapprobleem. In het onderzoek namen 50 patiënten deel, van wie 43 vrouwen. De gemiddelde leeftijd was 86 jaar (sd 9, range 60-100); de leeftijd in de controlegroep was significant lager dan in de interventiegroep. Patiënten in de twee interventiegroepen kregen ’s ochtends blootstelling aan daglichtlampen (> 2.500 lux) en melatonine (5 mg) ’s avonds respectievelijk ’s ochtends blootstelling aan daglichtlampen met een placebo ’s avonds. Patiënten in de controlegroep kregen alleen ‘gewoon’ licht (150-200 lux). De studie duurde 11 weken. Gekeken werd naar activiteiten en rust middels actigrafie. Er werden geen verschillen gevonden tussen de groepen daglichtlampen plus placebo en controle en tussen daglichtlampen plus melatonine en daglichtlampen plus placebo. Bij vergelijking van daglichtlampen plus melatonine met de controlegroep werd wel een verschil gevonden in met name de slaap overdag.
Een andere studie van Dowling et al. onderzocht de effectiviteit van blootstelling aan daglichtlampen ’s ochtends in vergelijking met ’s middags en blootstelling aan normaal licht.(102) Deze studie vond geen significante resultaten voor slaap- en waakparameters. De studie wordt verder niet beschreven, omdat sprake is van dubbeling van de gegevens met het eerder beschreven onderzoek van Dowling et al.(54)
Fetveit et al. onderzochten de duur van het effect van expositie aan daglichtlampen bij patiënten met dementie.(103, 104) Dit betreft een cohortonderzoek onder 11 patiënten, waarvan twee publicaties zijn geselecteerd voor deze review. De kwaliteit van de studie is zeer laag, omdat er geen sprake is van een vergelijkend onderzoek, er geen gecontroleerde omstandigheden zijn en er zeer weinig patiënten deelnemen aan het onderzoek. De patiënten in het onderzoek waren gemiddeld 86 jaar(sd 9, range 72-101) en hadden matige tot ernstige dementie en diverse comorbiditeit. De patiënten werden gedurende twee weken blootgesteld aan twee uur daglichtlampen ’s ochtends (6.000-8.000 lux), waarbij met statusonderzoek en actigrafie werd geëvalueerd. De auteurs concluderen dat de slaapefficiëntie verbeterde met 13% en dat de inslaapduur een uur korter was (niet significant). Ook geven zij aan dat het effect tot twaalf weken aan houdt. Kritisch bezien moet echter worden geconcludeerd dat deze verbanden niet zijn aangetoond in dit onderzoek.
Mishima et al. onderzochten de slaapbevorderende werking van passieve lichaamsverwarming bij oudere patiënten met vasculaire dementie en insomnia.(105) In dit onderzoek werden 13 patiënten > 70 jaar (gemiddelde leeftijd 77 jaar) geïncludeerd, die gedurende 13 dagen een protocol doorliepen: 7 dagen prestudie, dan 3 dagen baseline (niet slapen buiten de slaapkamer, verlichting < 10 lux in slaapperiode, urineren voor slapen), daarna 2 dagen passieve lichaamsverwarming (half uur in bad 40 graden, 2 uur voor slapen gaan), dan nog 1 dag postmeting. Geëvalueerd werd met behulp van actigrafie, melatoninespiegels en meting van het hartritme. De kwaliteit van deze studie was zeer laag, omdat er geen sprake was van een controlegroep, zeer weinig patiënten waren geïncludeerd en er geen sprake was van gecontroleerde omstandigheden Er bestaat een grote kans dat de gevonden resultaten het gevolg zijn van toeval of andere interventies dan de passieve lichaamsverwarming. De meeste resultaten waren niet statistisch significant; de tijd om in slaap te komen nam af van gemiddeld 27 minuten naar gemiddeld 16 minuten (p < 0,02). Dit verschil is volgens de richtlijnwerkgroep niet klinisch relevant.
Molinari et al. onderzochten in een pilot onderzoek of mental health assessment het gebruik van psychoactieve middelen zou kunnen verminderen.(106) In dit onderzoek werden 23 nieuwe verpleeghuisbewoners geïncludeerd in de interventiegroep; zij werden vergeleken met 25 controlebewoners. 94% van de patiënten was ouder dan 60 jaar. De patiënten in de interventiegroep kregen ‘mental health assessment’, dit was niet specifiek gericht op slaapproblemen. De patiënten in de controlegroep kregen deze interventie niet. Medicatievoorschriften van psychofarmaca werden geëvalueerd. De studie was van lage kwaliteit, omdat er geen sprake was van randomisatie en er een verschil was tussen de patiënten in de interventie- en de controlegroep. Bovendien was het aantal patiënten in de beide groepen niet erg hoog. In de interventiegroep stopte één patiënt met het gebruik van slaapmiddelen, in de controlegroep was dat geen patiënt (niet significant). In de assessmentgroep startten twee mensen met slaapmedicatie (9%), in de controlegroep waren dit er tien (40%) (p = 0,013). Deze resultaten geven eigenlijk geen antwoord op de uitgangsvraag.
In het onderzoek van Richards et al. werd het effect van krachttraining, looptraining, het aanbieden van sociale activiteiten en de combinatie daarvan onderzocht op de nachtelijke slaap.(107) Dit onderzoek betreft een RCT onder bewoners van 13 verpleeghuizen in de VS, bij bewoners ≥ 55 jaar, met een MMSE-score tussen 4 en 29, die minder dan zeven uur ’s nachts slapen en meer dan 30 minuten overdag. Patiënten met een niet-stabiele ernstige ziekte werden uitgesloten. In het onderzoek werden 193 deelnemers geïncludeerd, met een gemiddelde leeftijd van 82 jaar (range 57-90). Er was sprake van veel comorbiditeit. Patiënten werden gerandomiseerd over vier groepen: fysieke oefening, sociale activiteit, combinatie van beide en usual care. Met polysomnografie aan het begin en aan het eind van de studie (na 7 weken) werd primair gekeken naar de totale slaap ’s nachts. Overige slaapparameters waren secundair. De kwaliteit van de studie is matig, de groepen waren te klein voor een adequate power om de primaire uitkomstmaat te bepalen. Hierdoor zijn vooral voor-na vergelijkingen gedaan zonder statistische toets tussen de verschillende groepen. Bovendien is geen sprake van nieuwe of verergerende slaapproblemen. De nachtelijke slaap was in de groep met combinatie van sociale activiteiten en fysieke oefening 364 minuten in vergelijking met 329 minuten bij usual care (p = 0,01). Dit verschil wordt niet klinisch relevant geacht door de richtlijnwerkgroep. Vergelijking met de andere groepen was niet statistisch significant.
Het onderzoek van Riemersma et al. richtte zich op de langetermijneffecten van daglichtlampen en melatonine op het cognitieve systeem bij verpleeghuispatiënten.(108) In deze 2x2 factorial RCT werden 189 verpleeghuispatiënten met een gemiddelde leeftijd van 86 jaar (sd 5,5) geïncludeerd. Van alle patiënten had 92% enige vorm van dementie. Patiënten in de interventiegroepen kregen lichtexpositie tussen 9.00 en 18.00 uur van 1.000 lux en/of melatonine 2,5 mg 1 uur voor bedtijd. Patiënten in de controlegroepen kregen lichtexpositie op een lagere intensiteit en/of een placebotablet. Primair werd gekeken naar de cognitieve status met behulp van de MMSE; daarnaast waren en diverse parameters op gebied van gedrag, stemming en slaap. De studie kent een follow-up van gemiddeld 15 maanden (sd 12 maanden, tot 3,5 jaar). De studie is van matige kwaliteit, vanwege de behoorlijke kans op verstorende variabelen, vanwege het factoriële design van het onderzoek. Daarnaast is er een zeer forse drop-out (die overigens niet te voorkomen is in deze populatie met een lange follow-up). Ook is er geen sprake van nieuwe of verergerende slaapproblematiek. De slaapefficiëntie bleek beter in de groep met de gecombineerde interventie (licht plus melatonine) (3,5% verschil, p = 0,01 ten opzichte van de overige groepen). De totale slaapduur was hoger bij lichtexpositie (10 minuten; p = 0,04) en bij melatonine (27 minuten; p = 0,004), maar niet bij de combinatie van beide interventies.
Sloane et al. onderzochten de effectiviteit van licht met een hoge intensiteit en activiteiten overdag bij patiënten met dementie.(109) Deze studie betreft een voor-na vergelijking met verschillende interventies die achtereenvolgens zijn uitgevoerd gedurende drie weken elk: lichtexpositie van 2.500 lux van 7.00 tot 11.00 uur, vervolgens van 16.00-20.00 uur en in de laatste fase de hele dag (7.00-20.00 uur). De controlegroep kreeg expositie met een lichtintensiteit van 500 lux. De effectiviteit werd bepaald door middel van actigrafie in de laatste week van elke interventie. Daarnaast werd naar bijwerkingen gekeken. De kwaliteit van het onderzoek was laag, omdat er geen sprake is van randomisatie en omdat er een grote kans is dat de gevonden resultaten vertekend zijn door andere omstandigheden dan de interventie. Ook was er geen sprake van nieuwe of verergerende slaapproblemen. Het aantal uren slaap verschilde statistisch significant tussen de verschillende groepen: bij ochtendlichtexpositie was dit 5,54 uur, bij avondlicht 5,45 uur, bij lichtexpositie gedurende de hele dag 5,55 uur en bij standaardlicht 5,36 uur (p = 0,04). Dit verschil is niet klinisch relevant. De overige resultaten waren niet statistisch significant.
In het onderzoek van Sun et al. ten slotte werd de effectiviteit van HT7 acupressure op de slaapkwaliteit en insomnia onderzocht.(110) Deze RCT werd uitgevoerd in twee verpleeghuizen in Taiwan, onder patiënten die ten minste drie maanden in het verpleeghuis verbleven. Patiënten met een ernstige acute ziekte of die chronisch slaapmiddelen gebruikten werden geëxcludeerd. In het onderzoek namen 50 patiënten deel met een gemiddelde leeftijd van 70 jaar, van wie 64% een CVA had gehad. Patiënten in de interventiegroep kregen HT7 acupressure op beide polsen gedurende 5 seconden, dan 1 seconde rust, gedurende 5 minuten voor bedtijd, 5 weken lang. Patiënten in de controlegroep kregen een ‘placebo’: lichte druk in plaats van acupressure. De effectiviteit werd bepaald met de Athens Insomnia Scale (AIS). De kans op vertekening is groot doordat er sprake is van beperkte blindering, het aantal patiënten beperkt is en omdat de resultaten vanwege een andere populatie mogelijk niet extrapoleerbaar zijn naar de Nederlandse situatie. Er werden lagere scores op de AIS-schaal gevonden in de interventiegroep, vergeleken met de controlegroep. Die verschillen werden kleiner na afloop van de interventie. Er werd geen statistische toetsing uitgevoerd (en dat kan ook niet alsnog gedaan worden op basis van de data uit het artikel). De interpretatie van de resultaten is onduidelijk in het artikel.
Farmacologische interventies
Zeven onderzoeken bestudeerden de toepassing van farmacologische interventies in het verpleeghuis.(54, 108, 111-115) De studies van Dowling et al. en Riemersma et al. zijn bovenstaand reeds besproken.(54, 108)
Garzan et al. onderzochten het effect van melatonine op slaap en gedrag bij ouderen, waarbij zij ook keken naar het discontinueren van hypnotica/sedativa.(111) Dit onderzoek betreft een dubbelblinde RCT met cross-over design, waarbij patiënten van ‘community health centers’ met een leeftijd ouder dan 65 jaar met insomnia of voorbijgaande slaapproblemen door stress werden geïncludeerd. Patiënten met een ernstige ziekte of een secundaire slaapstoornis werden geëxcludeerd. Aan het onderzoek namen 22 patiënten deel, met een gemiddelde leeftijd van 75 jaar; 20 van hen hadden chronische slaapproblemen. Patiënten kregen gedurende acht weken 5 mg melatonine 1 dd ’s avonds, dan twee weken wash-out en vervolgens acht weken placebo, met daarbij gedurende het hele traject de stimulans om de dosering hypnotica te reduceren (en controlegroep net andersom). De effectiviteit werd geëvalueerd met de Northside Hospital Sleep Medicine Institute Test (NHSMI) (scorerange 0-8) en de slagingskans om hypnotica te verminderen. De studie was van lage kwaliteit omdat er weinig patiënten deelnamen en er een beperkte beschrijving van de resultaten was. Bovendien was er geen sprake van nieuwe of verergerende slaapproblemen. Er werd geen verschil in slaapscore gemeten met de NHSMI-test, gevonden tussen baselinemeting en placeboperiode. Wel tussen melatonineperiode en baselinemeting (gemiddeld verschil 3,7 (sd 0,40; p < 0,005)). Ook was er een significant verschil in slaapscore tussen melatonine en placebo (gemiddeld verschil 3,4 (sd 0,56 p < 0,025)). De werkgroep vindt dit verschil klinisch relevant.
Greco et al. onderzochten de associatie tussen het routinegebruik van psychoactieve medicatie en slaapkwaliteit bij bewoners van een verpleeghuis.(112) Dit onderzoek is een dwarsdoorsnede onder bewoners van een verpleeghuis die hulp nodig hebben als ze ’s nachts het bed uit moeten. Patiënten werden geëxcludeerd als ze terminaal waren of bij kortverblijf. De studie is van lage kwaliteit omdat er geen sprake is van experimenteel design en er ook geen interventie wordt bestudeerd. Bovendien is er waarschijnlijk sprake van onvergelijkbaarheid van groepen, die niet alleen te verklaren is door het gegeven of iemand psychoactieve medicatie gebruikt. In het onderzoek namen 210 bewoners deel, met een gemiddelde leeftijd van 84 jaar (sd 8,3). Van 80% van hen werden data gedurende drie nachten verkregen (inclusiecriterium), ongeveer 2/3 deel gebruikte psychoactieve medicatie. De slaapkwaliteit werd geëvalueerd met behulp van actigrafie en was laag in de gehele populatie en leek wat beter in de groep die psychoactieve medicatie gebruikte, maar er werd geen statistisch significant resultaat gevonden.
In het onderzoek van Li Pi Shan et al. werden de effectiviteit van lorazepam en zopiclone rechtstreeks vergeleken bij patiënten in een revalidatie-instelling met een beroerte of hersenbeschadiging en klachten van insomnia.(113) In deze dubbelblinde RCT werden 18 patiënten met een gemiddelde leeftijd van 57 jaar (range 20-78) gerandomiseerd. De interventie bestond uit zeven dagen 0,5-1,0 mg lorazepam, gevolgd door zeven dagen 3,75 mg zopiclon. De patiënt was hierbij zelf verantwoordelijk voor de dosering (controlegroep net andersom). De effectiviteit werd geëvalueerd met de door de patiënt zelf gerapporteerde slaapkwaliteit en de door de verpleegkundige gerapporteerde slaapduur. De studie was van zeer lage kwaliteit, omdat er geen sprake was een wash-out periode, omdat er naast farmacologische interventies ook andere maatregelen werden getroffen. Bovendien waren er maar heel weinig patiënten. In het onderzoek zijn geen significante verschillen gevonden tussen beide groepen.
Het onderzoek van Rondanelli et al. beschrijft de effectiviteit en veiligheid van de combinatie van melatonine, magnesium en zink voor het verbeteren van de slaapkwaliteit en alertheid overdag bij ouderen > 70 jaar met primaire insomnia.(114) Dit onderzoek is een dubbelblinde RCT onder verpleeghuispatiënten die ten minste drie maanden in het verpleeghuis verblijven. Patiënten met een slaapstoornis door een bekende oorzaak, met een psychiatrische of neurologie diagnose, restless legs of medicatie die het centraal zenuwstelsel of het slaapwaakritme beïnvloedt, werden geëxcludeerd. Aan het onderzoek namen 43 patiënten deel met een gemiddelde leeftijd van 78 jaar (sd 4 jaar). Patiënten in de interventiegroep kregen 1 uur voor bedtijd 100 gram peerpulp met toegevoegd 5 mg melatonine, 225 mg magnesium en 11,25 mg zink. Patiënten in de controlegroep kregen 100 gram peerpulp zonder toevoegingen. Primair werd gekeken naar de slaapkwaliteit met behulp van de Pittsburgh Sleep Quality Index (PSQI). De studie is van hoge kwaliteit, er is sprake van goede methodologie. Opgemerkt moet echter wel worden dat er geen sprake is van nieuwe of verergerende slaapproblemen en dat niet af te leiden is welk van de componenten van de interventie in welke mate bijdraagt aan het resultaat. Het verschil op de PSQI tussen de interventie- en de controlegroep na acht weken interventie was 6,8 punten (95% BI: 5,1-8,3). In de interventiegroep had 59% een score op de PSQI < 5; in de controlegroep was dit 14% (verschil 45; 95% BI: 20-70).
Het onderzoek van Simpson et al. ten slotte was een secundaire analyse van baseline data voor een RCT, waarin de voorgeschreven medicatie en het slaapgedrag van verpleeghuisbewoners met dementie werd beschreven.(115) In dit onderzoek namen 195 bewoners van gemiddeld 80 jaar deel die ten minste 30 minuten sliepen overdag. De meesten hadden een ernstige cognitieve stoornis, 71% gebruikte meerdere psychotrope geneesmiddelen. Gekeken werd naar medicatiedossiers en actigrafie gedurende vijf dagen en nachten. De kwaliteit van de studie is laag, omdat er geen interventies worden vergeleken en omdat er sprake is van een niet geplande analyse (dus geen gecontroleerd onderzoek). Gemiddeld sliepen de patiënten 505 minuten per etmaal, waarvan 70% ’s nachts. Patiënten die SSRI’s gebruikten sliepen ’s nachts 64% versus 72% bij niet-gebruikers (p = 0,005); trazodongebruikers sliepen 78% ’s nachts, in vergelijking met 70% bij niet-gebruikers (p = 0,04). Overige resultaten waren niet statistisch significant.
Om deze uitgangsvragen te beantwoorden werd een uitgebreide literatuursearch gedaan (zie zoekverantwoording). Er bleken geen goede systematische reviews te zijn, derhalve is een eigen systematische review uitgevoerd. De literatuursearches voor de beide vragen over niet-farmacologische interventies (dus in ziekenhuis en in verpleeghuis) zijn uitgevoerd middels één literatuursearch. Datzelfde geldt voor de beide vragen over farmacologische interventies. Deze beide literatuursearches leverden 199 respectievelijk 202 mogelijk relevante artikelen. Deze searches werden vervolgens samengevoegd, waarna een eerste selectie plaatsvond op basis van abstract. Hierbij bleven 81 artikelen over die werden opgevraagd. De meeste artikelen vielen af omdat ze niet over de juiste populatie gingen (geen merendeel oudere patiënten, of geen nieuwe of verergerende slaapproblemen (maar veelal bestaande problemen zoals OSAS)), omdat geen interventie werd bestudeerd (maar bijvoorbeeld meer epidemiologisch onderzoek over prevalentie van slaapproblematiek) of omdat het geen systematisch onderzoek betrof.(36-43) Derhalve zijn 72 fulltext beoordeeld op kwaliteit en inhoud. Deze zijn vermeld in de evidence tabel. Een aantal artikelen is daarna alsnog geëxcludeerd, omdat het onderwerp niet aansloot bij de uitgangsvraag of omdat het geen systematisch opgezet onderzoek betrof.(44-90) De overgebleven artikelen staan onderstaand beschreven per onderwerp. Additioneel werd gezocht naar evidence voor de effectiviteit van zopiclon. Dit leverde 34 abstracts; na selectie bleef één artikel over, dat onderstaand beschreven staat. (91)
- 54 - Dowling GA, Burr RL, Van Someren EJ, Hubbard EM, Luxenberg JS, Mastick J, et al. Melatonin and bright-light treatment for rest-activity disruption in institutionalized patients with Alzheimer's disease. Journal of the American Geriatrics Society. 2008;56(2):239-46.
- 99 - Kengetallen SF. Minder ouderen aan de benzo's. Pharm Weekblad. 2012;147(36).
- 100 - Alessi CA, Martin JL, Webber AP, Cynthia Kim E, Harker JO, Josephson KR. Randomized, controlled trial of a nonpharmacological intervention to improve abnormal sleep/wake patterns in nursing home residents. Journal of the American Geriatrics Society. 2005;53(5):803-10.
- 101 - Ancoli-Israel S, Martin JL, Kripke DF, Marler M, Klauber MR. Effect of light treatment on sleep and circadian rhythms in demented nursing home patients. Journal of the American Geriatrics Society. 2002;50(2):282-9.
- 102 - Dowling GA, Mastick J, Hubbard EM, Luxenberg JS, Burr RL. Effect of timed bright light treatment for rest-activity disruption in institutionalized patients with Alzheimer's disease. International journal of geriatric psychiatry. 2005;20(8):738-43.
- 103 - Fetveit A, Bjorvatn B. The effects of bright-light therapy on actigraphical measured sleep last for several weeks post-treatment. A study in a nursing home population. Journal of sleep research. 2004;13(2):153-8.
- 104 - Fetveit A, Skjerve A, Bjorvatn B. Bright light treatment improves sleep in institutionalised elderly--an open trial. International journal of geriatric psychiatry. 2003;18(6):520-6.
- 105 - Mishima Y, Hozumi S, Shimizu T, Hishikawa Y, Mishima K. Passive body heating ameliorates sleep disturbances in patients with vascular dementia without circadian phase-shifting. The American journal of geriatric psychiatry : official journal of the American Association for Geriatric Psychiatry. 2005;13(5):369-76.
- 106 - Molinari VA, Chiriboga DA, Branch LG, Greene J, Schonfield L, Vongxaiburana E, et al. Influence of mental health assessment on prescription of psychoactive medication among new nursing home residents. Clinical Gerontologist. 2013;36:33-45.
- 107 - Richards KC, Lambert C, Beck CK, Bliwise DL, Evans WJ, Kalra GK, et al. Strength training, walking, and social activity improve sleep in nursing home and assisted living residents: randomized controlled trial. Journal of the American Geriatrics Society. 2011;59(2):214-23.
- 108 - Riemersma-van der Lek RF, Swaab DF, Twisk J, Hol EM, Hoogendijk WJ, Van Someren EJ. Effect of bright light and melatonin on cognitive and noncognitive function in elderly residents of group care facilities: a randomized controlled trial. JAMA : the journal of the American Medical Association. 2008;299(22):2642-55.
- 109 - Sloane PD, Williams CS, Mitchell CM, Preisser JS, Wood W, Barrick AL, et al. High-intensity environmental light in dementia: effect on sleep and activity. Journal of the American Geriatrics Society. 2007;55(10):1524-33.
- 110 - Sun JL, Sung MS, Huang MY, Cheng GC, Lin CC. Effectiveness of acupressure for residents of long-term care facilities with insomnia: a randomized controlled trial. International journal of nursing studies. 2010;47(7):798-805.
- 111 - Garzan C, Guerrero JM, Aramburu O, Guzman T. Effect of melatonin administration on sleep, behavioral disorders and hypnotic drug discontinuation in the elderly: a randomized, double-blind, placebo-controlled study. Aging Clinical & Experimental Research. 2009;21(1):38-42.
- 112 - Greco KE, Deaton C, Kutner M, Schnelle JF, Ouslander JG. Psychoactive medications and actigraphically scored sleep quality in frail nursing home patients. Journal of the American Medical Directors Association. 2004;5(4):223-7.
- 113 - Li Pi Shan RS, Ashworth NL. Comparison of lorazepam and zopiclone for insomnia in patients with stroke and brain injury: a randomized, crossover, double-blinded trial. American journal of physical medicine & rehabilitation / Association of Academic Physiatrists. 2004;83(6):421-7.
- 114 - Rondanelli M, Opizzi A, Monteferrario F, Antoniello N, Manni R, Klersy C. The effect of melatonin, magnesium, and zinc on primary insomnia in long-term care facility residents in Italy: a double-blind, placebo-controlled clinical trial. Journal of the American Geriatrics Society. 2011;59(1):82-90.
- 115 - Simpson KM, Culpepper Richards K, Enderlin CA, O'Sullivan PS, Koehn M. Medications and sleep in nursing home residents with dementia. J Am Psychiatr Nurses Assoc. 2006;12(5):279-182.
Niet-farmacologische en farmacologische interventies
|
Eerste auteur |
Jaartal |
Setting* |
Farm./ niet farm. |
Doel onderzoek |
Studietype |
In-/exclusie-criteria |
Studieduur/ follow-up |
Patiëntenkarak-teristieken |
Interventie |
Controle |
Uitkomst-maten |
Resultaten |
Risk of bias |
Kwali-teit |
Opmerkingen |
|
Agostini |
2006 |
Ziekenhuis |
Niet-farma-ceutisch |
Onderzoeken effecten van computer-based interventie op de frequentie van voorschrijven van sedativa bij oudere opgenomen patiënten |
Prospectief voor-na onderzoek |
Opgenomen patiënten ≥65 in academisch zie-kenhuis met me-dicatievoor-schrift (zo nodig gebruik) voor slaapprobleem of insomnia. Medicatie: di-phenhydramine, diazepam, lora-zepam, trazo-don). Exclusie: voorschrift voor andere indicatie (bijv. angst) |
Dataverza-meling gedurende 1 jaar voor interventie en 1 jaar na start interventie |
25.509 patiënten, gemiddelde leeftijd 76 (sd 7), gemiddelde Charlson comorbiditeit score 2,3 (sd 1,9), 18% met slaapmedicatie bij opname, 1% met slaapprobleem bij opname, niet specifiek nieuw of verergerend tijdens opname |
Computerba-sed interventie (computeror-der entry screen als in-terventie of reminder bij bestellen van difenhydra-mine of diaze-pam; met aan-bevelingen voor niet-me-dicamenteuze en medica-menteuze in-terventies bij oudere patiënten) |
Geen |
Medicatie-voorschrift (sedativa), niet-farmacologi-sche interven-ties. Succes gedefinieerd als niet-farma-cologische interventie of voorschrift lorazepam of trazodon. Fa-len als voor-schrift difen-hydramine of diazepam |
Voorschrift medicatie daalde van 18% naar 15% (OR 0,82; 95%: 0,76-0,87), ARR: 3%, NNT: 33, succes bij 95% na interventie (maar voor interventie staat niet vermeld) |
Geen vergelijkend onderzoek (geen groepen, geen randomisatie), forse kans op bias (grote kans dat resultaten niet alleen het gevolg zijn van de interventie), grote kans op wegebben effect na gewenning interventie |
Laag |
Onderzoek sluit eigenlijk niet echt aan bij uitgangsvraag |
|
Alessi |
2005 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken multidimensio-nele interventie gericht op verschillende factoren voor verstoorde slaap in verpleeghuis en effect op slaapgewoonten |
RCT |
Bewoners vier verpleeghuizen in USA, met ≥15% slaap overdag, ≤80% slaap 's nachts; exclusie: acuut ziek, in isolatie, volledig bedlegerig |
5 dagen interventie |
118 patiënten in randomisatie, gemiddelde leeftijd 86 jaar (sd 9), 77% vrouw, 53% blank, waarschijnlijk groot aandeel met delirium of dementie, niet specifiek met nieuw of verergerend slaapprobleem |
Overdag: sti-mulans uit bed te blijven, ≥30 minuten zonlicht bui-ten, 3 maal/ dag deelname fysiek activi-teitenprogram-ma. Avond: minder geluid, lichten uit, persoonlijke zorg. Nacht: minimaal licht en geluid, zorg als patiënt wakker is en niet op gezette tijden |
Usual care |
Wrist actigraphy, pulsoximetrie, observatie gedrag |
Geen signifi-cante ver-schillen in slaaptijd, aan-tal keren ont-waakt en % slaap 's nachts. Ge-middelde duur wakker zijn 's nachts langer in con-trolegroep (13,8 vs 9,8 minuten; p= 0,042), en ge-middeld min-der slaap overdag (21% in interventie-groep vs 30% in controle-groep; p<0,001) |
Wel randomisatie, maar geen blindering (is ook niet mogelijk bij deze interventie) |
Matig |
Patiëntengroep sluit niet helemaal aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem |
|
Anconi-Israel |
2002 |
Verpleeghuis |
Niet-farm-aceutisch |
Onderzoeken of vergroten van daglichtexposi-tie slaap 's nachts verbetert en circadiane ritme normaliseert bij bewoners verpleeghuis |
RCT |
Bewoners verpleeghuis; exclusie: 'te ziek', bedlegerig, visuele beperking, niet in staat tot communicatie |
18 dagen, waarvan 10 dagen interventie |
77 patiënten, 75% vrouw, gemiddelde leeftijd 86 jaar (sd 7), 80% niet depressief, 71% score op MMSE <20 (dementie) |
3 groepen: avond daglichtlampen, ochtend daglichtlampen, avond gedimd rood licht |
Slaapre-strictie overdag |
Wrist actigraphy, slaaptijden |
Geen signifi-cante ver-schillen in slaap 's nachts of activiteiten overdag, wel beperkte ver-betering cir-cadiane ritme in de groep met ochtend lichtexpositie |
Geen blindering, beperkt aantal patiënten per groep |
Laag |
Patiëntengroep sluit niet helemaal aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem |
|
Andrade |
2001 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken effectiviteit en veiligheid melatonine bij zieken met insomnia |
Dubbelblinde RCT |
Opeenvolgende opgenomen patiënten met insomnia (>30 minuten inslaaptijd, meer dan 2 weken, klachten) |
8-16 dagen behandeling |
33 patiënten, gemiddeld 56 jaar, 24 mannen, opgenomen met diverse diagnoses (bijv. cardiovasculaire aandoening, hematologische aandoening, leveraandoening, longziekte); 18 patiënten met melatonine, 15 met placebo |
Melatonine 3 mg, 1-4 capsules per nacht |
Placebo |
Gemiddelde inslaaptijd, aantal keren wakker 's nachts, duur nachtelijke slaap (vergelijking start en eind), 5-puntsschaal verbetering slaap, vragenlijst slaapkwaliteit |
Na behande-ling: tijd tot inslapen: 0,3 uur (sd 0,2) bij melatoni-ne; 1,0 uur (sd 1,0) bij placebo (p= 0,05). Score verbetering: 2,5 (sd 1,0) bij melatonine, 1,6 (sd 1,3) bij placebo, op 5-puntsschaal (p=0,03), overige resul-taten niet significant |
Onvergelijk-baarheid groepen, bijv. in leeftijd, geslacht, primaire aandoening, duur en intensiteit gebruik melatonine/ placebo, weinig patiënten |
Laag |
Studie gefinancierd door farmaceut |
|
Azad |
2003 |
Ziekenhuis |
Beide |
Onderzoeken attitude t.a.v. niet-farmaceutische interventies bij opgenomen patiënten met slaapproblemen die met benzodiazepines worden behandeld |
Survey (niet-vergelijkend), interview |
Opgenomen patiënten in 3e lijns ziekenhuis, gebruik benzodiazepines, insomnia (patiënt reported). Exclusie: IC, trauma, neurowe-tenschappelijk onderzoek, psychiatrie, ernstig delirium/demen-tie, angst of comorbiditeit die communicatie bemoeilijkt |
Eén interview, geen follow-up |
100 patiënten, 51% jonger dan 65 jaar, 15% ouder dan 75 jaar, 49% man, MMSE > 24 bij 92%, 88% kortdurend benzodiazepine-gebruik, 25% 1e keer benzodiazepine-gebruik, 73% inslaapprobleem, 54% doorslaappro-bleem, 32% 's ochtends vroeg wakker |
Interview |
- |
Mening in interview |
79% denkt dat benzodia-zepines hel-pen, 15% heeft bijwer-kingen, 44% wist van tevo-ren dat bij-werkingen konden op-treden, 22% heeft hier in-structie over gehad, 11% kreeg alterna-tieven aange-boden (bijv. slaaphygiëne), 55% had er-varing met niet-farma-ceutische interventies; 32% vond dat benzodiaze-pines beter werken. 82% vindt niet-farmaceuti-sche interven-ties gezonder; 67% accep-teert niet-far-maceutische interventies (vrouwen meer dan mannen, nieuwe ge-bruikers ben-zodiazepines meer dan chronische gebruikers) |
Geen vergelijkend onderzoek, moment-opname, mogelijk sociaal wenselijke antwoorden |
Laag |
Onderzoek sluit eigenlijk niet echt aan bij uitgangsvraag |
|
Barthlen |
2002 |
|
|
|
|
|
|
|
|
|
|
|
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Exclusie |
|
Baskett |
2003 |
Algemene bevolking |
Farma-ceutisch |
Onderzoeken of melatonine slaap verbetert bij ouderen met en zonder slaap-problemen, in algemene bevolking |
Dubbelblinde RCT |
|
|
|
|
|
|
|
|
|
Populatie sluit niet aan bij onderwerp richtlijn → exclusie |
|
Benkert |
2006 |
Extramuraal |
Farma-ceutisch |
Onderzoeken verschillen in werkingsmecha-nisme mitraza-pine en venlafa-xine bij patiën-ten met ernstige depressie |
Dubbelblinde RCT |
|
|
|
|
|
Niet gericht op slaap |
|
|
|
Populatie sluit niet aan bij onderwerp richtlijn → exclusie |
|
Beullens |
2002 |
Verpleeghuis |
Beide |
Onderzoeken verstorende factoren slaap in verpleeghuis, effect hypnoti-ca, reductie hyp-noticagebruik, non-farmacologische interventies |
Systematische review, literatuur-onderzoek; geen meta-analyse |
Artikelen over slaapproblemen in verpleeghuis, met objectief gemeten slaapparameters |
- |
22 artikelen, geen beschrijving populaties, interventies, e.d.; 9 artikelen over effect hypnotica; 9 over non-farmacologische interventies |
Verschillende |
Verschil-lende |
Objectieve maten voor slaap |
Geen verschil in slaapduur, slaapefficiën-tie, dutjes overdag, slaapklachten tussen wel en geen gebruik hypnotica; ri-sico op vallen hoger bij ge-bruik hypno-tica. Geïndivi-dualiseerde verzorging positief voor slaap, reductie licht en lawaai geassocieerd met minder slaapproble-men; licht-therapie heeft gunstige in-vloed op slaap/waak-ritme, sociale interactie mo-gelijk van in-vloed, licha-melijke activi-teit lijkt slaap-problemen te verminderen |
Groot, geen beschrijving onderliggende studies en patiënten, alleen kwalitatieve resultaten |
Zeer laag |
Geen kwantitatieve resultaten → exclusie |
|
Borazan |
2010 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken effect melatonine als preoperatieve medicatie bij prostatectomie op pijnstilling, slaapkwaliteit en sedatie |
RCT |
52 ASA I-II patiënten ge-pland voor elec-tieve prostatec-tomie, 50-56 jaar. Exclusie: hartfalen, hart-klepaandoening, lever- of nierfa-len, psychiatri-sche aandoe-ning, slaappro-bleem, chro-nisch pijnsyn-droom, mentaal probleem, mid-delenmisbruik |
|
|
|
|
|
|
|
|
Patiënten met slaapproblemen zijn uitgesloten van deelname → exclusie |
|
Boyle |
2012 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effect amitripty-line, duloxetine en pregabaline bij diabeten met perifere neuro-pathische pijn |
Dubbelblinde RCT |
Volwassenen met diabetes en neuropathische pijn |
36 dagen |
83 patiënten met diabetes en neuropathische pijn, gemiddeld 65 jaar oud, 57 mannen |
27 patiënten pregabaline, 28 duloxetine, 28 amitryptiline |
Zie interventie, placebo run-in |
Pijn, kwaliteit van leven, slaap-parameters, |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, geen placebo, beperkt aantal patiënten |
Laag |
Geen patiënten met nieuwe of verergerende slaapproblemen, geen intramu-rale populatie → exclusie |
|
Byles |
2003 |
Extramuraal |
Geen inter-ventie |
Onderzoek naar continuïteit en medicatiege-bruik bij slaap-problemen bij oudere vrouwen |
Prospectief cohortonder-zoek |
Vrouwen van 70-75 jaar in Australië, uit algemene bevolking |
3 jaar |
10421 vrouwen, gemiddeld 72 jaar, 16,5% gebruikte slaapmedicatie |
Geen |
Geen |
Vragenlijston-derzoek naar slaapkwaliteit en gebruik medicatie |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
|
|
Geen interven-tie onderzoek, populatie geen patiënten met nieuwe of verergerende slaapproblemen → exclusie |
|
Clarfield |
2006 |
- |
- |
- |
Commentaar op een review over chronische slaapklachten |
|
|
|
|
|
|
|
|
|
Artikel betreft commentaar op eerdere review, die niet aan de inclusiecriteria voldoet → exclusie |
|
Conn |
2006 |
Verpleeghuis |
Farma-ceutisch |
Overzicht geven van slaapstoor-nissen bij oude-ren in verpleeg-huizen en het management daarvan |
Narratieve review |
|
|
|
|
|
|
|
Zeer groot, narratief over-zichtsartikel, geen systematisch onderzoek |
Zeer laag |
Geen kwantitatieve resultaten → exclusie |
|
Cooke |
2009 |
Extramuraal |
Niet-farma-ceutisch |
Onderzoeken langetermijn resultaten CPAP bij patiënten met Alzheimer en OSAS |
Niet-experimenteel vergelijkend onderzoek |
Patiënten met Alzheimer en OSAS die al eerder aan een 6 weken durende RCT hadden meegedaan |
Gemiddeld 13,3 maanden (sd 5,2 maanden; range 6-21 maanden) |
10 patiënten met Alzheimer en OSAS (7 mannen) en 9 partners; gemiddelde leeftijd 76 jaar, matige dementie |
CPAP |
Geen CPAP |
Vragenlijst naar diverse neuropsycholo-gische uit-komsten en slaapuitkom-sten |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, weinig patiënten, geen randomisatie, geen blindering |
Zeer laag |
Onderzoek sluit niet aan bij uitgangsvraag, voor richtlijn zouden patiën-ten met beken-de slaapstoor-nissen als OSAS niet meegenomen worden → exclusie |
|
Corbett |
2005 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken patiënten-voorkeuren voor dexmede-tomidine of propofol bij mechanische ventilatie op de IC |
RCT |
Patiënten met electieve CABG en verwachte ventilatie <24 uur; exclusie: geen informed consent, overge-voeligheid medi-catie, ernstige hypotensie of bradycardie, nier- of leverin-sufficiëntie, postoperatief vereiste neuro-musculaire on-derdrukking, epidurale of spinale anesthe-sie, ernstige obe-sitas, alcohol- of drugsmisbruik, ernstige neuro-logische handicap |
Max. 48 uur intubatie |
89 patiënten, 73 mannen, gemiddelde leeftijd 63 jaar, 43 met dex-medetomidine, 46 met propofol |
Dexmedetomi-dine (1 μg/kg laaddosis iv in 15 minuten, daarna 0,4 μg/kg/uur iv) |
propofol (5 μg/kg/ minuut iv getitreerd binnen range 0,2-0,7 μg/kg /uur of 5-75 μg/kg/ min iv) |
Demografische en patiëntken-merken, klinische parameters, bijwerkingen, vragenlijst (ge-modificeerde Hewitt sedation questionnaire) |
Omtrent slaap-parameters: Geen verschil tussen beide groepen op vraag 'How easy was it to sleep?'; overige vragen meer gericht op communicatie en angst e.d. |
Relatief laag, maar beperkte scope van patiënten; het is de vraag of de resultaten extrapoleer-baar zijn naar andere patiënten-groepen, geen blindering, niet alleen ouderen |
Matig |
Beperkte scope van patiënten |
|
Dowling |
2008 |
Verpleeghuis |
Beide |
Onderzoeken effect lichttherapie en melatonine op circadiane ritme en slaapritme, bij patiënten met Alzheimer |
RCT |
Bewoners van twee verpleeghuizen in VS, met Alzheimer en verstoring rust-activiteit ritme |
11 weken |
50 patiënten, 43 vrouwen, gemiddelde leeftijd 86 jaar (sd 9, range 60-100); patiënten in controlegroep significant jonger. 15 patiënten met daglichtlampen en melatonine, 18 met bright light en placebo, 17 controles |
Ochtend bright light (>2500 lux) blootstelling + melatonine (5 mg) 's avonds versus ochtend daglichtlampen blootstelling + placebo 's avonds |
Alleen 'gewoon' licht (150-200 lux) |
Activiteiten en rust middels Actiwatch (actigraphy) |
Geen ver-schillen tus-sen groepen met bright light + place-bo en contro-le. Bij verge-lijking daglichtlampen + mela-tonine met controle: minder slaap overdag, min-der dutjes overdag, meer activiteiten overdag en betere dag-nacht slaap-verdeling (re-gressieanalyse). Dus: alleen daglichtlampen lijkt onvol-doende om slaapkwaliteit te verbeteren. Combinatie met melatoni-ne lijkt effectiever. |
Groot geen blindering, beperkt aantal patiënten, niet bekend welk resultaat van welke interventie komt |
Laag |
Patiëntengroep sluit niet helemaal aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem |
|
Dowling |
2005 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effect lichttherapie op slaapritme, bij patiënten met Alzheimer |
RCT |
Bewoners twee verpleeghuizen in VS, met Alz-heimer en sta-biele medicatie; exclusie: overige neurologische diagnoses, gebruik van valeriaan, melatonine of slaappillen |
11 weken |
70 patiënten, gemiddeld 84 jaar (sd 10, range 58-98), 57 vrouwen. 29 's ochtends daglichtlampen, 24 's middags daglichtlampen, 17 controles |
Ochtend of middag daglichtlampen (>2500 lux), activiteiten in lichte ruimte of buiten |
Normaal licht (150-200 lux) en activi-teiten in gebruike-lijke omgeving |
Activiteiten en rust middels Actiwatch (actigraphy) |
Geen significante verschillen tussen groepen voor slaap- en waakparame-ters |
Behoorlijk: geen blindering, beperkt aantal patiënten, niet bekend welk resultaat van welke interventie komt |
Matig |
Patiëntengroep sluit niet hele-maal aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem; bovendien: gro-te overeenkom-sten met Dow-ling 2007, wel-licht dubbeling |
|
Dowson |
2012 |
Verpleeghuis |
Beide |
Onderzoeken evidence-based strategieën om slaap te verbeteren in verpleeghuizen |
Narratieve review |
|
|
|
|
|
|
|
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie. |
|
Epstein |
2007 |
Extramuraal |
Niet-farma-ceutisch |
Onderzoeken effectiviteit cog-nitieve gedrags-interventie om chronische in-somnia te be-handelen bij borstkanker survivors |
RCT |
Vrouwen, ten minste 3 maan-den na primaire behandeling borstkanker met insomnia gedu-rende 3 maan-den, die functio-neren overdag beïnvloedt; ex-clusie: cognitieve stoornis, OSAS, restless leg syn-drome, ernstige psychopatholo-gie |
6 weken |
81 patiënten, gemiddeld 58 jaar. In follow-up: 34 in interventiegroep, 38 in controle, langdurige insomnia (gemiddeld 6 jaar) |
Multicompo-nent interven-tie (stimulus controle, slaap beperking, slaapeducatie en slaaphygië-ne) |
Slaapedu-catie en slaaphygi-ëne |
Actigraphy, dagboek, vragenlijsten |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, geen blindering, forse lost-to-follow-up, geen intention-to-treat |
Laag |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem → exclusie |
|
Erman |
2006 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effectiviteit, veiligheid en dosis-respons van ramelteon bij patiënten met chronische insomnia |
Dubbelblinde RCT, met vijfmaal cross-over |
Patiënten met chronische insomnia van 18-64 jaar uit algemene bevolking |
steeds 2 weken behandeling, dan 5-12 dagen wash-out |
107 patiënten, leeftijd 18-64 jaar, geen verdere info over patiënten |
Ramelteon (in verschillende doseringen) |
Placebo |
Inslaaptijd, slaapstadia, subjectieve slaapkwaliteit, alertheid, veiligheid |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Laag |
Hoog |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, geen ouderen → exclusie |
|
Fetveit |
2004 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken duur effect behandeling met daglichtlampen bij patiënten met dementie |
Cohort-onderzoek |
Patiënten uit eerder onderzoek, follow-up data |
2 weken pretreatment, 2 weken behandeling, daarna bepaling effect na 4, 8, 12 en 16 weken |
11 patiënten met matige tot ernstige dementie, 10 vrouwen, gemiddelde leeftijd 86 jaar (sd 9, range 72-101); alle patiënten hadden comorbiditeit en gebruikten veel medicatie |
Daglichtlampen, 2 uur 's ochtends 6000-8000 lux |
Geen |
Actigraphy, statusonder-zoek |
Auteurs con-cluderen ge-vonden effect dat tot 12 we-ken na behan-deling aan-houdt; dat geldt maar voor 1 varia-bele (sleep onset laten-cy). Wanneer gekeken wordt naar slaapkwaliteit tussen 23,00 en 7,00 uur is effect veel kleiner en mogelijk kli-nisch niet relevant |
Zeer hoog, weinig patiënten, geen vergelijkend onderzoek, forse uitval, geen randomisatie, geen blindering, geen gecontroleerde omstandig-heden |
Zeer laag |
Geen nieuw of verergerend slaapprobleem, mogelijk toch relevant |
|
Fetveit |
2003 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effect daglichtlampen bij patiënten met dementie en slaapproblemen |
Cohortonder-zoek |
Patiënten uit eerder onderzoek |
2 weken pretreatment, 2 weken behandeling |
Zie Fetveit 2004 |
Zie Fetveit 2004 |
Zie Fetveit 2004 |
Actigraphy, statusonder-zoek |
Slaapefficiën-tie verbeterde met 13% (95%BI 5-21), inslaapduur gemiddeld een uur kor-ter (95%BI 0,17-1,44), ook andere parameters significant verbeterd; dat geldt ook voor door de staf geëvalu-eerde parameters |
Zie Fetveit 2004 |
Zeer laag |
Zie Fetveit 2004 |
|
Fetveit |
2005 |
|
|
|
|
|
|
|
|
|
|
|
|
|
is dubbelpublicatie van Fetveit 2004 → exclusie |
|
Florete |
2008 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effect tramadol met vertraagde afgifte op aan pijn gerelateerde slaapparameters bij patiënten met osteoarthritis |
Post-hoc analyse van dubbelblinde RCT |
Patiënten >18 jaar met osteoarthritis van knie of heup |
12 weken |
1608 patiënten tussen 20 en 80, gemiddelde leef-tijd 59, 37% man; 403 met tramadol 100, 400 met tramadol 200, 400 met tramadol 300 en 405 placebo |
Tramadol met vertraagde afgifte 100, 200 of 300 mg 1 dd |
Placebo |
Slaapkwaliteit gemeten met Chronic Pain Sleep Inventory |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, zeer forse uitval (46%), waarschijnlijk selectief vanwege onvoldoende effect en bijwerkingen |
Laag |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, geen ouderen → exclusie |
|
Fukuda |
2001 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effect daglichtlampen bij patiënten in geriatrisch ziekenhuis |
Case reports |
4 cases |
3 weken lichtexposi-tie bij lunch, effectmeting ook 3 weken voor en na lichtexposi-tie |
4 vrouwelijke patiënten (68, 87, 92 en 93 jaar), 2 met dementie, allen met slaapproblemen (divers) |
Daglichtlampen, 1 uur tijdens lunch, 8000 lux |
Geen |
Polysomnografie |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, geen vergelij-kend onder-zoek, zeer weinig patiën-ten, geen ge-controleerde omstandig-heden |
Zeer laag |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem + zeer grote kans op bias → exclusie |
|
Garzan |
2009 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken effect melatonine op slaap en gedrag bij ouderen en het discontinueren van hypnotica |
Dubbelblinde RCT met cross-over design |
Patiënten van 'community health centers', leeftijd >65 jaar, met insomnia of voorbijgaande slaapproblemen door stress. Exclusie: secundaire slaapstoornis, autoimmuun-ziekten, tumoren, dementie, psychose of andere ernstige psychische aandoening |
18 weken |
22 patiënten, 15 vrouwen, gemiddelde leeftijd 75 jaar, 20 met chronische slaapproblemen, 14 met gebruik van hypnotica |
8 weken 5 mg melatonine 1 dd 's avonds; 2 weken wash-out, 8 weken placebo, met stimulans om dosering hypnotica te reduceren gedurende de interventie |
Zie interventie |
Northside Hospital Sleep Medicine Institute Test (score 0-8), slagingskans om hypnotica te verminderen, bijwerkingen |
Geen verschil in slaapscore tussen place-bo en baseli-ne. Wel tus-sen melatoni-ne en baseline (3,7 (sd 0,40); p<0,005) (verschil met placebo: p< 0,025). 9/14 patiënten luk-te het te stop-pen met hyp-notica tijdens melatoninefa-se en niet tij-dens placebo, 1/14 stopte zowel tijdens melatonine als tijdens pla-cebo, 4/14 continueer-den hypnotica |
Behoorlijk weinig patiënten, beperkte beschrijving resultaten |
Laag |
Niet per se sprake van nieuw of verergerend slaapprobleem, meeste patiënten met chronisch slaapprobleem, mogelijk toch interessant |
|
Gordon |
2010 |
Verpleeghuis |
Beide |
Overzicht slaap-problemen in verpleeghuizen en interventies daarbij |
Narratieve review |
|
|
|
|
|
|
|
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onder-zoek |
Zeer laag |
Geen kwantita-tieve resultaten → exclusie |
|
Greco |
2004 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken associatie tussen routinegebruik psychoactieve medicatie en slaapkwaliteit bij bewoners verpleeghuis |
Dwarsdoor-snede onderzoek |
Bewoners ver-pleeghuis die hulp nodig heb-ben als ze 's nachts het bed uit moeten; ex-clusie: kortver-blijf, terminaal zieken, tremor in rust; ten min-ste drie dagen data |
Dataverza-meling gedurende 3 nachten |
210 bewoners, van wie er 80% data van 3 nach-ten hadden, ge-middelde leeftijd 84 (sd 8,3), 79% vrouw. 109 pati-ënten gebruikte psychoactieve medicatie, 59 patiënten niet |
Geen |
Geen |
Actigraphy |
Lage slaap-kwaliteit in hele popula-tie, lijkt wat beter in groep die psychoac-tieve medica-tie gebruikt, maar geen statistisch significant resultaat |
Groot, geen experimenteel design, dus waarschijnlijk onvergelijkbaarheid groepen, geen resultaten in de tijd, grote kans op vertekening |
Laag |
Geen nieuwe of verergerende slaapproblemen, mogelijk toch relevant |
|
Guelfi |
2001 |
Ziekenhuis |
Farma-ceutisch |
Vergelijken ef-fectiviteit en tolerantie van mirtazapine en venlafaxine bij patiënten met een ernstige depressie met melancholieke kenmerken |
Dubbelblinde RCT |
Opgenomen pa-tiënten met ern-stige depressie tussen 18-65 jaar; exclusie: > 12 maanden de-pressie, >2 eer-dere depressies die niet goed re-ageerden op an-tidepressiva, geen respons op eerdere medica-tie, sterke verbe-tering bij place-bo, suïcidaal, verschillende ty-pen depressie, angststoornissen, eetstoornissen, epilepsie, midde-lenmisbruik, psychotische aandoeningen, zwangeren of at risk, instabiele psychische aan-doening, abnor-male bevindin-gen bij lichame-lijk of laborato-riumonderzoek |
8 weken |
157 patiënten, gemiddelde leeftijd 45 jaar, 34% man, 78 met mirtazapine, 79 met venlafaxine |
Mirtazapine 8 weken |
Venlafaxi-ne 8 weken |
Veel uitkomstmaten op gebied van depressie en kwaliteit van leven, 1 parameter voor slaapstoornissen (HAM-D-17 sleep disturbance) |
Alleen voor slaapproblemen: mirtazapine scoorde beter dan venlafaxine op HAM-D-17 sleep disturbance (verschil 1,0; 95% BI: 0,5-1,6) |
Zeer laag |
Zeer hoog |
Het is niet bekend of het gevonden effect klinisch relevant is. Zeer beperkte patiëntengroep door grote hoeveelheid exclusiecriteria. Daarnaast: geen ouderen in patiëntenpopulatie en geen nieuwe of verergerende slaapproblemen →exclusie |
|
James |
2010 |
Extramuraal |
Farma-ceutisch |
Vergelijken effectiviteit en veiligheid buprenorphine patch met sublinguale toediening bij patiënten met osteoarthritis |
Dubbelblinde RCT |
Patiënten met osteoarthritis van knie/heup met matige-ern-stige pijn, leef-tijd 18-80; exclu-sie: opioïden in laatste 5 weken, langwerkende NSAID's in laatste 7 dagen, intraarticulaire injectie in laatste 6 weken, overige chronische pijn-patiënten en ge-wrichtsaandoe-ningen anders dan osteoarthritis |
Titratieperio-de van 21 dagen, dan behandeling 7 dagen |
238 patiënten, 37% man, gemiddelde leeftijd 64 jaar (range 42-81), 118 met patch, 120 met sublinguale tabletten |
Transdermale patch buprenorfine |
Sublingua-le tablet buprenor-fine |
Pijnintensiteit, gebruik nood-medicatie, slaap-stoornissen, kwaliteit van leven, acceptatie behandeling, veiligheid, gemak patch |
Alleen voor slaapproblemen: aantal nachten ont-waakt vanwe-ge pijn nam af in beide groepen van ongeveer 4 gemiddeld tot ongeveer 2,6 gemiddeld. Dit verschil is waarschijnlijk niet statistisch significant. Er is geen ver-schil tussen beide behan-delgroepen |
Groot, goed opgezet onderzoek, maar zeer forse uitval (>50%), met name vanwege het niet aangeven van alle pijnscores |
Laag |
Geen nieuwe of verergerende slaapproblemen, niet intramuraal en niet alleen oudere patiënten → exclusie |
|
Koba-yashi |
2001 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effectiviteit blootstelling aan daglichtlampen bij lunch op slaap-waakverhouding bij patiënten met slaappro-blemen in een geriatrisch ziekenhuis |
Voor-na vergelijking |
Niet genoemd |
3 weken lichtexposi-tie tijdens lunch, ef-fectmeting ook 3 weken voor en na lichtexposi-tie |
10 patiënten in geriatrische instelling, 6 vrouwen, gemiddelde leeftijd 81 jaar (sd 8,8) met verschillende slaapproblemen, 2 patiënten zonder dementie |
Daglichtlampen bij lunch 1 uur, gedurende 3 weken, 8000 lux |
Geen |
Door ver-pleegkundigen gerapporteerde waarnemingen (gemodificeer-de Matsubara Yamaguch radar) |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, geen vergelij-kend onder-zoek, zeer weinig patiën-ten, geen ge-controleerde omstandighe-den |
Zeer laag |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem + zeer grote kans op bias → exclusie |
|
Kosinski |
2007 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effect tramadol met vertraagde afgifte op aan pijn gerelateerde slaapparameters bij patiënten met osteoarthritis |
Dubbelblinde RCT |
Patiënten met osteoarthritis van knie/heup met pijnmedica-tie; exclusie: an-dere ziekte die niet onder con-trole is, andere arthritis, chroni-sche pijn, mid-delenmisbruik, gebruik medica-tie met interactie met tramadol |
12 weken |
1020 patiënten, gemiddelde leef-tijd 58 (sd 10), 62% vrouw; 202 met tramadol 100, 201 met tramadol 200, 201 met tramadol 300, 202 met tramadol 400, 205 placebo |
Tramadol met vertraagde afgifte 100, 200 of 300 mg 1 dd |
Placebo |
Pijn op VAS schaal, slaapkwaliteit met Chronic Pain Sleep Inventory |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, zeer forse uitval (45%), waarschijnlijk selectief vanwege onvoldoende effect en bijwerkingen |
Laag |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, geen ouderen → exclusie |
|
Krish-nan |
2008 |
|
Niet-farmaceu-tisch |
Overzicht geven diagnostiek en management geriatrische in-somnia door nurse practitioners |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
Krystal |
2008 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effectiviteit zolpidem met vertraagde afgifte gedurende 6 maanden bij patiënten met chronische insomnia |
Dubbelblinde RCT |
Patiënten met insomnia 18-64 jaar; exclusie: mensen met on-regelmatige diensten, >3 dutjes/week, >5 xanthinedrank-jes/week, ge-bruik slaapmedi-catie, primaire hypersomnie, narcolepsie, slaapstoornissen gerelateerd aan longen, hart of circadiane ritme, |
25 weken |
1025 patiënten met insomnia, 39% man, gemiddelde leeftijd 46 jaar (sd 11); 669 patiënten met zolpidem vertraagde afgifte, 349 met placebo |
Zolpidem 12,5 mg, max. 1 per dag, 3-7 keer per week |
Placebo |
Patiënt Global Impression, Clinical Global Impression, Patiënt Monitoring Questionnaire, Espworth Sleepiness Scale |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Klein, prima opgezette studie, primai-re uitkomst-maat wellicht wat discutabel. Maar, patiën-tengroep niet van toepassing op uitgangs-vraag |
Hoog |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, geen ouderen → exclusie |
|
Li Pi Shan |
2004 |
Verpleeghuis |
Farma-ceutisch |
Vergelijken effectiviteit lorazepam en zopiclon bij patiënten met een beroerte of hersenbeschadi-ging en insomnia |
Dubbelblinde RCT |
Patiënten op een revalidatieafde-ling met een beroerte of hersenbeschadi-ging die klaagden over insomnia; exclusie: acuut zieken, geen Engels/Frans, geen vragenlijst kunnen beantwoorden (bijv. afasie of posttraumati-sche amnesie) |
14 dagen |
18 patiënten, 10 mannen, gemiddelde leeftijd 57 jaar (range 20-78), 12 patiënten met beroerte (gemiddelde leeftijd 64 (range 46-78)) |
7 dagen 0,5-1,0 mg lorazepam, daarna 7 dagen 3,75-7,5 mg zopiclon; patiënt regelt zelf dosering |
Zie interventie, maar andersom |
Door patiënten gerapporteerde slaapkwaliteit, door verpleegkundigen gerapporteerde slaaptijd |
Totale slaap-tijd: 7,5 (sd 0,8) uur in lo-razepamgroep, 7,2 (sd 0,6) uur in zopi-clonegroep (p=0,09). Vergelijkbare scores door patiënten voor beide middelen op slaapkwaliteit, slaapdiepte, fitgevoel, alertheid en vermoeidheid (geen signifi-cante ver-schillen). Ver-gelijkbare scores door verpleegkundi-gen op alert-heid en fitge-voel (geen significante verschillen). Geen ver-schillen in subgroepana-lyses van pati-ënten met een beroerte |
Zeer groot: Geen wash-out periode; tegelijkertijd met interventie werden ook niet-farmaco-logische maatregelen getroffen, geen vergelijking met placebo, zeer weinig patiënten |
Zeer laag |
Het onderzoek is gedaan op een revalidatie-afdeling, acuut zieken zijn uitgesloten, beperkt aantal ouderen → onderzoek heeft beperkte waarde |
|
Lundahl |
2012 |
Slaaplabora-torium |
Farma-ceutisch |
Vergelijken effecten gaboxadol en zolpidem bij patiënten met primaire insomnia |
Post-hoc analyse van 2 dubbelblinde RCT's |
Patiënten met primaire insomnia van 18-65 jaar |
2 nachten in slaaplabora-torium voor beide medi-catie met 7-14 dagen ertussen |
66 patiënten, 45 vrouwen, gemid-delde leeftijd 34 (sd 11) |
Gaboxadol (in verschillende doseringen) |
Zolpidem 10 mg en placebo |
EEG analyse |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Behoorlijk: post-hoc analyse, dus niet gepland, mogelijke vertekening. |
Matig |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, geen ouderen, geen patiëntre-levante uit-komstmaten → exclusie |
|
Lyseng-William-son |
2012 |
Beide |
Farma-ceutisch |
Overzicht geven van melatonine met vertraagde afgifte bij patiënten met insomnia >55 jaar |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie. |
|
Maho-wald |
2007 |
Beide |
Beide |
Algemeen inlei-dend artikel over slaappro-blemen bij geriatrische patiënten |
Algemeen inleidend artikel zonder referenties |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie. |
|
Martin |
2007 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effectiviteit mul-ticomponent niet-farmacolo-gische interven-tie om slaap-waakritme te verbeteren bij verpleeghuis-bewoners |
RCT |
Bewoners verpleeghuis > 65 jaar, die niet aan bed gebonden of geïsoleerd zijn, met slaperigheid overdag of slaapstoornissen 's nachts |
5 dagen interventie |
118 patiënten in randomisatie, gemiddelde leeftijd 86 jaar (sd 9), 77% vrouw, 53% blank, waarschijnlijk groot aandeel met delirium of dementie, niet specifiek met nieuw of verergerend slaapprobleem |
Overdag: sti-mulans uit bed te blijven, ≥30 minuten zonlicht bui-ten, 3 maal/ dag deelname fysiek activi-teiten pro-gramma. Avond: min-der geluid, lichten uit, persoonlijke zorg. Nacht: minimaal licht en geluid, zorg als patiënt wakker is en niet op gezette tijden |
Usual care |
Activiteiten en rust middels Actiwatch (actigraphy) |
Zelfde studie als Alessi 2005 |
Wel randomi-satie, maar geen blinde-ring (is ook niet mogelijk bij deze interventie) |
Matig |
Is zelfde studie als Alessi 2005 → exclusie |
|
Martin |
2007 |
Beide |
Beide |
Overzichtsarti-kel over kwali-teitsindicatoren voor slaapstoor-nissen bij kwets-bare ouderen |
Overzichts-artikel |
|
|
|
|
|
|
|
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
McMil-lan |
2003 |
Niet vermeld |
Beide |
Comment bij artikel over cog-nitieve gedrags-therapie om benzodiazepine te stoppen bij patiënten met chronische insomnia |
Commentaar op een RCT |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, geen studie |
Zeer laag |
Comment → exclusie (RCT waarop com-mentaar is ge-geven behoeft niet te worden geïncludeerd, want gaat over patiënten met chronische insomnia) |
|
Mishima |
2005 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken slaapbevorderen-de werking pas-sieve lichaams-verwarming bij oudere patiënten met vasculaire dementie en insomnia |
Voor-na vergelijking |
Bewoners verpleeghuis met vasculaire dementie en insomnia |
13 dagen |
13 patiënten > 70 jaar (gemiddelde leeftijd 77 jaar), 11 vrouwen |
7 dagen pre-studie, dan 6 dagen trialses-sie: 3 dagen baseline (ver-boden te sla-pen buiten slaapkamer, verlichting <10 lux in slaapperiode, urineren voor slapen), daar-na 2 dagen passieve lic-haamsverwar-ming (half uur in bad 40 gra-den, 2 uur voor slapen gaan), 1 dag postmeting |
Geen |
Actigraphy, melatonine-levels, hartritme |
Slaapparame-ters: de tijd om in slaap te komen nam af van gemiddeld 27 minuten naar 16 minuten (p<0,02); overige verschillen niet statistisch significant |
Zeer groot, geen vergelijkend onderzoek, zeer weinig patiënten, geen gecontroleerde omstandighe-den; grote kans dat resultaten het gevolg zijn van toeval of andere interventies dan de passieve lichaamsver-warming |
Zeer laag |
Geen nieuwe of verergerende slaapproblemen, mogelijk toch relevant, maar kwaliteit is laag. Klinische relevantie gevonden effect laag. |
|
Molinari |
2013 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken of mental health assessment het gebruik van psychoactieve middelen zou kunnen verminderen |
Pilot studie |
Nieuwe verpleeghuisbewoners VS |
|
23 nieuwe ver-pleeghuisbewo-ners (interven-tie) + 25 contro-lebewoners verpleeghuis, 94% >60 jaar, 57% vrouw |
Mental health assessment, niet specifiek gericht op slaap-problemen |
Geen mental health assess-ment |
Medicatievoor-schrift psycho-actieve farma-ca, gebruik ge-dragsinterven-ties, zieken-huisopname, vallen |
T.a.v. slaap-problemen: assessment-groep: 1 pa-tiënt stopte met slaapmid-delen, in con-trolegroep geen (geen significant verschil); in assessment-groep startten 2 mensen (9%) met slaapmedica-tie, in contro-legroep 10 mensen (40% ); p=0,013 |
Groot, geen randomisatie, verschil in populatie tussen beide groepen (nieuwe bewoners vs. bestaande bewoners); gevonden resultaten waarschijnlijk niet alleen afhankelijk van mental health assessment |
Laag |
Niet bekend of het om nieuwe of verergerende slaapproblemen gaat |
|
Morin |
2004 |
Extramuraal |
Niet-farma-ceutisch |
Onderzoeken of medicatie afbouwen onder toezicht en/of cognitieve gedragstherapie het gebruik van benzodiazepine verminderen bij ouderen en het effect daarvan op het slaappatroon |
RCT |
Leeftijd > 55, gebruik benzo-diazepine voor slaapprobleem, langdurige slaap-problemen, ver-minderd functi-oneren overdag; exclusie: insom-nia gerelateerd aan andere ziek-te, slaapapneu of bewegende lede-maten tijdens slaap, psycho-therapie, gebruik psychoactieve farmaca anders dan benzodiaze-pinen, depressie of andere ernsti-ge psychopatho-logie |
10 weken behandeling met voor- en nadien 2 weken dagboek |
76 patiënten met slaapproblemen, gemiddelde leeftijd 63 (range 55-82), 38 mannen; 24 in groep cognitieve gedragstherapie, 25 in groep medicatie aanpassing onder supervisie, 27 met beide interventies; gemiddelde duur insomnia 22 jaar en gemiddeld 19 jaar benzo-diazepinegebruik |
1. medicatie aanpassing onder super-visie; 2. cogni-tieve gedrags-therapie; 3. combinatie van 1 en 2 |
Zie interventie |
Slaapdagboek, polysomno-grafie |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, geen blindering, forse hoeveel-heid data (dus kans op signi-ficantie alleen al daardoor groot), geen placebogroep of groep met geen interven-tie |
Laag |
Geen nieuwe of verergerende slaapproblemen, geen opgenomen patiënten → exclusie |
|
Mulsant |
2004 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken effectiviteit en veiligheid ris-peridon en olanzapine als antipsychotica bij patiënten met dementie |
Dubbelblinde RCT |
Patiënten >55 jaar met Alzhei-mer, vasculaire dementie of dementie van andere oorzaak, ten minste 1 jaar dement, en psy-chotische symp-tomen, MMSE tussen 7 en 26. Exclusie: deliri-um, onvermo-gen om orale medicatie te ne-men, psychose voor dementie diagnose |
6 weken, 80% follow-up |
86 patiënten, gemiddeld 84 jaar, 78% vrouw, MMSE gemiddeld 13,5, voornamelijk Alzheimer dementie, gemiddeld 12 jaar opgenomen in verpleeghuis |
Risperidon, getitreerd tot maximaal 1,5 mg/dag |
Olanzapi-ne, getri-treerd tot maximaal 10 mg/ dag |
Perifere anti-cholinerge effecten, symptomen, cognitieve assessment, bloedonder-zoek |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Laag |
Hoog |
Patiëntengroep sluit niet aan bij uitgangsvraag, geen nieuw of verergerend slaapprobleem, alleen gekeken naar slaappro-blemen als bijwerking medicatie bij dementie → exclusie |
|
Nagel |
2003 |
Verpleeghuis |
Beide |
Overzicht slaapproblemen in verpleeghui-zen en interven-ties daarbij |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
Potvin |
2012 |
Extramuraal |
Geen inter-ventie |
Onderzoeken prevalentie stemmingsstoor-nissen, angst-stoornissen, in-somnia en ben-zodiazepine af-hankelijkheid bij ouderen met cognitieve be-perkingen zon-der dementie |
Dwarsdoor-snede onderzoek |
Thuiswonende ouderen in Quebec, random sampling, MMSE ≥ 22, medische gegevens beschikbaar, niet dement, in staat tot interview |
Geen |
2414 mensen, gemiddelde leeftijd 74 jaar, 58% vrouw, 9,7% met cognitieve beperking |
Geen |
Geen |
Stemming, angst, insom-nia, benzodia-zepine afhan-kelijkheid |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Voor het doel van het onderzoek niet zo'n groot risico op bias, maar resultaten niet relevant voor evidence review |
|
Geen nieuwe of verergerende slaapproblemen, geen opgenomen patiënten, geen interventie → exclusie |
|
Richards |
2011 |
Verpleeghuis |
Niet-farm-aceutisch |
Onderzoeken effecten krachttraining, looptraining, sociale activiteiten en de combinatie daarvan op nachtelijke slaap |
RCT |
Bewoners van 13 verpleeghuizen in VS, ≥ 55 jaar, MMSE tussen 4 en 29, < 7 uur slaap 's nachts, > 30 minuten slaap overdag, kan zelfstandig staan, stabiele medicatie. Exclusie: terminale status, niet genezen kanker, behandeling met chemotherapie of steroïden, niet stabiele cardiovasculaire aandoening |
7 weken, 15% lost-to-follow-up |
193 deelnemers, gemiddelde leeftijd 82 jaar (range 57-90), 60% vrouw, veel comorbiditeit (bijv. hypertensie, depressie, hartaandoening, incontinent); 55 in groep fysieke oefening, 50 in groep sociale activiteiten, 41 in groep fysieke oefening + sociale activiteiten, 47 usual care |
1. Fysieke oefening: krachttraining van heup en arm, inclusief warm-up en cool-down + wandeloefeningen; 2. Sociale activiteit: 1 uur per dag individuele sociale activiteiten, bijv. spelletjes, muziek, sport, koken. 3. combinatie van 1 en 2 |
Usual care |
Polysomnogra-fie bij start en einde studie, primaire uitkomst: totale nachtelijke slaap, secundair: overige slaapparameters; actigraphy voor dutjes overdag |
Nachtelijke slaap gemid-deld in minu-ten: 341 in groep met fysieke oefe-ning, 342 in groep met sociale activi-teiten, 364 in combinatie-groep en 329 bij usual care. Combinatie-groep statis-tisch signifi-cant hoger dan usual care (p=0,01), overige verge-lijkingen niet statistisch sig-nificant. ≥ 60 minuten meer slaap 's nachts: 29% in groep met fysieke oefe-ning, 32% in groep met so-ciale activitei-ten, 46% in combinatie-groep en 19% bij usual care (geen statisti-sche toets) |
Behoorlijk, te kleine groepen om power te halen, geen blindering, onderzoekers proberen significante resultaten te vinden door voor-na vergelijkingen te doen, maar dat was niet de opzet (vergelijking vier groepen na interventie) |
Matig |
Geen nieuwe of verergerende slaapproblemen, mogelijk toch relevant. Het is de vraag of de gevonden resultaten klinisch relevant zijn |
|
Richards |
2013 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken gebruik zolpidem |
Dwarsdoor-snede onderzoek |
Patiënten zie-kenhuis (ortho-pedie, hartpati-ënten, stroke unit, oncologie), ≥ 50 jaar, ge-bruik zolpidem in ziekenhuis. Exclusie: zolpi-demgebruik voor opname |
Geen |
410 patiënten, 83% orthopedisch, 54% vrouw, gemiddelde leeftijd 71 (sd 11) |
Geen |
Geen |
Mentale assessment |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot, diverse confounders mogelijk, wei-nig gegevens bekend, geen vergelijkende interventiestu-die |
Laag |
Studie niet gericht op effect behande-ling slaapstoor-nissen → exclusie |
|
Riemers-ma |
2008 |
Verpleeghuis |
Beide |
Onderzoeken langetermijn effecten daglichtlampen en melatonine op cognitieve systeem bij verpleeghuis-patiënten |
RCT, 2x2 factorial design |
Bewoners ver-zorgingshuizen; exclusie: gebruik monoamine oxidase remmers, langdurig gebruik NSAID's, ernstige lever- of nierfunctiestoor-nissen, afakie (geen lens) |
Tot 3,5 jaar, gemiddeld 15 maanden (sd 12) |
189 verpleeghuispatiënten, gemiddelde leeftijd 86 (sd 5,5), 90% vrouw, 92% vorm van dementie; 49 patiënten alleen licht, 46 alleen melatonine, 49 licht + melatonine, 45 dubbel placebo |
1. Lichtexpositie: 9,00-18,00 uur 1000 lux; 2. melatonine 2,5 mg 1 uur voor bedtijd |
1. Controle-licht, lagere intensiteit, grotere afstand; 2. Placebo-tablet |
Primaire: cognitieve status met MMSE; secundair: stemming, eigen waardering, psychopatholo-gie, gedrag, ADL, actigraphy, slaaptijd, nachtelijke ontwaking |
M.b.t. slaap-parameters: slaapefficiën-tie beter bij gecombineer-de interventie (3,5%; p= 0,01), eerder in slaap bij gebruik mela-tonine (8 mi-nuten, p= 0,02), totale slaapduur ho-ger bij licht (10 minuten; p=0,04) en melatonine (27 minuten; p=0,004), maar niet bij combinatie, minder nach-telijke ruste-loosheid bij combinatie (1 minuut/uur; p=0,01), min-der waakperi-oden 's nachts met combina-tie (0,5; p= 0,01), kortere ontwaakperio-des 's nachts bij melatoni-ne (6 minu-ten, p=0,02) |
Behoorlijk, randomisatie van lichtexpo-sitie per ver-zorgingshuis, grote kans op andere verstorende variabelen; daarnaast zeer forse drop-out (maar dat is ook wel logisch gezien de populatie en de lange follow-up) |
Matig |
Geen nieuwe of verergerende slaapstoornis-sen, mogelijk toch relevant; geen echte lijn in resultaten, veel relaties met andere uitkomstmaten, het is de vraag of de gevonden resultaten klinisch relevant zijn |
|
Ronda-nelli |
2011 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken effectiviteit en veiligheid combinatie melatonine, magnesium en zink, voor het verbeteren van de slaapkwaliteit en de alertheid 's ochtends bij ouderen > 70 jaar met primaire insomnia |
Dubbelblinde RCT |
Verpleeghuispati-enten, met ten minste 3 maanden verblijf, > 70 jaar, primaire insomnia; exclusie: slaapstoornissen door een bekende oorzaak, psychiatrische of neurologische diagnose, restless legs, medicatie die het centraal zenuwstelsel of het slaapwaakritme beïnvloedt, gebruik bètablokkers |
8 weken |
43 patiënten, 63% vrouw, gemiddelde leeftijd 78 jaar (sd 4); 22 in interventiegroep, 21 placebo |
100 gram peerpulp met 5 mg melatonine, 225 magnesium en 11,25 mg zink, 1 uur voor bedtijd |
100 gram peerpulp zonder toevoegin-gen |
Primair: slaapkwaliteit (Pittsburgh Sleep Quality Index); verder: Leeds Sleep Evaluation Questionnaire, Epworth Sleepiness Scale, Sleep-Wake Activity Inventory, Short Insomnia Questionnaire, Actigraphy), veranderingen in slaapkwaliteit en activiteit overdag, stemming, kwaliteit van leven, voedings-toestand, bijwerkingen |
Pittsburgh Sleep Quality Index: behan-deleffect (in-terventie vs controle): 6,8 punten (95% BI: 5,4-8,3; p<0,001); PSQI<5: 59% in inter-ventiegroep, 14% in con-trolegroep (verschil 45 (95%BI: 20-70; p=0,004); ook signifi-cante resulta-ten op secun-daire uit-komsten (bijv. Leeds Sleep Evalua-tion Questi-onnaire), maar niet op Epworth Sleepiness Scale; secun-daire resulta-ten zijn hier niet gerappor-teerd want geven waar-schijnlijk dub-beling van de resultaten op de primaire uitkomstmaat |
Laag, er is sprake van blok randomisatie, het is de vraag of blindering gegarandeerd kan zijn |
Hoog |
Geen nieuwe of verergerende slaapproblemen, mogelijk toch relevant; het is niet duidelijk welk van de componenten van de interventie in welke mate bijdraagt aan het resultaat |
|
Rosz-kowska |
2010 |
Beide |
Beide |
Overzicht insomnia bij geriatrische patiënten en het beleid daarbij |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
Ruths |
2004 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken effect stoppen antipsychotica bij patiënten met dementie op gedrag en slaapkwaliteit |
Dubbelblinde RCT |
Verpleeghuispati-ënten met de-mentie die anti-psychotica ge-bruiken, gebruik risperidon, olan-zapine of halo-peridol ≥3 maanden in sta-biele dosering, ≥ 65 jaar; exclusie: antipsychotica voor primaire diagnose psy-chose, mentale retardatie, termi-nale ziekte, re-cente grote ver-anderingen in gezondheidstoe-stand |
4 weken |
30 patiënten, 80% vrouw, gemiddelde leeftijd 83 jaar (sd 7), gemiddeld 30 maanden in verpleeghuis, meeste gebruikten risperidon, gemiddelde medicatieduur 14 maanden (range 3-44); 15 in interventiegroep, 15 in controlegroep |
Stoppen met medicatie → dus placebo |
Eigen medicatie |
Gedrag (Neuropsychi-atric Inventory Questionnaire), actigraphy |
Stoppen was geassocieerd met een verminderde slaapefficiën-tie van 86% naar 75% (54 minuten minder slaap; p=0,03); overige maten niet statistisch significant |
Behoorlijk, weinig patiënten, het is de vraag of blindering gegarandeerd kan zijn |
Matig |
Geen nieuwe of verergerende slaapproblemen, maar juist 'inductie van slaapproblemen' door stoppen met medicatie → exclusie |
|
Ryu |
2011 |
Ziekenhuis |
Niet-farma-ceutisch |
Onderzoeken invloed muziek op slaap bij patiënten met PTCA op IC |
RCT |
≥ 20 jaar, coro-naire hartziekte, naar CCU na PTCA; exclusie: gebruik ventila-tie, dementie, neurologische ziekte, zintuig-aandoening, ge-bruik slaapmid-delen of sedati-va, slaappro-bleem voor op-name op CCU |
1 nacht, geen follow-up |
58 patiënten, gemiddelde leeftijd 61, 66% man; 29 in interventiegroep, 29 in controlegroep |
slaapverwekkende' muziek 53 minuten 's avonds + oogbandage |
oordopjes zonder muziek + oogbanda-ge |
duur (aantal uren slaap) en kwaliteit slaap (gemodificeer-de Verran and Synder-Hal-pern Scale), gevraagd door verpleegkundi-ge aan patiënt |
Aantal minu-ten slaap: 279 in interventie-groep, 243 in controlegroep (p=0,002); slaapkwaliteit: 36 in inter-ventiegroep, 29 in controlegroep (p<0,001) |
Behoorlijk: geen opeen-volgende pati-ënten, binde-ring niet gega-randeerd, zeer selecte patiën-tengroep, geen follow-up, slechts 1 me-ting, sociaal wenselijke ant-woorden bij patiënt of ver-pleegkundige mogelijk |
Matig |
Beperkt deel is oudere patiënten, geen separate resultaten voor ouderen, zeer selectie patiëntengroep; het is de vraag of de gevonden resultaten klinisch relevant zijn |
|
Simon-son |
2007 |
Beide |
Beide |
Overzicht geven insomnia bij ouderen en beleid daarbij |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
Simpson |
2006 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken voorgeschreven medicatie en slaapgedrag bij verpleeghuis-bewoners met dementie |
Secundaire analyse van baseline data voor een RCT |
Verpleeghuis-bewoners met dementie in 6 verpleeghuizen in VS; ≥ 55 jaar, ten minste 1 maand in verpleeghuis, ≥ 30 minuten slaap overdag |
5 dagen |
195 bewoners, gemiddeld 80 jaar, 52% man, meesten met ernstige cognitieve stoornis, 71% gebruikte meerdere psychotrope medicijnen |
Geen |
Geen |
Medicatiedos-sier en actigraphy gedurende 5 dagen en nachten (minuten slaap 's nachts en overdag, % slaap 's nachts) |
Gemiddeld 505 minuten slaap per et-maal, waarvan 70% 's nachts. SSRI-gebruikers sliepen 64% 's nachts vs 72% bij niet-gebruikers (p =0,005); tra-zodonege-bruikers slie-pen 78% 's nachts vs 70% bij niet-gebruikers (p =0,04); overi-ge resultaten niet statistisch significant (ook niet voor bijv. benzodiaze-pines) |
Groot, geen vergelijking van interventies, dus waarschijnlijk geen vergelijkbare groepen, grote kans op vertekening, niet geplande analyse |
Laag |
Geen nieuwe of verergerende slaapproblemen, uitgangsvraag sluit niet aan; mogelijk relevant als achtergrondin-formatie |
|
Sivert-sen |
2006 |
Polikliniek ziekenhuis |
Beide |
Onderzoeken korte en langetermijn effectiviteit cognitieve therapie versus zopiclon bij ouderen met primaire insomnia |
Dubbelblinde, placebogecontroleerde RCT |
>55 jaar met insomnia; exclusie: gebruik hypnotica, antidepressiva, dementie, depressie, slaapapneu, nachtdiensten, niet stoppen met slaapmiddelen, ernstige fysieke aandoening |
6 weken interventie, 6 maanden follow-up, 2 patiënten niet in follow-up |
46 patiënten, gemiddelde leeftijd 61, 48% vrouw, gemiddeld 14 jaar insomnia |
Cognitieve therapie (slaaphygiëne educatie, slaaprestrictie, stimuluscon-trole, cognit-ieve therapie, ontspannings-technieken)(n=18) Zopiclon 7,5 mg per nacht (n=18) |
Placebo (n=12) |
Polysomno-grafie, slaapdagboek |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Behoorlijk, relatief weinig patiënten, groepen vooraf niet vergelijkbaar, resultaten niet van toepassing op populatie van richtlijn (zie opmerkingen) |
Matig |
Geen nieuwe of verergerende slaapproblemen, geen opgenomen patiënten à exclusie |
|
Sloane |
2007 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effect hoge-intensiteit licht op slaap 's nachts en activiteiten overdag bij patiënten met dementie |
Voor-na vergelijking met verschillende interventies |
Patiënten met dementie uit vier verpleeghuizen, VS; exclusie: diabetische retinopathie, maculadegenera-tie, geen lens |
Elke interventie duurde 3 weken, achtereenvolgens |
66 patiënten, gemiddelde leeftijd 79, 53% man, participatie in verschillende interventies: ochtend licht: 49, avond licht: 44, hele dag licht: 45, standaard licht: 46 |
Lichtintensi-teit 2500 lux gedurende 3 weken. 1. ochtend (7-11 uur), 2. avond (16-20 uur), 3. hele dag (7-20 uur); doel was om ten minste 1-2 uur lichtexpositie te krijgen |
Lichtinten-siteit 500 lux |
Actigraphy (slaap 's nachts en 24-uurs ritme) in laatste week interventie, bijwerkingen |
Uren slaap 's nachts: och-tendlicht: 5,54, avond-licht: 5,45, hele dag licht: 5,55, stan-daardlicht: 5,36 (p=0,04); overige resul-taten niet sta-tistisch signi-ficant (behou-dens in sub-populaties) |
Groot, geen randomisatie, achtereenvol-gens verschil-lende interven-ties, grote kans op vertekening door andere omstandighe-den dan interventie, geen blindering |
Laag |
Geen nieuwe of verergerende slaapproblemen, forse kans op bias, mogelijk toch enigszins relevant; gevonden verschillen lijken klinisch niet relevant |
|
Spahr |
2007 |
Variërend |
Farma-ceutisch |
Onderzoeken effect antihistaminica op slaapproblemen bij patiënten met cirrose |
Dubbelblinde RCT |
Cirrose, leeftijd 18-70, >10 op Epworth Sleepi-ness Scale; ex-clusie: depressie, psychiatrische of neurologische aandoening, ge-bruik psychotro-pe medicatie, al-coholisme, con-traindicatie voor hydroxyzine, ≥3 maanden slaapproblemen |
10 dagen |
35 patiënten met cirrose, gemiddelde leeftijd 55 (range 36-69), 71% man, 69% poliklinisch |
25 mg hydroxyzine 10 dagen, 's ochtends |
Placebo |
Actigraphy, VAS-schalen voor slaapkwa-liteit, neuro-psychologische tests |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Behoorlijk: weinig patiënten, veel subjectieve maten |
Matig |
Geen nieuwe of verergerende slaapproblemen, geen ouderen → exclusie |
|
Su |
2004 |
Extramuraal |
Geen inter-ventie |
Onderzoeken prevalentie in-somnia bij Chi-nese thuiswo-nende ouderen |
Dwarsdoor-snede onderzoek |
Inwoners Taipei, ≥ 65 jaar, thuiswonend |
Geen |
2045 mensen, 57% man, 33% 65-69 jaar, 34% 70-74 jaar, 33% 75+ |
Geen |
Geen |
Prevalentie slaapproble-men en gebruik slaapmiddelen |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Behoorlijk: pa-tiëntenpopula-tie sluit niet aan bij NL po-pulatie, selec-tieve rekrute-ring |
Matig |
Geen nieuwe of verergerende slaapproblemen, extramurale populatie → exclusie |
|
Sudano |
2010 |
Extramuraal |
Farma-ceutisch |
Onderzoeken effect acetaminophen op bloeddruk bij patiënten met coronaire hartziekte |
Dubbelblinde RCT |
Patiënten met coronaire hart-ziekte, via acade-misch zieken-huis in Zwitser-land, met stabie-le cardiovascu-laire medicatie, 18-80 jaar; ex-clusie: acuut my-ocard infarct, onstabiele angi-na pectoris, be-roerte, coronaire interventie <3 maanden, hart-falen, gebruik analgetica, chro-nische pijn, ro-ken, alcohol- of middelenmis-bruik, onvol-doende contro-leerbare hoge bloeddruk, nier-falen, leveraan-doening, gebruik orale anticoagu-lantia, diverse andere medica-tie, ontstekings-ziekten |
2 weken interventie, 2 weken wash-out, 2 weken interventie |
33 patiënten, gemiddelde leeftijd 61 (sd 8,5), 85% man |
Acetamino-phen 1g 3dd |
Placebo |
Primair: bloeddruk; secundair: diverse bloedlab.para-meters |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Sterke patiëntselectie, dus extrapo-leerbaarheid waarschijnlijk laag. Onder-zoek verder wel prima opgezet, rela-tief weinig patiënten |
Matig |
Geen slaappara-meters, geen nieuwe of verergerende slaapproblemen, niet specifiek ouderen → exclusie |
|
Sun |
2010 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effectiviteit HT7 acupressure op slaapkwaliteit en insomnia |
RCT |
2 verpleeghuizen in Taiwan, ten minste 3 maanden verblijf, slaapproblemen; exclusie: hartproblemen, acute ziekte, trauma, polswonden, chronisch gebruik slaapmiddelen |
5 weken interventie + 2 weken follow-up |
50 patiënten, gemiddelde leeftijd 70 jaar, 64% man, 64% met CVA, 12% dementie |
HT7 acupressure op beide polsen, 5 seconden, 1 seconde rust, gedurende 5 minuten voor bedtijd, 5 weken |
placebo', lichte druk i.p.v. acu-pressure |
Athens Insomnia Scale (AIS) |
Lagere AIS-scores in ex-perimentele groep dan in controlegroep (bijv. 2,80 vs 20,0 in week 5), normalise-rend na af-loop interven-tie (week 7); geen statisti-sche toetsing verschillen |
Groot: beperk-te blindering, beperkte pati-ëntengroep, niet extrapo-leerbaar naar NL situatie, ondoorzichtige weergave resultaten |
Laag |
Geen nieuwe of verergerende slaapproblemen, patiënten-populatie niet vergelijkbaar met NL, mogelijk toch relevant, maar onduidelijke interpretatie resultaten |
|
Sunami |
2012 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken effect fluvoxamine bij CVA-patiënten met depressie op depressie en slaapstoornissen |
Vergelijkend onderzoek, geen randomisatie |
Opgenomen patiënten met CVA en depressie in ziekenhuis in Japan |
4 weken |
19 patiënten, gemiddelde leeftijd 75 jaar, 79% man |
Fluvoxamine getitreerd tot 75 mg/dag 1dd, 4 weken |
Geen interventie |
Pittsburgh Sleep Quality Index + depressiescha-len, melatonine |
Voor slaappa-rameters: wel verschil met baseline voor interventie (PSQI van 10,3 naar 5,1; 6,2 en 5,0 na 1, 2 en 4 we-ken (p< 0,05)); geen significant verschil met baseline in controlegroep (PSQI van 7,5 naar resp. 6,4; 6,0 en 4,2 (niet signifi-cant)). Geen directe verge-lijking tussen groepen; waarschijnlijk geen signifi-cant verschil |
Zeer groot: geen randomisatie, geen blindering, mogelijk dus geen vergelijkbare groepen, zeer weinig patiënten |
Zeer laag |
Onduidelijke interpretatie resultaten, mogelijk toch enigszins relevant |
|
Svarstad |
2002 |
Verpleeghuis |
Farma-ceutisch |
Onderzoeken risicofactoren gebruik benzodiazepines, prevalentie benzodiazepinegebruik en evaluatie beleid |
Dwarsdoor-snede onderzoek |
Bewoners verschillende verpleeghuizen VS, post-analyse |
Geen |
2060 patiënten, 75% vrouw, gemiddelde leeftijd 82 (sd 10), 40% dementie, 12% depressie, 55% gedragsproblemen, 34% pijn, 31% slaapproblemen |
Geen |
Geen |
Gebruik benzo-diazepines, patiëntenken-merken |
28% kreeg benzodiazepi-ne, 7% di-phenhydrami-ne, 2% overi-ge anxiolytica of hypnotica; meer benzo-diazepine gebruik bij vrouwen (OR: 1,30; 95%BI 1,01-1,67), bij de-pressie (OR 1,68; 95%BI: 1,25-2,27), pijn (OR: 1,20; 95%BI: 1,04-1,40) en slaapproble-men (OR: 2,23; 95%BI: 1,93-2,57) |
Zeer groot: geen interventie-onderzoek, oude data |
Zeer laag |
Analyse van data uit jaren 1986-1989, sluit niet aan bij uitgangsvraag → exclusie |
|
Tou-blanc |
2007 |
Ziekenhuis |
Niet-farma-ceutisch |
Vergelijken assist-control ventilatie vs low level pressure support ventilatie op slaapkwaliteit bij geïntubeerde IC-patiënten |
RCT |
Volwassen patiënten met chronische longziekte, geïntubeerd, mechanische ventilatie |
1 nacht, geen follow-up (4 uur ene interventie, dan 4 uur andere interventie) |
20 patiënten, 75% man, gemiddelde leeftijd 65 jaar (range 42-81), voornamelijk met COPD en pulmonaire infectie |
Assist-control ventilation (ACV): 10 ml/kg, 12/minuut, verhoogd tot verdwijnen inademings-arbeid |
Low level pressure support (low PSV): spontane ademha-ling met inspiratoire pressure (6cm H2), 7200 PB, 5l/min |
Polysomnogra-fie + eigen score patiënt |
Geen signifi-cante ver-schillen in slaap 'archi-tecture'; wel verschillen gevonden tussen beide slaapperioden (begin en ein-de nacht), maar dit lijkt niet gerela-teerd aan de interventie (hoewel de auteurs dat wel beweren) |
Groot: geen blindering, beperkt aantal patiënten, zeer kortdurende interventie, veel kans op vertekening |
Laag |
Mogelijk relevant, maar kwaliteit zeer beperkt |
|
Vaajoki |
2011 |
Ziekenhuis |
Niet-farma-ceutisch |
Onderzoeken effect muziek op pijn en pijnbeleving na abdominale chirurgie |
RCT |
Volwassen patiënten, Fins academisch ziekenhuis, met electieve abdominale chirurgie |
2 dagen |
168 patiënten, gemiddelde leef-tijd 62, 54% man, na abdomi-nale chirurgie, voornamelijk wegens maligniteit |
Muziek naar eigen keuze van patiënt, 30 minuten op dag 1 en 2 |
Geen muziek |
Pijn en pijnbeleving op VAS-schalen |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot: rando-misatieprocedu-re zeer ondui-delijk (1 week muziek, 2e week niet), niet blind |
Laag |
Gaat niet over slaapproblemen → exclusie |
|
Valto-nen |
2005 |
Verpleeghuis |
Niet-farma-ceutisch |
Onderzoeken effect melatonine in 'nachtmelk' op slaap en activiteiten bij ouderen |
Cross-over dubbelblinde RCT (2 studies) |
Ouderen uit verpleeghuizen in Finland |
8 weken interventie, 1 week wash-out, 8 weken interventie |
|
Nachtmelk': van koeien die 's nachts gemolken worden (gemiddeld 14 pg/ml melatonine) |
Normale melk |
Vragenlijsten door verpleeg-kundigen (op verschillende schalen per studie), over slaap 's nachts en activiteiten overdag |
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Groot: er lijkt sprake van ad hoc analyses voor verschil-lende groepen, onduidelijke rapportage, geen duidelijke vergelijking 'nachtmelk' en gewone melk |
Laag |
Geen nieuwe of verergerende slaapproblemen, onduidelijke rapportage → exclusie |
|
Vaz Fragoso |
2007 |
Extramuraal |
Beide |
Overzicht slaapproblemen bij ouderen die thuiswonen en beleid daarbij |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie. |
|
Weschu-les |
2006 |
Hospice (verpleeg-huis) |
Farma-ceutisch |
Onderzoeken nieuwe vs oude middelen (far-maceutisch) op symptoomver-lichting in een hospice |
Retrospectief cohortonder-zoek |
Hospiceprogram-ma en medica-tie voor pijn, insomnia of misselijkheid; exclusie in insomniacohort: eerder temaze-pam voor zolpidem |
Niet beschreven, retrospectief |
Voor insomniacohort: 100 patiënten, 50% vrouw, gemiddelde leeftijd 74 jaar, allen terminale patiënten, 59% vanwege kanker |
Temazepam |
Zolpidem |
Symptomen: pijn, insomnia, misselijkheid; numerieke schaal en verbale beschrijving |
Complete res-pons: temaze-pam: 52%, zolpidem: 22% (p= 0,0037); on-bekende uit-komst: tema-zepam: 18%, zolpidem: 38% (p=0,05). |
Zeer groot: retrospectief cohort, zeer selecte patiëntenpopulatie, geen vergelijkbare groepen vooraf, enz. |
Zeer laag |
Patiëntengroep sluit niet compleet aan bij uitgangsvraag, mogelijk toch relevant |
|
Wolf |
2001 |
Verpleeghuis + extramuraal |
Farma-ceutisch |
Vergelijking effectiviteit en veiligheid fluoxetine (SSRI) en trimipramine (TCA) voor behandeling depressie bij geriatrische patiënten |
Dubbelblinde RCT |
leeftijd ≥ 60, de-pressie; exclusie: plotselinge ver-ergering depres-sie (in placebo-groep!), suïci-daal, glaucoom, urineretentie, prostaathypertro-fie, ernstige car-diovasculaire aandoening, lever-, nier-, bloed- of long-aandoening, her-senziekte, epi-lepsie, schizofre-nie, schildklier-aandoening, middelen-misbruik |
5 weken |
19 patiënten (in follow-up!), gemiddelde leeftijd 70 (range: 61-85), 95% vrouw; 10 in fluoxetine-groep, 9 in trimi-praminegroep |
20 mg/dag fluoxetine 5 weken |
150 mg/ dag trimi-pramine 5 weken |
Polysomnogra-fie: slaaptijd, slaapefficiëntie, inslaaptijd, waaktijd 's ochtends, slaapstadia, REM latentie, REM dichtheid, slaapinterval |
Geen significante verschillen tussen groepen (wel voor beide behandelingen t.o.v. baseline), behalve % REM-slaap (hoger bij trimipramine) en % waaktijd (lager bij trimipramine) |
Zeer groot: maar 19/41 patiënten met complete follow-up; veel uitval vanwege bijwerkingen; inclusiemetho-de niet duidelijk |
Zeer laag |
Populatie gedeeltelijk van toepassing, maar ook deel extramuraal. Geen nieuwe of verergerende slaapproblemen → exclusie |
|
Wood-ward |
2012 |
Beide |
Beide |
Overzicht slaap en slaapproble-men bij ouderen en beleid |
Narratieve review |
|
|
|
|
|
|
Niet gerap-porteerd in deze evidence tabel, want niet van toepassing |
Zeer groot, narratief over-zichtsartikel, geen systema-tisch onderzoek |
Zeer laag |
Geen systema-tisch onderzoek → exclusie |
|
Zisberg |
2012 |
Ziekenhuis |
Farma-ceutisch |
Onderzoeken patronen in gebruik slaapmedicatie voor, gedurende en 1 en 3 maanden na hospitalisatie |
Prospectief observationeel onderzoek |
Patiënten opgenomen in 5 ziekenhuizen, ≥ 70 jaar, in Israel; exclusie: beroerte, coma, mechanische ventilatie, complete afhankelijkheid |
Tot 3 maanden na ontslag uit ziekenhuis |
485 patiënten (412 met complete follow-up), gemiddelde leeftijd 78 jaar (sd 6), 52% vrouw, gemiddeld 5,7 dagen ziekenhuis-verblijf, 31% rehospitalisatie binnen 3 maanden |
Geen |
Geen |
Interview over slaapmedicatie aan patiënten, bij opname in ziekenhuis, gedurende verblijf en na 1 en 3 maanden |
43% gebruik-te slaapmedi-catie voor op-name in zie-kenhuis (96% benzodiazepi-ne); 43% ge-bruikte slaap-medicatie tij-dens zieken-huisverblijf (82% al voor verblijf). Geen gebruik slaapmedica-tie tijdens verblijf was belangrijkste factor die ge-associeerd was met geen slaapmedica-tie na ontslag (OR: 3,91; 95%BI: 1,64-9,30) |
Zeer groot, sociaal wenselijke antwoorden, recall bias bij 1e interview, geen interventie |
Zeer laag |
Sluit niet aan bij uitgangsvraag → exclusie |
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-09-2015
Beoordeeld op geldigheid : 24-08-2015
Jaarlijks wordt door de commissie richtlijnen van de Nederlandse Internisten Vereniging bepaald of actualisatie van de richtlijn nodig is.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door de PROVA en gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn beoogt een leidraad te geven voor de dagelijkse praktijk van ‘nieuwe of verergerende slaapproblemen bij acuut opgenomen ouderen in ziekenhuis of verpleeghuis’.
Doelgroep
De primaire doelgroepen van deze richtlijn zijn zorgprofessionals1 en (potentiële) zorggebruikers2, waarbij de richtlijn vooral een hulpmiddel is bij het nemen van beslissingen en het maken van keuzen in de dagelijkse praktijk. Zorgprofessionals kunnen deze richtlijn tevens gebruiken voor het bijhouden van kennis, voor onderwijs- en nascholingsdoeleinden en voor het opstellen van samenwerkingsafspraken.
De belangrijkste zorgprofessionals die deze richtlijn kunnen gebruiken zijn: internisten, klinisch geriaters, specialisten ouderengeneeskunde en verpleegkundigen en verzorgenden die met de specifieke doelgroep van de richtlijn werken. Ook voor andere zorgverleners in ziekenhuis en verpleeghuis kan deze richtlijn nuttig zijn.
1 Onder zorgprofessionals worden alle BIG-geregistreerde zorgverleners verstaan.
2 Onder zorggebruikers worden patiënten, cliënten, familie van patiënten en cliënten, en mantelzorgers verstaan.
Samenstelling werkgroep
Op initiatief van de Nederlandse Internisten Vereniging is een werkgroep samengesteld, onder voorzitterschap van mw. prof. dr. S.E.J.A. de Rooij, internist ouderengeneeskunde. De richtlijnwerkgroep bestaat uit gemandateerde vertegenwoordigers van de belangrijkste wetenschappelijke verenigingen die met de zorg voor ouderen in het ziekenhuis en verpleeghuis te maken hebben. Dit zijn vertegenwoordigers van de volgende verenigingen:
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging voor Klinische Geriatrie
- Verpleegkundigen & Verzorgenden Nederland – Neuro & revalidatie
- Verpleegkundigen & Verzorgenden Nederland – Geriatrie verpleegkunde
- Verenso
De werkgroep is methodologisch en procedureel ondersteund door een epidemioloog (secretaris).
Werkgroep
- Mw. prof. dr. S.E.J.A. de Rooij, internist ouderengeneeskunde & klinisch geriater, Universitair Medisch Centrum Groningen, namens de Nederlandse Internisten Vereniging, voorzitter
- Mw. drs. M.K. Tuut, epidemioloog, PROVA, Varsseveld, secretaris
- Mw. drs. P.A. Genet, klinisch geriater, Waterlandziekenhuis Purmerend / Slotervaart Ziekenhuis Amsterdam, namens de Nederlandse Vereniging voor Klinische Geriatrie
- Mw. M.B. Gruppelaar, verpleegkundig specialist, ziekenhuisgroep Twente, Almelo/Hengelo, namens Verpleegkundigen & Verzorgenden Nederland – Neuro & Revalidatie
- Dhr. M.A. Weterman, verpleegkundig specialist, Universitair Medisch Centrum Utrecht, namens Verpleegkundigen & Verzorgenden Nederland – Geriatrie Verpleegkunde
- Mw. drs. A.H. van Pagee, specialist ouderengeneeskunde, Novicare, Kootwijkerbroek, namens Verenso, specialisten in ouderengeneeskunde
- Mw. dr. J.P. Brouwer, internist ouderengeneeskunde, Alrijne Ziekenhuis, Leiden, namens de Nederlandse Internisten Vereniging – sectie Ouderengeneeskunde
Belangenverklaringen
Alle werkgroepleden hebben een belangenverklaring ingevuld. Een overzicht hiervan is opgenomen in de hieronder weergegeven tabel.
|
Naam |
Hoofdfunctie |
Neven-werkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis-valorisatie |
Overige belangen |
|
Mw. prof. dr. S.E.J.A. de Rooij |
Internist ouderengeneeskunde UMCG |
Voorzitter NIV |
- |
- |
- |
- [ZonMw, Nuts Ohra] |
- |
- |
|
Mw. drs. M.K. Tuut |
Eigenaar PROVA |
|
- |
- |
- |
- |
- |
- |
|
Mw. drs. P.A. Genet |
Klinisch geriater, Waterland ziekenhuis, Slotervaart ziekenhuis |
|
- |
Overleg met voorzitter Nederlandse Vereniging voor Slaap- en Waak Onderzoek |
- |
- |
- |
- |
|
Mw. M.B. Gruppelaar |
Verpleegkundig specialist neurologie, Ziekenhuisgroep Twente |
- |
- |
- |
- |
- |
- |
- |
|
Dhr. M.A. Weterman |
Verpleegkundig specialist geriatrie, UMC Utrecht |
- |
- |
- |
- |
- |
- |
- |
|
Mw. A.H. van Pagee |
Specialist ouderengeneeskunde |
Visitatie werkgroep Verenso |
- |
- |
- |
- |
- |
- |
|
Mw. dr. J.P. Brouwer |
Internist ouderengeneeskunde |
- |
- |
- |
- |
- |
- |
- |
Inbreng patiëntenperspectief
Begrijpelijkerwijs is er geen patiëntenvereniging specifiek voor nieuwe of verergerende slaapproblemen bij ouderen in het ziekenhuis of verpleeghuis. Desalniettemin is via een ouderenvereniging geprobeerd om het patiëntenperspectief in de knelpunteninventarisatie mee te laten wegen. De werkgroep Senior Friendly Hospital is gevraagd om op onderdelen hun reactie te geven. Daarnaast is bij het benoemen van relevante uitkomstmaten geprobeerd te denken vanuit patiëntenperspectief. Een korte samenvatting van de richtlijn voor patiënten is opgenomen als aanverwant (‘Samenvatting van de richtlijn voor patiënten’).
Methode ontwikkeling
Evidence based
Implementatie
Gedurende het hele proces van richtlijnontwikkeling wordt rekening gehouden met implementatie van de richtlijn in de werkgroep, bijvoorbeeld bij de samenstelling van de werkgroep, de brede knelpunteninventarisatie en de uitgebreide commentaarronde.
Na autorisatie van de richtlijn wordt deze ten minste op de website van de Nederlandse Internisten Vereniging gepubliceerd. Ook andere deelnemende partijen zijn vrij de richtlijn op hun website te publiceren. Daarnaast wordt getracht samenvattingen van de richtlijn in Nederlandse tijdschriften te publiceren, om zo de implementatie van de richtlijn te bevorderen. Een handzame samenvattingskaart behorende bij de richtlijn wordt gemaakt.
Bij deze richtlijn hoort een implementatieplan. Hierin is per aanbeveling onderzocht welke factoren de invoering van de richtlijn kunnen bevorderen of belemmeren en welke oplossingsrichtingen hierbij mogelijk zijn. Het implementatieplan en een beperkte indicatorenset, behorende bij deze richtlijn, zijn opgenomen als aanverwant (‘Implementatieplan en indicatoren’).
Werkwijze
Knelpuntenanalyse
Bij de start van het richtlijnontwikkeltraject is een uitgebreide knelpuntenanalyse uitgevoerd. De voorzitter en secretaris van de richtlijnwerkgroep hebben knelpunten voorgeformuleerd en deze aan een brede groep ter commentaar en aanvulling voorgelegd. De volgende organisaties zijn gevraagd input te leveren op de knelpunten:
- Seniorenorganisatie ANBO
- Instituut voor Verantwoord Medicijngebruik
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging (sectie ouderengeneeskunde)
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Nederlandse Vereniging voor Anesthesiologie
- Nederlandse Vereniging voor Keel-, Neus-, Oorheelkunde en Heelkunde van het Hoofd-Halsgebied
- Nederlandse Vereniging voor klinische farmacologie en biofarmacie
- Nederlandse Vereniging voor Klinische Geriatrie
- Nederlandse Vereniging voor Neurologie
- Nederlandse Vereniging voor Psychiatrie
- Nederlandse Vereniging voor Ziekenhuis Apothekers
- Verenso
- Verpleegkundigen en Verzorgenden Nederland
De verzamelde knelpunten en het bijgevoegde commentaar zijn besproken in de eerste vergadering van de richtlijnwerkgroep. Op basis daarvan zijn de uitgangsvragen vastgesteld, die vervolgens met behulp van uitgebreid literatuuronderzoek zijn uitgewerkt.
Methode richtlijnontwikkeling
Deze (concept)richtlijn is opgesteld aan de hand van het Procedureboek NIV richtlijnen die aansluit bij het “Appraisal of Guidelines for Research & Evaluation II” (AGREE II) instrument (www.agreetrust.org). Dit instrument is een breed (internationaal) geaccepteerd instrument voor de beoordeling van de kwaliteit van richtlijnen.
Na vaststelling van de uitgangsvragen is naar literatuur gezocht met een expert op het gebied van literatuursearches. Van de werkgroepleden werd hiervoor medisch inhoudelijke input verkregen. De literatuursearches zijn vermeld onder zoekverantwoording. Er is gezocht in Medline, aangevuld met Cinahl (met focus op verpleegkundig onderzoek). Van de totale opbrengst werden de abstracts bestudeerd, hetgeen leidde tot een forse selectie. Daarbij werd geselecteerd op onderwerp (sluit het onderwerp aan bij de uitgangsvraag met name: gaat het om acute slaapproblematiek? En: bestaat de populatie ten minste voor een deel uit ouderen?) en kwaliteit van het artikel (met name exclusie van niet-systematisch opgezet onderzoek). Het proces van selectie staat grafisch weergegeven in de aanverwant ‘Literatuurselectie’. Na ontdubbeling werden alle geselecteerde abstracts fulltekst aangevraagd. Een beperkt aantal artikelen bleek niet leverbaar in Nederland. De overige artikelen zijn systematisch fulltekst beoordeeld op kwaliteit en inhoud. Alle artikelen zijn samengevat in evidence tabellen. De onderwerpen niet-farmacologische interventies en farmacologische interventies zijn hierbij samengenomen, omdat er veel overlap bleek in de artikelen. De evidence tabellen zijn per module in deze richtlijn opgenomen.
Voor het literatuuronderzoek is gebruik gemaakt van de GRADE methodiek. Hierbij wordt per uitgangsvraag de totale ‘body of evidence’ beoordeeld op kwaliteit bij van tevoren vastgestelde (patiëntrelevante) uitkomstmaten. Resultaten worden per uitkomstmaat samengevat, waarbij tevens de ‘overall’ kwaliteit van de onderliggende bewijslast (evidence) wordt aangegeven. Bij de beoordeling wordt dan gebruik gemaakt van de software ‘GRADEPro, waarmee per uitgangsvraag een tabel met bevindingen (Summary of Findings) en een tabel met beoordeling van het bewijs (GRADE Evidence Profile) wordt gemaakt. GRADE kent vier niveaus van conclusies. Per uitkomstmaat wordt de kwaliteit van het bewijs gegradeerd volgens de volgende indeling:
|
Kwaliteit van het bewijs |
Interpretatie |
|
Hoog (High) |
Er is veel vertrouwen dat het werkelijk effect dicht in de buurt ligt van de schatting van het effect |
|
Matig (Moderate) |
Er is matig vertrouwen in de schatting van het effect: het werkelijk effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt |
|
Laag (Low) |
Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
|
Zeer laag (Very low) |
Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect |
De kwaliteit van het bewijs wordt initieel bepaald op basis van studieopzet (randomised controlled trials of observationeel onderzoek) en kan worden verhoogd of verlaagd. Er zijn vijf factoren die kunnen zorgen voor een verlaging van de kwaliteit van het bewijs: beperkingen in de onderzoeksopzet (risk of bias), inconsistentie, indirectheid, imprecisie en publicatiebias. Drie factoren kunnen de kwaliteit van het bewijs verhogen: groot effect, aanwezigheid van een dosisresponsrelatie en confounding die het werkelijke effect onderschat of een niet bestaand effect overschat. Na bepaling van de mate van kwaliteit per uitgangsvraag volgt een beoordeling van de algehele kwaliteit van het bewijs. Waar mogelijk worden meta-analyses gemaakt. Hierbij is gebruik gemaakt van ReviewManager.
Niet alleen wetenschappelijke conclusies zijn van belang in richtlijnen. Belangrijke factoren voor het formuleren en waarderen van de uiteindelijke aanbevelingen zijn: algehele kwaliteit van het bewijs, grootte van en zekerheid over het netto gunstig effect van een interventie, waarden en voorkeuren van patiënten, kosten, professioneel perspectief, organisatie van zorg en maatschappelijk perspectief. Deze factoren tezamen bepalen of een sterke of zwakke/conditionele aanbeveling wordt geformuleerd. Deze zijn als volgt omschreven:
|
Sterkte van een aanbeveling |
Interpretatie |
Formuleringen |
Implicaties |
|
Sterk |
Er is veel vertrouwen dat de gewenste effecten van een (therapeutische) interventie de ongewenste effecten overtreffen |
Dienen, behoren |
Patiënten: De meeste patiënten willen de aanbevolen actie en enkel een klein deel niet. Clinici: De meeste patiënten zouden volgens de aanbeveling behandeld moeten worden. Beleidsmakers: De aanbeveling kan worden voorgeschreven als beleid in de meeste situaties. |
|
Zwak/ conditioneel |
Er is onzekerheid of de gewenste effecten de ongewenste effecten overtreffen; of de gunstige en ongunstige effecten houden elkaar in evenwicht |
Overwegen, verschillende opties |
Patiënten: De meerderheid van de patiënten wil de aanbevolen actie, maar een groot deel niet. Clinici: Wees voorbereid om patiënten te ondersteunen een beslissing te maken die past bij hun eigen waarden en voorkeuren. Beleidsmakers: Discussie met en betrokkenheid van stakeholders is hier van belang. |
Meer informatie over GRADE en een precieze beschrijving van de methodiek is te vinden op www.gradeworkinggroup.org. De indeling van de modules is gebaseerd op het rapport ‘Toepassen GRADE in Nederland’ van GRADE_NL, een Nederlandse expertgroep op het gebied van GRADE.(10)
Het volledig toepassen van de GRADE methodiek is momenteel nog voorbehouden aan uitgangsvragen op het gebied van (therapeutische) interventies. De onzekerheid omtrent diagnostische uitkomstmaten en patiëntrelevante consequenties is erg groot. Binnen de internationale GRADE Working Group en GRADE_NL wordt momenteel gewerkt aan de uitwerking van een model voor de beantwoording van diagnostische uitgangsvragen met behulp van GRADE. Voor de diagnostische uitgangsvragen in deze richtlijn is daarom zo veel mogelijk gebruik gemaakt van de principes van GRADE. Het is echter op dit moment nog niet mogelijk om de GRADE methodiek volledig toe te passen bij uitgangsvragen op het gebied van diagnostiek.
Alle in deze richtlijn gebruikte literatuur is vermeld in de literatuurlijst.
Een overzicht van kennishiaten, die zijn gevonden bij het literatuuronderzoek, is weergegeven als aanverwant.
Procedure voor commentaar en autorisatie
De richtlijnwerkgroep heeft gewerkt aan het totstandkomen van de conceptrichtlijn. Deze is ter commentaar aangeboden aan alle NIV-leden en de (deelspecialistische) verenigingen die bij de ontwikkeling van de richtlijn betrokken zijn. Daarnaast is de conceptrichtlijn ter commentaar verstuurd aan alle partijen die bij de knelpunteninventarisatie om input gevraagd zijn. Het binnengekomen commentaar is door de werkgroep beoordeeld en verwerkt in de richtlijn. Daarbij is beargumenteerd welke commentaren wel en welke niet zijn opgenomen.
Daarna is de richtlijn ter autorisatie voorgelegd aan de partijen die in de werkgroep vertegenwoordigd zijn. De richtlijn is geautoriseerd door de Nederlandse Internisten Vereniging, de Nederlandse Vereniging voor Klinische Geriatrie, Verenso en Verpleegkundigen & Verzorgenden Nederland.
Zoekverantwoording
Literatuursearch
Zoekresultaten
|
Naam file |
aantal |
|
med 20131107 vr diagnosis vanaf 2000 |
242 |
|
cin 20131110 vr diagnose inpatients inperking |
28 |
|
cin 20131110 vr diagnose deel 1 |
46 |
|
cin 20131110 vr diagnose deel 2 |
49 |
|
|
|
|
med 20131107 vr interventies non farmacol vanaf 2000 |
136 |
|
cin 20131110 vr interventie niet farmacol |
63 |
|
|
|
|
med 20131107 vr interventies farmacol vanaf 2000 |
148 |
|
cin 20131113 vr interventie farmacol |
54 |
|
|
|
|
med 20141117 aanvulling zopiclon 1990 tot nov 2013 |
8 |
|
cin 20141117 zoplicon aanvulling |
26 |
Er is gezocht vanaf 2000 tot nov 2013
Zoekhistory
Database: Ovid MEDLINE(R) In-Process & Other Non-Indexed Citations and Ovid MEDLINE(R) <1946 to Present>
Search Strategy:
--------------------------------------------------------------------------------
1 "zoekfilter Geriatrie conform inspiratie Cochrane".ti. (0)
2 (mini?mental adj3 state).tw. (89)
3 alzheimer*.tw. (93288)
4 ageing.tw. (24830)
5 (hip adj3 fractur*).tw. (11937)
6 dement*.tw. (71142)
7 (cognitive adj3 decli*).tw. (12012)
8 (cognitive adj3 impair*).tw. (36730)
9 (cognitive adj funct*).tw. (33835)
10 (activit* adj3 living).tw. (18499)
11 (daily adj3 living).tw. (19477)
12 Alzheimer Disease/ (69003)
13 Geriatric Psychiatry/ (2096)
14 psychogeriatri*.tw. (1596)
15 Accidental Falls/ (15462)
16 fall?.tw. (109998)
17 Dementia/ (37146)
18 exp Cognition Disorders/ (63816)
19 "Activities of Daily Living"/ (50920)
20 exp Hip Fractures/ (17775)
21 or/2-20 (437437)
22 "aanvulling van filter frail elderly".ti. (0)
23 "medline filter voor frail elderly".ti. (0)
24 frail elderly/ (6772)
25 "Aged, 80 and over"/ (622178)
26 Aged/ (2340395)
27 (vulnerabl* or frail* or very old or "over the age" or "older olds").tw. (66959)
28 ((old or older or elderly or aged or middle?aged or middle aged or aging or geriatric) adj3 (people or population or patient? or in?patient? or person? or men or women)).tw. (360245)
29 ((old or older or elderly or aged or aging or geriatric) adj3 (people or population or patient? or in?patient? or person? or men or women)).tw. (360226)
30 ((over or aged) adj2 ("65" or "70" or "75" or "80" or "85" or "90" or "95" or "100") adj3 (people or population or patient? or in?patient? or person? or men or women)).tw. (33024)
31 geriatric patient?.tw. (5311)
32 (institut* adj3 (old or elderly or aged)).tw. (3029)
33 or/24-32 (2566927)
34 senior?.tw. (24055)
35 aging.mp. or exp Aging/ (278610)
36 34 and 35 (1437)
37 geriatric?.af. (132940)
38 home care/ (27774)
39 residential facilities/ or assisted living facilities/ or homes for the aged/ or nursing homes/ or intermediate care facilities/ or skilled nursing facilities/ (41287)
40 37 or 38 or 39 (189152)
41 (resident* or population? or group? or people or senior? or elderly or old or aged).tw. (4405399)
42 40 and 41 (88243)
43 36 or 42 (89285)
44 33 or 43 (2582269)
45 " filter frail elderly of geriatrische patient stap 3 meest sensitief".ti. (0)
46 24 or 25 or 27 or 29 or 30 or 31 or 32 (957571)
47 26 and 40 (106557)
48 exp Patient Care/ (575200)
49 26 and 48 (158176)
50 ((nursing or long?term?care or long term care or geriatric or elderly or aged) adj5 (home? or facility or facilities or resident$)).tw. (39745)
51 (hospitali?ed or home?dwelling or home dwelling or community?dwelling or community dwelling or in?patient? or in patient?).tw. (1265145)
52 40 or 50 or 51 (1446366)
53 41 and 52 (585666)
54 47 or 49 or 53 or 24 or 25 or 27 or 29 or 30 or 31 or 32 (1478731)
55 " filter frail elderly of geriatrische patient stap 2 gemiddeld sensitief".ti. (0)
56 (25 or 26 or 29 or 30 or 31 or 32) and 27 (24149)
57 52 and 27 (13242)
58 24 or 56 or 57 (30230)
59 "filter frail elderly of geriatrische patient stap 1 maximaal specifiek".ti. (0)
60 "einde filter frail elderly CBO 22 april 2010 met 3 stappen".ti. (0)
61 21 or 33 or 36 or 40 or 50 or 51 (3653827)
62 "filter geriatrisch cbo met cochrane aanvulling".ti. (0)
63 33 or 36 or 40 or 50 or 51 (3409520)= aged
64 "slaapstoornissen searches".ti. (0)
65 exp Sleep Disorders/ (62752)
66 exp Sleep Apnea Syndromes/ (24589)
67 exp Sleep/ (62284)
68 Polysomnography/ (14814)
69 sleep monitoring.mp. (238)
70 polysomnograp*.tw. (11736)
71 sleep???.tw. (115717)
72 Wakefulness/ (14815)
73 (wakefuln* or polysomia* or insomnia* or sleep* or parasomnia*).tw. (125295)
74 sleepless*.tw. (616)
75 exp Circadian Rhythm/ (63355)
76 exp Chronobiology Phenomena/ (89986)
77 phase shift.mp. (4369)
78 circadian.tw. (37236)
79 65 or 66 or 67 or 68 or 69 or 70 or 71 or 72 or 73 or 74 or 75 or 76 or 77 or 78 (242041)=P
80 "P slaapstoornissen".ti. (0)
81 32 or 39 or 50 or 51 (1322464)
82 exp academic medical centers/ or exp hospital units/ or exp hospitals/ (301026)
83 hospital*.tw. (828921)
84 exp Inpatients/ (12802)
85 exp hospitalization/ or institutionalization/ or long-term care/ or night care/ or nursing care/ (210684)
86 81 or 82 or 83 or 84 or 85 (2176487)
87 "onderdeel setting".ti. (0)
88 63 and 79 and 86 (26882)=setting
89 (english or french or german or dutch).la. (20771633)
90 88 and 89 (24405)
91 questionnaire.mp. or exp Questionnaires/ (434672)
92 case finding.mp. (3444)
93 screening.tw. (335270)
94 assess*.tw. (1799637)
95 diagnos*.tw. (1657870)
96 exp Sleep Disorders/di (14368)
97 91 or 92 or 93 or 94 or 95 or 96 (3679590)
98 90 (24405)
99 limit 98 to yr="2000 -Current" (16748)
100 99 and 97 (9775)
101 (holland sleep adj3 quest*).tw. (1)
102 (msq or (mayo adj sleep adj3 question*) or psq or (pittsburg* adj sleep adj quest*) or ESS or (epworth adj sleep* adj scale)).tw. (4879)
103 (groninger adj8 (sleep or slaap)).tw. (1)
104 polysomnography.mp. or exp Polysomnography/ (17569)
105 97 or 101 or 102 or 103 or 104 (3687670)
106 99 and 105 (10918)
107 case finding.ti. (966)
108 screening.ti. (104628)
109 assess*.ti. (236498)
110 diagnos*.ti. (448906)
111 exp *Sleep Disorders/di (6890)
112 101 or 102 or 103 or 104 or 107 or 108 or 109 or 110 or 111 (802598)
113 91 or 112 (1201071)
114 99 and 113 (6709)= P + focus diagnostiek
115 (institut* adj3 (old or elderly or aged)).ti. (1237)
116 geriatric?.ti. (16951)
117 *residential facilities/ or *assisted living facilities/ or *homes for the aged/ or *nursing homes/ or *intermediate care facilities/ or *skilled nursing facilities/ (28580)
118 ((nursing or long?term?care or long term care or geriatric or elderly or aged) adj5 (home? or facility or facilities or resident$)).ti. (20020)
119 (hospitali?ed or home?dwelling or home dwelling or community?dwelling or community dwelling or in?patient? or in patient?).ti. (398560)
120 exp *academic medical centers/ or exp *hospital units/ or exp *hospitals/ (157823)
121 hospital*.ti. (226360)
122 84 (12802)
123 exp *hospitalization/ or *institutionalization/ or *long-term care/ or *night care/ or *nursing care/ (82906)
124 115 or 116 or 117 or 118 or 119 or 120 or 121 or 122 or 123 (803389)=focus setting
125 114 and 124 (2312)
126 65 or 67 or 71 or 72 or 73 or 74 or 75 or 76 or 78 (238261)
127 "ingeperkte P ".ti. (0)
128 exp *Sleep Disorders/ (49840)
129 exp *Sleep/ (38611)
130 sleep???.ti. (62499)
131 Wakefulness.ti. (1950)
132 *Wakefulness/ (5742)
133 (wakefuln* or polysomia* or insomnia* or sleep* or parasomnia*).ti. (67899)
134 sleepless*.ti. (164)
135 exp *Circadian Rhythm/ (34141)
136 exp *Circadian Rhythm/ (34141)
137 circadian.ti. (18188)
138 or/128-137 (121467)=P focus
139 "ingeperkte P met focus".ti. (0)
140 125 and 138 (1766)
141 33 or 36 or ageing.tw. (2581807)
142 140 and 141 (821)
143 'med081222 CBO diagnose filter Medline START'.ti. (0)
144 exp "sensitivity and specificity"/ (424848)
145 exp "diagnostic errors"/ (95222)
146 reproducibility of results/ (279922)
147 comparative study.pt. (1723490)
148 single-blind method/ (19575)
149 evaluation studies.pt. (203868)
150 compar$.ti. (469629)
151 versus.ti. (114995)
152 value.ti. (91047)
153 assess$.ti. (236498)
154 validation studies.pt. (70659)
155 predict$.ti. (182400)
156 accuracy.ti. (26997)
157 reproducibility.ti. (7657)
158 efficiency.ti. (29365)
159 reliability.ti. (22508)
160 correlat$.ti. (145995)
161 prospective studies/ (373210)
162 or/144-161 (3326288)
163 'med081222 CBO diagnose filter Medline EINDE'.ti. (0)
164 142 and 162 (341)
165 questionnaire?.ti. (20663)
166 exp *Questionnaires/ (31779)
167 112 or 165 or 166 (836024)
168 164 and 167 (277)
169 exp Letter/ (831138)
170 exp Editorial/ (351025)
171 exp Comment/ (579339)
172 case reports/ (1683945)
173 169 or 170 or 171 or 172 (2826731)
174 168 not 173 (273)
175 168 not 173 (273)=med 20131107 vr diagnostiek vanaf 2000
176 Light/ (82433)
177 air conditioning/ or heating/ or housing/ or housing for the elderly/ or lighting/ or temperature/ or ventilation/ (225153)
178 (temperatu* or light* or heating or housing or ventilat*).tw. (1006891)
179 Noise/ (16282)
180 noise.tw. (88920)
181 exp Night Care/ (1310)
182 (night adj3 car*).tw. (399)
183 Phototherapy/ (5633)
184 (light adj3 therap*).tw. (2359)
185 (light adj3 treatment).tw. (3448)
186 (white adj3 noise adj3 machin*).tw. (4)
187 fan?.tw. (5549)
188 exercise/ or muscle stretching exercises/ or walking/ (89374)
189 "activities of daily living"/ or music therapy/ (53219)
190 (soothing adj3 activi*).tw. (8)
191 relaxation.tw. (89554)
192 exp Relaxation/ or exp Relaxation Therapy/ (21576)
193 exp Chronotherapy/ or exp Sleep Phase Chronotherapy/ (760)
194 (routine or regular*).tw. (355910)
195 (time or timing or clock* or nap?).tw. (2123428)
196 exp Beds/ (3626)
197 (sleep adj3 hygiene).tw. (647)
198 drinking behavior/ or exp food habits/ or food preferences/ or habits/ (38444)
199 Caffeine/ (20245)
200 exp Coffee/ (4736)
201 (coffee or habit? or preference?).tw. (154658)
202 or/176-201 (3734181)
203 th.fs. (1438055)
204 202 and 203 (223719)
205 79 and 124 and 141 and 204 (350)
206 205 and 89 (319)
207 206 (319)
208 limit 207 to yr="2000 -Current" (235)
209 208 not 173 (229)
210 138 and 209 (145)=med 20131107 vr interventies niet farmacologisch
211 exp Benzodiazepines/ (59371)
212 (benzodiazepi* or chloordiazepo* or diazepam or lorazepam or oxazepam).tw. (43755)
213 exp Benzazepines/ (76408)
214 temazepam.mp. (982)
215 (zolpidem or lormetazepam).tw. (1895)
216 nitrazepam.tw. (935)
217 midazolam.mp. (11121)
218 dormicum.tw. (124)
219 Haloperidol/ (14924)
220 exp Antipsychotic Agents/ (122772)
221 exp Anticonvulsants/ (123029)
222 exp Antidepressive Agents/ (122843)
223 exp Morphine/ (44854)
224 analgesics/ or exp analgesics, non-narcotic/ or exp analgesics, opioid/ or analgesics, short-acting/ (386683)
225 from 210 keep 1-145 (145)
226 Melatonin/ (15235)
227 melatonin*.tw. (17483)
228 Drugs, Chinese Herbal/ (27302)
229 Valerian/ (592)
230 or/211-229 (787841)
231 79 and 124 and 141 and 230 (744)
232 89 and 231 (693)
233 limit 232 to yr="2000 -Current" (464)
234 "med091027 CBO filter sysrev & meta Medline START".ti. (0)
235 meta analysis.pt. (51580)
236 (meta-anal$ or metaanal$).af. (88507)
237 (quantitativ$ adj10 (review$ or overview$)).tw. (4699)
238 (systematic$ adj10 (review$ or overview$)).tw. (62562)
239 (methodologic$ adj10 (review$ or overview$)).tw. (7085)
240 medline.tw. and review.pt. (47204)
241 (pooled adj3 analy*).tw. (8506)
242 or/235-241 (161929)
243 "med091027 CBO filter sysrev & meta Medline EINDE".ti. (0)
244 233 and 242 (6)
245 "med101005 Cochrane Highly Sensitive Search Strategy for Randomized Trials in Medline START".ti. (0)
246 randomized controlled trial.pt. (389900)
247 controlled clinical trial.pt. (89890)
248 (randomized or randomised).ab. (371071)
249 placebo.ab. (163683)
250 drug therapy.fs. (1765672)
251 randomly.ab. (215907)
252 trial.ab. (321195)
253 groups.ab. (1371755)
254 or/246-253 (3433115)
255 254 not (exp animals/ not humans/) (2943451)
256 "med101005 Cochrane Highly Sensitive Search Strategy for Randomized Trials in Medline EINDE".ti. (0)
257 233 and 255 (334)
258 "med091027 CBO filter rct Medline START".ti. (0)
259 randomized-controlled-trial.pt. (389900)
260 controlled-clinical-trial.pt. (89890)
261 randomized controlled trial/ (389900)
262 randomi?ed controlled trial?.tw. (87371)
263 random-allocation.af. (82901)
264 double-blind-method.af. (131940)
265 single-blind-method.af. (19623)
266 (random adj8 (selection? or sample?)).tw. (35084)
267 random$.tw. (736054)
268 or/259-267 (976737)
269 "med091027 CBO filter rct Medline EINDE".ti. (0)
270 233 and 268 (168)
271 244 or 270 (169)
272 from 271 keep 1-169 (169) =med 20131107 vr interventies farmacologisch
273 210 (170)
274 175 (295)
275 Imovane.tw. (24)
276 43200-80-2.rn. (628)
277 zopiclon?.tw. (803)
278 275 or 276 or 277 (920)
279 230 or 278 (801153)
280 79 and 124 and 141 and 279 (762)
281 280 and 278 (17)
282 281 (17)
283 limit 282 to yr="2000 - 2013" (8) aanvulling zopiclon
Literatuurselectie
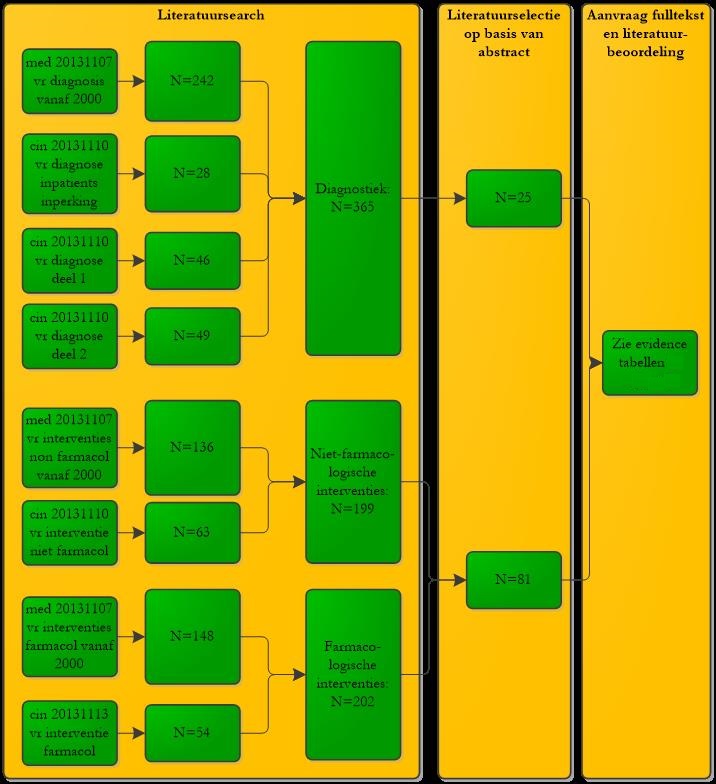
In november 2014 werd aanvullend gezocht naar evidence over behandeling met zopiclon. Hierbij werden aanvullend 34 abstracts gevonden. Na selectie leverde dit 1 extra artikel op, dat in de tekst van de richtlijn en in de evidence tabellen is besproken.
