B4. Herpes genitalis
Aanbeveling
Zie onderbouwing en samenvattingskaart (link)
Onderbouwing
Achtergrond
B4.1 Algemeen
Genitale herpes is de meest voorkomende ulceratieve soa in de westerse wereld (Looker, 2015a; Looker, 2015b). Herpes genitalis en andere vormen van herpessimplexvirusinfectie worden in klassieke gevallen gekenmerkt door typische in groepjes gelegen blaasjes die soms overgaan in pijnlijke erosies, soms met korstvorming en/of pussig beslag. Het virus blijft latent aanwezig (zonder laesies) en kan vooral lokaal frequent recidieven vertonen.
Samenvatting literatuur
B4.2 Ziekte
B4.2.1 Verwekker
Herpessimplexvirussen zijn dubbelstrengs DNAvirussen behorend tot de familie van de herpesvirussen. Er zijn meer dan 100 herpesvirussen, waarvan er minimaal 9 bij de mens voor kunnen komen. De officiële benaming van herpesvirussen die infecties veroorzaken bij de mens is humaan herpesvirus (HHV), waarbij elk type een nummer heeft gekregen.
Bekende ziektebeelden zijn:
- herpes labialis (koortslip) door herpessimplexvirus type 1 (HSV1, officieel HHV1);
- herpes genitalis door zowel HSV1 als HSV2 (HHV2);
- waterpokken en gordelroos door het varicellazostervirus (VZV, HHV3);
- mononucleosis infectiosa door het epsteinbarrvirus (EBV, HHV4);
- cytomegalovirus (CMV, HHV5);
- zesde ziekte (exanthema subitum, roseola infantum) (HHV6 en 7);
- Kaposi sarcoom (HHV8).
De herpessimplexvirussen type 1 en type 2 zijn nauw aan elkaar verwant en vertonen dezelfde genoomstructuur (Pellet, 2013).
B4.2.2 Pathogenese
De pathogenese van genitale herpes, dat door zowel HSV1 als HSV2 wordt veroorzaakt, verschilt niet van die van herpes labialis, die vooral wordt veroorzaakt door HSV1. Een primaire of primoinfectie treedt op wanneer er nooit eerder een herpesinfectie is geweest. Is er in het verleden wel een labiale HSV1 of 2infectie geweest, dan spreekt men van een eersteepisodeherpes genitalis. Ook hier betreft het een contactinfectie, in dit geval met de huid of slijmvliezen van de anogenitale regio. Op de plaats van de primaire infectie ontstaat een blaasje, dat na een ulceratief stadium uiteindelijk indroogt met korstvorming. Primaire infecties verlopen in ongeveer de helft van de gevallen symptoomloos.
Na de primaire infectie nestelt het herpessimplexvirus zich door retrograad transport via axonen in het regionale sensibele dorsale ganglion, dat naast het ruggenmerg is gelegen. Tijdens een primaire infectie met HSV worden humorale en cellulaire afweer opgebouwd. Echter dit voorkomt reactivatie niet, doordat het virus zich verspreidt via zenuwcellen die slecht toegankelijk zijn voor het immuunsysteem. Van hieruit vindt periodiek en kortdurend (sub)klinische of (a)symptomatische reactivatie plaats met virusuitscheiding langs de zenuw naar de huid of slijmvliezen in het verzorgingsgebied (Mark, 2008). Reactivatie van latent virus kan door verschillende stimuli worden veroorzaakt zoals UVlicht, stress, menstruatie, koorts en immuunsuppressie.
B4.2.3 Incubatieperiode
De incubatieperiode duurt 2 tot 12 dagen.
B4.2.4 Ziekteverschijnselen
De aard en ernst van de ziekteverschijnselen worden bepaald door het type HSV, gastheerspecifieke factoren zoals lokalisatie, vroegere nietgenitale HSVinfectie, geslacht, immuunstatus van de persoon en of er sprake is van een primoinfectie (meestal heftiger verloop) of een recidief. Er is geen verschil in ziekteverschijnselen tussen herpes genitalis door HSV1 en HSV2 (Holmes, 2008).
Volgens de literatuur is slechts 37% van de nieuwe (primaire infectie) HSV2infecties symptomatisch; voor HSV1 ligt dit rond 67%. De rest van de infecties, en dus de meerderheid van de genitale herpesinfecties, verloopt asymptomatisch of wordt niet als zodanig herkend. Bij mannen zijn de infecties vaker asymptomatisch dan bij vrouwen.
Bij een symptomatische primoinfectie heeft 40% van de mannen en 70% van de vrouwen een prodromale fase, bestaande uit koorts, malaise en spierpijn (Holmes, 2008). Hierna volgen bij vrouwen klachten als pijn, jeuk, dysurie, vaginale afscheiding en regionale lymfadenopathie. Bij mannen komen ook urethritisklachten voor en kan de mictie zodanig pijnlijk verlopen dat urineretentie optreedt. Zes tot 7 dagen na de eerste symptomen volgen de huid en slijmvliesafwijkingen met soms ontwikkeling van de karakteristieke, met helder vocht gevulde blaasjes. De laesies duren bij een primoinfectie 7-28 dagen en genezen zonder littekens. Men dient rekening te houden met atypische laesies, die zich presenteren als fissuren, furunkels, plaatselijke erytheem, lineaire ulceraties of excoriaties.
Verder kan een herpetische proctitis ontstaan, met anorectale pijn, obstipatie en ulcererende herpetiforme laesies.
Bij mannen zijn de laesies voornamelijk gelegen op de schacht van de penis met uitzondering van de anorectale herpes). Bij vrouwen zijn de laesies verspreid over de hele vulva en het perineum (Wald, 2001). Minder bekend is dat bij vrouwen ook de cervix uteri vaak betrokken is bij een primoinfectie. Dit kan zeer pijnlijk zijn, waardoor een onderzoek van de cervix in speculo niet goed mogelijk is en de diagnose gemist wordt.
HSV is in een veel uitgebreider gebied aantoonbaar dan alleen het gebied van de zichtbare laesies (Tata, 2010). De frequentie van de recidieven wisselt sterk, afhankelijk van het virustype en de lokalisatie. Het gemiddelde aantal recidieven is na een eerste episode zeer variabel met een mediaan van 4 per jaar voor HSV2 en 1 per jaar voor HSV1 (Laferty, 1987; Benedetti, 1994; Engelberg, 2003). Bij de meeste patiënten is er een afname in de tijd en in ernst, maar ook dit patroon is zeer variabel (Benedetti, 1999). Bij HSV2 neemt het aantal recidieven af na het eerste jaar, maar blijft daarna vrij constant gedurende jaren (Phipps, 2011).
Complicaties van een genitale herpesinfectie treden vrijwel alleen op bij een primaire infectie met HSV1 of HSV2. Een voorbeeld is aseptische meningitis (nekstijfheid, hoofdpijn en fotofobie), die vaker bij HSV2 dan bij HSV1 voorkomt. Ook kan autonome dysfunctie of myelitis transversa optreden. Symptomen van de autonome dysfunctie kunnen zijn: hyperesthesie of anesthesie in de lumbale of sacrale regio en urineretentie (het syndroom van Elsberg) of obstipatie.
Zwangeren
Primaire infecties bij zwangeren kunnen asymptomatisch verlopen. Twee derde van de zwangeren, seropositief voor HSV2, bleek geen ulceraties gehad te hebben (Westhoff, 2011).
Patiënten met constitutioneel eczeem
Zie LCI-richtlijn Herpessimplexvirusinfecties.
Neonaten
HSV1 en HSV2 infectie kunnen bij neonaten milde tot zeer ernstige symptomen geven. Er zijn 3 klinische verschijningsvormen van neonatale herpes te onderscheiden (James, 2015; Forsgren, 2009).
- Bij de eerste vorm blijft de infectie beperkt tot de huid en de slijmvliezen van ogen en/of mond (in de Engelstalige literatuur Skin Eye Mouth (SEM) manifestatie genoemd). De gemiddelde incubatieduur is dan 7-12 dagen. Een lokale infectie heeft een veel betere prognose, maar kan gepaard gaan met oogschade, waaronder herpes keratitis. Neurologische schade, waaronder retinanecrose, kan later aan het licht komen (510%).
- De tweede verschijningsvorm van neonatale herpes met een gemiddelde incubatieduur van 26 weken betreft een infectie van het centraal zenuwstelsel met of zonder betrokkenheid van de huid/slijmvliezen. Bij alleen symptomen van een infectie van het centraal zenuwstelsel is de mortaliteit >50%. Maar een derde van de kinderen met centraal zenuwstelsel betrokkenheid heeft een normale ontwikkeling. HSV2 infectie heeft een slechtere prognose dan HSV1 besmetting.
- De derde klinische vorm met een incubatieduur van 4-11 dagen betreft een gegeneraliseerde infectie waarbij zowel huid, slijmvliezen, lever, bijnieren, longen als centraal zenuwstelsel aangetast zijn. De symptomen bij deze vorm zijn meestal algemene verschijnselen als koorts, sufheid, slecht drinken, braken en ademhalingsproblemen. In een later stadium kunnen verschijnselen optreden van acidose, shock, anemie, pneumonie, convulsies, hepatomegalie, encefalitis en meningitis. Bij een gegeneraliseerde infectie is de sterfte zonder antivirale therapie hoog (>80%) met fulminant leverfalen of multiorgaanfalen en bestaat er een grote kans op restverschijnselen.
Slechts in ongeveer 50% van de gevallen van neonatale herpes zijn blaasjes aanwezig, zodat de diagnose vaak moeilijk te stellen is. Herkennen van de symptomen en snelle start van behandeling zijn van belang voor een goede uitkomst (Forsgren, 2009).
Bij oudere kinderen en adolescenten verloopt een infectie met HSV veelal asymptomatisch. Bij genitale herpes verloopt de infectie vergelijkbaar als bij volwassenen.
B4.2.5 Immuniteit
Na een primaire infectie ontstaan antistoffen die wel beschermen tegen een reinfectie, maar recidieven niet kunnen voorkomen. De IgGantistoffen en specifieke geheugenTcellen worden transplacentair overgedragen van moeder op kind. Het is echter onbekend welke mate van bescherming deze bieden. Bovendien is het zo dat HSV1 en 2 kruisreagerende antistoffen induceren, die gedeeltelijke kruisbescherming bieden en die de ernst van een eersteziekteepisode verminderen, maar geen invloed hebben op het aantal recidieven.
B4.3 Besmetting
B4.3.1 Reservoir
De mens. Er is geen tussengastheer.
B4.3.2 Besmettingsweg
Genitale herpes ontstaat via seksueel contact: genitogenitaal, anogenitaal of orogenitaal. Dit laatste verklaart hoe HSV1 genitale herpes kan veroorzaken en HSV2 labiale herpes.
Van moeder op kind kan besmetting op de volgende manieren geschieden: prenataal (5% is transplacentair, durante partu (75-95% is ascenderend bij langdurig gebroken vliezen of tijdens de partus) of postnataal (Kimberlin, 2005).
Ook kan neonatale herpes ontstaan via besmetting door iemand anders met een labiale herpesinfectie, bijvoorbeeld door knuffelen of zoenen van het kind (‘kiss of death’).
Infectie van de handen van medisch of verpleegkundig personeel door contact met een HSVdrager, kan leiden tot fijt (bindweefselontsteking aan de binnenkant van een vingertop), ook wel ‘herpetic whitlow’ genoemd (zie ook paragraaf B4.8.4).
B4.3.3 Besmettelijke periode
De besmettelijke periode is niet goed vast te stellen. Bij aanwezigheid van laesies is tot 10 dagen na ontstaan nog HSV aantoonbaar. Ook zonder aanwezigheid van laesies kunnen patiënten echter nog besmettelijk zijn door asymptomatische uitscheiding.
B4.3.4 Besmettelijkheid
De besmettelijkheid is het hoogst vlak voor, tijdens en vlak na de symptomatische periode. Bij vaginale coïtus is de transmissiekans hoger van mannen naar vrouwen dan andersom. De transmissie kans is hoger bij frequenter onbeschermde seks.
Bij monogame serodiscordante paren waarvan bekend was dat er 1 partner HSVseropositief was, varieerde de transmissiekans van 12-30% per jaar (Drake, 2000).
Bij symptomatische patiënten is bij 70% HSV2 aantoonbaar; bij asymptomatische patiënten is dat 13%. Dat betekent dat dus ook bij asymptomatische patiënten virusuitscheiding plaats kan vinden. HSV wordt periodiek in episoden uitgescheiden, HSVvirusdetectie is mogelijk tot 9 dagen bij patiënten met laesies en tot 4 dagen bij patiënten zonder frequente laesies (Corey, 2004; Tronstein, 2011). De uitscheiding van HSV2 wordt gekenmerkt door een snelle toe en ook weer afname van virale load waarbij er een extreme variatie is in hoogte van virale load en de duur van verschillende episoden. Het nettoeffect is zeer frequente perioden van uitscheiding met hoge virale loads (Schiffer, 2011). De meerderheid van de besmettingen blijkt via asymptomatische dragers te gebeuren.
Het herpessimplexvirus wordt snel geïnactiveerd bij kamertemperatuur en in droge omstandigheden. Aerogene besmetting vindt dan ook niet plaats. Borstvoeding is mogelijk indien geen laesies in dermatomen van het borstgebied (thoracaal 2 t/m 6) en actieve laesies elders zijn afgeplakt/gedekt (mondmasker) en goede handhygiëne wordt betracht.
B4.4 Diagnostiek
B4.4.1 Klinische diagnostiek
Met behulp van een goede (seksuele) anamnese en het klinische beeld kan bij een typisch verlopende herpesgenitalisinfectie een klinische diagnose gesteld worden. Het onderscheid tussen een primo/eersteepisodeinfectie, of een heftig recidief is niet goed mogelijk omdat ook patiënten die een asymptomatische primo/eersteepisodeinfectie hebben doorgemaakt zich kunnen presenteren met een (ernstig) recidief. Differentiaaldiagnostisch komen vooral de andere ulceratieve soa’s in aanmerking (Holmes, 2008; Langenberg, 1999).
De blaasjes doorlopen verschillende stadia. Een blaasje kan spontaan opengaan of door krabben, en zo het aspect van een ulcus aannemen. Als de blaasinhoud daarna opdroogt, treedt het crusteuze stadium in, waarin weinig tot geen infectieus virus meer wordt uitgescheiden. Daarna geneest de laesie doorgaans restloos. De totale duur kan variëren van 3 tot 7 dagen.
Bij het opnemen van de anamnese zal men zeker vragen of de patiënt deze (vroege) symptomen herkent van een eerdere gelegenheid.
B4.4.2 Microbiologische diagnostiek
De eerste keus voor het aantonen van het virus is de nucleïnezuuramplificatietest (NAAT). Met een swab kan langs de basis van de laesie of het vocht van een blaasje worden gegaan. Deze techniek wordt aanbevolen als diagnosticum bij genitale herpes en voor het onderzoek van liquor bij verdenking op HSVmeningitis (Patel, 2017). Hierbij bestaat de mogelijkheid in sommige laboratoria om een onderscheid te maken tussen type 1 en type 2herpesvirus. Bij afwezigheid van laesies sluit een negatieve NAAT een HSVinfectie niet uit, aangezien het virus zich intermitterend verspreidt. Bij een orgaan of gegeneraliseerde herpesinfectie zoals hepatitis is een HSVviraleloadbepaling in bloed aangewezen.
De viruskweek, voorheen beschouwd als de gouden standaard, is minder sensitief dan nucleïnezuurtechnieken en meer afhankelijk van transportomstandigheden en stadium van de laesie. Viruskweek wordt daarom in de routine achterwege gelaten (Wald, 2003). Bij patiënten met afweerstoornissen of ernstige therapieresistente recidieven kan het van belang zijn om resistentiebepalingen uit te voeren op geïsoleerde stammen die via de conventionele celkweken zijn verkregen of met sequentietechnieken op de geïsoleerde virale nucleïnezuren (Pinninti, 2012; Van der Beek, 2012).
Bij vermoeden van intraoculaire herpesinfecties wordt door de oogarts materiaal uit het oog afgenomen middels een voorsteoogkamerpunctie of vitrectomie. Het materiaal wordt serologisch onderzocht op lokale productie van antistoffen door berekenen van een goldmannwitmercoëfficiënt. Er is sprake van een lokale productie van antistoffen als deze coëfficiënt groter is dan 3. Tevens wordt door middel van een polymerase chain reaction (PCR) de aanwezigheid van DNA van HSV1 of 2 bepaald.
Serologie
Het bepalen van HSVtypespecifieke antistoffen kent in de dagelijkse praktijk weinig toepassing. De serologie kan van nut zijn in seroepidemiologische studies en indien men wil vaststellen of de klinische verschijnselen berusten op een primaire infectie of op een recidief. Met de huidige tests zijn bij een primaire infectie op het moment van de eerste klinische verschijnselen nog geen typespecifieke antistoffen aantoonbaar (soms pas >12 weken). Dit maakt dat ook bij de eerste recidieven serologie nog negatief kan zijn. Soms treedt er zelfs seroreversie (weer negatief worden) op, een probleem dat vooral bij zwangeren zou spelen (Arvaja, 1999; Eskild, 2000; Van Rooijen, 2016) Serologische analyses maken op basis van het typespecifieke glycoproteïne G (gG) onderscheid tussen HSV1 (glycoproteïne G1) en HSV2 (glycoproteïne G2). De sensitiviteit van deze glycoproteïne Gtypespecifieke testen voor de detectie van HSVantilichamen varieert tussen de 80% en 90% voor HSV2 en tussen de 69 en 98% voor HSV1. Foutnegatieve resultaten treden sneller op in het vroege stadium van de infectie. De specificiteit is 93-97% voor HSV2 en 92-95% voor HSV1 (AshleyMorrow, 2004; Mark, 2007; Morrow, 2003; Summerton, 2007). Ondanks een redelijke specificiteit is bij lage prevalentie (geldt met name voor HSV2) de positiefvoorspellende waarde laag. De aanwezigheid van HSV2typespecifieke antilichamen impliceert een anogenitale infectie. Bij gebrek aan symptomen kan een HSV1positieve uitslag geen onderscheid maken in anogenitale, orolabiale of een cutane infectie. Men dient rekening te houden dat zelfs testen met goede sensitiviteit en specificiteit matige positiefvoorspellende waarden hebben bij lage prevalenties.
De typespecifieke HSVserologische testen kunnen zinvol zijn bij:
- een patiënt die niet bekend is met genitale herpes maar diens partner wel;
- zwangeren indien er tijdens de zwangerschap of baring een verdenking is op (een) primoinfectie met herpes genitalis; vergelijk met serum van in het begin van de zwangerschap indien voorhanden;
- recidiverende genitale laesies zonder bekende oorzaak op moment dat deze niet zichtbaar zijn.
Diagnostiek bij neonatale herpes
Onderzoek van: EDTAbloed, urine, nasofaryngeale uitstrijk, conjunctiva, huidblaasjes (indien aanwezig), en liquor cerebrospinalis voor HSVPCR. In geval van SEM wordt maar in 24% van de gevallen HSVDNA gevonden in de liquor cerebrospinalis (na 48 uur, kolonisatie van de baby door de moeder in het geboortekanaal is dan niet meer te detecteren). Bij symptomen van centraal zenuwstelsel betrokkenheid is dat in 7678% van de gevallen. In combinatie met bloedonderzoek stijgt dit naar 90% (Kimberlin, 2007; Malm, 1999). Bij een verdenking op neonatale herpes dient een oogarts te worden betrokken om onder meer middels fundoscopie en onderzoek van oogvocht retinanecrose uit te sluiten.
Followup van de virale load in serum en in liquor geeft informatie over de effectiviteit van de behandeling en de prognose (Kimura, 2002). Serologisch onderzoek bij moeder en kind is niet van grote waarde in de acute fase.
Retrospectief kan na 12-18 maanden na de geboorte onderzoek worden gedaan naar HSV2specifieke antilichamen. Dan zijn de maternale antilichamen niet langer aanwezig. HSV1besmetting kan ook postnataal of op vroege kinderleeftijd zijn opgetreden. HSV1antilichamen zijn om die reden minder informatief om een neonatale infectie op te sporen (Forsgren, 2009).
B4.5 Risicogroepen
B4.5.1 Verhoogde kans op infectie
Zoals bij alle soa’s is de kans dat iemand wordt besmet afhankelijk van het aantal seksuele partners en de aard van seksuele activiteiten. Risicofactoren voor HSV1seropositiviteit zijn: vrouw, hogere leeftijd, geen autochtone achtergrond en lagergemiddeld educatieniveau. Risicofactoren voor HSV2 zijn gelijk aan de factoren bij HSV1 behalve dat HSV2 vaker wordt gezien bij hogere educatieniveaus (Woestenberg, 2016). Inmiddels is goed gedocumenteerd in meerdere studies dat het hebben van genitale ulcera zoals bij herpes genitalis de transmissie van hiv bevordert. Genitale ulcera maken de patiënt ontvankelijker voor een hivinfectie. Enkele studies laten zien dat hivpatiënten met genitale ulcera een verhoogde uitscheiding van hiv laten zien, waarschijnlijk door synergistische mechanismen (Nagot, 2007; Gray, 2004; Schacker, 2002; Celum, 2005).
B4.5.2 Verhoogde kans op ernstig beloop
Zwangeren
Voor de zwangere vrouw verloopt de ziekte zelden ernstiger dan bij nietzwangeren. Wel is het mogelijk dat het aantal recidieven hoger ligt bij zwangeren (Holmes, 2008).
Neonaten
Neonatale herpes omvat prenataal, durante partu en postnataal verworven HSVinfecties (in twee derde van de gevallen veroorzaakt door HSV1). Besmetting van het kind durante partu, door direct contact van het kind met vaginaal secreet of ascenderend bij langdurig gebroken vliezen, is de meest gebruikelijke transmissieroute (90% van de gevallen). Het ontbreken van passief via de moeder overgedragen antistoffen is waarschijnlijk een belangrijke risicofactor voor een ernstig beloop van de infectie. Het betreft meestal een vlak voor de partus opgelopen eersteepisodeinfectie bij de moeder, waardoor de moeder nog geen beschermende antistoffen kan doorgeven aan het kind. Een primaire infectie geeft een 10 tot 30 keer grotere kans op transmissie in vergelijking tot een recidiverende infectie van de moeder.
Een prenataal verworven infectie komt zeer zelden voor en betreft casuïstiek van mogelijke transplacentaire besmetting bij ogenschijnlijk intacte vliezen. Daarnaast kan in zeldzame gevallen ook postnataal verworven HSV via de handen of mond van verzorgers tot ernstige infecties leiden bij neonaten (tot de leeftijd van ongeveer 1 maand). Neonatale ziekteverschijnselen bij transmissie durante partu beginnen ongeveer 5 dagen na de geboorte.
Immunoincompetente personen
Personen met een gestoorde cellulaire immuniteit hebben vaker HSVreactivaties en een hoger risico op een ernstiger beloop. De meeste studies rapporteren over hivpositieve personen met <200 CD4 cellen/ul, patiënten met maligniteiten en (hematopoëtischestamcel)transplantatiepatiënten. Bij hen verlopen lokale (orale en genitale, primo en recidief) infecties vaak ernstiger. Ook kan een gedissemineerde infectie (betrokkenheid van diverse orgaansystemen waaronder pneumonie, colitis, oesophagitis, meningoencefalitis, retinanecrose) met een hoge mortaliteit ontstaan.
B4.6 Epidemiologie
B4.6.1 Verspreiding in de wereld
Herpes genitalis komt overal in de wereld voor en is de belangrijkste ulceratieve soa in de westerse wereld met een geschatte prevalentie van 417 miljoen HSV2geïnfecteerden wereldwijd (WHO, 2016). De laatste 20 tot 30 jaar is er wereldwijd een stijging in de seroprevalentie (Holmes, 2008). In GrootBrittannië is de incidentie (primoinfectie) in 5 jaar tijd met 15% toegenomen (in 1995 16.479 en in 2004 19.180 gerapporteerde gevallen). In de Verenigde Staten hebben naar schatting 40-60 miljoen mensen de infectie met een incidentie van 12 miljoen infecties en 600.000800.000 klinische casussen per jaar. De prevalentie van genitale herpes in ontwikkelingslanden varieert van 2% tot 74% (Sen, 2007).
B4.6.2 Voorkomen in Nederland
In 2015 werd 428 keer de diagnose herpes genitalis gesteld (47,7% vrouw, 26,9% heteroseksuele mannen en 25,5% MSM) in de Nederlandse soaklinieken. In de huisartsenpraktijk werd het geschatte aantal episoden van genitale herpes gesteld op 21.974 in 2014 (1,3 op de 1000 personen) met een verhouding man:vrouw van 1,9:0,7/1000 mensen (Van den Broek, 2016). Het aandeel genitale HSV1 is in de huisartsenpraktijk aanzienlijk hoger bij met name jongere leeftijd en bij vrouwen (gegevens Brabant Zuid Oost 20022010). Oorzaken voor meer genitale HSV1 zouden kunnen zijn: frequenter orogenitaal contact en minder “beschermende” immuniteit door pas op latere leeftijd in contact komen met herpes labialis. De beschikbare prevalentie en incidentiegegevens zijn echter niet betrouwbaar omdat diagnostiek niet routinematig wordt uitgevoerd. Vanwege een hoog percentage asymptomatische infecties is onderrapportage zeer waarschijnlijk. Seroprevalentie voor HSV1 en HSV2 in Nederland uitgevoerd op Pienter1 (19956) en Pienter2 (20067) sera was respectievelijk 47,7 en 6,8% (Pienter1) en 42,7% en 6% (Pienter2) (zie ook figuur B41). Een significant lagere seroprevalentie voor HSV1 werd waargenomen in Pienter2 vergeleken met Pienter1 in de leeftijd van 1014 jaar, dit maakt dat jongvolwassenen meer at risk zijn voor een genitale HSV1infectie (Woestenberg, 2016). Incidentie van neonatale herpes in Nederland in de periode 20062011 is 4,7/100.000 geboorten. Hemelaar et al. constateren een suboptimale adherentie aan richtlijnen bij ondervraagde gynaecologen en kinderartsen betreffende neonatale herpes (Hemelaar, 2015).

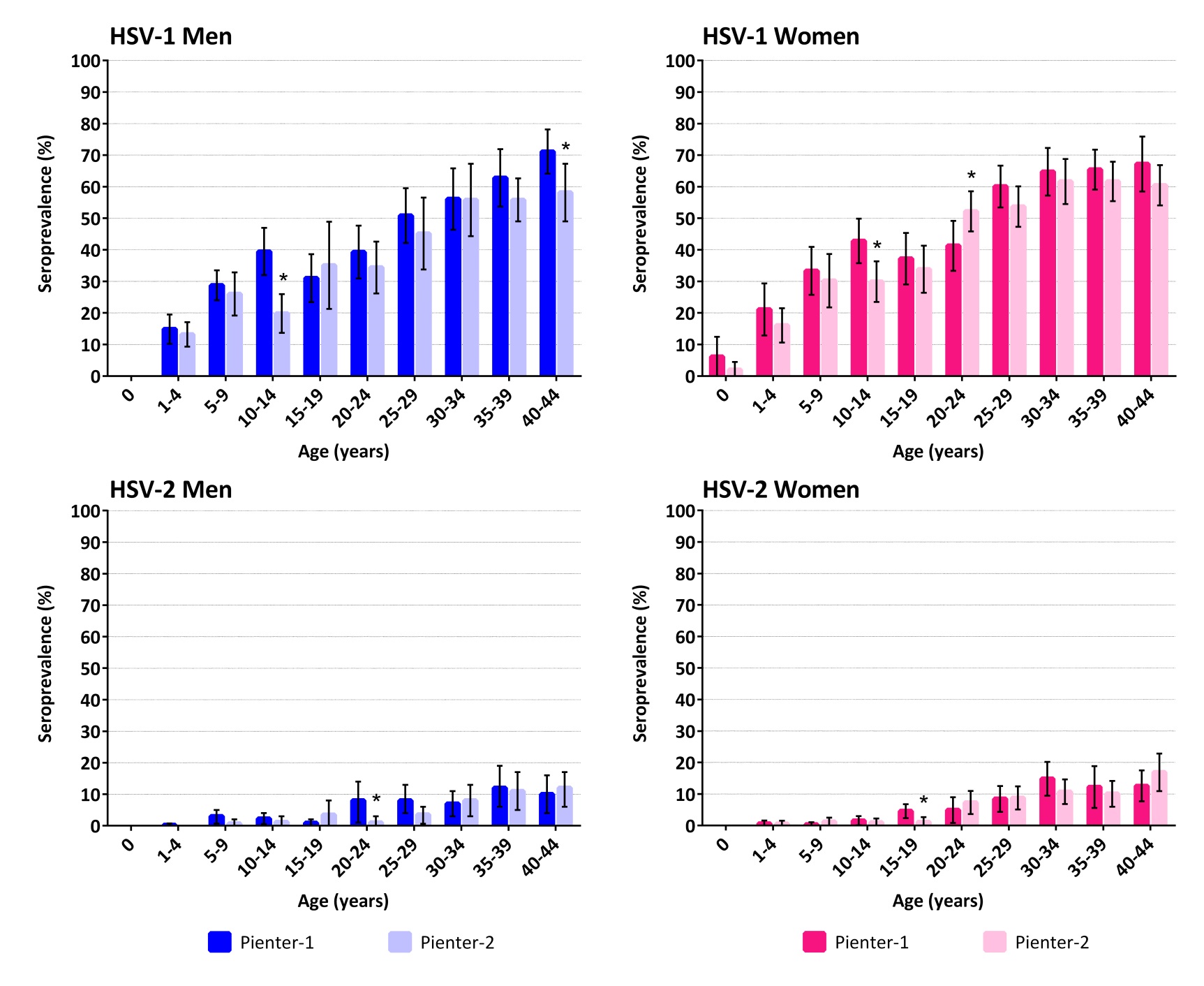
Figuur B41. Seroprevalentie van HSV1 en HSV2 met geslacht, leeftijd en Pienterstudie.
*Verschil in seroprevalentie tussen Pienter1 en Pienter2 is statistisch significant (p<0,05) (Woestenberg, 2016).
B4.7 Preventie
B4.7.1 Immunisatie
Er is vooralsnog geen effectief vaccin tegen HSV1 en HSV2 beschikbaar (Holmes, 2008; Mindel, 1998).
B4.7.2 Algemene preventieve maatregelen
Voorlichting en persoonlijke hygiëne vormen de basis van de preventieve maatregelen.
Contact met laesies of geïnfecteerd (lichaams)materiaal moet men proberen te vermijden.
Het gebruik van condooms kan de transmissiekans van HSV verlagen, maar transmissie niet geheel voorkomen.
B4.7.3 Desinfectie
Conform de LCI-richtlijn Reiniging, desinfectie en sterilisatie in de openbare gezondheidszorg.
Personeel op de kraam of kinderafdeling met herpes labialis gewoon kan doorwerken met inachtneming van bepaalde hygiënische maatregelen: niet met de handen aanraken van de laesies, frequent handen wassen en dragen van een mondmasker bij de verzorging van een baby totdat de laesies zijn ingedroogd (WIP, 2011).
Een moeder met herpes labialis kan gewoon op de afdeling verpleegd kan worden. Personeel wordt aangeraden de handen goed te wassen. Voorwerpen en kleding die met laesies in aanraking zijn geweest, dienen als besmet te worden beschouwd. Het kind kan gewoon bij de moeder verblijven onder voorwaarde dat ze haar baby niet kust, goed de handen wast en een mondmasker draagt bij de verzorging, totdat de laesies zijn ingedroogd. Daarnaast dienen eventuele herpetische laesies elders op het lichaam bedekt te worden. Borstvoeding is toegestaan mits er geen laesies zijn aan de tepel (WIP, 2010).
B4.8 Maatregelen
B4.8.1 Meldingsplicht
Voor herpesvirusinfecties geldt sinds december 2008 alleen meldingsplicht voor alle artsen aan de GGD als zij een voor hun praktijk ongewoon aantal gevallen van HSVinfecties vaststellen, als die een gevaar vormen voor de volksgezondheid (Wet Publieke Gezondheid, Hfdst V paragraaf 2, Artikel 21.3).
B4.8.2 Contactonderzoek en partnerwaarschuwing
Zie ook module C4. Gezien de hoge seroprevalentie voor HSV1 in de bevolking en het grote aantal asymptomatische HSV2dragers, heeft contactonderzoek weinig zin; ‘don’t hunt the virus’.
Het kan in vaste relaties wel zinvol zijn om de partner te waarschuwen en eventueel te testen. Zijn beide partners positief voor hetzelfde type HSV (aangetoond door kweek of NAAT of door typespecifieke serologie), dan hoeven binnen de relatie verder geen preventieve maatregelen genomen te worden. Bij hivpositieven kan het ook nuttig zijn de HSVstatus van de partner te weten (Van der Meijden, 1999).
In verband met de onrust die een soa kan geven in een relatie is goede en duidelijke informatie over het (asymptomatische) beloop van de infectie en kans op recidieven belangrijk.
B4.8.3 Maatregelen ten aanzien van patiënt en contacten
Effectieve preventie van herpes labialis en genitalis is bijzonder lastig, gezien de mogelijke levenslange besmettelijkheid en het feit dat herpes vaak overgedragen wordt door asymptomatische dragers. Toch kunnen bepaalde maatregelen genomen worden om de transmissiekans te verlagen.
Preventie van herpes labialis
Contact met actieve laesies of geïnfecteerd (lichaams)materiaal (kussen op de mond) moet men zoveel mogelijk vermijden. Daarnaast is goede handhygiëne van belang.
Preventie van herpes genitalis
Preventie van herpes genitalis omvat patiëntinstructies, gebruik van condooms en chronisch suppressieve behandeling. Counseling na de gestelde diagnose herpes genitalis omvat preventie van transmissie. Er moet worden uitgelegd dat transmissie kan plaatsvinden in afwezigheid van laesies. Indien er sprake is van een prodromale fase of als er actieve laesies zijn, wordt seksueel contact ontraden, ook met condoom (CDC, 2015).
Hoewel HSVtransmissie met condoomgebruik (ook in de asymptomatische fase) niet uitgesloten is, wegens uitscheiden van het virus op onbedekte slijmvliezen, wordt consistent condoomgebruik, ook in de asymptomatische fase, geadviseerd.
Een andere benadering van preventie is die van de chronisch suppressieve behandeling bij discordante paren. In de praktijk moeten de voordelen van chronisch suppressieve behandeling (reductie van HSV2transmissie van 3,6% naar 1,9% in 8 maanden; Corey, 2004) afgewogen worden tegen de nadelen (medicalisering, kans op resistentieontwikkeling).
Preventie van neonatale herpes
Onderstaande adviezen zijn afgeleid van verschillende richtlijnen (Foley, 2014).
Zwangerschap/baring:
Bij de zwangere dient, naast een nucleïnezuuramplificatietest (NAAT) van een verdachte laesie, typespecifiek serologisch onderzoek naar HSV (immunoglobuline Gantilichamen tegen HSV1 en HSV2) te worden verricht als tijdens de zwangerschap of baring er verdenking is op (een) primoinfectie met herpes genitalis. Vergelijk met serum van in het begin van de zwangerschap indien voorhanden. Wanneer dezelfde typespecifieke antilichamen gevonden worden als het HSV geïsoleerd in de NAAT is een primoinfectie niet waarschijnlijk en kan een sectio caesarea achterwege blijven.
Bij een (vermoedelijke) primaire anogenitale HSVinfectie in de laatste 6 weken van de zwangerschap wordt een sectio caesarea aanbevolen.
Bij verdenking op herpes recidivans of na een primoinfectie ontstaan voor 34 weken amenorroeduur kan een vaginale baring plaatsvinden. Bij aanwezigheid van verdachte laesies is het advies de vliezen zo lang mogelijk te laten staan en wordt het gebruik van invasieve monitoring; schedelelektrode en microbloedonderzoek afgeraden.
Neonaat
Bij neonaten van zwangeren met (een) voor herpes genitalis verdachte laesie(s) durante partu dient materiaal voor HSVonderzoek te worden afgenomen. Ook dient rekening gehouden te worden met serodiscordante koppels waarbij de vrouw seronegatief kan zijn voor HSV1 en HSV2, maar de partner seropositief is voor HSV1 en/of HSV2 (transmissiekans manvrouw 3,7%; Kimberlin, 2005).
Het is van belang materiaal af te nemen van zowel conjunctivae als orofarynx, bij voorkeur 24-48 uur post partum. Bij algemene verschijnselen ook NAATonderzoek van serum of plasma uitvoeren.
Ten aanzien van een ieder met een (recidiverende) herpes labialis die tijdens de geboorte of in de neonatale periode intensief met het kind omgaat (ouders, familie, ziekenhuispersoneel, kraamverzorgende, verloskundige):
- Voorkom direct contact tussen de laesie(s) en het kind (bijvoorbeeld niet kussen).
- Was de handen goed voor de verzorging van het kind.
- Bedek de laesies bij de verzorging van het kind met een mondmasker totdat de laesies zijn ingedroogd.
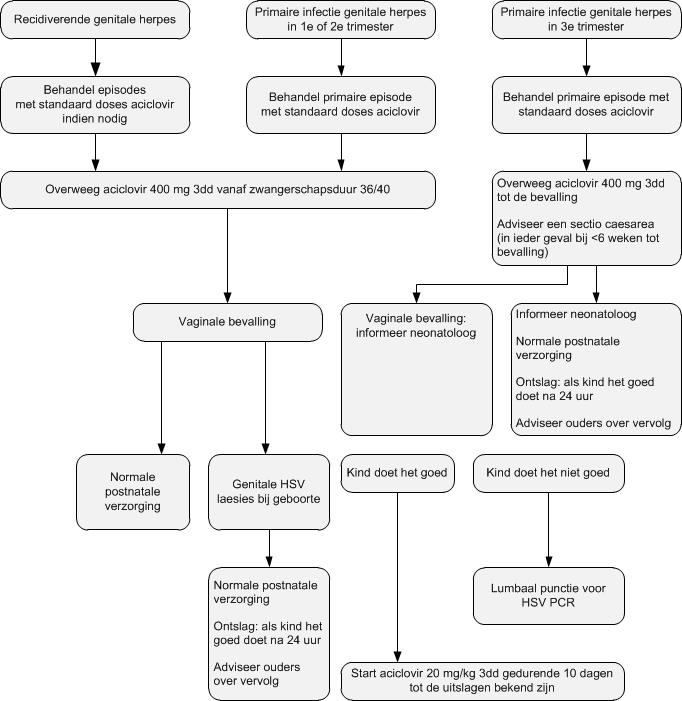
Figuur B4.2. Beleid bij herpes tijdens de zwangerschap en zorg voor de neonaat (bron: Foley 2014).
B4.8.4 Profylaxe
Het geven van profylaxe aan partners of andere contacten van personen met labiale en/of genitale herpeslaesies heeft over het algemeen weinig zin. Voor profylaxe dan wel vroegtijdige behandeling van neonatale herpes, zie onder paragraaf 4.8.3. Voor profylaxe dan wel onderhoudsbehandeling van patiënten, zie paragraaf B4.9.
Wering van werk, school, kinderdagverblijf en consultatiebureau
Wering van personen met herpes labialis is vanuit volksgezondheidsperspectief niet zinvol. Wel wordt aangeraden extra hygiënemaatregelen te treffen bij verzorgend personeel met actieve herpes labialis en werkzaam met neonaten (tot de leeftijd van 1 maand) of immunoincompetenten (Roizman, 2007; American Academy of Pediatrics, 2006). Maatregelen betreffen het dragen van een mondkapje bij verzorgende werkzaamheden en het in acht nemen van goede handhygiëne.
De Nederlandse Werkgroep Infectie Preventie (WIP) raadt aan personeel werkzaam in de directe patiëntenzorg met een (zeldzame) actieve herpetische laesie aan de vinger (fijt, ‘herpetic whitlow’) een werkverbod op te leggen (Daha, 1997). Hoewel er geen vergelijkende studies zijn verricht over transmissie bij fijt, wordt door sommige experts aangenomen dat het dragen van handschoenen mogelijk niet voldoende zou zijn om transmissie te voorkomen, en wordt verzorging van neonaten (en immunoincompetenten) door personeel met fijt afgeraden (Roizman, 2007; American Academy of Pediatrics, 2006).
Aangezien oudere, immunocompetente kinderen in principe geen risico meer hebben op het ontwikkelen van een ernstige herpesinfectie, zijn maatregelen voor personeel werkend met oudere kinderen (leidsters kinderdagverblijf, etc.) niet nodig.
Er zijn geen aanwijzingen dat personeelsleden met een herpes genitalis een besmettingsrisico vormen voor de patiënt bij handhaving van normale hygiëne.
B4.9 Behandeling
De indicaties voor behandeling bij herpes genitalis zijn een primoinfectie en hinderlijke recidieven. Therapie met nucleoside analoga (van aciclovir afgeleide middelen) onderdrukt de replicatie van het virus, maar heeft geen effect op het latent aanwezige virus, zodat na stoppen van de behandeling HSVreactivatie kan optreden. Dit wil zeggen dat alleen de duur en de ernst van de klachten erdoor worden bekort en de virusuitscheiding wordt beperkt. Mogelijk wordt ook het transmissierisico verkleind. Er is kortom, buiten de het verkorten van de duur van de klachten, nog veel onduidelijk over de zin tot behandelen. Het al dan niet starten van behandeling kan met de patiënt worden besproken.
B4.9.1 Primaire behandeling
Aanbevolen behandeling van HSV bij nietzwangere volwassenen
Het starten van therapie bij het vermoeden van een primoinfectie wordt doorgaans uitsluitend op de klinische presentatie gedaan (binnen 5 dagen na start van de symptomen), omdat diagnostiek in de praktijk niet snel mogelijk is. Primoinfecties geven meestal meer klachten dan recidieven en worden behandeld met orale toediening van (val)aciclovir of een analoog middel (Patel, 2017).
Het advies om primoinfecties met milde klachten al dan niet in alle gevallen te behandelen, kan niet goed worden onderbouwd. Onduidelijk is of behandeling van een primoinfectie de recidiefkans verlaagt. Tevens is in veel gevallen een als zodanig aangeduide primoinfectie, in feite een recidief. Anderzijds ontwikkelt een herpesinfectie zich geleidelijk en kan het enige tijd duren voor kan worden vastgesteld of sprake is van een ernstige infectie, waardoor in dat geval vertraging optreedt alvorens gestart wordt met een behandeling. Een eenduidig advies is niet te geven. De arts besluit samen met de patiënt of bij primoinfecties met milde klachten een behandeling wordt gestart of dat het beloop wordt afgewacht. Er is geen plaats voor topicale behandeling met nucleoside analogons zoals aciclovircrème vanwege gebrek aan bewijs omtrent de werkzaamheid.
Immuuncompetente volwassenen (Patel, 2017):
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen; of:
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; of:
- famciclovir 250 mg p.o., 3 dd gedurende 5 dagen.
Indien na 5 dagen nog nieuwe blaasjes ontstaan, dan kuur verlengen.
Immunoincompetente volwassenen:
- valaciclovir 1000 mg p.o., 2 dd gedurende 10 dagen of tot reepithelialisatie van de laesies; of:
- aciclovir 800 mg p.o., 3 dd gedurende 10 dagen of tot reepithelialisatie van de laesies, of:
- famciclovir 500 mg p.o., 3 dd gedurende 10 dagen of tot reepithelialisatie van de laesies.
Indien na 10 dagen nog nieuwe blaasjes ontstaan, dan kuur verlengen.
B4.9.2 Behandeling bij recidief/onderhoudsbehandeling
Aanbevolen behandeling van HSV bij niet zwangere volwassenen
Bij behandeling van een recidief kan als symptoombestrijding volstaan worden met een indrogende therapie, bijvoorbeeld indifferente crème met zinkoxide of zinksulfaat (zinkoxide vaselinecrème 10% FNA of zinksulfaat vaselinecrème 0,5% FNA) (Farmacotherapeutisch kompas, 2017). Bij veel pijnklachten kan pijnstilling worden gegeven (lokaal: lidocaïne zinkoxidesmeersel 5% FNA, of lidocaïnespray, of systemische pijnstilling). Het is belangrijk alert te zijn op eventuele secundaire bacteriële infecties en deze te behandelen.
Over de behandeling bestaat een grote mate van consensus. In vrijwel alle richtlijnen worden dezelfde behandelschema’s gepresenteerd (Patel, 2017, CDC, 2015; Holmes, 2008). Bij deze recidiverende infecties wordt zo snel mogelijk, maar in ieder geval binnen 48 uur na het ontstaan van de eerste tekenen (prodromen), met de antivirale medicatie gestart om enig effect te kunnen bewerkstelligen. Het is dan ook aan te bevelen bij frequente en/of hinderlijk ervaren recidieven de patiënt een voorraad in huis te laten halen, om bij het begin van een volgende episode direct te kunnen starten.
Immuun(in)competente volwassenen (Patel, 2017):
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen; of:
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; of:
- famciclovir 125 mg p.o., 2 dd gedurende 5 dagen.
Korte therapieën zijn te overwegen bij frequente recidieven (Patel, 2017):
- valaciclovir 500 mg p.o., 2 dd gedurende 2 dagen; of:
- aciclovir 800 mg p.o., 3 dd gedurende 2 dagen; of:
- famciclovir 1000 mg p.o., 2 dd voor 1 dag.
Onderhoudsbehandeling
Patiënten met zeer frequente recidiverende infecties (>6 per jaar) en veel klachten komen in aanmerking voor onderhoudstherapie met (val)aciclovir of een analoog middel. Antivirale therapie voor recidiverende herpes genitalis reduceert het aantal recidieven met 70-80% en verkort de duur van de laesies.
Onderhoudsbehandeling om recidieven te voorkomen:
- valaciclovir 500 mg p.o., 1 dd;
- valaciclovir 1000 mg p.o., 1 dd;
- aciclovir 400 mg p.o., 2 dd;
- famciclovir 250 mg p.o., 2 dd.
B4.9.3 Behandeling van HSV bij zwangerschap, van pasgeborenen en kinderen
Behandeling van HSV bij zwangerschap
Voor preventie van neonatale herpes, zie onder paragraaf 4.8.3. Zwangeren met een, al dan niet primaire, herpes genitalis die veel klachten veroorzaakt, kunnen met aciclovir, valaciclovir en famciclovir behandeld worden, onafhankelijk van de duur van de zwangerschap. Er is wel een voorkeur voor aciclovir, omdat daar de meeste gegevens over zijn (Foley, 2014; Westhoff, 2011).
Risicofactoren voor transmissie van HSV naar neonaat (Pinninti, 2014):
- type maternale infectie: eerste periode met primaire infectie HSV1;
- maternale HSVantistoffenstatus;
- wijze van partus (vaginaal of sectio caesarea);
- duur gebroken vliezen;
- integriteit huidbarrière (gebruik schedel electrode en ander instrumentarium);
- type HSV (HSV1 en HSV2).
Primaire infectie
Behandeling:
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; of:
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen; en:
- overweeg in de laatste 4 weken van de zwangerschap aciclovir 400 mg 3 dd p.o.
Partusbeleid:
- sectio caesarea wordt geadviseerd bij >28 weken amenorroe en <6 weken tot bevalling;
- indien moeder geen sectio wil, overweeg dan aciclovir 3 dd 5 mg/kg i.v. intrapartum met daarna behandeling neonaat;
- bij asymptomatische excretie dient bij zwangeren foetale monitoring middels schedelelektrode en kunstverlossing vermeden te worden (Westhoff, 2011).
Vroeg gebroken vliezen:
- weinig evidence, besluit is afhankelijk van gestatieduur, daarom multidisciplinair overleg noodzakelijk;
- bij besluit tot geboorte blijft er het voordeel van een sectio, bij een conservatief beleid is intraveneus aciclovir aangewezen.
Recidiverende infectie
Onafhankelijk van amenorroeduur:
- in principe geen antivirale behandeling, alleen ondersteunend;
- overweeg in de laatste 4 weken van de zwangerschap suppressieve therapie met aciclovir 400 mg p.o., 3 dd.
Vroeg gebroken vliezen <34 weken:
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; of:
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen.
Vroeg gebroken vliezen >34 weken:
- aanwezigheid van laesies heeft geen invloed op neonatale morbiditeit of mortaliteit.
Hiv + HSV bij zwangerschap
Primaire infectie
Zoals aanbevolen behandeling van HSV (zie hierboven).
Recidiverende infectie
Overweeg suppressieve behandeling met aciclovir 3 dd 400 mg vanaf 32 weken.
Behandeling van HSV bij pasgeborenen en kinderen
Tijdens de baring wordt bij onverwachte aanwezigheid van verdachte laesies bij de zwangere durante partu materiaal afgenomen voor onderzoek op HSV:
- direct afname EDTAbloed en liquor voor PCR op HSV;
- na 2448 uur swabs huid, conjunctiva, orofarynx en rectum (dit om directe contaminatie van moeder uit te sluiten);
- neonaten met een symptomatische herpessimplexinfectie, een significante klinische verdenking en/of met een positieve kweek of NAAT moeten direct behandeld worden met (i.v.) aciclovir.
Ouders, verzorgers, familie en vrienden krijgen een advies over het risico van postnatale transmissie van herpes bij actieve orale laesies.
Primaire infectie
Sectio:
- behandeling conservatief, geen afname van kweken, normale neonatale behandeling na 24 uur observatie.
Vaginaal:
- afname swabs huid, conjunctiva, orofarynx en rectum 24-48 uur na geboorte (dit om directe contaminatie van moeder uit te sluiten);
- start empirische behandeling (zie onder voor dosering) tot infectie met diagnostiek onwaarschijnlijk is gemaakt.
Recidiverende infectie
Geen afname van materiaal en geen actieve behandeling.
Congenitale HSVinfectie
A terme neonaat:
- aciclovir 60 mg/kg/dag i.v., in 3 doses;
- behandelduur:
- CNS en verspreid: 21 dagen;
- beperkt tot lokaal huid, oog en mond: 14 dagen.
Herpes simplex encefalitis
03 maanden:
- aciclovir 60 mg/kg/dag i.v., in 3 doses gedurende 14-21 dagen.
3 maanden18 jaar:
- aciclovir 30 mg/kg/dag i.v., in 3 doses gedurende 14-21 dagen.
Behandeling van complicaties bij volwassenen
Indien er complicaties aanwezig zijn, is klinische behandeling aangewezen, eventueel met intraveneuze antivirale therapie. Intraveneuze antivirale therapie is ook aangewezen bij neurologische complicaties (onder andere meningoencefalitis) en ernstige HSVinfectie:
- aciclovir 10 mg/kg i.v., elke 8 uur gedurende 14-21 dagen tot klinische verbetering optreedt.
Bij oogheelkundige herpesaandoeningen dient met spoed verwezen te worden naar de oogarts. Bij een herpetische keratitis kan de infectie in verschillende lagen van het hoornvlies tot uiting komen, waarvoor vaak tot 1 jaar orale systemische antivirale (valaciclovir) en lokale behandeling (steroïden, aciclovir) noodzakelijk is.
Herpesvirussen kunnen een uveitis anterior veroorzaken waarvoor bij frequente recidieven ook minimaal 1 jaar orale systemische antivirale (valaciclovir 500 mg 2 dd) en lokale behandeling (steroïden) gegeven worden.
Een acute retina necrose is de meest ernstigste vorm. Een klinische behandeling met aciclovir 10 mg/kg i.v. elke 8 uur gedurende 1421 dagen is aangewezen, eventueel na 1 week aangevuld met prednison om ontstekingsverschijnselen te temperen. Hierna volgt ook systemische antivirale behandeling voor minimaal 1 jaar.
B4.9.4 Nacontrole
Indien complicaties of ernstig verloop wordt gevreesd, bijvoorbeeld vanwege een onderliggend lijden.
Referenties
- American Academy of Pediatrics. Herpes simplex. In: Pickering LK, Baker CJ, Long SS, McMillan JA. Red Book: 2006 Report of the Committee on Infectious Deseases. 27th Edition. American Academy of Pediatrics, 2006: 361-371.
- Arvaja M, Lehtinen M, Koskela P, Lappalainen M, Paavonen J, Vesikari T. Serological evaluation of herpes simplex virus type 1 and type 2 infections in pregnancy. Sex Transm Infect 1999; 75: 168171.
- AshleyMorrow R, Nollkamper J, Robinson NJ, Bishop N, Smith J. Performance of focus ELISA tests for herpes simplex virus type 1 (HSV1) and HSV2 antibodies among women in ten diverse geographical locations. Clin Microbiol Infect 2004; 10: 530536.
- Benedetti J, Corey L, Ashley R. Recurrence rates in genital herpes after symptomatic firstepisode infection. Annals of Internal Medicine 1994; 121: 847854.
- Benedetti JK, Zeh J, Corey L. Clinical reactivation of genital herpes simplex virus infection decreases in frequency over time. Annals of Internal Medicine 1999; 131: 1420.
- CDC. Genital HSV infections. In: 2015 Sexually transmitted diseases treatment guidelines. Centers for Disease Control and Prevention, 2015. https://www.cdc.gov/std/tg2015/herpes.htm.
- Celum CL, Robinson NJ, Cohen MS. Potential effect of HIV type 1 antiretroviral and herpes simplex virus type 2 antiviral therapy on transmission and acquisition of HIV type 1 infection. J Infect Dis 2005; 191 Suppl 1: S107S114.
- Corey L, Wald A, Patel R, Sacks SL, Tyring SK, Warren T, Douglas JM Jr, Paavonen J, Morrow RA, Beutner KR, Stratchounsky LS, Mertz G, Keene ON, Watson HA, Tait D, VargasCortes M. Oncedaily valacyclovir to reduce the risk of transmission of genital herpes. N Engl J Med 2004; 350: 1120.
- Daha, T. Herpes Simlex Virus. Tijdschrift Hygiëne en Infectiepreventie 1997; 4: 144.
- Drake S, Taylor S, Brown D, Pillay D. Improving the care of patients with genital herpes. BMJ 2000; 321: 619623.
- Engelberg P, Carrell D, Krantz E, Corey L, Wald A. Natural history of genital herpes simplex virus type 1 infection. Sex Transm Dis 2003; 30: 174 177.
- Eskild A, Jeansson S, Hagen JA, Jenum PA, Skrondal A. Herpes simplex virus type-2 antibodies in pregnant women: the impact of the stage of pregnancy. Epidemiol Infect 2000; 125: 685-692.
- Farmacotherapeutisch kompas. 2017. https://www.farmacotherapeutischkompas.nl/
- Foley E, Clarke E, Beckett VA, Harrison S, Pillai A, FitzGerald M, Owen P, LowBeer N, Patel R. Management of genital herpes in pregnancy. BASHH/RCOG, 2014.
- Forsgren M, Klapper PE. Herpes simplex virus type 1 and type 2. In: Zuckerman AJ, Banatvala JE, Schoub BD, Griffiths PD, Mortimer P. Principles and practice of clinical virology. 6th Edition. Wiley-Blackwell, 2009: 124126.
- Gray RH, Li X, Wawer MJ, Serwadda D, Sewankambo NK, WabwireMangen F, Lutalo T, Kiwanuka N, Kigozi G, Nalugoda F, Meehan MP, Robb M, Quinn TC. Determinants of HIV1 load in subjects with early and later HIV infections, in a generalpopulation cohort of Rakai, Uganda. J Infect Dis 2004; 189: 12091215.
- Hemelaar SJAL, Pouran J, Steegers EAP, van der Meijden W. Neonatal herpes infections in The Netherlands in the period 20062011. J Matern Fetal Neonatal Med 2015; 28: 905909.
- Holmes KK, Sparling PF, Stamm WE, Piot P, Wasserheit JN, Corey L, Cohen MS, Watts DH. Sexually transmitted diseases. 4th Edition. Mc GrawHill, 2008.
- James SH, Kimberlin DW. Neonatal herpes simplex virus infection. Infect Dis Clin North Am 2015; 29: 391400.
- Kimberlin DW. Herpes simplex infections in neonates and early childhood. Semin Pediatr Infect Dis 2005; 16: 271281.
- Kimberlin DW. Herpes simplex infections of the newborn. Seminars in Perinatology 2007; 31: 1925.
- Kimura H, Ito Y, Futamara M, Ando Y, Yabuta Y, Hoshino Y, Nishiyama Y, Morishima T. Quantitation of viral load in neonatal herpes simplex virus infections and comparison between type 1 and type 2. J Med Virol 2002; 67; 349353.
- Lafferty WE, Coombs RW, Benedetti J, Critchlow C, Corey L. Recurrences after oral and genital herpes simplex virus infection. Influence of site of infection and viral type. N Engl J Med 1987; 316: 1444-1449.
- Langenberg AG, Corey L, Ashley RL, Leong WP, Straus SE. A prospective study of new infections with herpes simplex virus type 1 and type 2. N Engl J Med 1999; 341: 14321438.
- Looker KJ, Magaret AS, May MT, Turner KM, Vickerman P, Gottlieb SL, Newman LM. Global and regional estimates of prevalent and incident herpes simplex virus infection type 1 in 2012. PLos One 2015a; 10: e0140765.
- Looker KJ, Magaret AS, Turner KM, Vickerman P, Gotlieb SL, Newman LM. Global and regional estimates of prevalent and incident herpes simplex virus infection type 2 in 2012. PLoS One 2015b; 10: e114989.
- Malm G, Forsgren M. Neonatal herpes simplex infections: HSV DNA in cerebrospinal fluid and serum. Arch Dis Child Fetal Neonatal Ed 1999; 81: F24F29.
- Mark HD, Nanda JP, Roberts J, Rompalo A, Melendez JH, Zenilman J. Performance of focus ELISA tests for HSV1 and HSV2 antibodies among university students with no history of genital herpes. Sex Transm Dis 2007; 34: 681685.
- Mark KE, Wald A, Magaret AS, Selke S, Olin F, Huang ML, Corey L. Rapidly cleared episodes of herpes simplex virus reactivation in immunocompetent adults. J Infect Dis 2008; 198: 11411149.
- Mindel A. Genital herpes: how much of a public health problem? Lancet 1998; 351 (suppl 3): 16-18.
- Morrow RA, Friedrich D, Krantz E. Performance of the focus and kalon enzymelinked immunosorbent assays for antibodies to herpes simplex virus type 2 glycoprotein G in culturedocumented cases of genital herpes. J Clin Microbiol 2003; 41: 52125214.
- Nagot N, Ouédraogo A, Foulongne V, Konaté I, Weiss HA, Vergne L, Defer MC, Djagbaré D, Sanon A, Andonaba JB, Becquart P, Segondy M, Vallo R, Sawadogo A, Van de Perre P, Mayaud P. Reduction of HIV1 RNA levels with therapy to suppress herpes simplex virus. N Engl J Med 2007; 356: 790799.
- Patel R, Kennedy OJ, Clarke E, Geretti A, Nilsen A, Lautenschlager S, Green J, Donders G, van der Meijden W, Gomberg M, Moi H, Foley E. 2017 European guidelines for the management of genital herpes. Int J STD AIDS. 2017 Dec;28(14):1366-1379.
- Pellet PE, Roizman B. Herpesviridae. In: Knipe DM, Howley PM. Fields Virology. 6th Edition. Wolters Kluwer/Lippincott Williams & Wilkins, 2013: 1802-1822.
- Phipps W, Saracino M, Magaret A, Selke S, Remington M, Huang ML, Warren T, Casper C, Corey L, Wald A. Persistent genital herpes simplex virus2 shedding years following the first clinical episode. J Infect Dis 2011; 203: 180187.
- Pinninti SG, Angara R, Feja KN, Kimberlin DW, Leach CT, Conrad DA, McCarthy CA, Tolan RW Jr. Neonatal herpes disease following maternal antenatal antiviral suppressive therapy: a multicenter case series. J Pediatr 2012 Feb 14.
- Pinninti SG, Kimberlin DW. Management of neonatal herpes simplex virus infection and exposure. Arch Dis Child Fetal Neonatal Ed 2014; 99: F240F244.
- Roizman B, Knipe Dm, Whitley RJ. Herpes simplex viruses. In: Knipe DM, Howley PM. Fields virology. 5th Edition. Wolters Kluwer/Lippincott Williams & Wilkins, 2007: 2501.
- Schacker T, Zeh J, Hu H, Shaughnessy M, Corey L. Changes in plasma human immunodeficiency virus type 1 RNA associated with herpes simplex virus reactivation and suppression. J Infect Dis 2002; 186: 17181725.
- Schiffer JT, Wald A, Selke S, Corey L, Magaret A. The kinetics of mucosal herpes simplex virus2 infection in humans: evidence for rapid viralhost interactions. J Infect Dis 2011; 204: 554561.
- Sen P, Barton SE. Genital herpes and its management: clinical review. BMJ 2007; 334: 10481052.
- Summerton J, Riedesel M, Laeyendecker O, Gaydos C, Maldeis NE, Hardick A, Morriw RA, Quinn TC. Effect of sexually transmitted disease (STD) coinfections on performance of three commercially available immunosorbent assays used for detection of herpes simplex virus type 2specific antibody in men attending Baltimore, Maryland, STD clinics. Clin Vaccine Immunol 2007; 14: 15451549.
- Tata S, Johnston C, Huang ML, Selke S, Magaret A, Corey L, Wald A. Overlapping reactivations of herpes simplex virus type 2 in the genital and perianal mucosa. J Infect Dis 2010; 201: 499-504.
- Tronstein E, Johnston C, Huang ML, Selke S, Magaret A, Warren T, Corey L, Wald A. Genital shedding of herpes simplex virus among symptomatic and asymptomatic persons with HSV2 infection. JAMA 2011; 305: 14411449.
- Van den Broek IVF, van Aar F, van Oeffelen AAM, Woestenberg PJ, Heijne JCM, den Daas C, Hofstraat SHI, Hoenderboom BM, van Wees D, van Sighem Al, Nielen MMJ, van Benthem BHB. Sexually transmitted infections in the Netherlands in 2015. RIVM Rapport 2015-0026. Rijksinstituut voor Volksgezondheid en Milieu, 2016. http://www.rivm.nl/Documenten_en_publicaties/Wetenschappelijk/Rapporten/2016/juni/Sexually_transmitted_infections_in_the_Netherlands_in_2015.
- Van der Beek MT, Laheij AM, RaberDurlacher JE, von dem Borne PA, Wolterbeek, van der Blijde Brouwer CS, van Loveren C, Claas EC, Kroes AC, de Soet JJ, Vossen AC. Viral loads and antiviral resistance of herpesviruses and oral ulcerations in hematopoietic stem cell transplant recipients. Bone Marrow Transplant 2012; 47: 1222-1228.
- Van der Meijden WI. Expertmeeting partnerwaarschuwing: zin en onzin van partnerwaarschuwing bij virale SOA. Notulen 1999.
- Van Rooijen MS, Roest W, Hansen G, Kwa D, de Vries HJ. Falsenegative typespecific glycoprotein G antibody responses in STI clinic patients with recurrent HSV1 or HSV2 DNA positive genital herpes, The Netherlands. Sex Transm Infect 2016; 92: 257260.
- Wald A, Langenberg AG, Link K, Izu AE, Ashley R, Warren T, Tyring S, Douglas JM Jr, Corey L. Effect of condoms on reducing the transmission of herpes simplex virus type 2 from men to women. JAMA 2001; 285: 31003106.
- Wald A, Huang ML, Carrell D, Selke S, Corey L. Polymerase chain reaction for detection of herpes simplex virus (HSV) DNA on mucosal surfaces: comparison with HSV isolation in cell culture. J Infect. Dis 2003; 188: 13451351.
- Westhoff GL, Little SE, Caughey AB. Herpes simplex virus and pregnancy: a review of the management of antenatal and peripartum herpes infections. Gynecol Surv 2011; 66: 629638.
- WHO. Guidelines for the treatment of genital herpes simplex virus. World Health Organizaion, 2016.
- WIP. Richtlijn Babyvoeding. Werkgroep Infectie Preventie, 2010. http://www.rivm.nl/Documenten_en_publicaties/Professioneel_Praktisch/Richtlijnen/Infectieziekten/WIP_Richtlijnen/WIP_Richtlijnen/Ziekenhuizen/WIP_richtlijn_Babyvoeding_ZKH.
- WIP. Richtlijn veilig werken op de afdeling Neonatologie. Werkgroep Infectie Preventie, 2011. http://www.rivm.nl/Documenten_en_publicaties/Professioneel_Praktisch/Richtlijnen/Infectieziekten/WIP_Richtlijnen/WIP_Richtlijnen/Ziekenhuizen/WIP_richtlijn_Neonatologie_veilig_werken_ZKH.
- Woestenberg PJ, Tjhie JH, de Melker HE, van der Klis FR, van Bergen JE, van der Sande MA, van Benthem BH. Herpes simplex virus type 1 and type 2 in the Netherlands: seroprevalence, risk factors and changes during a 12year period. BMC Infect Dis 2016; 16: 364.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 25-02-2019
Laatst geautoriseerd : 25-02-2019
Geplande herbeoordeling :
Een richtlijn heeft alleen zeggingskracht als op continue basis onderhoud plaatsvindt, op grond van systematische monitoring van zowel de medisch wetenschappelijke literatuur als praktijkgegevens en door gebruikers van de richtlijn aangeleverde commentaren. Voor deze richtlijn is afgesproken periodiek de literatuur te bekijken om nieuwe ontwikkelingen te volgen. Bij essentiële ontwikkelingen kan besloten worden om de gehele richtlijnwerkgroep bij elkaar te roepen, de richtlijn aan te passen en deze onder de belanghebbenden te verspreiden.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn doet aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering en is gericht op het vaststellen van goed medisch handelen.
Doelgroep
Soa’s zijn bij uitstek een multidisciplinair onderwerp. Zo kunnen clinici zoals dermatologen, gynaecologen, urologen, kinderartsen, internisten, neurologen, oogartsen, reumatologen en huisartsen geconfronteerd worden met soagerelateerde klachten en hulpvragen. Daarnaast is specifieke diagnostische expertise aanwezig bij medisch microbiologen en zijn de publieke gezondheidszorg en infectiepreventie-gerelateerde aspecten het werkterrein van de GGD. Tevens kan seksuologische of psychologische problematiek, zoals seksverslaving en identiteitsproblemen, een verhoogd risico op een soa opleveren. De richtlijn is bestemd voor leden van de desbetreffende medische en verpleegkundige beroepsgroepen. Voor patiënten kan algemene en specifieke informatie omtrent de meeste soa’s gevonden worden via www.thuisarts.nl of Soa Aids Nederland (www.soaaids.nl). Hier zijn ook patiëntenfolders en voorlichtingsmateriaal te bestellen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een werkgroep samengesteld, bestaande uit een vertegenwoordiging van dermatologen, gynaecologen, artsenmicrobioloog, huisartsen, internisten, kinderartsen, een oogarts, artsen maatschappij en gezondheid, een neuroloog en een uroloog. Daarnaast zijn er leden aangeschoven van buiten de curatiefmedische sector, zoals van het RIVM, V&VN en Soa Aids Nederland. Verder nam een patiëntvertegenwoordiger van de Hiv Vereniging Nederland deel. Bij het samenstellen van de werkgroep is rekening gehouden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en nietacademische achtergrond. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel lid ontving gunsten met het doel de richtlijnen te beïnvloeden. De conceptversie van de richtlijn is voor commentaar ook toegestuurd aan de Nederlandse Vereniging voor Reumatologie, de Nederlandse Vereniging voor Cardiologie, de Nederlandse Vereniging van MaagDarmLeverartsen en de Nederlandse Vereniging voor KeelNeusOorheelkunde en Heelkunde van het HoofdHalsgebied. Bij een volgende versie van de richtlijn kan overwogen worden de werkgroep uit te breiden met meer aanpalende specialismen.
Werkgroep herziening 2018
|
Naam |
Functie |
Affiliatie |
Vertegenwoordiging |
|
prof. dr. H.J.C. de Vries |
Dermatoloog, voorzitter werkgroep |
AMC, GGD Amsterdam |
NVDV |
|
dr. A.P. van Dam |
Artsmicrobioloog, medevoorzitter werkgroep |
OLVG |
NVMM |
|
dr. C.J. Bax |
Gynaecoloog |
AMC |
NVOG |
|
prof. dr. J.E.A.M. van Bergen |
Huisarts, epidemioloog, public health arts |
Soa Aids Nederland |
Soa Aids Nederland / NHG |
|
drs. Y.Y. Chung |
Artsonderzoeker richtlijnontwikkeling |
NVDV |
NVDV |
|
drs. N.H. ten Dam-van Loon |
Oogarts |
UMC Utrecht |
NOG |
|
dr. J.J.E. van Everdingen |
Directeur NVDV |
NVDV |
NVDV |
|
K. Geelen |
Coördinator beleid en kwaliteit richtlijnontwikkeling |
NVDV |
NVDV |
|
dr. H. Götz |
Arts Maatschappij en Gezondheid, Infectieziektebestrijding |
GGD Rotterdam-Rijnmond |
NVIB / WASS |
|
drs. E. Hoornenborg |
Internist-infectioloog |
GGD |
NVHB |
|
drs. A.G.W van Hulzen |
Verpleegkundig specialist |
Isala |
V&VN |
|
dr. S.H. Kardaun |
Dermatoloog |
UMC Groningen |
NVDV |
|
dr. E. Lanjouw |
Dermatoloog |
VUmc |
NVDV |
|
dr. E. van Leeuwen |
Gynaecoloog |
AMC |
NVOG |
|
drs. B. Meijer |
Uroloog |
Flevoziekenhuis |
NVU |
|
J. Moorlag |
Patiëntvertegenwoordiger |
Poz and Proud, Hiv Vereniging |
Hiv Vereniging |
|
T. Oomen |
Beleidsadviseur / sociaal verpleegkundige (n.p.) |
RIVM |
RIVM |
|
dr. P.M. Oostvogel |
Arts-microbioloog |
Streeklaboratorium GGD Amsterdam |
GGD Amsterdam |
|
prof dr. P. Portegies |
Neuroloog |
OLVG, AMC |
NVN |
|
dr. K.D. Quint |
Dermatoloog |
LUMC |
NVDV |
|
dr. B.J.A. Rijnders |
Internist |
Erasmus MC |
NVHB |
|
dr. G.I.J.G. Rours |
Kinderarts, klinisch epidemioloog |
Erasmus MC |
NVK |
|
drs. A.A.J. van der Sande |
Arts-onderzoeker richtlijnontwikkeling |
NVDV |
NVDV |
|
dr. M.A.B. van der Sande |
Arts-epidemioloog |
RIVM |
RIVM |
|
dr. H.J. Scherpbier |
Kinderarts |
AMC, Emma kinderziekenhuis |
NVK |
|
dr. M. Schim van der Loeff |
Arts-epidemioloog |
AMC/ GGD Amsterdam |
GGD Amsterdam |
|
dr. V. Sigurdsson |
Dermatoloog |
UMC Utrecht |
NVDV |
|
drs. R. Soetekouw |
Internist |
Spaarne Gasthuis |
NIV |
|
dr. J. van Steenbergen |
Arts-epidemioloog |
RIVM |
RIVM |
|
drs. A.H. Teeuw |
Kinderarts sociale pediatrie |
AMC |
NVK |
|
dr. H.T. Tjhie |
Arts-microbioloog |
Stichting PAMM |
NVMM |
|
dr. C. E. Vergunst |
Dermatoloog |
GGD Amsterdam |
NVDV |
|
drs. L. Verlee |
Huisarts / wetenschappelijk medewerker |
NHG |
NHG |
Werkgroep versie 2012
|
Naam |
Functie |
Affiliatie |
Vertegenwoordiging |
|
prof. dr. H.J.C. de Vries |
Dermatoloog, voorzitter werkgroep |
AMC, GGD Amsterdam |
NVDV |
|
prof. dr. G.J.J. van Doornum |
Arts-microbioloog |
AMC |
NVMM |
|
dr. C.J. Bax |
Gynaecoloog |
AMC |
NVOG |
|
prof. dr. J.E.A.M. van Bergen |
Huisarts, epidemioloog, public health arts |
Soa Aids Nederland |
Soa Aids Nederland |
|
drs. J. de Bes |
Arts-onderzoeker richtlijnontwikkeling |
NVDV |
NDVD |
|
dr. A.P. van Dam |
Arts-microbioloog |
OLVG |
NVMM |
|
dr. J.J.E. van Everdingen |
Directeur NVDV |
NVDV |
NVDV |
|
dr. H. Götz |
Arts infectieziekten |
GGD Rotterdam-Rijnmond |
GGD |
|
drs. A.G.W van Hulzen |
Verpleegkundig specialist |
Isala klinieken |
V&VN |
|
dr. S.H. Kardaun |
Dermatoloog |
UMC Groningen |
NVDV |
|
dr. E. Lanjouw |
AIOS dermatologie |
Erasmus MC |
NVDV |
|
dr. E. van Leeuwen |
Gynaecoloog |
AMC |
NVOG |
|
drs. M.T.W. Lock |
Uroloog |
UMC Utrecht |
NVU |
|
prof dr. P. Portegies |
Neuroloog |
OLVG Amsterdam, AMC |
NVN |
|
dr. K.D. Quint |
AIOS dermatologie |
LUMC |
NVDV |
|
dr. B.J.A. Rijnders |
Internist |
Erasmus MC |
NVHB |
|
Kinderarts, klinisch epidemioloog |
Erasmus MC |
NVK |
|
|
dr. M.A.B. van der Sande |
Arts-epidemioloog |
RIVM |
RIVM |
|
dhr. L. Schenk |
Patiëntvertegenwoordiger |
Poz and Proud, Hiv vereniging |
Hiv Vereniging |
|
dr. H.J. Scherpbier |
Kinderarts |
AMC, Emma kinderziekenhuis |
NVK |
|
dr. V. Sigurdsson |
Dermatoloog |
UMC Utrecht |
NVDV |
|
drs. R. Soetekouw |
Internist |
Kennemer Gasthuis |
NIV |
|
dr. J. van Steenbergen |
Arts-epidemioloog |
RIVM |
RIVM |
|
dr. H.T. Tjhie |
Arts-microbioloog |
Stichting PAMM |
NVMM |
|
drs. L. Verlee |
Huisarts / wetenschappelijk medewerker |
NHG |
NHG |
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de ontwikkeling van het concept van de richtlijn is zoveel mogelijk rekening gehouden met de implementatie van de richtlijn en de daadwerkelijke uitvoerbaarheid van de aanbevelingen. De richtlijn wordt verspreid onder alle relevante beroepsgroepen en ziekenhuizen. Ook wordt een samenvatting van de richtlijn aangeboden aan het Nederlands Tijdschrift voor Geneeskunde en zal in de specifieke vaktijdschriften aandacht worden besteed aan de richtlijn.
Werkwijze
De werkgroep werkte in 2016 aan een conceptrichtlijntekst, gebaseerd op de 2012 versie. De werkgroepleden werden verdeeld in subgroepen die zich elk bogen over een module. Via een algemene search en controle van referenties is bruikbare literatuur die na 2012 is gepubliceerd, verzameld. De werkgroepleden hebben de literatuur beoordeeld op inhoud en kwaliteit. Bij het tot stand komen van de 2012 versie bleek de bewijskracht voor de beantwoording van de toenmalig geformuleerde uitgangsvragen teleurstellend (er kwamen geen adviezen met een bewijskracht boven niveau 4 uit). De richtlijn is daarom hoofdzakelijk gebaseerd op de mening van de werkgroep na uitvoerige discussie, aanvullend gericht literatuuronderzoek en de hierboven genoemde eerder gepubliceerde richtlijnen. De teksten werden tijdens subgroepvergaderingen en een tweedaagse plenaire bijeenkomst besproken en na verwerking van de commentaren geaccordeerd. Er is getracht om de samenhang en afstemming tussen de richtlijnen die door de verschillende echelons worden gebruikt te versterken. Als basistekst is uitgegaan van de soarichtlijnen van het LCI die eerder door de in Nederland aanwezige deelexperts zijn samengesteld.
De uiteindelijke teksten vormden samen de conceptrichtlijn die in 2017 aan alle betrokken beroepsverenigingen en instanties werd aangeboden. Tevens werd men in staat gesteld om via websites van de desbetreffende verenigingen commentaar op de richtlijn te geven. De commentaren zijn in deze definitieve versie van de richtlijn verwerkt.
De update 2019 op de richtlijn is tot stand gekomen op basis van commentaar op de vorige versie (2018), en evaluatie door de werkgroep. Er zijn geen substantiële wijzigingen aangebracht, maar storende fouten zoals in doseringen zijn gecorrigeerd en verduidelijkingen zijn waar nodig aangebracht.
Wetenschappelijke bewijsvoering
De aanbevelingen uit deze richtlijn zijn, voor zover mogelijk, gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek. Daarbij ligt de nadruk op de diagnostiek en de behandeling. Een literatuuronderzoek werd verricht via PubMed vanaf het jaar 2000 met gebruikmaking van relevante zoektermen. Na screening op titel en samenvatting werden de studies ingedeeld volgens de criteria van mate van bewijs. Artikelen van matige of slechte kwaliteit werden uitgesloten. Na deze selectie bleven de artikelen over die als onderbouwing in de richtlijn staan vermeld. Daar waar geen gepubliceerd bewijs voorhanden was, is gebruik gemaakt van expert opinies zoals deze tijdens de retraite in september 2016 en later werden geformuleerd. Daarnaast is additioneel literatuuronderzoek gedaan, dat per module wordt vermeld. Een belangrijk hulpdocument ter ondersteuning van de wetenschappelijke bewijsvoering vormden de Evidence Papers for the CDC Sexually Transmitted Diseases Treatment Guidelines, gepubliceerd als supplement van het tijdschrift Clinical Infectious Diseases (supplement 8 van 15 december 2015), alsmede de 2016 herziening van de WHOrichtlijnen.
Begripsbepaling
Seksueel overdraagbare aandoeningen (soa's) behoren tot de infectieziekten die onze voortdurende aandacht behoeven. Omdat veel soa’s asymptomatisch verlopen, en er dus eigenlijk ook geen zichtbare aandoening is, gaat soms de voorkeur uit om, in navolging van de term sexually transmitted infections uit de Engelstalige literatuur, te spreken van seksueel overdraagbare infecties (SOI) (Van der Bij, 2016). In deze richtlijn wordt gesproken van soa, omdat deze term in het algemeen taalgebruik gangbaar is en om zo verwarring te voorkomen. Waar in de richtlijn ‘patiënt’ wordt gebruikt, kan ook aan ‘cliënt’ gedacht worden.
In de huidige versie van deze richtlijn is ervoor gekozen de in Nederland meest voorkomende soagerelateerde syndromen in deel A te behandelen: urethritis, fluor vaginalis en vaginitis, epididymitis, pelvic inflammatory disease, balanitis, proctitis en genitale ulcera. In deel B worden de in Nederland meest voorkomende soa’s per specifieke verwekker behandeld: Chlamydia trachomatis (chlamydiainfectie inclusief lymphogranuloma venereum), Neisseria gonorhoeae (gonorroe), Treponema pallidum (syfilis), herpessimplexvirus (herpes genitalis), humaanpapillomavirus (condylomata acuminata), Sarcoptes scabiei (scabiës) en Mycoplasma genitalium. De behandeling van hepatitis B, hepatitis C en hiv is buiten beschouwing gelaten omdat hiervoor al uitgebreide richtlijnen voor de 2e lijn zijn beschreven door de desbetreffende wetenschappelijke verenigingen, respectievelijk de Nederlandse Vereniging van MaagDarmLeverartsen (NVMDL) en de Nederlandse Vereniging van HIV Behandelaren (NVHB). Omdat aanpalende specialisten patiënten met verhoogd risico op deze infecties wel zien, is het voor hen wel van belang deze te herkennen en te diagnosticeren voor verwijzing naar een aangewezen behandelaar. In deel C tot slot zijn 4 procedurele modules opgenomen omtrent het soaconsult, soa in relatie tot hiv, hepatitis C, AIN, PreP, PEP (bij MSM en hoogrisicogroepen), soascreening bij (een vermoeden op) seksueel misbruik bij kinderen en partnerwaarschuwing. Dit vanwege de relevantie in het kader van de soabestrijding in de 2e lijn. De richtlijn pretendeert niet compleet te zijn, maar geeft hopelijk een handvat voor de clinicuspracticus werkzaam in de 2e lijn voor het handelen in relatie de in Nederland meest voorkomende soa’s.
Risicogroepen
Soa’s worden veelal overgebracht door slijmvliesslijmvliescontact tussen 2 personen, maar de overdracht kan ook op een andere wijze tot stand komen. Het oplopen van een soa hangt in hoge mate af van iemands seksueel risicogedrag. Seks met meerdere partners is een bekende risicofactor, zeker als seksuele relaties elkaar in de tijd overlappen en er geen condoom wordt gebruikt. Seks voor geld of goederen, recreatief drugsgebruik en seks met partners die zijn ontmoet via internet (datingsites en chatboxen) zijn eveneens geassocieerd met een verhoogd risico op een soa. Bij een patiënt met een hulpvraag of klachten met betrekking tot een soa kan de (seksuele) anamnese uitsluitsel geven over het gelopen risico. Dit vereist dat de hulpverlener beschikt over gesprekstechnieken om op een heldere manier en zonder gêne over seks met de betrokkene te praten.
Risicogroepen voor het oplopen van een soa veranderen in de tijd. Zo werden tot de jaren zeventig van de vorige eeuw vaak zeelieden gezien op soapoliklinieken. Zeelieden hadden destijds een relatief groter risico op een soa door wisselende seksuele contacten tijdens het passagieren in havens als schepen werden gelost en geladen. Huidige risicogroepen zijn onder meer jongeren en jongvolwassenen die nog maar kort seksueel actief zijn. In deze levensfase zijn er vaker wisselende seksuele contacten en kan er sprake zijn van onervarenheid met veilige seks. Dit leidt ertoe dat in deze leeftijdsgroep relatief vaker urogenitale chlamydiainfecties worden aangetroffen. Mannen die seks hebben met mannen (MSM) vormen een andere groep waarbij op basis van epidemiologische gegevens vaker soa’s worden gediagnosticeerd.
Het begrip MSM vereist een nadere toelichting. Voor een goede inschatting van gelopen risico op een soa is niet zozeer iemands seksuele identiteit/genderidentiteit (o.m. homoseksueel, heteroseksueel georiënteerd) van belang. Een getrouwde, zich als monogaam heteroseksueel identificerende man kan buiten zijn vaste relatie ook seks hebben met mannen en vrouwen en daarmee een verhoogd risico lopen op een soa. Als hiernaar niet specifiek wordt gevraagd (‘Hebt u seks met mannen en/of met vrouwen?’), kan relevante informatie omtrent risicogedrag worden gemist. In dezelfde trant wordt er gesproken over mannen die seks hebben met vrouwen (MSV), vrouwen die seks hebben met mannen (VSM) en vrouwen die seks hebben met vrouwen (VSV).
Epidemiologische ontwikkelingen
Na een duidelijke daling van het aantal gerapporteerde soa’s in de jaren tachtig en het begin van de jaren negentig steeg het aantal soa’s in het begin van de 21e eeuw. Sindsdien is het aantal geregistreerde testen elk jaar toegenomen. Daarbij is het vindpercentage voor chlamydiainfecties in 1e lijn en soacentra de laatste jaren gestegen. Het aantal nieuwe hivdiagnoses onder MSM is de afgelopen jaren gedaald; de syfilis en gonorroeincidentie zijn echter toegenomen in deze risicogroep.
Bij het presenteren van epidemiologische cijfers is het van groot belang te vermelden op welke populatie deze betrekking hebben. De Nederlandse prevalentiecijfers in de literatuur hebben vaak betrekking op bezoekers van aan de GGD verbonden soapoliklinieken (recent op veel plaatsen omgedoopt tot centra seksuele gezondheid). Dit is per definitie een groep patiënten met een verhoogd risico op soa’s en de cijfers vormen dan ook geen representatieve afspiegeling van het voorkomen van soa’s in de gehele populatie. De cijfers van soapoliklinieken/centra seksuele gezondheid zijn in het bijzonder relevant omdat zij: 1) inzicht verschaffen in epidemiologische veranderingen in de tijd; en 2) veel patiënten uit de hoogrisicopopulaties zien.
Meldingsplicht
De volgende infecties die in deze richtlijn aan bod komen zijn meldingsplichtig: hepatitis B, acute hepatitis C en shigellose. De meldingsplicht is geregeld in de Wet publieke gezondheid (2008), artikel 21:
- De arts die bij een door hem onderzocht persoon een ziektebeeld vaststelt met een volgens de stand van de wetenschap onbekende oorzaak, waarbij een gegrond vermoeden bestaat van besmettelijkheid en ernstig gevaar voor de volksgezondheid, meldt dit onverwijld aan de gemeentelijke gezondheidsdienst.
- De arts die een voor zijn praktijk ongewoon aantal gevallen vaststelt van een infectieziekte, niet behorend tot groep A, B1, B2 of C, die een gevaar vormt voor de volksgezondheid, meldt dit binnen 24 uur aan de gemeentelijke gezondheidsdienst.
Zie voor meer informatie:
- http://wetten.overheid.nl/BWBR0024705/2016-08-01#HoofdstukV
- http://www.rivm.nl/Onderwerpen/W/Wet_publieke_gezondheid
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Wanneer bewust van de richtlijn wordt afgeweken, moet dit echter worden beargumenteerd en gedocumenteerd, en waar nodig in overleg met de patiënt worden gedaan.
Literatuur
- Van der Bij AK, de Vries HJC. Seksueel overdraagbare infecties. In: Hoepelman AIM, Kroes ACM, Sauerwein RW, Verbrugh HA. Microbiologie en infectieziekten. Vierde herziene druk. Bohn Stafleu Van Loghum, 2016.
- RIVM. Update thermometer seksuele gezondheid. Update november 2016. Rijksinstituut voor Volksgezondheid en Milieu, 2016. http://www.rivm.nl/Documenten_en_publicaties/Algemeen_Actueel/Brochures/Infectieziekten/Update_thermometer_seksuele_gezondheid.
