Deliver through-strategie versus wachten op volgende wee
Uitgangsvraag
Wat is de waarde van het wachten op de volgende wee in vergelijking met de 'deliverthrough-strategie' ter verbetering van de uitkomsten bij schouderdystocie?
Aanbeveling
Wacht na de geboorte van het hoofd op de volgende wee, als de situatie het toelaat, , zodat de schouder voldoende tijd heeft om te roteren tijdens de baring, om een mogelijke schouderdystocie en neonatale complicaties te voorkomen.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De systematische literatuuranalyse laat zien dat het wachten op een volgende wee positieve effecten lijkt te hebben op het reduceren van claviculafracturen, neonatale plexusbrachialuslaesie en schouderdystocie, in vergelijking met de deliver through-strategie. De overall bewijskracht van de literatuur werd gegradeerd als laag tot zeer laag. Dit heeft te maken met imprecisie van de bevindingen, en risico op bias vanwege het observationele onderzoeksdesign. De meta-analyses laten zien dat wanneer er wordt gewacht op de volgende wee er significant minder kinderen zijn met claviculafracturen (0,06% versus 0,3%) en plexusbrachialuslaesie (0% versus 0,09%). Er zijn geen studies gevonden die maternale uitkomsten hebben meegenomen.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Het verdient de voorkeur om bij een normale uitdrijving na de geboorte van het hoofd te wachten op een volgende wee, gezien de mogelijke voordelen voor het kind en afwezigheid van nadelen voor de moeder.
Kosten (middelenbeslag)
Voor beide ingrepen zijn geen extra middelen nodig. De werkgroep voorziet geen verschuiving in kosten wanneer één van beide strategieën wordt aangehouden.
Aanvaardbaarheid, haalbaarheid en implementatie
Er zijn aanwijzingen gevonden dat het wachten op een volgende wee positieve effecten heeft voor de neonatale uitkomsten. De werkgroep voorziet geen barrières ten aanzien van de aanvaardbaarheid, haalbaarheid en implementatie.
Rationale van de aanbeveling.
Het wachten op een volgende wee leidt voor zover bekend niet tot slechtere neonatale uitkomsten als de volgende wee op zich laat wachten. In de studie van Zhang (2017) komt naar voren dat een head-to-shoulder-interval langer kan duren dan 60 seconden. In 96,7% duurde het head-to-shoulder-interval maximaal 150 seconden; slechts bij 3,3% duurde dit interval langer dan 150 seconden. Indien gewacht wordt op de volgende wee in vergelijking met de deliver through-strategie voorkomt dit mogelijk een schouderdystocie, clavicula fractuur of plexusbrachialuslaesie
Onderbouwing
Van een schouderdystocie wordt gesproken als de zorgprofessional tijdens de uitdrijving van een kind in hoofdligging extra handgrepen moet toepassen om de schouders van het kind geboren te laten worden. Schouderdystocie ontstaat als de voorste, of zeldzamer, de achterste schouder van het kind haakt respectievelijk op de maternale symfyse of het sacrale promontorium en het vast komt te zitten. Er wordt grote variatie gerapporteerd in incidentie van schouderdystocie. Wanneer een schouderdystocie optreedt wordt er een verhoogde maternale/neonatale morbiditeit en mortaliteit gezien, ook al wordt deze tijdig en technisch correct opgelost. Voorbeelden van maternale morbiditeit zijn fluxus post partum en derde- en vierdegraadsperineumrupturen (OASIS: Obstetric Anal Sphincter Injuries). Een plexusbrachialuslaesie bij het kind is de meest belangrijke foetale complicatie. Schouderdystocie is slecht voorspelbaar.
Twee mogelijke bevallingsstrategieën bij schouderdystociepreventie zijn: 1) wachten op ten minste één volgende wee (hands off) en de schouder voldoende tijd geven om te roteren tijdens de baring nadat het hoofd is geboren; of 2) zodra het hoofd is geboren, wordt sacraalwaarts druk uitgeoefend op het foetale hoofd totdat de voorste schouder bij het ostium vaginae verschijnt. Er zijn aanwijzingen dat het wachten op een volgende wee tijdens een normale bevalling mogelijk positieve effecten heeft op de neonatale uitkomsten. Het achterliggende mechanisme is dat indien gewacht wordt op de volgende wee de schouders meer tijd hebben om te roteren en vervolgens in te dalen. Indien niet gewacht wordt kan het zijn dat de schouders niet geroteerd zijn en de voorste schouder tegen de symfyse wordt getrokken. In deze module zullen beide strategieënmet elkaar worden vergeleken om te bepalen welke strategie het meest bijdraagt aan gunstige uitkomsten bij een schouderdystocie.
|
Very low GRADE |
Waiting for the next contraction may reduce the rate of shoulder dystocia compared to the deliver through strategy but the evidence is very uncertain.
Sources: (Zhang, 2017) |
|
Low GRADE |
Waiting for the next contraction may reduce clavicular fractures in newborns compared to the deliver through strategy.
Sources: (Li, 2014; Li and Zang, 2016; Wang, 2013) |
|
Low GRADE |
Waiting for the next contraction may reduce neonatal brachial plexus injuries compared to the deliver through strategy.
Sources: (Li, 2014; Li and Zang, 2016; Wang, 2013) |
|
Very low GRADE |
Waiting for the next contraction may result in little to no effect on the number of children with a one- and five-minute apgarscore < 7 compared with the deliver through strategy but the evidence is very uncertain.
Sources: (Zhang, 2018) |
Description of studies
De systematic review of Huang (2018) is used for the syntheses of the literature. Huang (2018) assessed the effects of two usual methods of delivery for shoulder presentation, 1-step and 2-step. In the 1-step deliver through-strategy, as soon as the head is delivered, downward pressure is applied on the fetal head until the anterior shoulder appears at the introitus. The 2-step method is to wait for at least another contraction, not to push or pull, instead, allowing the shoulder enough time to rotate in all vaginal deliveries after the head is delivered. Studies that met all the following criteria were included: 1) studies that had clear criteria for inclusion and exclusion of participants; 2) controlled studies that adopted 2 methods of shoulder delivery: 1-step and 2-step method; 3) studies reporting any or all of the 3 outcomes: (i) primary outcome was the incidence of neonatal asphyxia; (ii) secondary outcomes included rates of neonatal brachial plexus injury and clavicular fracture of newborns; 4) studies published either in English or Chinese language. Huang (2018) identified 1959 articles, excluded 473 as these were duplicate articles and 1317 were excluded based on a review of the title and abstract. Two authors reviewed the full text of the remaining 169 articles. Finally, seven studies met the inclusion criteria and were included for the meta-analysis (Cui, 2015; Huang, 2014; Huang, 2015; Li, 2014; Li en Zang, 2016; Wang, 2013; Qi, 2016). The total number of participants in the 7 studies was 14 627. All women had successful vaginal deliveries (no caesarean section): in 7415 women the 1-step (deliver through) method was used, and in 7212 women the 2-step method (waiting until next contraction) of shoulder delivery was used. The following outcome measures were included: clavicular fracture (fracture of the clavicular bone immediately after birth, usually defined as presenting within 24 hours after birth) and brachial plexus injury.
In addition, the study of Zhang (2017) was included. The study of Zhang (2017) was published after the search date of Huang (2018). Zhang (2017) described a randomized control trial and compared the two-step method of shoulder delivery (n=359) with the one-step method (n=252). Zhang (2017) included women scheduled for vaginal delivery without severe complications. These women were randomly assigned into two groups. Women in the study group were delivered by the two-step method for shoulder delivery, to promote the natural delivery of shoulder. Women in the control group were delivered by the one-step method (deliver through). The following outcome measures were included: rate of shoulder dystocia (diagnoses by doctors in clinical setting when additional maneuvers were applied to deliver the shoulder), and 5-minute apgarscore.
Results
Shoulder dystocia
The study of Zhang (2017) investigated the rate of shoulder dystocia in women scheduled for vaginal delivery, without severe complications, in the two-step (waiting for next contraction) group (rate 0/364) and the one-step group (deliver through) (rate 4/257). Zhang (2017) performed a non-parametric test and reported that the rate of shoulder dystocia in the two-step group (waiting for the next contraction) was significantly lower than in the on-step group (deliver through) (x2= 4.27; p=0.03).
Level of evidence of the literature
The level of evidence regarding the outcome shoulder dystocia was downgraded by three levels because of study limitations (risk of bias) and imprecision as reflected by the wide 95% confidence intervals (small sample size, one single study). The level of evidence was very low GRADE.
Clavicular fractures
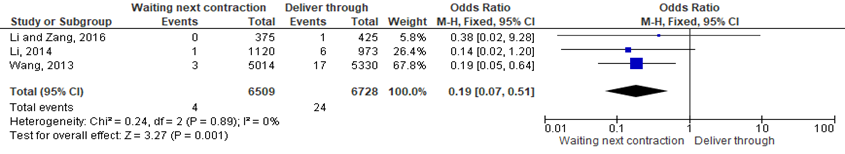
Three articles reported the rates of clavicular fracture of newborns (Li, 2014; Li and Zang, 2016; Wang, 2013). Four newborns in the 2-step group (n=6509) and 24 in the 1-step group (n=6728) had a clavicular fracture. There was no statistical heterogeneity among the studies (p=0.89, I2=0%). Analysis using the fixed effect model showed significant differences between the groups with clavicular fracture being higher in the 1-step deliver through group (RR=0.19; 95%CI= (0.07; 0.51); p=0.001; Figure 1).
Figure 1 Forest plot with meta-analysis for the difference in clavicular fracture in newborns between the waiting for next contraction group and deliver through
Level of evidence of the literature
The level of evidence regarding the outcome clavicular fracture of newborns was downgraded by two levels because of study limitations (risk of bias) and not meeting the optimal information size as reflected by the wide 95% confidence intervals (imprecision). The level of evidence was Low GRADE.
Brachial plexus injury
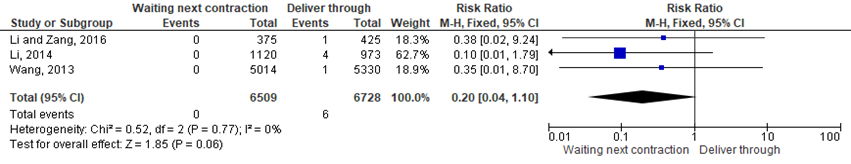
Neonatal brachial plexus injury was also reported in three articles. No event occurred in the 2-step group (n=6509) but 6 events occurred in the 1-step (n=6728) group. There was no statistical heterogeneity among the studies (p=0.77, I2=0%). The fixed effect model showed that the difference in neonatal brachial plexus injury rate between the groups was not statistically significant (RR=0.20; 95%CI= (0.04; 1.10); p=0.06; Figure 2).
Figure 2 Forest plot with meta-analysis for the difference in clavicular fracture in newborns between the waiting for next contraction group and deliver through
Level of evidence of the literature
The level of evidence regarding the outcome neonatal brachial plexus injury was downgraded because of study limitations (risk of bias) and not meeting the optimal information size as reflected by the wide 95% confidence intervals (imprecision). The level of evidence was Low GRADE.
One-minute infant apgarscore
The study of Zhang (2017) investigated the number of children with an apgarscore < 7 at one minute in women scheduled for vaginal delivery, without severe complications, in the two-step (waiting for next contraction) group and the one-step group (deliver through). Zhang (2017) reported that 5/364 children in the two-step group (waiting for next contraction) had a one-minute apgarscore < 7, and that 5/257 children had a one-minute apgarscore < 7 in the one-step group (deliver through); no difference between groups; X2=0.310; p=0.577.
Level of evidence of the literature
The level of evidence regarding the outcome measure one-minute apgarscore was downgraded because of risk of bias (blinding was not possible) and imprecision (number of included patients, single study). The level of evidence was low GRADE.
Five-minute infant apgarscore
The study of Zhang (2017) investigated the number of children with an apgarscore < 7 at five minutes in women scheduled for vaginal delivery, without severe complications, in the two-step (waiting for next contraction) group and the one-step group (deliver through). Zhang (2017) reported that 0/364 children in the two-step group (waiting for next contraction) had a five-minute apgarscore < 7, and that 0/257 children had a one-minute apgarscore < 7 in the one-step group (deliver through); no difference between groups (no statistics performed).
Level of evidence of the literature
The level of evidence regarding the outcome measure one-minute apgarscore was downgraded because of risk of bias (blinding was not possible) and imprecision (number of included patients, single study). The level of evidence was very low GRADE.
Other outcomes
No studies were included that reported on the outcome measures offspring mortality, early neurodevelopmental morbidity, cord blood, birth trauma, NICU admission, disability in childhood, Longer-term maternal outcomes (at three months), blood transfusion, thromboembolism, urinary retention requiring bladder catheter > 24hours longer as local protocol prescribes, OASIS (Obstetric Anal Sphincter Injuries), breastfeeding failure, perineal pain; any pain; dyspareunia, urinary incontinence, flatus incontinence, or fecal incontinence.
A systematic review of the literature was performed to answer the following research questions:
PICO
What are the benefits and harms of the deliver through strategy versus expectant management (waiting for the next contraction) in women giving birth to prevent shoulder dystocia?
P: patients women giving birth;
I: intervention deliver through strategy;
C: control expectant management (waiting for the next contraction);
O: outcome neonatal outcomes: brachial plexus injury, shoulder dystocia, neonatal mortality, early neurodevelopmental morbidity, apgarscore, pH in cord blood, birth trauma, NICU admission, death, disability in childhood.
maternal outcomes: harm to mother from intervention, maternal mortality, longer-term maternal outcomes (at three months), emergency caesarean section, postpartum hemorrhage (TBL>1000ml), blood transfusion, thromboembolism, urinary retention requiring bladder catheter > 24 hours or longer as local protocol prescribes, OASIS (Obstetric Anal Sphincter Injuries), breastfeeding failure, perineal pain, any pain, dyspareunia, urinary incontinence, flatus incontinence, fecal incontinence.
Relevant outcome measures
The guideline development group considered offspring and maternal mortality, shoulder dystocia, brachial plexus injury as critical outcome measures for decision making; and disability in childhood, neurodevelopmental morbidity, Apgar-score, NICU admissions as an important neonatal outcome for decision making.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 2019-07-19. The literature search was updated at 2020-11-30. The detailed search strategy is depicted under the tab Methods. The systematic literature search (combined search PICO 1 and PICO 2) resulted in 27 hits. Studies were selected based on the following criteria, systematic review, RCTs, and cohort studies meeting the PICO criteria, published > 1990. 3 studies were initially selected based on title and abstract screening. After reading the full text, 1 study was excluded (see the table with reasons for exclusion under the tab Methods), and two studies included. Study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Cui FY, Zhao L, Ma SZ. Clinical analysis on improving measurements of natural delivery. Shanxi Med J 2015;44:1136-9.
- Huang JH. Effects of improved natural delivery mode on the delivery outcome of primipara. J Qilu Nurs 2014;20:11-13.
- Huang LM. Effect analysis on improving maternal delivery quality by mid-wifery care. J Med Theory Pract 2015;28:1110-12.
- Huang H, Yang M, Zhou H, Lin C, Li X, Zhang H. Method of shoulder delivery and neonatal outcomes: A meta-analysis of prospective controlled studies. Natl Med J India. 2018 Nov-Dec;31(6):324-328. doi: 10.4103/0970-258X.262897. PubMed PMID:31397362.
- Iffy L, Varadi V, Papp Z. Epidemiologic aspects of shoulder dystocia-related neurological birth injuries. Arch Gynecol Obstet. 2015 Apr;291(4):769-77. doi:10.1007/s00404-014-3453-8. Epub 2014 Sep 11. PubMed PMID: 25209350.
- Kotaska A, Campbell K. Two-step delivery may avoid shoulder dystocia: head-to-body delivery interval is less important than we think. J Obstet Gynaecol Can. 2014 Aug;36(8):716-720. doi: 10.1016/S1701-2163(15)30514-4. PubMed PMID: 25222167.
- Li Y, Tan CJ, Liu XL, Jin P, Qin LZ, Yan R. Observation of effects of late shoulder delivery in preventing newborn birth injury. J Nurs Sci 2014;29:39-40.
- Li L, Zhang LP. Effects of natural delivery (waiting at least one contraction) on newborn and maternal birth injury. Shanxi Med J 2016;45:443-5.
- Qi ZY, Zhang DR, Dang CL, Huo LM. Clinical research on effects of delivery outcome by delivery position and natural shoulder delivery. Hebei Med J 2016;38: 1215-19.
- Wang CH, Zhang HY, Hong LH, Cao YH. Observation of effects of natural shoulder delivery (waiting at least one contraction) on preventing shoulder dystocia and newborn birth injury. China Medical Herald 2013;10:150-2.
- Zhang H, Zhao N, Lu Y, Chen M, Guo Z, Ling Y. Two-step shoulder delivery method reduces the incidence of shoulder dystocia. Clin Exp Obstet Gynecol. 2017;44(3):347-352. PubMed PMID: 29949271.
Research question: What is the effect of calcium prophylaxis in pregnant women to prevent pre-eclampsia and preterm birth?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Huang, 2017
|
SR and meta-analysis of RCTs Literature search up to September 31 Oktober 2016 A: Wang, 2013 B: Huang, 2014 C: Li, 2014 D: Huang, 2015 E: Cui, 2015 F: Li and Zhang, 2016 G: Qi, 2016
|
Inclusion criteria SR: 1. Studies that had clear criteria for inclusion and exclusion of participants 2. Controlled studies that adopted 2 methods of shoulder delivery: 1-step and 2-step method. 3. Studies reporting any or all of the 3 outcomes were included: (i) primary outcome was the incidence of neonatal asphyxia; (ii) secondary outcomes included rates of neonatal brachial plexus injury and clavicular fracture of newborns. Neonatal asphyxia is a medical condition resulting from deprivation of oxygen to a newborn infant for longer than 1 minute. Neonatal brachial plexus injury is an injury to the brachial plexus, the network of nerves that conducts signals from the spinal cord to the shoulder, arm and hand. Clavicular fracture of newborns is fracture of the clavicular bone immediately after birth (usually defined as within 24 hours after birth). 4. Studies published either in English or Chinese language.
Exclusion criteria SR: 1. Not a prospective controlled study of 1-step and 2-step methods 2. Studies that did not report the outcomes that we were assessing 3. Studies that had errors or unreliable data 4. Duplicate published articles. type of intervention. Important patient characteristics at baseline: A: 822 women randomised. Women with singleton fetus with cephalic presentation and no contraindications to vaginal delivery. Women were screened between 36-38 weeks' gestation and those with a fetus with an estimated weight above the 95th percentile at 37 to 38 weeks of gestation, confirmed clinically and then by sonography were included. B: 273 women with clinical or previous ultrasound suspicion of macrosomia, or with past history of macrosomia, underwent an ultrasound examination. Women were eligible if ultrasound estimated fetal weight, performed at 38 completed weeks or more, was between 4000 g and 4500 g. Women with diabetes, non-cephalic presentation, previous caesarean section, or indication for labour induction other than macrosomia were excluded. C: 40 women at 37 to 42 weeks, with an ultrasound estimated fetal weight between 4000 g and 4750 g.
D: Women 18-45 years age with large for gestational age or suspected macrosomic babies 38 to 40 + 3 weeks' gestation with singleton pregnancy, cephalic presentation with estimated fetal weight 3800 to 4500 g. Women with diabetes, major fetal malformation or previous caesarean birth excluded. Proposed sample: 474 women. |
A-G: 2-step method |
A-G: Deliver through method
|
Endpoint follow-up: A-G: follow up until delivery participants were no complete outcome data available: risk attrition/amount attrition? Not reported
|
Outcome measure-1 Neonatal fracture of clavicle F: RR= 0.38 (0.02– 9.28) C: RR= 0.14 (0.02- 1.20) B: RR= 0.19 (0.05- 0.64) Total: 0.19 (0.07 - 0.51) Outcome measure-2 Brachial plexus injury F: RR= 0.38 (0.02– 9.28) C: RR= 0.10 (0.01- 1.79) B: RR= 0.35 (0.01- 8.74) Total: RR= 0.20 (0.04 – 1.10) Outcome measure-3 One-minute infant Apgar score 5/257 children had a one-minute Apgar score<7 in the one-step group (deliver through); no difference between groups; X2=0.310; p=0.577. Outcome measure-4 Five-minute infant Apgar score 0/257 children had a one-minute Apgar score<7 in the one-step group (deliver through); no difference between groups (no statistics performed).
|
Facultative: Current evidence supports the use of 2-step method of shoulder delivery with no major adverse neonatal outcomes, lower incidence of neonatal asphyxia rate, and neonatal clavicular fracture rate than delivery by the 1-step method. The clinical value is high for the adoption of 2-step method for better neonatal outcomes. |
Table of quality assessment
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Huang, 2018 |
Yes |
Yes |
Yes |
Yes (only description of individual calcium regimes is missing) |
Not applicable |
Yes |
Yes |
Yes |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Zhang, 2018 |
Wrong intervention |
|
Hishikawa, 2020 |
Does not met the PICO-criteria: no comparison |
Beoordelingsdatum en geldigheid
Publicatiedatum : 10-10-2022
Beoordeeld op geldigheid :
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Wachten op de volgende wee bij schouderdystocie |
NVOG |
2020 |
2025 |
Elke 5 jaar |
NVOG |
Nieuwe literatuur |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Deze richtlijn is ontwikkeld in samenwerking met:
- Koninklijke Nederlandse Organisatie van Verloskundigen
- Patiëntenfederatie Nederland
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2019 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor zwangere vrouwen met een kind met een dreigende schouderdystocie.
Werkgroep
- Dr. C.J. (Caroline) Bax, gynaecoloog-perinatoloog, werkzaam in het Amsterdam UMC locatie AMC, NVOG, (voorzitter, vanaf januari 2020)
- Dr. A.C.C. (Annemiek) Evers, gynaecoloog, werkzaam in het Universitair Medisch Centrum Utrecht, NVOG (voorzitter, tot december 2019)
- Drs. A. (Ayten) Elvan-Taspinar, gynaecoloog, werkzaam in het Universitair Medisch Centrum Groningen, Groningen, NVOG
- Dr. F. (Frédérique) van Dunné, gynaecoloog, werkzaam in het Medisch Centrum Haaglanden, Den Haag, NVOG
- Drs. A.J.M. (Anjoke) Huisjes, gynaecoloog-perinatoloog, werkzaam in de Gelre ziekenhuizen, Apeldoorn en omgeving, NVOG
- Dr. H.J.H.M. (Thierry) van Dessel, gynaecoloog, werkzaam in het Elisabeth- TweeSteden Ziekenhuis, Tilburg, NVOG
- J. (Julia) Bloeming, eerstelijns verloskundige , werkzaam in Verloskundigepraktijk Vechtdal in Hardenberg, KNOV
- MSc J.C. (Anne) Mooij, adviseur, Patientenfederatie Nederland
- Dr. S.V. (Steven) Koenen, gynaecoloog, werkzaam in het ETZ, locatie Elisabeth Ziekenhuis, NVOG, lid stuurgroep
- Dr. Duvekot, gynaecoloog, werkzaam in het Erasmus MC, NVOG, lid stuurgroep
Meelezer
- Leden van de Otterlo- werkgroep (2019)
Met ondersteuning van
- Dr. W.J. (Wouter) Harmsen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. L. (Laura) Viester, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Evers* |
Gynaecoloog, UMCU |
"Lid van Ciekwal, voorzitter 50 geboortemodules NVOG Werkgroep multidisciplinaire richtlijn extreme vroeggeboorte, NVOG" |
Geen |
Geen actie. |
|
Elvan-Taspinar
|
Gynaecoloog UMCG, Groningen |
Geen |
Geen |
Geen actie. |
|
van Dunné
|
Gynaecoloog Medisch Centrum Haaglanden, Den Haag |
Geen |
Geen |
Geen actie. |
|
Huisjes
|
Gynaecoloog Gelre Ziekenhuizen |
"Onderwijs coördinator Gelre ziekenhuizen (betaald) Voorzitter Stichting M.O.E.T. (onbetaald) Lid DB Stichting A.L.S.G. (onbetaald) Expertise-werkzaamheden (betaald) Klachtencommissie Gelre ziekenhuizen (betaald) Docent Opleiding tot Klinisch Verloskundige (Universiteit Utrecht) (betaald)" |
Geen |
Geen actie. |
|
Van Dessel
|
Gynaecoloog, Elisabeth- TweeSteden Ziekenhuis, Tilburg
|
Geen |
Geen |
Geen actie. |
|
Bloeming |
"Klinisch verloskundige praktijk Vechtdal in Hardenberg |
Geen |
Geen |
Geen actie. |
|
Mooij |
Adviseur Patientenbelang, Patientenfederatie Nederland |
Niet van toepassing |
Geen |
Geen actie. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van patiëntvertegenwoordigers van verschillende patiëntverenigingen voor de Invitational conference en afvaardiging van patiëntenverenigingen in de clusterwerkgroep. Het verslag hiervan is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie per module ook ‘Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)’. De conceptrichtlijn wordt tevens ter commentaar voorgelegd aan de betrokken patiëntenverenigingen (Vereniging van Ouders van Couveusekinderen (VOC) en Stichting Kind en Ziekenhuis).
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten rondom de zorg voor zwangere vrouwen met een kind met een dreigende schouderdystocie. Tevens zijn er knelpunten aangedragen door patiëntenverenigingen tijdens de Invitational conference. Een verslag hiervan is opgenomen in de bijlagen.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1946 – september 2019
|
1 (shoulder adj3 dystocia*).ti,ab,kw. or exp Brachial Plexus Neuropathies/ or (obstetric* adj3 brachial plexus).ti,ab,kw. or obpp.ti,ab,kw. or exp Asphyxia/ or asphyxia.ti,ab,kw. (20201) 2 (two step or restitut* or 2 step).ti,ab,kw. (39975) 3 1 and 2 (27) 4 limit 3 to english language (20)
= 20 |
27 |
|
Embase (Elsevier) |
('shoulder dystocia'/exp OR ((shoulder NEAR/3 dystocia*):ti,ab) OR 'obstetrical brachial plexus palsy'/exp OR ((obstetric* NEAR/3 'brachial plexus'):ti,ab) OR obpp:ti,ab OR 'brachial plexus neuropathy'/exp OR 'asphyxia'/exp OR asphyxia:ti,ab) AND ('two step':ti,ab OR restitut*:ti,ab OR '2 step':ti,ab) AND ((english)/lim OR (dutch)/lim) NOT 'conference abstract':it
= 23 |
