Wisseling levothyroxine preparaten
Uitgangsvraag
Is het verantwoord om te wisselen van levothyroxine preparaat (merk of samenstelling) zonder medische noodzaak?
Aanbeveling
Vermijd het wisselen van levothyroxine preparaten zonder medische noodzaak. Indien wisseling noodzakelijk is (in verband met beschikbaarheid) en er klachten ontstaan, dan is het raadzaam om het TSH tenminste 6 weken na dato te laten controleren.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De bewijskracht voor de geïncludeerde studie van Vaisman (2001) is zeer laag. Tevens betreft dit een studie in slechts 25 patiënten, en betreft het slechts de vergelijking van twee preparaten, waardoor we geen aanbeveling kunnen geven gebaseerd op deze studie. Na het uitvoeren van de zoekstrategie is een Nederlandse studie gepubliceerd over de associatie tussen wisseling van preparaten en plasma TSH-concentraties (Flinterman, 2019). Deze studie bestond uit twee groepen: patiënten die gedurende de studie alleen Thyrax hebben ontvangen en patiënten die gewisseld zijn naar een ander merk van levothyroxine (Euthyrox of levothyroxine Teva). TSH werd opnieuw gemeten met een interval van tenminste 6 weken. In de groep zonder wisseling van merk en met een dosering ≤ 100 µg per dag had 19% een afwijkende tweede TSH-meting en dit was 24% bij patiënten die gewisseld waren (p<0,0001). Bij een hogere Thyrax dosis (>100µg) was dit 24% en 64% voor de groep zonder en met wisseling, respectievelijk. Verder was de kans op biochemische tekenen van overdosering (verlaagd TSH) in de groep met wisseling naar een ander merk bij de tweede meting 5x zo hoog als in de groep zonder wisseling.
Waarden en voorkeuren van patiënten
De ervaring van de werkgroep en patiëntvertegenwoordigers is dat patiënten hebben over het algemeen een grote voorkeur om niet te hoeven wisselen van levothyroxine preparaat.
Kosten
Indien na een switch naar een ander preparaat klachten optreden, of de biochemische instelling niet meer optimaal is, zullen extra kosten noodzakelijk zijn voor labbepalingen en spreekuurbezoek dan wel telefonische consulten.
Aanvaardbaarheid, haalbaarheid en implementatie
Het is duidelijk dat als een gegeven levothyroxine preparaat niet leverbaar is, er geen andere keus is dan omzetten naar een ander middel.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Er is geen harde aanbeveling te geven op basis van de beschikbare literatuur. Wel is er een standpunt geformuleerd vanuit de European Thyroid Association (ETA, 2018) in samenwerking met de overkoepelende internationale schildklierpatiënten vereniging (TFI), waarin wisselen zonder noodzaak werd ontraden. Ook de Amerikaanse Thyroid Association (ATA, 2003) raadt wisselen zonder noodzaak af. Wanneer er onverhoopt toch gewisseld moet worden, wordt in beide position papers geadviseerd om extra controles van TSH uit te voeren na 6 weken. Bij opmerkelijke reacties dient het TSH eerder gecontroleerd te worden. De recente studie van Flinterman (2019) geeft weer dat wisseling van levothyroxine merk kan leiden tot een groter percentage afwijkende TSH-waarden ten opzichte van de normale variatie in TSH bij levothyroxine gebruik. Daarom lijkt het vermijden van wisseling van levothyroxine preparaten het meest veilig, en dit heeft ook de voorkeur voor patiënten.
Onderbouwing
In Europa was de afgelopen jaren een groot aantal patiënten met behandelde hypothyreoïdie genoodzaakt om te wisselen van levothyroxinepreparaat. Dit kwam deels doordat het preparaat tijdelijk niet leverbaar was bij een fabrikant. Een andere oorzaak was dat een fabrikant de samenstelling van een bestaand preparaat wijzigde. Dit leidde vaak tot ongerustheid bij de patiënten, en ging samen met een forse toename van het aantal gemelde bijwerkingen en met extra zorgconsumptie (Casassus, 2018). De European Thyroid Association (ETA) publiceerde naar aanleiding hiervan een position statement, mede namens de overkoepelende patiëntorganisatie TFI, waarin wisselen zonder noodzaak wordt ontraden (Fliers, 2018). Het is echter de vraag of de wisseling van preparaten resulteert in veranderingen in bloedwaarden en bijwerkingen en wat het advies moet zijn van de zorgprofessionals aan patiënten die van levothyroxine preparaat wisselen.
Farmacologische parameters (T4 en TSH)
|
Zeer laag GRADE |
Het effect van de wisseling van levothyroxine preparaat op de farmacologische parameters is onzeker.
Bronnen: (Vaisman, 2001) |
Bijwerkingen
|
- GRADE |
Er zijn geen studies beschikbaar over wisseling van preparaten en het ontstaan van bijwerkingen. |
Onder/over dosering
|
- GRADE |
Er zijn geen studies beschikbaar over wisseling van preparaten en onder- en overdosering. |
Kwaliteit van leven
|
- GRADE |
Er zijn geen studies beschikbaar over wisseling van preparaten en kwaliteit van leven. |
Beschrijving studies
De cross-over studie van Vaisman (2001) vergeleek de bio-equivalentie van 100 µg levothyroxine van Puran T4® (interventie) met een Braziliaans referentieproduct (referentie) met dezelfde dosering. Er werden 25 patiënten geïncludeerd die reeds succesvol werden behandeld voor primaire hypothyreoïdie met een van bovengenoemde middelen (n=25; 92% vrouw; gemiddelde leeftijd = 53 jaar (range 36 tot 64)). Na inclusie werden patiënten gerandomiseerd naar twee groepen: (1) 42 dagen de interventie, gevolgd door 42 dagen referentie (n = 12) en (2) vice versa. Er was geen wash-out periode. Bloedmonsters werden afgenomen vóór en 1, 2, 3, 4, 6, 8 en 24 uur na het innemen van het laatste tablet (referentie of interventie) met 150 ml kraanwater (zie evidencetabel voor het gehele protocol). Er werd in het artikel niets gerapporteerd over randomisatie en blindering. De uitkomstmaten T4- en TSH-waarden werden gerapporteerd.
Resultaten
Farmacologische parameters (T4 en TSH)
De totale serum levothyroxine concentraties tijdens de verschillende meetmomenten is weergegeven in onderstaande grafiek (overgenomen uit Vaisman, 2001). Na 42 dagen was TSH 1,91 µIU/ml in de groep interventiegroep en 1,06 µIU/ml in de referentiegroep (p<0,01) (Vaisman, 2001).
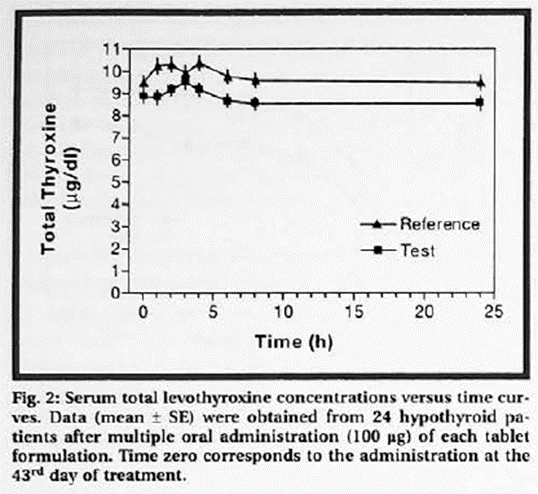
Bijwerkingen
Er zijn geen studies beschikbaar over wisseling van preparaten en het ontstaan van bijwerkingen.
Onder-/overdosering
Er zijn geen studies beschikbaar over wisseling van preparaten en onder- of overdosering.
Kwaliteit van leven
Er zijn geen studies beschikbaar over wisseling van preparaten en kwaliteit van leven.
Bewijskracht van de literatuur
De bewijskracht voor RCT’s begint hoog. De bewijskracht voor de uitkomstmaat farmacologische parameters is met drie niveaus verlaagd tot zeer laag gezien risico op bias (beperkingen in de onderzoeksopzet: geen beschrijving van randomisatie, blindering onduidelijk) en het geringe aantal patiënten (imprecisie).
Er zijn geen studies van voldoende kwaliteit die de overige door de werkgroep geformuleerde uitkomstmaten (bijwerkingen, klachten) hebben onderzocht.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag (vragen):
Wat zijn de (on)gunstige effecten van wisseling van levothyroxine preparaat (merk of samenstelling) in dezelfde dosering bij patiënten met behandelde hypothyreoïdie?
P (Patiënten): volwassen patiënten met primaire hypothyreoïdie;
I (Interventie): wisseling van levothyroxinepreparaat X (in merk of samenstelling; dezelfde dosering als de controle);
C (Controle): naar levothyroxinepreparaat Y (in merk of samenstelling; dezelfde dosering als de interventie) of geen wisseling;
O (Outcome): farmacologische parameters (T4- en TSH-waarden), bijwerkingen, onder-/over dosering, kwaliteit van leven.
Relevante uitkomstmaten
De werkgroep achtte rondom de wisseling van levothyroxine preparaat beschreven farmacologische parameters (T4- en TSH-waarden), bijwerkingen, klachten, kwaliteit van leven en onder- dan wel overdosering, voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde de genoemde uitkomstmaten niet a priori volgens eigen criteria, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 19 augustus 2018 met relevante zoektermen gezocht naar alle typen studies over de (on)gunstige effecten van de wisseling van levothyroxinepreparaat bij patiënten met primaire hypothyreoïdie. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 319 treffers op. Vergelijkende studies over volwassen patiënten met primaire hypothyreoïdie die wisselen van het ene levothyroxinepreparaat naar een ander levothyroxinepreparaat (in merk of samenstelling, maar met dezelfde dosering) werden geïncludeerd. Studies waarin verschillende toedieningsvormen met elkaar werden vergeleken (bijvoorbeeld tablet versus drank) werden geëxcludeerd.
Op basis van titel en abstract werden in eerste instantie 33 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 32 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 1 studie definitief geselecteerd (Vaisman, 2001).
Resultaten
Eén studie is opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- 1 - Casassus, B. (2018). Risks of reformulation: French patients complain after Merck modifies levothyroxine pills. BMJ: British Medical Journal (Online), 360.
- 2 - Fliers, E., Demeneix, B., Bhaseen, A., & Brix, T. H. (2018). European thyroid association (ETA) and thyroid federation international (TFI) joint position statement on the interchangeability of levothyroxine products in EU countries. European thyroid journal, 7(5), 238-242.
- 3 - Flinterman LE, Kuiper JG, Korevaar JC, Van Dijk L, Hek K, Houben E, Herings R, Franken A, Graaf JP, Horikx A, Janssens M, Meijer R, Wijbenga A, Van Puijenbroek E, Wolffenbuttel BH, Links TP, Bisschop PH, Fliers E. Impact of a forced dose-equivalent levothyroxine brand switch on plasma TSH; a cohort study. Thyroid, in press.
- 4 - Vaisman, M., Spina, L.D., Eksterman, L.F., dos Santos, M.J., Lima, J.S., Volpato, N.M., da Silva, R.L., de Brito, A.P., & Noël, F. (2001). Comparative bioavailability of two oral L-thyroxine formulations after multiple dose administration in patients with hypothyroidism and its relation with therapeutic endpoints and dissolution profiles. Arzneimittelforschung, 51(3), 246-52.
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Control (C) |
Follow-up |
Outcome measures and effect size |
|
Vaisman (2001) |
Type of study: Open label crossover study Setting and country: Outpatient clinic population treated at the endocrinology service, Brasilia Funding and conflicts of interest: |
Inclusion criteria: Outpatient clinic population treated at the endocrinology service. Once they were considered successfully treated for primary hypothyroidism, for at least six months, with one of the two 100µg oral levothyroxine formulations, as assessed by LT4 and TSH levels within the normal range and clinical endpoints. Exclusion criteria:
N total at baseline: 25 patients (two groups of twelve)
Important prognostic factors2: Sex Groups comparable at baseline? |
Describe intervention (treatment/procedure/test):
|
Describe control (treatment/procedure/test):
(see intervention) |
Length of follow-up: 86 days (two times 42 days)
Loss-to-follow-up: Intervention / control: N = 1 (2%) Reasons (describe):
Not described.
|
Outcome measures and effect size (include 95%CI and p-value if available):
Cavg (µg/dl) 9.60 Test Total TSH Reference
* (ANOVA (performed on log transformed values) |
Risk of bias tabel: gerandomiseeerd onderzoek
|
Study reference
|
Describe method of randomisation |
Bias due to inadequate concealment of allocation?
|
Bias due to inadequate blinding of participants to treatment allocation? |
Bias due to inadequate blinding of care providers to treatment allocation?) |
Bias due to inadequate blinding of outcome assessors to treatment allocation? |
Bias due to selective outcome reporting on basis of the results?
|
Bias due to loss to follow-up?
|
Bias due to violation of intention to treat analysis? |
|
Vaisman (2001) |
Unclear (method of randomization is not described in the study). Randomization for the order of treatment is preferred in a cross-over study) |
Unclear (allocation concealment is not described in the study) |
Unlikely (hard (objective) outcome measures LT4 en TSH levels) |
Unlikely (hard (objective) outcome measures LT4 en TSH levels) |
Unlikely (hard (objective) outcome measures LT4 en TSH levels) |
Unlikely |
Unlikely (One patient was excluded during the study because of carbamazepine use) |
Unlikely |
Beoordelingsdatum en geldigheid
Publicatiedatum : 19-07-2020
Beoordeeld op geldigheid : 01-07-2020
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepaalt het bestuur van de NIV of de modules van deze richtlijn nog actueel zijn. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NIV is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Goedgekeurd door:
- Nederlands Huisartsen Genootschap
- Schildklierorganisatie Nederland
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn geeft aanbevelingen ten aanzien van behandeling van volwassen patiënten (leeftijd ≥18 jaar) met schildklierfunctiestoornissen. Doel van deze gedeeltelijke herziening is om een richtlijn te verkrijgen waarin de meeste recente medische kennis omtrent de zorg voor patiënten met schildklierfunctiestoornissen wordt meegenomen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Werkgroep
- Prof. dr. E. Fliers (voorzitter vanaf 1 mei 2019), internist-endocrinoloog, NIV
- Prof. dr. R. Peeters (voorzitter tot 1 mei 2019), internist-endocrinoloog, NIV
- Dr. W.E. Visser, internist-endocrinoloog, NIV
- Dr. A. Roos, internist-endocrinoloog, NIV
- Dr. M. Medici, internist-endocrinoloog, NIV
- Dr. A.F. Muller, internist-endocrinoloog, NIV
- Prof. dr. O.M. Dekkers, internist-endocrinoloog en klinisch epidemioloog, NIV
- Dr. A.A. Bouman, SON
- R. Nix, SON (tot 1 september 2019)
Meelezers
- Dr. M.M.E. van Rumste, gynaecoloog, NVOG (vanaf 1 april 2019)
- Drs. M. Sijbom, huisarts, NHG (vanaf 1 juli 2019)
- Dr. S. van der Berg, klinisch chemicus, NVKC (vanaf 1 augustus 2019)
Met ondersteuning van
- Drs. L. Boerboom, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.R. Zwakenberg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. N.L. van der Zwaluw, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met evt. belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Prof. dr. E. Fliers, internist-endocrinoloog, NIV (voorzitter vanaf 1-5-2019) |
Hoofd- afdeling Endocrinologie en Metabolisme, Amsterdam UMC, Hoogleraar Endocrinologie UvA |
Board memberships, committees: - ETA guideline committee diagnosis and management of central hypothyroidism (2017-2018) - Executive Committee European Thyroid Association (tot 2019) - Program organizing committee ETA Annual Meeting 2017, 2018, 2019 - Member Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Voorzitter Medische Adviesraad Schildklier Organisatie Nederland (SON) |
geen |
Geen |
|
Prof. dr. R. Peeters, internist-endocrinoloog, NIV (voorzitter tot 1-05-2019) |
Erasmus MC, Internist-endocrinoloog, hoogleraar schildklierziekten |
Member of International guideline committees: American Thyroid Association Task Force: Guidelines for thyroid disease and pregnancy (not remunerated)
Board memberships and committees of professional societies: - Programme Organizing Committee of the 2019 European Congress of Endocrinology. 2018 Annual Meeting of the American Thyroid Association - Iodine Global Network (https://www.ign.org/), National representative for the Netherlands (not remunerated) - Chair of the Scientific Advisory Board of the World Iodine Association (not remunerated) - Treasurer of the Dutch Thyroid Club / Foundation for Thyroid Research (not remunerated) |
Zie transparantieregister voor financiële banden (red: diverse diensten met onkosten) vergoeding van Shire International licenising, Genzyme Europe BV, Ipsen Farmaceutica BV, Merck BV, IBSA, Bayer, - Adviesraad Eisai BV (vergoeding) |
Geen; vergoedingen waren niet gerelateerd aan de richtlijn
|
|
Dr. W.E. Visser, internist-endocrinoloog, NIV |
Erasmus MC, Internist-endocrinoloog |
Member of international committees - European Thyroid Association Task Force: Guideline on Diagnosis and Management of Resistance to Thyroid Hormone & other disorders of thyroid hormone action (2016 - present) - Educational Committee of the European Thyroid Association (2017 - present) - Chair Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Editorial Board membership - Editorial Board of Frontiers in Neurogenomics (2013 - present) - Editorial Board of the Journal of Endocrinology (2016 - present) - Editorial Board of the Journal of Molecular Endocrinology (2016 - present) - Editorial Board of the Endocrinology, Diabetes and Metabolism (2016 - present) - Editorial Board of the European Thyroid Journal (2017 - present)
Management role in International Consortia - Founder and chair MCT8 patient registry (2016 - present). - Chair rare thyroid hormone signalling disorders in Endo-ERN (European Reference Networks) (2016 - present) - Chair Thyroid Group of Endo-ERN EuRRECa (2018 - present)" |
geen |
Vergoedingen niet gerelateerd aan richtlijn (diabetes, schildklierkanker) |
|
Drs. A. Roos, internist-endocrinoloog, NIV |
Internist-endocrinoloog Martini Ziekenhuis, Groningen |
Geen |
Geen |
Geen |
|
Dr. M. Medici, internist-endocrinoloog, NIV |
Internist-Endocrinoloog radboudUMC (0,6 fte) en Erasmus MC (0,4 fte) |
Geen;
|
Erasmus Universiteit Fellowship: geen belang bij het advies van de richtlijn. |
geen |
|
Dr. A.F. Muller, internist-endocrinoloog, NIV |
Internist, Diakonessenhuis |
Zie transparantieregister (red: diverse diensten met (onkosten)vergoeding voor Novo Nordisk, Eli Lilly and Company (adviesraad), Amgen, Sanofi) |
|
Vergoedingen waren niet gerelateerd aan de richtlijn (diabetes, schildklierkanker)
|
|
Prof. dr. O.M. Dekker, internist, NIV |
Hoogleraar Interne Geneeskunde LUMC Leiden |
Collegelid CBG (betaald) Lid Gezondheidsraad (onbetaald) Voorzitter Vereniging Epidemiologie (onbetaald)" |
Geen |
Geen |
|
Dr. A.A. Bouman, SON |
Gepensioneerd (tot 1-9-2012 werkzaam als Klinisch chemicus bij het Vumc) |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden van de patiëntenvereniging Schildklier Organisatie Nederland (SON). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (Richtlijn schildklierfunctiestoornissen, 2012) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door middel van een schriftelijke invitational conference. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg en patiëntveiligheid.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep en de adviseur concept-uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De gespecificeerde zoekstrategieën zijn op te vragen bij het Kennisinstituut.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: Cochrane - voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS - voor observationeel onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (eindconclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een eindconclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg. De module over organisatie van zorg wordt opgenomen in deel 2 van de richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialist.

