TPO-schildklierantistoffen zwangerschap bij schildklierfunctiestoornissen
Uitgangsvraag
Dienen euthyreote vrouwen van wie bekend is dat zij positief zijn voor TPO-schildklierantistoffen, voorafgaand aan of tijdens de zwangerschap te worden behandeld met levothyroxine?
Aanbeveling
Er is geen plaats voor een behandeling met levothyroxine bij euthyreote vrouwen met TPO-schildklierantistoffen met zwangerschapswens of zwangerschap.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Verschillende interventiestudies hebben gekeken naar de effecten van behandeling met levothyroxine in euthyreote vrouwen met TPOAb+ met zwangerschapswens of zwangerschap. De studies vonden geen aanwijzingen dat behandeling met levothyroxine leidt tot een vermindering van miskramen, perinatale sterfte of vroeggeboorte in euthyreote TPOAb+ vrouwen.
De geïncludeerde studies zijn mogelijk te beperkt van omvang en hanteren verschillende normaalwaarden voor TSH. De grootste placebo gecontroleerde studie, van methodologische hoge kwaliteit, laat geen effect zien van levothyroxine op miskraam, perinatale sterfte en vroeggeboorte (Dhillon-Smit, 2019).
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
De belasting van de interventie (behandeling van euthyreote TPOAb+ vrouwen die zwanger zijn of een zwangerschapswens hebben) lijkt gering en te overzien. Er is een groot risico op het medicaliseren van gezonde zwangere vrouwen.
Kosten (middelenbeslag)
De financiële kosten van de medicatie zijn laag maar de kosten van extra ziekenhuisbezoek en aanvullende laboratoriumbepalingen zijn onbekend maar niet onaanzienlijk.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
De studies vonden geen aanwijzingen dat behandeling met levothyroxine een vermindering van miskramen, perinatale sterfte of vroeggeboorte in euthyreote TPOAb+ vrouwen geeft. Evenmin werden op de genoemde eindpunten ongunstige effecten vastgesteld. Er zijn geen gegevens bekend over de mogelijke lange termijn effecten van levothyroxine tijdens de zwangerschap op cognitief functioneren van het kind. Ongunstige effecten voor de moeder lijken - zolang het TSH normaal blijft - onwaarschijnlijk. In de beschreven studies komt wel een positieve correlatie naar voren tussen de hoogte van het TSH en de kans op ongunstige zwangerschapsuitkomsten maar er is geen bewijs dat behandeling met schildklierhormoon deze uitkomsten gunstig beïnvloeden. De relatie tussen een verhoogde vrije T4-concentratie en (latere) cognitieve ontwikkeling is nog onduidelijk.
De werkgroep is van mening dat er te weinig bewijskracht is voor gunstige effecten aangaande de gedefinieerde eindpunten en dat er te veel onzekerheden zijn wat betreft mogelijke ongunstige effecten op langere termijn om het gebruik van levothyroxine bij euthyreote TPOAb+ vrouwen met zwangerschapswens of tijdens zwangerschap te adviseren.
De werkgroep ziet op grond van de beschikbare gegevens dus geen rol voor behandeling met thyroxine van euthyreote TPOAb+ vrouwen die zwanger zijn of een zwangerschapswens hebben.
Screening op schildklierfunctiestoornissen bij vrouwen met TPOAb+ wordt aanbevolen (zie module 'Screening op overte hypothyreoïdie in het eerste trimester van de zwangerschap').
Onderbouwing
Achtergrond
Momenteel worden zwangeren of vrouwen met kinderwens niet standaard gescreend op TPO-schildklierantistoffen (TPOAb+). Er zijn aanwijzingen dat euthyreote vrouwen (TSH binnen de referentiewaarden) met TPOAb+ een hoger risico hebben op negatieve zwangerschapsuitkomsten. Behandeling met levothyroxine zou mogelijk het risico op een miskraam, vroeggeboorte, perinatale sterfte of verminderde ontwikkeling van het kind kunnen verminderen/voorkomen.
Conclusies / Summary of Findings
Miskraam
|
Redelijk GRADE |
Behandeling met levothyroxine resulteert waarschijnlijk niet in een vermindering van miskramen bij euthyreote TPOAb+ vrouwen.
Bronnen: (Nazarpour, 2017; Negro, 2016; Dhillon-Smit, 2019; Negro, 2006; Wang, 2017) |
Perinatale sterfte
|
Laag GRADE |
Behandeling met levothyroxine lijkt niet te resulteren in een vermindering van perinatale sterfte bij euthyreote TPOAb+ vrouwen.
Bronnen: (Nazarpour, 2017; Dhillon-Smit, 2019) |
Vroeggeboorte
|
Laag GRADE |
Behandeling met levothyroxine lijkt niet in een vermindering van vroeggeboortes bij euthyreote TPOAb+ vrouwen te resulteren.
Bronnen: (Nazarpour, 2017; Negro, 2016; Dhillon-Smit, 2019; Negro, 2006; Wang, 2017) |
Ontwikkeling van het kind
|
- GRADE |
Er is onvoldoende onderzoek uitgevoerd bij euthyreote TPOAb+ vrouwen met zwangerschapswens of die zwanger zijn, om de effecten van levothyroxine op de ontwikkeling van het kind te kunnen beoordelen. |
Samenvatting literatuur
Er zijn vijf studies gevonden die de effecten van behandeling met levothyroxine beschreven bij euthyreote TPOAb+ vrouwen, met een zwangerschapswens of zwangerschap.
- Nazarpour (2017) voerde een gerandomiseerde studie uit bij euthyreote zwangere vrouwen, welke geïncludeerd werden in het eerste trimester (gemiddelde zwangerschapsduur bij inclusie: 11 weken) en gevolgd tot aan de bevalling. Vrouwen met TPOAb+ werden willekeurig verdeeld in twee groepen: groep A (n=65) werd behandeld met levothyroxine en groep B (n=66) ontving geen behandeling. De zwangere vrouwen die negatief waren voor TPOAb (TPOAb-) dienden als controlegroep (groep C, n=1028). Vrouwen in groep A ontvingen een levothyroxine ochtenddosis van 0,5 μg/kg/dag bij TSH <1,0 mIU /ml, een dosis van 0,75 μg/kg/dag bij TSH tussen 1,0 en 2,0 mIU/ml en een 1 μg/kg/dag dosis bij TSH> 2,0 mIU/ml of een TPOAb-titer van meer dan 1500 IU/ml; doseringen werden tijdens de zwangerschap gehandhaafd. Primaire uitkomstmaten waren vroeggeboorte, gedefinieerd als geboorte vóór 37 weken, en miskraam, gedefinieerd als het verlies van een embryo of foetus vóór de 20e week van de zwangerschap. Prenatale sterfte was een secundaire uitkomstmaat, en werd gedefinieerd als overlijden van foetus in de baarmoeder vanaf 20 weken zwangerschap.
- Negro (2016) voerde een prospectieve gerandomiseerde studie uit naar het effect van levothyroxine op het optreden van een miskraam en vroeggeboorte bij euthyreote vrouwen, met TSH-waarden tussen 0,5 en 2,5 mIU/L en TPOAb+ tijdens de zwangerschap. Vrouwen in het eerste trimester van de zwangerschap werden gescreend op TSH en schildklierantilichamen, en werden onderverdeeld in drie groepen. Groep A bestond uit euthyreote TPOAb+ vrouwen (n=198) behandeld met levothyroxine, groep B bestond uit onbehandelde euthyreote TPOAb+ vrouwen (n=195), en groep C bestond uit onbehandelde TPOAb- vrouwen (n=197). Vrouwen in groep A ontvingen een levothyroxinedosis van 0,5 μg/kg/dag bij TSH-waarden tussen 0,5 en 1,5 mIU/L, en een dosis van 1,0 μg/kg/dag bij TSH-waarden tussen 1,5 en 2,5 mIU/L. TSH-waarden werden eenmaal in het tweede en eenmaal in het derde trimester gecontroleerd. Bij een TSH-waarde > 3,0 mIU/L in het tweede trimester, werd de dosis levothyroxine verhoogd met 12,5 μg/dag, en bij een TSH-waarde < 0,5 mIU/L werd de dosis levothyroxine verlaagd met 12,5 μg/dag. Vrouwen met een TSH-waarde tussen 0,5 en 3,0 mIU/L bleven dezelfde dosis levothyroxine gebruiken. Uitkomstmaten waren vroeggeboorte, gedefinieerd als spontane geboorte vóór de 37e week van de zwangerschap, en miskraam, welke niet werd gedefinieerd in de studie.
- Dhillon-Smith (2019) voerde een dubbelblind placebo-gecontroleerde (TABLET) trial uit om te onderzoeken of behandeling met levothyroxine het percentage levendgeborenen verhoogt bij euthyreote TPOAb+ vrouwen en een voorgeschiedenis van miskramen of onvruchtbaarheid. Euthyreoïdie werd gedefinieerd als een TSH-gehalte van 0,44 tot 3,63 mIU/L en een vrij thyroxine (FT4) niveau van 10,0 tot 21,0 pmol/L. Een totaal van 952 vrouwen met een zwangerschapswens werden willekeurig toegewezen om ofwel 50 μg/dag levothyroxine (n=476) of placebo (n=476) te ontvangen vóór de conceptie tot het einde van de zwangerschap. In de levothyroxinegroep ondergingen 45,4% van de vrouwen vruchtbaarheidsbehandeling en in de controlegroep 44,7%. Een totaal van 266 van 470 vrouwen in de levothyroxinegroep (56,6%) en 274 van 470 vrouwen in de controlegroep (58,3%) raakten zwanger. De primaire uitkomstmaat was het percentage vrouwen dat randomisatie onderging en een levendgeborene had na ten minste 34 voltooide weken zwangerschap. Vooraf gespecificeerde secundaire uitkomsten waren: klinische zwangerschap bij 7 weken; voortdurende zwangerschap bij 12 weken; miskraam vóór 24 weken; doodgeboorte (intra-uteriene dood na 24 weken); buitenbaarmoederlijke zwangerschap; beëindigen van de zwangerschap; levendgeborene vóór 28 weken, vóór 34 weken en na 34 weken; zwangerschapsduur bij bevalling; geboortegewicht; en Apgar score op 1 en 5 minuten.
- Negro (2006) voerde een gerandomiseerde studie uit naar het effect van levothyroxine op het optreden van zwangerschapscomplicaties bij euthyreote vrouwen met TPOAb+ tijdens de zwangerschap. Vrouwen in het eerste trimester van de zwangerschap werden gescreend op TSH en schildklierantilichamen, en werden onderverdeeld in drie groepen. Groep A bestond uit euthyreote TPOAb+ vrouwen (n=57) behandeld met levothyroxine, groep B bestond uit onbehandelde euthyreote TPOAb+ vrouwen (n=58), en groep C bestond uit een onbehandelde TPOAb- controlegroep (n=869). Vrouwen in groep A ontvingen een levothyroxine ochtenddosis van 0,5 μg/kg/dag bij TSH < 1,0 mIU /ml, een dosis van 0,75 μg/kg/dag bij TSH tussen 1,0 en 2,0 mIU/ml en een 1 μg/kg/dag dosis bij TSH > 2,0 mIU/ml of een TPOAb-titer van meer dan 1500 IU/ml; doseringen werden tijdens de zwangerschap gehandhaafd. Uitkomstmaten waren vroeggeboorte, gedefinieerd als spontane geboorte vóór de 37e week van de zwangerschap, en miskraam, welke niet werd gedefinieerd in de studie.
- Wang (2017) onderzocht in een open-label gerandomiseerde trial 600 vrouwen die in-vitrofertilisatie (IVF) en embryotransfer (ET) ondergingen en die positief testten op TPOAb. Deze POSTAL-studie evalueerde of behandeling met levothyroxine voor IVF-ET de kans op miskramen doet afnemen en de kans op een levendgeborene doet toenemen, in euthyreote vrouwen positief voor TPOAb. Vrouwen in de interventiegroep (n=300) werden behandeld met levothyroxine vanaf 2 tot 4 weken vóór de gecontroleerde ovariële hyperstimulatie en tot het einde van de zwangerschap. Voor vrouwen met TSH-niveau ≥ 2,5 mIU/L was de startdosis 50 μg/dag; voor vrouwen met TSH-niveau < 2,5 mIU/L was de startdosis 25 μg/dag. Voor vrouwen met een lichaamsgewicht < 50 kg werd de startdosis verlaagd met 50%. De dosis levothyroxine werd getitreerd om het TSH-niveau binnen 0,1 tot 2,5 mIU/L te houden in het eerste trimester, 0,2 tot 3,0 mIU/L in het tweede trimester en 0,3 tot 3. 0 mIU/L in het derde trimester. Vrouwen in de controlegroep (n=300) ontvingen geen levothyroxine. Een totaal van 107 van de 300 vrouwen in de levothyroxinegroep (35,7%) en 113 van de 300 vrouwen in de controlegroep (37,7%) raakten zwanger. De primaire uitkomst was miskraam (zwangerschapsverlies vóór 28 weken zwangerschap). Vroeggeboorte werd gedefinieerd als een levendgeborene vóór 37 weken zwangerschap.
Resultaten
Miskraam
Vijf studies rapporteerden miskraam als uitkomstmaat bij de behandeling met levothyroxine (Nazarpour, 2017; Negro, 2016; Dhillon-Smit, 2019; Negro, 2006; Wang, 2017).
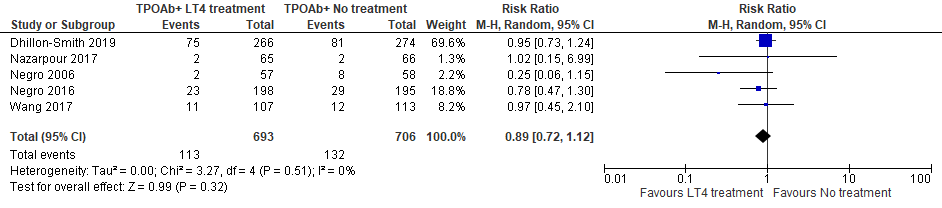
In de meta-analyse van de vijf studies, waarin de resultaten werden vergeleken in zwangere TPOAb+ vrouwen die wel of geen levothyroxine ontvingen, werd geen effect gevonden van levothyroxine op het optreden van miskraam in TPOAb+ vrouwen (figuur 1).
Figuur 1 Meta-analyse effect van levothyroxine op miskraam in TPOAb+ vrouwen
Perinatale sterfte
Twee studies rapporteerden perinatale sterfte als uitkomstmaat bij de behandeling met levothyroxine. Nazarpour (2017) vond geen significante verschillen tussen de drie groepen in perinatale sterfte (aantal sterfgevallen: groep A: 0 (0%), groep B: 0 (0%), groep C: 2 (0,2%)). Ook Dillon-Smith (2019) vond geen significant verschil in perinatale sterfte tussen de interventiegroep (n=1, 0,4%) en de controlegroep (n=0, 0%).
Vroeggeboorte
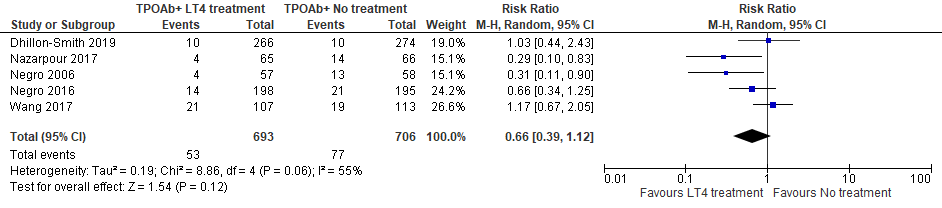
Vijf studies rapporteerden vroeggeboorten als uitkomstmaat bij de behandeling met levothyroxine (Nazarpour, 2017; Negro, 2016; Dhillon-Smit, 2019; Negro, 2006; Wang, 2017). In de meta-analyse van de vijf studies, waarin de resultaten werden vergeleken in TPOAb+ vrouwen die wel of geen levothyroxine ontvingen, werd geen effect gevonden van levothyroxine op het optreden van vroeggeboorte in TPOAb+ vrouwen (figuur 2).
Figuur 2 Meta-analyse effect van levothyroxine op vroeggeboorte in TPOAb+ vrouwen
Ontwikkeling van het kind
De uitkomstmaat ontwikkeling van het kind is niet gerapporteerd als uitkomstmaat in de studies naar de effecten van levothyroxine bij euthyreote TPOAb+ vrouwen met zwangerschapswens of die zwanger zijn.
Bewijskracht van de literatuur
De bewijskracht van RCT’s begint op hoog.
- De bewijskracht voor de uitkomstmaat miskraam is met één niveau verlaagd tot redelijk door het geringe aantal patiënten (imprecisie).
- De bewijskracht voor de uitkomstmaat perinatale sterfte is met twee niveaus verlaagd tot laag door het geringe aantal patiënten (imprecisie).
- De bewijskracht voor de uitkomstmaat vroeggeboorte is met twee niveaus verlaagd tot laag gezien het geringe aantal patiënten (imprecisie) en inconsistentie in de onderzoeksresultaten.
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat zijn de (on)gunstige effecten van behandeling met levothyroxine bij euthyreote TPOAb+ vrouwen met zwangerschapswens of zwangerschap.
P: euthyreote vrouwen (met zwangerschapswens of zwanger) met TPOAb+;
I: levothyroxine;
C: placebo, andersoortige behandeling;
O: miskraam, perinatale sterfte, vroeggeboorte, ontwikkeling van het kind.
Relevante uitkomstmaten
De werkgroep achtte miskraam een voor de besluitvorming cruciale uitkomstmaat; en perinatale sterfte en vroeggeboorte voor de besluitvorming als belangrijke uitkomstmaten.
De werkgroep definieerde de uitkomstmaten als volgt:
- Miskraam: eindigen van zwangerschap voor 24 weken.
- Perinatale sterfte: overlijden van foetus vanaf 24 weken zwangerschap tot in de eerste 7 dagen na de geboorte.
- Vroeggeboorte: geboorte voor 37 weken.
De werkgroep definieerde statistisch significant minder miskramen, minder vroeggeboorte, minder perinatale sterfte als een klinisch relevant verschil.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID), en Embase (via Embase.com) is op 11 september 2019 met relevante zoektermen gezocht naar studies gepubliceerd vanaf het jaar 2000 die de effecten beschrijven van behandeling met levothyroxine van euthyreote vrouwen met zwangerschapswens of zwangerschap en TPOAb+. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 165 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: RCT’s, behandeling met levothyroxine, aanwezigheid van TPOAb+. Op basis van titel en abstract werden in eerste instantie 18 studies voorgeselecteerd. Na raadpleging van de volledige tekst werden vervolgens 14 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en vier studies definitief geselecteerd. Daarnaast is er één studie toegevoegd die niet uit de literatuurzoekactie kwam, maar uit een review.
Resultaten
Vijf onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
Referenties
- 1 - Dhillon-Smith, R. K., Middleton, L. J., Sunner, K. K., Cheed, V., Baker, K., Farrell-Carver, S.,... & Ghobara, T. (2019). Levothyroxine in women with thyroid peroxidase antibodies before conception. New England Journal of Medicine, 380(14), 1316-1325.
- 2 - Nazarpour, S., Tehrani, F. R., Simbar, M., Tohidi, M., Majd, H. A., & Azizi, F. (2017). Effects of levothyroxine treatment on pregnancy outcomes in pregnant women with autoimmune thyroid disease. European journal of endocrinology, 176(2), 253-265.
- 3 - Negro, R., Schwartz, A., & Stagnaro-Green, A. (2016). Impact of levothyroxine in miscarriage and preterm delivery rates in first trimester thyroid antibody-positive women with TSH less than 2.5 mIU/L. The Journal of Clinical Endocrinology & Metabolism, 101(10), 3685-3690.
- 4 - Negro, R., Mangieri, T., Coppola, L., Presicce, G., Casavola, E. C., Gismondi, R.,... & Hassan, H. (2005). Levothyroxine treatment in thyroid peroxidase antibody-positive women undergoing assisted reproduction technologies: a prospective study. Human reproduction, 20(6), 1529-1533.
- 5 - Wang, H., Gao, H., Chi, H., Zeng, L., Xiao, W., Wang, Y.,... & Zhou, Z. (2017). Effect of levothyroxine on miscarriage among women with normal thyroid function and thyroid autoimmunity undergoing in vitro fertilization and embryo transfer: a randomized clinical trial. Jama, 318(22), 2190-2198.
Evidence tabellen
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Nazarpour, 2017 |
Randomization was performed in blocks of four using a computer-generated list |
Likely Masking to treatment allocation was not possible |
Unlikely Objective outcomes |
Unlikely Physicians were blinded to treatment allocation |
Unlikely Physicians were blinded to treatment allocation |
Unlikely |
Unclear No reasons for loss to follow-up described. |
Unlikely No participants were excluded from the primary intention-to-treat analysis for protocol violations. |
|
Negro, 2016 |
Two computer-generated concealed randomized schedules were created using permuted blocks of 4 to assign patients to group A or B. |
Unclear Not reported |
Unlikely Not described, but unlikely to affect outcomes. |
Unlikely Not described, but unlikely to affect outcomes. |
Unlikely Not described, but unlikely to affect outcomes. |
Unlikely |
Unclear No reasons for loss to follow-up described. |
Unclear |
|
Dhillon-Smit, 2019 |
Computerized randomization was performed centrally through a secure Internet application. |
Unlikely Computerized randomization was performed centrally through a secure Internet application. |
Unlikely Throughout the trial, the participants, clinicians, and trial nurses were unaware of the trial-group assignments. |
Unlikely Throughout the trial, the participants, clinicians, and trial nurses were unaware of the trial-group assignments. |
Unlikely Throughout the trial, the participants, clinicians, and trial nurses were unaware of the trial-group assignments. |
Unlikely |
Unlikely |
Unlikely Outcomes in all women who underwent randomization (pregnant and nonpregnant) were included in the trial intention-to-treat analysis. |
|
Negro, 2006 |
A computer program was used to randomly assign the patients to one or the other group. A sealed opaque envelope was assigned to each patient |
Unlikely |
Unlikely Not described, but unlikely to affect outcomes. |
Unlikely Physicians were blinded to treatment allocation |
Unlikely Physicians were blinded to treatment allocation |
Unlikely |
Unclear No reasons for loss to follow-up described. |
Unclear |
|
Wang, 2017 |
Randomisation sequence generated in a 1:1 ratio by producing a 600 unique random-number list using EpiCalc 2000 software |
Unclear No details mentioned |
Unlikely Not blinded, but unlikely to affect outcomes. |
Unlikely Not blinded, but unlikely to affect outcomes. |
Unlikely Not blinded, but unlikely to affect outcomes. |
Unlikely Reported on important outcomes |
Unlikely |
Unlikely Intention-to-treat analyses were performed. |
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Akhtar, 2019 |
Onbekende TPO status |
|
Negro, 2005 |
Vergelijkingen niet relevant voor de PICO |
|
Nazarpour, 2016 |
Achtergrondartikel. |
|
Medenica, 2015 |
Achtergrondartikel. |
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 01-11-2021
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2026 bepaalt het bestuur van de NIV of de modules van deze richtlijn nog actueel zijn. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NIV is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Deze richtlijn is goedgekeurd door:
- Nederlands Huisartsen Genootschap
- Schildklier Organisatie Nederland
Doel en doelgroep
Doel
Deze richtlijn geeft aanbevelingen ten aanzien van behandeling van volwassen patiënten (leeftijd ≥ 18 jaar) met schildklierfunctiestoornissen. Doel van deze gedeeltelijke herziening is om een richtlijn te verkrijgen waarin de meeste recente medische kennis omtrent de zorg voor patiënten met schildklierfunctiestoornissen wordt meegenomen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Werkgroep
- Prof. dr. E. Fliers (voorzitter vanaf 1 mei 2019), internist-endocrinoloog, NIV
- Prof. dr. R. Peeters (voorzitter tot 1 mei 2019), internist-endocrinoloog, NIV
- Dr. W.E. Visser, internist-endocrinoloog, NIV
- Dr. A. Roos, internist-endocrinoloog, NIV
- Dr. M. Medici, internist-endocrinoloog, NIV
- Dr. A.F. Muller, internist-endocrinoloog, NIV
- Prof. dr. O.M. Dekkers, internist-endocrinoloog en klinisch epidemioloog, NIV
- Dr. A.A. Bouman, SON
- Dr. M.M.E. van Rumste, gynaecoloog, NVOG (vanaf 1 april 2019)
- Drs. M. Sijbom, huisarts, NHG (vanaf 1 juli 2019)
- Dr. S.A.A van den Berg, klinisch chemicus, NVKC (vanaf 1 augustus 2019)
- Drs. J.H. Scheffer, bedrijfsarts, NVAB (vanaf 1 september 2020)
Met ondersteuning van
- Drs. L. Boerboom, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.R. Zwakenberg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. N.L. van der Zwaluw, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.J. Versteeg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met evt. belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Prof. dr. E. Fliers, internist-endocrinoloog, NIV (voorzitter vanaf 1-5-2019) |
Hoofd- afdeling Endocrinologie en Metabolisme, Amsterdam UMC, Hoogleraar Endocrinologie UvA |
Board memberships, committees: - ETA guideline committee diagnosis and management of central hypothyroidism (2017-2018) - Executive Committee European Thyroid Association (tot 2019) - Program organizing committee ETA Annual Meeting 2017, 2018, 2019 - Member Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Voorzitter Medische Adviesraad Schildklier Organisatie Nederland (SON) |
Geen |
Geen |
|
Prof. dr. R. Peeters, internist-endocrinoloog, NIV (voorzitter tot 1-05-2019) |
Erasmus MC, Internist-endocrinoloog, hoogleraar schildklierziekten |
Member of International guideline committees: American Thyroid Association Task Force: Guidelines for thyroid disease and pregnancy (not remunerated)
Board memberships and committees of professional societies: - Programme Organizing Committee of the 2019 European Congress of Endocrinology. 2018 Annual Meeting of the American Thyroid Association - Iodine Global Network (https://www.ign.org/), National representative for the Netherlands (not remunerated) - Chair of the Scientific Advisory Board of the World Iodine Association (not remunerated) - Treasurer of the Dutch Thyroid Club / Foundation for Thyroid Research (not remunerated) |
Zie transparantieregister voor financiële banden (red: diverse diensten met onkosten) vergoeding van Shire International licenising, Genzyme Europe BV, Ipsen Farmaceutica BV, Merck BV, IBSA, Bayer, - Adviesraad Eisai BV (vergoeding) |
Vergoedingen waren niet gerelateerd aan de richtlijn
|
|
Dr. W.E. Visser, internist-endocrinoloog, NIV |
Erasmus MC, Internist-endocrinoloog |
Member of international committees - European Thyroid Association Task Force: Guideline on Diagnosis and Management of Resistance to Thyroid Hormone & other disorders of thyroid hormone action (2016 - present) - Educational Committee of the European Thyroid Association (2017 - present) - Chair Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Editorial Board membership - Editorial Board of Frontiers in Neurogenomics (2013 - present) - Editorial Board of the Journal of Endocrinology (2016 - present) - Editorial Board of the Journal of Molecular Endocrinology (2016 - present) - Editorial Board of the Endocrinology, Diabetes and Metabolism (2016 - present) - Editorial Board of the European Thyroid Journal (2017 - present)
Management role in International Consortia - Founder and chair MCT8 patient registry (2016 - present). - Chair rare thyroid hormone signalling disorders in Endo-ERN (European Reference Networks) (2016 - present) - Chair Thyroid Group of Endo-ERN EuRRECa (2018 - present)" |
Geen |
Vergoedingen niet gerelateerd aan richtlijn (diabetes, schildklierkanker) |
|
Dr. A. Roos, internist-endocrinoloog, NIV |
Internist-endocrinoloog Martini Ziekenhuis, Groningen |
Geen |
Geen |
Geen |
|
Dr. M. Medici, internist-endocrinoloog, NIV |
Internist-Endocrinoloog radboudUMC (0,6 fte) en Erasmus MC (0,4 fte) |
Management role in International Consortia
Memberships (inter)national committees:
Editorial Board memberships:
|
Erasmus Universiteit Fellowship: geen belang bij het advies van de richtlijn. |
Geen |
|
Dr. A.F. Muller, internist-endocrinoloog, NIV |
Internist, Diakonessenhuis |
Zie transparantieregister (red: diverse diensten met (onkosten)vergoeding voor Novo Nordisk, Eli Lilly and Company (adviesraad), Amgen, Sanofi) |
|
Vergoedingen waren niet gerelateerd aan de richtlijn (diabetes, schildklierkanker)
|
|
Prof. dr. O.M. Dekker, internist, NIV |
Hoogleraar Interne Geneeskunde LUMC Leiden |
Collegelid CBG (betaald) Lid Gezondheidsraad (onbetaald) Voorzitter Vereniging Epidemiologie (onbetaald)" |
Geen |
Geen |
|
Dr. A.A. Bouman, SON |
Gepensioneerd (tot 1-9-2012 werkzaam als Klinisch chemicus bij het Vumc) |
Geen |
Geen |
Geen |
|
Drs. J.H. Scheffer, NVAB |
Bedrijfsarts |
Geen |
Geen |
Geen |
|
Dr. M.M.E. van Rumste, gynaecoloog, NVOG |
Gynaecoloog, Catherinaziekenhuis |
Geen |
Geen |
Geen |
|
Drs. M. Sijbom, huisarts, NHG |
Huisarts |
Geen |
Geen |
Geen |
|
Dr. S.A.A van den Berg, klinisch chemicus, NVKC |
Klinisch Chemicus, Erasmus MC |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden van de patiëntenvereniging Schildklier Organisatie Nederland (SON). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (Richtlijn schildklierfunctiestoornissen, 2012) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door middel van een schriftelijke invitational conference. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg en patiëntveiligheid.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep en de adviseur concept-uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De gespecificeerde zoekstrategieën zijn op te vragen bij het Kennisinstituut.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: Cochrane - voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS - voor observationeel onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (eindconclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een eindconclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg. De module over organisatie van zorg wordt opgenomen in deel 2 van de richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialist.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
