Biochemische bepalingen bij schildklierfunctiestoornissen
Uitgangsvraag
Wat is het gewenste gebruik van biochemische bepalingen in het kader van diagnostiek van schildklierfunctiestoornissen?
Aanbeveling
De eerste biochemische test om schildklierdysfunctie uit te sluiten is het meten van de serum TSH-concentratie. Voor de bepaling van TSH wordt gebruik gemaakt van een sandwich immunoassay.
Wanneer sprake is van een afwijkende TSH-concentratie of bij een klinisch sterk vermoeden op een zeldzame schildklierfunctiestoornis of hypofysedysfunctie, is bepaling van de FT4-concentratie van belang. Wanneer het laboratorium niet de referentie methode voert is het van belang dat de juiste referentie-intervallen gehanteerd worden.
Bij ongebruikelijke combinaties van TSH en FT4 dienen analytische interferenties te worden uitgesloten.
Het bepalen van de FT3-concentratie is alleen in specifieke gevallen aangewezen. Bij een onmeetbaar laag TSH met FT4-concentraties binnen het referentieinterval is een FT3 bepaling relevant om te onderzoeken of er sprake is van T3-toxicose. De (F)T3-concentratie is ook van toegevoegde waarde wanneer aan een van de schildklierhormoonresistentiesyndromen wordt gedacht. Voor (F)T3 is een referentie methode beschikbaar, maar geen gedefinieerd of geharmoniseerd referentie interval. Het is dan ook belangrijk dat ieder laboratorium zich er van vergewist het juiste interval te gebruiken.
Overwegingen
TSH
Wanneer TSH bepalen?
De eerste biochemische test om schildklierdysfunctie uit te sluiten is het meten van de serum TSH-concentratie. Een TSH-concentratie binnen het referentie-interval sluit primaire schildklierdysfunctie vrijwel uit (negatief voorspellende waarde 99,7%) (Rege, 1996; Wiersinga, 1986; Wiersinga, 2003).
Zeldzame entiteiten waarbij er een dysfunctie is van de schildklierhormoonhuishouding kunnen gepaard gaan met een TSH-concentratie binnen het referentie-interval. Tot deze ziektebeelden behoren een centrale hypothyreoïdie, een TSH-producerend hypofyseadenoom (TSH-oma) of schildklierhormoonresistentiesyndromen (schildklierhormoonresistentie ten gevolge van een mutatie in het gen dat codeert voor de schildklierhormoonreceptor (THRB of THRA; deficiëntie in de schildklierhormoontransporter MCT8 of OATP1C1; deficiëntie in SBP2)).
Assays
Anno 2020 wordt voor de bepaling van TSH voornamelijk gebruik gemaakt van de 3e generatie sandwich immunoassay. Deze generatie heeft een functionele sensitiviteit (de laagst betrouwbaar te meten concentratie) rond 0.01 tot 0.02 mIU/l (Spencer, 2017). Er zijn grote verschillen in de kalibratie tussen de verschillende immunochemische methoden voor schildklier parameters. Voor TSH is om deze reden vanuit The International Federation of Clinical Chemistry and Laboratory Medicine een harmonisatie traject gestart (Thienpont, 2017). Standaardisatie van de TSH bepaling is helaas nog niet mogelijk, gegeven het ontbreken van een referentie methode. Standaardisatie moet er voor zorgen dat uitslagen vergelijkbaar zijn tussen laboratoria. Omdat harmonisatie nog geen feit is moet het laboratorium zich er van vergewissen dat het de juiste referentie-intervallen voert. In de ideale situatie wordt een betrouwbaar referentie interval vastgesteld door in de eigen populatie volgens de daarvoor geldende criteria een aantal bepalingen te doen met de eigen assays. Het is namelijk niet per definitie waar dat een door de leverancier voorgesteld interval van toepassing is op de populatie waarin metingen worden gedaan (Kratzch, 2005; Barth, 2018; Naafs, 2020).
Interpretatie
Binnen de algemene populatie zijn TSH-waarden lognormaal verdeeld (Hollowoell, 2002). Binnen een individu ligt het TSH-referentiegebied nauwer onder fysiologische omstandigheden (Hadlow, 2013). Zaken als tijdstip op de dag en vasten kunnen leiden tot fysiologische veranderingen binnen één individu.
Een verhoogde serum TSH-concentratie wijst meestal op een tekort aan schildklierhormoon. De oorzaak is bijna altijd in de schildklier gelegen. Een verhoogde serum TSH-concentratie die gepaard gaat met een verlaagde FT4-concentratie past bij een primaire hypothyreoïdie. Een verlaagde serum TSH-concentratie die gepaard gaat met een verhoogde FT4-concentratie past bij een thyreotoxicose. Een verhoogde of verlaagde serum TSH-concentratie met een normaal serum FT4 past respectievelijk bij een subklinische hypo- of hyperthyreoïdie.
Bij een centrale hypothyreoïdie kan echter ook een verhoogde TSH-waarde (tot 15 mIU/L) voorkomen (Persani, 2000); een veranderde glycosylering van het TSH-molecuul leidt tot een TSH dat minder bioactief is. Een verhoogd TSH kan ook uiting zijn van een TSH-oma, hetgeen dan gepaard gaat met verhoogde FT4-concentraties. (Figuur 1 laat veel voorkomende combinaties en de interpretatie zien).
Andere factoren kunnen de productie of secretie van TSH beïnvloeden (zie tabel 1).
Verder kan een verhoogd TSH het gevolg zijn van macro-TSH. Dit is het gevolg van binden van TSH aan immuunglobulines, vergelijkbaar met macro-prolactine. Belangrijk is te weten dat macro-TSH frequent voorkomt in de populatie die wordt verdacht van subklinische hypothyreoïdie (0.5 tot 3.0%, afhankelijk van de populatie) (Mills, 2013; Giusti, 2017; Hattori, 2016; Hattori, 2015). PEG precipitatie is een veelgebruikt en relatief eenvoudig protocol om macro-TSH aan te tonen, waarbij het laboratorium de methode specifieke afkapwaarde dienst vast te stellen. Uiteraard kunnen ook andere antistoffen de uitslag beinvloeden zoals heterofiele of humaan-anti-muis antistoffen (HAMA) indien het detectieantilichaam in muizen is opgewerkt (Bolstad, 2013).
Uiteraard moet bij een niet verwachte combinatie van uitslagen nagegaan worden of er sprake is van interferentie in één of meerdere van de biochemische metingen. Een uitgebreid algoritme is beschreven (Favresse, 2018). Hierbij moet worden genoemd dat de interferentie van biotine in streptavidine/biotine afhankelijke methoden anno 2021 grotendeels is opgelost voor de gangbare immunochemische platforms (Moerman, 2020).
Als er sprake is van schildklierhormoon antistoffen is het vaak assay specifiek, en geeft herhaalde meting op een tweede platform vaak een juiste uitslag (Zouwail, 2008). De overige vormen van interferentie komen minder vaak tot zelden voor, of zijn methode specifiek (e.g. ruthenium antistoffen vormen enkel in de Elecsys assay een probleem).
Tabel 1 Effecten van geneesmiddelen op analytische en pre-analytische factoren van belang bij de interpretatie van biochemische parameters in het kader van de diagnostiek van stoornissen in de schildklierhormoonhuishouding

* karakteristieke veranderingen in TSH en FT4
# alleen relevant bij patiënten die behandeld worden met LT4
Figuur 1 Biochemische bepalingen bij schildklierfunctiestoornissen
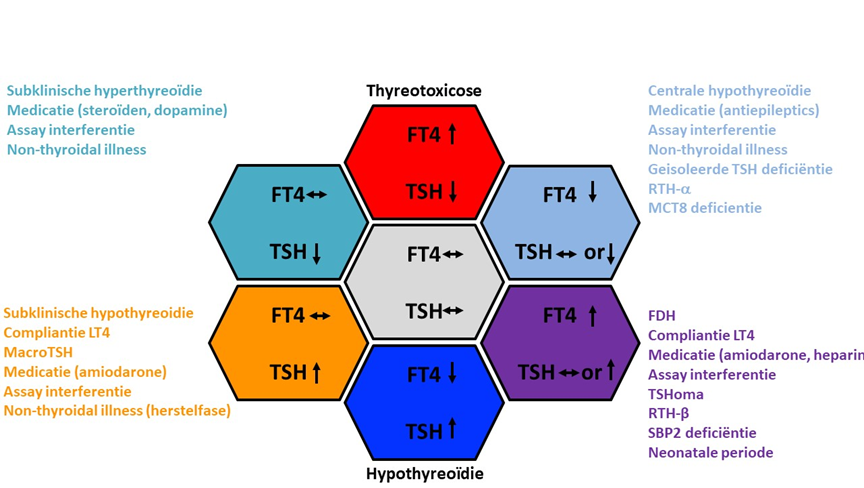
FT4
Wanneer FT4 bepalen?
Wanneer sprake is van een afwijkende TSH-concentratie of bij een klinisch sterk vermoeden op een zeldzame schildklierfunctiestoornis of hypofysedysfunctie, is bepaling van de FT4-concentratie in het serum van belang. De vrije hormoonfractie is beschikbaar voor opname in de weefsels en omzetting naar het bioactieve hormoon T3.
Assays
Voor FT4 is een referentie methode beschikbaar (van Houcke, 2011) (evenwichtsdialyse, gevolgd door isotoop dilutie vloeistofchromatografie - massaspectrometrie) en een gedefinieerd referentie interval voor volwassenen (13,5 tot 24,3 pM). FT4 wordt echter in het merendeel van de laboratoria met een competitieve immunoassay gemeten. Wanneer het laboratorium niet de referentie methode voert is het van belang dat de juiste referentie-intervallen gehanteerd worden want er zijn grote verschillen in de kalibratie van de methoden (de Grande, 2017). Het overnemen van referentie-intervallen zoals deze door de fabrikant van de test worden aangeleverd (bijvoorbeeld. uit een bijsluiter) is niet voldoende (ISO15189:2012, normelement 5.5.2). Immers, de bias van een methode ten opzichte van de referentie methode wordt niet altijd gereflecteerd in de meegeleverde referentie-intervallen (de Grande, 2017).
Interpretatie (danwel interferentie)
Binnen 1 persoon zijn FT4 en TSH aan elkaar gekoppeld (Hadlow, 2013).
Een verhoogde serum FT4-concentratie die gepaard gaat met een verlaagde TSH-concentratie past bij een thyreotoxicose. Een verlaagde serum FT4-concentratie die gepaard gaat met een verhoogde TSH-concentratie past bij een primaire hypothyreoïdie.
Ongebruikelijk is een situatie waarbij de serum FT4-concentratie verhoogd of verlaagd is bij een normale TSH-concentratie. Een verhoogde serum FT4-concentratie met een normaal TSH-concentratie kan uiting zijn van analytische interferenties. Dit dient eerst te worden uitgesloten alvorens verder onderzoek wordt gedaan. Antistoffen tegen schildklier hormoon (T3 en T4) zijn relatief prevalent (13% in een cohort met hematologische maligniteiten onder behandeling met TK inhibitors (Mondello, 2016), 5% in zwangere vrouwen (Benvenga, 2019), maar vormen zelden een bron van interferentie. Alternatieve verklaringen zijn een TSH-producerend hypofyseadenoom, FDH (familiale dysalbuminemische hyperthyroxinemie) of schildklierhormoonresistentie (ten gevolge van een mutatie in THRB; resistance to thyroid hormone beta (RTH-b)). In FDH, een entiteit die het gevolg is van een mutatie in albumine, leidt in de meeste assays tot een verhoogde serum FT4-concentratie. Heparine en low-molecular weight heparin (LMWH) kunnen leiden tot een toename in vrije vetzuurconcentraties, hetgeen meer uitgesproken wordt in omstandigheden waarbij er hoge triglyceridenconcentraties zijn, die T4 verdringen van het TBG in vitro, resulterend in verhoogde FT4-concentraties in vitro. Bij een onverwacht hoge FT4-concentratie en verdenking op heparine interactie kan totaal T4 gemeten worden; dit is dan niet afwijkend. Een verlaagde serum FT4-concentratie met een normale TSH-concentratie kan uiting zijn van een centrale hypothyreoïdie (Figuur 1). Tevens kan dit uiting zijn van interferentie van medicamenten in de assays (Tabel 1).
T3
Wanneer T3 bepalen?
Het bepalen van de (F)T3-concentratie is alleen in specifieke gevallen aangewezen. De (F)T3-concentratie kan in bepaalde gevallen behulpzaam zijn bij de differentiaal diagnose (bijvoorbeeld onderscheid tussen M. Graves versus thyreoiditis). Bij een onmeetbaar laag TSH met FT4-concentraties binnen het referentieinterval is een (F)T3 bepaling zeker relevant om te onderzoeken of er sprake is van T3-toxicose. De (F)T3-concentratie is ook van toegevoegde waarde wanneer aan een van de schildklierhormoonresistentiesyndromen wordt gedacht.
Assays
Voor T3 is een referentie methode beschikbaar (Thienpont, 2005) (isotoop dilutie vloeistofchromatografie – massaspectrometrie), maar er is geen gedefinieerd of geharmoniseerd referentie interval beschikbaar. Het is dan ook belangrijk dat ieder laboratorium zich er van vergewist het juiste interval te gebruiken. Voor FT3 is geen referentie methode en gedefinieerd/geharmoniseerd referentieinterval beschikbaar, en ook daar is het belangrijk dat ieder laboratorium zich er van vergewist het juiste interval te gebruiken.
Interpretatie (danwel interferentie)
In situaties waarin de serum TSH-concentratie is verlaagd en de serum concentratie FT4 normaal is, kan het serum (F)T3-concentratie bepaald worden. Een verlaagde serum TSH-concentratie met normale FT4-concentratie kan passen bij een T3-toxicose. T3-toxicose kan voorkomen bij een autonome nodus, een multinodulair struma en een beginnende M. Graves. Biochemisch wordt dit gekenmerkt door een verhoogd (F)T3 in combinatie met een onderdrukt TSH en normaal FT4 bij een T3 toxicose. In de context van bepaalde klinische verschijnselen is een verhoogde serum T3-concentratie met een verlaagde of laag-normale serum FT4-concentratie en een normale serum TSH-concentratie passend bij MCT8 deficiëntie. Daarnaast leidt schildklierhormoonresistentie ten gevolge THRA mutatie tot specifieke klinische verschijnselen. Biochemisch wordt dit beeld gekenmerkt door een veranderde (F)T3/(F)T4 ratio waarbij (F)T3 verhoogd en (F)T4 verlaagd is bij een niet afwijkend TSH. Een verlaagde serum (F)T3-concentratie bij een normaal of verhoogde serum FT4-concentratie kan passen bij een minder efficiënte omzetting van T4 naar T3. Dit kan passen bij gebruik van amiodaron, propranolol of steroïden. Uiteraard kan ook in de (F)T3 bepaling interferentie optreden; deze zijn vaak gelijk van aard en presentatie als interferenties in de (F)T4 bepaling. Zoals benoemd zijn antistoffen tegen schildklier hormoon relatief prevalent maar vormen zelden een bron van interferentie (zie voor meer informatie de interpretatie paragraaf FT4).
Onderbouwing
Bij het vermoeden van een stoornis in de schildklierhormoonhuishouding staan verschillende methoden ter beschikking. In deze module bespreken we wanneer thyreoïdstimulerend hormoon (TSH), vrij thyroxine (FT4) en triiodothyronine (T3) bepaald moeten worden, de assays en de interpretatie daarvan. Deze module is voornamelijk gericht op de diagnostiek van schildklierfunctiestoornissen.
Er is geen systematische literatuuranalyse uitgevoerd om de uitgangsvraag te beantwoorden, maar deze module is opgezet op basis van expert opinie.
- 1 - Barth, J. H., Luvai, A., Jassam, N., Mbagaya, W., Kilpatrick, E. S., Narayanan, D., & Spoors, S. (2018). Comparison of method-related reference intervals for thyroid hormones: studies from a prospective reference population and a literature review. Annals of clinical biochemistry, 55(1), 107-112.
- 2 - Benvenga, S., Vita, R., Di Bari, F., Re, C. L., Scilipoti, A., Giorgianni, G.,... & Le Donne, M. (2019). Assessment of serum thyroid hormone autoantibodies in the first trimester of gestation as predictors of postpartum thyroiditis. Journal of clinical & translational endocrinology, 18, 100201.
- 3 - Bolstad, N., Warren, D. J., & Nustad, K. (2013). Heterophilic antibody interference in immunometric assays. Best practice & research Clinical endocrinology & metabolism, 27(5), 647-661.
- 4 - De Grande, L. A., Van Uytfanghe, K., Reynders, D., Das, B., Faix, J. D., MacKenzie, F.,... & Thienpont, L. M. (2017). Standardization of free thyroxine measurements allows the adoption of a more uniform reference interval. Clinical chemistry, 63(10), 1642-1652.
- 5 - Favresse, J., Burlacu, M. C., Maiter, D., & Gruson, D. (2018). Interferences with thyroid function immunoassays: clinical implications and detection algorithm. Endocrine reviews, 39(5), 830-850.
- 6 - Giusti, M., Conte, L., Repetto, A. M., Gay, S., Marroni, P., Mittica, M., & Mussap, M. (2017). Detection of polyethylene glycol thyrotropin (TSH) precipitable percentage (macro-TSH) in patients with a history of thyroid cancer. Endocrinology and Metabolism, 32(4), 460.
- 7 - Hadlow, N. C., Rothacker, K. M., Wardrop, R., Brown, S. J., Lim, E. M., & Walsh, J. P. (2013). The relationship between TSH and free T4 in a large population is complex and nonlinear and differs by age and sex. The Journal of Clinical Endocrinology & Metabolism, 98(7), 2936-2943.
- 8 - Hattori, N., Ishihara, T., & Shimatsu, A. (2016). Variability in the detection of macro TSH in different immunoassay systems. Eur J Endocrinol, 174(1), 9-15.
- 9 - Hattori, N., Ishihara, T., Yamagami, K., & Shimatsu, A. (2015). Macro TSH in patients with subclinical hypothyroidism. Clinical endocrinology, 83(6), 923-930.
- 10 - Hollowell, J. G., Staehling, N. W., Flanders, W. D., Hannon, W. H., Gunter, E. W., Spencer, C. A., & Braverman, L. E. (2002). Serum TSH, T4, and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). The Journal of Clinical Endocrinology & Metabolism, 87(2), 489-499.
- 11 - Kratzch, J, Fiedler, G. M., Leichtle, A., Brugel, M., Buchbinder, S., Otto, L.,... & Thiery, J. (2005). New reference intervals for thyrotropin and thyroid hormones based on National Academy of Clinical Biochemistry criteria and regular ultrasonography of the thyroid. Clinical chemistry, 51(8), 1480-1486.
- 12 - Mills, F., Jeffery, J., Mackenzie, P., Cranfield, A., & Ayling, R. M. (2013). An immunoglobulin G complexed form of thyroid-stimulating hormone (macro thyroid-stimulating hormone) is a cause of elevated serum thyroid-stimulating hormone concentration. Annals of clinical biochemistry, 50(5), 416-420.
- 13 - Moerman, A., & R. Delanghe, J. (2020). Sense and nonsense concerning biotin interference in laboratory tests. Acta Clinica Belgica, 1-7.
- 14 - Mondello, P., Mian, M., Pitini, V., Cuzzocrea, S., Sindoni, A., Galletti, M.,... & Benvenga, S. (2016). Thyroid hormone autoantibodies: are they a better marker to detect early thyroid damage in patients with hematologic cancers receiving tyrosine kinase inhibitor or immunoregulatory drug treatments?. Current Oncology, 23(3), e165.
- 15 - Naafs, J. C., Heinen, C. A., Zwaveling-Soonawala, N., van der Schoor, S. R., van Tellingen, V., Heijboer, A. C.,... & van Trotsenburg, A. P. (2020). Age-Specific Reference Intervals for Plasma Free Thyroxine and Thyrotropin in Term Neonates During the First Two Weeks of Life. Thyroid, 30(8), 1106-1111.
- 16 - Persani, L., Ferretti, E., Borgato, S., Faglia, G., & Beck-Peccoz, P. (2000). Circulating thyrotropin bioactivity in sporadic central hypothyroidism. The Journal of Clinical Endocrinology & Metabolism, 85(10), 3631-3635.
- 17 - Rege, V., Mojiminiyi, O., Wilcox, H., & Barron, J. (1996). Comparison of Kodak Amerlite FT4 and TSH-30 with T4 and TSH as first-line thyroid function tests. Clinical biochemistry, 29(1), 1-4.
- 18 - Spencer, C. A. (2017). Assay of thyroid hormones and related substances. Endotext (Internet).
- 19 - Thienpoint, L. M., Van Uytfanghe, K., Marriot, J., Stokes, P., Siekmann, L., Kessler, A.,... & Tai, S. (2005). Metrologic traceability of total thyroxine measurements in human serum: efforts to establish a network of reference measurement laboratories. Clinical chemistry, 51(1), 161-168.
- 20 - Thienpont, L. M., Van Uytfanghe, K., De Grande, L. A., Reynders, D., Das, B., Faix, J. D.,... & Williams, P. (2017). Harmonization of serum thyroid-stimulating hormone measurements paves the way for the adoption of a more uniform reference interval. Clinical chemistry, 63(7), 1248-1260.
- 21 - Van Houcke, S. K., Van Uytfanghe, K., Shimizu, E., Tani, W., Umemoto, M., Thienpont, L. M. (2011). IFCC international conventional reference procedure for the measurement of free thyroxine in serum. Clin Chem Lab Med, 49, 1275-81.
- 22 - Wiersinga, W. M. (1986). The value of sensitive TSH measurements in clinical practice. Journal of endocrinological investigation, 9, 67-76.
- 23 - Wiersinga, W. M. (2003). The interpretation of the thyroid stimulating hormone (TSH) assay. Nederlands tijdschrift voor geneeskunde, 147(24), 1156-1158.
- 24 - Zouwail, S. A., O’Toole, A. M., Clark, P. M., & Begley, J. P. (2008). Influence of thyroid hormone autoantibodies on 7 thyroid hormone assays. Clinical chemistry, 54(5), 927-928.
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-05-2022
Beoordeeld op geldigheid : 01-11-2021
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2026 bepaalt het bestuur van de NIV of de modules van deze richtlijn nog actueel zijn. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NIV is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Deze richtlijn is goedgekeurd door:
- Nederlands Huisartsen Genootschap
- Schildklier Organisatie Nederland
Doel en doelgroep
Doel
Deze richtlijn geeft aanbevelingen ten aanzien van behandeling van volwassen patiënten (leeftijd ≥ 18 jaar) met schildklierfunctiestoornissen. Doel van deze gedeeltelijke herziening is om een richtlijn te verkrijgen waarin de meeste recente medische kennis omtrent de zorg voor patiënten met schildklierfunctiestoornissen wordt meegenomen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met schildklierfunctiestoornissen.
Werkgroep
- Prof. dr. E. Fliers (voorzitter vanaf 1 mei 2019), internist-endocrinoloog, NIV
- Prof. dr. R. Peeters (voorzitter tot 1 mei 2019), internist-endocrinoloog, NIV
- Dr. W.E. Visser, internist-endocrinoloog, NIV
- Dr. A. Roos, internist-endocrinoloog, NIV
- Dr. M. Medici, internist-endocrinoloog, NIV
- Dr. A.F. Muller, internist-endocrinoloog, NIV
- Prof. dr. O.M. Dekkers, internist-endocrinoloog en klinisch epidemioloog, NIV
- Dr. A.A. Bouman, SON
- Dr. M.M.E. van Rumste, gynaecoloog, NVOG (vanaf 1 april 2019)
- Drs. M. Sijbom, huisarts, NHG (vanaf 1 juli 2019)
- Dr. S.A.A van den Berg, klinisch chemicus, NVKC (vanaf 1 augustus 2019)
- Drs. J.H. Scheffer, bedrijfsarts, NVAB (vanaf 1 september 2020)
Met ondersteuning van
- Drs. L. Boerboom, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.R. Zwakenberg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. N.L. van der Zwaluw, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.J. Versteeg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met evt. belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Prof. dr. E. Fliers, internist-endocrinoloog, NIV (voorzitter vanaf 1-5-2019) |
Hoofd- afdeling Endocrinologie en Metabolisme, Amsterdam UMC, Hoogleraar Endocrinologie UvA |
Board memberships, committees: - ETA guideline committee diagnosis and management of central hypothyroidism (2017-2018) - Executive Committee European Thyroid Association (tot 2019) - Program organizing committee ETA Annual Meeting 2017, 2018, 2019 - Member Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Voorzitter Medische Adviesraad Schildklier Organisatie Nederland (SON) |
Geen |
Geen |
|
Prof. dr. R. Peeters, internist-endocrinoloog, NIV (voorzitter tot 1-05-2019) |
Erasmus MC, Internist-endocrinoloog, hoogleraar schildklierziekten |
Member of International guideline committees: American Thyroid Association Task Force: Guidelines for thyroid disease and pregnancy (not remunerated)
Board memberships and committees of professional societies: - Programme Organizing Committee of the 2019 European Congress of Endocrinology. 2018 Annual Meeting of the American Thyroid Association - Iodine Global Network (https://www.ign.org/), National representative for the Netherlands (not remunerated) - Chair of the Scientific Advisory Board of the World Iodine Association (not remunerated) - Treasurer of the Dutch Thyroid Club / Foundation for Thyroid Research (not remunerated) |
Zie transparantieregister voor financiële banden (red: diverse diensten met onkosten) vergoeding van Shire International licenising, Genzyme Europe BV, Ipsen Farmaceutica BV, Merck BV, IBSA, Bayer, - Adviesraad Eisai BV (vergoeding) |
Vergoedingen waren niet gerelateerd aan de richtlijn
|
|
Dr. W.E. Visser, internist-endocrinoloog, NIV |
Erasmus MC, Internist-endocrinoloog |
Member of international committees - European Thyroid Association Task Force: Guideline on Diagnosis and Management of Resistance to Thyroid Hormone & other disorders of thyroid hormone action (2016 - present) - Educational Committee of the European Thyroid Association (2017 - present) - Chair Thyroid Network of Dutch Endocrine Society (NVE) (2017 - present)
Editorial Board membership - Editorial Board of Frontiers in Neurogenomics (2013 - present) - Editorial Board of the Journal of Endocrinology (2016 - present) - Editorial Board of the Journal of Molecular Endocrinology (2016 - present) - Editorial Board of the Endocrinology, Diabetes and Metabolism (2016 - present) - Editorial Board of the European Thyroid Journal (2017 - present)
Management role in International Consortia - Founder and chair MCT8 patient registry (2016 - present). - Chair rare thyroid hormone signalling disorders in Endo-ERN (European Reference Networks) (2016 - present) - Chair Thyroid Group of Endo-ERN EuRRECa (2018 - present)" |
Geen |
Vergoedingen niet gerelateerd aan richtlijn (diabetes, schildklierkanker) |
|
Dr. A. Roos, internist-endocrinoloog, NIV |
Internist-endocrinoloog Martini Ziekenhuis, Groningen |
Geen |
Geen |
Geen |
|
Dr. M. Medici, internist-endocrinoloog, NIV |
Internist-Endocrinoloog radboudUMC (0,6 fte) en Erasmus MC (0,4 fte) |
Management role in International Consortia
Memberships (inter)national committees:
Editorial Board memberships:
|
Erasmus Universiteit Fellowship: geen belang bij het advies van de richtlijn. |
Geen |
|
Dr. A.F. Muller, internist-endocrinoloog, NIV |
Internist, Diakonessenhuis |
Zie transparantieregister (red: diverse diensten met (onkosten)vergoeding voor Novo Nordisk, Eli Lilly and Company (adviesraad), Amgen, Sanofi) |
|
Vergoedingen waren niet gerelateerd aan de richtlijn (diabetes, schildklierkanker)
|
|
Prof. dr. O.M. Dekker, internist, NIV |
Hoogleraar Interne Geneeskunde LUMC Leiden |
Collegelid CBG (betaald) Lid Gezondheidsraad (onbetaald) Voorzitter Vereniging Epidemiologie (onbetaald)" |
Geen |
Geen |
|
Dr. A.A. Bouman, SON |
Gepensioneerd (tot 1-9-2012 werkzaam als Klinisch chemicus bij het Vumc) |
Geen |
Geen |
Geen |
|
Drs. J.H. Scheffer, NVAB |
Bedrijfsarts |
Geen |
Geen |
Geen |
|
Dr. M.M.E. van Rumste, gynaecoloog, NVOG |
Gynaecoloog, Catherinaziekenhuis |
Geen |
Geen |
Geen |
|
Drs. M. Sijbom, huisarts, NHG |
Huisarts |
Geen |
Geen |
Geen |
|
Dr. S.A.A van den Berg, klinisch chemicus, NVKC |
Klinisch Chemicus, Erasmus MC |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden van de patiëntenvereniging Schildklier Organisatie Nederland (SON). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging.
Methode ontwikkeling
Consensus based
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (Richtlijn schildklierfunctiestoornissen, 2012) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door middel van een schriftelijke invitational conference. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg en patiëntveiligheid.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep en de adviseur concept-uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De gespecificeerde zoekstrategieën zijn op te vragen bij het Kennisinstituut.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: Cochrane - voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS - voor observationeel onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (eindconclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een eindconclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg. De module over organisatie van zorg wordt opgenomen in deel 2 van de richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialist.
