Schildkliercarcinoom - 131I na thyreoïdectomie
Uitgangsvraag
Dosis 131I na thyreoïdectomie: welke dosis radioactief jodium moet worden gebruikt voor ablatie bij patiënten met een gedifferentieerd schildkliercarcinoom die een totale thyreoïdectomie hebben ondergaan?
Stimulatie met recombinant humaan TSH versus onttrekking: wanneer is voorbehandeling met recombinant-humaan TSH geïndiceerd en wanneer voorbehandeling middels onttrekken van thyroxine ter ablatie met radioactief jodium na totale thyreoidectomie?
Aanbeveling
Dosis 131I na thyreoïdectomie
De werkgroep adviseert om patiënten met een unifocaal T1-2folliculair of klassiek papillair schildkliercarcinoom bij wie het schildkliercarcinoom volledig verwijderd is, zonder lymfekliermetastasen in situ na de operatie, of met uitsluitend verwijderde lymfekliermetastasen in level VI zonder extranodale groei in eventueel verwijderde lymfekliermetastasen en die geen afstandmetastasen hebben, te behandelen met 1,1 GBq 131I voor ablatie in plaats van met 3,7 GBq.
Stimulatie met recombinant humaan TSH versus onttrekking
De werkgroep is van mening dat bij patiënten met een unifocaal T1-2 folliculair of klassiek papillair schildkliercarcinoom bij wie het schildkliercarcinoom volledig verwijderd is, zonder lymfekliermetastasen in situ na de operatie en zonder extranodale groei in eventueel verwijderde lymfekliermetastasen en die geen afstandmetastasen hebben, de ablatie verricht kan worden zowel na stimulatie met rhTSH als na onttrekken van schildklierhormoon.
Er zijn onvoldoende gegevens voor patiënten met multifocale tumoren, T3-4 tumoren, achtergebleven tumor, andere histologie dan folliculair of klassiek papillair schildkliercarcinoom, lymfekliermetastasen in situ na operatie, extranodale groei in verwijderde lymfekliermetastasen, of afstandsmetastasen om een onderbouwde uitspraak te doen over de ablatie. Er wordt geadviseerd ablatietherapie na onttrekken van schildklierhormoon te geven, tenzij vanwege comorbiditeit hypothyreoïdie slecht verdragen wordt.
Overwegingen
Dosis 131I na threoÏdectomie
In bovengenoemde studies werd geen verschil gevonden in ablatie tussen een lage of hoge ablatiedosis. Omdat meerdere studies niet-statistisch significant verschillende maar toch net iets lagere ablatiesuccessen lieten zien voor de laaggedoseerde therapiegroep is het mogelijk dat er toch een klein verschil zou kunnen zijn dat statistisch significant zou kunnen worden bij grotere studies. Een verklaring voor het feit dat dit verschil vaker ten nadele van de lage dosisgroep uitvalt is de definitie van behandelsucces. Studies die het criterium ‘geen uptake in de hals op een speurdosis 131I scintigram' gebruiken als onderdeel van de definitie van behandelsucces laten vaker een niet-significant (en bij een studie wel statistisch significant [Fallahi, 2012 (2)] lagere kans op ablatiesucces zien. Een speurdosis retentiescintigram tijdens de follow-up is echter niet meer standaard voor responsevaluatie en risicoclassificatie en is niet zo belangrijk als succescriterium. Een zeer geringe hoeveelheid benigne restschildklierweefsel op het scintigram is namelijk niet klinisch relevant.
Belangrijke overwegingen die in ogenschouw genomen moeten worden zijn de mate waarin het mogelijk is de resultaten van deze studies naar de Nederlandse situatie te extrapoleren en het feit dat er nog geen lange termijn follow-up is. Bovengenoemde studies zijn met name uitgevoerd in gespecialiseerde schildkliercarcinoomcentra waar de patiënten routinematig pre-operatief goed worden gescreend op de aanwezigheid van lymfekliermetastasen, waar goede thyreoidectomieën worden uitgevoerd (dus geringe of zelfs helemaal geen benigne schildklierrest) en waar laagdrempelig, goede halsklierdissecties worden verricht. De sensitiviteit van de pre-operatieve diagnostiek is afhankelijk van de ervaring van de beeldvormer, en vanwege de lage prevalentie van schildkliercarcinoom is de sensitiviteit van beeldvormers in kleinere niet-gespecialiseerde centra meestal lager. Ook de uitgebreidheid en radicaliteit van de operatie zijn afhankelijk van de ervaring van het chirurgisch team met schildkliercarcinoom en zijn in gespecialiseerde centra over het algemeen beter. Derhalve kunnen de resultaten van de studies niet zonder meer naar de Nederlandse situatie worden geëxtrapoleerd.
Verder zijn er nog geen lange-termijn data van de studies, dus kan alleen nog worden geconcludeerd dat onder genoemde voorwaarden er geen verschil in succeskans van de ablatie is, maar kunnen er nog geen definitieve uitspraken worden gedaan over de recidiefkans. Het is immers mogelijk (maar nooit aangetoond, danwel uitgesloten) dat de schildklierestablatie bij sommige patiënten ook micrometastasen behandelt en de effectiviteit daarvan zou wel kunnen verschillen tussen de lage en hoge dosis. Deze informatie zal beschikbaar komen tijdens de follow-up van de grote gerandomiseerde studies.
Er zijn echter wel voordelen aan het behandelen met een lagere dosis 131I: door met een lagere dosis 131I te behandelen kan de opnameduur worden verkort, hetgeen prettiger is voor de patiënt en kosten reduceert.
Behandeling met een lagere dosis 131I leidt tot een lagere stralingsbelasting voor het lichaam: 1,1 GBq 131I geeft een effectieve dosis van 80 mSv en 3,7 GBq een effectieve dosis van 270 mSv. Door verlaging van de lichaamsdosis, wordt het (toch al lage) risico op het ontwikkelen van een secundaire maligniteit ten gevolge van de stralingsexpositie nog lager.
De frequentie en de ernst van acute bijwerkingen (bijv. sialoadenitis, misselijkheid, smaakstoornissen) zijn dosisafhankelijk en worden lager bij behandeling met een kleinere hoeveelheid radioactief jodium. Ook het effect van 131I therapie op de semenkwaliteit bij mannen is dosisafhankelijk en duidelijk waarneembaar als een voorbijgaande stijging van het FSH, en is kleiner bij een lagere dosering131I, hoewel hiervoor geldt dat ook na eenmalig 3,7 GBq 131I zelden een persisterend verhoogde FSH- spiegel ontstaat.
De werkgroep is zich er van bewust dat naast deze discussie om de ablatiedosis te verlagen er tevens internationaal onderzoek gaande is om te beoordelen of 131I ablatie bij laag-risicopatiënten helemaal achterwege kan blijven. Het is voorstelbaar dat onder de voorwaarden van goede pre-operatieve diagnostiek en goede chirurgische interventie bij laag-risicopatiënten de ablatie met radioactief jodium helemaal kan worden weggelaten. Het is nu echter nog te vroeg om dat te concluderen.
Bij patiënten met multifocale tumoren, T3-4-tumoren, achtergebleven tumorrest, andere histologie dan folliculair of klassiek papillair schildkliercarcinoom, lymfekliermetastasen in situ na de operatie, verwijderde lymfekliermetastasen met extranodale groei of afstandmetastasen zijn er onvoldoende gegevens om de optimale dosis 131I voor ablatie te bepalen. Deze groep is nogal heterogeen en het is raadzaam individueel te kijken naar de beste behandeling, waarbij ook heroperatie nog een optie is.
Stimulatie met recombinant humaan TSH versus onttrekking
Ook bij de vergelijking ablatie na stimulatie met rhTSH vs. onttrekken van schildklierhormoon gelden de reeds bij de vergelijking hoge vs. lage dosis 131I genoemde restricties. Belangrijkste restrictie is dat deze data met name afkomstig zijn uit gespecialiseerde schildkliercarcinoomcentra met zeer goede preoperatieve diagnostiek en zeer goede chirurgische interventies, waarbij alleen relatief laagrisicopatiënten werden geïncludeerd. Daarnaast was er geen uniforme definitie van ablatiesucces. Deze data zijn niet zonder meer valide in andere klinische settings.
Daarnaast is alleen nog de korte termijn uitkomst (ablatie) bekend en zijn er geen lange termijn follow-up gegevens, waardoor niet duidelijk is of de recidiefkansen ook vergelijkbaar zijn. Het is immers mogelijk dat de schildklierestablatie bij sommige patiënten ook micrometastasen behandelt, dus eigenlijk een adjuvante therapie is (hoewel dit voor de meeste patiëntgroepen niet is aangetoond/uitgesloten) en de effectiviteit daarvan zou in theorie kunnen verschillen tussen rhTSH-stimulatie of onttrekken van schildklierhormoon. Onder genoemde restricties heeft deze patiëntgroep echter sowieso een relatief lage recidiefkans.
Behandeling met rhTSH heeft enige voordelen boven onttrekken van schildklierhormoon, maar met name op de korte termijn, rondom de ablatie. Het belangrijkste voordeel is dat de patiënt niet hypothyreoot hoeft te zijn voor de therapie met 131I. Hypothyreoïdie is geassocieerd met een lagere kwaliteit van leven. Daarnaast kan na rhTSH-stimulatie de ablatie enkele weken eerder worden gedaan, hetgeen medisch geen verschil maakt maar door sommige patiënten als plezieriger kan worden ervaren. Verder is de stralingsbelasting voor het lichaam iets lager doordat de renale klaring van 131I sneller verloopt in euthyreoïdie dan in hypothyreoïdie.
Bij patiënten met multifocale tumoren, T3-4 tumoren, achtergebleven tumor, andere histologie dan folliculair of klassiek papillair schildkliercarcinoom, lymfekliermetastasen in situ na operatie, extranodale groei in verwijderde lymfekliermetastasen, of afstandmetastasen zijn er onvoldoende gegevens om een evidence based uitspraak te doen over de ablatie. Derhalve wordt geadviseerd bij deze patiënten ablatietherapie na onttrekken van schildklierhormoon te geven, tenzij vanwege comorbiditeit hypothyreoïdie slecht verdragen wordt.
Onderbouwing
Conclusies
Dosis 131I na threoÏdectomie
Het is aangetoond dat een lage (1,1 of 1,85 GBq) of een hoge ablatiedosis 131I (3,7 GBq) niet leidt tot een verschil in adequate ablatie bij patiënten met een T1-2folliculair of klassiek papillair schildkliercarcinoom, mits het schildkliercarcinoom volledig is verwijderd, en er geen lymfekliermetastasen in situ zijn na de operatie, en de eventueel verwijderde lymfekliermetastasen geen extranodale groei vertoonden én er geen afstandmetastasen zijn.
Niveau2:A2 Fallahi 2012 (15); B Mallick 2012 (16), Maenpaa 2008 (3), Schlumberger 2012 (4), Johansen 1991 (5), Caglar 2012 (6), Pilli 2007 (7), Zaman 2006 (8), Bal 2012 (10), Bal 1996
Bij patiënten met multifocale tumoren, met T3-4-tumoren, met achtergebleven tumor na de operatie, andere histologie dan folliculair of klassiek papillair, met lymfekliermetastasen in situ na de operatie, of verwijderde lymfekliermetastasen met extranodale groei of afstandmetastasen ten tijde van de schildklierrest ablatie zijn er onvoldoende gegevens om verschillende doseringen 131I met elkaar te vergelijken.
Niveau 4:Mening van de werkgroep
Stimulatie met recombinant humaan TSH versus onttrekking
Het is aannemelijk dat rhTSH of onttrekking van schildklierhormoon niet leidt tot een verschil in adequate ablatie bij patiënten met een T1-2 folliculair of klassiek papillair schildkliercarcinoom mits het schildkliercarcinoom volledig is verwijderd en er geen lymfekliermetastasen in situ zijn na de operatie en er geen extranodale groei is in de evt. verwijderde lymfekliermetastasen en er geen afstandmetastasen zijn.
Mallick 2012 (3), Lee 2010 (17), Schlumberger 2012 (4), Taieb 2009 (14)
Bij patiënten met multifocale tumoren, T3-T4-tumoren, met achtergebleven tumor, andere histologie dan folliculair of klassiek papillair, lymfekliermetastasen in situ na de operatie, met verwijderde lymfekliermetastasen met extranodale groei, of afstandmetastasen in situ ten tijde van de ablatie zijn er onvoldoende gegevens om rhTSH met onttrekking van schildklierhormoon te vergelijken voor de effectiviteit van ablatie.
Mening van de werkgroep
Samenvatting literatuur
131I na threoÏdectomie
Het primaire doel van de ablatietherapie is het verwijderen van het na de thyreoïdectomie nog resterende schildklierweefsel. Bij vrije snijranden van het resectiepreparaat bij een unifocale tumor betreft dit in principe benigne schildklierweefsel. Als de snijranden niet vrij zijn is er sprake van therapie van rest-schildkliercarcinoom en niet alleen van ablatie. Daarnaast zou het zo kunnen zijn dat met de ablatietherapie ook micro-metastasen worden behandeld (hoewel dat voor de meeste patiëntgroepen niet is aangetoond, maar ook niet is uitgesloten). Dan is er eigenlijk sprake van adjuvante therapie. De grens tussen ablatie en adjuvante therapie is niet duidelijk. Bij duidelijke metastasen is er uiteraard sprake van therapie en niet alleen van ablatie.
Tien gerandomiseerde studies vergeleken het effect van een lage dosis 131I met een hoge dosis 131I als ablatietherapie na een thyreoïdectomie voor een niet-gemetastaseerd gedifferentieerd schildkliercarcinoom [Mallick 2012, Fallahi 2012, Maenpaa 2008, Schlumberger 2012, Johansen 1991, Caglar 2012, Pilli 2007, Zaman 2006, Bal 2012, Bal 1996 (1) (2) (3) (4) (5) (6) (7) (8) (9) (10)]. In totaal werden 2598 patiënten gerandomiseerd. De volgende ablatiedosissen werden vergeleken:
- 30 mCi (1110 MBq) vs. 100 mCi (3700 MBq) [Mallick 2012, Fallahi 2012, Maenpaa 2008, Schlumberger 2012 (1) (2) (3) (4)],
- 29 mCi (1073 MBq) vs. 100 mCi [Johansen 1991 (5)],
- 25 mCi (925 MBq) vs. 50 mCi (1850 MBq) vs. 100 mCi [Bal 2012 (9)],
- 21,6 mCi (800 MBq) vs. 100 mCi [Caglar 2012 (6)],
- 50 mCi vs. 100 mCi [Pilli 2007, Zaman 2006 (7) (8)].
Twee recente studies gebruikten een 2x2-factorial design, waarbij de geïncludeerde patiënten enerzijds gerandomiseerd werden naar stimulatie met recombinant humaan TSH of onttrekking van schildklierhormoon, en anderzijds naar een lage (30 mCi) of een hoge ablatiedosis 131I (100 mCi) [Mallick 2012, Schlumberger 2012 (1) (4)].
In vier studies werd de methode van randomisatie niet beschreven [Caglar 2012, Johansen 1991, Pilli 2007, Zaman 2006 (6) (5) (7) (8)]. Slechts in één studie werden de patiënten en behandelaars expliciet geblindeerd [Fallahi 2012]. Twee studies waren open-label studies [Maenpaa 2008, Schlumberger 2012 (3) (4)], in de andere zeven studies werd blindering niet gerapporteerd. De definitie van adequate ablatie verschilde in belangrijke mate tussen de tien studies, dit zowel wat betreft de gebruikte criteria als het tijdstip van de evaluatie (zie Tabel 1). Daarnaast waren er ook verschillen in uitgebreidheid van voorafgaande chirurgie en het interval tussen chirurgie en ablatie.
De meerderheid van de studies vond geen significant verschil in adequate ablatie tussen een lage en hoge ablatiedosis. Alleen Fallahi vond een significant voordeel van 100 mCi ten opzichte van 30 mCi, zowel na 6 maanden (RR 0,61, 95%BI 0,49-0,76) als na 12 maanden (68,8% versus 41,5%, p<0.0001) [Fallahi 2012 (2)].
In de studie van Mallick werden de patiënten gerandomiseerd met stratificatie volgens centrum, T-stadium en N-stadium [Mallick 2012]. Bij patiënten met een T3-tumor (30 mCi: 80,9%; 100 mCi: 81,6%) of met positieve lymfeklieren in het resectiepreparataat (30 mCi: 86,7%; 100 mCi: 81,8%) werd geen significant verschil in adequate ablatie gevonden.
Bal et al. stratificeerden de patiënten volgens histologie en vonden geen significant verschil in adequate ablatie voor papillaire (25 mCi: 81,7%; 50 mCi: 85,5%; 100 mCi: 88,1%; p=0,446) of folliculaire carcinomen (25 mCi: 80,8%; 50 mCi: 81,0%; 100 mCi: 90,9%; p= 0,729) [Bal 2012 (9)].
Er is ook een meta-analyse verschenen die deze studies kritisch bespreekt [Cheng 2013 (11)].
Hoewel de inclusiecriteria in deze tien studies wat varieerden werd de inclusie over het algemeen beperkt tot T1-3-patiënten die na operatie in de meeste studies (met uitzondering van Maenpaa et al.) geen aanwijzingen hadden voor lymfekliermetastasen. In geen enkele studie waren er aanwijzingen voor metastasen op afstand. In meerdere studies werden zelfs reeds geïncludeerde patiënten weer geëxcludeerd als op de posttherapiescan verdenking was op lymfeklier- of afstandsmetastasen. In principe includeerden alle studies dus alleen relatief laag-risicopatiënten. Alleen in de studie van Maenpaa zijn wel patiënten met bekende lymfekliermetastasen in situ na de operatie geïncludeerd [Maenpaa 2008 (3)]. Bij slechts twee van deze 12 patiënten was de ablatie succesvol.
Als voor de drie grootste studies [Schlumberger 2012, Mallick 2012, Bal 2012 (4) (1) (9)] niet naar de inclusiecriteria gekeken wordt, maar naar de karakteristieken van de daadwerkelijk geïncludeerde patiënten blijken er vrijwel alleen relatief laag-risicopatiënten te zijn geïncludeerd. Van deze studies includeerde Schlumberger slechts twee patiënten met een pT3-tumor in een populatie van 752 patiënten. Het betrof in deze studie dus vrijwel alleen pT1-2-tumoren en de pT2-tumoren waren vrijwel allemaal pN0. Mallick includeerde 22% pT3 tumoren. Bal 2012 rapporteerde het T-stadium niet, maar vermeldde 19% stadium 3 patiënten te hebben geïncludeerd, en rapporteerde dat 74% van de patiënten N0 was.
Ook als gekeken wordt naar de Tg-spiegel ten tijde van de ablatie, dan blijkt dat in de studie van Schlumberger bijna de helft van de patiënten ten tijde van de ablatie al een gestimuleerd Tg kleiner of gelijk aan 1,5 pmol/l had, en in de studie van Mallick een kwart van de patiënten een gestimuleerd Tg <3,0 pmol/l. Dit wijst er op dat deze patiënten een zeer goede thyreoïdectomie hadden gehad en waarschijnlijk geen rest schildkliercarcinoom of metastasen (meer) hadden. De resultaten zijn derhalve niet valide voor T3-patiënten of voor patiënten met lymfekliermetastasen in situ.
Ook voor de subgroep patiënten met verwijderde lymfekliermetastasen met extranodale groei (hetgeen wijst op agressiever gedrag van de tumor en een risicofactor is voor een recidief) zijn er onvoldoende data.
De resultaten van deze studies lijken dus m.n. te kunnen worden geëxtrapoleerd naar patiënten met een T1-2 folliculair of klassiek papillair schildkliercarcinoom waarbij het schildkliercarcinoom volledig is verwijderd die en geen lymfekliermetastasen in situ hebben na de operatie en, waarbij eventueel verwijderde lymfekliermetastasen geen extranodale groei vertoonden en, die geen afstandmetastasen hebben.
Tabel - Overzicht gerandomiseerde studies lage versus hoge ablatiedosis (zie Aanverwant)
Stimulatie met recombinant humaan TSH versus onttrekking
Eén Cochrane-review vergeleek het effect van stimulatie met recombinant humaan TSH (rhTSH) versus onttrekking van schildklierhormoon als voorbereiding op ablatie met 131I na thyreoidectomie voor een niet-gemetastaseerd gedifferentieerd schildkliercarcinoom [Ma 2010]. De auteurs vonden twee kleine relevante gerandomiseerde studies, en vonden geen verschil in adequate ablatie (odds ratio 0,48, 95%BI 0,4-5,68).
Sinds deze review werden nog vier gerandomiseerde studies gepubliceerd [Mallick 2012, Lee 2010, Schlumberger 2012, Taieb 2009]. In totaal werden 1555 patiënten gerandomiseerd. In geen enkele studie werden patiënten met een T4-tumor of afstandsmetastasen geïncludeerd en de proportie geincludeerde T3 patiënten was zeer klein. Twee studies gebruikten een 2x2-factorial design, waarbij de geïncludeerde patiënten enerzijds gerandomiseerd werden naar stimulatie met recombinant humaan TSH of onttrekking van schildklierhormoon, en anderzijds naar een lage (30 mCi) of een hoge ablatie dosis 131I (100 mCi) [Mallick 2012, Schlumberger 2012 (1) (12)]. Lee et al. vergeleken stimulatie met rhTSH versus T4-onttrekking of T3-onttrekking [Lee 2010].
In twee studies werd de methode van randomisatie niet beschreven [Lee 2010, Taieb 2009 (13) (14)]. Drie studies waren open-label studies [Lee 2010, Schlumberger 2012, Taieb 2009], in de andere studie werd blindering niet gerapporteerd. De definitie van adequate ablatie verschilde in belangrijke mate tussen de vier studies, dit zowel wat betreft de gebruikte criteria als het tijdstip van de evaluatie.
Geen enkele studie vond een significant verschil in adequate ablatie tussen rhTSH en onttrekking van schildklierhormoon. In de studie van Mallick et al. werden de patiënten gerandomiseerd met stratificatie volgens centrum, T-stadium en N-stadium [Mallick 2012 (1)]. Bij patiënten met een T3-tumor (rhTSH: 83,3%; onttrekking: 79,2%) of met positieve lymfeklieren in het resectiepreparaat (rhTSH: 81,8%; onttrekking: 86,7%) werd geen significant verschil in adequate ablatie gevonden.
Tabel - Overzicht gerandomiseerde studies rhTSH versus onttrekking van schildklierhormoon (zie Aanverwant)
Referenties
- 1 - Mallick U, Harmer C, Yap B et al. Ablation with low-dose radioiodine and thyrotropin alfa in thyroid cancer. N Engl J Med. 2012;366(18):1674-85. # http://www.ncbi.nlm.nih.gov/pubmed/22551128
- 2 - Fallahi B, Beiki D, Takavar A et al. Low versus high radioiodine dose in postoperative ablation of residual thyroid tissue in patiënts with differentiated thyroid carcinoma: a large randomized clinical trial. Nucl Med Commun. 2012;33(3):275-82. # http://www.ncbi.nlm.nih.gov/pubmed/22124360
- 3 - Maenpaa HO, Heikkonen J, Vaalavirta L et al. Low vs. high radioiodine activity to ablate the thyroid after thyroidectomy for cancer: a randomized study. PLoS ONE [Electronic Resource]. 2008;3(4):e1885. # http://www.ncbi.nlm.nih.gov/pubmed/18382668
- 4 - Schlumberger M, Catargi B, Borget I et al. Strategies of radioiodine ablation in patiënts with low-risk thyroid cancer. N Engl J Med. 2012;366(18):1663-73. # http://www.ncbi.nlm.nih.gov/pubmed/22551127
- 5 - Johansen K, Woodhouse NJ, Odugbesan O. Comparison of 1073 MBq and 3700 MBq iodine-131 in postoperative ablation of residual thyroid tissue in patiënts with differentiated thyroid cancer. J Nucl Med. 1991;32(2):252-4. # http://www.ncbi.nlm.nih.gov/pubmed/1992028
- 6 - Caglar M, Bozkurt FM, Akca CK et al. Comparison of 800 and 3700 MBq iodine-131 for the postoperative ablation of thyroid remnant in patiënts with low-risk differentiated thyroid cancer. Nucl Med Commun. 2012;33(3):268-74. # http://www.ncbi.nlm.nih.gov/pubmed/22205241
- 7 - Pilli T, Brianzoni E, Capoccetti F et al. A comparison of 1850 (50 mCi) and 3700 MBq (100 mCi) 131-iodine administered doses for recombinant thyrotropin-stimulated postoperative thyroid remnant ablation in differentiated thyroid cancer. J Clin Endocrinol Metab. 2007;92(9):3542-6. # http://www.ncbi.nlm.nih.gov/pubmed/17609306
- 8 - Zaman Mu, Toor R, Kamal S et al. A randomized clinical trial comparing 50mCi and 100mCi of iodine-131 for ablation of differentiated thyroid cancers. JPMA J Pak Med Assoc. 2006;56(8):353-6. # http://www.ncbi.nlm.nih.gov/pubmed/16967785
- 9 - Bal C, Chandra P, Kumar A et al. A randomized equivalence trial to determine the optimum dose of iodine-131 for remnant ablation in differentiated thyroid cancer. Nucl Med Commun. 2012;33(10):1039-47.#http://www.ncbi.nlm.nih.gov/pubmed/22760303
- 10 - Bal C, Padhy AK, Jana S et al. Prospective randomized clinical trial to evaluate the optimal dose of 131 I for remnant ablation in patiënts with differentiated thyroid carcinoma. Cancer. 1996;77(12):2574-80.#http://www.ncbi.nlm.nih.gov/pubmed/8640708
- 11 - Chen L, Luo Q, Shen Y et al. Incremental value of 131I SPECT/CT in the management of patiënts with differentiated thyroid carcinoma. J Nucl Med 2008; 49(12): 1952-7. # http://www.ncbi.nlm.nih.gov/pubmed/18997044
- 12 - Sawka AM, Lakra DC, Lea J et al. A systematic review examining the effects of therapeutic radioactive iodine on ovarian function and future pregnancy in female thyroid cancer survivors. Clin Endocrinol (Oxf). 2008 Sep;69(3):479-90. # http://www.ncbi.nlm.nih.gov/pubmed/18284643
- 13 - Lee SK, Kim SH, Hur SM et al. The efficacy of lateral neck sentinel lymph node biopsy in papillary thyroid carcinoma. World Journal of Surgery 35(12), 2675-2682 (2011). # http://www.ncbi.nlm.nih.gov/pubmed/21993615
- 14 - Taieb D, Sebag F, Cherenko M et al. Quality of life changes and clinical outcomes in thyroid cancer patiënts undergoing radioiodine remnant ablation (RRA) with recombinant human TSH (rhTSH): a randomized controlled study. Clin Endocrinol (Oxf). 2009;71(1):115-23. # http://www.ncbi.nlm.nih.gov/pubmed/18803678
- 15 - Eustatia-Rutten, C. F., Corssmit, E. P., Pereira, A. M. et al. (2006). Quality of life in longterm exogenous subclinical hyperthyroidism and the effects of restoration of euthyroidism, a randomized controlled trial. Clinical Endocrinology, 64(3), 284-291. # http://www.ncbi.nlm.nih.gov/pubmed/16487438
- 16 - Mallick U, Harmer C, Yap B et al. Ablation with low-dose radioiodine and thyrotropin alfa in thyroid cancer. N Engl J Med. 2012;366(18):1674-85. # http://www.ncbi.nlm.nih.gov/pubmed/22551128
- 17 - Lee J, Yun MJ, Nam KH et al. Quality of life and effectiveness comparisons of thyroxine withdrawal, triiodothyronine withdrawal, and recombinant thyroid-stimulating hormone administration for low-dose radioiodine remnant ablation of differentiated thyroid carcinoma. Thyroid. 2010;20(2):173-9. # http://www.ncbi.nlm.nih.gov/pubmed/20151824
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 16-02-2015
Laatst geautoriseerd : 16-02-2015
Geplande herbeoordeling :
Laatst gewijzigd: 2015-02-16, Versie: 2.0
Actualisatie
Deze module is goedgekeurd op 3 juli 2014.IKNL bewaakt samen met betrokken verenigingen de houdbaarheid van deze en andere onderdelen van de richtlijn. Zo nodig zal de richtlijn tussentijds op onderdelen worden bijgesteld.
Houderschap richtlijn
De houder van de richtlijn moet kunnen aantonen dat de richtlijn zorgvuldig en met de vereiste deskundigheid tot stand is gekomen. Onder houder wordt verstaan de verenigingen van beroepsbeoefenaren die de richtlijn autoriseren.
Integraal Kankercentrum Nederland draagt zorg voor het beheer en de ontsluiting van de richtlijn.
Juridische betekenis van richtlijnen
De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. Er kunnen zich feiten of omstandigheden voordoen waardoor het wenselijk is dat in het belang van de patiënt van de richtlijn wordt afgeweken.
Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd gedocumenteerd te worden. De toepassing van de richtlijnen in de praktijk is de verantwoordelijkheid van de behandelende arts.
Algemene gegevens
Inleiding
Schildkliercarcinoom is een zeldzame aandoening. De incidentie is 2/100.000/jaar bij mannen en 4,5/100.000/jaar bij vrouwen. De cijfers van de Nederlandse Kankerregistratie (NKR) geven een stijging van de incidentie weer, van 356 nieuwe patiënten met schildkliercarcinoom in 2001 tot 611 in 2011. Gezien de relatief gunstige prognose en het ouder worden van mensen in het algemeen is de prevalentie hoog. De prevalentie is toegenomen van 2988 in 2007 naar 3821 in 2012. De 5-jaars relatieve overleving was 15 jaar geleden 74% en bedraagt nu 84%.
De meest voorkomende vormen van schildkliercarcinoom zijn het papillair schildkliercarcinoom en het folliculair schildkliercarcinoom; samen 80-85% van alle schildkliercarcinomen, in een verhouding van papillair: folliculair van 4:1. In Nederland was de incidentie in 2011 respectievelijk 395 en 104. Papillaire en folliculaire schildkliercarcinoom worden ook wel aangeduid als gedifferentieerd schildkliercarcinoom. Door de specifieke tumorkarakteristieken (jodiumopnemend vermogen, productie van thyreoglobuline) vormen de goed gedifferentieerde papillaire en folliculaire schildkliercarcinomen wat betreft behandeling en follow-up een aparte groep. Deze goed gedifferentieerde schildkliercarcinomen worden in deze richtlijn besproken.
De resterende groep schildkliercarcinomen (10-15%) bestaat uit medullair (ongeveer 5-10%) en anaplastisch (ongeveer 6%) schildkliercarcinoom. De behandeling en follow-up van deze tumoren blijft in deze richtlijn buiten beschouwing. Het medullaire schildkliercarcinoom is weliswaar een gedifferentieerde tumor, maar wordt niet tot de goed gedifferentieerde schildkliercarcinomen gerekend gezien de origine uit de C-cellen in plaats van uit folliculair epitheel, de andere tumor biologie en de behandeling. Voor de diagnostiek, behandeling en follow-up wordt verwezen naar de internationale richtlijnen van de ATA en de ETA.
In 2007 werd de eerste Nederlandse richtlijn gedifferentieerd (niet-medullair) schildkliercarcinoom gepubliceerd, die is gebaseerd op de principes van ‘Evidence Based Medicine'. De richtlijn werd ontwikkeld op initiatief van de Nederlandse Vereniging voor Nucleaire Geneeskunde en de Nederlandse Vereniging voor Endocrinologie in samenwerking met het Kwaliteitsinstituut voor Gezondheidszorg CBO en de Vereniging van Integrale Kankercentra.
In 2012 werd, zoals vastgelegd in de richtlijn, een nieuwe multidisciplinaire werkgroep geïnstalleerd voor een volledige herziening van de eerste versie van de richtlijn op initiatief van de Nederlandse Vereniging voor Endocrinologie en in samenwerking met Integraal Kankercentrum Nederland (IKNL). In deze werkgroep zijn zorgverleners vanuit verschillende (para)medische disciplines betrokken.
Knelpuntenanalyse
De resultaten van de knelpuntenanalyse, zie Aanverwant.
Doel en doelgroep
Doelstelling
De richtlijn is zoveel mogelijk gebaseerd op wetenschappelijk onderzoek of consensus. Het betreft een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering van zorgverleners die betrokken zijn bij patiënten met een (mogelijk) schildkliercarcinoom. De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. De richtlijn kan door de professional gebruikt worden bij de klinische besluitvorming. Bij de besluitvorming is de professional zich ervan bewust dat keuzes altijd gemaakt worden in samenspraak met de patiënt (shared decision making). Het is van belang de patiënt goed te informeren over de verschillende opties en hem/haar te betrekken bij de besluitvorming omdat dit leidt tot een hogere patiënttevredenheid en betere uitkomsten van zorg. 987 988 989 990 991 992.
De richtlijn Schildkliercarcinoom geeft aanbevelingen over diagnostiek, behandeling, nacontrole, nazorg en organisatie van zorg bij patiënten met (een mogelijk) schildkliercarcinoom. De richtlijn beoogt hiermee de kwaliteit van de zorgverlening te verbeteren, het klinisch handelen meer te baseren op wetenschappelijk bewijs dan op ervaringen en meningen, de transparantie te vergroten en de diversiteit van handelen door professionals te verminderen.
Gezien de complexiteit van zowel de diagnose, de behandeling, en de follow-up van schildkliercarcinoom, worden organisatorische aanbevelingen gedaan om tot kwalitatief hoogstaande zorg voor deze patiënten in Nederland te komen. De richtlijn wordt tevens gebruikt bij het ontwikkelen van (digitaal) patiëntenvoorlichtingmateriaal van Schildklier Organisaties Nederland (SON).
Doelpopulatie
De richtlijn is van toepassing op alle volwassen patiënten (> 18 jaar) met een (mogelijk) gedifferentieerd (niet-medullair) schildkliercarcinoom.
Doelgroep
De richtlijn is bestemd voor alle professionals die betrokken zijn bij de diagnostiek, behandeling, follow-up en voorlichting en begeleiding van patiënten met een gedifferentieerd schildkliercarcinoom, zoals internist-endocrinologen, kno-artsen, internist-oncologen, nucleair geneeskundigen, chirurgen, pathologen, radiologen en radiotherapeuten, huisartsen, oncologieverpleegkundigen, verpleegkundig specialisten, diëtisten en IKNL-consulenten.
Samenstelling werkgroep
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in april 2012 een multidisciplinaire werkgroep samengesteld, bestaande uit vertegenwoordigers van alle bij de diagnostiek en behandeling van patiënten met een gedifferentieerd schildkliercarcinoom betrokken medische en paramedische disciplines, een vertegenwoordiger van de Schildklierstichting Nederland en medewerkers van Integraal Kankercentrum Nederland.
Bij het samenstellen van de werkgroep is rekening gehouden met de geografische spreiding van de werkgroepleden, met een evenredige vertegenwoordiging van de verschillende betrokken verenigingen en instanties, alsmede met een spreiding al dan niet in academische achtergrond. De werkgroepleden hebben onafhankelijk gehandeld en waren gemandateerd door hun vereniging.
Werkgroepleden 2014
Voorzitter
Mw. prof. dr. Thera Links, internist-endocrinoloog, Universitair Medisch Centrum Groningen, gemandateerd namens de NIV
Procesbegeleider/contactpersoon
Mw. Janina Schrier, MSc, adviseur richtlijnen IKNL, j.schrier@iknl.nl / 06-53 67 94 21
Drs. Jos de Groot, adviseur richtlijnen IKNL (tot mei 2013)
Leden
Prof. dr. M.W.M. van den Brekel (namens Nederlandse Vereniging KNO, Antoni van Leeuwenhoek) Mw. M.A. Dagelet (namens NFK)
Dr. L.J.M. de Heide (namens NIV, Medisch Centrum Leeuwarden)
Dr. M.J.R. Janssen (namens NVNG, Radboudumc)
Mw. dr. H.W. Kapiteijn (namens NIV, Leids Universitair Medisch Centrum)
Prof. dr. J. Kievit (namens NVVH, Leids Universitair Medisch Centrum)
Dr. J.M.H. de Klerk (namens NVNG, Meander Medisch Centrum)
Dr. E.G.W.M. Lentjes (namens NVKC, Universitair Medisch Centrum Utrecht)
Prof. dr. A. van der Lugt (namens NVVR, Erasmus Medisch Centrum)
Mw. dr. F.H. van Nederveen (namens NVVP, Laboratorium voor Pathologie Dordrecht)
Mw. A. Ormeling (namens NFK)
Prof. dr. J.Th.M. Plukker (namens NVVH, Universitair Medisch Centrum Groningen)
Mw. J. van der Putten-Van Gils (namens V&VN, Leids Universitair Medisch Centrum)
Prof. dr. J.W.A. Smit (namens NIV, Radboudumc)
Dr. C.H.J. Terhaard (namens NVRO, Universitair Medisch Centrum Utrecht)
Dr. M.R. Vriens (namens NVVH, Universitair Medisch Centrum Utrecht)
Mw. dr. J.E. van der Wal (namens NVVP, Martini Ziekenhuis)
Ondersteuning
Mw. T.T.M. (Thekla) Bluemink-Holkenborg, secretaresse IKNL
Dhr. dr. J. Vlayen, literatuuronderzoeker, ME-TA
Werkgroepleden 2007
Kernredactie
Mw. dr. T.P. Links, internist-endocrinoloog, Universitair Medisch Centrum Groningen, voorzitter
Drs. L.J.M. de Heide, internist-endocrinoloog, Medisch Centrum Leeuwarden
Mw. M.S.C. van Heerden, secretaresse, namens Integraal Kankercentrum Noord- Nederland, Groningen
Mw. drs. E.W. Klokman, adviseur, Kwaliteitsinstituut voor de Gezondheidszorg CBO, Utrecht
Mw. drs. C.J.G.M. Rosenbrand, senior adviseur, Kwaliteitsinstituut voor de Gezondheidszorg CBO, Utrecht
Mw. Drs. Y. van der Wel, hoofd medische zaken, Integraal Kankercentrum Noord-Nederland, Groningen
Werkgroep
Dr. M.W.M. van den Brekel, KNO-arts, Nederlands Kankerinstituut, Amsterdam
Drs. W.I. de Bruin, nucleair geneeskundige, Medisch Spectrum Twente, Enschede
Prof.dr. A.P. Bruïne, patholoog, Academisch Ziekenhuis Maastricht
Dr. A.A.M. Franken, internist-endocrinoloog, Isala Klinieken, Zwolle
Prof.dr. J.F.Hamming, chirurg, Leids Universitair Medisch Centrum, Leiden
Mw. dr. D.A.K.C.J.M. Huysmans, nucleair geneeskundige, Catharina Ziekenhuis, Eindhoven
Prof.dr. J. Kievit, chirurg, Leids Universitair Medisch Centrum, Leiden
Dr. J.M.H. de Klerk, nucleair geneeskundige, Meander Medisch Centrum, Amersfoort
P.F. Lakwijk, Schildklierstichting Nederland, Amersfoort
Dr. M. van Leeuwen, Radioloog, Universitair Medisch Centrum Utrecht
Dr. E.G.W.M. Lentjes, klinisch chemicus, Universitair Medisch Centrum Utrecht
Prof.dr. P.C. Levendag, radiotherapeut, Erasmus Medisch Centrum, Rotterdam
Dr. W.I.B. Mastboom, chirurg, Medisch Spectrum Twente, Enschede
Prof.dr. J. Morreau, patholoog, Leids Universitair Medisch Centrum, Leiden
Dr. H. van Overhagen, radioloog, HagaZiekenhuis, Den Haag
Mw. drs. R. van Pel, patholoog, Nederlands Kankerinstituut, Amsterdam
Drs. H. van Pelt, medisch maatschappelijk werk, Medisch Centrum Leeuwarden
Drs. J. Puylaert, radioloog, Medisch Centrum Haaglanden, Den Haag
Drs. A.P.M. Schellekens, klinisch chemicus, Catharina Ziekenhuis, Eindhoven
Mw. I. Siersema, verpleegkundige, Universitair Medisch Centrum Utrecht
Prof.dr. J.W.A. Smit, internist-endocrinoloog, Leids Universitair Medisch Centrum, Leiden
Dr. C.H.J. Terhaard, radiotherapeut, Universitair Medisch Centrum Utrecht
Mw. prof.dr. E.G.E. de Vries, internist-oncoloog, Universitair Medisch Centrum Groningen
Drs. P. Wessels, Huisarts, Hilversum
Prof.dr. W.M. Wiersinga, internist-endocrinoloog, Academisch Medisch Centrum, Amsterdam
Dr. J.H.W. de Wilt, Chirurg, Erasmus MC, Rotterdam
Mandaterende verenigingen/organisaties
Nederlandse Vereniging voor Heelkunde
Nederlandse Vereniging voor Keel-, Neus- en Oorheelkunde
Nederlandse Vereniging voor Klinische Chemie
Nederlandse Vereniging voor Internisten
Nederlandse Vereniging voor Nucleaire Geneeskunde
Nederlandse Vereniging voor Pathologie
Nederlandse Federatie van Kankerpatiëntenorganisaties
Nederlandse Vereniging voor Nucleaire Geneeskunde
Nederlandse Vereniging voor Radiologie
Nederlandse Vereniging voor Radiotherapie en Oncologie
Verpleegkundigen & Verzorgenden Nederland
Schildklier Organisatie Nederland
Belangenverklaringen
Alle leden van de richtlijnwerkgroep hebben verklaard onafhankelijk gehandeld te hebben bij het opstellen van de richtlijn. Een onafhankelijkheidsverklaring ‘Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling' zoals vastgesteld door onder meer de KNAW, KNMG, Gezondheidsraad, CBO, NHG en Orde van Medisch Specialisten is door de werkgroepleden bij aanvang en bij afronding van het traject ingevuld.
De belangenverklaringen bij aanvang van het traject vindt u via:
- belangenverklaringen deel 1
- belangenverklaringen deel 2
De belangenverklaringen bij afronding van het traject worden nog geplaatst.
Inbreng patiëntenperspectief
Bij de ontwikkeling van deze richtlijn is tijdens alle fasen gebruik gemaakt van de input van patiënten. Deze input is nodig voor de ontwikkeling van kwalitatief goede richtlijnen. Goede zorg voldoet immers aan de wensen en eisen van zowel zorgverlener als patiënt.
Door middel van onderstaande werkwijze is informatie verkregen en zijn de belangen van de patiënt meegenomen:
- Bij aanvang van het richtlijntraject hebben de patiëntvertegenwoordigers knelpunten aangeleverd. Dit is gerealiseerd door het organiseren van een focusgroepbijeenkomst in juni 2012. Op basis van de uitkomsten van de focusgroepbijeenkomst is één uitgangsvraag geselecteerd die is uitgewerkt volgens de evidence based methodiek.
-
Tijdens het richtlijntraject heeft een gesprek plaatsgevonden waarbij de patiëntvertegenwoordigers, de verpleegkundigen, de procesbegeleider en de voorzitter aanwezig waren.
Het gesprek heeft plaatsgevonden ten tijde van het literatuuronderzoek van de evidence based vragen. Hierdoor kon het patiëntperspectief worden meegenomen in de overige overwegingen bij het bespreken van de conclusies uit de literatuur.
- Het perspectief van de patiënt met schildkliercarcinoom is zo breed mogelijk geïnventariseerd met behulp van het International Classification of Functioning, Disability and Health (ICF)-model. Hierbij valt te denken aan de beleving van de patiënt op het niveau van functies, activiteiten en maatschappelijke participatie.
-
De gestructureerde inventarisatie maakte de bijdrage vanuit het patiëntperspectief inzichtelijk en is met name terug te vinden in de overige overwegingen en in de aanbevelingen.
-
De inventarisatie was beschikbaar toen de (sub)werkgroep begon met schrijven van overige overwegingen en aanbevelingen, en is daarin meegenomen.
-
De patiëntvertegenwoordigers waren aanwezig bij alle vergaderingen van de richtlijnwerkgroep. De patiëntvertegenwoordigers hebben de conceptteksten beoordeeld teneinde het patiëntenperspectief in de formulering van de definitieve tekst te optimaliseren.
-
De Nederlandse Federatie van Kankerpatiëntenorganisatie (NFK) is geconsulteerd in de externe commentaarronde.
Methode ontwikkeling
Evidence based
Implementatie
Bevorderen van het toepassen van de richtlijn in de praktijk begint met een brede bekendmaking en verspreiding van de richtlijn.
Bij verdere implementatie gaat het om gerichte interventies om te bevorderen dat professionals de nieuwe kennis en kunde opnemen in hun routines van de oncologische en palliatieve zorgpraktijk, inclusief borging daarvan.
Als onderdeel van elke richtlijn stelt IKNL een implementatieplan op.
Activiteiten en interventies voor verspreiding en implementatie vinden zowel op landelijk als regionaal niveau plaats. Deze kunnen eventueel ook op maat gemaakt worden per instelling of specialisme. Informatie hierover is te vinden op www.iknl.nl/opleidingen.
Het implementatieplan bij deze richtlijn is een belangrijk hulpmiddel om effectief de aanbevelingen uit deze richtlijn te implementeren voor de verschillende disciplines. Het implementatieplan wordt ontwikkeld naar aanleiding van het definitieve document
Werkwijze
Werkwijze werkgroep
De werkgroep is in april 2012 voor de eerste maal bijeengekomen. Op basis van een eerste inventarisatie van de knelpunten door de werkgroepleden is, door middel van een enquête onder professionals die betrokken zijn bij patiënten met schildkliercarcinoom, een knelpunteninventarisatie gehouden. Na het versturen van de enquête hebben 120 professionals gereageerd en knelpunten geprioriteerd en/of ingebracht. Op basis van de uitkomsten van de enquête zijn vijf uitgangsvragen geselecteerd die zijn uitgewerkt volgens de evidence based methodiek.
Voor iedere uitgangsvraag werd uit de richtlijnwerkgroep een subgroep geformeerd. Bij de beantwoording van deze uitgangsvragen verzorgde een externe methodoloog het literatuuronderzoek. Dit betrof het uitvoeren van een systematische literatuursearch, het kritisch beoordelen van de literatuur en het verwerken van de literatuur in evidence tabellen. Daarnaast werd door de methodoloog een concept literatuurbespreking met bijbehorende conclusies aangeleverd voor deze uitgangsvragen. Vervolgens pasten de subwerkgroepleden, na interne discussie met de methodoloog, de concept literatuurbespreking en conclusies aan en stelden overige overwegingen en aanbevelingen volgens een checklist ‘overige overwegingen en formuleren van aanbevelingen'. Bij de ontwikkeling van deze richtlijn is tijdens alle fasen gebruik gemaakt van de input van patiënten. Zie ‘Inbreng patiëntenperspectief’. De werkgroep heeft gedurende achttien maanden gewerkt aan de tekst van de conceptrichtlijn. Alle teksten zijn tijdens plenaire vergaderingen besproken en na verwerking van de commentaren door de werkgroep geaccordeerd.
De conceptrichtlijn is op 30 januari 2014 ter becommentariëring aangeboden op Richtlijnendatabase en Oncoline en aan alle voor de knelpuntenanalyse benaderde wetenschappelijke, beroeps- en patiëntenverenigingen en de landelijke en regionale tumorwerkgroepen. Het commentaar geeft input vanuit het veld om de kwaliteit en de toepasbaarheid van de conceptrichtlijn te optimaliseren en landelijk draagvlak voor de richtlijn te genereren. Circa 60 respondenten (zowel individuen als groepen) maakten van deze mogelijkheid gebruik. Een landelijke bijeenkomst op 16 april is georganiseerd naar aanleiding van de publicatie van de conceptrichtlijn en ter afsluiting van de commentaarfase. Alle commentaren werden vervolgens beoordeeld en verwerkt door de richtlijnwerkgroep. De richtlijn is inhoudelijk vastgesteld op 3 juli 2014. Ten slotte is de richtlijn ter autorisatie/accordering gestuurd naar de betrokken verenigingen/instanties.
Financiering
Deze richtlijn is gefinancierd door Integraal Kankercentrum Nederland (IKNL). De inhoud van de richtlijn is niet beïnvloed door de financierende instantie.
Procesbegeleiding en verantwoording
IKNL is het kennis- en kwaliteitsinstituut voor professionals en bestuurders in de oncologische en palliatieve zorg. IKNL draagt bij aan het verbeteren van de zorg rond kanker door het verzamelen van gegevens, het opstellen van richtlijnen, het bewaken van kwaliteit en het faciliteren van samenwerkingsverbanden. Ons doel is de beste zorg voor iedere patiënt.
IKNL werkt aan multidisciplinaire richtlijnontwikkeling voor de oncologische en palliatieve zorg. Naast het reviseren van richtlijnen faciliteert IKNL ook het onderhoud, het beheer, de implementatie en de evaluatie van deze richtlijnen.
De kwaliteit van ontwikkelen, implementeren en evalueren van evidence en consensus based richtlijnen waarborgt IKNL door aan te sluiten bij de criteria opgesteld in de Richtlijn voor Richtlijnen (maart 2012), AGREE II en de Medisch specialistische richtlijnen 2.0.
Evidence based uitgangsvragen 2014
Uitgangsvraag 1 (EB)
Wat is de rol van de echografie in de initiële diagnostiek van patiënten met een palpabele nodus?
Vraag beantwoord door De Heide, Kievit, Van der Lugt, Van der Wal/Van Nederveen
Uitgangsvraag 2 (EB)
Leidt een nieuwe strategie om patiënten, die na initiële behandeling (operatie en 131I ablatie) geen verdenking op locale tumor aanwezigheid hebben, te verdelen in een laag-risico groep en een niet-laag risico groep, gebaseerd op de combinatie basale Tg-bepaling onder TSH-suppressie en echografie van de hals t.o.v. de huidige indeling (conform de ATA-richtlijn 2009) tot een betere inschatting van de recidiefkans en daarmee een betere follow-up strategie voor de beide patiëntengroepen?
Vraag beantwoord door De Heide en Links, Janssen/De Klerk, Plukker, Van der Lugt, Lentjes (TG-bepaling)
Uitgangsvraag 3 (EB) Bij welke karakteristieken op beeldvorming is FNAC nodig bij patiënten die een bij toeval ontdekte nodus hebben op 1) echografie 2) CT scan, 3) MRI, 4) FDG-PET (CT)?
Vraag beantwoord door Van der Lugt (nodus en echo), Janssen (FDG-PET), De Heide, Kievit, Van Nederveen
Uitgangsvraag 4 (EB)
Welke dosis radioactief jodium moet worden gebruikt voor ablatie bij patiënten met een gedifferentieerd schildkliercarcinoom die een totale thyreoïdectomie hebben ondergaan?
Vraag beantwoord door Janssen, Smit, Vriens
Uitgangsvraag 5 (EB)
Wat zijn de vroege en/of late gevolgen op de kwaliteit van leven voor patiënten met gedifferentieerd schildkliercarcinoom als gevolg van de ziekte en/of behandeling door chirurgie, ablatie en hormoontherapie?
Vraag beantwoord door Dagelet/Schrier, Ormeling, Van der Putten, Smit
Uitgangsvragen 2007
Diagnostiek
- Wat is de a-priori kans op schildkliercarcinoom / gedifferentieerd schildkliercarcinoom in de eerste lijn?
-
Wat is de definitie van een "nodus", is er een minimale maat voor diagnostiek?
-
Welke diagnostiek kan verricht worden door / via de huisarts en wanneer dient verwijzing plaats te vinden en naar wie?
-
Welke plaats neemt FNA in bij de diagnostiek van schildklierafwijkingen? Hoe betrouwbaar is FNA/kan FNA zijn?
-
Hoe kan de verwerking van cytologisch materiaal worden geoptimaliseerd en hoe dient de verslaglegging van schildklier FNA te zijn?
-
Is er een indicatie voor FNA bij een multinodulair beeld? Zo ja, wat is de consequentie van een FNA uitslag "folliculaire proliferatie" of "Hürthle cell proliferatie" bij een multinodulair beeld?
-
Wat is de indicatie voor echo, TSH bepaling (routine?), calcitoninebepaling en scintigrafie? En wat is de toegevoegde waarde hiervan?
-
Is er een plaats voor scintigrafie in de besluitvorming tot een diagnostische hemithyreoidectomie bij een folliculaire laesie?
-
Kan preoperatief ook groei buiten de schildklier worden vastgesteld? Welke patiënten zijn beter uit in een centrum en hoe identificeer je die?
-
Welke zijn klachten of afwijkingen suggestief voor maligniteit en hoe worden deze meegewogen in de besluitvorming tot een diagnostische hemithyreoidectomie of een totale thyreoidectomie?
-
Hoe kan de beoordeling van histologisch materiaal worden geoptimaliseerd en gestandaardiseerd?
-
Hoe is het beleid bij een positieve familie anamnese voor papillair schildklier carcinoom bij een patiënt met een nodus?
-
Wat zijn de diagnostische criteria voor "papillair carcinoom folliculaire variant" (PCFV)? Wat te doen bij focaal papillaire kenmerken?
-
Wat zijn de diagnostische criteria voor "minimally invasive" folliculair carcinoom? en hoe dient daarbij het klinisch beleid te zijn?
-
Dient de TNM classificatie standaard ingevoerd te worden bij de rapportage of alleen de ingrediënten hiertoe?
Primaire chirurgie en ablatie
- Wat is de behandeling van lymfekliermetastasen?
-
Wat is een (on)gunstige uitgangspositie en welke classificatie moet hiervoor gehanteerd worden?
-
Wat is de plaats van halsklierdissectie indien preoperatief sprake is van een maligniteit?
-
Wat is de waarde van een SN procedure?
-
Wat is de plaats van externe radiotherapie (+/- chemotherapie) bij gedifferentieerde T4 tumoren en welke dosis en doelvolume/fractionering zou moeten worden toegepast?
-
Wat is de hoogte van de ablatie?
-
Wat is de plaats van het pre-ablatie scintigram ?
-
Is het zinvol peroperatieve vriescoupes te verrichten?
-
Wat is het beleid bij stembandstilstand postoperatief?
-
Is pre-postoperatieve controle van de stembanden zinvol?
-
Hoe wordt perioperatieve zorg vastgesteld en afgestemd met overige subwerkgroepen?
-
Zijn er specifieke maatregelen ten aanzien van kinderen nodig?
- Zijn er specifieke maatregelen ten aanzien van zwangerschap nodig?
Follow up (algemeen) 1
- Welke kwaliteitseisen worden gesteld aan thyreoglobuline bepaling?
-
Welke strategie moet worden gevolgd bij aanwezigheid van Tg-antilichamen?
-
Onder welke omstandigheden moet Tg worden afgenomen: on or off thyroxine, of na recombinant hTSH (rhTSH)?
-
Is er een grenswaarde aan te geven voor de Tg of de stijging ervan die moet leiden tot actie?
-
Wat is de waarde van Tg-mRNA in de follow-up?
-
Indicatie van rhTSH voor de I-scintigrafie?
-
Welk radiopharmacon dient er gebruikt te worden, 123I, of 131I, in welke dosis en wanneer?
-
Welke waarden van TSH en Tg zijn adekwaat voor onthouden of geven van I-therapie bij negatieve scan?
-
Wat is de waarde van de echografie in de follow-up?
-
Welke controle en welke diagnostiek is nodig na de initiële ablatie therapie?
-
Is er altijd een reden voor het nogmaals onttrekken van schildklierhormoon en het doen van I-scintigrafie en dient dit dan na bv 3 of 6 mnd plaats te vinden? Moeten subgroepen worden onderscheiden in verband met risico's?
-
Is er een streefwaarde voor de TSH, met name voor suppressietherapie, en hoe moet deze worden bepaald?
-
Dient er een routine X-thorax te worden gemaakt?
-
Is er ander localiserend onderzoek nodig en in welke volgorde? Tc-Sesta-MIBI, Thallium, Pet-scan?
-
Wat zijn de consequenties voor follow-up met betrekking tot Tg suppressie therapie?
-
Is er een modificatie van de richtlijn tijdens zwangerschap en bij kinderen?
-
Hoe dient de substitutietherapie te zijn, voorafgaand aan I-scintigrafie?
-
Is er een rol voor jodiumbeperkt dieet voorafgaand aan I-scintigrafie?
Follow up (recidief) 2
- Tweede therapie bij afstand jodium opnemende metastasen en/of inoperabel processen: standaard dosis of vooraf tracer/dosimetrie?
-
Toe te dienen dosis afhankelijk van uptake en/of lokalisatie metastasen?
-
Wat is de frequentie van 131I therapie bij succes ? Wat is de maximale cumulatievedosis 131I?
-
Hoe wordt succes bepaald? Hoe wordt succes gedefinieerd? daling van Tg?
-
Plaats van rTSH bij 131I therapie?
-
Wat zijn de indicaties voor uitwendige radiotherapie?
-
131I, externe radiotherapie of chirurgie bij locale recidieven in de hals? Wat is de rol van probe guided surgery?
-
Wat te doen bij een geïsoleerd recidief in de hals zonder voorafgaande behandeling hals? na voorafgegane locale therapie hals? na al voorafgaande halsklierdissectie?
-
Wat is de plaats van radiofrequente ablatie?
-
Wat te doen bij negatief tracer onderzoek? Blinde dosis 131I? Tracer onderzoek nodig voorafgaande aan blinde therapeutische dosis?
-
Wat te doen bij negatieve post-therapie scan en aantoonbaar Tg en positief beeldend ander onderzoek?
-
Is er een indicatie voor chirurgie voor niet in de hals gelegen metastasen? Altijd bevestiging PA nodig voor verdere behandeling?
-
Wat is de plaats van Lithium in de voorbereiding van de behandeling met 131I?
-
Wat is de rol van bisfosfonaten bij skeletmetastasen?
-
Embolisatie?
Organisatie van zorg
Multidisciplinaire werkgroep schildkliercarcinoom?
- Heeft ieder ziekenhuis een multidisciplinaire werkgroep schildkliercarcinoom?
-
Zo niet, in welk gremium worden de patiënten met schildkliercarcinoom besproken?
-
Wat is de minimale vs optimale samenstelling van de werkgroep?
-
Welke eisen stelt men aan de deelnemers van de werkgroep?
-
Hoe vindt inbedding van de werkgroep plaats, zowel lokaal als regionaal?
-
Is een landelijk PA-panel/registratie patiënten wenselijk/noodzakelijk?
Behandeling schildkliercarcinoom
- Is centralisatie van behandeling wenselijk of noodzakelijk en hoe wordt dit dan georganiseerd? Wat zijn de criteria voor behandelcentra en wie bepaalt dat?
-
Welke eisen stelt men aan betrokken chirurg/internist/radioloog/patholoog/nucleair geneeskundige?
-
Wanneer en hoe te verwijzen naar behandelcentra?
-
Wat is de rol van de huisarts in het diagnostisch en behandeltraject?
Patiënteninformatie
- Op welk moment is de patiënt een schildkliercarcinoompatiënt?
-
Welke eisen stelt dat aan de begeleiding van de patiënt?
-
Wat betekent dit voor de behandeling en de samenstelling van de multidisciplinaire werkgroep?
-
Aan welke eisen dient de patiënteninformatie te voldoen ?
- Welke eisen stelt dit aan de patiëntenorganisaties (van kankerpatiënten en van patiënten met schildkliercarcinoom)?
Wetenschappelijke onderbouwing
Module is uitgewerkt volgens EBRO-methodiek.
De EBRO-methodiek
Opbouw
Elke module van de richtlijn is volgens een vast stramien opgebouwd: de uitgangsvraag en aanbevelingen, de onderbouwing (samenvatting literatuur, referentielijst, conclusies en evidence tabellen), de overwegingen en de verantwoording. Voor het evidence based uitwerken van vragen rondom diagnostische interventies hanteren we de EBRO-methodiek, voor therapeutische interventies de GRADE methodiek.
De antwoorden op de uitgangsvragen (derhalve de aanbevelingen in deze richtlijn) zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek.
Selectie
Aanbevelingen werden gebaseerd op ‘beste evidence' en daarom werd naast selectie op relevantie tevens geselecteerd op bewijskracht. Hiervoor werd gebruik gemaakt van de volgende hiërarchische indeling van studiedesigns gebaseerd op bewijskracht:
- Meta-analyses en systematische reviews;
- Gerandomiseerde gecontroleerde studies (RCT's);
- Niet gerandomiseerde gecontroleerde studies (CCT's).
Waar deze niet voorhanden waren werd verder gezocht naar vergelijkend cohortonderzoek.
Critical appraisal
De geselecteerde artikelen zijn vervolgens beoordeeld op de kwaliteit van het onderzoek door middel van het invullen van de checklist critical appraisal. Hierbij is het wetenschappelijk bewijs beoordeeld op vertekening (bias) en gegradeerd naar mate van bewijs. In de laatste kolom van de evidence tabellen wordt een samenvatting gegeven van de critical appraisal (zie bijlage 11/evidence tabellen). De mate van bewijskracht en het niveau van bewijs zijn in de conclusies van de verschillende hoofdstukken of paragrafen weergegeven. De belangrijkste literatuur waarop de conclusies zijn gebaseerd, is daarbij vermeld.
Indeling van onderzoeksresultaten naar mate van bewijskracht
Tabel 1. Diagnostische tests
Indeling van onderzoeksresultaten naar mate van bewijskracht
|
A1 |
Onderzoek naar de effecten van diagnostiek op klinische uitkomsten bij een prospectief gevolgde goed gedefinieerde patiëntengroep met een tevoren gedefinieerd beleid op grond van de te onderzoeken testuitslagen, of besliskundig onderzoek naar de effecten van diagnostiek op klinische uitkomsten, waarbij resultaten van onderzoek van A2-niveau als basis worden gebruikt en voldoende rekening wordt gehouden met onderlinge afhankelijkheid van diagnostische test. |
|
A2 |
Onderzoek ten opzichte van een referentietest, waarbij van tevoren criteria zijn gedefinieerd voor de te onderzoeken test en voor een referentietest, met een goede beschrijving van de test en de onderzochte klinische populatie; het moet een voldoende grote serie van opeenvolgende patiënten betreffen, er moet gebruik gemaakt zijn van tevoren gedefinieerde afkapwaarden en de resultaten van de test, en de ‘gouden standaard' moeten onafhankelijk zijn beoordeeld. Bij situaties waarbij multiple, diagnostische test een rol spelen, is er in principe een onderlinge afhankelijkheid en dient de analyse hierop te zijn aangepast, bijvoorbeeld met logistische regressie. |
|
B |
Vergelijking met een referentietest, beschrijving van de onderzochte test en van de onderzochte populatie, maar niet de kenmerken die verder onder niveau A1 en A2 staan genoemd. |
|
C |
Niet-vergelijkend onderzoek |
|
D |
Mening van deskundigen (bijvoorbeeld werkgroepleden) |
Tabel 2. Niveau van bewijskracht van de conclusie op basis van het aan de conclusie ten grondslag liggend bewijs
|
Niveau van bewijs |
Conclusie gebaseerd op |
Formulering |
|
1 |
Eén systematische review (A1) of ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A1 of A2 |
Het is aangetoond dat... |
|
2 |
Ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
Het is aannemelijk dat... |
|
3 |
Eén onderzoek van niveau A2, B of C |
Er zijn aanwijzingen dat... |
|
4 |
Mening van deskundigen (bijvoorbeeld de werkgroepleden) |
De werkgroep is van mening dat... |
Methode voor het formuleren van ‘Overwegingen'
Naast de conclusies uit de literatuur zijn er andere overwegingen die kunnen meespelen bij het formuleren van de aanbeveling. Deze aspecten worden besproken onder het kopje ‘Overwegingen' in de richtlijntekst. Hierin wordt de context van de dagelijkse praktijk beschreven en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van de conclusie(s) in combinatie met deze overwegingen.
Per uitgangsvraag:
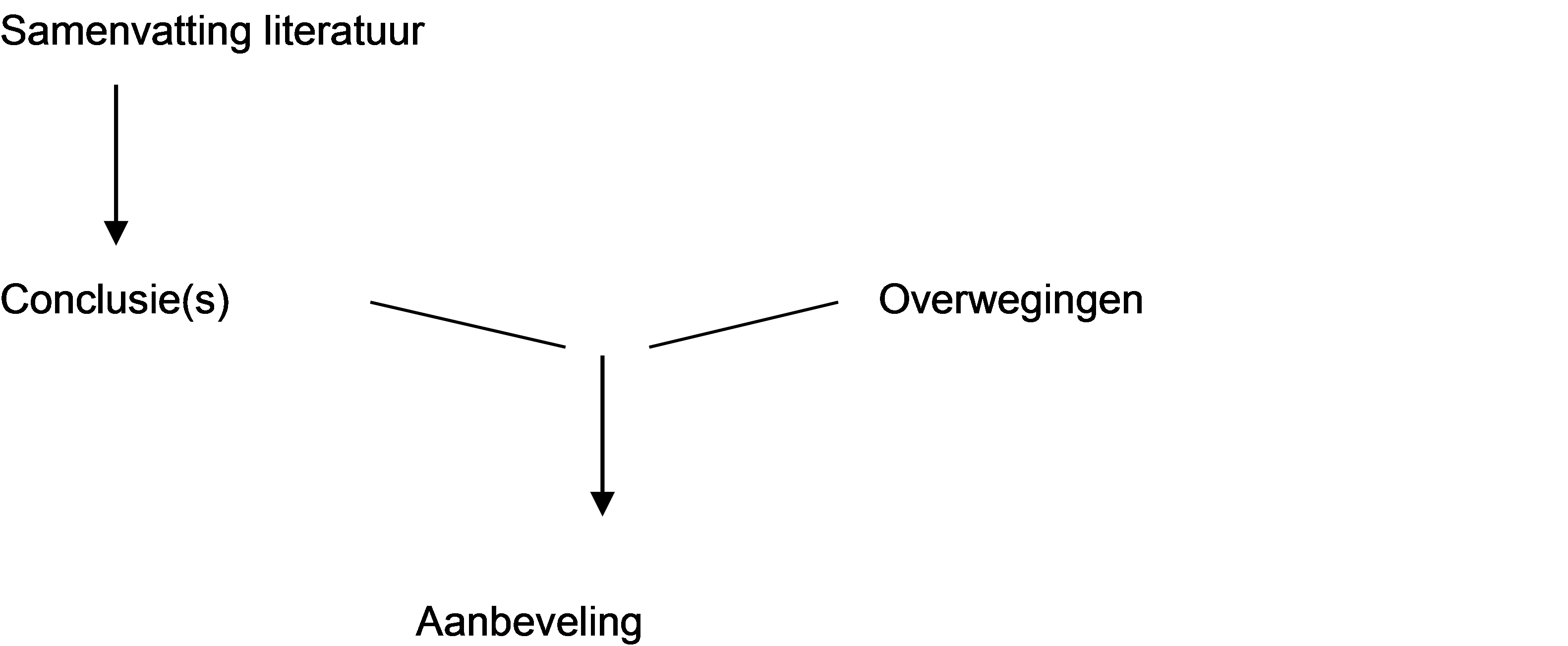
Figuur 1 Van bewijs naar aanbeveling
Checklist ‘overwegingen'
Eén of meerdere conclusies leiden tot één aanbeveling. Bij evidence based richtlijnen wordt voor de formulering van de aanbeveling één checklist ‘Overwegingen' ingevuld. Deze checklist en de bijbehorende uitleg kunnen ook worden gebruikt bij het schrijven van de overwegingen. Als een bepaald diagnostisch instrument of bepaalde behandeling volgens de conclusies niet werkzaam is, dient geen gebruik gemaakt te worden van dit diagnostisch instrument of deze behandeling. Overwegingen dragen dan niet bij en worden niet beschreven.
|
Items |
A) Wordt het item meegewogen in het opstellen van de concept aanbeveling? |
B) Indien ja, beschrijving van deze overwegingen. Deze tekst wordt weergegeven in de richtlijn onder het tabblad 'overwegingen'. |
|
1. Klinische Relevantie |
□ Ja □ Nee |
|
|
2. Veiligheid |
□ Ja □ Nee |
|
|
3. Patiënten perspectief |
□ Ja □ Nee |
|
|
4. Professioneel perspectief |
□ Ja □ Nee |
|
|
5. Kosten effectiviteit |
□ Ja □ Nee |
|
|
6. Organisatie |
□ Ja □ Nee |
|
|
7. Maatschappij |
□ Ja □ Nee |
|
Uitleg items checklist ‘overwegingen'
1. Klinische relevantie: bepalen door professionals en evt. literatuuronderzoek
- Sterkte van het effect vergeleken met geen interventie
- Consistentie van het beschikbare bewijs uit de verschillende studies
- Generaliseerbaarheid
- Voorbeeld: een bepaalde behandeling kan een significante verbetering van symptomen geven die patiënten echter niet als zodanig ervaren, dus klinisch niet relevant
2. Veiligheidsissues: bepalen door professionals en evt. literatuuronderzoek
- Bijwerkingen, risico's of complicaties op korte en lange termijn
- Gebruik bij co-morbiditeit / gelijktijdig gebruik medicatie en/of interventie
- Voorbeeld: fysieke comorbiditeit kan bepaalde behandelingen uitsluiten.
3. Patiëntenperspectief: bepalen door professionals, patiënten en eventueel literatuuronderzoek
- Voorkeuren / te verwachten compliance / te verwachten tevredenheid / kwaliteit van leven
- Voorbeeld: diagnostiek of behandeling waarvoor minder ziekenhuisbezoek nodig is; behandeling die makkelijker toe te dienen is; behandeling die sneller effect laat zien
4. Professioneel perspectief: bepalen door professionals
- Kennis en ervaring met technieken/therapie
- Risico's die professional loopt bij het toepassen van de interventie / tijdbesparing of het verlies aan tijd door het invoeren van de interventie
- Houding, normen en waarden van de professional
- Voorbeeld: een nieuwe techniek die nog niet alle professionals beheersen.
5. Kosteneffectiviteit: bepalen door professionals, indien gewenst en mogelijk kosteneffectiviteits-analyse door expert
- Kosteneffectiviteit in verhouding tot bestaande ingrepen/behandelingen voor deze ziekte
6. Organisatorische factoren: bepalen door professionals
- De beschikbaarheid/aanwezigheid van faciliteiten & medicijnen
- De wijze waarop de organisatie van de zorg aangeboden dient te worden / grootte van de verandering in het organisatie-zorgproces / infrastructuur voor implementatie
- Voorbeeld: een bepaalde diagnostiek of behandeling kan alleen in bepaalde centra worden uitgevoerd in verband met de aanwezigheid van faciliteiten zoals een PET scan.
7. Maatschappelijke factoren: bepalen door professionals
- Vergoeding door verzekeraars / Industriële belangen / Ethische overwegingen / Juridische overwegingen / Politieke en strategische consequenties
- Voorbeeld: indien twee behandelingen even effectief zijn waarvan één behandeling wordt vergoed, zal deze laatste behandeling worden aanbevolen.
Checklist formuleren van aanbevelingen
|
Niveau van bewijs conclusie |
Effect overwegingen op concept aanbeveling |
Classificatie aanbeveling |
Formulering aanbeveling |
|
1 of 2 Hoge mate van bewijs |
Versterkt concept aanbeveling of is neutraal |
Sterke aanbeveling |
Er dient |
|
1 of 2 Hoge mate van bewijs |
Verzwakt concept aanbeveling |
Aanbeveling |
Er wordt geadviseerd |
|
3 of 4 Lage mate van bewijs |
Versterkt concept aanbeveling of is neutraal |
Aanbeveling |
Er wordt geadviseerd |
|
3 of 4 Lage mate van bewijs |
Verzwakt concept aanbeveling |
Geen aanbeveling |
Er kan geen aanbeveling worden gegeven. Optioneel: de werkgroep is van mening dat |
Methode voor het formuleren van aanbevelingen
In de praktijk kunnen er per uitgangsvraag meerdere conclusies zijn, met verschillend niveau van bewijs. Indien er meerdere conclusies bij de uitgangsvraag zijn geformuleerd is het van belang de conclusies te prioriteren. Het niveau van bewijs van de conclusie die het meest van belang is voor het formuleren van de aanbeveling wordt meegenomen in de checklist ‘formuleren van aanbevelingen'.
Evidence tabellen
Literatuuronderzoek evidence based vragen
Hieronder de evidence tabellen van de vijf evidence based behandelde uitgangsvragen (zie Aanverwant):
Uitgangsvraag 1 (EB)
Wat is de rol van de echografie in de initiële diagnostiek van patiënten met een palpabele nodus?
Uitgangsvraag 2 (EB)
Leidt een nieuwe strategie om patiënten, die na initiële behandeling (operatie en 131I ablatie) geen verdenking op locale tumor aanwezigheid hebben, te verdelen in een laag-risico groep en een niet-laag risico groep, gebaseerd op de combinatie basale Tg-bepaling onder TSH-suppressie en echografie van de hals t.o.v. de huidige indeling (conform de ATA-richtlijn 2009) tot een betere inschatting van de recidiefkans en daarmee een betere follow-up strategie voor de beide patiëntengroepen?
Uitgangsvraag 3 (EB)
Bij welke karakteristieken op beeldvorming is FNAC nodig bij patiënten die een bij toeval ontdekte nodus hebben op 1) echografie 2) CT scan, 3) MRI, 4) FDG-PET (CT)?
Uitgangsvraag 4 (EB)
Welke dosis radioactief jodium moet worden gebruikt voor ablatie bij patiënten met een gedifferentieerd schildkliercarcinoom die een totale thyreoïdectomie hebben ondergaan?
Uitgangsvraag 5 (EB)
Wat zijn de vroege en/of late gevolgen op de kwaliteit van leven voor patiënten met gedifferentieerd schildkliercarcinoom als gevolg van de ziekte en/of behandeling door chirurgie, ablatie en hormoontherapie?
Evaluatie
Tijdens de ontwikkeling van de richtlijn zijn indicatoren voor de evaluatie van de aanbevelingen in de richtlijn opgesteld. Met gegevens uit de NKR en eventuele andere bronnen registreren we deze indicatoren. Hiermee stellen we vast in hoeverre de richtlijn wordt nageleefd. De resultaten van de evaluatie nemen we mee in de volgende revisie van de richtlijn. Ook kunnen de resultaten voor een aanpassing van de implementatie, in lopende trajecten, zorgen. De indicatoren voor deze richtlijn worden ontwikkeld naar aanleiding van het definitieve document.
Verklarende woordenlijst
|
CB |
consensus based |
|
DTC |
Gedifferentieerd schildkliercarcinoom (Differentiated thyroid cancer) |
|
EB |
evidence based |
|
ESR |
european standardized rate |
|
PPV |
positieve voorspellende waarde (positive predictive value) |
|
NPV |
negatieve voorspellende waarde (negative predictive value) |
|
RAI |
radioactief jodiumbehandeling (RadioActive Iodine) |
|
RT |
Radiotherapie |
|
Tg |
Thyreoglobuline |
|
TgAb |
anti-Thyreoglobuline antistoffen |
|
TgOFF-bepaling |
Tg-bepaling nadat tevoren de schildklierhormoonsubstitutie tijdelijk is gestaakt |
|
TgON-bepaling |
Tg-bepaling tijdens schildklierhormoonsubstitutie |
|
WBS |
whole body scan |
