Oogbescherming
Uitgangsvraag
Wanneer draagt oogbescherming, gedragen als arbo- en/of infectiepreventiemaatregel, bij aan het verkleinen van de kans op de transmissie van micro-organismen en de kans op (zorggerelateerde) infecties via en/of naar medewerkers?
Aanbeveling
Draag een oogbeschermingsmiddel in de volgende situaties:
- wanneer er kans is dat het oogslijmvlies in contact komt met lichaamsvloeistoffen;
- bij contact met patiënten in isolatie waarbij het risico bestaat op besmetting door micro-organismen via de ogen.
Overwegingen
Voor- en nadelen van de aanbeveling en de kwaliteit van het bewijs
De resultaten van de literatuuranalyse laten een duidelijk trend zien waarbij het dragen van oogbescherming mogelijk bijdraagt aan het voorkomen van virale infecties van de zorgmedewerker. De bewijskracht hiervoor is matig. Er zijn geen vergelijkende studies gevonden die uitspraak doen over de bescherming van een oogbeschermingsmiddel op het voorkomen van infecties als gevolg van spatten van lichaamsvocht.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Oogbescherming wordt vooral gedragen bij zorghandelingen waarbij er een kans is op een spataccident met bloed of andere lichaamsvloeistoffen, bijvoorbeeld bij een operatieve ingreep. Een zorgmedewerker kan door een spataccident blootgesteld worden aan bloedoverdraagbare aandoeningen. Oogbescherming kan spatten in het oogslijmvlies voorkomen.
Oogbescherming kan ook als onderdeel van isolatiezorg gedragen worden, bijvoorbeeld bij virussen die hoogbesmettelijk zijn. Het oogslijmvlies van zorgmedewerkers wordt in dat geval door gebruik van oogbescherming niet blootgesteld aan het betreffende virus waardoor infectie wordt voorkomen.
Kosten (middelenbeslag)
Verwacht wordt dat het dragen van oogbescherming bij ingrepen of zorgsettingen waarbij er een kans is op spataccidenten geen of een verwaarloosbare organisatorische of financiële impact zal hebben op zorginstellingen die hiermee werken.
Aanvaardbaarheid, haalbaarheid en implementatie
Het type oogbescherming wordt gekozen op basis van risico-inschatting. Het dragen van het juiste type oogbescherming moet middels een Risico-Inventarisatie en -Evaluatie (RI&E) beoordeeld worden. Een arbodienst en/of arbeidshygiënist/bedrijfsarts kan helpen bij het uitvoeren van een (RI&E) en schrijft voor welk type bril geschikt is per risico. De meeste eigen brillen voldoen niet aan de gestelde criteria voor een spatbril. De werkgever dient in deze gevallen conform de Arbowet een alternatief te voorzien.
Een voorwaarde voor het werken met oogbescherming is dat zorgmedewerkers goed geschoold en geïnformeerd zijn over de volgende punten:
- Het type oogbeschermingsproduct(en) waarmee zij kunnen werken.
- Wanneer zij oogbescherming moeten dragen in relatie tot de kans op spataccidenten.
- Hoe zij veilig werken met oogbescherming in relatie tot handhygiëne en reiniging en desinfectie. De handen kunnen gecontamineerd raken bij het afzetten van de oogbescherming.
Scholing en deskundigheid draagt ook bij aan motivatie voor het correct en veilig gebruik van oogbescherming.
Duurzaamheid en hergebruik
In de huidige zorginfrastructuur is het gebruik van oogbescherming gemeengoed. De faciliteiten en voorzieningen zijn aanwezig op locaties waar het risico op besmetting en veiligheid groot is (zoals operatiekamers of isolatie kamers). Hierbij is ook oog voor duurzame voorzieningen, aangezien de meeste oogbescherming kan worden hergebruikt na reiniging.
Bij oogbescherming die kan worden hergebruikt, is controle op beschadigingen of verbuigingen van groot belang. Door eventuele beschadigingen of verbuigingen sluit het product mogelijk niet meer goed aan op de ogen waardoor deze onvoldoende bescherming biedt.
Reinigen en desinfecteren van een herbruikbaar oogbeschermingsmiddel.
Reinig en indien nodig desinfecteer een herbruikbaar oogbeschermingsmiddel na gebruik volgens voorschrift van de fabrikant met een desinfectans dat de fabrikant voorschrijft. Hiervoor wordt verwezen naar de SRI richtlijn Reiniging en desinfectie ruimte.
Randvoorwaarden voor gebruik
- Plaats het oogbeschermingsmiddel voor het gezicht/de ogen en zorg dat het de ogen beschermt.
- Verwissel de oogbescherming zo snel mogelijk als deze verontreinigd of nat is.
- Verwijder, na gebruik of bij verwisselen, het oogbeschermingsmiddel door de bandjes of de pootjes beet te pakken en raak daarbij de voorkant van het oogbeschermingsmiddel niet aan met de handen. Dit verkleint de kans op contaminatie van de handen.
- Desinfecteer de oogbescherming direct na gebruik en pas handhygiëne toe om verspreiding van micro-organismen via de handen te voorkomen.
Onderbouwing
Achtergrond
Oogbescherming wordt gedragen bij vormen van isolatiezorg waarbij risico bestaat op verspreiding van micro-organismen via spatten of spetten. Oogbescherming wordt ook gedragen indien er kans is op spatten van lichaamsvocht. Een voorbeeld hiervan is bijvoorbeeld de kans op spat/spuugaccidenten bij niet-coöperatieve patiënten op de SEH of in de GGZ.
Er zijn diverse soorten oogbescherming beschikbaar. Dit zijn verschillende modellen van brillen en gelaatsschermen die gedragen worden om de ogen te beschermen.
Doel van deze module is het beschrijven wanneer het gebruik van oogbescherming bijdraagt aan het (doelmatig en kosteneffectief) verkleinen van de kans op transmissie van micro-organismen via en/of naar medewerkers. Hierbij wordt aandacht besteed aan indicaties voor gebruik van oogbescherming op basis van de eigenschappen van deze middelen conform wet- en regelgeving.
Conclusies / Summary of Findings
|
Moderate GRADE |
Wearing eye protection likely reduces viral respiratory healthcare-related infections compared to not wearing eye protection by health care workers.
Sources: Chu, 2020; Tian, 2021 |
Samenvatting literatuur
Description of studies
Chu (2020) performed a systematic review investigating prevention of person-to-person infections of SARS-CoV2 and COVID-19 by physical distance, face masks and eye protection. A literature search was performed on 26-03-2020, in databases: Medline, PubMed, Embase, CINAHL, the Cochrane Library, COVID-19 Open Research Dataset Challenge, COVID-19 Database (WHO), Epistemonikos, EPPI centre living systematic map of the evidence, ClinicalTrials.gov, WHO International Clinical Trials Registry Platform, relevant documents on websites of governments, reference lists of studies and of systematic reviews. Up to May 3, 2020, the authors hand searched preprint servers and coronavirus resource centres of the Lancet, JAMA, and NEJM. No language restrictions were applied. All study designs, all publication types, and all settings were included. Only studies with patients with confirmed (laboratory confirmation with or without symptoms) or probable (suspected to be infected without laboratory confirmation) WHO-defined COVID-19, SARS, or MERS were included. No exclusion criteria were applied. The search resulted in 20013 records, of which 604 were assessed full text. Of those, 172 studies met inclusion criteria for the systematic review, of which 44 comparative studies were included in the meta-analyses. GRADE was applied to determine the level of evidence. Risk of bias was assessed using the Newcastle-Ottawa Scale. For this module, we only included 14 studies about eye protection in the systematic literature analysis.
Tian (2021) performed a systematic review to study risk factors and protective measures for highly infectious viral respiratory epidemics. A literature search was performed on 6-7-2020, in databases: Medline, PubMed, Embase, CINAHL and Cochrane Central. Inclusion criteria were article written in English, study focused on human subjects, study population comprised of health care workers (HCWs), and about pandemic respiratory diseases (such as COVID-19, MERS, SARS, H1N1, H5N1). Case studies, case series, editorials, narrative reviews, opinion papers, news articles and letters (to the editor) were excluded, as well as studies with small number of patients). The search resulted in 5715 hits, of which 206 were assessed full text. In total, 54 studies met inclusion criteria and were included in the meta-analysis. GRADE was applied to determine the level of evidence per outcome measure. Risk of bias was assessed using the Newcastle-Ottawa Scale. For this module, we only included 11 studies about face protection (visors, goggles, face shields, etc.).
Results
Preventing transmission of micro-organisms and health care related infections
Data of two systematic reviews were combined in our analysis. In total, 18 studies were included which reported on the use of eye protection in preventing viral respiratory infections (Figure 1). Seven studies were included in both systematic reviews (Alraddadi, 2016; Caputo, 2006; Chen, 2009; Kim, 2016; Liu, 2009; Pei, 2006; Lau, 2004). Seven studies were only included in the systematic review by Chu (2020) because of the low number of participants and/or the article being written in Chinese (Burke, 2020; Ki, 2019; Ma, 2004; Park, 2004; Peck, 2004; Ryu, 2019; Yin, 2004). Two studies were only included by the systematic review of Tian (2021), because of the micro-organism (influenza virus) (Kuster, 2013; Toyokawa, 2011), one because of the publication date being after the search date of Chu (2021) (Chatterjee, 2020), and one for unknown reasons (Raboud, 2010).
For the outcome measure infections, pooling of data resulted in a risk ratio of 0.41 (95% CI: 0.27 – 0.61; Figure 5.1), in favor of wearing eye protection. This result is clinically relevant and statistically significant.
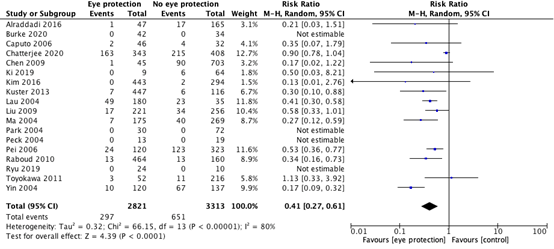
Figure 5.1. Forest plot of results of included studies. Wearing of eye protection versus not wearing eye protection and its effect on preventing viral respiratory infections in HCW. Pooled risk ratio, random effects model.
Level of evidence of the literature
The level of evidence regarding the outcome measure infections started at GRADE low (comparative, observational studies) and was not downgraded. Although the heterogeneity (I2) is 80%, the level of evidence was not downgraded, since all but one (small) study favor eye protection. Following the GRADE handbook, the pooled effect size is considered large and new studies are very likely to observe the same effect. The level of evidence was therefore upgraded to GRADE moderate.
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question: When does the wearing of eye protection provide added value in limiting the chance of transmitting health care related infections via and/or to health care workers?
P: Health care worker in contact with patients or body fluids of patients
I: Wearing eye protection
C: Not wearing eye protection
O: Preventing transmission of micro-organisms and health care related infections
Relevant outcome measures
The guideline development group considered prevention of transmission of micro-organisms and health care related infections as a critical outcome measure for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The working group defined the GRADE-standard limit of 25% difference for dichotomous outcomes (RR < 0.8 or > 1.25), and 10% for continuous outcomes as a minimal clinically (patient) important difference.
Search and select (methods)
The databases Embase, Ovid/Medline and Cinahl were searched with relevant search terms from 1 January 2014 until 18 May 2022. For this guideline, all PICOs for different types of PPE were taken together in one search, except for gowns. The detailed search strategy is available on request (info@sri-richtlijnen.nl). The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 671 hits. Studies were selected based on the following criteria: reporting on personal protective equipment (PPE) and its role in transmission of micro-organisms. The search was limited to systematic reviews and RCTs, since the number of hits for observational studies was impracticable. Studies regarding the operating room were excluded since these issues are addressed in the SRI guideline “Infectiepreventie op het OK-complex”. For eye protection, 9 studies were initially selected based on title and abstract screening. After reading the full text, two systematic reviews were included (Chu 2020, Tian 2021) and 7 studies were excluded (see the table with reasons for exclusion under the tab Methods).
Results
Two systematic reviews were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables. Included articles of the systematic reviews were compared and discrepancies were identified and analyzed. Only studies about eye protection were included in this analysis. The summary of literature, results and evidence tables are included below.
Referenties
- Alraddadi BM, Al-Salmi HS, Jacobs-Slifka K, Slayton RB, Estivariz CF, Geller AI, Al-Turkistani HH, Al-Rehily SS, Alserehi HA, Wali GY, Alshukairi AN, Azhar EI, Haynes L, Swerdlow DL, Jernigan JA, Madani TA. Risk Factors for Middle East Respiratory Syndrome Coronavirus Infection among Healthcare Personnel. Emerg Infect Dis. 2016 Nov;22(11):1915-1920. doi: 10.3201/eid2211.160920. PMID: 27767011; PMCID: PMC5088034.
- Burke RM, Balter S, Barnes E, Barry V, Bartlett K, Beer KD, Benowitz I, Biggs HM, Bruce H, Bryant-Genevier J, Cates J, Chatham-Stephens K, Chea N, Chiou H, Christiansen D, Chu VT, Clark S, Cody SH, Cohen M, Conners EE, Dasari V, Dawson P, DeSalvo T, Donahue M, Dratch A, Duca L, Duchin J, Dyal JW, Feldstein LR, Fenstersheib M, Fischer M, Fisher R, Foo C, Freeman-Ponder B, Fry AM, Gant J, Gautom R, Ghinai I, Gounder P, Grigg CT, Gunzenhauser J, Hall AJ, Han GS, Haupt T, Holshue M, Hunter J, Ibrahim MB, Jacobs MW, Jarashow MC, Joshi K, Kamali T, Kawakami V, Kim M, Kirking HL, Kita-Yarbro A, Klos R, Kobayashi M, Kocharian A, Lang M, Layden J, Leidman E, Lindquist S, Lindstrom S, Link-Gelles R, Marlow M, Mattison CP, McClung N, McPherson TD, Mello L, Midgley CM, Novosad S, Patel MT, Pettrone K, Pillai SK, Pray IW, Reese HE, Rhodes H, Robinson S, Rolfes M, Routh J, Rubin R, Rudman SL, Russell D, Scott S, Shetty V, Smith-Jeffcoat SE, Soda EA, Spitters C, Stierman B, Sunenshine R, Terashita D, Traub E, Vahey GM, Verani JR, Wallace M, Westercamp M, Wortham J, Xie A, Yousaf A, Zahn M. Enhanced contact investigations for nine early travel-related cases of SARS-CoV-2 in the United States. PLoS One. 2020 Sep 2;15(9):e0238342. doi: 10.1371/journal.pone.0238342. PMID: 32877446; PMCID: PMC7467265.
- Caputo KM, Byrick R, Chapman MG, Orser BJ, Orser BA. Intubation of SARS patients: infection and perspectives of healthcare workers. Can J Anaesth. 2006 Feb;53(2):122-9. doi: 10.1007/BF03021815. PMID: 16434750.
- Chatterjee P, Anand T, Singh KJ, Rasaily R, Singh R, Das S, Singh H, Praharaj I, Gangakhedkar RR, Bhargava B, Panda S. Healthcare workers & SARS-CoV-2 infection in India: A case-control investigation in the time of COVID-19. Indian J Med Res. 2020 May;151(5):459-467. doi: 10.4103/ijmr.IJMR_2234_20. PMID: 32611916; PMCID: PMC7530442.
- Chen WQ, Ling WH, Lu CY, Hao YT, Lin ZN, Ling L, Huang J, Li G, Yan GM. Which preventive measures might protect health care workers from SARS? BMC Public Health. 2009 Mar 13;9:81. doi: 10.1186/1471-2458-9-81. PMID: 19284644; PMCID: PMC2666722.
- Chu, D. K., Akl, E. A., Duda, S., Solo, K., Yaacoub, S., Schünemann, H. J., & COVID-19 Systematic Urgent Review Group Effort (SURGE) study authors (2020). Physical distancing, face masks, and eye protection to prevent person-to-person transmission of SARS-CoV-2 and COVID-19: a systematic review and meta-analysis. Lancet (London, England), 395(10242), 19731987. https://doi.org/10.1016/S0140-6736(20)31142-9.
- Ki HK, Han SK, Son JS, Park SO. Risk of transmission via medical employees and importance of routine infection-prevention policy in a nosocomial outbreak of Middle East respiratory syndrome (MERS): a descriptive analysis from a tertiary care hospital in South Korea. BMC Pulm Med. 2019 Oct 30;19(1):190. doi: 10.1186/s12890-019-0940-5. PMID: 31666061; PMCID: PMC6822455.
- Kim T, Jung J, Kim SM, Seo DW, Lee YS, Kim WY, Lim KS, Sung H, Kim MN, Chong YP, Lee SO, Choi SH, Kim YS, Woo JH, Kim SH. Transmission among healthcare worker contacts with a Middle East respiratory syndrome patient in a single Korean centre. Clin Microbiol Infect. 2016 Feb;22(2):e11-e13. doi: 10.1016/j.cmi.2015.09.007. Epub 2015 Sep 15. PMID: 26384679; PMCID: PMC7128147.
- Kuster SP, Coleman BL, Raboud J, McNeil S, De Serres G, Gubbay J, Hatchette T, Katz KC, Loeb M, Low D, Mazzulli T, Simor A, McGeer AJ; Working Adult Influenza Cohort Study Group. Risk factors for influenza among health care workers during 2009 pandemic, Toronto, Ontario, Canada. Emerg Infect Dis. 2013 Apr;19(4):606-15. doi: 10.3201/eid1904.111812. PMID: 23631831; PMCID: PMC3647716.
- Lau JT, Lau M, Kim JH, Tsui HY, Tsang T, Wong TW. Probable secondary infections in households of SARS patients in Hong Kong. Emerg Infect Dis. 2004 Feb;10(2):235-43. doi: 10.3201/eid1002.030626. PMID: 15030689; PMCID: PMC3322902.
- Liu W, Tang F, Fang LQ, De Vlas SJ, Ma HJ, Zhou JP, Looman CWN, Richardus JH, Cao WC. Risk factors for SARS infection among hospital healthcare workers in Beijing: a case control study. Trop Med Int Health. 2009 Nov;14(Suppl 1):529. doi: 10.1111/j.1365-3156.2009.02255.x. Epub 2009 Jun 5. PMCID: PMC7169729.
- Ma HJ, Wang HW, Fang LQ, Jiang JF, Wei MT, Liu W, Zhao QM, Ma J, Cao WC. [A case-control study on the risk factors of severe acute respiratory syndromes among health care workers]. Zhonghua Liu Xing Bing Xue Za Zhi. 2004 Sep;25(9):741-4. Chinese. PMID: 15555351.
- Park BJ, Peck AJ, Kuehnert MJ, Newbern C, Smelser C, Comer JA, Jernigan D, McDonald LC. Lack of SARS transmission among healthcare workers, United States. Emerg Infect Dis. 2004 Feb;10(2):244-8. doi: 10.3201/eid1002.030793. PMID: 15030690; PMCID: PMC3322937.
- Peck AJ, Newbern EC, Feikin DR, Issakbaeva ET, Park BJ, Fehr J, LaMonte AC, Le TP, Burger TL, Rhodes LV 3rd, Weltman A, Erdman D, Ksiazek TG, Lingappa JR; SARS Pennsylvania Case Investigation Team. Lack of SARS transmission and U.S. SARS case-patient. Emerg Infect Dis. 2004 Feb;10(2):217-24. doi: 10.3201/eid1002.030746. PMID: 15030686.
- Pei LY, Gao ZC, Yang Z, Wei DG, Wang SX, Ji JM, Jiang BG. Investigation of the influencing factors on severe acute respiratory syndrome among health care workers. Beijing Da Xue Xue Bao Yi Xue Ban. 2006 Jun 18;38(3):271-5. PMID: 16778970.
- Raboud J, Shigayeva A, McGeer A, Bontovics E, Chapman M, Gravel D, Henry B, Lapinsky S, Loeb M, McDonald LC, Ofner M, Paton S, Reynolds D, Scales D, Shen S, Simor A, Stewart T, Vearncombe M, Zoutman D, Green K. Risk factors for SARS transmission from patients requiring intubation: a multicentre investigation in Toronto, Canada. PLoS One. 2010 May 19;5(5):e10717. doi: 10.1371/journal.pone.0010717. PMID: 20502660; PMCID: PMC2873403.
- Ryu B, Cho SI, Oh MD, Lee JK, Lee J, Hwang YO, Yang JS, Kim SS, Bang JH. Seroprevalence of Middle East respiratory syndrome coronavirus (MERS-CoV) in public health workers responding to a MERS outbreak in Seoul, Republic of Korea, in 2015. Western Pac Surveill Response J. 2019 Jun 6;10(2):46-48. doi: 10.5365/wpsar.2018.9.3.002. PMID: 31720054; PMCID: PMC6831962.
- Tian, C., Lovrics, O., Vaisman, A., Chin, K. J., Tomlinson, G., Lee, Y., Englesakis, M., Parotto, M., & Singh, M. (2022). Risk factors and protective measures for healthcare worker infection during highly infectious viral respiratory epidemics: A systematic review and meta-analysis. Infection control and hospital epidemiology, 43(5), 639650. https://doi.org/10.1017/ice.2021.18.
- Toyokawa T, Sunagawa T, Yahata Y, Ohyama T, Kodama T, Satoh H, Ueno-Yamamoto K, Arai S, Araki K, Odaira F, Tsuchihashi Y, Takahashi H, Tanaka-Taya K, Okabe N. Seroprevalence of antibodies to pandemic (H1N1) 2009 influenza virus among health care workers in two general hospitals after first outbreak in Kobe, Japan. J Infect. 2011 Oct;63(4):281-7. doi: 10.1016/j.jinf.2011.05.001. Epub 2011 May 8. PMID: 21723615.
- Yin WW, Gao LD, Lin WS, Gao LD, Lin WS, Du L, Zhang XC, Zou Q, Li LH, Liang WJ, Peng GW, He JF, Yu DW, Zhou DH, Lin JY, Zeng G. [Effectiveness of personal protective measures in prevention of nosocomial transmission of severe acute respiratory syndrome]. Zhonghua Liu Xing Bing Xue Za Zhi. 2004 Jan;25(1):18-22. Chinese. PMID: 15061941.
Evidence tabellen
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Chu, 2020 PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of RCTs / cohort / case-control studies Searched up to 26-3-2020, snowballing up to 3-5-2020. Databases: A: Alraddadi (2016) Study design: all are non-randomized comparative studies Setting and Country: Source of funding and conflicts of interest: |
Inclusion criteria SR: Exclusion criteria SR: 172 studies in review, of which 44 studies in meta-analysis, of which 13 for eye protection (which are included in this review) Important patient characteristics: |
Describe intervention: Eye protection (visors, goggles, face shields, etc.) |
Describe control: No eye protection |
Endpoint of follow-up: For how many participants were no complete outcome data available? |
Outcome measure Effect measure: RR [95% CI]: aOR: 0·22 (0·12–0·39) (2 studies: Yin, Ma) favouring eye protection |
Facultative: Sensitivity analyses: Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroup analysis) |
|
Tian, 2021 |
SR and meta-analysis of RCTs / cohort / case-control studies Searched up to 06-07-2020 Databases: MEDLINE (via Ovid), PubMed, Embase, CINAHL (via Ovid), Cochrane Central A: Alraddadi (2016) A until G are similar to Chu (2020) and are therefore not specified in this row. Study design: Setting and Country: Source of funding and conflicts of interest: from text: “Support was provided solely from institutional and/or departmental sources. MS is supported by the Canadian Anesthesiologists Society Career Scientist Award, as well as the Merit Awards Program from the Department of Anesthesia at the University of Toronto… M.S. serves on the medical advisory board of the Hypersomnia Foundation on a voluntary basis. The remaining authors declare no competing interests.” |
Inclusion criteria SR: Exclusion criteria SR: 54 studies included of which 11 for face protection Important patient characteristics: |
Describe intervention: Face protection (visors, goggles, face shields, etc.) |
Describe control: No face protection |
Endpoint of follow-up: For how many participants were no complete outcome data available? |
Outcome measure Effect measure: OR [95% CI]: Pooled effect (random effects model): (including A until K): |
Facultative: Newcastle Ottowa Scale was used for all studies. Sensitivity analyses (excluding small studies; excluding studies with short follow-up; excluding low quality studies; relevant subgroup-analyses); mention only analyses which are of potential importance to the research question Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroup analysis) |
Exclusie-tabel
|
Author and year |
Reason for exclusion |
|
Matos AG, Sarquis IC, Santos AAN, Cabral LP. COVID-19: risk of ocular transmission in health care professionals. Rev Bras Med Trab. 2021 Apr 30;19(1):82-87. doi: 10.47626/1679-4435-2021-598. PMID: 33986784; PMCID: PMC8100763. |
Wrong study design (literature review, not systematic) |
|
Nguyen-Van-Tam JS, Killingley B, Enstone J, Hewitt M, Pantelic J, Grantham ML, Bueno de Mesquita PJ, Lambkin-Williams R, Gilbert A, Mann A, Forni J, Noakes CJ, Levine MZ, Berman L, Lindstrom S, Cauchemez S, Bischoff W, Tellier R, Milton DK; EMIT Consortium. Minimal transmission in an influenza A (H3N2) human challenge-transmission model within a controlled exposure environment. PLoS Pathog. 2020 Jul 13;16(7):e1008704. doi: 10.1371/journal.ppat.1008704. PMID: 32658939; PMCID: PMC7390452. |
Better systematic review available |
|
Hegde S. Which type of personal protective equipment (PPE) and which method of donning or doffing PPE carries the least risk of infection for healthcare workers? Evid Based Dent. 2020 Jun;21(2):74-76. doi: 10.1038/s41432-020-0097-3. PMID: 32591668; PMCID: PMC7317256. |
Better systematic review available |
|
French CE, McKenzie BC, Coope C, Rajanaidu S, Paranthaman K, Pebody R, Nguyen-Van-Tam JS; Noso-RSV Study Group, Higgins JP, Beck CR. Risk of nosocomial respiratory syncytial virus infection and effectiveness of control measures to prevent transmission events: a systematic review. Influenza Other Respir Viruses. 2016 Jul;10(4):268-90. doi: 10.1111/irv.12379. Epub 2016 Mar 24. PMID: 26901358; PMCID: PMC4910170. |
Better systematic review available |
|
Byambasuren O, Beller E, Clark J, Collignon P, Glasziou P. The effect of eye protection on SARS-CoV-2 transmission: a systematic review. Antimicrob Resist Infect Control. 2021 Nov 4;10(1):156. doi: 10.1186/s13756-021-01025-3. PMID: 34736533; PMCID: PMC8567128. |
Better systematic review available |
|
Chatterjee P, Anand T, Singh KJ, Rasaily R, Singh R, Das S, Singh H, Praharaj I, Gangakhedkar RR, Bhargava B, Panda S. Healthcare workers & SARS-CoV-2 infection in India: A case-control investigation in the time of COVID-19. Indian J Med Res. 2020 May;151(5):459-467. doi: 10.4103/ijmr.IJMR_2234_20. PMID: 32611916; PMCID: PMC7530442. |
Included in the systematic review |
|
Chughtai AA, Chen X, Macintyre CR. Risk of self-contamination during doffing of personal protective equipment. Am J Infect Control. 2018 Dec;46(12):1329-1334. doi: 10.1016/j.ajic.2018.06.003. Epub 2018 Jul 17. PMID: 30029796. |
Better systematic review available |
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 11-11-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule is ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en is gefinancierd door het ministerie van VWS. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep samengesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep).
De werkgroep bestaat uit:
- Dr. M.S.L. Liem (voorzitter), chirurg, Nederlandse Vereniging voor Heelkunde (NVvH)
- Dr. S.J. Vainio, arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. H.F. Wunderink, arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. K.E. Veldkamp, arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. J.M.T. Klein Gunnewiek, klinisch chemicus, Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde (NVKC)
- Dr. A.M.L. Oude Lashof, internist-infectioloog, Nederlandse Vereniging van Internist-Infectiologen (NIV/NVII)
- Dr. J. Honings, KNO-arts/Hoofd-hals chirurg, Nederlandse Vereniging voor KNO-heelkunde (NVKNO)
- Dr. L.A.M. Bruijstens, anesthesioloog, Nederlandse Vereniging voor Anesthesiologen (NVA)
- M. den Otter, Verpleegkundig specialist, Verpleegkundigen & Verzorgenden Nederland (V&VN)
- Drs. A. Harteloh-Schepers, Specialist Ouderengeneeskunde, Verenso(t/m juli 2022)
- Drs. D.C.M. aan de Stegge. Specialist Ouderengeneeskunde, Verenso(vanaf oktober 2022)
- Drs. K. Weijdema, deskundige infectiepreventie, Rijksinstituut voor Volksgezondheid en Milieu (RIVM)
- Dr. H. Ruijs, arts maatschappij en gezondheid, Rijksinstituut voor Volksgezondheid en Milieu (RIVM)
- G. Stoffer BSc, deskundige infectiepreventie, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- Ing. E. de Bruijne, deskundige infectiepreventie, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- Drs. R.J. Naber, bedrijfsarts, Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB)
- J. Luijten, arbeidshygiënist, Nederlandse Vereniging voor Arbeidshygiëne (NVvA)
Met ondersteuning van:
- Dr. I. van Dusseldorp, literatuurspecialist, Kennisinstituut van Federatie Medisch Specialisten
- Dr. E. Belfroid, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. A.E. Sussenbach, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- A. Eikelenboom-Boskamp, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.J. Versteeg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. H. Graveland, senior adviseur, Kennisinstituut van Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard dat zij in de laatste drie jaar wel/geen directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. M.S.L. Liem |
chirurg, Medisch manager operatie-kamers, MST - Enschede |
SKMS beoordelingen kwaliteitsprojecten (vacatie-gelden). Penningmeester DLSG (onbetaald). Richtlijn commissie NVvH (tot 1 jan. 2022 – onbetaald). Wetenschappelijke cie, DHBA (onbetaald; soms vacatiegelden) |
geen |
Geen actie vereist |
|
Dr. S.J. Vainio |
arts-microbioloog (medisch specialist niet in loondienst), St Antonius Ziekenhuis |
geen |
geen |
Geen actie vereist |
|
Dr. H.F. Wunderink |
arts-microbioloog, UMCU |
geen |
geen |
Geen actie vereist |
|
Dr. K.E. Veldkamp |
arts-microbioloog, hoofd eenheid Infectiepreventie en voorzitter Infectie-commissie LUMC |
Voorzitter werkgroep Hygiëne en Infectiepreventie van de NVMM – onbetaald. Lid algemene visitatiecommissie Medische Microbiologie van de NVMM – onbetaald (m.u.v. vacatiegelden voor visitaties). OMT COVID-19, RIVM –vacatiegelden. |
geen |
Geen actie vereist |
|
Dr. J.M.T. Klein Gunnewiek |
senior adviseur bij Zorgverzekeraars Nederland |
Extern auditor bij de Raad van Accreditatie (ISO 15189). |
geen |
Geen actie vereist |
|
Dr. A.M.L. Oude Lashof |
internist-infectioloog Maastricht UMC+ |
geen |
geen |
Geen actie vereist |
|
Dr. J. Honnigs |
KNO-arts / hoofd-hals chirurg Radboud UMC |
geen |
geen |
Geen actie vereist |
|
Dr. L.A.M. Bruijstens |
anesthesioloog, Radboud UMC |
geen |
geen |
Geen actie vereist |
|
M. den Otter |
verpleegkundig specialist AGZ, St Jansdal ziekenhuis |
V&VN VS bestuur, vacatieregeling |
geen |
Geen actie vereist |
|
Drs. A. Harteloh-Schepers |
Specialist ouderengeneeskunde bij Archipelzorggroep |
RCT lid Rezisto |
geen |
Geen actie vereist |
|
Drs. D.C.M. aan de Stegge |
Werkgever: Beweging 3.0 te Amersfoort. Specialist Ouderengeneeskunde |
geen |
geen |
Geen actie vereist |
|
Drs. K. Weijdema |
deskundige infectiepreventie SRI namens RIVM en LCI |
Lid Green Team infectiepreventie NL |
geen |
Geen actie vereist |
|
Dr. H. Ruijs |
arts maatschappij en gezondheid/Infectieziektebestrijding RIVM, Centrum Infectieziektebestrijding |
geen |
geen |
Geen actie vereist |
|
G. Stoffer BSc |
Deskundige infectiepreventie |
Lid KRIZ commissie |
geen |
Geen actie vereist |
|
Ing. E. de Bruijne |
Deskundige infectiepreventie |
geen |
geen |
Geen actie vereist |
|
Drs. R.J. Naber |
Bedrijfsarts, arbodienst Amsterdam UMC |
Secretaris NVAB werkgroep BaZ. Lid NVAB commissie richtlijnontwikkeling en wetenschap. Lid NVAB commissie Intercollegiale toetsing en deskundigheidsbevordering. |
geen |
Geen actie vereist |
|
J. Luijten |
Arbeidshygiënist en Veiligheidskundige. Werkgever: Isala Zwolle
|
Werkzaam als Arbeidshygiënist en Veiligheidskundige bij de interne arbodienst van Isala in Zwolle. Dit betreft mijn hoofdwerkzaamheden (fulltime) en is een betaalde functie. |
geen |
Geen actie vereist |
Inbreng patiëntenperspectief
Met het uitnodigen van Patiëntfederatie Nederland (PFNL) voor de invitational conference is aandacht besteed aan het patiëntenperspectief. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan PFNL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz en kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wet kwaliteit, klachten en geschillen zorg (Wkkgz). Bij de richtlijn is conform de Wkkgz een kwalitatieve raming uitgevoerd van mogelijke substantiële gevolgen van de aanbevelingen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|
Module wet- en regelgeving |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar is (zijn) (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module handschoenen |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar is (zijn) (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module beschermende kleding (schorten) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module (chirurgische) mondneusmaskers en ademhalingsbeschermingsmaskers |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module pasvormtest (fittest) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module oogbescherming |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module beschermende hoofdbedekking |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module overschoenen en laarzen |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg met betrekking tot persoonlijke beschermingsmiddelen. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnen ‘Persoonlijke beschermingsmiddelen ziekenhuizen’, ‘Persoonlijke beschermingsmiddelen revalidatiecentra’ en ‘Persoonlijke beschermingsmiddelen verpleeghuizen, woonzorgcentra en voorzieningen voor kleinschalig wonen’ op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door SVN, NVP, ActiZ, NOG, IGJ, NVAVG, VGN, NVDV, NVIC en NVR via de invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep conceptuitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid waarin de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
er is hoge zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is zeer onwaarschijnlijk dat de literatuurconclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Redelijk |
er is redelijke zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is mogelijk dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Laag |
er is lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; er is een reële kans dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Zeer laag |
er is zeer lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; de literatuurconclusie is zeer onzeker. |
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet een-op-een vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk om mee te wegen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert-opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van de aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zou de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Randvoorwaarden (organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Formuleren van kennislacunes
Tijdens de ontwikkeling van de richtlijn Persoonlijke beschermingsmiddelen is systematisch gezocht naar onderzoeksbevindingen die nuttig kunnen zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de hiervoor opgestelde zoekvragen is met het resultaat van deze zoekacties te beantwoorden, een groot deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat er nog kennislacunes bestaan. De werkgroep is van mening dat (vervolg)onderzoek wenselijk is om in de toekomst een duidelijker antwoord te kunnen geven op vragen uit de praktijk. Om deze reden heeft de werkgroep per module aangegeven waar wetenschappelijke kennis beperkt is en dus op welke vlakken nader onderzoek gewenst is.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule is aan de betrokken (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S,Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
