Behandeling externe rectumprolaps
Uitgangsvraag
Wat is de optimale chirurgische behandeling van externe rectumprolaps?
Aanbeveling
Behandel een externe rectum prolaps bij voorkeur met een laparoscopische ventrale rectopexie.
Behandel patiënten waarbij transabdominale benadering gecontra-indiceerd is, met een perineale benadering. Bij Delorme’s procedure wordt een combinatie met levatorplastiek geadviseerd. Overweeg bij een Altemeier een combinatie met levatorplastiek.
Overwegingen
De literatuuranalyse om deze uitgangsvraag te beantwoorden heeft zich gericht op gecontroleerde (gerandomiseerde) onderzoeken.
Echter bleek gedurende de zoektocht naar geschikt bewijs dat er weinig kwalitatief goed vergelijkend onderzoek beschikbaar was. Tevens waren de vergelijkende groepen vaak inhomogeen. Zo is binnen de abdominale groep de laparotomische en laparoscopische vaak door elkaar geïncludeerd. En ook werden verschillende operatietechnieken door elkaar gebruikt. Tevens was het onderscheid tussen ERP en IRP ook niet altijd duidelijk.
Of de robot geassisteerde ingreep de voorkeur geniet boven de laparoscopische ingreep is onderzocht in een meta-analyse door Ramage (Ramage, 2015). Drie van de vijf geïncludeerde onderzoeken deden onderzoek naar externe rectum prolaps. Hieruit kon geconcludeerd worden dat er geen significant verschil is in functionele uitkomst, complicaties en aantal recidieven. Dit vraagstuk zou in een grotere trial onderzocht moeten worden met als aanvulling een kostenbatenanalyse, daar waar de robot hogere kosten met zich meebrengt. De werkgroep rectumprolaps adviseert dat het centrum zelf mag beslissen of de laparoscopische rectopexie al dan niet met de robot plaats vindt mits er voldoende expertise aanwezig is.
Tot op heden wordt de perineale benadering verkozen boven een abdominale benadering bij patiënten met een hoge comorbiditeit. Gedateerde onderzoeken tonen namelijk aan dat een abdominale benadering een hoger complicatierisico geeft in vergelijking met een perineale benadering. Echter wordt hier vergeleken met open abdominale chirurgie. De ontwikkeling in minimaal invasieve abdominale chirurgie heeft de ingreep veiliger gemaakt voor patiënten met een hoge comorbiditeit. Zodoende wordt eerdergenoemde stelling langzaamaan in twijfel getrokken. Senapati is de enige gerandomiseerde studie die de perineale benadering heeft vergeleken met een laparoscopische abdominale benadering, echter er worden ook open abdominale benaderingen geïncludeerd zonder dat er onderscheid tussen beiden wordt gemaakt. De uitkomst is dat er geen significant verschil kan worden aangetoond tussen beide groepen op het gebied van zowel complicaties, recidieven als functionele uitkomst. De aantallen zijn bij deze studie wel erg klein (25 versus 19) (Senapati, 2013). Oudere kwalitatief mindere onderzoeken tonen echter wel een significant hogere recidiefkans aan bij de perineale benadering (Kim, 1999; Maramin, 2010). De werkgroep heeft consensus bereikt dat een abdominale benadering de voorkeur geniet en dat een perineale benadering enkel de voorkeur heeft bij patiënten waarbij een abdominale chirurgie is gecontra-indiceerd. Hierbij moet gedacht worden aan patiënten waarbij algehele anesthesie te grote risico’s met zich meebrengt in verband met ernstige cardiale of pulmonale comorbiditeit en/of bij patiënten waarbij de buik ontoegankelijk zou zijn. Bijvoorbeeld wanneer de patiënt multipele abdominale ingrepen heeft ondergaan of een ernstige peritonitis heeft doormaakt met uitgebreide adhesies als gevolg.
Uit de enige geïncludeerde gerandomiseerde studie die de vraag onderzoekt of rectopexie moet worden toegevoegd aan de mobilisatie van het rectum blijkt het bewijs duidelijk dat het toevoegen van een rectopexie, open of laparoscopisch, de kans op een recidief (1,5 versus 8,6%) vermindert (Karas, 2011). De werkgroep is van mening dat bij patiënten met een ERP een rectopexie te prefereren is boven mobilisatie van het rectum alleen.
De vraag of een resectie-rectopexie beter is dan een ventrale mesh rectopexie is een lastig vraagstuk en nooit gerandomiseerd uitgezocht. Aan de ene kant is bewezen dat een resectie-rectopexie een betere uitkomst heeft op ODS-klachten, maar tegelijkertijd een grotere kans heeft op ernstige complicaties, omdat er een naad wordt aangelegd. Senapati heeft in een klein gerandomiseerde groep de resectiegroep vergeleken met een suture rectopexie. Hieruit komt geen significant verschil in recidieven. Wel geeft de resectiegroep significant minder postoperatieve obstipatieklachten dan de suturerectopexie, wat hypothetisch te verklaren is, omdat bij de suturerectopexie een knik in het overtollige colon blijft, die bij de resectierectopexie gereseceerd wordt. Daartegenover bevestigt Senepati een hoger complicatiepercentage in de resectiegroep, maar deze is niet significant (Senapati, 2013). Dit vraagstuk zou in grotere gerandomiseerde trials uitgezocht moeten worden, waarbij gezien de huidige praktijk de LRR vergeleken moet worden met de LVR.
De werkgroep adviseert een laparoscopische ventrale rectopexie (LVR) als eerste keus voor behandeling van een externe rectum prolaps.
De twee meest gebruikte perineale benaderingen zijn Altemeier’s en Delorme’s. Senapati is de enige studie die deze twee ingrepen gerandomiseerd heeft vergeleken, waarbij er geen significant verschil in functionele uitkomst, aantal recidieven en complicaties werd aangetoond (Senapati, 2013). Wel wordt geadviseerd om een Delorme’s te combineren met een levatorplastiek, omdat bewezen is dat dit significant minder recidieven geeft (Youssef, 2013; Voor de Altemeierprocedure is dit vraagstuk enkel retrospectief uitgezocht. Uit deze studie kan geconcludeerd worden dat ook hier een levatorplastiek significant minder recidieven geeft (Chun, 2004). Echter in verband met laag kwalitatief onderzoek is deze studie niet geïncludeerd voor deze richtlijn. De werkgroep adviseert op het moment wanneer een perineale benadering is aangewezen, te kiezen tussen de Altemeier’s of Delorme’s procedure. Welke procedure is de voorkeur van de chirurg. Wanneer er wordt gekozen voor de Delorme’s, adviseert de werkgroep deze te combineren met een levatorplastiek. Over de toevoeging van een levatorplastiek bij een Altemeiere kan de werkgroep geen uitspraak doen en wordt overgelaten een de lokale expertise.
Onderbouwing
Voor de externe rectum prolaps (ERP) wordt onderscheid gemaakt in perineale technieken, de Delorme- en Altemeier procedure, en abdominale technieken, verdeeld in de rectopexie met of zonder resectie van het rectosigmoïd.
Voor de perineale benadering worden twee technieken beschreven, namelijk de Delorme- en Altemeier procedure. Bij de operatie volgens Delorme wordt de prolaberende mucosa gestript en de spierlagen van de prolaps geplisseerd (Youssef, 2013). Bij de techniek volgens Altemeier wordt de gehele prolaps full-thickness gereseceerd vanuit de perineale benadering (Ris, 2012).
Traditioneel wordt perineale chirurgie vooral voorbehouden aan (oudere) patiënten met een hoge comorbiditeit aangezien deze procedure geen abdominale benadering behoeft en vaak met behulp van locoregionale anesthesie kan worden uitgevoerd. Dit zou daarmee een lager perioperatief morbiditeitsrisico, minder pijn, en een kortere opnameduur hebben. Echter heeft de ontwikkeling in minimaal invasieve abdominale chirurgie de voorkeur voor perineale behandeling voor ouderen in twijfel getrokken (Young, 2015).
De abdominale benadering kan verdeeld worden in open, laparoscopisch of robot-geassisteerd. Heden ten dage gaat de voorkeur niet meer uit naar een open benadering, omdat uit de literatuur zou blijken dat dit een significant hoger complicatierisico, hogere kosten, langere opnameduur en een verschil in cosmetisch effect met zich mee zou brengen en geen voordeel biedt op de functionele uitkomst of recidiefkans (Richtlijn Prolaps, NVOG).
De abdominale techniek kan worden verdeeld in de rectopexie met of zonder resectie van het rectosigmoïd. Binnen de rectopexie zijn vele verschillende technieken beschreven. In Nederland wordt de ventrale rectopexie zoals beschreven door D'Hoore het meest toegepast (D'Hoore, 2006). Hierbij wordt alleen de ventrale zijde van het rectum gemobiliseerd en blijven de zenuwen welke van lateraal komen gespaard. De hypothese is dat dit tot minder postoperatieve functionele problemen leidt zoals obstipatie. Het lijkt erop dat dit tot minder postoperatieve obstipatieklachten leidt.
De meest gebruikte abdominale technieken zijn LVR en laparoscopische resectie rectopexie (LRR). Bij beide technieken wordt het rectum alleen ventraal gemobiliseerd wat inhoudt dat de autonome zenuwen aan de laterale zijde worden gespaard. Bij de LVR wordt het ventrale rectum met een mat aan het promotorium bevestigd (D’Hoore, 2006). Bij de LRR wordt het rectosigmoïd gereseceerd en vervolgens wordt het rectum met hechtingen (suture rectopexie) aan het sacrum gefixeerd (Stevenson, 1998). Met het reseceren van het rectosigmoïd wordt de knik in het distale colon opgeheven. De theorie is dat dit tot minder postoperatieve obstipatie leidt (Cadeddu, 2012). Daartegenover staat het aanleggen van een anastomose met alle risico's van dien. Vanwege het risico op naadlekkage wordt geen mat gebruikt bij de LRR. Hoewel meer dan 100 verschillende technieken voor behandeling van RP zijn beschreven bestaan er weinig tot geen goede vergelijkende studies. Bewijs is veelal gebaseerd op losse series waarin een enkele techniek wordt beschreven. Hierdoor beperkt de werkgroep richtlijn rectumprolaps zich tot het beschrijven van deze series in de overwegingen. In deze module worden alleen de operaties beschreven die heden ten dage vaak worden uitgevoerd en beschreven.
Delorme versus Delorme met Levatorplastiek
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat residuele fecale incontinentie vaker voorkomt in de Delorme met Levatorplastiek.
Bronnen (Youssef, 2013) |
Delorme versus Delorme met Levatorplastiek
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat er geen verschil is in obstipatie-klachten tussen de twee benaderingen.
Bronnen (Youssef, 2013) |
Delorme versus Delorme met Levatorplastiek
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat de maximum rest- en druk lager is in de Delorme groep.
Bronnen (Youssef, 2013) |
Delorme versus Delorme met Levatorplastiek
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat de postoperatieve rectale sensatie lager is in de Delorme met Levatorplastiekgroep.
Bronnen (Youssef, 2013) |
Delorme versus Delorme met Levatorplastiek
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat de postoperatieve patiënt-tevredenheid hoger is in de Delorme-groep.
Bronnen (Youssef, 2013) |
Delorme versus Altemeier
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat er geen verschillen zijn in de functionele uitkomsten incontinentie en darmfunctie tussen de Delorme en Altemeier technieken.
Bronnen (Senapati, 2013) |
Delorme versus Altemeier
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat er geen verschil is in het aantal recidieven van de prolaps tussen de Delorme en Altemeier technieken.
Bronnen (Senapati, 2013) |
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie
|
Zeer laag GRADE |
Er zijn zeer voorzichtige aanwijzingen dat functionele uitkomsten in beide groepen dezelfde resultaten geven.
Bronnen (Speakman 1991; Selvaggi 1993; Mollen 2000)) |
Laparoscopische versus open procedure
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat de laparoscopische procedure minder complicaties geeft ten opzichte van de open procedure
Bronnen (Tou, 2015 (specifieke studie: Solomon, 2002)) |
Laparoscopische versus open procedure
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat de laparoscopische procedure gelijke functionele uitkomsten geeft in vergelijking met de open procedure.
Bronnen (Tou, 2015 (specifieke studie: Solomon, 2002; Boccansanta, 1998)) |
Laparoscopische versus open procedure
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat de laparoscopische procedure gelijke uitkomsten geeft wat betreft recidief in vergelijking met de open procedure.
Bronnen (Tou, 2015 (specifieke studie: Solomon, 2002; Boccansanta, 1998)) |
Perineale versus abdominale benadering
|
Zeer laag GRADE |
Er zijn zeer voorzichtige aanwijzingen dat er geen verschillen zijn in recidief, complicaties en functionele uitkomsten tussen de twee benaderingen.
Bronnen (Deen, 1994; Senepati, 2013) |
Resectie versus geen resectie rectopexie
|
Zeer laag GRADE |
Er zijn zeer voorzichtige aanwijzingen dat de functionele uitkomsten en complicaties gelijke uitkomsten geeft voor beide technieken.
Bronnen (Senepati, 2013; Lukkonen, 1992; McKee, 1992) |
Rectopexie versus geen rectopexie
|
Laag GRADE |
Er zijn voorzichtige aanwijzingen dat rectopexie gelijke uitkomsten geeft wat betreft complicaties in vergelijking met geen rectopexie.
Bronnen (Senapati, 2013) |
Rectopexie versus geen rectopexie
|
Matig GRADE |
Er zijn aanwijzingen dat rectopexie leidt tot minder recidieven van rectum prolaps vergeleken met alleen rectale mobilisatie (geen rectopexie).
Bronnen (Karas, 2011) |
Laparoscopisch versus robot geassisteerd
|
Laag GRADE |
Er zijn geen verschillen in de functionele uitkomst incontinentie tussen de laparoscopische en robot-geassisteerde technieken.
Bronnen (De Hoog, 2009; Mehmood, 2014) |
Laparoscopisch versus robot geassisteerd
|
Laag GRADE |
Er zijn geen verschillen in het aantal recidieven van de prolaps tussen de laparoscopische en robot-geassisteerde technieken.
Bronnen (De Hoog, 2009; Mehmood, 2014) |
Laparoscopisch versus robot geassisteerd
|
Laag GRADE |
Er zijn geen verschillen in het aantal postoperatieve complicaties tussen de laparoscopische en robot-geassisteerde technieken.
Bronnen (Mehmood, 2014) |
Beschrijving studies
Twee systematische reviews onderzochten het effect van verschillende chirurgische interventies voor RP bij volwassenen.
In de review van Tou (2015) werden enkel prospectieve gerandomiseerde trials geïncludeerd die de effecten van verschillende chirurgische technieken onderzochten voor de behandeling van een externe rectum prolaps. De zoekstrategie werd in februari 2015 uitgevoerd. De geïncludeerde studies hadden betrekking op vijf verschillende chirurgische technieken voor behandeling van externe rectumprolaps, namelijk: Thiers procedure, perineale resectie, transabdominale rectopexie, transabdominale resectie, en transabdominale mobilisatie van het rectum.
Uiteindelijk werden er vijftien (quasi-) gerandomiseerde gecontroleerde trials in de review geïncludeerd, met in totaal 1.007 patiënten. De vier primaire uitkomstmaten waren: het aantal patiënten met een recidief rectum prolaps, het aantal patiënten met een residuele mucosale prolaps, het aantal patiënten met fecale incontinentie en het aantal patiënten met obstipatie. De heterogeniteit aan interventies en uitkomsten in de studies maakt het moeilijk om zij met elkaar te vergelijken. In deze trials werden negen verschillende vergelijkingen tussen interventies gemaakt. De vergelijkingen uit de richtlijn prolaps (Richtlijn Prolaps NVOG, 2014) werden als uitgangspunt genomen en geüpdatet met de nieuwe informatie uit Tou (2015).
Voor de literatuuranalyse werden de volgende vergelijkingen meegenomen:
- vergelijkingen van twee perineale benaderingen: Delorme’s procedure (Youssef, 2013) en Altemeiers’s procedure (Senapati, 2013);
- behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie (Speakman 1991; Selvaggi 1993; Mollen 2000);
- laparoscopsich versus open procedure (Boccasanta, 1998 en Solomon, 2002);
- abdominale versus perineale benadering (Deen, 1994; Senapati, 2013);
- resectie versus geen resectie rectopexie (Lukkonen, 1992; McKee, 1992; Senapati, 2013);
- rectopexie versus geen rectopexie (Karas, 2011);
- laparoscopisch versus robot geassisteerd (Mehmood, 2014; de Hoog 2009; Heemskerk, 2007).
In de review van Ramage (2015) werd gezocht naar studies die een vergelijking maakten tussen robot geassisteerde ventrale rectopexie en niet-robot geassisteerde laparoscopische ventrale rectopexie bij patiënten met een rectum prolaps. De zoekstrategie werd in mei 2014 uitgevoerd. In totaal zijn in deze review vijf studies geïncludeerd, waarvan er één gerandomiseerd was, drie niet-gerandomiseerd en één een retrospectieve cohortstudie betrof. In totaal beschreven deze vijf studies gezamenlijk 244 patiënten. De belangrijkste uitkomstmaten waren: Intra-operatieve tijd, conversie naar open rectopexie, aantal complicaties (intra-operatief en postoperatief), opnameduur, recidief, postoperatieve Cleveland-score.
Perineale benaderingen
Delorme versus Delorme met Levatorplastiek (Tou, 2015)
Eén studie in de review van Tou, 2015, beschreef deze vergelijking (Youssef, 2013). In deze studie werden 41 patiënten gerandomiseerd naar de Delorme met Levatorplastiek en 41 patiënten naar de Delorme techniek.
Delorme versus Altemeier (Tou, 2015)
In de review van Tou (2015) werd één studie geïncludeerd (Senapati, 2013). In de studie van Senapati (2013) werden drie vergelijkingen gemaakt, één daarvan was de vergelijking tussen de Altemeier’s of Delorme’s procedure. Patiënten (n=293) werden volgens een gerandomiseerde procedure verdeeld tussen abdominale of perineale chirurgie. Daarna werden de patiënten uit de perineale chirurgie groep nogmaals gerandomiseerd ofwel volgens de voorkeur van de chirurg ingedeeld tussen Altemeier’s (n=106) en Delorme’s (n=107).
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie (Tou, 2015)
Drie kleine studies (Speakman 1991; Selvaggi 1993; Mollen 2000) vergeleken de effecten van klieven versus behoud van de ligamenten. Eén van de drie studies was alleen als abstract beschikbaar (Selvaggi, 1993). Daarom zijn de uitkomsten gebaseerd op twee studies (Speakman 1991, Mollen 2000), waarbij er 21 patiënten in de conservatieve groep zaten en 23 in de groep waarbij de ligamenten werden gekliefd.
Laparoscopische versus open procedure (Tou, 2015)
Twee kleine studies (Boccasanta, 1998; Solomon, 2002) beschreven deze vergelijking. In totaal werden 28 patiënten met de laparoscopische techniek behandeld en 32 volgens open benadering.
Perineale versus abdnominale benadering (Tou, 2015)
Twee kleine studies (Deen, 1994; Senepati, 2013) beschreven de vergelijking tussen de abdominale benadering (totaal van de twee studies: n=29) en de perineale benadering (totaal van de twee studies: n=35). De gerandomiseerde trial van Senepati (2013) is de enige die dit onderzocht heeft. Hierbij werden 44 patiënten gerandomiseerd naar abdominale en perineale benadering. Echter wordt er bij het includeren van de abdominale ingrepen geen onderscheid gemaakt tussen open en laparoscopische benadering.
Resectie versus geen resectie rectopexie (Tou, 2015)
In de gerandomiseerde trial van Senapati (2013) werden drie vergelijkingen gemaakt, één daarvan was de vergelijking tussen suture rectopexie en resectie rectopexie. Patiënten (n=293) werden volgens een gerandomiseerde procedure verdeeld tussen abdominale of perineale chirurgie. Patiënten gerandomiseerd naar de groep abdominale chirurgie werden vervolgens tussen suture rectopexie (n=38) en resectie rectopexie (n=40) ingedeeld, deels door middel van een nieuwe randomisatie en deels op grond van de voorkeur van de chirurg.
In de studie van Lukkonen (1992) (n=30) werd suture resectie rectopexie vergeleken met mesh rectopexie. In de studie van McKee (1992) (n=18): werd in de één groep suture resectie rectopecie uitgevoerd en in de andere groep suture rectopexie.
Rectopexie versus geen rectopexie (Tou, 2015)
In de review van Tou (2015) werd één studie geïncludeerd die betrekking heeft op deze vergelijking (Karas, 2011). In deze multicenter RCT voor patiënten met een ERP werd het rectum bij beide groepen gemobiliseerd tot aan de levator ani. Vervolgens werd bij een van de twee groepen een mesh dan wel suture rectopexie (n=136, 45 laparoscopisch, 91 open) uitgevoerd en vergeleken met een groep (n=116, 48 laparoscopisch, 68 open) waarbij het bleef bij mobilisatie. In hoeverre het rectum verder werd gemobiliseerd (ook posterior of 360°) werd ter plekke door de chirurg bepaald. Echter werd ook hier geen onderscheid gemaakt tussen open en laparoscopische abdominale procedure. Patiënten met preoperatie obstipatie, ondergingen bijkomend een rectosigmoïd resectie. In de geen rectopexie werd in bijna 59% van de gevallen het rectosigmoïd gereseceerd, in de rectopexiegroep was dit 18.3%.
Laparoscopisch versus robot geassisteerd (Ramage, 2015)
In de review van Ramage (2015) werd een vergelijking gemaakt tussen robot-geassisteerde ventrale rectopexie en niet-robot geassisteerde laparoscopische ventrale rectopexie. Er werden vijf studies geïncludeerd met in totaal 244 patiënten. In de review werd van vijf studies uitgegaan, maar omdat drie van de studies specifiek externe rectum prolaps betrof, zijn alleen de resultaten deze drie studies hier beschreven. In alle studies werd de D’Hoore techniek toegepast om de mat te fixeren. Drie studies vergeleken de laparoscopische rectopexie met de robotgeassisteerde rectopexie voor de behandeling van externe rectumprolaps (Mehmood, 2014; De Hoog, 2009; Heemskerk, 2007). Deze studies omvatten in totaal 119 patiënten, waarvan 63 in de laparoscopische groep en 56 in de robot-geassisteerde groep. Van deze drie studies zijn voor deze uitgangsvraag de resultaten, indien mogelijk, gepoold.
Resultaten
Altemeier versus Altemeier met Levatorplastiek
Deze uitgangsvraag is niet met literatuur te onderbouwen, omdat er geen vergelijkende studies zijn gepubliceerd die dit vraagstuk heeft onderzocht en voldoen aan de bovengenoemde inclusiecriteria.
Delorme versus Delorme met Levatorplastiek (Tou, 2015)
De belangrijke resultaten worden beschreven, voor details kunt u de evidence tabel raadplegen.
Er waren geen significante verschillen tussen de twee technieken wat betreft recidief van de prolaps en complicaties.
Functionele uitkomsten
Residuele faecale incontinentie kwam vaker voor in de groep van Delorme met levatorplastiek (OR 0,07; 95%BI van 0,01 tot 0,56, n=82). Obstipatie verschilde niet tussen de technieken. Postoperatieve maximum rustdruk en persdruk waren beide significant lager in de Delormegroep (gemiddeld verschil 8,6; 95%BI van 6,41 tot 10,79 respectievelijk -10,20; 95%BI van 3,96 tot 8,64, n=82). De postoperatieve rectale sensatie was significant lager in de Delorme met levatorplastiek (gemiddeld verschil -10,20; 95%BI van -13,26 tot -7,14, n=82).
Patiënt tevredenheidsscore na de operatie
Patiënten in de Delormegroep scoorden significant hoger op postoperatieve patiënt-tevredenheid ten opzichte van Delorme met levatorplastiek (gemiddeld verschil 1,5; 95%BI van 1,02 tot 1,98, n=82).
Delorme versus Altemeier (Tou, 2015)
De vergelijking tussen de Delorme en de Altemeier procedure werd in één studie gevonden (Senapati, 2013). Geen van de gerapporteerde uitkomsten (recidief, incontinentie score, darmfunctie, kwaliteit van leven) gaven een significant verschil tussen de twee technieken. Pijn/dyspareunia en complicaties werden niet als uitkomstmaten meegenomen in de studie van Senapati. De gedetailleerde uitkomsten kunt u terugvinden in de evidence tabellen.
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie (Tou, 2015)
In de groep waarbij de laterale ligamenten behouden werden, waren minder patiënten met obstipatieklachten na de operatie (OR 0,32; 95%BI van 0.08 tot 1,23, heterogeniteit (I2) van 59%, n=44) maar dit verschil was niet significant. Wel werden in de groep waar de ligamenten werden gekliefd minder recidieven gezien. (OR (fixed) 15,35 met een95% BI van 0,73 tot 321,58). Echter was ook dit verschil niet significant.
De overige uitkomsten werden alleen in één van beide studies beschreven. De defecatie frequentie was lager in de groep waarbij de ligamenten werden behouden (gemiddeld verschil -1; 95%BI van -1,39 tot -0,61, n=18). De verschillen tussen de behandelingen voor obstipatie score, anale druk en postoperatieve complicaties waren niet significant. Voor specifieke uitkomsten kunt u de evidence tabel raadplegen.
Laparoscopische versus open procedure (Tou, 2015)
De uitkomsten werden alleen in één van beide studies beschreven. Geen van de recidief of functionele uitkomsten gaven een significant verschil. Complicaties kwamen significant minder vaak voor in de laparoscopische groep (OR 0,15, 95%BI van 0,04 tot 0,62, n=39). Voor specifieke uitkomsten kunt u de evidence tabel raadplegen.
Perineale versus abdominale benadering (Tou, 2015)
Recidief van de prolaps kwam minder vaak voor in de perinealegroep (OR 0,64, 95%CI van 0,12 tot 3,55, n=43) maar dit verschil was niet significant. Ook postoperatieve complicaties kwamen minder vaak voor in de perineale groep (OR 0,46, 95%BI van 0,15 tot 1,37, n=54), maar dit verschil was niet significant. Geen van de functionele uitkomsten en de patiënt tevredenheid uitkomsten gaven een significant verschil tussen de beide benaderingen. Specifieke details kunt u vinden in de evidence tabellen.
Resectie versus geen resectie rectopexie (Tou, 2015)
De volgende uitkomsten werden gepoold: obstipatieklachten door de operatie, residuele fecale incontinentie en postoperatieve complicaties.
Het aantal patiënten met obstipatieklachten direct na de operatie was significant hoger in de geen resectie-groep met een OR van 0,14 (95%BI van 0,04 tot 0,44; heterogeniteit (I2) van 0%; n=82). Tijdens follow-up was er geen verschil meer in deze klachten.
Het aantal patiënten met residuale fecale incontinentie was iets lager in de resectie-groep, maar dit verschil was niet significant (OR 0,93; 95%BI van 0,43 tot 2,03; heterogeniteit (I2) van 11%; n=115).
Postoperatieve complicaties kwamen minder vaak voor in de geen resectie-groep maar dit verschil was niet significant (OR 1,89; 95%BI van 0,76 tot 4,73; heterogeniteit (I2) van 0%; n=97).
De overige uitkomsten (darmfunctie, anale rust druk, kwaliteit van leven, recidief en incontinentie score) werden steeds voor één van de drie studies apart beschreven en gaven geen significante verschillen tussen de beide procedures. De uitkomsten pijn/dyspareunia werden niet gerapporteerd voor deze vergelijking.
Rectopexie versus geen rectopexie (Tou, 2015)
In de studie van Karas (2011) had de rectopexie groep statistisch significant minder recidieven van rectum prolaps vergeleken met de geen rectopexiegroep (OR 6,32; 95% BI van 1,36 tot 29,47, n=252).
De geen-rectopexiegroep had minder complicaties maar dit verschil was niet significant verschillend (OR 0,51; 95%BI van 0,24 tot 1,11, n=252). Uitkomsten pijn/dyspareunia werden niet gerapporteerd voor deze vergelijking.
Laparoscopisch versus robot geassisteerd (Ramage, 2015)
In twee studies (De Hoog, 2009; Mehmood 2014) werd gerapporteerd wat het verschil in effect was op incontinentie tussen de twee behandelingen. Er werd geen statistisch significant verschil gevonden (mean difference=-1,02; 95% BI -2,67 tot 0,63; heterogeniteit (I2) van 0%; n=83). (zie figuur 1)
Figuur 1 Incontinentie
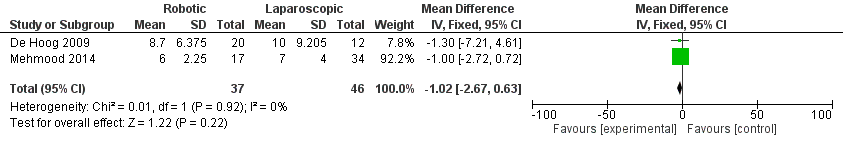
Recidief van de prolaps
In twee studies (De Hoog, 2009; Mehmood 2014) werd gerapporteerd wat het effect van de twee behandelingen was op het aantal recidieven. Er werd geen statistisch significant verschil gevonden (OR=0,69; 95% BI 0,14 tot 3,35, n=86).
Postoperatieve complicaties
In de review van Ramage (2015) werd één studie geïncludeerd die laparoscopische rectopexie vergeleek met de robotgeassisteerde rectopexie voor de behandeling van externe rectumprolaps, met als uitkomstmaat postoperatieve complicaties (Mehmood, 2014). Er werd een trend gezien van minder postoperatieve complicaties in de robot-geassisteerde groep, maar dit was niet statistisch significant (OR=0,13; 95% BI 0,01 tot 2,36, n=34).
De uitkomstmaat pijn/dyspareunia werd niet meegenomen in de geïncludeerde studies.
Bewijskracht van de literatuur
De bewijskracht voor alle uitkomsten in de vergelijking tussen Delorme zonder en met levatorplastiek startte op hoog vanwege de RCT-opzet en is met twee niveaus verlaagd naar lage bewijskracht vanwege het geringe aantal patiënten (imprecisie) en beperkingen in de onderzoeksopzet (onduidelijkheid over randomisatie).
De bewijskracht alle uitkomsten in de vergelijking tussen de Delorme en Altemeier procedure startte op hoog vanwege de RCT-opzet en is met twee niveaus verlaagd naar lage bewijskracht gezien beperkingen in de onderzoeksopzet (onduidelijkheid over blindering) en het geringe aantal patiënten (imprecisie).
De bewijskracht voor alle uitkomsten in de vergelijking tussen behoud van ligamenten versus klieven startte op hoog vanwege de RCT-opzet en is met drie niveaus verlaagd naar zeer lage bewijskracht gezien beperkingen in de onderzoeksopzet (onduidelijkheid over blindering en randomisatie) en het geringe aantal patiënten (imprecisie).
De bewijskracht voor alle uitkomsten in de vergelijking tussen laparoscopische versus open procedure startte op hoog vanwege de RCT-opzet en is met drie niveaus verlaagd naar zeer lage bewijskracht gezien beperkingen in de onderzoeksopzet (onduidelijkheid over blindering en randomisatie) en het geringe aantal patiënten (imprecisie).
De bewijskracht alle uitkomsten in de vergelijking tussen de perineale versus abdominale benadering startte op hoog vanwege de RCT-opzet en is met drie niveaus verlaagd naar zeer lage bewijskracht gezien beperkingen in de onderzoeksopzet (onduidelijkheid over blindering) en het zeer geringe aantal patiënten (twee niveaus voor imprecisie).
De bewijskracht voor alle uitkomsten in de vergelijking tussen resectie versus geen resectie rectopexie startte op hoog vanwege de RCT-opzet en is met drie niveaus verlaagd naar zeer lage bewijskracht gezien beperkingen in de onderzoeksopzet (onduidelijkheid over randomisatie en blindering) en imprecisie.
De bewijskracht voor recidief van de prolaps in de vergelijking tussen rextopexie versus geen rectopexie startte op hoog vanwege de RCT-opzet en is verlaagd naar matige bewijskracht gezien beperkingen in de rapportage van de uitkomstmaten.
De bewijskracht voor complicaties van de prolaps in de vergelijking tussen rextopexie versus geen rectopexie startte op hoog vanwege de RCT-opzet en is met twee niveaus verlaagd naar lage bewijskracht gezien beperkingen in de rapportage van de uitkomstmaten en imprecisie (geen significante verschillen).
De bewijskracht voor functionele uitkomsten, recidief van de prolaps en postoperatieve complicaties in de vergelijking tussen laparoscopisch en robot-geassisteerde rectopexie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (geen randomisatie) en het geringe aantal patiënten (imprecisie).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende wetenschappelijke vraagstelling:
Wat zijn de (on)gunstige effecten van verschillende operatieve benaderingen ter behandeling van externe rectum prolaps?
P patiënten met functionele klachten en externe rectumprolaps;
I alle mogelijke chirurgische technieken ;
Operatief (eventueel met preoperatieve conservatieve behandeling);
Transabdominaal:
Benadering: Laparoscopische versus open versus robotchirurgie;
Technieken: Resectie rectopexie (met of zonder mat), Rectopexie (Lap recto(vagino)pexie, Sutured rectopexie, Wells technique, Ripstein, Orr-Logu, andere technieken);
Transanaal/ transperineaal:
Technieken (STARR (double-stapling PPH), Transtar contour stapler, Transanale mucosectomie volgens Delormes met/zonder levatorplastiek, Transanale mucosectomie volgens Altemeier met/zonder levatorplastiek;
O Functionele uitkomsten, pijn/dyspareunia, recidief van de prolaps en complicaties inclusief infecties en/of erosie van de mesh.
Relevante uitkomstmaten
De werkgroep achtte recidief en complicaties een voor de besluitvorming kritieke uitkomstmaten; en functionele uitkomsten (fecale incontinentie en residuale obstipatie) en pijn/dyspareunia een voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
Voor de modules Chirurgie bij externe rectumprolaps en Chirurgie bij interne rectumprolaps is gebruik gemaakt van de literatuur review uit het hoofdstuk 4.5 Chirurgische behandeling van een rectumprolaps van de richtlijn Prolaps (NVOG in samenwerking met NVVH, 2014). De zoekactie van de module is geüpdatet door deze te herhalen in de databases Medline (OVID) en Embase voor de periode mei 2013 tot en met 20 juli 2015. Er is met relevante zoektermen gezocht naar gerandomiseerde en niet-gerandomiseerde gecontroleerde studies. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De zoekactie leverde 60 resultaten op. Hiervan werden zeven studies op titel en abstract geselecteerd. Na raadpleging van de volledige tekst artikelen zijn vijf studies alsnog geëxcludeerd en zijn twee studies (systematische reviews) definitief geïncludeerd.
Module 4.5 chirurgische behandeling van externe rectum prolaps uit de richtlijn Prolaps, werd beoordeeld op relevante literatuur. Daarin is de Cochrane review van Tou, 2008 geïncludeerd. In de update van de zoekactie werd een update van de Cochrane review geïdentificeerd (Tou, 2015). Deze review werd geïncludeerd voor de huidige richtlijn. De chirurgische vergelijkingen uit de prolaps richtlijn worden hieronder weergegeven, met de resultaten van de review van Tou (2015) daaraan toegevoegd. Andere studies die in de prolaps richtlijn werden beschreven, voldeden niet aan de hierboven beschreven criteria (bijvoorbeeld geen vergelijkende studie) en zijn daarom uit deze module weggelaten (n=11, zie exclusie tabel).
(Resultaten)
Twee systematische reviews (Tou, 2015; Ramage, 2015) zijn opgenomen in de literatuuranalyse. De evidence-tabel en beoordeling van de studiekwaliteit kunt u vinden onder het tabblad Onderbouwing.
- Boccasanta P, Rosati R, Venturi M, et al. Comparison of laparoscopic rectopexy with open technique in the treatment of complete rectal prolapse: clinical and functional results. Surgical Laparoscopy & Endoscopy. 1998;8(6):4605.
- Cadeddu F, Grande M, Sileri P, et al. Focus on abdominal rectopexy for full-thickness rectal prolapse: A meta-analysis of literature. Techniques in Coloproctology. 2012;16(1):105.
- Chun SW, Pikarsky AJ, You SY, et al. Wexner Perineal rectosigmoidectomy for rectal prolapse: role of levatorplasty; Tech Coloproctol. 2004;8:39. DOI 10.1007/s10151-004-0042-z.
- de Hoog DE, Heemskerk J, Nieman FHM, et al. Recurrence and functional results after open versus conventional laparoscopic versus robot-assisted laparoscopic rectopexy for rectal prolapse: a case control study. Int J Colorectal Dis. 2009;24:12011206.
- Deen KI, Grant E, Billingham C, et al. Abdominal resection rectopexy with pelvic floor repair versus perianal rectosigmoidectomy and pelvic floor repair for full-thickness rectal prolapse. The British Journal of Surgery. 1994;81(2):3024.
- D'Hoore A, Penninckx F. Laparoscopic ventral recto(colpo)pexy for rectal prolapse: surgical technique and outcome for 109 patients. Surg.Endosc. 2006;20(12):1919-1923.
- Heemskerk J, de Hoog DE, van Gemert WG, et al. Robot-assisted versus conventional laparoscopic rectopexy for rectal prolapse: a comparative study on costs and time. Dis Colon Rectum. 2007;50:18251830.
- Karas JR, Uranues S, Altomare DF, et al. No rectopexy versus rectopexy following rectal mobilisation for full-thickness rectal prolapse: a randomised controlled trial. Diseases of Colon and Rectum. 2011;54(1):2934.
- Kim DS, Tsang CB, Wong WD, et al. Complete rectal prolapse: evolution of management and results. Dis Colon Rectum. 1999;42(4):460-6; discussion 466-9.
- Lukkonen P, Mikkonen U, Jarvinen H. Abdominal rectopexy with sigmoidectomy versus rectopexy alone for rectal prolapse: a prospective, randomized study. International Journal of Colorectal Disease. 1992;7(4):21922.
- Mckee RF, Lauder JC, Poon FW, et al. A prospective randomized study of abdominal rectopexy with and without sigmoidectomy in rectal prolapse. Surgery, Gynecology and Obstretics. 1992;174(2):1458.
- Mehmood RK, Parker J, Bhuvimanian L, et al. Short-term outcome of laparoscopic versus robotic ventral mesh rectopexy for full-thickness rectal prolapse. Is robotic superior? Int J Colorectal Dis. 2014;29(9):1113-8. doi: 10.1007/s00384-014-1937-4. Epub 2014 Jun 26. PMID: 24965859.
- Mollen RM, Kuijpers JH, Van Hoek F. Effect of rectal mobilisation and lateral sphincter division on colonic and anorectal function. Diseases of the Colon and Rectum. 2000;43(9):12837.
- NVOG. Richtlijn prolapse. 2014.
- Ramage L, Georgiou P, Tekkis P, et al. Is robotic ventral mesh rectopexy better than laparoscopy in the treatment of rectal prolapse and obstructed defecation? A meta-analysis. Tech Coloproctol. 2015;19(7):381-389. PubMed PMID: 26041559.
- Riansuwan W, Hull TL, Bast J, et al. Comparison of perineal operations with abdominal operations for full-thickness rectal prolapse. World J Surg. 2010;34(5):1116-22. doi: 10.1007/s00268-010-0429-0.
- Ris F, Colin JF, Chilcott M, et al. Altemeier's procedure for rectal prolapse: analysis of long-term outcome in 60 patients. Colorectal Disease. 2012;14(9):1106-1111.
- Selvaggi F, Scotto di Carlo E, Silvestri L, et al. Surgical treatment of rectal prolapse: a randomised study [Abstract]. The British Journal of Surgery. 1993;80(Suppl): S89.
- Senapati A, Gray RG, Middleton LJ, et al. PROSPER: a randomised comparison of surgical treatments for rectal prolapse. Colorectal Disease. 2013;15(7):85868.
- Solomon MJ, Young CJ, Eyers AA, et al. Randomized clinical trial of laparoscopic versus open abdominal rectopexy for rectal prolapse. The British Journal of Surgery. 2002;89(1):359.
- Speakman CTM, Madden MV, Nicholls RJ, et alA. Lateral ligament division during rectopexy causes constipation but prevents recurrence: results of a prospective randomized study. The British Journal of Surgery. 1991;78 (12):14313.
- Stevenson AR, Stitz RW, Lumley JW. Laparoscopic-assisted resection-rectopexy for rectal prolapse: early and medium follow-up. Diseases of the Colon and Rectum. 1998;41(1):46-54.
- Tou S, Brown SR, Malik AI, et al. Surgery for complete rectal prolapse in adults. Cochrane Database of Systematic Reviews 2008, Issue 4. [DOI: 10.1002/ 14651858.CD001758.pub2].
- Tou S, Brown SR, Nelson RL. Surgery for complete (full-thickness) rectal prolapse in adults. Cochrane Database Syst Rev. 2015;11:CD001758. Review. PubMed PMID: 26599079.
- Young MT, Jafari MD, Phelan MJ, et al. Carmichael; Surgical treatments for rectal prolapse: how does a perineal approach compare in the laparoscopic era?; Surg Endosc. 2015;29:607613. DOI 10.1007/s00464-014-3707-3.
- Youssef M, Thabet W, El Nakeeb A, et al. Comparative study between Delorme operation with or without postanal repair and levateroplasty in treatment of complete rectal prolapse. International Journal of Surgery. 2013;11(1):528.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Tou, 2015
|
SR and meta-analysis of 15 randomized controlled trials
Literature search up to February 2015
A: Boccasanta, 1998 B: Boccasanta, 2006 C: Deen, 1994 D: Galili, 1997 E: Karas, 2011 F: Lukkonen, 1992 G: McKee, 1992 H: Mollen, 2000 I: Novell, 1994 J: Selvaggi, 1993 K: Senapati, 2013 L: Solomon, 2002 M: Speakman, 1991 N: Winde, 1993 O: Youssef, 2013
Study design: RCT
Setting and Country: A: single centre, Italy B: single centre, Italy C: single centre, UK D: single centre, Israel E: Multicentre, multiple countries F: single centre, Finland G: single centre, UK H: single centre, Netherlands I: single centre, UK J: single centre, Italy K: multiple centre, multiple countries L: single centre, Australia M: single centre, UK N: single centre, Germany O: single centre, Egypt
Source of funding: non-commercial
|
Inclusion criteria SR: All RCT’s of surgery for managing full-thickness rectal prolapse in adults.
Exclusion criteria SR: studies that were not RCTs or if they did not make the prespecified comparisons
15 studies included
Important patient characteristics at baseline: N, mean age, % Male A: 21 patients, 57.3 yrs, 4.7% M B: 40 patients, 72.2 yrs, 7.5% M C: 20 patients, 68 yrs, 0% M D: 37 patients, 70 yrs, 10.8% M E: 252 patients, 56.5 yrs, 26.6% M F: 30 patients, 66 yrs, 6.7% M G: 18 patients, 69.5 yrs, sex unclear H: 18 patients, 56.3 yrs, 11.1% M I: 63 patients, 76.5 yrs, 1.6% J: 20 patients, 62 yrs, 0% M K: 293 patients, 73/58 yrs, 14.3% M L: 39 patients, no details on age+sex M: 26 patients, 54 yrs, 11.5% M N: 47 patients, 59 yrs, 4.3% M O: 82 patients, 40 yrs, 37.8% M
|
A: Laparoscopic stapled mesh (Marlex) rectopexy B: Perineal rectosigmoidectomy with Ultracision and stapled anastomosis C: Perineal rectosigmoidectomy and pelvic floor repair D: Open polyglycolic acid mesh suture rectopexy E: Rectopexy F: Open resection (sigmoid) and suture rectopexy G: Open sigmoid resection and suture rectopexy H: Posterior mesh rectopexy (Well’s procedure) with division I: Open abdominal Ivalon sponge rectopexy J: Anteroposterior Marlex rectopexy with either division of the lateral ligaments K: 1) Abdominal surgery; 2) Delorme’s operation; 3) suture rectopexy L: Laparoscopic M: Open mesh rectopexy with division of lateral ligaments N: Open abdominal mesh (polyglycolic acid) rectopexy O: Delorme’s procedure
|
A: open suture mesh (Mersilene in 6 cases and Marlex in 7) rectopexy B: diathermy and handsewn anastomosis C: abdominal resection rectopexy with pelvic floor repair D: open polypropylene mesh suture rectopexy. E: rectal mobilisation only (no rectopexy). F: open (polyglycolic acid) mesh rectopexy G: open abdominal suture rectopexy H: preservation of the lateral ligaments I: open abdominal suture rectopexy. J: Anteroposterior Marlex rectopexy with preservation of the lateral ligaments K: 1) perineal surgery; 2) Altemeier’s operation; 3) resection rectopexy L: open abdominal rectopexy M: open polypropylene mesh rectopexy with preservation of lateral ligaments
N: open abdominal mesh rectopexy (polyglactin). O: Delorme’s with postanal repair/levatorplasty
|
End-point of follow-up: A: mean 29.5 months B: mean 28.4 months C: median 17 months D: mean 3.7 years E: 5 years F: 6 months G: mean 20 months H: mean 42 months I: mean 47 months J: mean 14 months K: 3 years L: mean 24.2 months M: median 12 months N: mean 50.5 months O: 1 year
For how many participants were no complete outcome data available? (intervention/control) A: no details B: 0 C: no details D: no details E: I: 9; C: 18 F: no details G: I: 1 H: I: 3; C:1 I: 0 J: no details K: 15 did not have surgery, including 1 who died and 1 who withdrew from the trial. No details on 8 patients with regards to surgery or follow-up L: 1 M: no details N: 12:no details O: I: 2; C: 1
|
1a. Delorme’s procedure with levatorplasty versus Delorme’s procedure without levatorplasty Relapse prolaps Recurrent full-thickness prolapse (number of patients) O: OR 0.15 (95%CI 0.02 to 1.27) favouring Delorme with levatorplasty Functional outcomes Residual faecal incontinence (number of patients) O: OR 0.07 (95%CI 0.01 to 0.56) favouring Delorme with levatorplasty Constipation after surgery (number of patients) O: OR 0.61 (95%CI 0.20 to 1.91) favouring Delorme with levatorplasty Postoperative maximum resting pressure O: Mean difference 8.6 (95%CI 6.41 to 10.79) favouring Delorme’s Postoperative maximum squeeze pressure O: Mean difference 6.3 (95%CI 3.96 to 8.64) favouring Delorme’s Postoperative rectal sensation O: Mean difference -10.20 (95%CI -13.26 to -7.14) favouring Delorme’s with Levatorplasty Complications Postoperative complications (number of patients) O: OR 1.54 (95%CI 0.24 to 9.73) favouring Delorme’s with levatorplasty Patient satisfaction Patient’s postoperative satisfaction score. O: Mean difference 1.05 (95%CI 1.02 to 1.98) favouring Delorme’s
1b. Delorme’s versus Altemeier’s: Relapse prolaps Recurrent full-thickness prolapse (number of patients) K: OR 0.67 (95% CI 0.36 to 1.26) favouring Altemeier’s Functional outcomes Vaizey incontinence score K: mean difference 0.20 (95% CI -2.88 to 3.28) favouring Delorme’s Bowel function (thermometer) K: mean difference 0.0 (95% CI -13.96 to 13.96) Patient satisfaction Quality of life score (EQ-5D at 3 years) K: mean difference 0.04 (95%CI: -0.11 to 0.19) favouring Delorme’s.
2. Preservation versus division of the lateral ligaments during open mesh rectopexy Relapse prolaps Recurrent full-thickness prolapse (number of patients) H: Not estimable M: OR 15.35 (95%CI 0.73 to 321.58) favouring division Residual mucosal prolapse only (number of patients) M: OR 6.9 (95%CI 0.3 to 159.29) favouring division Functional outcomes Constipation after surgery (number of patients) Pooled effect (M+H): fixed effects model. OR 0.32 (95%CI 0.08 to 1.23) favouring preservation. Heterogeneity (I2): 59%; Constipation score H: Mean difference 0.3 (95%CI -1.9 to 2.5) favouring division Defecation frequency (per day) H: Mean difference -1.00 (95%CI -1.39 to -0.61) favouring preservation Resting anal pressure (mmHg) H: Mean difference 9.00 (95%CI -2.58 to 20.58) favouring division Anal squeeze pressure (mmHg) H: Mean difference 4.00 (95%CI -10.84 to 18.84) favouring division Complications Postoperative complications (number of patients) M: No complications in treatment or control group
3. Laparoscopic versus open procedure Relapse prolapse Recurrent full-thickness prolapse (number of patients) L: OR 0.30 (95%CI 0.01 to 7.85) favouring laparoscopic Residual mucosal prolapse only (number of patients) A: OR 0.49 (95%CI 0.02 to 13.52) favouring laparoscopic Functional outcomes Incontinence score (number of patients) L: OR -0.4 (95%CI -1.89 to 1.09) favouring laparoscopic Constipation after surgery (number of patients) A: OR 0.18 (95%CI 0.01 to 3.91) favouring laparoscopic Maximum resting anal pressure(cmH2O) A: Mean difference 0.0 (95%CI -33.87 to 33.87) Maximum squeeze pressure A: Mean difference 1.0 (95%CI -28.39 to 30.39) favouring open Complications Postoperative complications (number of patients) L: OR 0.15 (95%CI 0.04 to 0.62) favouring laparoscopic
4. Abdominal versus perineal approach. Relapse prolapse Recurrent full-thickness prolapse (number of patients) C+K: Pooled effect (fixed effects model): OR 0.64 (95% CI 0.12 to 3.55] favoring perineal Heterogeneity (I2): 36% Residual mucosal prolapse only (number of patients) C: OR 1.00 (95% CI 0.11 to 8.95) Functional outcomes Vaizey incontinence score 3 years post-operative K: mean difference 0.40 (95% CI -5.44 to 6.24) favouring abdominal Residual faecal incontinence (number of patients) Pooled effect (fixed effects model): OR 2.26 (95%CI: 0.61 to 8.4) favouring abdominal Heterogeneity (I2): 75% Bowel function (bowel thermometer) 3 years poster-operative K: Mean difference -2.00 (95%CI: -31.69 to 27.69) favouring perineal Straining 3 years postoperative (number of patients) K: OR: 0.06 (95%CI: 0.00 to 1.33) favouring perineal Maximal squeeze pressure (cmH2O) C: Mean difference -12.10 (95%CI: -37.65 to 13.45) favouring perineal Maximum resting pressure (cmH2O) C: Mean difference: 5.4 (-30.05 to 40.85) favouring abdominal Complications Postoperative complications Pooled effect (fixed effects model): OR 0.46 (95% CI 0.15 to 1.37) favouring perineal Heterogeneity (I2): 17% Patient satisfaction Quality of Life EQ-5D at 3 years) K: Mean difference 0.13 (95%CI: -0.14 to 0.4) favouring abdominal
5. Resection versus no resection rectopexy. Recurrent full-thickness prolapse K: OR 0.41 (95% CI 0.11 to 1.50) favouring resection Functional outcomes Residual faecal incontinence (number of patients) F,G,K: Pooled effect (fixed effects model) OR 0.93 (95%CI 0.43 to 2.03) favouring resection. Heterogeneity (I2):11% Vaizey incontinence score 3 years post-operative K: mean difference -0.30 (95% CI -3.51 to 2.91) favouring resection Number of patients with constipation due to surgery F, G, K: Pooled effect (fixed effects model) OR 0.14 (95%CI 0.04 to 0.44) favouring resection. Heterogeneity (I2): 0% Bowel function (thermometer, 3 years post-operative) K: Mean difference 3.00 (95%CI: -19.02 to 25.02) favouring no resection Maximum resting anal pressure (mmHg) G: Mean difference -16.00 (95%CI: -49.35 to 17.35) favouring resection Postoperative complications Pooled effect (fixed effects model): OR 1.89 (95% CI 0.76 to 4.73) favouring no resection Heterogeneity (I2): 0% Patient satisfaction Quality of life score (EQ-5D) K: Mean difference 0.12 (95%BI -0.08 to 0.32) favouring no resection
6. Rectopexy versus no rectopexy. Relapse Prolapse Recurrent full-thickness prolapse E: OR 6.32 (95% CI 1.36 to 29.47) favouring rectopexy Complications E: OR 0.51 (95% CI 0.24 to 1.11) favouring no rectopexy |
Author conclusion: The lack of high quality evidence on different techniques, together with the small sample size of included trials and their methodological weaknesses, severely limit the usefulness of this review for guiding practice. It is impossible to identify or refute clinically important differences between the alternative surgical operations.
|
|
Ramage, 2015
|
SR and meta-analysis of randomized and non-randomised controlled trials
Literature search up to May 2014
A: Heemskerk, B: De Hoog, C: Mantoo, D: Mäkelä-Kaikkonen E: Mehmood
Study design: A-C: Non-randomised controlled trials D: Retrospective cohort study E: RCT
Setting and Country: A: Netherlands B: Netherlands C: France D: Italy E: Germany
Source of funding: Not reported
|
Inclusion criteria SR: - compare the outcomes of laparoscopic versus robotic approaches in ventral mesh rectopexy - report on at least one outcome measure
Exclusion criteria SR: - no comparison of robotic and laparoscopic approaches - evidence of overlapping data from the same unit with the same clinical outcomes reported.
5 studies included
Important patient characteristics at baseline: N, mean age, sex A: 33 patients, 52 yrs, 33% M B: 35 patients, 56.4 yrs, 13% M C: 118 patients, 61.5 yrs, 0% M D: 40 patients, 15% M E: 51 patients, 6% M
Groups were comparable in sex and BMI at baseline |
All studies; laparoscopic approaches. All studies followed D’Hoore’s technique of mesh fixation (not further described in article).
|
All studies; robotic approaches (not further described in article)
|
End-point of follow-up: Not reported
|
1. Recurrence Pooled effect (fixed effects model): OR 0.91 (95% CI 0.32 to 2.63) favouring robotic Heterogeneity (I2): 0%
2. Postoperative complications Pooled effect (fixed effects model): OR 0.49 (95% CI 0.20 to 1.20) favouring robotic Heterogeneity (I2): 7%
3. Post-operative Wexner score Pooled effect (fixed effects model): OR 0.17 (95% CI -.85-0.51) favouring robotic Heterogeneity (I2): 0%
|
Only little information about study characteristics.
No quality assessment of included studies performed.
Not clear which diagnosis was used: internal prolapse, external prolapse or both. |
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Tou, 2015 |
Yes |
Yes |
Yes |
Yes |
Not applicable, only RCT’s included |
Yes |
Yes |
Yes |
No |
|
Ramage, 2015 |
Yes |
No, search strategy not described |
Yes |
No |
No |
No |
Yes |
No |
No |
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score no. Score yes if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a yes, source of funding or support must be indicated for the systematic review AND for each of the included studies.
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Young, 2015 (update search) |
Retrospectieve cohortstudie, geen (quasi-)gerandomiseerde trial |
|
Makineni, 2014 (update search) |
Trial is niet (quasi-)gerandomiseerd |
|
Senepati, 2013 (update search) |
Opgenomen in review Tou (2015) |
|
Makela-Kaikkonen, 2013 (update search) |
Opgenomen in review Ramage (2015) |
|
Mehmood, 2014 (update search) |
Opgenomen in review Ramage (2015) |
|
Caddedu, 2012 (Prolaps richtlijn) |
Systematic review van Tou (2015) en Ramage (2015) zijn recenter |
|
De Hoog, 2009 (Prolaps richtlijn) |
Opgenomen in review Ramage (2015) |
|
Fleming, 2012 (Prolaps richtlijn) |
Case serie, geen vergelijkende studie |
|
Karas, 2011 (Prolaps richtlijn) |
Opgenomen in review Tou (2015) |
|
Youssef, 2013 (Prolaps richtlijn) |
Opgenomen in review Tou (2015) |
|
Chun, 2004 (Prolaps richtlijn) |
Geen gerandomiseerde studie |
|
Samaranyaka, 2010 (Prolaps richtlijn) |
Geen vergelijkende studie |
|
Schiedeck, 2005 (Prolaps richtlijn) |
Geen gerandomiseerde studie |
|
Tsunoda, 2003 (Prolaps richtlijn) |
Case serie, geen vergelijkende studie |
|
Zbar, 2002 (Prolaps richtlijn) |
Geen systematic review of primair onderzoek |
|
Tou, 2008(Prolaps richtlijn) |
Vervangen door Tou, 2015 |
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-11-2017
Beoordeeld op geldigheid : 01-07-2017
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Op modulair niveau is een onderhoudsplan beschreven, zie de tabel hieronder. Het bestuur van de Nederlandse Vereniging voor Heelkunde (NVvH) bepaalt of de modules nog actueel zijn. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVvH is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module |
Eerstvolgende beoordeling actualiteit richtlijn |
|
ARFO |
2021 |
|
Diagnostiek |
2021 |
|
Scoringssystemen FI |
2021 |
|
Scoringssystemen OD |
2021 |
|
Work-up |
2021 |
|
Conservatieve therapie OD |
2021 |
|
Conservatieve therapie FI |
2021 |
|
Indicatiestelling |
2021 |
|
Chirurgische behandeling IRP |
2019 |
|
Chirurgische behandeling ERP |
2019 |
|
Materiaalkeuze |
2021 |
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kennisinstituut.nl) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Er bestaat behoefte aan uniformiteit met betrekking tot de indicatiestelling voor conservatief- of operatief beleid alsmede de inhoud van het beleid, in het bijzonder in geval van operatief beleid (operatietechnieken en materiaalkeuze). De indicatistelling dient optimaal recht te doen aan de patiënt. Dat wil zeggen dat de indicatiestelling zo gekozen wordt dat patiënten niet onnodig een operatie ondergaan maar ook andersom er niet te veel patiënten, die veel baat bij een operatie zouden hebben, een operatie ontzegd worden. De patiënteninformatie bijhorende deze richtlijn kan ertoe bijdragen dat een patiënt beter geïnformeerd is over de behandelopties en de mogelijke risico’s. Dit stelt de patiënt in staat om een goede afwezging te maken en mee te beslissen over de keuze tussen conservatief en operatiefbeleid.
Doelgroep
De op te stellen richtlijn is in wezen een professioneel technische standaard op de eerste plaats bedoeld voor de doelgroep gevormd door chirurgen, MDL-artsen, gynaecologen, bekkenfysiotherapeuten, urologen en radiologen. In tweede plaats is de richtlijn bedoeld om zorgverleners die te maken hebben met patiënten met RP zoals huisartsen, continentieverpleegkundigen, verpleegkundig specialisten en physician assistant te informeren. Er zijn geen aanbevelingen voor de eerste lijn opgenomen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met (verdenking op) een rectum prolaps (zie hieronder).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. N.A.T. Wijffels, chirurg, Antonius ziekenhuis, NVvH (voorzitter)
- Dr. E. Consten, chirurg, Meander MC, Amersfoort, NVvH
- Dr. S.J. van der Hagen, chirurg, Treant Zorggroep Stadskanaal, Emmen en Hoogeveen, NVvH
- Dr. A. Pronk, chirurg, Diakonessenhuis, Utrecht, NVvH
- Dr. R.J.F. Felt-Bersma, Maag-, darm- en leverarts, VU medisch centrum, Amsterdam, NVMDL
- Drs. M. Stegeman, gynaecoloog,Elisabeth-TweeSteden Ziekenhuis, Tilburg, NVOG
- Drs. E.J.L. Bosboom, radioloog, ZiekenhuisGroep Twente, Almelo, NVvR
- J.A.J. Kalkdijk MSc., bekkenfysiotherapeut, Bekken en Bekkenbodem Zorgcentrum, Leeuwarden, NVFB
- Drs. D.A van Reijn, bekkenfysiotherapeut, Bekkenfysiotherapie Baarn, Proctos Kliniek Bilthoven, NVFB
- Drs. A.H.P. Meier, uroloog, VieCuri, Venlo, NVU
- T.J.C. Paulides MSc., arts in opleiding tot chirurg (aios chirurgie), Meander MC, Amersfoort, NVvH
Klankbordgroep
- Drs. G.G.A. (Alec) Malmberg, patiëntvertegenwoordiger/gynaecoloog, Universitair Medisch Centrum Groningen, Bekkenbodem4All
- T. (Thea) Boele, patiëntvertegenwoordiger, Bekkenbodem4All, Brandwijk
- Prof. Dr. W.A. Bemelman, chirurg, Academisch Medisch Centrum, Amsterdam, NVvH
- Dr. S. Festen, chirurg, OLVG, Amsterdam, NVvH
- Dr. D.D.E. Zimmerman, colorectaal chirurg, Elisabeth-TweeSteden Ziekenhuis, Tilburg, NVvH
Met ondersteuning van
- E.A. Rake MSc., junior adviseur, Kennisinstituut van Medisch Specialisten (vanaf januari 2016)
- H.L. Vreeken MSc., adviseur, Kennisinstituut van Medisch Specialisten (tot december 2015)
- Dr. W.A. van Enst, senior adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in de tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Achternaam |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
|
Stegeman |
Gynaecoloog |
Medisch Manager |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 27-05-2015 |
|
Wijffels |
Gastro-intestinaal chirurg, regiomaatschap Chirurgie Midden-Nederland |
Lid bestuur werkgroep coloproctologie (WCP) |
geen |
geen |
WCP |
geen |
geen |
Gedeelten van de NVvH en WCP worden door diverse partijen gesponsord |
ja, 09-06-2015 |
|
Felt-Bersma |
MDL arts |
MDL arts VuMC consultant MDL arts MCV de Veluwe, Apeldoorn consultant MDL arts Proctoskliniek Bilthoven |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 09-06-2015 |
|
Consten |
Gastro-intestinaal chirurg. |
Voorzitter NVEL opleiding Heelkunde, Meander MC |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 09-06-2015 |
|
Pronk |
gastro-intestinaal chirurg, Diakonessenhuis Utrecht en Zeist |
|
werkzaam colorectaal chirurg in ziekenhuis (Diakonessenhuis) |
geen |
2002-2008 lid beroepsbelangen vereniging heelkunde |
geen |
geen |
geen |
ja, 12-06-2015 |
|
Bosboom |
Fellow radioloog ZGT almelo |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 15-06-2015 |
|
Van der Hagen |
gastro-intestinaal chirurg in TREANT Zorggroep |
Bestuurslid stafbestuur MSN NON (betaald) Bestuurslid stafbestuur TREANT zorggroep (betaald) |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 13-06-2015 |
|
Huisman |
gynaecoloog Haga Bekkenbodem Centrum |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
15-7-2015 |
|
Kalkdijk |
Bekkenfysiotherapeut Promovendus Heelkunde Onderzoeker Anorectaal Functiecentrum UMCG |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 13-07-2015 |
|
Meier |
Uroloog |
geen |
geen financiele belangen |
Geen persoonlijke relaties die baat kunnen hebben bij een bepaalde uitkomst of advies |
geen belangen, geen deelname |
Geen extern gefinancieerd onderzoek |
Expertise op gebied van colpopromontoriopexie voor urogenitale prolaps Expertise centrum voor de ALTIS SIS tape voor stress-urine-incontinentie van de Fa.Coloplast |
geen |
ja, 16-10-2015 |
|
Van Reijn |
Bekkenfysiotherapeut |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 01-12-2015 |
|
Malmberg |
Gynaecoloog en sectie voorzitter algemene gynaecologie Bestuurslid Bekkenbodem4All (voormalig SBP) |
Ambassadeur compassion for care onbetaald ontwikkelen en onderzoeken e health mogelijkheden, #PCiCare BIJVOORBEELDonbetaald |
geen lidmaatschap van adviescommissie (s) aandeelhouder in #PCiCare BV |
directe collega F. Hoogenboom colorectaal chiruge umcg vriendenkring bekkenfysiotherapeut |
Bestuurslid Bekkenbodem4All Ambassadeur Compassion for care, car for sustainable health, noorden duurzaam. Biotoop bijeenkomstenGroningen |
geen |
geen |
niet dat ik weet |
ja, 27-11-2015 |
|
Boele |
Bestuurslid Patiëntenorganisatie Bekkenbodem4All |
Telefoniste informatie-advieslijn Bekkenbodem4All |
geen |
geen |
Wij nemen deel aan deze commissie om de belangen van patiënten te behartigen en de goede communicatie tussen arts en patiënt te bewerkstellingen. |
Wij schrijven voor sommige onderzoeken brieven waarin wij het onderzoek aanbevelen, uitsluitend als wij daar ook als bestuur geheel achter staan. Voor het schrijven van deze brieven vragen wij een kleine vergoeding, nogmaals uitsluitend om als patiënten geen vereniging onszelf staande te houden. |
geen |
geen |
ja, 22-03-2016 |
|
Paulides |
Promovendus Heelkunde |
Literatuuronderzoek en meeschrijven aanbeveling (onbetaald). |
geen |
geen |
geen |
geen |
geen |
nee |
ja, 22-03-2016 |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door de focusgroep die bij de richtlijn prolaps werd gehouden, te gebruiken. Een verslag van de patientenfocusgroep uit de richtlijn Prolaps (bijlage Notulen patiëntenfocusgroep) is besproken in de werkgroep. De knelpunten die betrekking hadden op deze richtlijn zijn verwerkt. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Bekkenbodem4All (een fusie van Patiëntvereniging Gynaecologie en Stichting Bekkenbodem Patiënten) en de Patiëntenfederatie Nederland. Gedurende de commentaarfase is patiënteninformatie ontwikkeld (Patiënteninformatietool) in samenwerking met de Patiëntenfederatie Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten (Implementatieplan). De werkgroep heeft tevens een interne kwaliteitsindicator ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (zie Indicatorontwikkeling en Indicatoren).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens werden de volgende stakeholders schriftelijk uitgenodigd te reageren op het concept-raamwerk van de richtlijn rectum prolaps: IGZ, NVZ, NFU, STZ, ZKN, Lareb, Nefarma, NVvH, NVMDL, NVOG, NVvR, KNGF-NVFB, NVU, PGN, SBP, (tegenwoordig zijn PGN en SBP gefuseerd tot Bekkenbodem4All) NVA, V&VN, Patiëntenfederatie Nederland, Zorginstituut Nederland, ZN, NGH. De invitational conference van de Richtlijn Prolaps werd hierbij als uitgangspunt genomen. Een overzicht van de binnengekomen suggesties en de reactie van de werkgroep hierop is opgenomen onder aanverwante producten (Knelpuntanalyse).
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ROBINS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
C) Voor vragen over de waarde van meet- of classificatie-instrumenten (klinimetrie)
Deze instrumenten werden beoordeeld op validiteit, intra- (test-hertest) en inter-beoordelaarsbetrouwbaarheid, responsiviteit (alleen bij meetinstrumenten) en bruikbaarheid in de praktijk. Bij ontbreken van een gouden standaard, werd een beoordeling van de bewijskracht van literatuurconclusies achterwege gelaten.
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in een aparte module over Organisatie van Zorg.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de richtlijn werd er een interne kwaliteitsindicator ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (Indicatoren). Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten; Kennislacunes).
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Kennisinstituut van Medisch Specialisten. Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html. 2012.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) mei 2013 – juli 2015 |
1 Rectal Prolapse/ or Rectocele/ or ((rectal or anal) adj5 prolapse*).tw. or enteroc?ele*.tw. or proctoc?ele*.tw. or sigmoidoc?ele*.tw. or Intussusception/ or Intussusception*.tw. or rectal invagination*.tw. (12714) 10 (LVR or LRR or STARR or delorme* or altemeier* or rectopex* or mucosectom* or proctosigmoidectom*).tw. (5468) 11 ((stapled adj7 transanal) or (stapled adj7 trans-anal)).tw. (193) 12 Rectocele/su or Rectal Diseases/su or Rectal Prolapse/su or Digestive System Surgical Procedures/ or Laparoscopy/ (76231) 13 10 or 11 or 12 (80952) 14 1 and 13 (2400) 15 9 and 14 (3) 16 9 not 15 (2) 17 limit 14 to (dutch or english) (1849) 18 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or (systematic* adj review$1).tw. or (systematic adj overview$1).tw. or exp Review Literature as Topic/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and review/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (177031) 19 17 and 18 (40) 20 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1498465) 21 17 and 20 (192) 22 19 or 21 (209) 23 limit 22 to yr=2013 -Current (33) |
60
|
|
Embase (Elsevier) |
(((rectal OR anal) NEAR/5 prolapse*):ab,ti OR rectocele*:ab,ti OR enterocele*:ab,ti OR proctocele*:ab,ti OR sigmoidocele*:ab,ti OR intussusception*:ab,ti OR (rectal NEAR/2 invagination*):ab,ti OR 'rectum prolapse'/exp/mj AND (lvr:ab,ti OR lrr:ab,ti OR starr:ab,ti OR delorme*:ab,ti OR altemeier*:ab,ti OR rectopex*:ab,ti OR mucosectom*:ab,ti OR proctosigmoidectom*:ab,ti OR (stapled NEAR/7 transanal):ab,ti OR (stapled NEAR/7 'trans-anal'):ab,ti OR 'rectocele'/exp/mj/dm_su OR 'rectum disease'/exp/mj/dm_su OR 'rectum prolapse'/exp/mj/dm_su OR 'laparoscopy'/exp/mj) OR ('rectocele'/exp/mj/dm_su OR 'rectum disease'/exp/mj/dm_su OR 'rectum prolapse'/exp/mj/dm_su AND (lvr:ab,ti OR lrr:ab,ti OR starr:ab,ti OR delorme*:ab,ti OR altemeier*:ab,ti OR rectopex*:ab,ti OR mucosectom*:ab,ti OR proctosigmoidectom*:ab,ti OR (stapled NEAR/7 transanal):ab,ti OR (stapled NEAR/7 'trans-anal'):ab,ti))) AND ([dutch]/lim OR [english]/lim) AND [embase]/lim OR
AND 'meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de NOT (animal* NOT human*)
OR ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it)
AND [2013-2015]/py (=50) |
