Preventie van terugval: afweging en interventies
Uitgangsvraag
Uitgangsvraag 1a:
Hoe kunnen de voor en nadelen van een recidief tegen elkaar worden afgewogen?
Uitgangsvraag 1b:
Welke interventies zijn effectief bij het voorkomen van een recidief bij personen met een episodische of aanhoudend psychotische stoornis?
Aanbeveling
Bepaal in samenwerking met de patiënt en de naasten het belang van recidiefpreventie voor deze specifieke patiënt en hoe dit zich verhoudt tot hersteldoelen.
Betrek hierbij de ernst van en het mogelijk opgetreden ernstig nadeel bij eerdere psychotische episodes.
Betrek hierbij ook de ernst van iatrogene schade door behandeling bij deze specifieke patiënt. Dit kan gaan over bijwerkingen van interventies die als doel recidiefpreventie hebben, maar óók over schade door (gedwongen) opnames en separaties die juist een gevolg van recidief kunnen zijn.
Als de patiënt wilsonbekwaam wordt geacht bij afwegingen hierover, betrek dan een wettelijk vertegenwoordiger bij de afwegingen.
Bespreek dat het gebruik van antipsychotica de kans op een recidief en de kans op een heropname verkleint.
Bespreek dat er voorzichtige aanwijzingen zijn dat een standaard dosering van een antipsychoticum vergeleken met een lage en zeer lage dosering van hetzelfde middel de kans op een recidief verkleint.
Bespreek dat er voorzichtige aanwijzingen zijn dat langwerkende intramusculaire antipsychotica ten opzichte van oraal toegediende antipsychotica de gecombineerde kans op het optreden van een heropname of een recidief verkleinen.
Bespreek dat er voorzichtige aanwijzingen zijn dat clozapine de kans op heropname verkleint ten opzichte van andere orale antipsychotica.
Bespreek dat er geen bewijs is voor de meerwaarde van antipsychotische polyfarmacie voor recidiefpreventie ten opzichte van monotherapie in RCT’s, maar dat in observationele studies aanwijzingen zijn dat antipsychotische polyfarmacie de kans op heropname verkleint.
Bespreek dat er voorzichtige aanwijzingen zijn dat niet-farmacologische interventies zoals CGT, familie-georiënteerde interventies en psycho-educatie als aanvulling op standaardtherapie (vaak betreft dat farmacotherapie) het risico op recidief verlagen op de middenlange termijn. Er is geen bewijs voor verschil in effect van deze verschillende interventie-vormen.
Overwegingen
Kwaliteit van het bewijs
- De representativiteit van randomized controlled trials - Meta-analyses van randomized controlled trials (RCT’s) gelden als de hoogste vorm van wetenschappelijk bewijs voor effectiviteit. Randomisatie en (bij voorkeur) dubbele blindering van patiënt en behandelaar maken dat allerlei mogelijke verklaringen voor eventuele gevonden verschillen tussen twee interventies worden uitgesloten in RCT’s. Dit maakt het veel aannemelijker dat een gevonden verschil berust op een werkelijk effectverschil. Er is echter een probleem bij het generaliseren van de resultaten uit RCT’s naar de dagelijkse praktijk. Dit komt doordat RCT’s strikte in- en exclusiecriteria hanteren, waardoor zo’n 80% van de patiënten niet in aanmerking komt voor deelname (Taipale e.a. 2022). Hieruit volgt dat in de uitkomsten van medicatieonderzoek slechts een vijfde van alle patiënten gerepresenteerd is. Daarnaast is blindering bij sommige interventies moeilijk of onmogelijk.
- Bij RCT’s naar de effectiviteit van interventies met als doel recidiefpreventie bij mensen met een psychosegevoeligheid speelt dit probleem in sterke mate. Deelname aan een dergelijke RCT vergt de bereidheid en het vermogen om gerandomiseerd te worden, interventies of placebo-behandeling te ondergaan, en metingen te ondergaan. Meestal is daar in enige mate overeenstemming voor nodig met de onderzoekers en behandelaren over de probleemdefinitie van wat er met de persoon aan de hand is en over het nut van de studie. Dit betekent dat mensen met een psychosegevoeligheid die zelf weinig problemen ervaren en/of geen behandelwens hebben en/of negatieve ervaringen hebben met de GGZ, niet gerepresenteerd worden in RCT’s. Dat leidt tot beperkte generaliseerbaarheid van de resultaten naar de gehele groep van mensen met een psychosegevoeligheid. Verder wordt in RCT’s met intramusculaire depotmedicatie vaak niet geblindeerd (dan moet namelijk een placebo-injectie gegeven worden).
- Observationele cohortstudies kunnen daarom van aanvullend belang zijn. Omdat in deze studies niet gerandomiseerd en geblindeerd wordt, zijn meerdere vormen van vertekening mogelijk. Resultaten uit observationele studies zijn daarom minder valide en betrouwbaar dan resultaten van RCT’s en kunnen deze in wetenschappelijk opzicht niet vervangen. Wel zijn de beide onderzoeksopzetten complementair aan elkaar, en de gecombineerde informatie kan relevant zijn voor patiënten in de ‘echte’ wereld (Groenwold e.a. 2021). Daarom volgt onderaan, in aanvulling op de systematische search naar (meta-analyses van) RCT’s, een kort overzicht van resultaten uit observationele studies.
- Psychosociale interventies - Bij psychosociale interventies om recidieven (inclusief heropnames) te voorkomen bij psychotische stoornissen was er spreiding in de kwaliteit van het bewijs. De sterkte van bewijs liep van zeer laag tot hoog, waarbij het meeste bewijs als zeer laag of laag werd beoordeeld. Bij cognitieve gedragstherapie (CGT) in combinatie met standaard zorg (vaak farmacotherapie) varieerde de kwaliteit van het bewijs van zeer laag tot laag. In het merendeel van de uitkomsten waarbij de kwaliteit van het bewijs op zeer laag en laag werd geschat was er een verhoogd risico op vertekening bij de geïncludeerde studies, onduidelijke of verhoogde risk of bias, heterogeniteit in de resultaten en waren de uitkomsten vaak op een klein aantal observaties gebaseerd. De kwaliteit van bewijs voor sociale vaardigheidstrainingen, psycho-educatie en familie georiënteerde interventies varieerde van zeer laag tot laag. Hierbij was er vaak sprake van heterogeniteit in de uitkomsten tussen de verschillende studies en waren de geobserveerde effecten klein, onnauwkeurig en vaak gebaseerd op een klein aantal observaties.
- Farmaceutische interventies - Bij farmacotherapie om recidieven (inclusief heropnames) te voorkomen bij psychotische stoornissen was er spreiding in de kwaliteit van het bewijs, van zeer laag tot redelijk. Wanneer er gekeken wordt naar de behandeling met verschillende typen intramusculaire langwerkende medicatie (‘depot’) versus placebo wordt het bewijs tussen zeer laag en hoog ingeschat. Wanneer intramusculaire langwerkende medicatie vergeleken wordt met oraal toegediende medicatie varieert het vertrouwen in bewijs van zeer laag tot laag. Dit omdat de effectschatting in veel gevallen onnauwkeurig was en de resultaten tussen afzonderlijke studies inconsistent. Wanneer 2de generatie antipsychotica met 1ste generatie antipsychotica werden vergeleken, varieerde het vertrouwen in het bewijs van zeer laag tot laag; Bij de meeste studies werden verschillende definities gehanteerd voor het optreden van een recidief, gebruikten studies verschillende controlegroepen en was de effectschatting in veel gevallen onnauwkeurig.
- Werd er gekeken naar het gebruik van 2de generatie antipsychotica ten opzichte van placebo, dan varieerde het vertrouwen in het bewijs bij het merendeel van studies tussen zeer laag en laag, met één uitschieter bij het effect van olanzapine dat als redelijk betrouwbaar werd beoordeeld. Zo waren er aanwijzingen voor een publicatiebias en bij de studies die laag scoorden was er een onnauwkeurige effectschatting. Als er gekeken werd naar de inzet van antipsychotica in het algemeen ten opzichte van placebo werd het vertrouwen in het bewijs beoordeeld als laag tot redelijk. Geïncludeerde studies hanteerden verschillende definities voor een recidief en er was sprake van een verhoogd risico op vertekening en risk of bias.
- Wanneer er gekeken wordt naar verschillende doseringsstrategieën van antipsychotica, werd het vertrouwen in het bewijs beoordeeld als zeer laag. Studies hanteerden verschillende definities voor het optreden van een recidief en in veel gevallen was de effectschatting onnauwkeurig en waren er aanwijzingen voor een verhoogde risk of bias.
- Ten slotte, het vertrouwen in het bewijs bij studies die keken naar de inzet van polyfarmacie ten opzichte van enkelvoudige medicatie was zeer laag. Hierbij was een verhoogde kans op vertekening en was er grote heterogeniteit tussen de studies. Ook was de effectschatting onnauwkeurig. Wanneer er gekeken werd naar het overstappen van een polyfarmaceutische behandeling naar een monofarmaceutische, was het vertrouwen in het bewijs zeer laag. Geïncludeerde studies hadden een verhoogd risico op vertekening, de resultaten waren inconsistent en de effectschatting was onnauwkeurig.
Samenvatting van bewijs uit RCT’s en meta-analyses van RCT’s
- Het lijkt dat, wanneer er gekeken wordt naar het optreden van een recidief, weinig tot geen verschil is in de effectiviteit van cognitieve gedragstherapie, familie-georiënteerde therapievormen en psycho-educatie. CGT, familie-georiënteerde therapievormen en psycho-educatie worden vaak gegeven in combinatie met standaardzorg en lijken ten opzichte van standaardzorg (in de meeste gevallen een farmacotherapeutische behandeling) alleen op de midden-lange termijn de kans op het optreden van een recidief te verkleinen.
- Over het algemeen lijkt het gebruik van een antipsychoticum de kans op het optreden van een recidief en heropnames te verkleinen. Als er naar specifieke middelen wordt gekeken, komt het volgende beeld naar voren: aripiprazol, olazapine, ziprasidon en zotepine lijken allen ten opzichte van placebo de kans op een recidief te verkleinen. Sertindol en ziprasidon lijken ten opzichte van 1ste generatie antipsychotica de kans op een recidief te verkleinen. Voor andere 2de generatie antipsychotica werd een soortgelijk effect niet gevonden of was de bewijslast niet toereikend om een harde uitspraak hierover te doen.
- Bij de inzet van intramusculaire langwerkende medicatie lijken paliperidone (1 maand en 3 maanden dosis), aripiprazole, flupentixol, flufenazine, risperidon, pipothiazine (niet in Nederland verkrijgbaar), olanzapine en haloperidol ten opzichte van placebo de kans op een recidief significant te verkleinen. Wanneer er gekeken wordt naar het effect van intramusculaire langwerkende medicatie ten opzichte van hetzelfde middel maar dan oraal toegediend, zijn er voorzichtige aanwijzingen dat de gecombineerde kans van het optreden van een heropname en recidief wordt verkleind.
- Als er naar verschillende doseringen van antipsychotica wordt gekeken, blijkt een standaarddosering effectiever in het voorkomen van een recidief in vergelijking met een lage of zeer lage dosering van hetzelfde middel. Er lijkt geen verschil te zijn in het voorkomen van heropnames tussen een standaard, lage en zeer lage dosering. Ten slotte, er lijkt geen verschil in effectiviteit in het voorkomen van een recidief tussen het gebruik van één of meer antipsychotica.
Aanvullend bewijs na de searchdatum en commentaarronde
- Leucht (2021): In een meta-analyse uitgevoerd door Leucht werd de optimale dosering van anti-psychotica nodig voor relapse preventie bekeken. RCTs waarin een vaste dosering tweede generatie anti-psychotica, haloperidol of fluphenazine werden vergelijken bij mensen met een stabiele schizofreniespectrumstoornis werden geïncludeerd in deze meta-analyse. De primaire uitkomstmaat was relapse, andere uitkomstmaten waren afname van PANSS of BPRS totaalscore na baseline, discontinuatie van medicatie en uitval door bijwerkingen. In totaal werden 26 studies (n=4776) geanalyseerd. De aan werkzaamheid gerelateerd dose-response curve had de vorm van een hyperbool: de kans op relapse nam snel af met het toenemen van de doseringen tot een bovengrens van 5/ mg dag risperidone equivalent (relatief relapse risico, 0.43; 95% CI, 0.31-0.57; gestandaardiseerd gemiddeld verschil voor Positive and Negative Syndrome Scale total score afname, -0.55; 95% CI, -0.68 tot -0.41), maar nam daarna snel af. De uitval uit de studie door bijwerkingen bleef oplopen bij doseringen hoger dan 5/ mg dag risperidone equivalent. In een subgroep mensen in remissie, werd eerder een plateau bereikt, bij ongeveer 2.5 / mg dag risperidone equivalent
Aanvullend bewijsresultaten observationele cohortstudies
- Zoals hierboven besproken (‘de representativiteit van randomized controlled trials’) zijn resultaten uit observationele cohortstudies van aanvullend belang naast resultaten uit RCT’s. Er zijn (meta-analyses van) RCT’s besproken. De werkgroep beschrijft hieronder in aanvulling hierop de resultaten uit enkele zeer grote cohortstudies. Dit is geen systematisch en uitputtend overzicht van cohortstudies naar recidiefpreventie.
- Kishimoto e.a. (2021) voerden een meta-analyse uit van RCT’s, pre-post studies en cohortstudies. De conclusies uit de RCT’s zijn al besproken. Kishimoto e.a. concluderen dat langwerkende intramusculaire antipsychotica in alle drie de designs een verlaagde kans op heropname óf symptomatisch recidief (gecombineerde uitkomstmaat) geven.(RCT’s: 29 studies, 7833 patiënts, RR 0·88 [95% CI 0·79-0·99], p=0·033; cohort studies: 44 studies, 106 136 patiënts, RR 0·92 [0·88-0·98], p=0·0044; pre-post studies: 28 studies, 17 876 patiënts, RR 0·44 [0·39-0·51], p<0·0001 Kortom, de resultaten van de prepost en cohortstudies ondersteunen die van de RCt’s.
- Tiihonen e.a. 2017 - Nationale registerstudie 2006-2013 naar het risico op heropname onder alle patiënten met een diagnose van schizofrenie in Zweden (n=29823) in de leeftijd van 16-64 jaar oud jaar in 2006. Tijdens follow-up werden 43.7% van de patiënten heropgenomen. Het risico op heropname was het laagst bij het gebruik van langwerkende intramusculaire medicatie (HR 0.51-0.86, alle met 95% betrouwbaarheidsinterval onder de 1, alle ten opzichte van géén antipsychoticagebruik) en bij het gebruik van clozapine (HR 0.51). Orale flupentixol, quetiapine en orale perfenazine waren geassocieerd met het hoogste risico op heropname (HR 0.83-0.92, 95% betrouwbaarheidsinterval bij quetiapine en flupentixol overlappend met de 1, alle ten opzichte van géén antipsychoticagebruik). Langwerkende intramusculaire medicatie was geassocieerd met een 20-30% lager risico op heropname dan de vergelijkbare orale middelen.
- Tiihonen e.a. 2019 - Nationale registerstudie 1996-2015 naar het risico op heropname onder alle patiënten met een diagnose van schizofrenie in Finland die psychiatrisch opgenomen zijn geweest, vanaf het moment van ontslag (n=62250 patiënten). In deze studie werden alle vormen van polyfarmacotherapie van antipsychotica apart (iedere combinatie afzonderlijk) meegenomen in de analyse. Alle monotherapieën en polyfarmacotherapieën van antipsychotica gaven een significant lager risico op heropname in vergelijking met géén antipsychoticagebruik, behalve de combinatie van aripiprazol en risperidon (HR 0.42 – 0.93, ten opzichte van géén antipsychoticagebruik, alle met 95% betrouwbaarheidsinterval onder de 1). De combinatie van clozapine + aripiprazol was geassocieerd met het laagste risico op heropname in het totale cohort, en deze combinatie gaf een lager risico dan clozapine alleen, met een verschil in kans op heropname van 14% (HR 0.86 ten opzichte van clozapine). Alle antipsychotische polyfarmacieën waren geassocieerd met een 7-13% lager risico op heropname in vergelijking met iedere monotherapie. Clozapine was de enige monotherapie in de top 10 van meest effectieve therapieën.
- Taipale e.a. 2018 - Nationale registerstudie van 1972-2014 naar het risico op heropname onder alle patiënten met een diagnose van schizofrenie in Finland die psychiatrisch opgenomen zijn geweest, vanaf het moment van ontslag (n=62250 patiënten). In deze studie werden alle vormen van polyfarmacotherapie van antipsychotica als één categorie (polyfarmacotherapie) meegenomen in de analyse. Het risico op heropname was het laagst bij het gebruik van langwerkende intramusculaire medicatie (HR 0.46-0.63, alle met 95% betrouwbaarheidsinterval onder de 1, alle ten opzichte van géén antipsychoticagebruik) en bij het gebruik van clozapine (HR 0.51). Orale perfenazine, flufenazine en quetiapine waren geassocieerd met het hoogste risico op heropname (HR 0.81-0.91, 95% betrouwbaarheidsinterval bij flufenazine overlappend met de 1, alle ten opzichte van géén antipsychoticagebruik). De top 5 van meest effectieve therapieën bestond uit vier langwerkende intramusculaire preparaten en orale clozapine.
Patiëntenperspectief en naastenperspectief
- Afwegen voor en nadelen van een recidief - Een recidief psychose heeft vaak veel negatieve consequenties. Om die reden wordt in de behandeling vaak sterk ingezet op het voorkomen van recidief. Onlosmakelijk daaraan verbonden is de discussie over het continueren van medicatie.
- Aanpak terugvalpreventie - Na de remissie van een eerste psychose is het een belangrijke vraag of medicatie nodig is voor terugvalpreventie. Leidraad is dat bij mensen bij wie de symptomen tenminste een half jaar in remissie zijn, geleidelijk afbouwen van medicatie te overwegen is. Als dit leidt tot een gedeeltelijke terugval is dat een aanwijzing dat medicatie nodig is voor terugvalpreventie. Indien doorgegaan wordt met gebruik van medicatie, te zoeken naar de laagst mogelijke dosering voor terugvalpreventie. Een langzame afbouw (weken tot maanden) verdient de voorkeur. Hierbij kunnen onttrekkingsverschijnselen optreden. Deze kunnen worden voorkomen door zeer geleidelijke dosisverlaging. Tapering strips kunnen daarbij behulpzaam zijn.
- Een leidend principe in het besluit medicatie af te bouwen is ‘dignity of risk’ : het recht op zelfbeschikking en het nemen van aanvaardbare risico’s zoals een recidief psychose. Aan de hand van goede voorlichting zou deze beslissing zoveel mogelijk in samenspraak gemaakt worden. Als in samenspraak gekozen wordt voor afbouw van medicatie, is goede samenwerking met patiënt en naasten van groot belang. Het verdient aanbeveling bij de aanvang van de afbouw samen met patiënt en naasten een crisisplan op te stellen, voor het geval symptomen onverhoopt toch weer toenemen. De afbouw van medicatie dient zorgvuldig te gebeuren, om de kans op een recidief te minimaliseren. De ervaring leert dat de opbouw van medicatie veel zorgvuldiger plaatsvindt dan de afbouw. Onzorgvuldige, onverhoedse afbouw leidt tot een sterke risicoverhoging voor het optreden van een recidief. In het afbouwbeleid dient verder ook de medicatie ter mitigatie van bijwerkingen betrokken te worden, en ook de medicatie die een nevendoel dienen, zoals een antidepressivum. Een separate afbouw van deze ondersteunende nevenmedicatie kan een recidief ontlokken, daar het evenwicht verstoord wordt. De afbouw van medicatie kan met onttrekkingsverschijnselen gepaard gaan. Een nauwkeurig volgen is noodzakelijk om uit te sluiten dat het hier niet gaat om pre-psychotische signalen. Patiënt leert door eigen ervaring en door coaching daarbij na afbouw na psychose tools, om terugval te voorkomen, voor het signaleren van rand-psychotisch gedrag. Dit zal het risicobewustzijn van patiënt en naasten ten aanzien van een recidief verhogen en de kans op optreden van terugval kunnen verkleinen.
- In het crisisplan legt de patiënt vast hoe te handelen bij terugval. Voor het opstellen van het crisisplan kan patiënt een beroep doen op zijn informele en formele netwerk. Het verdient aanbeveling dat het crisisplan door patiënt gedeeld wordt onder de betrokkenen, waaronder ten minste twee betrokken naasten, zodat al deze betrokkenen elkaar bemoedigen om er uitvoering aan te geven, zodra dit nodig is, en zij elkaar over en weer dan goed en regelmatig gaan informeren en bijstaan over het beloop, conform de geuite wensen van de patiënt.
Professioneel perspectief
- Risicofactoren zijn doorgaans niet statisch en veranderen over de tijd. Het is daarom van belang behandelbeleid ten aanzien van recidiefpreventie met regelmaat te evalueren. Het is mogelijk dat iemands weerbaarheid behoorlijk verbeterd is, maar dat die persoon toch nog een recidief meemaakt
- Afwegen voor- en nadelen van een recidief - Bij adviezen over recidief is individueel advies op basis van het kwetsbaarheid-stress-coping model van belang, waarbij aan de hand van een individuele analyse van kwetsbaarheid en veerkracht wordt samengewerkt bij het uitzetten van toekomstig behandelbeleid. Het positief her-labelen van stagnatie als een moment om even op adem te komen van een recidief in het proces van ‘ontwikkelende weerbaarheid’ zoals hierboven beschreven, is noodzakelijk om een herstelgerichte proces een kans te geven. Door te veel aandacht te besteden aan de bescherming, loop je het risico dat mensen uitdagingen gaan vermijden en uiteindelijk een redelijk gemarginaliseerd leven overhouden waarin er geen levenskwaliteit meer overblijft.
- Wanneer er vaker sprake is van een recidief, zal de moedeloosheid bij de persoon, diens omgeving en soms ook bij de hulpverlening, kunnen toenemen. Bovenstaande betekent dat de eerste cruciale vraag is hoe belangrijk recidiefpreventie is bij een specifieke patiënt. Die vraag kan alleen beantwoord worden in overleg tussen patiënt, behandelaar, en naasten. Naasten zijn hierbij expliciet van belang, omdat zij deze risico-afweging soms anders inschatten dan de patiënt zelf. Als dat het geval is, is het cruciaal om hun argumenten hiervoor te kennen en mee te wegen. Het belang van het voorkómen van een recidief, de effectiviteit van antipsychotica bij deze patiënt, en de ervaren nadelen moeten via ‘shared decision making’ leiden tot een advies m.b.t. antipsychotische medicatie voor recidiefpreventie.
- Aanpak terugvalpreventie - Behandelaren worstelen vaak net als hun patiënten met complexe dilemma’s bij het onderwerp recidiefpreventie. Hulpverleners zouden kunnen benadrukken dat een ‘psychose’ ernstig kan zijn, maar geen voorspeller is voor een uitzichtloze toekomst. De herstelbeweging heeft ons geleerd dat we ons steeds moeten oprichten. Voor herstel is het belangrijk om gericht te zijn op een betekenisvolle toekomst, en te leren omgaan met psychotische ervaringen, in plaats van om deze ervaringen te vermijden.
- Ook de hulpverleners kunnen soms meegesleept worden in gevoelens van moedeloosheid en machteloosheid. Het leidt soms tot conclusie dat mensen uitbehandeld zijn, of therapieresistent. Deze begrippen passen niet in een herstelgericht denken of in het denken vanuit een kwetsbaarheidsstress-model. Tijdens een recidief wordt de focus op veranderen en leren tijdelijk opgeschort, om later ruimte te maken voor een nieuw perspectief.
- Farmacotherapie - Het daadwerkelijk gebruik van voorgeschreven medicatie is een belangrijke beschermende factor. Om dit te bevorderen dient met de patiënt samengewerkt te worden aan een acceptabel medicatiebeleid. Er zijn sterke aanwijzingen dat het gebruik van antipsychotica de kans op een recidief verkleint en er zijn voorzichtige aanwijzingen dat het gebruik van langwerkende intramusculaire medicatie de kans op een recidief verkleint ten opzichte van het gebruik van orale middelen. Antipsychotica hebben echter ook veel bijwerkingen. Daarnaast zijn sommige patiënten veel meer in staat tot stappen op het gebied van maatschappelijk en persoonlijk herstel wanneer zij geen antipsychotica gebruiken. Er zijn tot slot ook patiënten bij wie recidieven gepaard gaan met ernstig nadeel voor henzelf of de omgeving. Wanneer de patiënt als wilsonbekwaam wordt beschouwd ten aanzien van deze beslissing, is het noodzakelijk een wettelijk vertegenwoordiger te benoemen (afhankelijk van de situatie een naaste of een professionele vertegenwoordiger) die mede het belang van de patiënt kan behartigen. Wanneer eerdere recidieven leidden tot ernstig nadeel voor de patiënt zelf en/of omgeving, en de patiënt desondanks niet bereid is antipsychotische medicatie te gebruiken, heeft de zorgprofessional de plicht om af te wegen of er redenen zijn om verplichte zorg te verlenen in het kader van de Wvggz.
- Dosering medicatie tbv terugvalpreventie - Er zijn aanwijzingen dat anti-psychotica doseringen hoger dan 5 mg per dag risperidone equivalent weinig extra bijdragen aan de voorkoming van een terugval, maar dat er bij hogere doseringen wel extra bijwerkingen optreden. Bij remissie kan een dosering van 2,5 mg per dag risperidone equivalent al voldoende zijn. Verdere verlaging van de dosering gaat samen met een disproportioneel risico op terugval. Aangezien bovenstaande aanbevelingen zijn gebaseerd op gemiddelden, moet rekening gehouden worden met factoren als een langzaam of snel metabolisme, leeftijd, stadium van de aandoening, comorbiditeiten, interacties met andere medicatie. Aangenomen wordt daarom dat voor individuele patiënten op basis van deze factoren een hogere of juist lagere dosering optimaal is (Leucht, 2021).
- Niet-farmacologische interventies - Er zijn voorzichtige aanwijzingen dat niet-farmacologische interventies zoals CGT, familie-georiënteerde interventies en psycho-educatie als aanvulling op standaardtherapie (vaak betreft dat farmacotherapie) het risico op recidief verlagen op de middellange termijn. Er is geen bewijs voor verschil in effect van deze verschillende interventie-vormen. Nadelige effecten worden over het algemeen als veel kleiner ervaren dan bij farmacotherapie. Professionals hebben dus alle reden om het belang van deze interventies te benadrukken. In deze richtlijn is niet expliciet gekeken naar de effecten van leefstijlinterventies op terugval, maar gezien de relatie tussen leefstijl en terugval verdient de inzet van dergelijke interventies aanbeveling.
Middelenbeslag
- Opnames zijn duur en regelmatig is een opname nodig bij een recidief, dit betekent dat voorkomen van een recidief vaak samengaat met lagere zorgkosten. Vanuit kostenperspectief is voorkomen van recidief dus lonend. Soms botst dat met de herstelgedachte waarbij risico’s nemen (verhoogde kans op recidief) nodig kan zijn. De herstelgedachte is dan het leidend principe.
Organisatie van zorg
- Voor elke patiënt dienen farmacologische en niet-farmacologische interventies (o.a. CGT, psycho-educatie, familie-georiënteerde interventie) toegankelijk zijn. Shared decision making is het uitgangspunt in de zorg, behandelaar en patiënt nemen in dialoog de beslissingen over het te volgen behandelbeleid. In geval van een recidief is van belang dat de zorg snel kan worden opgeschaald. Bij voorkeur is er de mogelijkheid tot IHT bij crisis, ter preventie van een opname.
Maatschappelijk perspectief
- Een recidief kan in sommige gevallen tot risico’s voor anderen en maatschappij, bijvoorbeeld als mensen vanuit psychotische belevingen gevaarlijk gedrag gaan vertonen. Soms kunnen mensen vanuit de psychose verward gedrag vertonen. Dit kan bijdragen aan stigmatisering van en intolerantie jegens mensen met een psychotische stoornis.
Onderbouwing
Voor aanbevelingen omtrent het opstarten en monitoren van een behandeling met antipsychotica of behandeling van aanhoudende psychotische klachten wordt verwezen naar de richtlijn schizofrenie uit 2012 en aanvullende relevante literatuur over dit onderwerp die daarna verschenen is. Een samenvatting van deze literatuur valt buiten het bereik van deze module.
|
Psychosociale interventies om recidieven te voorkomen bij psychotische stoornissen. |
|
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg, in vergelijking met standaard zorg alleen, de kans op een recidief op de korte termijn niet verkleint.
(Jones, Hacker, Xia, et al., 2018) |
|
⊕⊕⊕⊕ |
Cognitieve gedragstherapie in combinatie met standaardzorg resulteert in een reductie van de kans op het optreden van een recidief op de midden lange termijn.
(Jones, Hacker, Xia, et al., 2018) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg, in vergelijking met standaard zorg alleen, de kans op een recidief op de lange termijn niet verkleint.
(Jones, Hacker, Xia, et al., 2018) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg de kans op het krijgen van een recidief op de korte en lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie georiënteerde therapievormen.
(Jones, Hacker, Meaden, et al., 2018) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg de kans op het krijgen van een recidief op de midden lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie georiënteerde therapievormen.
(Jones, Hacker, Meaden, et al., 2018) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg de kans op heropnames niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie georiënteerde therapie.
(Jones, Hacker, Meaden, et al., 2018) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat een sociale vaardigheidstraining ten opzichten van standaardzorg de kans op een recidief en heropnames verkleint.
(Almerie et al., 2015) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat familie georiënteerde interventies, in vergelijking met andere interventies en TAU, de kans op een recidief verlagen tijdens de eerste 12 maanden van de interventie.
(Pilling et al., 2002) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat familie georiënteerde interventies, vergeleken met andere interventies en TAU, op de lange termijn geen verschil laten zien in de kans van het optreden van een recidief.
(Pilling et al., 2002) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat wanneer familie georiënteerde interventies vergeleken worden met andere actieve interventies er geen verschil is de kans van het optreden van een recidief tijdens het eerste jaar van de interventie.
(Pilling et al., 2002) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat psycho-educatieve interventies bij de kans op het optreden van een recidief op het moment van afronding verkleint.
(Lincoln et al., 2007) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies de kans op het optreden van een recidief op de korte en midden lange en lange termijn verkleint.
(Lincoln et al., 2007) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies de kans op het optreden van een recidief op de lange termijn niet verkleint.
(Lincoln et al., 2007) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies waarin familieleden worden betrokken de kans op het optreden van een recidief op de midden lange termijn verkleint.
(Lincoln et al., 2007) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies waarin familieleden niet worden betrokken de kans op het optreden van een recidief op de midden lange termijn niet verkleint.
(Lincoln et al., 2007) |
|
farmacologische interventies om recidieven te voorkomen bij psychotische stoornissen. |
|
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat het gebruik van antipsychotica vergeleken met placebo resulteert in een grote reductie van de kans op het optreden van een recidief.
(Leucht et al., 2012) |
|
⊕⊕⊕⚪ |
Het is aannemelijk dat het gebruik van antipsychotica vergeleken met placebo resulteert in een grote reductie van de kans op heropnames.
(Leucht et al., 2012) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat Amisulpride vergeleken met placebo de kans op een recidief niet verkleint.
(Leucht et al., 2009) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat Aripiprazole in vergelijking met placebo de kans op een recidief verkleint.
(Leucht et al., 2009) |
|
⊕⊕⊕⚪ |
Het is aannemelijk dat Olazapine in vergelijking met placebo de kans op een recidief verkleint.
(Leucht et al., 2009) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat Ziprasidone en Zotepine in vergelijking met placebo de kans op een recidief verkleint.
(Leucht et al., 2009) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat Amisulpride, Arpiprazole, Clozapine, Iloperidone, Quetiapine en Olanzapine vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief.
(Kishimoto et al., 2013) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat Risperidone en Ziprasidone vergeleken met een 1ste generatie antipsychoticum leidt tot een afname in de kans van het optreden van een recidief.
(Kishimoto et al., 2013) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat Sertindole vergeleken met een 1ste generatie antipsychoticum leidt tot een afname in de kans van het optreden van een recidief.
(Kishimoto et al., 2013) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat Pimozide in vergelijking met placebo de kans op een recidief niet verkleint.
(Mothi & Sampson, 2013) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat er geen verschil in de kans van het optreden van een recidief is wanneer Pimozide vergeleken wordt met andere antipsychotica.
(Mothi & Sampson, 2013) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat wanneer Pimozide gecombineerd wordt met een ander antipsychoticum dit de kans verkleint op het optreden van een recidief in vergelijking met een behandeling met een enkel antipsychoticum.
(Mothi & Sampson, 2013) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat een standaard dosering van een antipsychoticum vergeleken met een lage en zeer lage dosering van hetzelfde middel de kans op een recidief verkleint.
(Højlund et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat er geen verschil in de kans is van het optreden van een opname wanneer een lage en een zeer lage dosering van een antipsychoticum wordt vergeleken met de standaard dosering.
(Højlund et al., 2021) |
|
⊕⊕⊕⊕ |
Zowel een 1 maandelijkse of 3 maandelijkse injectie dosis van paliperdone ten opzichte van een placebo lijkt de kans op een recidief te verkleinen.
(Ostuzzi et al., 2021) |
|
⊕⊕⊕⚪ |
Het is aannemelijk dat aripiprazole, risperidone, pipothiazine en olanzapine injecties in vergelijking met placebo de kans op een recidief verkleint.
(Ostuzzi et al., 2021) |
|
⊕⊕⚪⚪ |
Er zijn aanwijzingen dat flupenthixol en fluphenazine injecties in vergelijking met placebo de kans op een recidief verkleint.
(Ostuzzi et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat haloperidol injecties in vergelijking met placebo de kans op een recidief verkleint.
(Ostuzzi et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat zuclopenthixol en bromperidol injecties in vergelijking met placebo de kans op een recidief niet verkleint.
(Ostuzzi et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat depotmedicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de gecombineerde kans op het optreden van een heropname of een recidief verkleint.
(Kishimoto et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat depotmedicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de kans op het optreden van een heropname verkleint.
(Kishimoto et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat depotmedicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de kans op het optreden van een recidief niet verkleint.
(Kishimoto et al., 2021) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat er geen verschil in kans is op een recidief tussen poly-antipsychotica therapieën en mono-antipsychotica therapieën.
(Ortiz-Orendain et al., 2017) |
|
⊕⚪⚪⚪ |
Er zijn voorzichtige aanwijzingen dat de kans op een recidief en heropnames niet verhoogd wanneer met van een poly-antipsychotica therapie overstapt naar een mono-antipsychotica regime.
(Matsui et al., 2019) |
Almerie2015
In een Cochrane review uitgevoerd door Almerie en collega’s (2015) werd het effect van het volgen van sociale vaardigheidstrainingen op onder andere het optreden van een recidief en heropnames bij mensen met schizofrenie in vergelijking met standaardzorg onderzocht. In deze review worden sociale vaardigheidstrainingen gedefinieerd als gedragstherapieën en technieken waarin mensen wordt geleerd hun emoties en behoeftes uit te spreken naar andere toe. In totaal werden er 13 RCT’s (n = 975) meegenomen waarvan er twee keken naar de kans van het optreden van een recidief en 1 naar de kans van heropnames. Uit de uitgevoerde meta-analyse kwam naar voren dat het volgen van een sociale vaardigheidstrainingsprogramma de kans op een recidief en de kans op heropnames verkleint vergelijking met standaardzorg. Echter, doormiddel van GRADING werd het vertrouwen in het bewijs door Almerie en collega’s als zeer laag ingeschaald. Voor deze GRADING zie tabel 2 in Evidence tabellen.
Jones2018a
In een Cochrane review uitgevoerd door Jones en collega’s (2018)a werd het effect van cognitieve gedragstherapie (CGT) in combinatie met standaard zorg vergeleken met standaard zorg in combinatie met andere vormen van therapie bij mensen met schizofrenie. De auteurs definieerde andere vormen van therapie als therapie vormen die geen cognitief gedragscomponent hadden zoals bijvoorbeeld psycho-educatie, familietherapie en andere vormen die niet onder CGT vallen. In totaal werden er 36 studies meegenomen (n=3542). Van de 36 studies keken er 5 (n=375) naar het optreden van een recidief op de lange termijn. Hierbij werd er geen verschil tussen CGT en andere vormen van therapie gevonden. De meta-analyse op basis van 8 studies (n=943) vond ook geen verschil in heropnames op de lange termijn. In de tabel 3 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen. Wanneer de GRADING score overgenomen is uit Jones2019 wordt dit doormiddel van een * aangegeven.
Jones2018b
De Cochrane review van Jones en collega’s (2018b) onderzocht het effect van CGT in combinatie met standaardzorg op het optreden van een recidief bij mensen met schizofrenie. In totaal includeerden de auteurs 60 studies (n=5992). Een therapie werd als cognitieve gedragstherapie gezien wanneer het een afgebakende therapievorm betrof waarin men inzicht kreeg in de associaties tussen en herwaardering van de eigen symptomen, overtuigingen en gedachten en de hieruit voortvloeiende gedragingen en ervaren stress. Standaardzorg betrof in de meeste gevallen een behandeling met een antipsychoticum, opnames en gebruik van psychiatrische dag voorzieningen. Dertien studies (n=1538) onderzochten de kans op het optreden van een recidief, waarbij onderscheid werd optreden van een recidief op de korte termijn (binnen 24 weken vanaf studie aanvang), de midden lange termijn (tussen de 24 weken en 52 weken na studie aanvang) en de lange termijn (na 52 weken van studie aanvang). Hier werd er geen verschil gevonden in de kans van het optreden van een recidief op de lange termijn voor CGT in combinatie met standaardzorg in vergelijking met standaardzorg alleen. Doormiddel van GRADING schaalde Jones en collega’s het vertrouwen van bewijs als laag in. Op basis van 2 RCT’s (n=92) werd er op de korte termijn geen verschil gevonden in de kans van het optreden van een recidief. Wel liet CGT op de midden lange termijn een reductie in de kans van het optreden van een recidief zien (5 RCT’s , n= 667). In de tabel 4 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen. Wanneer de GRADING overgenomen is uit het originele artikel wordt dit aangegeven met een *.
Lincoln2007
In een meta-analyses uitgevoerd door Lincoln et al. (2007) werd het effect van psycho-educatieve interventies bij mensen met psychotische stoornissen onderzocht in vergelijking met TAU of een wachtlijst controle groep. Men keek hierbij ook specifiek naar het effect op het optreden van een recidief vlak na afronding (< 6 maanden), midden lange termijn (7 t/m 12 maanden) en de lange termijn (>12 maanden). De psycho-educatieve interventies konden verdeeld worden in interventies gericht op de persoon met een psychotische stoornis, interventies gericht op naasten en interventies die een combinatie van beide waren. In totaal werden er 18 studies (n=1534) meegenomen in deze meta-analyse. Er werd gevonden dat psycho-educatieve interventies direct na afronding (5 RCT’s , n =452) , op de korte termijn (4 RCT’s, n =387) en op de midden lange termijn (7 RCT’s , n =362) een reductie in recidief lieten zien. Dit was niet het geval op de lange termijn (3 RCT’s, n =144). Interventies waarin familieleden werden betrokken lieten op de midden lange termijn een reductie in heropnames zien (6 RCT’s, n =322), dit was niet het geval voor interventies zonder familiebetrokkenheid (2 RCT’s, n =101). In de tabel 5 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Pilling2002
In een meta-analyse uitgevoerd door Pilling et al. (2002) werden de effecten van familie georiënteerde interventies onderzocht voor mensen met schizofrenie. Familie interventie studies werden meegenomen wanneer deze o.a. een gezamenlijke familie sessie bevatte in combinatie met een psycho-educatieve component, een probleem oplossend of crisis management component of een combinatie van deze componenten. De duur van de interventies was minimaal zes weken. In totaal werden 18 studies (n=1467) in de meta-analyse meegenomen. Wanneer familie interventies vergeleken werden met andere type interventies (inclusief TAU) werden er minder recidieven gerapporteerd tijdens de eerste 12 maanden van de interventie (11 RCT’s, n=729). Wanneer familie interventies vergeleken werden met actieve interventies (exclusief TAU) werd er geen verschil gevonden in recidieven (5 RCT’s, n=357). Wanneer er gekeken werd tot aan 15 maanden na afronding van de interventie, werd er geen verschil gevonden in gerapporteerde recidieven tussen familie interventies gericht op één familielid en andere type interventies (4 RCT’s, n=228). In tabel 6 en tabel 7 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Resultaten farmacologische interventies
Effecten van verschillende antipsychotica op recidieven en heropnames.
Leucht2009
Leucht en collega’s (2009) voerde een meta-analyse uit waarin atypische antipsychotica vergeleken werden met een placebo controle conditie. In totaal werden er 38 studies (n=7323) meegenomen waarin atypische antipsychotica vergeleken werden met placebo bij de behandeling van schizofrenie. In totaal waren er 8 studies die keken naar het optreden van een recidief na 6 tot 12 maanden na aanvang van de studie. Van deze 8 studies keken er 2 studies (n=246) naar amisulpride, 1 studie (n =310 ) naar aripiprazole, 3 studies (n=559) naar olanzapine, 1 studie (n=227) naar ziprasidone en 1 studie (n=119) naar zotepine. Van deze antipsychotica werd er alleen bij amisulpride geen afname in de kans van het optreden van een recidief gevonden. Voor de resultaten van alle vergelijkingen van specifieke antipsychotica wordt verwezen naar tabel 8 in Evidence tabellen. In deze tabel wordt ook het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Leucht2012
In een meta-analyse uitgevoerd door Leucht e.a. (2012) werd onderzocht wat het effect van antipsychotica is op recidief preventie in vergelijking met placebo. In totaal werden er 65 studies(n=6493) meegenomen waarin antipsychotica werd gebruikt voor de behandeling van schizofrenie of gerelateerde stoornissen. Er werden verschillende antipsychotica meegenomen, en er werd geen onderscheid gemaakt tussen depot of orale toediening van de medicatie. De mediaan van de looptijd van deze studies was 26 weken. Van deze 65 studies keken er 24 studies (n=2669) naar de kans van het optreden van een recidief binnen de 7 en 12 maanden. Er werd gevonden dat de kans op een recidief werd verkleind bij het gebruik van antipsychotica, vergeleken met placebo. zestien studies (n=2090) onderzochten ook het effect op heropnames, het gebruik van een antipsychoticum verkleinde de kans op heropnames. In tabel 9 van bijlage 17 wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Kishimoto2013
Kishimoto en collega’s (2013) voerde een meta-analyse uit waarin 1ste generatie antipsychotica vergeleken werden met 2de generatie antipsychotica (amisulpiride, aripirpazol, clozapine, iloperidone, olanzapine, quetiapine, risperidon, sertindol en ziprasidone) bij mensen met schizofrenie of gerelateerde stoornissen. In totaal werden in de meta-analyse 23 studies (n=4504) meegenomen waarin deze twee klassen van medicatie met elkaar werden vergeleken. Geïncludeerde studies hadden een looptijd van minimaal zes maanden. In totaal werd erbij negen 2de generatie antipsychotica gekeken wat de kans van het optreden van een recidief was op het moment van studie afronding. Van deze 9 antipsychotica werd bij risperidon (6 RCT's, n = 1124) , sertindol (1 RCT, n =203) en ziprasidone (1 RCT, n =66) een significante afname in de kans van het optreden van een recidief gevonden ten opzichte van 1ste generatie antipsychotica. Voor de resultaten van alle vergelijkingen tussen specifieke antipsychotica en de bij bijbehorende GRADING wordt verwezen naar tabel 10 in Evidence tabellen.
Mothi2013
In een Cochrane review uitgevoerd door Mothi en Sampson (2013) werd pimozide vergeleken met placebo, andere antipsychotica of geen behandeling bij de behandeling van schizofrenie en gerelateerde stoornissen. In totaal werden er 32 studies geïncludeerd. In termen van recidieven werd gevonden dat wanneer pimozide wordt vergeleken met placebo er geen verschil was op de midden lange termijn (3 tot 12 maanden, 1 RCT, n=20). Wanneer pimozide werd vergeleken met andere antipsychotica werd er geen verschil gevonden in de kans van het optreden van een recidief (7 RCT’s, n=227). Wel werd er gevonden dat wanneer pimozide wordt gecombineerd met een ander antipsychoticum er minder recidieven op treden in vergelijking met een antipsychoticum alleen (1 RCT, n=69).
In de tabellen 11, 12 en 13 in bijlage 17 wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen. De GRADING is gedeeltelijk overgenomen zoals deze wordt beschreven in Mothi et al. (2013) en deze worden aangegeven doormiddel van een * in de tabellen.
Effecten van medicatie dosering op recidieven en heropnames.
Højlund2021
In een meta-analyse uitgevoerd door Højlund en collega’s (2021) werd het effect van verschillende doseringsstrategieën van antipsychotica op het optreden van een recidief onderzocht. Hierbij werden een standaard dosering (een dosis hoger dan de laagst vastgestelde standaardwaarde zoals gedefinieerd door de ‘International Consensus Study’), een lage dosering (50 tot 99% van het laagste limiet van de standaard dosering) en een zeer lage dosering (minder dan 50% van het laagste limiet van de standaard dosering) met elkaar vergeleken. Deze vergelijkingen werden binnen hetzelfde antipsychoticum gedaan bij mensen die ten minste 24 weken gediagnostiseerd waren met schizofrenie of een schizoaffectieve stoornis. In de meta-analyse werden 22 studies meegenomen (n=3282). Vergeleken met een standaard dosering lijkt een lage dosering de kans op het optreden van een recidief te verhogen (16 RCT’s, n = 1920) en dit was ook het geval bij een zeer lage dosering (13 RCT’s, n=2058). Er werd geen significant verschil gevonden tussen een lage en een zeer lage dosering in termen van het optreden van een recidief (5 RCT’s, n=686). Er werden geen significante verschillen gevonden in het optreden van heropnames wanneer een standaard dosering vergeleken werd met een lage dosering (5 RCT’s, n=431) of een zeer lage dosering (6 RCT’s, n =743). In de tabel 14 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Effect van depotmedicatie op recidieven en heropnames
Ostuzzi2021
In een netwerk meta-analyse uitgevoerd door Ostuzzi en collega’s (2021) werd het gebruik van verschillende langdurig werkende antipsychotica injecties vergeleken met placebo en met elkaar. Voor onze huidige vraagstelling is de vergelijkingen met placebo relevant. In totaal werden er 78 studies (n=11505) meegenomen in de netwerk analyse. Voor de uitkomst maat van het optreden van een recidief werd gekeken naar het optreden van een recidief aan het einde van een studie. In het grootste deel van de geïncludeerde studies waren deelnemers mensen met schizofrenie en in een klein aantal studies waren deelnemers mensen met een schizoaffectieve stoornis. De auteurs maken hierbij wel de kanttekening dat de diagnose criteria tussen studies verschilde, mede doordat de studies over een groot tijdbestek uitgevoerd waren. Een CINeMA assessment werd door de auteurs uitgevoerd om het vertrouwen in het bewijs te boordelen. Deze methode heeft gelijkenissen met de GRADE methode maar is toegespitst op het gebruik bij meta netwerkanalyses. De uitgevoerde CINeMA assessment zoals beschreven in Ostuzzi et al. (2021) is overgenomen in deze richtlijn. In de meeste gevallen werd het vertrouwen in het bewijs ‘afgewaardeerd’’ door een verhoogde risk of bias op het gebied van ‘reporting’, ‘attrition’ en ‘sponsorship’.
Wanneer er gekeken wordt naar de kans van het optreden van een recidief blijken alleen zuclopenthixol en broomperidol injecties de kans op een recidief niet te verkleinen ten opzichte van placebo. Bij paliperidone (zowel bij een 1 maand of 3 maanden dosis) was hierbij het vertrouwen in het bewijs het hoogst. Een overzicht van alle type injecties en het vertrouwen in bewijs wordt in onderstaande tabel weergegeven.
De vermindering in de kans van het optreden van een recidief voor antipsychotica injecties ten opzichten van placebo.
|
Type injectie |
RR (95% BI) |
Vertrouwen in het bewijs** |
|
Paliperidon (3 maanden dosis) |
0.27 (0.17;0.42) * |
Hoog |
|
Aripiprazol |
0.29 (0.21;0.39) * |
Redelijk |
|
Flupenthixol |
0.32 (0.16;0.65) * |
Laag |
|
Fluphenazine |
0.34 (0.24;0.48) * |
Laag |
|
Risperidon |
0.34 (0.23;0.52) * |
Redelijk |
|
Pipothiazine |
0.35 (0.20;0.62) * |
Redelijk |
|
Olanzapine |
0.37 (0.26;0.53) * |
Redelijk |
|
Paliperidon (1 maand dosis) |
0.39 (0.30;0.50) * |
Hoog |
|
Zuclopenthixol |
0.41 (0.13;1.31) |
Zeer laag |
|
Broomperidol |
0.50 (0.22;1.15) |
Zeer laag |
|
Haloperidol |
0.57 (0.33;0.97) * |
Zeer laag |
.* Significant effect (p < 0.05). ** CINeMA assessment beoordeling overgenomen uit Ostuzzi et al. 2021
Kishimoto2021
In een meta-analyse uitgevoerd door Kishimoto en collega’s (2021) werd het effect van langdurig werkende antipsychotica injecties vergeleken met antipsychotica die oraal worden toegediend bij mensen met schizofrenie of gerelateerde stoornissen. In deze meta-analyse werden zowel RCT’s, cohort studies en pre-post studies meegenomen. Hier wordt alleen verder ingegaan op de RCT resultaten. In totaal werden er 32 RCT’s (n =8577) in deze meta-analyse meegenomen en hadden onderhouds-en recidiefpreventiestudies een looptijd van minimaal 6 maanden. De kans op het optreden van zowel een heropname of een recidief voor depotmedicatie was significant kleiner in vergelijking met orale antipsychotica (29 RCT’s, n=7833). Wanneer er naar heropnames alleen gekeken wordt dan is de kans op een heropname kleiner voor depotmedicatie in vergelijking met orale antipsychotica (18 RCT’s, n=4310) maar werd er geen significant verschil gevonden in het optreden van een recidief (27 RCT’s, n=7407). In de tabel 15 wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Effecten van verschillende medicatie strategieën op het optreden van recidieven en heropnames
Ortiz-Orendain2017
In een Cochrane review uitgevoerd door Ortiz-Orendain en collega’s (2017) werden poly-farmaca behandelingen vergeleken met mono-farmaca behandelingen bij schizofrenie of aanverwante stoornissen. In totaal werden er 62 studies meegenomen in deze review. Van deze studies keken 3 RCT’s naar het effect op recidief preventie: 1 RCT (n=70) vergeleek de combinatie van clozapine met sulpiride met het gebruik van clozapine alleen. Er werd geen significant verschil gevonden het optreden van een recidief tussen beide condities. In 2 RCT’s (n= 442) werd de combinatie van een klassiek antipsychoticum met zowel pimozide of perphenazine vergeleken met het gebruik van een klassiek antipsychoticum alleen. Ook hier werd er geen significant verschil gevonden in het optreden van een recidief. In tabel 16 in Evidence tabellen wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Matsui2019
In een meta-analyse uitgevoerd door Matsui en collega’s (2019) werd het effect van overstappen van een antipsychotica polyfarmaca therapie (waarbij tweeof meer anti psychotische medicijnen worden ingezet) naar monotherapie (waarbij 1 type antipsychotica wordt gebruikt) bij de behandeling van schizofrenie en gerelateerde stoornissen onderzocht. In totaal werden er 6 RCT’s (n= 341) meegenomen in deze meta-analyse en werden er verschillende soorten antipsychotica gebruikt. In termen van de kans van het optreden van recidieven werd er geen verschil gevonden tussen het switchen naar monotherapie of het blijven bij een polyfarmaca therapie (4 RCT’s, n= 123). Ook werd er geen effect gevonden op de kans van het optreden van heropnames (1 RCT, n= 114). In de tabel 17 wordt het vertrouwen in het bewijs doormiddel van GRADE weergegeven inclusief de redenen hoe deze score tot stand is gekomen.
Uitgangsvraag 1a is bij uitstek een vraag met een zeer persoonlijk antwoord, die niet goed te beantwoorden is op grond van RCT’s. Voor uitgangsvraag 1a is daarom geen PICO geformuleerd. Overwegingen bij uitgangsvraag 1a worden daarom apart besproken. Voor uitgangsvraag 1b wordt hieronder de literatuur review beschreven.
PICO voor uitgangsvraag 3 (zie bijlage review protocol).
|
P |
Personen met een psychotische stoornis met een episodisch of aanhoudend beloop (mensen met een episodisch of aanhoudend psychotische stoornis, in (partiele) remissie, stages 3 en 4) |
|
I |
Plannen om recidief te voorkomen (bv crisisplan of kaart, terugvalpreventieplan of signaleringsplan) Cognitieve gedragstherapie met als doel om recidief te voorkomen therapietrouwheidstherapie Alle antipsychotica welke in Nederland geregistreerd zijn voor de onderhoudsbehandeling van psychosen, incl depotmedicatie |
|
C |
Placebo Care as usual (CAU) Wachtlijst Een van de eerder genoemde actieve interventies als alternatieve behandeling |
|
O |
Relapse (frequentie en tijd tot eerste recidiefpsychose) Relapse (Ziekenhuisopname door recidiefpsychose) Ernst symptomen (positieve en negatieve) Kwaliteit van leven Depressieve symptomen (Psycho)sociaal functioneren (bijv mbv WHODAS-II) |
|
T |
gedurende een bepaalde tijdsperiode (geen restricties) |
Selectie van studies
Op 20 en 21 december 2020 is er een search gedaan in Pubmed, PsycInfo, Medline en de Cochrane Library, de zoekstrategie is opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase. Op 10 maart 2021 is er nog een aanvullende search uitgevoerd in Medline en Embase omdat de eerste search vooral systematische reviews en meta-analyses opleverde voor terugvalpreventie na het optreden van een eerste psychotische episode. De search leverde na ontdubbelen 475 systematische reviews en meta-analyses op. Na selectie op titel en abstract bleven er 51 artikelen over. Op basis van de selectie op de volledige teksten zijn er 13 reviews meegenomen ter beoordeling. Reden voor exclusie waren dat de patiënten groep toch niet overeenkwamen met de PICO, recidief cijfers toch niet geanalyseerd bleken te zijn, recentere Cochrane updates bleken te zijn en dat er overlap tussen de in de reviews geïncludeerde studies was. In het geval van overlap is er gekozen om alleen de meest recente meta-analyse te beoordelen. Omdat er tijdens het proces van het opstellen van de richtlijn er sinds maart 2021 zeer relevante meta-analyses zijn verschenen is er nog een laatste search gedaan. Deze was hetzelfde als de voorgaande search maar was beperkt over een de tijdsinterval van maart tot aan juli 2021. Uit deze search kwamen 119 referenties waarvan er op basis van de beoordeling van titel, abstract en volledige teksten 3 meta-analyses meegenomen zijn voor verdere beoordeling.
Na deze laatstse search en het voltooien van de commentaarversie van deze richtlijn verscheen nog een relevante meta-analyse van Leucht et al (2021) over de optimale dosering van antipsychotica bij terugvalpreventie. Gezien de relevantie van deze publicatie is deze alsnog in de module opgenomen. Omdat deze studie buiten de hier gebruikte systematische zoekstrategie valt (ivm de datum van verschijnen die na de searchdatum valt), is deze studie beschreven in de praktijkoverwegingen. In een toekomstige herziening van dit onderwerp zal de studie in de systematische search verschijnen, worden ge-GRADE en worden meegenomen in de wetenschappelijke conclusie.
- Castelein S, Timmerman ME; PHAMOUS investigators, van der Gaag M, Visser E. Clinical, societal and personal recovery in schizophrenia spectrum disorders across time: states and annual transitions. Br J Psychiatry. 2021 Jul;219(1):401-408. doi: 10.1192/bjp.2021.48. PMID: 35048855; PMCID: PMC8529640.
- Almerie, M. Q., Okba Al Marhi, M., Jawoosh, M., Alsabbagh, M., Matar, H. E., Maayan, N., & Bergman, H. (2015). Social skills programmes for schizophrenia. Cochrane Database of Systematic Reviews. https://doi.org/10.1002/14651858.CD009006.pub2
- Groenwold RH., Brenkman HJF, Houwert RM. Trials, observationeel onderzoek en de 'echte' wereld Ned Tijdschr Geneeskd. 2021;165:D5514
- Højlund, M., Kemp, A. F., Haddad, P. M., Neill, J. C., & Correll, C. U. (2021). Standard versus reduced dose of antipsychotics for relapse prevention in multi-episode schizophrenia: a systematic review and meta-analysis of randomised controlled trials. The Lancet Psychiatry, 8(6), 471-486. https://doi.org/10.1016/S2215-0366(21)00078-X
- Jones, C., Hacker, D., Meaden, A., Cormac, I., Irving, C. B., Xia, J., Zhao, S., Shi, C., & Chen, J. (2018a). Cognitive behavioural therapy plus standard care versus standard care plus other psychosocial treatments for people with schizophrenia. Cochrane Database of Systematic Reviews. https://doi.org/10.1002/14651858.CD008712.pub3
- Jones, C., Hacker, D., Xia, J., Meaden, A., Irving, C. B., Zhao, S., Chen, J., & Shi, C. (2018b). Cognitive behavioural therapy plus standard care versus standard care for people with schizophrenia. Cochrane Database of Systematic Reviews. https://doi.org/10.1002/14651858.CD007964.pub2
- Kishimoto, T., Agarwal, V., Kishi, T., Leucht, S., Kane, J. M., & Correll, C. U. (2013). Relapse prevention in schizophrenia: a systematic review and meta-analysis of second-generation antipsychotics versus first-generation antipsychotics. Molecular Psychiatry, 18(1), 53-66. https://doi.org/10.1038/mp.2011.143
- Kishimoto, T., Hagi, K., Kurokawa, S., Kane, J. M., & Correll, C. U. (2021). Long-acting injectable versus oral antipsychotics for the maintenance treatment of schizophrenia: a systematic review and comparative meta-analysis of randomised, cohort, and pre-post studies. The Lancet Psychiatry, 8(5), 387404. https://doi.org/10.1016/S2215-0366(21)00039-0
- Leucht, S., Arbter, D., Engel, R. R., Kissling, W., & Davis, J. M. (2009). How effective are second-generation antipsychotic drugs? A meta-analysis of placebo-controlled trials. Molecular Psychiatry, 14(4), 429-447. https://doi.org/10.1038/sj.mp.4002136
- Leucht, S., Tardy, M., Komossa, K., Heres, S., Kissling, W., Salanti, G., & Davis, J. M. (2012). Antipsychotic drugs versus placebo for relapse prevention in schizophrenia: a systematic review and meta-analysis. The Lancet, 379(9831), 2063-2071. https://doi.org/10.1016/S0140-6736(12)60239-6
- Leucht S, Bauer S, Siafis S, Hamza T, Wu H, Schneider-Thoma J, Salanti G, Davis JM. Examination of Dosing of Antipsychotic Drugs for Relapse Prevention in Patients With Stable Schizophrenia: A Meta-analysis. JAMA Psychiatry. 2021 Nov 1;78(11):1238-1248. doi: 10.1001/jamapsychiatry.2021.2130. PMID: 34406325; PMCID: PMC8374744.
- Lincoln, T., Wilhelm, K., & Nestoriuc, Y. (2007). Effectiveness of psychoeducation for relapse, symptoms, knowledge, adherence and functioning in psychotic disorders: A meta-analysis. Schizophrenia Research, 96(1-3), 232-245. https://doi.org/10.1016/j.schres.2007.07.022
- Matsui, K., Tokumasu, T., Takekita, Y., Inada, K., Kanazawa, T., Kishimoto, T., Takasu, S., Tani, H., Tarutani, S., Hashimoto, N., Yamada, H., Yamanouchi, Y., & Takeuchi, H. (2019). Switching to antipsychotic monotherapy vs. staying on antipsychotic polypharmacy in schizophrenia: A systematic review and meta-analysis. Schizophrenia Research, 209, 50-57. https://doi.org/10.1016/j.schres.2019.05.030
- Mothi, M., & Sampson, S. (2013). Pimozide for schizophrenia or related psychoses. Cochrane Database of Systematic Reviews. https://doi.org/10.1002/14651858.CD001949.pub3
- Ortiz-Orendain, J., Castiello-de Obeso, S., Colunga-Lozano, L. E., Hu, Y., Maayan, N., & Adams, C. E. (2017). Antipsychotic combinations for schizophrenia. Cochrane Database of Systematic Reviews. https://doi.org/10.1002/14651858.CD009005.pub2
- Ostuzzi, G., Bertolini, F., Del Giovane, C., Tedeschi, F., Bovo, C., Gastaldon, C., Nosé, M., Ogheri, F., Papola, D., Purgato, M., Turrini, G., Correll, C. U., & Barbui, C. (2021). Maintenance Treatment With Long-Acting Injectable Antipsychotics for People With Nonaffective Psychoses: A Network Meta-Analysis. American Journal of Psychiatry, 178(5), 424-436. https://doi.org/10.1176/appi.ajp.2020.20071120
- Pilling, S., Bebbington, P., Kuipers, E., Garety, P., Geddes, J., Orbach, G., & Morgan, C. (2002). Psychological treatments in schizophrenia: I. Meta-analysis of family intervention and cognitive behaviour therapy. Psychological Medicine, 32(05). https://doi.org/10.1017/S0033291702005895
- Schennach R, Obermeier M, Spellmann I, Seemüller F, Musil R, Jäger M, Schmauss M, Laux G, Pfeiffer H, Naber D, Schmidt LG, Gaebel W, Klosterkötter J, Heuser I, Bauer M, Adli M, Zeiler J, Bender W, Kronmüller KT, Ising M, Brieger P, Maier W, Lemke MR, Rüther E, Klingberg S, Gastpar M, Möller HJ, Riedel M. Remission in schizophrenia - What are we measuring? Comparing the consensus remission criteria to a CGI-based definition of remission and to remission in major depression. Schizophr Res. 2019 Jul;209:185-192. doi: 10.1016/j.schres.2019.04.022. Epub 2019 May 25. PMID: 31138482.
- Taipale H, Mehtälä J, Tanskanen A, Tiihonen J. Comparative Effectiveness of Antipsychotic Drugs for Rehospitalization in Schizophrenia-A Nationwide Study With 20-Year Follow-up. Schizophr Bull. 2018 Oct 17;44(6):1381-1387. doi: 10.1093/schbul/sbx176. Erratum in: Schizophr Bull. 2019 Oct 24;45(6):1381. PMID: 29272458; PMCID: PMC6192491.
- Taipale, H., Schneider-Thoma, J., Pinzon-Espinosa, J., Radua, J., Efthimiou, O., Vinkers, C. H., Mittendorfer- Rutz, E., Cardoner, N., Pintor, L., Tanskanen, A., Tomlinson, A., Fusar-Poli, P., Cipriani, A., Vieta, E., Leucht, S., Tiihonen, J., & Luykx, J. J. (2022). Representation and Outcomes of Individuals With Schizophrenia Seen in Everyday Practice Who Are Ineligible for Randomized Clinical Trials. JAMA Psychiatry, 79(3), 210-218. https://doi.org/10.1001/jamapsychiatry.2021.3990
- Tiihonen J, Mittendorfer-Rutz E, Majak M, Mehtälä J, Hoti F, Jedenius E, Enkusson D, Leval A, Sermon J, Tanskanen A, Taipale H. (2017) Real-World Effectiveness of Antipsychotic Treatments in a Nationwide Cohort of 29 823 Patiënts With Schizophrenia. JAMA Psychiatry; 74(7):686-693. doi: 10.1001/jamapsychiatry.2017.1322. PMID: 28593216; PMCID: PMC5710250.
- Tiihonen J, Taipale H, Mehtälä J, Vattulainen P, Correll CU, Tanskanen A. (2019) Association of Antipsychotic Polypharmacy vs Monotherapy With Psychiatric Rehospitalization Among Adults With Schizophrenia. JAMA Psychiatry; 76(5):499-507. doi:10.1001/jamapsychiatry.2018.4320
Tabel 1. Risicofactoren voor terugval bij gebruik van depot-medicatie
|
Uitkomsten |
Aantal deelnemers |
Certainty of the evidence |
Relatief effect |
|
Risico op recidief voor cohorten in VS |
(19 RCT’s) |
⨁⨁⨁◯ |
HR 1.55 (1.27 tot 1.90) |
|
Risico op recidief voor personen met een ernstiger ziektebeeld bij baseline |
(19 RCT’s) |
⨁⨁⨁◯ |
HR 1.28 (1.12 tot 1.48) |
|
Risico op recidief voor personen met tardieve kinesie |
(17 RCT’s) |
⨁⨁◯◯ |
HR 2.39 (1.05 tot 5.42) |
|
Risico op recidief voor personen met comorbide verslaving |
(4 RCT’s) |
⨁⨁◯◯ |
HR 1.55 (1.15 tot 2.10) |
|
Risico op recidief voor mannen |
(19 RCT’s) |
⨁⨁◯◯ |
HR 1.19 (1.03 tot 1.39) |
|
Recidief voor personen met een slechter algemeen functioneren |
(19 RCT’s) |
⨁⨁◯◯ |
HR 1.01 (1.01 tot 1.02) |
|
Recidief voor personen met een hogere leeftijd bij onset |
(17 RCT’s) |
⨁⨁◯◯ |
HR 0.97 (0.96 tot 0.99) |
a. Heterogeniteit niet in te schatten, b. Laag aantal personen met tardieve kinesie binnen het totaal (n=145), c. Laag aantal personen met comorbide verslaving binnen het totaal (n=346), d. Na Bonferroni-correctie niet meer significant, e. Zeer klein effect (kijken of dit moet worden aangepast in de formulering?
|
Almerie2015 |
||||||
|
Tabel 2. Sociale vaardigheidstrainingen vs. TAU bij schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met TAU |
Risico met Sociale vaardigheidstrainingen |
|||||
|
Recidief |
351 per 1.000 |
183 per 1.000 |
RR 0.52 |
263 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat een sociale vaardigheidstraining ten opzichten van standaardzorg de kans op een recidief verkleint. |
|
Heropnames |
366 per 1.000 |
194 per 1.000 |
RR 0.53 |
143 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat een sociale vaardigheidstraining ten opzichten van standaardzorg de kans op heropnames verkleint. |
* zoals gerapporteerd door Almerie2015 a. De geïncludeerde studies hadden allen een verhoogde RoB. b. Er was heterogeniteit tussen de resultaten. c. Er was een sterk vermoeden op publication bias omdat een minderheid van alle studies deze uitkomst meenamen. d. de studie liet een verhoogd RoB zien. e. Gebaseerd op een klein aantal events.
|
Jones2018a |
||||||
|
Tabel 3. Cognitieve gedragstherapie + standaardzorg vs. andere therapievormen + standaardzorg bij schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met andere therapievormen + standaardzorg |
Risico met CBT + standaardzorg |
|||||
|
Recidief korte termijn |
38 per 1.000 |
28 per 1.000 |
RR 0.72 |
62 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat CBT in combinatie met standaard zorg de kans op het krijgen van een recidief op de korte termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
|
Recidief midden lange termijn |
230 per 1.000 |
232 per 1.000 |
RR 1.01 |
150 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat CBT in combinatie met standaard zorg de kans op het krijgen van een recidief op de midden lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
|
Recidief lange termijn |
463 per 1.000 |
486 per 1.000 |
RR 1.05 |
375 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat CBT in combinatie met standaard zorg de kans op het krijgen van een recidief op de lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
|
Heropnames korte termijn (bij afronding) |
212 per 1.000 |
93 per 1.000 |
RR 0.44 |
65 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat CBT in combinatie met standaard zorg de kans op heropnames op de korte termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
|
Heropnames midden lange termijn |
244 per 1.000 |
210 per 1.000 |
RR 0.86 |
344 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat CBT in combinatie met standaard zorg de kans op heropnames op de midden lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
|
Heropnames |
375 per 1.000 |
360 per 1.000 |
RR 0.96 |
943 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat CBT in combinatie met standaard zorg de kans op heropnames op de lange termijn niet verkleint in vergelijking met andere vormen van therapie zoals psychoeducatie of familie therapieën. |
* Grading overgenomen van Jones2019. a. klein aantal events en 95% BI doorkruist gebied van geen verschil. b. Bij meerdere studies is er een verhoogd RoB. c. 95% BI doorkruist het gebied van geen verschil.
Jones2018b
|
Tabel 4. Cognitieve gedragstherapie + standaardzorg vs. standaardzorg alleen bij schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met standaardzorg |
Risico met CGT + standaardzorg |
|||||
|
Recidief op de korte termijn |
159 per 1.000 |
35 per 1.000 |
RR 0.22 |
92 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg, in vergelijking met standaard zorg alleen, de kans op een recidief op de korte termijn niet verkleint. |
|
Recidief op de midden lange termijn |
268 per 1.000 |
142 per 1.000 |
RR 0.53 |
667 |
⨁⨁⨁⨁ |
Cognitieve gedragstherapie in combinatie met standaardzorg resulteert in een reductie van de kans op het optreden van een recidief op de midden lange termijn. |
|
Recidief op de lange termijn* |
333 per 1.000 |
260 per 1.000 |
RR 0.78 |
1538 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat cognitieve gedragstherapie in combinatie met standaard zorg, in vergelijking met standaard zorg alleen, de kans op een recidief op de lange termijn niet verkleint. |
a. Gebaseerd op een klein aantal events en breed 95% BI. b. Deel van de studies laat een verhoogd RoB zien. c. Heterogeniteit tussen de studies. d. 95% BI doorkruist het gebied van geen verschil.
|
Lincoln2007 |
||||||
|
Tabel 5. Psycho educatie versus TAU of wachtlijst controle groep in schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met TAU of wachtlijst |
Risico met psycho educatie |
|||||
|
Recidief direct na afronding |
|
ES 0.53 hoger |
- |
452 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat psycho-educatieve interventies bij de kans op het optreden van een recidief op het moment van afronding verkleint. |
|
Recidief op korte termijn |
|
ES 0.35 hoger |
- |
387 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies de kans op het optreden van een recidief op de korte termijn verkleint. |
|
Recidief op midden lange termijn |
|
ES 0.48 hoger |
- |
362 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies de kans op het optreden van een recidief op de midden lange termijn verkleint. |
|
Recidief op de lange termijn |
|
ES 0.21 hoger |
- |
144 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies de kans op het optreden van een recidief op de lange termijn niet verkleint. |
|
Recidief op de midden lange termijn (interventie met familie betrokkenheid) |
|
ES 0.48 hoger |
- |
322 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies waarin familieleden worden betrokken de kans op het optreden van een recidief op de midden lange termijn verkleint. |
|
Recidief op de midden lange termijn (interventie zonder familie betrokkenheid) |
|
ES 0.18 hoger |
- |
101 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat psycho-educatieve interventies waarin familieleden niet worden betrokken de kans op het optreden van een recidief op de midden lange termijn niet verkleint. |
a. Er was sprake van heterogeniteit tussen de studies. b. Gebaseerd op een klein aantal events en er is sprake van een klein effect. c. Gebaseerd op een klein aantal events. Er is sprake van een klein effect en het 95% BI doorkruist het gebied van geen verschil. e. Studies hadden onduidelijke of verhoogde risk of bias.
|
Pilling2002 |
||||||
|
Tabel 5. Familie georiënteerde interventies vs. andere interventies (inc. TAU) voor schizofrenie |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met andere interventies (inc. TAU) |
Risico met familie georiënteerde interventies |
|||||
|
Recidief tijdens 1ste jaar van interventie |
|
|
OR 0.52 |
(11 RCT’s) |
⨁⨁◯◯ |
Er zijn aanwijzingen dat familie georiënteerde interventies, in vergelijking met andere interventies en TAU, de kans op een recidief verlagen tijdens de eerste 12 maanden van de interventie. |
|
Recidief |
|
|
OR 0.70 |
(4 RCT’s) |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat familie georiënteerde interventies, vergeleken met andere interventies en TAU, op de lange termijn geen verschil laten zien in de kans van het optreden van een recidief. |
a. Er was heterogeniteit in de uitkomsten. b. Gebaseerd op een klein aantal events en 95%BI doorkruist het gebied van geen verschil. c. Studies hadden onduidelijke of verhoogde risk of bias.
|
|
|
|
||||||
|
|
||||||||
|
Tabel 6. Familie georiënteerde interventies vs. andere interventies (excl. TAU) voor schizofrenie |
||||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|||
|
Risico met andere interventies (excl. TAU) |
Risico met Familie georiënteerde interventies |
|||||||
|
Recidief tijdens de 1ste 12 maanden van de interventie |
|
|
OR 1.67 |
(5 RCT’s) |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat wanneer familie georiënteerde interventies vergeleken worden met andere actieve interventies er geen verschil is de kans van het optreden van een recidief tijdens het eerste jaar van de interventie. |
||
a. Er was heterogeniteit tussen de uitkomsten. b. Gebaseerd op een klein aantal events. c. Studies hadden onduidelijke of verhoogde risk of bias.
|
Leucht2009 |
||||||
|
Tabel 8. Atypische antipsychotica versus placebo voor schizofrenie |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met placebo |
Risico met atypische antipsychotica |
|||||
|
Recidief: Amisulpride |
0 per 1.000 |
0 per 1.000 |
RR 0.50 |
246 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Amisulpride vergeleken met placebo de kans op een recidief niet verkleint |
|
Recidief: Aripiprazole |
0 per 1.000 |
0 per 1.000 |
RR 0.59 |
310 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat Aripiprazole in vergelijking met placebo de kans op een recidief verkleint. |
|
Recidief: Olazapine |
0 per 1.000 |
0 per 1.000 |
RR 0.29 |
559 |
⨁⨁⨁◯ |
Het is aannemelijk dat Olazapine in vergelijking met placebo de kans op een recidief verkleint. |
|
Recidief: Ziprasidone |
0 per 1.000 |
0 per 1.000 |
RR 0.57 |
277 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Ziprasidone in vergelijking met placebo de kans op een recidief verkleint. |
|
Recidief: Zotepine |
0 per 1.000 |
0 per 1.000 |
RR 0.18 |
119 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Zotepine in vergelijking met placebo de kans op een recidief verkleint. |
a. klein aantal events en 95% BI doorkruist het gebied van geen verschil b. gerapporteerde funnel plot geeft een indicatie voor publication bias c. gebaseerd op een klein aantal events. d. Studie(s) met verhoogde risk of bias.
|
Leucht2012 |
||||||
|
Tabel 8. Antipsychotica versus placebo voor schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met placebo |
Risico met antipsychotica |
|||||
|
Optreden van recidief |
642 per 1.000 |
257 per 1.000 |
RR 0.40 |
2669 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat het gebruik van antipsychotica vergeleken met placebo resulteert in een grote reductie van de kans op het optreden van een recidief. |
|
Heropnames |
256 per 1.000 |
97 per 1.000 |
RR 0.38 |
2090 |
⨁⨁⨁◯ |
Het is aannemelijk dat het gebruik van antipsychotica vergeleken met placebo resulteert in een grote reductie van de kans op heropnames. |
a. Tussen de studies was er verschil in de definitie van een recidief b. Onduidelijkheid over RoB van geïncludeerde studies.
Kishimoto2013
|
Tabel 10. 2de generatie antipsychotica versus 1ste generatie antipsychotica voor psychotische stoornissen |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Certainty of the evidence |
Opmerkingen |
|
|
Risico met 1ste generatie antipsychotica |
Risico met 2de generatie antipsychotica |
|||||
|
Kans op recidief (afronding studie) - Amisulpride |
270 per 1.000 |
183 per 1.000 |
RR 0.68 |
144 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Amisulpride vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Aripirpazol |
212 per 1.000 |
171 per 1.000 |
RR 0.81 |
633 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Arpiprazole vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Clozapine |
196 per 1.000 |
141 per 1.000 |
RR 0.72 |
355 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Clozapine vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Iloperidone |
535 per 1.000 |
530 per 1.000 |
RR 0.99 |
473 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Iloperidone vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Olanzapine |
327 per 1.000 |
288 per 1.000 |
RR 0.88 |
1140 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Olanzapine vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Quetiapine |
500 per 1.000 |
500 per 1.000 |
RR 1.00 |
68 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Quetiapine vergeleken met een 1ste generatie antipsychoticum niet leidt tot een toe of afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Risperidon |
514 per 1.000 |
386 per 1.000 |
RR 0.75 |
1124 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Risperidone vergeleken met een 1ste generatie antipsychoticum leidt tot een afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Sertindol |
147 per 1.000 |
43 per 1.000 |
RR 0.29 |
203 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat Sertindole vergeleken met een 1ste generatie antipsychoticum leidt tot een afname in de kans van het optreden van een recidief. |
|
Kans op recidief (afronding studie) - Ziprasidone |
500 per 1.000 |
175 per 1.000 |
RR 0.35 |
66 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Ziprasidone vergeleken met een 1ste generatie antipsychoticum leidt tot een afname in de kans van het optreden van een recidief. |
a. Studies hanteren verschillende definities van een recidief, verschillende type controle groepen b. 95% BI doorkruist het gebied van geen verschil en klein aantal events c. klein effect en 95% BI doorkruist het gebied van geen verschil d. 95 % BI doorkruist het gebied van geen verschil e. klein aantal events f. Statistische heterogeniteit tussen studies g. Zeer klein aantal events. h. Geïncludeerde studie(s) hebben een onduidelijke of verhoogde risk of bias.
Mothi2013
|
|
||||||
|
Tabel 11. Pimozide versus Placebo voor Psychotische stoornissen |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met Placebo |
Risico met Pimozide |
|||||
|
Optreden van recidief (3-12 maanden)* |
375 per 1.000 |
83 per 1.000 |
RR 0.22 |
20 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat Pimozide in vergelijking met placebo de kans op een recidief niet verkleint. |
a. bij een selectie van de respondenten werd gestopt met het geven van medicatie of placebo. b. zeer klein aantal events
|
Tabel 12. Pimozide versus andere antipsychotica voor Psychotische stoornissen |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met andere antipsychotica |
Risico met Pimozide |
|||||
|
Optreden van recidief (3- 12 maanden) |
298 per 1.000 |
245 per 1.000 |
RR 0.82 |
227 |
⨁⨁◯◯ |
Er zijn aanwijzingen dat er geen verschil in de kans van het optreden van een recidief is wanneer Pimozide vergeleken wordt met andere antipsychotica. |
a. 95% BI doorkruist gebied van geen verschil en klein aantal events
|
|
||||||
|
Tabel 13. Pimozide + add-on antipsychotica versus antipsychotica voor Psychotische stoornissen |
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met antipsychotica |
Risico met Pimozide + add-on antipsychotica |
|||||
|
Optreden van een recidief (3 – 12 maanden) |
0 per 1.000 |
0 per 1.000 |
RR 0.28 |
(1 RCT) |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat wanneer Pimozide gecombineerd wordt met een ander antipsychoticum dit de kans verkleint op het optreden van een recidief in vergelijking met een behandeling met een enkel antipsychoticum. |
a. gebaseerd op incomplete data b. zeer klein aantal events
|
Højlund2021 |
||||||
|
Tabel 13. Lagere dosering versus standaard dosering voor schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Opmerkingen |
|
|
Risico met standaard dosering |
Risico met lagere dosering |
|||||
|
Opnames: lage dosering vs. standaard dosering |
164 per 1.000 |
180 per 1.000 |
RR 1.10 |
431 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat er geen verschil in de kans van het optreden van een opname is wanneer lage dosering van een antipsychoticum wordt vergeleken met de standaard dosering. |
|
Opnames: zeer lage dosering vs. standaard dosering |
139 per 1.000 |
201 per 1.000 |
RR 1.45 |
743 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat er geen verschil in de kans van het optreden van een opname is wanneer een zeer lage dosering van een antipsychoticum wordt vergeleken met de standaard dosering. |
|
Recidief: lage dosering vs. standaard dosering |
159 per 1.000 |
229 per 1.000 |
RR 1.44 |
1920 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat er grotere kans is op het optreden van een recidief wanneer een lage dosering antipsychoticum wordt vergeleken met de standaard dosering. |
|
Recidief: zeer lage dosering vs. standaard dosering |
165 per 1.000 |
284 per 1.000 |
RR 1.72 |
2058 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat een standaard dosering van een antipsychoticum vergeleken met een zeer lage dosering van hetzelfde middel de kans op een recidief verkleint. |
a. Aanwijzingen voor een verhoogde RoB bij een aantal van de geïncludeerde studies. b. Er is sprake van een klein effect. c. 95%BI doorkruist het gebied van geen verschil. d. 95%BI van geïncludeerde studies liggen aan verschillende kanten van punt van geen verschil. e. Er is statistische heterogeniteit tussen de studie uitkomsten. f. Studies includeren verschillende type medicatie die zowel oraal als intramusculair toegediend worden.
|
Kishimoto2021 |
||||||
|
Tabel 15. Antipsychotica injecties versus orale antipsychotica voor psychotische stoornissen |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met orale antipsychotica |
Risico met antipsychotica injecties |
|||||
|
Heropname/recidief (op laatst gemeten follow-up moment) |
|
|
RR 0.88 |
7833 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat depot medicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de gecombineerde kans op het optreden van een heropname of een recidief verkleint. |
|
Heropname (op laatst gemeten follow-up moment)) |
|
|
RR 0.83 |
4310 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat depot medicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de kans op het optreden van een heropname verkleint. |
|
Recidief (op laatst gemeten follow-up moment)) |
|
|
RR 0.89 |
7407 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat depot medicatie (in de vorm van injecties) ten opzichte van oraal toegediende antipsychotica de kans op het optreden van een recidief niet verkleint. |
a. Klein effect en BI doorkruist het gebied van klinisch geen verschil. b. Geïncludeerde studies hadden op meerdere punten een verhoogde of onduidelijke RoB. c. 95%BI van de afzonderlijke studies liggen aan verschillende kanten van het gebied van geen verschil. d. Het gevonden effect is klein.
|
Ortiz-Orendain2017 |
||||||
|
Tabel 16. Poly-farmaca versus mono-farmaca bij schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met monofarmaca |
Risico met polyfarmaca |
|||||
|
Recidief korte termijn (12 weken) tot lange termijn (>26 weken) bij klassiek antipsychotica + pimozide/perphenazine |
298 per 1.000 |
161 per 1.000 |
RR 0.54 |
442 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat er geen verschil is in de kans van een recidief wanneer een klassiek antipsychoticum geven wordt in combinatie met pimozide/perphenazine in vergelijking met een klassiek antipsychoticum alleen. |
|
Recidief op lange termijn (>26 weken) bij Clozapine + Sulpiride |
559 per 1.000 |
475 per 1.000 |
RR 0.85 |
70 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat er geen verschil is in de kans van een recidief wanneer Clozapine in combinatie geven wordt met Sulpiride in vergelijking met Clozapine alleen.
|
a. Studies hadden verhoogde RoB. b. De heterogeniteit tussen de studies was zeer hoog (> 85%) c. Het 95% BI doorkruist het gebied van geen verschil d. Studie liet verhoogde RoB zien op bijna alle criteria e. klein aantal events en 95% BI doorkruist gebied van geen verschil
|
Matsui2019 |
||||||
|
Tabel 17. Overstappen naar mono-farmaca vs. blijven bij poly-farmaca in schizofrenie |
||||||
|
|
||||||
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Conclusie |
|
|
Risico met blijven bij poly-farmaca |
Risico met overstappen naar mono-farmaca |
|||||
|
Recidief (bij afronding interventie) |
54 per 1.000 |
77 per 1.000 |
RR 1.43 |
123 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat de kans op een recidief niet verhoogd wanneer met van een poly-antipsychotica therapie overstapt naar een mono-antipsychotica regime. |
|
Heropnames (bij afronding interventie) |
89 per 1.000 |
121 per 1.000 |
RR 1.35 |
114 |
⨁◯◯◯ |
Er zijn voorzichtige aanwijzingen dat de kans op heropnames niet verhoogd wanneer met van een poly-antipsychotica therapie overstapt naar een mono-antipsychotica regime. |
a. Studies hadden verhoogd RoB door missen van duidelijke random sequence generation en allocation concealment. b. Geen eenduidigheid tussen uitkomsten tussen de studies c .Gebaseerd op een klein aantal events en breed 95%BI. d .Gebaseerd op 1 RCT met een klein aantal events en effect doorkruist gebied van geen klinisch relevant verschil
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-02-2025
Beoordeeld op geldigheid : 15-11-2024
Het Nederlands Huisartsen Genootschap heeft verklaard geen bezwaar te hebben tegen de richtlijn.
Algemene gegevens
In opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) is er een multidisciplinaire richtlijn Psychosespectrum ontwikkeld. De ontwikkeling van de module werd methodologisch en organisatorisch ondersteund door het Trimbos-instituut.
Doel en doelgroep
De multidisciplinaire richtlijn Psychosespectrum geeft aanbevelingen en handelingsinstructies voor de samenwerking, diagnostiek en behandeling met mensen met een psychose, inclusief mensen met een verhoogd risico op het ontwikkelen van een psychose. De voorliggende richtlijn geeft aanbevelingen voor mensen met terugkerende of chronische psychotische klachten. Deze richtlijn wordt bij uitgave digitaal samengevoegd met de eerder ontwikkelde EBRO module vroege psychose (2018). Samen bieden zij aanbevelingen voor het volledige spectrum van psychotische stoornissen.
De richtlijn geeft aanbevelingen ter ondersteuning van de praktijkvoering van professionals in de GGZ, die betrokken zijn bij de zorgverlening aan deze groepen patiënten. Op basis van de resultaten van wetenschappelijk onderzoek en overige overwegingen geeft de richtlijn een overzicht van goed (‘optimaal’) handelen als waarborg voor kwalitatief hoogwaardige zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek op het gebied van psychotische stoornissen.
De richtlijn beoogt een leidraad te geven voor diagnostiek en behandeling van een psychotische stoornis. Vanuit de multidisciplinaire ontwikkelprocedure poogt de richtlijn een positief effect te hebben op de multidisciplinaire samenwerking in de dagelijkse praktijk. Daarnaast moet de richtlijn gezien worden als een leidende richtlijn, waarvan een vertaling kan plaatsvinden naar de lokale situatie in een instelling of behandelteam. Het opstellen van lokale zorgprogramma’s en andere vormen van werkkaders op basis van deze richtlijn wordt door de werkgroep aangemoedigd, omdat dat voor de implementatie van de in de richtlijn beschreven optimale zorg bevorderlijk is.
Indien de aanbevelingen uit deze richtlijn in de concrete situatie niet aansluiten bij de wensen of behoeften van de patiënt met een psychose, dan moet het mogelijk zijn beredeneerd af te wijken van de richtlijn, tenzij de wensen of behoeften van de patiënt naar de mening van de behandelaar hem/haar kunnen schaden dan wel geen toegevoegde waarde hebben.
Afbakening
Deze richtlijn betreft samenwerking, diagnostiek en behandeling van en met mensen met terugkerende of chronische psychose, waarbij in beginsel sprake is van een niet affectieve psychose (kortdurende psychotische stoornis, schizofreniforme stoornis, psychotische stoornis NAO, waanstoornis, schizofrenie). De diagnostiek en behandeling van mensen met een terugkerende of chronische psychose vindt primair plaats binnen de specialistische GGZ. In de SGGz kan de beschreven zorg ook geboden worden door vrijgevestigde professionals.
Studies over personen vanaf 12 jaar zijn meegenomen. In de richtlijn is gezocht naar oorspronkelijke onderzoeken zonder begindatum tot en met februari 2022. Nog niet gepubliceerde onderzoeken zijn niet meegenomen (wel onderzoeken 'in press'). Zie voor meer informatie over de afbakening van de richtlijn in de bijlagen. Per module is een bijlage opgenomen met toelichting over de gebruikte reviewstrategie (reviewprotocollen per uitgangsvraag).
Samenstelling werkgroep
De Multidisciplinaire richtlijn Psychosespectrum is ontwikkeld door de werkgroep Psychosespectrum, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De werkgroep bestond uit: psychiaters, psychologen, verpleegkundig specialisten, een vaktherapeut en (familie-) ervaringsdeskundigen, welke door de respectievelijke beroepsverenigingen en familie- en patiëntenverenigingen werden afgevaardigd. Voorafgaande aan het ontwikkeltraject werden kennismakingsgesprekken gevoerd met verscheidene kandidaat leden voor de werkgroep. Uit deze groep belangstellenden werden de huidige werkgroepleden geselecteerd. Naast de werkgroep waren enkele adviseurs betrokken, welke delen hebben meegeschreven en die werd gevraagd voorafgaand aan de commentaarfase schriftelijk te reageren op onderdelen van de concepttekst. Deze adviseurs konden tevens worden gevraagd om tijdens een werkgroepbijeenkomst mee te denken over een specifieke uitgangsvraag. De werkgroep werd methodologisch en organisatorisch ondersteund door het technisch team van het Trimbos-instituut. Dit technisch team bestond uit een projectleider, informatiespecialist, literatuur reviewers, een notulist en een projectassistente. Onderstaande schema's geven een overzicht van de samenstelling van de werkgroep, de adviseurs en het ondersteunend technisch team. Alle werkgroepleden rapporteerden bij aanvang hun mogelijke belangenverstrengelingen en aan het begin van elke vergadering werd hen gevraagd of hier wijzigingen in waren opgetreden. Een rapportage hiervan is in te zien via de Nederlandse vereniging voor psychiatrie (NVvP).
Leden Werkgroep
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Dr. Harm Gijsman (voorzitter) |
Dimence |
Psychiater, NVvP |
|
2. |
Mw. Carola van Alphen |
Anoiksis |
Vertegenwoordiger patiëntperspectief, Anoiksis |
|
3. |
Drs. Rob van Alphen
|
Inforsa |
Vaktherapeut, FVB |
|
4. |
Prof Dr. Nynke Boonstra |
NHL Stenden Hogeschool, Kien |
Verpleegkundig specialist, V&VN |
|
5. |
Prof Dr. Wiepke Cahn |
UMC Utrecht |
Psychiater, NVvP |
|
6. |
Prof Dr. Philippe Delespaul
|
Universiteit Maastricht, Mondriaan |
Psycholoog, NIP |
|
7. |
Drs. Frits Dorleijn
|
Ypsilon |
Vertegenwoordiger familieperspectief, Ypsilon |
|
8. |
Dhr. Frank van Es
|
UMC Groningen |
Psychiater, NVvP |
|
9. |
Dr. Mariken de Koning |
Mentrum |
Psychiater, NVvP |
|
10. |
Dhr. Thijs van Oeffelt |
Altrecht |
Psychiater, NVvP |
|
11. |
Prof Dr. Marieke Pijnenborg |
Universiteit van Groningen, GGZ Drenthe |
Psycholoog, NIP |
|
12. |
Dr. Erin Wagenaar
|
Ypsilon |
Vertegenwoordiger familieperspectief, Ypsilon |
|
13. |
Mw. Inge Wagter
|
Anoiksis |
Vertegenwoordiger patiëntperspectief, Anoiksis |
|
14. |
MSc. Geeske van der Weerd
|
BuurtzorgT Groningen
|
Verpleegkundig specialist, V&VN |
Adviseurs en co-auteurs
|
THEMA |
Naam |
Organisatie |
Functie |
Rol in richtlijn |
|
Samenwerking |
Drs. Bart Schut |
UMC Utrecht |
Lid patiënten- adviesgroep |
Adviseur |
|
|
Drs. Ellen Beenen |
UMC Utrecht |
Lid patiënten- adviesgroep |
Adviseur |
|
Diagnostiek |
Dr. Jeanet Nieuwenhuis |
GGNet |
Psychiater |
Adviseur en co-auteur |
|
Psychosociale Interventies |
Dr. Selene Veerman |
GGZ-NHN |
Psychiater |
Adviseur |
Methodologische ondersteuning
|
Naam
|
Ondersteuning |
|
Danielle van Duin |
Projectleider, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Egbert Hartstra |
Reviewer, Trimbos-instituut |
|
Elena Vos |
Reviewer, Trimbos-instituut |
|
Erika Papazoglou |
Reviewer, Trimbos-instituut |
|
Bram Zwanenburg |
Reviewer, Trimbos-instituut |
|
Lex Hulsbosch |
Reviewer, Trimbos-instituut |
|
Beatrix Vogelaar |
Reviewer, Trimbos-instituut |
|
Piet Post |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Chris van der Grinten |
Notulist, namens Trimbos-instituut |
|
Freeke Perdok |
Project assistent, Trimbos-instituut |
|
Isa Reijgersberg |
Project assistent, Trimbos-instituut |
In totaal kwam de werkgroep Psychosespectrum voorafgaand aan de commentaarfase 11 keer bijeen in een periode van 21 maanden (juni 2020 – maart 2022). In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze in evidence tabellen, forest plots, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies. Leden van de werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (beschreven in de sectie “-Overwegingen”) en aanbevelingen. De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren zijn verwerkt in een commentaartabel, die tijdens een werkgroepbijeenkomst is besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen is de definitieve richtlijn aan de opdrachtgever aangeboden.
Belangenverklaringen
Alle werkgroepleden rapporteerden bij aanvang hun mogelijke belangenverstrengelingen en aan het begin van elke vergadering werd hen gevraagd of hier wijzigingen in waren opgetreden. Een rapportage hiervan is in te zien via de Nederlandse vereniging voor psychiatrie (NVvP).
Werkwijze
Uitgangsvragen
De richtlijn is ontwikkeld op geleide van uitgangsvragen, die gebaseerd zijn op knelpunten die worden ervaren rondom samenwerking, diagnostiek en behandeling van en met volwassenen met terugkerende of chronische psychose.
De richtlijn is geen leerboek waarin zoveel mogelijk beschikbare kennis over een onderwerp wordt opgenomen, maar een document met praktische aanbevelingen rondom knelpunten uit de praktijk. Dat betekent dat praktijkproblemen zoveel als mogelijk uitgangspunt zijn van de teksten in de richtlijn. Dat betekent ook dat méér aandacht gegeven wordt aan de wijze waarop die praktijkproblemen worden opgelost, dan aan degene door wie die problemen worden aangepakt of opgelost. De richtlijn is een document waarin staat hoe optimale samenwerking, diagnostiek en behandeling er inhoudelijk uitziet. Indien mogelijk wordt ook beschreven in welke vorm een interventie het beste aangeboden kan worden. Daarnaast worden aanbevelingen gedaan voor de organisatie van zorg. In deze richtlijn worden de hieronder beschreven ‘klinische uitgangsvragen’ behandeld in de verschillende modules.
Uitgangsvragen in de richtlijn Psychosespectrum zijn:
|
THEMA |
Uitgangsvragen |
|
Samenwerking |
|
|
Diagnostiek |
|
|
Psychosociale interventies |
|
|
Preventie van terugval |
|
|
Organisatie van zorg |
|
De richtlijn Psychosespectrum is ontwikkeld volgens de methodiek van de evidence based richtlijnontwikkeling (EBRO).
Zoekstrategie
Om de klinische uitgangsvragen te beantwoorden is door de informatiespecialist, in overleg met de werkgroepleden, op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar bestaande (buitenlandse) evidence-based richtlijnen voor de zorg aan mensen met een vroege psychose, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse, Nederlandse, Franse, en Duitse taalgebieden. Voor het zoeken naar publicaties is gebruik gemaakt van de volgende informatiebronnen:
- Cochrane Database of Systematic Reviews (CDSR)
- Psychological Information Database (PsycINFO)
- PubMed
- Cumulative Index to Nursing and Allied Health Literature (CINAHL)
- Excerpta Medica database (Embase)
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd:
- Geeft het onderwerp van het gevonden onderzoek voldoende antwoord op de uitgangsvraag: worden de binnen GRADE vastgestelde kritische en belangrijke uitkomstmaten in het onderzoek geëvalueerd? (Zie voor meer informatie over GRADE verderop in deze paragraaf);
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn;
- Is er sprake van een meta-analyse, systematic-review, randomised controlled trial (RCT), cohortonderzoek, cross-sectioneel onderzoek, patiëntcontrole onderzoek of wetenschappelijke verantwoord kwalitatief onderzoek? Bij een longitudinaal onderzoek: Is er sprake van een voldoende lange follow-up periode?;
- Zie voor meer informatie over de zoekstrategie de bijlagen per module en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de bijlagen per module.
Beoordeling van de kwaliteit van het bewijs
Studies werden indien mogelijk door twee personen beoordeeld op het risico op bias met behulp van de Cochrane Collaboration Risico van Bias Assessment Tool (Higgins 2008). Elke studie werd gewaardeerd op de wijze van randomisatie en toewijzing; blindering van de deelnemers, beoordelaars, en therapeuten; gehanteerde methode om met uitval van deelnemers om te gaan; en of alle uitkomsten zijn gerapporteerd. Risico op bias kon als hoog (serieuze kans op beïnvloeding van het resultaat), laag (waarschijnlijk geen invloed op het resultaat), of onduidelijk worden beoordeeld.
Voor het bewijs rondom interventies is daarna het bewijs van de onderzoeken per uitkomstmaat gegradeerd met behulp van GRADE[1]. De kwaliteit van het bewijs kent daarbij vier niveaus, te weten; zeer laag, laag, matig en hoog. In deze richtlijn is gekozen om de GRADE niveaus weer te geven met behulp van de volgende neutrale en internationaal toepasbare weergave:
|
Hoog |
⊕⊕⊕⊕ |
|
Matig |
⊕⊕⊕⚪ |
|
Laag |
⊕⊕⚪⚪ |
|
Zeer laag |
⊕⚪⚪⚪ |
[1] GRADE: Grading of Recommendations Assessment, Development and Evaluation
Het studiedesign bepaalt de uitgangspositie van de kwaliteit van bewijs. Gerandomiseerde, gecontroleerde studies (RCT's) hebben over het algemeen meer bewijskracht dan observationele studies. Daarom is hun uitgangspositie hoog, terwijl de uitgangspositie van observationele studies laag is. De kwaliteit van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 2.1). GRADE is niet toegepast bij vragen rondom screening en diagnostiek. De reden hiervoor is dat GRADE momenteel nog vooral geschikt is voor onderzoeken rond diagnostische accuratesse. Voor deze onderwerpen is de kwaliteit van de studies beoordeeld met behulp van het QUADAS-2 instrument.
Tabel 2.1: GRADE: Factoren voor downgraden en upgraden
Het niveau van de kwaliteit van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandeling.
[2] Het blinderen van deelnemers en therapeuten is in deze richtlijn niet meegenomen in de beoordeling van studies rond psychosociale niterventies, omdat blinderen van de deelnemers en therapeuten niet goed mogelijk is bij deze interventies.
Samenvatten van resultaten in ‘evidence tabel’ en ‘forest plot’
Van elk artikel is een samenvatting gemaakt in een zogenaamde 'evidence tabel', waarin de belangrijkste kenmerken van individuele onderzoeken zijn opgenomen (bij een RCT zijn dat bijvoorbeeld het doel van het onderzoek, het onderzoeksdesign, patiëntkenmerken, interventies, uitkomstmaten en de resultaten). Bij de uitgangsvragen over interventies is voor elke kritische uitkomstmaat een meta-analyse uitgevoerd, om de omvang van het klinisch effect van de interventie samen te vatten. De data uit oorspronkelijke onderzoeken worden hiervoor verwerkt in een forest plot, welke een grafische weergave van de meta-analyse geeft (zie tabel 2.2 voor een voorbeeld van een forest plot).
Tabel 2.2: Voorbeeld van een forest plot met toelichting

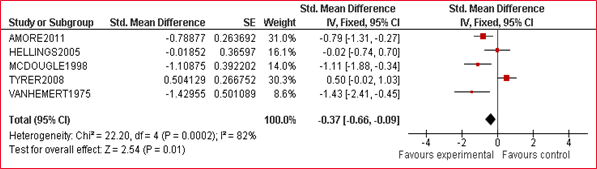
Wanneer er onvoldoende data beschikbaar waren om een meta-analyse uit te voeren, stelden de reviewers in enkele gevallen een narratieve (beschrijvende) review van het beschikbare bewijs op (zonder ‘gepoolde’ resultaten en berekening van mate van heterogeniteit, maar met een beschrijving van de kwaliteit). De kwaliteitsbeoordeling en een samenvattende beschrijving van de verschillende onderzoeken welke zijn geselecteerd vanuit de systematische literatuur search worden voor elke uitgangsvraag beschreven onder het kopje ‘wetenschappelijke onderbouwing’.
Conclusies
De formulering van de conclusies, gebaseerd op de studies uit de systematische literatuur search, is afgestemd op het GRADE niveau (zie tabel 2.3). Deze formulering sluit ook aan bij de ‘levels of evidence’ welke indeling (niveau 1 t/m 4) voorheen werd gebruikt in onder andere de multidisciplinaire richtlijn Schizofrenie.
Tabel 2.3 Formulering conclusies n.a.v. GRADE niveau
|
GRADE |
Levels of evidence |
Formulering conclusies |
|
⊕⊕⊕⊕ |
Niveau 1 |
“Het is aangetoond dat…” |
|
⊕⊕⊕⚪ |
Niveau 2 |
“Het is aannemelijk dat…” |
|
⊕⊕⚪⚪ |
Niveau 3 |
“Er zijn aanwijzingen dat…” |
|
⊕⚪⚪⚪ |
Niveau 4 |
“Er zijn voorzichtige aanwijzingen dat…” |
Overwegingen
Naast de wetenschappelijke onderbouwing, waarin vanuit de systematische literatuursearch de conclusies zijn getrokken op basis van het best beschikbare bewijs, is voor elke uitgangsvraag expert kennis verzameld. Hiervoor hebben de leden van de werkgroep gebruik gemaakt van een GRADE checklist ‘Van bewijs naar aanbeveling’, waarmee systematisch wordt nagegaan of er relevante overwegingen zijn voor een aantal vooraf bepaalde factoren, waaronder: balans tussen gewenste en ongewenste effecten, patiëntenperspectief, middelenbeslag en maatschappelijk perspectief. De vertegenwoordigers vanuit patiëntenperspectief en naastenperspectief hebben zoveel mogelijk geprobeerd hun overwegingen vanuit een gezamenlijk perspectief te formuleren, welke is beschreven onder het vaste kopje patiëntenperspectief. Wanneer deze perspectieven uit elkaar liepen is er een apart kopje naastbetrokkenenperspectief toegevoegd in het format van de richtlijntekst. De overwegingen werden onderbouwd vanuit ‘grijze literatuur’ (studies, rapporten en andere teksten die niet vanuit de systematische literatuursearch en -selectie zijn verwerkt in de wetenschappelijke conclusies). De aanbevelingen werden gebaseerd op de combinatie van de wetenschappelijke conclusies en de overwegingen.
Aanbevelingen
Aanbevelingen kunnen gegradeerd worden als ‘sterk’ (onvoorwaardelijk) of ‘zwak’ (voorwaardelijk). Wanneer de kwaliteit van het bewijs voor de positieve en negatieve effecten van een interventie hoog is, kan dit leiden tot een sterke aanbeveling, en omgekeerd, wanneer de bewijskracht laag tot zeer laag is, kan dit een zwakke aanbeveling opleveren (zie tabel 2.4 voor de indeling van sterke en zwakke aanbevelingen). Een zwakke aanbeveling geeft meer ruimte om af te wijken en aandacht te schenken aan alternatieven die passen bij de behoeften van de patiënt, terwijl bij een sterke aanbeveling die ruimte beperkt is. Echter, de kracht van het wetenschappelijke bewijs is niet de enige factor die de sterkte van de aanbevelingen bepaalt. De aanbevelingen zijn gebaseerd op wetenschappelijk bewijs enerzijds, en overige overwegingen, zoals praktijkervaringen van de werkgroepleden, ervaringen en voorkeuren van patiënten met een vroege psychose en familie, kosten, beschikbaarheid en organisatorische aspecten, anderzijds. Deze laatste zijn opgenomen onder het kopje ‘Overwegingen’.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is zoveel mogelijk de volgende indeling aangehouden (zie tabel 2.4):
Tabel 2.4 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Sterkte van aanbeveling
|
Positieve aanbeveling |
Negatieve aanbeveling |
|
Sterk (1)
|
“Dienen, horen, is eerste keuze, is aanbevolen, heeft de voorkeur, is standaard, is vereist” |
“Dient niet, niet aan te bevelen, wordt ontraden, verdient geen aanbeveling” |
|
Zwak (2)
|
“Te overwegen, is een optie, kan, kan zinvol zijn, er is mogelijk plaats, de werkgroep adviseert” |
“Is wellicht geen plaats voor, lijkt niet zinvol, is terughoudendheid geboden, de werkgroep adviseert geen” |
Gevers, J.K.M., & Aalst, A. van (1998). De rechter en het medisch handelen (3e druk). Deventer: Kluwer.
Higgins, J.P.T., Green, S., & Cochrane Collaboration (2008). Cochrane handbook for systematic Reviews of interventions. Chichester, England/Hoboken, NJ: Wiley-Blackwell.
Zoekverantwoording
Zoekstrategie Terugval preventie - vraag 1
Database: Ovid MEDLINE(R) ALL <1946 to December 15, 2020>
Search Strategy:
1 exp Psychotic Disorders/ (52726)
2 exp Psychotic Disorders/dt, rh, th (17363)
3 exp *Psychotic Disorders/dt, rh, th (10432)
4 guideline?.ti,kw. (83418)
5 exp guideline/ or practice guideline/ (35143)
6 3 and (4 or 5) (66)
7 recidi*.ti. (1424)
8 2 and 7 (14)
9 Recurrence/ (185615)
10 (recrudesc* or recurren* or relaps*).tw,kw. (732563)
11 9 or 10 (799088)=recurrence
12 2 and 11 (1019)
13 3 and 12 (654)
14 "filter SR".ti. (0)
15 meta analysis.pt. (123930)
16 (meta-anal$ or metaanal$).tw,kf. (191225)
17 (quantitativ$ adj10 (review$ or overview$)).tw. (9970)
18 (systematic$ adj10 (review$ or overview$)).tw. (211124)
19 (methodologic$ adj10 (review$ or overview$)).tw. (12542)
20 (quantitativ$ adj10 (review$ or overview$)).kf. (80)
21 (systematic$ adj10 (review$ or overview$)).kf. (22619)
22 (methodologic$ adj10 (review$ or overview$)).kf. (81)
23 medline.tw. and review.pt. (81127)
24 (pooled adj3 analy*).tw. (21310)
25 (pooled adj3 analy*).kf. (292)
26 "cochrane$".fc_jour. (15167)
27 or/15-26 (383255)=SR filter
28 "einde SR filter".ti. (0)
29 12 and 27 (95)
30 exp Antipsychotic Agents/ (124531)
31 exp Psychotherapy/ (198492)
32 (psychological adj2 treatment?).ti,kw. (1086)
33 Cognitive Behavioral Therapy/ (26039)
34 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (18533)
35 or/30-34 (326169)
36 1 and 35 (12643)
37 2 or 36 (19931)
38 27 and 37 (659)
39 11 and 38 (103)
40 (dutch or english or german).la. (28169466)
41 39 and 40 (95)
42 antipsychot*.ti,kw. (16194)
43 3 or 42 (25376)
44 43 and (4 or 5) and 40 (170)
45 guideline.pt. (16335)
46 44 and 45 (12)
47 (1 or 42) and 40 and 45 (18)= richtlijnen Psychose
48 from 46 keep 1-12 (12)
49 from 47 keep 1-18 (18)
50 "prognose filter".ti. (0)
51 incidence/ (268719)
52 exp Mortality/ (390485)
53 Follow-Up Studies/ (652936)
54 (prognos* or predict* or course*).tw,kw. (2661153)
55 (cohort or (first adj8 episode?)).ti,ab,kw. (591728)
56 51 or 52 or 53 or 54 or 55 (3931474)
57 27 and 40 and 43 and 56 (368)
58 11 and 57 (57)
59 27 and (42 or 1) and 40 and 56 (685)=SR +psychose + talen + prognose in beloop
60 11 and 59 (90)= )=SR +psychose + talen + prognose in beloop + recurrence= vraag 1
Medline search van 21 12 2020
Database: Ovid MEDLINE(R) ALL <1946 to December 18, 2020>
Search Strategy:
1 exp Psychotic Disorders/ (52707)= deel1 van P
2 exp Psychotic Disorders/dt, rh, th (17363)
3 exp *Psychotic Disorders/dt, rh, th (10432)
4 guideline?.ti,kw. (83403)
5 exp guideline/ or practice guideline/ (35127)
6 3 and (4 or 5) (65)
7 recidi*.ti. (1421)
8 2 and 7 (14)
9 Recurrence/ (185537)
10 (recrudesc* or recurren* or relaps*).tw,kw. (732403)
11 9 or 10 (798908)=recurrence
12 2 and 11 (1019)
13 3 and 12 (654)
14 "filter SR".ti. (0)
15 meta analysis.pt. (123779)
16 (meta-anal$ or metaanal$).tw,kf. (191084)
17 (quantitativ$ adj10 (review$ or overview$)).tw. (9950)
18 (systematic$ adj10 (review$ or overview$)).tw. (210939)
19 (methodologic$ adj10 (review$ or overview$)).tw. (12543)
20 (quantitativ$ adj10 (review$ or overview$)).kf. (80)
21 (systematic$ adj10 (review$ or overview$)).kf. (22571)
22 (methodologic$ adj10 (review$ or overview$)).kf. (81)
23 medline.tw. and review.pt. (81076)
24 (pooled adj3 analy*).tw. (21298)
25 (pooled adj3 analy*).kf. (290)
26 "cochrane$".fc_jour. (15175)
27 or/15-26 (383012)=SR
28 "einde SR filter".ti. (0)
29 12 and 27 (95)
30 exp Antipsychotic Agents/ (124503)
31 exp Psychotherapy/ (198423)
32 (psychological adj2 treatment?).ti,kw. (1085)
33 Cognitive Behavioral Therapy/ (26035)
34 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (18530)
35 or/30-34 (326070)= behandeling
36 1 and 35 (12641)
37 2 or 36 (19929)
38 27 and 37 (659)
39 11 and 38 (103)
40 (dutch or english or german).la. (28164929)=talen
41 39 and 40 (95)
42 antipsychot*.ti,kw. (16190)
43 3 or 42 (25373)
44 43 and (4 or 5) and 40 (167)
45 guideline.pt. (16339)
46 44 and 45 (12)
47 (1 or 42) and 40 and 45 (18)
48 "Psychosis relapse during treatment with long-acting injectable antipsychotics in individuals with schizophrenia-spectrum disorders: an individual participant data meta-analysis".fc_titl. (1)
49 "Long-acting injectable antipsychotics for the prevention of relapse in patiënts with recent-onset psychotic disorders".fc_titl. (1)
50 48 or 49 (2)
51 "Evidence-based guidelines for the pharmacological treatment of schizophrenia: Updated recommendations from the British Association for Psychopharmacology".fc_titl. (1)
52 "Comparative effects of 18 antipsychotics on metabolic function in patiënts with schizophrenia, predictors of metabolic dysregulation, and association with psychopathology: a systematic review and network meta-analysis".fc_titl. (1)
53 Secondary Prevention/ (20791)
54 "Delayed-Action Preparations"/ (37384)
55 (psychos?s or (psychotic adj2 disorder?) or (reactive adj2 psychos?s) or (schizoaffective adj2 disorder?) or (schizophreniform adj2 disorder?)).tw,kw. (57066)= deel2 van P
56 exp *Psychotic Disorders/ (41160)=deel 1 van P focus
57 (psychos?s or (psychotic adj2 disorder?) or (reactive adj2 psychos?s) or (schizoaffective adj2 disorder?) or (schizophreniform adj2 disorder?)).ti,kw. (30959)= deel2 van P focus
58 56 or 57 (51147)= p focus
59 ((relapse adj2 prevention?) or (secondary adj2 prevention?) or (early adj2 therap*)).tw,kw. (38920)
60 11 or 53 or 59 (836087)
61 58 and 60 (2157)
62 27 and 40 and 61 (138)
63 48 or 49 (2)
64 antipsychotic*.tw,kw. (40899)
65 antipsychotic*.ti,kw. (16180)
66 exp *Antipsychotic Agents/ (76842)
67 58 or 65 or 66 (125693)
68 "P psychosis focus".ti. (0)
69 27 and 40 and 60 and 67 (422)
70 58 and 69 (138)
71 35 or 42 (329573)
72 70 and (71 or 35) (81)
73 "rct filter medline".ti. (0)
74 controlled-clinical-trial.pt. (93971)
75 randomized-controlled-trial.pt. (519221)
76 randomized controlled trial/ (519221)
77 randomi?ed controlled trial?.tw. (188040)
78 randomi?ed controlled trial?.kf. (12293)
79 random-allocation.tw,kf. (1766)
80 double-blind-method.tw,kf. (501)
81 single-blind-method.tw,kf. (90)
82 (random adj8 (selection? or sample?)).kf,tw. (46682)
83 random*.tw,kf. (1186779)
84 or/74-83 (1397332)
85 "rct filter".ti. (1)
86 67 and 60 and (35 or 65 or 66) and 40 and 27 (365)
87 67 and 60 and (35 or 65 or 66) and 40 and 84 (868)
88 from 87 keep 1 (1)
89 exp Comparative Study/ (1878182)
90 compar*.ti. (657057)
91 89 or 90 (2141068)
92 meta-analysis/ or "systematic review"/ (205684)
93 (meta?analys* or (overview adj2 clinical adj2 trials) or (network adj2 analys*)).ti. (9409)
94 91 or 92 or 93 (2336534)
95 86 and 94 (239)
96 ((relapse adj2 prevention?) or (secondary adj2 prevention?) or (early adj2 therap*)).ti,kw. (8649)
97 *Secondary Prevention/ (3684)
98 *Recurrence/ (2132)
99 (recrudesc* or recurren* or relaps*).ti,kw. (171765)
100 96 or 97 or 98 or 99 (181394)
101 67 and 60 and (35 or 65 or 66) and 40 and 27 and 100 (49)
102 exp *Psychotic Disorders/pc (350)
103 57 and pc.fs. (678)
104 102 or 103 (803)
105 102 and (35 or 65 or 66) and 40 and 27 and 60 (3)
106 104 and (35 or 65 or 66) and 40 and 27 (20)
107 101 or 106 (67)
108 (network adj2 analys*).ti,ab. (25511)
109 86 and 108 (7)
110 107 or 109 (73)
111 (67 and 60 and (35 or 65 or 66) and 40 and 84 and 100) not 27 (161)
112 1 or 55 (81692)
113 112 and 11 and 58 and 35 and 40 (635)
114 112 and 11 and 58 and 35 and 40 and 27 (73)
115 112 and 11 and 35 and 40 and 27 (150)= SR
116 115 not 114 (77)
117 (112 and 11 and 35 and 40 and 84) not 27 (192)=rct
Embase guidelines
Database: Embase <1974 to 2020 December 17>
Search Strategy:
1 psychosis/ (89761)
2 psychosis/pc (600)
3 practice guideline/ (440607)
4 guideline.ti. (21311)
5 3 or 4 (446083)
6 *psychosis/ (43554)
7 5 and 6 (611)
8 3 and 6 (603)
9 psychosis/dm (712)
10 5 and 9 (51)
11 6 and 10 (30)= guidelines
Embase vr 3 en 4 SR en rct
Database: Embase <1974 to 2020 December 18>
Search Strategy:
1 "psychose searches".ti. (0)
2 "Long-acting injectable antipsychotics for the prevention of relapse in patiënts with recent-onset psychotic disorders: A systematic review and meta-analysis of randomized controlled trials".fc_titl. (1)
3 "Psychosis relapse during treatment with long-acting injectable antipsychotics in individuals with schizophrenia-spectrum disorders: an individual participant data meta-analysis".fc_titl. (1)
4 "prognose filter".ti. (0)
5 prognosis/ or probability/ or proportional hazards models/ or uncertainty/ or likelihood functions/ or logistic models/ or proportional hazards models/ (941620)
6 ((risk adj prediction) or (predictor adj variabl??) or (increas* adj risk)).tw. (403548)
7 ((risk adj assessement?) or (predict* adj risk?) or (risk adj factor?) or (validat* or predict* or rule*)).tw. (3707130)
8 ((predict* and (outcome* or risk* or model*)) or ((history or variable* or criteria or scor* or characteristic* or finding* or factor*) and (predict* or model* or decision* or identi* or prognos*)) or (decision* and (model* or clinical* or (logistic adj3 models)))).tw. (5168801)
9 or/5-8 (7234241)
10 2 or 3 (2)
11 from 10 keep 1-2 (2)
12 psychosis/ (89814)
13 recurrent disease/ (182726)
14 (recrudesc* or recurren* or relaps*).tw,kw. (1120307)
15 (cessation* or withdraw* or discontinu* or halt* or stop* or drop adj1out* or dropout* or drop?out or rehospitalis* or relaps* or maintain* or maintenance* or recur*).tw,kw. (2841919)
16 secondary prevention/ (29108)
17 psychosis/pc (600)
18 12 and (16 or 13 or 15) (11540)
19 ((psychos* or schizophr* or schizoaff*) adj2 (cessation* or withdraw* or discontinu* or halt* or stop* or drop adj1out* or dropout* or drop?out or rehospitalis* or relaps* or maintain* or maintenance* or recur*)).tw,kw. (2386)
20 18 or 19 (13285)= P + relapse
21 "filter SR".ti. (0)
22 meta analysis/ (203709)
23 (meta-anal$ or metaanal$).tw,kw. (250705)
24 (quantitativ$ adj10 (review$ or overview$)).tw. (11994)
25 (systematic$ adj10 (review$ or overview$)).tw. (263440)
26 (methodologic$ adj10 (review$ or overview$)).tw. (14671)
27 (quantitativ$ adj10 (review$ or overview$)).kw. (147)
28 (systematic$ adj10 (review$ or overview$)).kw. (33150)
29 (methodologic$ adj10 (review$ or overview$)).kw. (86)
30 medline.tw. and review.pt. (77042)
31 (pooled adj3 analy*).tw. (32527)
32 (pooled adj3 analy*).kw. (548)
33 "cochrane$".fc_jour. (20949)
34 or/22-33 (504885)=SR
35 "einde SR filter".ti. (0)
36 20 and 34 (809)
37 ((psychos* or schizophr*) adj2 (cessation* or withdraw* or discontinu* or halt* or stop* or drop adj1out* or dropout* or drop?out or rehospitalis* or relaps* or maintain* or maintenance* or recur*)).tw,kw. (2364)
38 18 or 37 (13271)=P
39 34 and 38 (809)=P + SR
40 patiënt care/ or case management/ or patiënt care planning/ (338281)
41 psychosis/dm (715)
42 medication compliance/ (33742)
43 (adherence adj2 therap*).tw,kw. (7315)
44 exp neuroleptic agent/dt [Drug Therapy] (96631)
45 exp psychotherapy/ (256080)
46 exp cognitive behavioral therapy/ (14761)
47 (psychological adj2 treatment?).ti,kw. (1780)
48 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (28540)
49 long acting drug/ (6462)
50 exp *psychotherapy/ (122720)
51 40 or 41 or 42 or 43 or 44 or 46 or 47 or 48 or 49 or 50 (611280)= alle typen behandeling
52 39 and 51 (341)
53 (dutch or english or german).la. (31506409)
54 52 and 53 (326)
55 *psychosis/ (43568)= P focus
56 ((psychos* or schizophr* or schizoaff*) adj2 (cessation* or withdraw* or discontinu* or halt* or stop* or drop adj1out* or dropout* or drop?out or rehospitalis* or relaps* or maintain* or maintenance* or recur*)).ti,kw. (668)= P focus
57 54 and (55 or 56) (147)
58 from 57 keep 1-147 (147)
59 random$.mp. (1839747)
60 factorial$.mp. (66252)
61 (crossover$ or cross-over$).mp. (122148)
62 (crossover$ or cross-over$).mp. (122148)
63 placebo$.mp. or PLACEBO/ (466267)
64 (doubl$ adj blind$).mp. (264947)
65 (singl$ adj blind$).mp. (52667)
66 (assign$ or allocat$).mp. (579452)
67 volunteer$.mp. or VOLUNTEER/ (273497)
68 Crossover Procedure/ (65450)
69 Randomized Controlled Trial/ (636178)
70 Double Blind Procedure/ (179422)
71 Single Blind Procedure/ (41243)
72 or/59-71 (2698091)
73 ((55 or 56) and 53 and 51 and 38 and 72) not 34 (340)
74 limit 73 to article (238)
75 (55 or 56) and 34 and 9 and 20 (162)
76 from 74 keep 1-238 (238)
77 from 75 keep 1-162 (162)
78 20 and (55 or 56) and 53 and 51 and 34 (147)=SR
79 (20 and (55 or 56) and 53 and 51 and 72) not 34 (340)= rct
Psycinfo
Database: APA PsycInfo <1806 to December Week 2 2020>
Search Strategy:
1 "psychose preventie recidives".ti. (0)
2 psychosis/ or schizophrenia/ (109126)
3 psychosis/ (28277)
4 (psychos?s or (psychotic adj2 disorder?) or (reactive adj2 psychos?s) or (schizoaffective adj2 disorder?) or (schizophreniform adj2 disorder?)).tw,id. (66150)
5 3 or 4 (70321)
6 "relapse (disorders)"/ or relapse prevention/ (9424)
7 ((relapse adj2 prevention?) or (secondary adj2 prevention?) or (early adj2 therap*)).tw,id. (9261)
8 (recrudesc* or recurren* or relaps*).tw,id. (56952)
9 ((psychos* or schizophr* or schizoaff*) adj2 (cessation* or withdraw* or discontinu* or halt* or stop* or drop adj1out* or dropout* or drop?out or rehospitalis* or relaps* or maintain* or maintenance* or recur*)).tw,id. (1952)
10 or/6-9 (62012)
11 5 and 10 (3252)
12 exp neuroleptic drugs/ (31577)
13 exp psychotherapy/ (205073)
14 exp cognitive behavior therapy/ (22313)
15 (psychological adj2 treatment?).ti,id. (2986)
16 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,id. (28909)
17 treatment compliance/ or disease management/ or treatment dropouts/ or treatment refusal/ (25386)
18 (adherence adj2 therap*).tw,id. (1294)
19 or/12-18 (285822)=behandeling
20 11 and 19 (964)
21 (dutch or english or german).la. (4612614)=talen
22 "psycinfo rct filters sensitief".ti. (0)
23 randomi?ed controlled trial*.tw. (33502)
24 controlled clinical trial*.tw. (3174)
25 random allocation.tw. (265)
26 double blind method*.tw. (91)
27 double blind stud*.tw. (2575)
28 single blind stud*.tw. (150)
29 or/23-28 (39222)=rct
30 "Meta Analysis".md. (23393)
31 "systematic review".md. (27894)
32 "systematic review"/ or meta analysis/ (5295)
33 "filter systematic reviews psycinfo".ti. (0)
34 (meta-anal* or metaanal*).tw. (39954)
35 (quantitativ* adj5 (review* or overview*)).tw. (2597)
36 (systematic* adj5 (review* or overview*)).tw. (37824)
37 (methodolo* adj5 (review* or overview*)).tw. (7046)
38 (medline or cochrane).tw. (18111)
39 (review* or overview*).ti. (167733)
40 (literature adj5 review).tw. (80627)
41 (synthes* adj3 (literature* or research or studies or data)).tw. (9437)
42 (pooled adj5 analys*).tw. (2423)
43 (data adj2 pool*).tw. (2402)
44 (medline or medlars or embase or cinahl or scisearch or psycinfo or psyclit or psychlit).ti. (76)
45 ((hand or manual* or database* or computer* or electronic*) adj2 search*).tw. (11785)
46 or/34-45 (273271)
47 30 or 31 or 32 or 46 (275720)= SR
48 "nw SR filter psycinfo".ti. (0)
49 5 and 10 and 21 and 19 and 47 (111)
50 49 (111)
51 limit 50 to all journals (106)
52 (5 and 10 and 21 and 19 and 29) not 47 (53)
53 52 (53)
54 limit 53 to all journals (51)
55 "Long-acting injectable antipsychotics for the prevention of relapse in patiënts with recent-onset psychotic disorders: A systematic review and meta-analysis of randomized controlled trials".fc_titl. (1)
56 "psychosis relapse".fc_titl. (5)
57 55 or 56 (6)
58 relapse prevention/ or exp maintenance therapy/ or "relapse (disorders)"/ (13979)
59 from 51 keep 1-106 (106)
60 from 54 keep 1-51 (51)
61 from 57 keep 1-6 (6)
62 symptom remission/ or exp "remission (disorders)"/ (3785)
63 10 or 62 (64805)= recurrency breed
64 2 and 63 (5502)= P breed voor psychose remissie
65 maintenance therapy/ or exp treatment/ (1073419)
66 19 or 65 (1082779)= behandeling breed
67 64 and 66 and 63 and 21 and 47 (367)
68 *maintenance therapy/ or exp *treatment/ (945367)
69 64 and (68 or 19) and 63 and 21 and 47 (354)
70 69 (354)
71 limit 70 to all journals (339)
72 exp treatment outcomes/ (124962)
73 (treatment adj2 outcome?).tw,id. (28996)
74 72 or 73 (137553)
75 71 and 74 (124)= SR met outcome
76 (64 and (68 or 19) and 63 and 21 and 29) not 47 (178)=rct
77 "prognose filter".ti. (0)
78 prognosis/ or "clinical judgment (not diagnosis)"/ or exp clinical models/ or exp disease course/ or exp prediction/ (54491)
79 statistical estimation/ or exp estimation/ or "predictability (measurement)"/ (17093)
80 risk assessment/ or risk factors/ or exp risk management/ (102435)
81 ((risk adj prediction) or (predictor adj variabl??) or (increas* adj risk)).tw,id. (41318)
82 limit 81 to all journals (34140)
83 ((risk adj assessment?) or (predict* adj risk?) or (risk adj factor?) or (validat* or predict* or rule*)).tw,id. (697996)
84 ((predict* and (outcome* or risk* or model*)) or ((history or variable* or criteria or scor* or characteristic* or finding* or factor*) and (predict* or model* or decision* or identi* or prognos*)) or (decision* and (model* or clinical* or (logistic adj3 models)))).tw,id. (1042739)
85 or/78-84 (1350233)
86 64 and 85 and 63 and 21 and 47 (216)
87 risk.ti,ab,id. (371800)
88 86 and 87 (83)= vr1 risk prognose
89 treatment guidelines/ (7318)
90 guideline?.ti,id. (14448)
91 89 or 90 (16938)
92 91 and 5 and 10 and 21 (34)
93 prospective study.md. (44158)
94 guideline?.ti. (7809)
95 89 or 94 (12485)
96 95 and 5 and 10 and 21 (29)
97 96 (29)
98 limit 97 to all journals (25)
99 from 96 keep 1-29 (29)
100 from 98 keep 1-25 (25) richtlijnen
