Interne fixatie van pertrochantere fracturen
Uitgangsvraag
Beschrijf de optimale augmentatie en techniek van repositie bij interne fixatie van pertrochantere fracturen 31-A.1, -A.2, -A.3?
Subuitgangsvragen
- Leidt een valgusrepositie of een anatomische repositie bij interne fixatie van trochantere fracturen tot betere uitkomsten?
- Leidt cementaugmentatie bij interne fixatie van trochantere fracturen tot betere uitkomsten dan interne fixatie zonder augmentatie?
Aanbeveling
Reponeer de pertrochantere fractuur volgens de specifieke criteria in deze module, in een anatomische of valgusstand. Open repositie is nodig indien gesloten repositie niet leidt tot een bevredigend resultaat.
Fixeer de pertrochantere fractuur onder doorlichting volgens de specifieke criteria in de module. Bedenk dat bij suboptimale distale vergrendeling van een intramedullaire pen een verhoogde kans bestaat op het ontstaan van een postoperatieve fractuur van de femurschacht ter plaatse van de grendelschroef.
Cementaugmentatie van de collumschroef is toegestaan bij de fixatie van trochantere fracturen, maar meer onderzoek is nodig om eventuele meerwaarde aan te tonen.
Researchaanbeveling
Verricht onderzoek naar de klinische effecten van cementaugmentatie bij de fixatie van de collumschroef bij pertrochantere fracturen.
Overwegingen
Gesloten repositie van trochantere femurfracturen met behulp van een tractietafel heeft de voorkeur en is de meest aangewezen techniek. In geval een gesloten repositie als onvoldoende wordt beoordeeld, dient overgegaan te worden tot een open repositie alvorens met de feitelijke fixatie wordt aangevangen.
Het verdient aanbeveling de volgende criteria aan te houden voor optimale repositie (figuur 3):
- AP opname: Caput-collum-diaphyse (CCD)-hoek van het proximale femur dient tenminste 130° te bedragen, hetgeen gemiddeld met een anatomische repositie overeenkomt. Repositie in meer valgus is toegestaan indien de omstandigheden daarom vragen, maar heeft weinig meerwaarde. Een röntgenopname van de contralaterale zijde draagt bij aan het bepalen van de juiste CCD hoek. Voorkom repositie in varus!
- Laterale opname: Er dient een goed alignement te zijn tussen de as van de femurschacht en de as van het collum femoris. Er dient meer dan 50% contactoppervlak te zijn tussen de hoofdfragmenten van de fractuur: caput-collum proximaal en femurdiaphyse distaal.
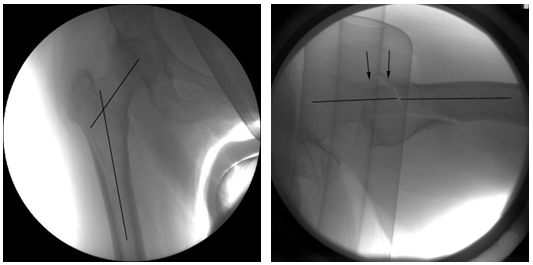
Figuur 3 AP en axiale röntgenopname van een trochantere fractuur na onbloedige repositie.
Trochantere fractuur type 31 A2, optimale reductiecriteria bereikt:
Foto links: AP Caput Collum Diaphyse (CCD) hoek > 130˚
Foto rechts: Axiaal, goed axiaal alignement en voldoende (vrijwel 100%) contact fractuurdelen in dorsoventrale richting
Bij een GHS wordt via een laterale benadering achter de musculus vastus lateralis langs de laterale cortex van de femurschacht vrijgeprepareerd. Via deze benadering is tevens een eventuele open repositie van een gedislokeerde fractuur mogelijk. Als eerste wordt de glijdende heupschroef gecanuleerd over een voerdraad ingebracht. Optimale positionering van de schroef is op de AP projectie in het centrum of de caudale helft van de kop, met een afstand van vijf tot tien mm van de tip van de schroef tot de rand van de femurkop (Tip-Apex Distance, subchondrale bot biedt optimaal houvast). Bij axiale projectie dient de schroef in het centrum van de hals en kop te liggen, dan wel in de dorsale helft (zie figuur 4). Na positionering van de heupschroef kan de plaat aan de femurschacht bevestigd worden. De operatietechniek is relatief eenvoudig en veilig.
Hoewel de positie van de collumschroef bij een pertrochantere fractuur minder kritisch is dan bij de collum femoris fractuur, gaat de voorkeur van de werkgroep uit naar een mid-midpositie in de femurkop tot één cm onder het gewrichtsoppervlak. Indien twijfel bestaat over de mate van fixatie van de collumschroef in de femurkop is augmentatie een optie.
De werkgroep is van mening dat het aanbrengen van compressie op de fractuur door de operateur na het inbrengen van het implantaat – en na het beëindigen van tractie – essentieel is. Gebruik van een compressieschroef daartoe is optioneel.
Voor een stabiele 31-A.1 pertrochantere fractuur die wordt behandeld met een sliding hip screw systeem, biedt een 2-gats GHS plaat voldoende stabiliteit. Voor een instabiele 31-A.2 of 31-A.3 fractuur is fixatie met vier bicorticale schroeven in de GHS plaat noodzakelijk.
Gegeven de verhoogde incidentie van fracturen rondom het implantaat na intramedullaire fixatie, gaat in geval van twijfel de voorkeur uit naar lange pensystemen.
Patiënten met een pertrochantere fractuur moeten in opzet snel belast gaan mobiliseren. Alle hedendaagse implantaten laten directe belasting na fixatie toe.
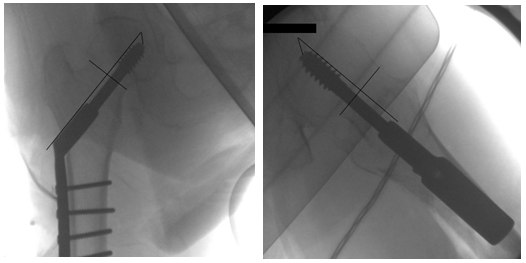
Figuur 4 AP en axiale röntgenopname van een 31A1 fractuur met GHS fixatie.
Foto links: Trochantere fractuur AP, stabilisatie met GHS 135˚ gepositioneerd in het centrale dan wel caudale deel van de femurkop, afstand tot de rand van de kop (centrale deel) < 10 mm.
Foto rechts: Trochantere fractuur axiale opname, GHS gepositioneerd in het centrale dan wel het dorsale deel van de femurkop, afstand tot de rand van de kop (centrale deel) < 10 mm
Bij een IM osteosynthese wordt na optimale repositie een percutane insertiemethode toegepast, waarvan aangenomen wordt dat dit tot minder peroperatief bloedverlies en een lager infectiepercentage leidt. Vanaf de craniale zijde wordt via een kleine incisie een entreepunt naar de mergholte van het femur gecreëerd, die is gelegen om en nabij de tip van de trochanter major. Afhankelijk van het type pen (diameter) zal de mergholte van de femurschacht eventueel opgeboord moeten worden, om een veilige insertie tot in de mergholte te garanderen. Indien het entreepunt niet exact gekozen wordt, bestaat het gevaar voor een additionele fractuur van de femurschacht wanneer de pen te krachtig in de femurschacht wordt ingebracht.
De positie van de heupschroef, of bij sommige typen twee heupschroeven dient dusdanig te zijn, dat op de AP projectie de (meest caudale) schroef in de caudale helft van de hals en de kop wordt gepositioneerd, eveneens tot in het subchondrale bot. Op de axiale foto is een centrale of dorsale ligging als optimaal te kwalificeren. Deze positionering is in feite conform de plaatsing van de schroef bij een GHS (zie figuur 4).
Distale vergrendeling van de pen in de femurschacht is niet zonder gevaar. Indien de vergrendeling niet goed lukt, dient men zich te realiseren dat ook dit de kans op een additionele distale fractuur van de schacht met zich mee kan brengen.
Cementaugmentatie
Na GRADE analyse blijkt cementaugmentatie van de collumschroef bij IF van een trochantere fractuur mogelijk van invloed op pijn in de eerste zes weken postoperatief; daarna is er geen meerwaarde. Dit kan van invloed zijn op comfort van de patient in de eerste periode en vertaalt zich in mogelijke verlaging van de opnameduur. Het betreft uitkomsten van enkele studies, waarin onduidelijk is welke factoren nog meer voor verkorting van opnameduur zorgen. Cementaugmentatie heeft geen invloed op de mobiliteit op middellange termijn (één jaar). De NICE en AAOS richtlijnen uit het VK en de VS bevatten geen onderzoek of aanbeveling over cementaugmentatie na trochantere fractuur.
Voor de positie van de collumschroef bij een pertrochantere fractuur, gaat de voorkeur van de werkgroep uit naar een mid-midpositie in de femurkop tot één cm onder het gewrichtsoppervlak. Indien twijfel bestaat over de mate van fixatie van de collumschroef in de femurkop is augmentatie op theoretische gronden een optie.
Voor een stabiele pertrochantere fractuur die wordt behandeld met een GHS systeem, biedt een 2-gats plaat voldoende stabiliteit (Říha, 2010; Verhofstad, 2004; Bolhofner, 1999). Bij instabiele fracturen is fixatie met een vier-gats GHS plaat aangewezen (Baird, 2014).
Gegeven de verhoogde incidentie van fracturen rondom het implantaat na intramedullaire fixatie, gaat in geval van twijfel de voorkeur uit naar lange pensystemen.
De werkgroep is van mening dat het aanbrengen van compressie op de fractuur door de operateur na het inbrengen van het implantaat – en na het beëindigen van tractie – essentieel is. Gebruik van een compressieschroef daartoe is optioneel.
Onderbouwing
Gedislokeerde pertrochantere fracturen dienen gereponeerd te worden; zowel gesloten als open repositie technieken worden in de literatuur beschreven. Glijdende heupschroeven (GHS), plaatfixatie en intramedullaire implantaten worden gebruikt voor de interne fixatie (IF) van (niet) gedislokeerde pertrochantere femurfracturen. Deze dienen volgens specifieke criteria ingebracht te worden. Het is daarnaast onduidelijk of cementaugmentatie in de femurkop bijdraagt aan betere mechanische stabiliteit.
1.
|
GRADE Laag |
Er lijkt geen verschil in risico op ‘cut-out’ (het uitbreken van het osteosynthesemateriaal uit het bot) te bestaan tussen valgusrepositie of anatomische repositie bij osteosynthese van trochantere fracturen.
Bronnen (Parker, 2009) |
|
GRADE Matig |
Er lijkt geen verschil in het risico op het falen van de fixatie in bredere zin te zijn tussen valgusrepositie of anatomische repositie bij trochantere fracturen.
Bronnen (Parker, 2009) |
|
GRADE Laag |
Er lijkt geen verschil in het risico op diepe wondinfectie te zijn tussen valgusrepositie of anatomische repositie bij osteosynthese van trochantere fracturen.
Bronnen (Parker, 2009) |
|
GRADE Matig |
Er lijkt geen verschil in het risico op overlijden te zijn tussen valgusrepositie of anatomische repositie bij osteosynthese van trochantere fracturen.
Bronnen (Parker, 2009) |
|
GRADE Laag |
Er lijkt geen verschil te zijn in het aantal patiënten dat terugkeert op het pretraumatische niveau van mobiliteit na behandeling met valgusrepositie of anatomische repositie bij osteosynthese van trochantere fracturen.
Bronnen (Parker, 2009) |
2.
|
GRADE Laag |
Er zijn aanwijzingen dat patiënten met trochantere fracturen die geholpen zijn met cementaugmentatie bij de fixatie minder lang in het ziekenhuis verblijven dan patiënten die zonder cementaugmentatie gefixeerd zijn.
Bronnen (Lee, 2010; Dall’Oca, 2010) |
|
GRADE Laag |
Cementaugmentatie bij de fixatie van trochantere fracturen leidt één week postoperatief tot minder pijn dan fixatie zonder cementaugmentatie.
Bronnen (Mattsson, 2005) |
|
GRADE Laag |
Cementaugmentatie bij de fixatie van trochantere fracturen leidt zes weken postoperatief tot minder pijn dan fixatie zonder cementaugmentatie.
Bronnen (Mattsson, 2005) |
|
GRADE Matig |
Het is onduidelijk of cementaugmentatie bij de fixatie van trochantere fracturen na meer dan zes maanden na de operatie tot minder pijn leidt dan fixatie zonder cementaugmentatie.
Bronnen (Mattsson, 2005; Lee, 2010) |
|
GRADE Laag |
Er lijkt een jaar postoperatief geen verschil in de mobiliteitsscore te zijn tussen patiënten geholpen met cementaugmentatie bij fixatie van trochantere fracturen en patiënten zonder cementaugmentatie bij fixatie.
Bronnen (Lee, 2010) |
1. Leidt een valgusrepositie of een anatomische repositie bij interne fixatie van trochantere fracturen tot betere uitkomsten?
Beschrijving studies
In de searchresultaten werd één Cochrane review over dit onderwerp gevonden (Parker, 2009). Uit de searchresultaten kwamen geen andere SRs of RCTs naar voren die aan de Cochrane review konden worden toegevoegd. In deze systematische review werden vijf RCTs beschreven, welke allemaal voor 2004 zijn gepubliceerd. Ondanks het feit dat de RCTs zijn gepubliceerd vóór 2004 is besloten om vanwege het gebrek aan meer recente studies, de geïncludeerde RCTs op te nemen in de literatuuranalyse. De vijf RCTs, allemaal gepubliceerd tussen 1980 en 1999 (Hubbard, 1990; Clark, 1990; Desjardins, 1993; Gargan, 1994; Kumar, 1996), beschrijven in totaal 530 patiënten. Eén RCT vergelijkt (sarmiento) osteotomie met anatomische repositie bij behandeling middels een ‘fixed nail plate’, de overige vier RCTs beschrijven de vergelijking osteotomie (Sarmiento, Dimon & Hughston of medialisatie) versus anatomische repositie bij behandelingen middels een glijdende heupschroef. Osteotomie werd gezien als interventie en anatomische repositie als controle. Follow-up varieerde van drie tot 11 maanden, en de ‘loss to follow-up’ was maximaal 14%. De studies zijn uitgevoerd in de UK (3x), India & Canada.
In vier studies lag de gemiddelde leeftijd rond de 81 jaar en was +/- 20% man; één RCT beschreef een afwijkende studiepopulatie met een gemiddelde leeftijd van 58 jaar en 59% man. De beschreven uitkomstmaten waren cut-out, falen van fractuurfixatie, diepe wondinfectie, mortaliteit (aan eind follow-up) en terugkeer naar niveau mobiliteit voor fractuur.
Resultaten
Uitkomstmaat ‘cut-out’ (een vorm van falen fixatie)
Deze uitkomstmaat is in drie studies beschreven bij 271 patiënten. Er waren vier casus in de interventiegroep (N=127) en zes casus in de controlegroep (N=144), dit resulteerde in een RR van 0,85 [95% CI 0,25 – 2,91], met een lage mate van heterogeniteit (0%). Gezien de resultaten lijkt er geen verschil in het risico op ‘cut-out’ te zijn tussen de controle- en interventiegroep.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘cut-out’ is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (matige kwaliteit geïncludeerde RCTs) en het geringe aantal patiënten (imprecisie). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Uitkomstmaat ‘alle vormen van falen fixatie’
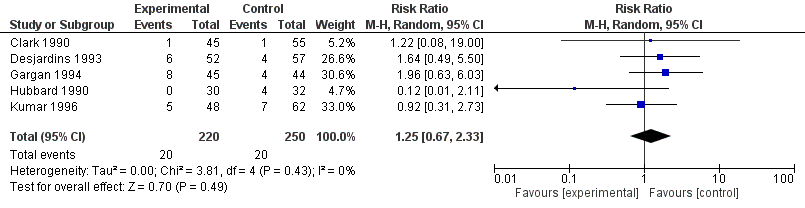
De uitkomstmaat ‘falen van fixatie’ is in vijf RCTs beschreven en werd gedefinieerd als ‘nonunion, cut-out en andere chirurgische complicaties als gevolg van de fixatie’. Er zijn in totaal 470 patiënten beschreven, met 40 casus van ‘falen van fixatie’. Relatief kwamen er in de interventiegroep iets meer casus voor dan in de controlegroep (respectievelijk 20/220 vs. 20/250). Dit heeft een RR van 1,25 [95% CI 0,67 tot 2,33] tot gevolg (figuur 1). Gezien de resultaten lijkt er geen verschil in het risico op ‘falen fixatie’ te zijn tussen de controle- en interventiegroep.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘falen fixatie’ is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (matige kwaliteit geïncludeerde RCTs). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Matig’.
Figuur 1 Forest-plot uitkomstmaat 'Falen van Fixatie'
Uitkomstmaat ‘diepe wondinfectie’
Deze uitkomstmaat is in drie studies beschreven bij 271 patiënten. Er was één casus in de interventiegroep (N=127) en drie casus in de controlegroep (N=144), dit resulteerde in een RR van 0,63 [95% CI 0,11 tot 3,83], met een lage mate van heterogeniteit (0%). De betrouwbaarheidsintervallen van de individuele studies en van het gepoolde effect zijn erg breed, daarnaast zijn komen er maar weinig casus voor. Dit draagt bij aan de onzekerheid omtrent deze uitkomstmaat. Gezien de resultaten lijkt er geen verschil in het risico op ‘diepe wondinfectie’ te zijn tussen de controle- en interventiegroep.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘diepe wondinfectie’ is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (matige kwaliteit geïncludeerde RCTs) en het geringe aantal patiënten (imprecisie). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Uitkomstmaat ‘mortaliteit’
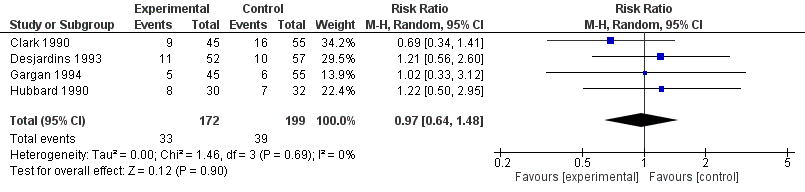
De uitkomstmaat ‘mortaliteit’ is in vier studies beschreven, met in totaal 371 patiënten. In de interventiegroep overleden 33 patiënten (N=172), in de controlegroep 39 (N=199). Dit resulteert in een RR van 0,97 [95% CI 0,64 tot 1,48] (figuur 2). Er lijkt geen verschil te zijn in het risico op overlijden tussen de twee groepen.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘mortaliteit’ is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (matige kwaliteit geïncludeerde RCTs). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Matig’.
Figuur 2 Forest-plot uitkomstmaat 'Mortaliteit'
Uitkomstmaat ‘terugkeer niveau mobiliteit voor fractuur’
De uitkomstmaat ‘terugkeer naar niveau mobiliteit voor fractuur’ is in drie studies beschreven. In de systematische review is deze uitkomstmaat niet verder gespecificeerd, ook is niet aangegeven hoe deze in de individuele studies is beoordeeld. In de interventiegroep waren 46 van de 99 (46%) patiënten in staat de prefractuur mobiliteit te behalen, in de controlegroep waren dat 49 van de 109 patiënten (45%). Dit leidde tot een RR van 0,96 [95% CI 0,75 tot 1,23] in het voordeel van de interventiegroep. Dit verschil is echter niet significant. Er lijkt voor deze uitkomstmaat dus geen verschil te zijn.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘terugkeer niveau mobiliteit voor fractuur’ is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (matige kwaliteit geïncludeerde RCTs) en het geringe aantal patiënten (imprecisie). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
2. Leidt cementaugmentatie bij interne fixatie van trochantere fracturen tot betere uitkomsten dan interne fixatie zonder augmentatie?
Beschrijving studies
De search naar deze vergelijking leverde verschillende relevante studies op. Er werd één relevante systematische review over het onderwerp gevonden (Namdari, 2013), echter werden er in dit artikel zowel RCTs als observationele studies beschreven. Alle RCTs uit de systematische review bleken ook in de literatuursearch van de commissie naar voren te komen. Uiteindelijk voldeden drie RCTs aan de inclusiecriteria (Lee, 2010; Dall’Oca, 2010; Mattsson, 2005). Deze studies vergeleken het gebruik van cementaugmentatie bij de fixatie van instabiele trochantere fracturen. In totaal zijn 300 patiënten geïncludeerd, gemiddelde leeftijd was boven de 80 jaar en tussen de 20 en 45% van de verschillende studiepopulaties was man. De studies komen uit Zweden, Italië en Taiwan en de methodologische kwaliteit is acceptabel. In de studie van Lee is een inadequate manier van randomiseren gebruikt (aan de hand van patiëntnummer, even is behandeling, oneven controlegroep).
Resultaten
Uitkomstmaat ‘duur verblijf ziekenhuis’
Deze uitkomstmaat is in twee studies beschreven (Lee, 2010; Dall’Oca, 2010). In de studie van Lee verbleef de groep patiënten met cementaugmentatie gemiddeld 8,5 dagen in het ziekenhuis, ten opzichte van 9,8 dagen in de controlegroep, dit verschil was significant (p=0,01). In de studie van Dall’Oca verbleven patiënten met cementaugmentatie gemiddeld 9 dagen in het ziekenhuis, waar de controlegroep 10,5 dagen in het ziekenhuis verbleef, dit verschil was echter niet significant. De gegevens van in totaal 188 patiënten zijn voor deze uitkomstmaat beschreven.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘duur verblijf ziekenhuis’ is met twee niveaus verlaagd gezien het geringe aantal patiënten en het feit dat niet beide studies een significant effect rapporteerden (imprecisie). Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Uitkomstmaat ‘postoperatieve pijn na één week’
Deze uitkomstmaat is alleen in de studie van Mattsson, 2005 beschreven. De postoperatieve pijn is gemeten met een VAS van 0 tot 100. Dit is op verschillende manieren gedaan, er is voor gekozen om de pijnscore te meten na de vraag ‘hoeveel pijn heeft u vandaag aan uw heup’. De interventiegroep (N=55) scoorde 39 ± 14, de controlegroep (N=57) 47 ± 16. Dit resulteert in een mean difference van -8,00 [95% CI -13,56 tot -2,44], hetgeen betekent dat de interventiegroep significant minder pijn heeft één week postoperatief.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘postoperatieve pijn na één week’ is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten. Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Uitkomstmaat ‘postoperatieve pijn na zes weken’
Deze uitkomstmaat is alleen in de studie van Mattsson, 2005 beschreven. De postoperatieve pijn is gemeten met een VAS. Dit is op verschillende manieren gedaan, er is voor gekozen om de pijnscore te meten na de vraag ‘hoeveel pijn heeft u vandaag aan uw heup’. De interventiegroep (N=55) scoorde 14 ± 11, de controlegroep (N=57) 28 ± 12. Dit resulteert in een mean difference van -14,00 [95% CI -18,26 tot -9,74], hetgeen betekent dat de interventiegroep significant minder pijn heeft zes weken postoperatief.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘postoperatieve pijn na zes weken’ is met één niveau verlaagd gezien het geringe aantal patiënten. Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Uitkomstmaat ‘postoperatieve pijn na minimaal zes maanden’
Deze uitkomstmaat is in twee studies gemeten (Mattsson, 2005; Lee, 2010). In Mattsson, de pijnmeting het langst na de operatie was na zes maanden. In Lee vond de meting één jaar na de operatie plaats. De postoperatieve pijn is op verschillende manieren gemeten in de twee studies. Om die reden is de standarized mean difference voor de uitkomstmaat berekend, deze komt uit op -0,49 [95% CI -1,06 tot 0,09], hetgeen inhoudt dat er een voordeel lijkt voor cementaugmentatie, maar dat dit echter niet statistisch significant is. Er kan dus niet geconcludeerd worden dat cementaugmentatie op de lange termijn leidt tot minder pijn.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘postoperatieve pijn na minimaal zes maanden’ is met één niveau verlaagd gezien het geringe aantal patiënten. Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Matig’.
Uitkomstmaat ‘mobiliteit één jaar postoperatief’
De mobiliteit na operatie is in één studie beschreven (Lee, 2010). Eén jaar na operatie is de mobiliteit gemeten met de ‘mobility score of Parker and Palmer’, dit is een schaal van 0 tot 9 waar de waarde 0 ‘complete disability’ betekent en de waarde 9 ‘no difficulty’, geen beperkingen. Preoperatief verschilden de groepen niet significant, de controlegroep had een iets hogere score (6,2 vs. 5,8). Een jaar postoperatief scoorde de interventiegroep 5,3 ± 2,4 en de controlegroep 4,2 ± 2,2. Dit verschil was echter volgens de auteurs niet statistisch significant (p=0,073).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ‘mobiliteit een jaar postoperatief’ is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten. Vanwege het studiedesign van de geïncludeerde studies (RCTs) is de uitgangspositie ‘Hoog’, de uiteindelijke bewijskracht komt uit op ‘Laag’.
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht naar de volgende vraagstellingen:
- Leidt een valgusrepositie of een anatomische repositie bij interne fixatie van trochantere fracturen tot betere uitkomsten?
- Leidt cementaugmentatie bij interne fixatie van trochantere fracturen tot betere uitkomsten dan interne fixatie zonder augmentatie.
Relevante uitkomstmaten
De werkgroep achtte voor 1. mortaliteit, terugkeer naar mobiliteit voor fractuur- en fixatie gerelateerde complicaties kritieke uitkomstmaten.
De werkgroep achtte voor 2. duur van het ziekenhuisverblijf, postoperatieve pijn, en mobiliteit kritieke uitkomstmaten.
De werkgroep definieerde niet à priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), Embase (Elsevier) is met relevante zoektermen gezocht naar studies waarin de behandeling van trochantere fracturen middels interne fixatie is beschreven. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 662 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- primair vergelijkend onderzoek;
- studiedesign: (quasi) RCTs of een systematische review van (quasi) RCTs;
- gepubliceerd tussen 2004 en augustus 2015;
- full-tekst artikel in het Engels of Nederlands;
- patiëntenpopulatie: volwassen patiënten met trochantere (extracapsulaire) fracturen;
- beschrijving van minimaal een van de vergelijkingen;
- beschrijving van minimaal een van de uitkomstmaten.
Voor 1. (open repositie versus anatomische repositie), is er een Cochrane review gevonden die een anatomische repositie met osteotomie heeft vergeleken. De werkgroep heeft besloten om deze vergelijking verder uit te werken. Deze vergelijking wordt vergelijking A2 genoemd. Op basis van titel en abstract werden in eerste instantie voor vergelijking A2 en B 14 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens tien studies geëxcludeerd (zie exclusietabel), en vier studies definitief geselecteerd (vergelijking A2 n=1, vergelijking B n=3).
De evidence-tabellen hiervan en de beoordeling van individuele studiekwaliteit kunt u in onder het tabblad Onderbouwing vinden.
- Baird RP, O'Brien P, Cruickshank D. Comparison of stable and unstable pertrochanteric femur fractures managed with 2- and 4-hole side plates. Can J Surg. 2014;57(5):327-30.
- Bolhofner BR, Russo PR, Carmen B. Results of intertrochanteric femur fractures treated with a 135-degree sliding screw with a two-hole side plate. J Orthop Trauma. 1999;13(1):5-8.
- Dall'Oca C, Maluta T, Moscolo A, et al. Cement augmentation of intertrochanteric fractures stabilised with intramedullary nailing. Injury. 2010;41(11):1150-5.
- Lee P, Hsieh P, Chou Y, et al. Dynamic hip screws for unstable intertrochanteric fractures in elderly patients--encouraging results with a cement augmentation technique. J Trauma. 2010;68(4):954-64.
- Mattsson P, Alberts A, Dahlberg G, et al. Resorbable cement for the augmentation of internally-fixed unstable trochanteric fractures. A prospective, randomised multicentre study. J Bone Joint Surg Br. 2005;87(9):1203-9.
- Namdari S, Rabinovich R, Scolaro J, et al. Absorbable and non-absorbable cement augmentation in fixation of intertrochanteric femur fractures: systematic review of the literature. Arch Orthop Trauma Surg. 2013;133(4):487-94.
- Parker M, Handoll H. Osteotomy, compression and other modifications of surgical techniques for internal fixation of extracapsular hip fractures. Cochrane Database Syst Rev. 2009;(2):CD000522.
- Ríha D, Bartonícek J. Internal fixation of pertrochanteric fractures using DHS with a two-hole side-plate. Int Orthop. 2010;34(6):877-82.
- Verhofstad MH, van der Werken C. DHS osteosynthesis for stable pertrochanteric femur fractures with a two-hole side plate. Injury. 2004;35(10):999-1002.
Repositie
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Parker, 2009
PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of RCTs
Literature search up to [February/march, 2008]
A: Hubbard, 1990 B: Clark, 1990 C: Desjardins, 1993 D: Gargan, 1994 E: Kumar, 1996
Study design: (quasi)-RCT
Setting and Country: Multicentre setting in various countries (India, UK, & Canada)
Source of funding: • University of Teesside, Middlesbrough, UK. • Peterborough and Stamford Hospitals NHS Foundation Trust, Peterborough, UK.
No external sources of support supplied. |
Inclusion criteria SR: - (quasi) RCTs; - Skeletally mature patients with an extracapsular proximal femoral Fracture; - Comparing anatomic reduction with valgus (osteotomy) reduction;
Exclusion criteria SR: - none mentioned
5 studies included
Important patient characteristics at baseline:
N, mean age A: 65 patients, 82 yrs B: 100 patients, 83 yrs C: 127 patients, 80,5 yrs D: 100 patients, 82 yrs E: 138 patients, 58 yrs
Sexe: A: not mentioned B: 14 % Male C: 23% Male D: 15% Male E: 59% Male
Groups comparable at baseline. |
Describe intervention:
A: Sarmiento osteotomy B: Sarmiento osteotomy C: Dimon and Hughston medial displacement osteotomy D: Sarmiento valgus osteotomy or Dimon and Hughston medial displacement osteotomy E: Medialisation osteotomy
|
Describe control:
A: Anatomical reduction B: Anatomical reduction C: Anatomical reduction D: Anatomical reduction E: Anatomical reduction
|
End-point of follow-up:
A: mean 3 months B: 3 months C: mean 11 months D: Not available E: 6 months
For how many participants were no complete outcome data available? A: 0% B: 3% (not further specified) C: 14% (not further specified) D: 0% E: 13 % not further specified)
|
Outcome measure-Fracture fixation complications (cut-out)
A: I: 0/30 C: 2/32 B: I: 1/45 C: 1/55 C: I:3/52 C: 3/57
RR: 0,85 [0,25 – 2,91]
Outcome measure-Fracture fixation complications (fixation failure)
A: I: 0/30 C: 4/32 B: I: 1/45 C: 1/55 C: I: 6/52 C: 4/57 D: I:8/45 C: 4/55 E: I: 5/48 C: 7/62
RR: 1,25 [ 0,67 – 2,33]
Outcome measure-Fracture fixation complications (deep sepsis)
Effect measure: RR, RD, mean difference [95% CI]: A: I: 1/30 C: 0/32 B: I: 0/45 C: 1/55 C: I: 0/52 C: 2/57
RR: 0,63 [0,11 – 3,83]
Outcome measure-Mortality A: I: 8/30 C: 7/32 B: I: 9/45 C: 16/55 C: I: 11/52 C: 10/57 D: I: 5/45 C: 6/55
RR: 0,97 [ 0,64 – 1,48]
Outcome measure-Regain pre fracture mobility A: I: 11/22 C: 9/25 B: I:16/33 C: 21/36 C: I: 19/44 C: 19/48
RR: 0,96 [0,75 – 1,23] |
Outcome: fracture fixation complications: • cut-out of the implant proximally (penetration of the implant from the proximal femur either into the hip joint or external to the femur). • non-union of the fracture within the follow-up period (the definition of non-union was that used within each individual study). • other surgical complications of fixation (as detailed in each study) • fracture fixation failure rate (sum of the above three) • re-operation (within the follow-up period of the study) • superficial wound infection (infection of the wound in which there is no evidence that the infection is deep to the deep fascia layer or extends to the site of the implant) • deep wound infection (infection below the deep fascia layer)
Mortality (at end of follow-up) Not further specified
Regain pre fracture mobility Not further specified |
Cementaugmentatie
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Lee, 2010 |
Type of study: RCT
Setting: Single center
Country: Taiwan
Source of funding: Not mentioned |
Inclusion criteria: - unstable intertrochanteric fractures’ - 75 years or older; - Exclusion criteria: - stable fractures; - open fractures; - multiple fractures; - pathologic fractures; - previous ipsilateral hip or femur surgery; - developmental abnormality; - ASA classification 4 or 5. N total at baseline: Intervention: 55 Control:53
Important prognostic factors2: age ± SD: I: 82,6 ± 4,9 C: 81,3 ± 5,8
Sex: I: 45 % M C:45 % M
Groups comparable at baseline.
|
Describe intervention:
Cement augmentation:
DHS applied with PMMA (Surgical Simplex P, Stryker-Howmedica, Limerick, Ireland) bone cement for unstable intertrochanteric fractures in elderly patients.
|
Describe control:
No cement augmentation
DHS applied without bone cement for unstable intertrochanteric fractures in elderly patients. |
Length of follow-up: Minimum 12 months
Loss-to-follow-up: 15 patients, not further specified.
Incomplete outcome data: Not mentioned
|
Outcome measures and effect size:
Pain (measured on a 4-point scale, at 1-year follow-up) I: 1,6 ± 0,6 C: 2,2 ± 0,9 P=0,008
Mobility score (at 1 year follow-up) I: 5,3 ± 2,4 C: 4,2 ± 2,2 P=0,073
Cut-out I: 0/55 C:5/53 RR: 0,09 [0,00-1,55]
LOS I: 8,5 ± 2,4 C: 9,8 ± 2,8 P=0,009 |
Pain defined as: Pain was graded on a four-point scale: (1) no pain; (2) mild pain not affecting walking or requiring regular analgesic medication; (3) moderate pain affecting walking and/or requiring regular medication; (4) severe pain, even at rest, requiring stronger analgesics.
Mobility score: Walking ability before injury was graded from 0 to 9 using the mobility score of Parker and Palmer, which reflects the sum of patients’ ability to walk indoors, walk outdoors, and participate in social activities. A value of 0 indicates complete disability, and a value of 9 indicates no difficulty. |
|
Dall’Oca, 2010 |
Type of study: RCT
Setting: Single center
Country: Italy
Source of funding: The author did not receive any outside funding or grants in support of their research for or preparation of this work. Neither they nor a member of their immediate families received payments or other benefits or a commitment or agreement to provide such benefits from commercial entity. |
Inclusion criteria: - unstable trochanteric fracture; - age 80 or older; - Singh score of 1 or 2; Exclusion criteria: - dementia; - neuromuscular or musculo-skeletal deficiency which could limit the ability to perform objective functional tests; - malignancy; - massive corticosteroid treatment; - concurrent other fractures or operations which could affect post-operative functional outcome; N total at baseline: Intervention: 40 Control:40
Important prognostic factors2: age: I: 85,3 C: 82,3
Sex: I:35 % M C: 25% M
Groups comparable at baseline. |
Describe intervention:
Augmentation technique with cement
|
Describe control:
Conventional technique |
Length of follow-up: Minimum 6 months (range 6-12 months)
Loss-to-follow-up: 9 patients died.
Incomplete outcome data: Not mentioned
|
Outcome measures and effect size:
HHS pre-op I: 56,49 C: 56,75
HHS post-op 1 month I:48,2 C:49,31
HHS post-op 6 months I:54,71 C:56,42
HHS post-op 12 months I:57,91 C:59,86
LOS I: 9 C:10,5 P=0,1 |
|
|
Mattsson, 2005 |
Type of study: RCT
Setting: Multi-center
Country: Sweden
Source of funding: The authors thank Stratec (Stockholm, Sweden) for providing the implants for this study and Trygg Hansa for the research grant. No benefits in any form have been received or will be received from a commercial party related directly or indirectly to the subject of this article. |
Inclusion criteria: - an unstable trochanteric fracture; - age more than 65 years; - walking with or without support; - less than 72 hours between the fracture and surgery.
Exclusion criteria: dementia, serious concomitant illness or mental instability, neurosensory, neuromuscular or musculoskeletal deficiency which limited the ability to perform objective functional tests, soft-tissue infection at the operation site, ongoing radiotherapy or chemotherapy for malignancy, pathological fracture, a clotting disorder, corticosteroid treatment exceeding 5 mg/day, a concurrent fracture which would affect the post-operative functional outcome or an earlier operation on the contralateral hip
N total at baseline: Intervention: 55 Control: 57
Important prognostic factors2: age ± SD: I:81,2 ± 7,0 C: 82,0 ± 6,3
Sex: I:20 % M C:18 % M
Groups comparable at baseline. |
Describe intervention:
Cement augmentation: internal fixation with a sliding screw device combined with augmentation using a calcium phosphate degradable cement (Norian SRS)
|
Describe control:
No cement augmentation: Internal fixation with a sliding screw device alone. |
Length of follow-up: 6 months
Loss-to-follow-up: Intervention: N=7 (12%) Reasons (concurrent illness or weakness which made it impossible for them to attend for review)
Control: N=7 (12%) Reasons (concurrent illness or weakness which made it impossible for them to attend for review)
Incomplete outcome data: Intervention: N (%) Reasons (describe)
Control: N (%) Reasons (describe) |
Outcome measures and effect size:
Pain (VAS) at 1 week I: 39 ± 14 C: 47 ± 16 P=0,005 Pain (VAS) at 6 weeks I: 14 ± 11 C: 28 ± 12 P< 0,001
Pain (VAS) at 6 months I:7 ± 9 C: 9 ± 11 P=0,3
Cut-out I: 0/55 C: 0/57 NS
|
|
Risk of bias
Repositie
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Parker, 2009 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes (limitations in included studies) |
Yes |
no |
unclear |
Cement augmentatie
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Lee, 2010 |
Divided based on even or odd medical number. |
unclear |
unlikely |
unlikely |
unclear |
unlikely |
unclear |
likely |
|
Dall’Oca, 2010 |
Sealed envelope randomisation |
Unlikely |
Unlikely |
Unlikely |
Unclear |
Unlikely |
Unlikely |
unlikely |
|
Mattsson, 2005 |
Sealed envelope randomisation |
unlikely |
unlikely |
unlikely |
likely |
Unlikely |
Unlikely |
unlikely |
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-11-2016
Beoordeeld op geldigheid : 01-11-2016
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2021 bepaalt het bestuur van de NVvH in overleg met de NOV of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVvH en de NOV zijn regiehouder van deze richtlijn en zijn de verantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kennisinstituut.nl) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Patiëntenparticipatie bij deze richtlijn werd mede gefinancierd uit de Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ.
De financier heeft tijdens het ontwikkelproces op geen enkele wijze invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Reduceren van praktijkvariatie in de zorg rondom proximale femurfracturen.
Doelgroep
Zorgverleners die met de betreffende patiëntengroep in aanraking komen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met proximale femurfracturen te maken hebben. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dhr. dr. M.J. Heetveld, traumachirurg, werkzaam in het Kennemer Gasthuis, Haarlem, Nederlandse Vereniging voor Heelkunde, (voorzitter).
- Dhr. prof. dr. M.H.J. Verhofstad, traumachirurg, werkzaam in het Erasmus MC, Rotterdam, Nederlandse Vereniging voor Heelkunde.
- Dhr. dr. J.H. Hegeman, traumachirurg, werkzaam bij Ziekenhuisgroep Twente, Almelo-Hengelo, Nederlandse Vereniging voor Heelkunde.
- Dhr. drs. M. Holla, orthopedisch chirurg, werkzaam in het Radboudumc, Nijmegen, Nederlandse Orthopaedische Vereniging.
- Dhr. dr. J.B.A. van Mourik, orthopedisch chirurg, werkzaam in het Máxima Medisch Centrum, Veldhoven, Nederlandse Orthopaedische Vereniging.
- Mw. dr. M.C. Willems, klinisch geriater, werkzaam in het Academisch Medisch Centrum, Amsterdam, Nederlandse Vereniging voor Klinische Geriatrie.
- Dhr. dr. T.J. Hoogeboom, fysiotherapeut, werkzaam in het Radboudumc, Nijmegen, Koninklijk Nederlands Genootschap voor Fysiotherapie.
- Dhr. dr. R. van Balen, specialist ouderengeneeskunde, werkzaam bij Laurens, Rotterdam, Verenso.
- Mw. E.C. Folbert MANP, verpleegkundig specialist, werkzaam bij Ziekenhuisgroep Twente, Almelo-Hengelo, Verpleegkundigen & Verzorgenden Nederland (V&VN).
- Mw. dr. M.C.O. van den Nieuwenhuyzen, anesthesioloog, werkzaam in het Ikazia ziekenhuis, Rotterdam, Nederlandse Vereniging voor Anesthesiologie.
- Mw. R. Lammers MSc, patiëntvertegenwoordiger, Patiëntenfederatie Nederland, Utrecht.
Met ondersteuning van:
- Mw. dr. M.A. Pols, senior-adviseur Kennisinstituut van Medisch Specialisten, Utrecht.
- Dhr. A.A. Lamberts MSc, junior-adviseur Kennisinstituut van Medisch Specialisten, Utrecht.
- Mw. M.E. Wessels MSc, literatuurspecialiste, Kennisinstituut van Medisch Specialisten, Utrecht.
Met dank aan:
- Mw. C.S. Scherphof MSc, patiëntvertegenwoordiger, Patiëntenfederatie Nederland, Utrecht.
Belangenverklaringen
De “Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling” is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf directe financiële (betrekking commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonslijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
|
Folbert |
verpleegkundig specialist traumatologie |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Heetveld |
Plaatsvervangend opleider SEG |
penningmeester OTC Nederland sponsor betaalt alleen cursus (educatie) uren. Bestuursleden OTC participeren en educatie cursus. |
geen |
geen |
OTC Nederland Penningmeester |
FAITH trial - geen belang bij richtlijn |
geen |
geen |
|
Hegeman |
Chirurg-traumachirurg ziekenhuisgroep Twente (ZGT) |
vz stichting Netwerk v Geriatrische Traumalogie (onbetaald) |
geen |
geen |
geen |
geen |
geen |
lezingen over traumatologische onderwerpen, geriatrische traumatologie en osteoporose waarvoor sprekervergoedingen worden ontvangen van de DePuy Synthes en Eli Lily in de afgelopen 2 jaar. De Stichting Netwerk voor Geriatrische traumatologie wordt ondersteund door DePuy Synthes dmv een educational grant |
|
Holla |
orthopedisch chirurg-traumatoloog Radboud MUC |
voorzitter OTC educatiecommissie Nederland |
geen |
geen |
geen |
geen |
Auteur van Holla's medische statusvoering en Holla's orthopaedic pocketcards. |
geen |
|
Hoogeboom |
postdoc aan MUMC+ |
Gastdocent Fysiotherapie |
geen |
geen |
geen |
geen |
geen |
geen |
|
Lamberts |
Junior adviseur Kennisinstituut van Medisch Specialisten |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Lammers |
beleidsadviseur Patiëntenfederatie Nederland |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Pols |
Senior adviseur Kennisinstituut van Medisch Specialisten |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Van Balen |
specialist ouderengeneeskunde Laurens Rotterdam |
senior onderzoeker afdeling public health en eerste lijnsgeneeskunde LUMC, onbetaald |
geen |
geen |
geen |
geen |
geen |
geen |
|
Van den Nieuwenhuyzen |
anesthesioloog ikazia ziekenhuis, opleider |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Van Mourik |
orthopedisch chirurg 50%.Hoofd zorggroep Klinische chemie, Apotheek en Radiologie 50%. |
bestuurslid STZ, onbetaald Spreker voor DePuySynthes: Medical Education voor operatiekamerpersoneel, Trauma Basis Principes (2016) (betaald), spreker voor de AO cursus Principes van Operatieve Fractuur Behandeling (2015) (betaald). |
geen |
geen |
geen |
geen |
geen |
geen |
|
Verhofstad |
hoogleraar traumachirurg erasmus MC |
onafhankelijk deskundige bij aansprakelijkheidsstellingen en rechtzaken (incidenteel betaald) |
geen |
geen |
beoogd voorzitter ongevalstichting Ned. Sept 2014. |
geen |
geen |
geen |
|
Willems |
klinisch geriater |
NVKG, voorzitter, vacatievergoeding |
geen |
geen |
NVKG, voorzitter |
geen |
expertise op het gebied van fractuurrisico en osteoporose bij ouderen. Geen specifieke producten die zich lenen voor vermarkting. |
geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afvaardiging van de Patiëntenfederatie Nederland zitting te laten nemen in de werkgroep. Tijdens de ontwikkelfase van de richtlijn heeft de Patiëntenfederatie Nederland interviews met patiënten gehouden, deze uitkomsten zijn meegenomen bij het schrijven van de richtlijntekst. Het verslag van deze interviews staat onder 'aanverwant'. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Zie ook het implementatieplan onder 'aanverwant'.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is, en op de ‘richtlijn voor richtlijnen’ voor de beoordeling van de kwaliteit van richtlijnen (www.zorginstituutnederland.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseurs de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende veldpartijen via de invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (Schünemann; 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie (zie http://www.guidelinedevelopment.org/handbook/).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
De GRADE-methodiek is door de Nederlandse werkgroep GRADE-NL (nog) niet vastgesteld voor dit type vraagstelling. De bewijskracht van de conclusie is bepaald volgens de EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Voor vragen over de waarde van diagnostische tests, over schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in één of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen
Om te komen tot een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals criteria die van invloed zijn op de aanbeveling, de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Indicatoren
De werkgroep heeft besloten om niet specifiek voor deze richtlijn indicatoren te ontwikkelen. In het kader van de DHFA worden er al reeds indicatoren ontwikkeld. Tijdens het schrijven van de richtlijn is expliciet met deze indicatoren rekening gehouden. De indicatoren die in het kader van de DHFA ontwikkeld worden kan men gebruiken om de implementatie van de richtlijn te meten.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als researchaanbeveling in de Kennislacunes beschreven onder 'aanverwant'.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers M, Kho M, Browman GP, et al. for the AGREE Next Steps Consortium. AGREE II: Advancing guideline development, reporting and evaluation in healthcare. Can Med Assoc J. 2010;182:E839-842.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from www.guidelinedevelopment.org/handbook.
Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline
2004-aug. 2015
Engels, |
1 Femoral Fractures/ or Hip Fractures/ (24570) 2 (pertrochant* or intertrochant* or trochanteric or subtrochanteric or extracapsular*).ti,ab. (12363) 3 1 or 2 (33652) 4 exp "Fracture Fixation, Internal"/ or "Fracture Healing"/ or "Bone Screws"/ or "Bone Nails"/ or Internal Fixators/ (56114) 5 ((internal adj3 Fixat*) or Screw* or Nail* or pin* or GHS or CHS or DHS or osteosynthes*).ti,ab. (169169) 6 4 or 5 (192702) 7 3 and 6 (10489) 8 limit 7 to (yr="2004 -Current" and (dutch or english)) (3749) 9 (angle* or reduction* or position* or valgus or varus or repostition* or technique* or augment* or CCD).ti,ab. or bone cements/ or (cement* or uncement*).ti,ab. or (is or mt or ae).fs. (6184863) 10 8 and 9 (3037) 11 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (248785) 12 10 and 11 (89) – 83 uniek 13 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1510354) 14 10 and 13 (385) 15 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective.tw. or prospective.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (2212779) 16 10 and 15 (1298) – not SR OR RCT (1060) – niet in file 17 14 not 12 (339) – 328 uniek |
662 |
|
Embase (Elsevier) |
'femur fracture'/exp/mj OR ((hip* OR femur* OR femoral* OR trochant* OR pertrochant* OR intertrochant* OR subtrochant* OR extracapsular) NEAR/4 fracture*):ab,ti AND ([dutch]/lim OR [english]/lim) AND [embase]/lim AND [2004-2015]/py
AND ('osteosynthesis'/exp OR 'fracture healing'/exp OR 'bone screw'/exp OR 'bone nail'/exp OR 'internal fixator'/exp OR (internal NEAR/3 fixat*):ab,ti OR screw*:ab,ti OR nail*:ab,ti OR pin*:ab,ti OR ghs:ab,ti OR chs:ab,ti OR dhs:ab,ti OR osteosynthes*:ab,ti) AND ('bone cement'/exp OR angle*:ab,ti OR reduction*:ab,ti OR position*:ab,ti OR valgus:ab,ti OR varus:ab,ti OR repostition*:ab,ti OR technique*:ab,ti OR augment*:ab,ti OR ccd:ab,ti OR cement*:ab,ti OR uncement*:ab,ti OR 'side effect':lnk)
AND 'meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp)) (59) - 0 uniek
AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it NOT ('femur fracture'/exp/mj OR ((hip* OR femur* OR femoral* OR trochant* OR pertrochant* OR intertrochant* OR subtrochant* OR extracapsular) NEAR/4 fracture*):ab,ti AND ([dutch]/lim OR [english]/lim) AND [embase]/lim AND [2004-2015]/py) ) (327) – 215 uniek |
Exclusietabellen
|
Nummer in search |
Auteur + jaartal |
Inclusie / Exclusie |
Toelichting |
|
Systematische reviews |
|||
|
SR22 |
Zhou, 2012 |
Exclusie |
Geen antwoord op PICO |
|
SR51 |
Parker, 2009 |
Inclusie |
Inclusie, beschrijft ook RCTs van voor 2004. |
|
SR67 |
Whatling, 2006 |
Exclusie |
Geen antwoord op PICO |
|
Nummer in search |
Auteur + jaartal |
Inclusie / Exclusie |
Toelichting |
|
Systematische reviews |
|||
|
SR15 |
Namdari, 2013 |
Exclusie |
SR met vier RCTs beschreven, echter zijn deze RCTs ook in de literatuursearch naar voren gekomen. |
|
SR51 |
Parker, 2009 |
Exclusie |
SR met twee RCTs, echter zijn deze RCTs ook in de literatuursearch naar voren gekomen |
|
SR71 |
Parker, 2006 |
Exclusie |
Geen antwoord op PICO. |
|
SR79 |
Craig, 2005 |
Exclusie |
Geen antwoord op PICO. |
|
R54 |
Pesce, 2014 |
Exclusie |
Geen antwoord op PICO. |
|
R73 |
Kammerlander, 2014 |
Exclusie |
Geen vergelijkend onderzoek |
|
R267 |
Kammerlander, 2011 |
Exclusie |
Geen vergelijkend onderzoek |
|
R319 |
Lee, 2010 |
Inclusie |
RCT |
|
R330 |
Dall’Oca, 2010 |
Inclusie |
RCT |
|
R505 |
Mattsson, 2005 |
Inclusie |
RCT |
|
R534 |
Mattsson, 2004 |
Inclusie |
RCT |
