Diagnostische prostaat MRI
Uitgangsvraag
Wat is de plaats van prostaat MRI voor het detecteren van prostaatcarcinoom (PCa) bij mensen met een klinische verdenking op aggressief PCa?
Deelvragen
- Wat is de diagnostische accuratesse van MRI, de MRI-pathway (met zo mogelijk MRI- gerichte biopten) en het huidige zorgpad van systematische TRUS-geleide biopten?
- Hoe verhoudt zich de detectie van zowel agressieve als niet-agressieve kankers tussen de MRI-pathway en de huidige standaard van TRUS-geleide biopten?
- Wat is de additionele diagnostische waarde van zowel de MRI-pathway op het huidige zorgpad, als de systematische biopten op de MRI-pathway?
Aanbeveling
Algemene aanbevelingen ten aanzien van prostaat MRI diagnostiek
Gebruik prostaat MRI niet als een eerste middel voor screening.
Committeer aan de meest recente PI-RADS richtlijnen voor prostaat MRI acquisitie en interpretatie, en evalueer MRI resultaten in multidisciplinair verband met pathologie correlatie.
Aanbevelingen in biopsie-naïeve mannen
Verricht een MRI alvorens een prostaat biopsie te verrichten.
Combineer gerichte met systematische biopten wanneer de MRI positief is (PI-RADS ≥ 3).
Overweeg systematische biopten achterwege te laten, in gezamenlijke besluitvorming met patiënt, wanneer prostaat MRI negatief is (PI-RADS ≤ 2), en het risico op agressief prostaatkanker laag is.
Aanbevelingen in mannen met een eerder negatieve systematische prostaat biopsie
Verricht een MRI alvorens een prostaat biopsie te verrichten.
Verricht gerichte biopten wanneer prostaat MRI positief is (PI-RADS ≥ 3).
Verricht systematische biopsie, in gezamenlijke besluitvorming met patiënt, wanneer prostaat MRI negatief is (PI-RADS ≤ 2), en het risico op agressief prostaatkanker hoog is.
Overwegingen
Multiparametrsche MRI en MRI-gerichte biopsie verbetert de detectie van ISUP-graad ≥ 2 prostaatkanker (Drost, 2019). Deze verbetering is meest prominent bij patiënten die in aanmerking komen voor herhaal biopten, met slechts een marginale toegevoegde waarde van systematische biopsie. De verbetering met behulp van MRI-gerichte biopten is minder uitgesproken in biopsie-naïeve mannen, bij wie systematische biopsie een hogere toegevoegde waarde geeft, mits het de detectie van ISUP graad ≥ 2 kankers betreft. Het is evident dat de MRI-gerichte biopsie een substantieel minder aantal ISUP graad 1 kankers detecteert dan de systematische biopsie.
MRI-gerichte biopsie kan in twee verschillende diagnostische paden worden gebruikt: 1) de 'gecombineerde pathway', waarbij patiënten met een positieve MRI een gecombineerde systematische en MRI-gerichte biopsie ondergaan en patiënten met een negatieve MRI alleen systematische biopsie ondergaan; 2) de 'MRI-pathway’, waarbij patiënten met een positieve MRI alleen een MRI-gerichte biopsie ondergaan en patiënten met een negatieve MRI helemaal geen biopten ondergaan. In deze pathway wordt de MRI als ‘triage-test’ geduid.
De MRI als triage-test is aantrekkelijk, omdat deze het aantal biopsie procedures zou kunnen verminderen, de detectie van laaggradige (niet-agressieve, indolente) prostaatkanker zou kunnen verminderen, terwijl de detectie van agressief prostaatkanker kan worden behouden (of zelfs verbeterd) in vergelijking met systematische biopsie. De interpretatie van de MRI kenmerkt zich echter door een bescheiden reproduceerbaarheid tussen de radiologen (Rosenkrantz, 2016). Bovendien is MRI-gerichte biopsie niet gestandaardiseerd en is de reproduceerbaarheid tussen de biopteurs niet onderzocht. Dit geldt echter ook voor de systematische biopsie procedure.
De 'MRI-pathway' alleen is slechts geëvalueerd bij patiënten bij wie het risico op agressief prostaatkanker hoog genoeg was om biopsie te ondergaan. Pre-biopsie MRI mag niet worden gebruikt bij patiënten die geen indicatie hebben voor een prostaat biopsie; de indicatie is gebaseerd op familiegeschiedenis en klinische en biochemische parameters. Vanwege de lage specificiteit zou het gebruik van MRI bij patiënten met een zeer laag risico op prostaatkanker leiden tot een toename van vals-positieve bevindingen en daaropvolgende onnodige MRI-gerichte biopsie.
Het diagnostische resultaat en het aantal biopsie procedures dat mogelijk wordt vermeden door de MRI als triage-test in te zetten, hangt af van de PI-RADS drempel die wordt gebruikt om een MRI als positief (afwijkend) te definiëren. De radiologische PI-RADS v2 classificatie voor het inschatten van hooggradig prostaatkanker wordt gecategoriseerd op een 5-punts schaal (Weinreb, 2016). In gepoolde data van de gemixte populatie, zou een PI-RADS-drempel van ≥ 3 resulteren in 30% (95% BI: 23 tot 38%) niet-afwijkende (negatieve) MRIs en derhalve ook 30% minder biopsie procedures, terwijl dan 11% (95% CI: 6 tot 18%) van alle ISUP graad ≥ 2 kankers zou worden gemist (sensitiviteit 0.89 (95% BI: 0.82 tot 0.94) (Drost, 2019). Verhoging van de PI-RADS drempel tot ≥ 4 zou resulteren in 59% (95%BI: 43 tot 78%) minder biopsie procedures, terwijl dan 28% (95% BI: 14 tot 48) van alle ISUP graad ≥2 kankers zouden worden gemist (Drost, 2019). Van belang hierbij zijn de percentages negatieve (niet-afwijkende) MRI (PI-RADS score ≤ 2) die kunnen variëren, zoals bijvoorbeeld de percentages in MRI-FIRST, PRECISION en 4M met respectievelijk 21,1%, 28,9% en 49% (Rouvière, 2018; Kasivisvanathan, 2018; van der Leest, 2018). Een toenemende ervaring kan het percentage negatieve MRIs substantieel verhogen (49%) (van der Leest, 2018).
Als een agressieve prostaatkanker door de MRI-pathway wordt gemist, kan dit het gevolg zijn van slechte beeldkwaliteit, een verkeerde interpretatie door de radioloog, een “niet” zichtbare kanker op MRI, of het gevolg van een gerichte biopsie-fout (het doel werd gemist of onvoldoende gebiopteerd). De PRECISION-studie vond een duidelijk verschil in ISUP graad ≥2 prostaatkanker tussen MRI-gerichte en systematische biopsieën (detectieverhouding: 1.46 (95%BI: 1.12 tot 1.90) die de MRI-FIRST-studie of de 4M-studie niet konden reproduceren (detectie ratio: 1.08 (95%BI: 0.83 tot 1.40) en 1.09 (95%BI: 0.90 tot 1.32)) (Rouvière, 2018). Interessant is dat PRECISION vier gerichte biopten per laesie toeliet, terwijl MRI-FIRST er maar drie toestond. In een retrospectieve studie van 211 patiënten met een unilaterale MRI-laesie detecteerde alleen MRI-gerichte biopsie 73,5% van alle ISUP-klasse ≥ 2 prostaatkankers; 96% werd gedetecteerd door middel van de combinatie van MRI-gerichte en systematische biopten van de kwab met de MRI-laesie, en slechts 82% wanneer de combinatie de contralaterale kwab biopteerde (Bryk, 2017). Het verschil kan wijzen op richtfouten die leiden tot onvoldoende sampling van de tumor. Het verhogen van het aantal genomen biopten per afwijking kan deze onnauwkeurigheid mogelijk gedeeltelijk compenseren (Bryk, 2017). Er is dus een grote behoefte om deze procedures te verbeteren, of ten minste om het minimale aantal gerichte biopten te definiëren die van elke laesie moet worden genomen, als een functie van zijn grootte en locatie, en als een functie van het prostaatvolume, zoals voorgesteld door Lu (2019). Zonder een strikte standaardisatie van MRI-interpretatie en van de MRI-gerichte biopsie techniek, kan de 'MRI-pathway leiden tot suboptimale zorg buiten de expertise centra. Ook dit geldt voor de systematische biopsie procedure. Van belang hierbij is dat de resultaten van MRI als ook de MRI-gerichte biopsie in multidisciplinair verband worden besproken. Tevens dienen hierbij de meest recente PI- RADS richtlijnen te worden gevolgd.
De negatief voorspellende waarde van een diagnostische test neemt af wanneer de prevalentie van de ziekte toeneemt, of wel wanneer het vooraf-risico van de patiënt op de ziekte toeneemt. Daarom is de hoge negatief voorspellende waarde (NPV) voor MRI gerapporteerd in de literatuur mogelijk niet van toepassing op patiënten met een hoog vooraf risico op prostaatkanker (Moldovan, 2017). PSA-densiteit (Distler, 2017; Hansen, 2017; Panebianco, 2018) of risico tabellen (Schoots, 2019) kunnen patiënten selecteren met een hoog risico op klinisch significante prostaatkanker bij wie een MRI negatief voorspellende waarde laag is, en die mogelijk nog steeds kunnen profiteren van een systematische biopsie, juist als de MRI negatief is. Verschillende groepen hebben nomogrammen gepubliceerd die MRI bevindingen combineren met eenvoudige klinische gegevens die een goede voorspelling van de resultaten van een daaropvolgende biopsie kunnen geven, en zelfs beter kunnen presteren dan voorspellers zoals de ERSPC-gebaseerde prostaatwijzer (Alberts, 2018; Lee, 2017; Mehralivand, 2018; Radtke 2017). In de toekomst kunnen dergelijke nomogrammen helpen bij het selecteren van de juiste patiënten bij wie systematische en/of MRI-gerichte biopten noodzakelijk zijn. Deze moeten eerst nog op grote schaal worden gevalideerd (Schoots, 2019).
Bij elke aanbeveling aangaande prostaat MRI wordt uitgegaan dat dit een kundig verricht onderzoek betreft, volgens de meest recente PI-RADS richtlijnen, vergelijkbaar met die van andere diagnostische testen. In het kader van kwaliteitsborging wordt interne kwaliteitscontrole aangemoedigd, zoals het vastleggen en bespreken van uitkomsten in multidisciplinaire besprekingen, alsook data-analyses van diagnostische bevindingen met robuuste uitkomstmaten. Tevens is het zeer wel aan te moedigen de adviezen hieromtrent te volgen van nationale of internationale instanties (bijv. Nederlandse Vereniging van Radiologie (NVVR), Nederlandse Vereniging van Urologie (NVU), European Society of Urogenital Radiology (ESUR), of PI-RADS Steering Committee). Van belang hierbij is dat criteria worden opgesteld die de gehele keten van prostaatkanker diagnostiek waarborgen, inclusief MRI, MRI-gerichte biopten, alsook de histopathologische analyse van de biopten.
Onderbouwing
Prostaat MRI, met of zonder MRI gerichte biopsie, is mogelijk een aanvullende dan wel een alternatieve test voor systematische (transrectale echografie (TRUS) - geleide) biopsie voor de detectie van prostaatcarcinoom (PCa) bij mannen met een klinische verdenking op PCa. Het huidige diagnostische traject bestaat uit een combinatie van counseling, rectaal toucher, PSA-bepaling, risico inschatting, en systematische TRUS geleide biopten. Vanwege de lage specificiteit leidt het diagnostisch traject voorafgaand aan biopten tot een hoog aantal fout- positieve uitslagen en onnodige systematische biopten. Eveneens is TRUS onvoldoende geschikt om te differentiëren tussen niet-agressieve (indolente) en agressieve tumoren. Het huidige diagnostische traject leidt ertoe dat patiënten zonder PCa onnodig worden gebiopteerd. Tevens leidt deze diagnostiek tot het vinden van indolente tumoren. Een deel hiervan kan worden beschouwd als overdiagnose (fout-positief), en kan vervolgens onnodig worden (over)behandeld. Een deel van deze niet-agressieve tumoren kan ook worden onderschat (fout-negatief), en kan zo onder-behandeld worden. Diagnostische testen met een hogere sensitiviteit en specificiteit die onnodig biopteren verminderen en waarmee men agressieve van niet-agressieve tumoren kan worden onderscheiden is wenselijk. Prostaat MRI is een techniek die in deze behoefte zou kunnen voorzien. In deze module wordt de plaats van prostaat MRI bepaald voor het detecteren van PCa bij patiënten met een klinische verdenking op agressief PCa.
ISUP graad ≥ 2 prostaatcarcinoom
|
Laag GRADE |
Per 1000 mannen met een verdenking van prostaatcarcinoom, bij een prevalentie van 30% ISUP graad ≥ 2 prostaatcarcinoom suggereert:
Bronnen: (Drost, 2019) |
|
Laag GRADE |
Per 1000 mannen met een verdenking van prostaatcarcinoom, bij een prevalentie van 30% ISUP graad ≥2 prostaatcarcinoom suggereert:
de MRI-pathway 672 terecht negatieve uitslagen en de systematische biopsie 700 terecht negatieve uitslagen.
Bronnen (Drost, 2019) |
|
Laag GRADE |
Per 1000 mannen met een verdenking van prostaatcarcinoom, bij een prevalentie van 30% ISUP graad ≥ 2 prostaatcarcinoom suggereert:
Bronnen: (Drost, 2019) |
|
Laag GRADE |
Per 1000 mannen met een verdenking van prostaatcarcinoom, bij een prevalentie van 30% ISUP graad ≥ 2 prostaatcarcinoom suggereert:
Bronnen: (Drost, 2019) |
|
Laag GRADE |
De sensitiviteit van de MRI-pathway is hoger dan de sensitiviteit van systematische biopsie in de detectie van ISUP graad ≥ 2 prostaatcarcinoom.
Bronnen: (Drost, 2019) |
|
Laag GRADE |
De directe vergelijking tussen de MRI-pathway en systematische biopsie suggereert dat de MRI-pathway 12% meer ISUP graad ≥ 2 prostaatcarcinoom detecteert dan systematische biopsie.
Bronnen: (Drost, 2019) |
De literatuursamenvatting is gebaseerd op een Cochrane systematische review van Drost (2019) waarin de diagnostische testeigenschappen van de MRI-pathway (MRI met of zonder MRI-geleide biopsie) wordt vergeleken met de systematische biopsie voor de detectie van ISUP graad ≥ 2, graad ≥ 3, en graad 1 prostaatcarcinoom. Studies in Drost (2019) includeerden patiënten die de diagnostische accuratesse onderzochten van systematische biopsie, de MRI en de MRI-pathway; deze patiënten konden een MRI-positieve (bij wie vervolgens een MRI-geleide biopsie werd uitgevoerd) en MRI-negatieve bevinding hebben (bij wie geen MRI geleide biopsie werd uitgevoerd). Een MRI-geleide bioptie-werd bevestigd met histopathologie. Een negatieve MRI-pathway werd gedefinieerd als een negatieve MRI of een negatieve MRI geleide biopsie. Template geleide biopsie werd geselecteerd als de referentiestandaard. Twee verschillende technieken werden gebruikt: de transperineale template geleide mapping biopsie (TTMB) en de template saturatie biopsie (TSB). TTMB werd gedefinieerd als "transperineaal TRUS geleide biopsieën van de prostaat met de patiënt in lithotomie positie (met behulp van een 5 mm brachytherapie-rooster en minstens één biopsie in elk venster). TSB wordt gedefinieerd als ≥ 20 transperineale of transrectale TRUS-geleide biopsieën van de prostaat uitgevoerd met de intentie om de “volledige” prostaat te onderzoeken volgens een vooraf gedefinieerd patroon. Om de diagnostische accuratesse te bepalen van de MRI-pathway zijn gepoolde schattingen gemaakt van de sensitiviteit en specificiteit met behulp van een bivariaat model. De heterogeniteit is bepaald aan de hand van visuele beoordeling van de forest plots. Likelihood ratio’s werden berekend om te onderzoeken of de sensitiviteit en specificiteit van de MRI-pathway verschilden met de indextest. In de studie van Drost (2019) werden acht studies (n= 2257 mannen) geïncludeerd die de diagnostische accuratesse van de MRI-pathway onderzochten (Dal Moro, 2019; Distler, 2017; Hansen, 2016; Hansen, 2017; Kesch, 2017; Lawrence, 2014; Mortezavi, 2018; Pepe, 2013). De volgende voor de werkgroep relevante uitkomsten werden meegenomen voor diagnosestelling ISUP graad ≥2 prostaatcarcinoom: sensitiviteit, specificiteit, terecht positieven, fout negatieven, terecht negatieven en fout positieven.
Resultaten
Diagnostische accuratesse
Target conditie: ISUP graad ≥ 2 prostaatcarcinoom
Sensitiviteit ISUP graad ≥ 2 prostaatcarcinoom
De gepoolde sensitiviteit van de MRI voor de diagnosestelling van ISUP graad ≥ 2 prostaatcarcinoom was 91% (95% BI: 83 tot 95%).
De gepoolde sensitiviteit van de MRI-pathway voor de diagnosestelling van ISUP graad ≥2 prostaatcarcinoom was 72% (95% BI: 60 tot 82%).
De gepoolde sensitiviteit van systematische biopsie voor de diagnosestelling van ISUP graad ≥2 prostaatcarcinoom was 63% (95% BI: 19 tot 93%).
Specificiteit ISUP graad ≥ 2 prostaatcarcinoom
De gepoolde specificiteit van de MRI voor de diagnosestelling van ISUP graad ≥2 prostaatcarcinoom was 37% (95% BI: 29-46%).
De gepoolde specificiteit van de MRI-pathway voor de diagnosestelling van ISUP graad ≥2 prostaatcarcinoom was 96% (95% BI: 94-98%).
De gepoolde specificiteit van systematische biopsie voor de diagnosestelling van ISUP graad ≥2 prostaatcarcinoom was 100% (95% BI: 91-100%).
2x2 tabellen ISUP graad ≥ 2 prostaatcarcinoom op een populatie van 1000 mannen
In de 2x2 tabellen voor ISUP graad ≥ 2 prostaatcarcinoom van de diagnostische accuratesse van MRI, MRI-pathway en systematische biopsie (Figuur 1.1) worden de aantallen terecht positieven, terecht negatieven, fout positieven, en fout negatieven weergegeven op een populatie van 1000 mannen. Bij een veronderstelling van een vaste prevalentie van 30% ISUP graad ≥ 2 prostaatcarcinoom in de geteste populatie, zijn ook de positief en negatief voorspellende waarden per diagnostische test gegeven. Aanvullend zijn summary receiver operating curve (ROC) plots gegeven in een figuur ter visualisatie van de 95% betrouwbaarheidsinterval (streepjeslijn) en de heterogeniteit (stippellijn).
Samenvatting ISUP graad ≥ 2 prostaatcarcinoom.
Als we de MRI met de MRI-pathway vergelijken, zien we een aanzienlijke afname in sensitiviteit (van 0,91 tot 0,72) en een toename in specificiteit (van 0,37 tot 0,96), die beide statistisch significant waren (P <0,01). Als we de MRI-pathway vergelijken met de systematische biopsie, zien we een verdere afname in sensitiviteit (van 0,72 tot 0,63; P = 0,06) en was de specificiteit vergelijkbaar. Hieruit kan geconcludeerd worden dat MRI een hoge sensitiviteit heeft, maar dat door de beperkte accuratesse van de gerichte biopsie methode er een relevant aantal agressieve kankers worden gemist. Dit aantal gemiste agressieve kankers wordt groter als de systematische biopsie wordt gehanteerd. Deze getallen zijn gebaseerd op een populatie van zowel biopsie-naïeve mannen en mannen waarbij middels een eerdere systematische biopsie geen prostaatkanker was gevonden. Een verdere onderverdeling naar biopsie-naïeve mannen was niet mogelijk.
Target conditie: ISUP graad = 1 prostaatcarcinoom Sensitiviteit ISUP graad 1 prostaatcarcinoom
De gepoolde sensitiviteit van de MRI-pathway voor de diagnosestelling van ISUP graad 1 prostaatcarcinoom was 34% (95% BI: 19 tot 53%).
De gepoolde sensitiviteit van systematische biopsie voor de diagnosestelling van ISUP graad 1 prostaatcarcinoom was 55% (95% BI: 25 tot 83%).
Specificiteit ISUP graad 1 prostaatcarcinoom
De gepoolde specificiteit van de MRI-pathway voor de diagnosestelling van ISUP graad 1 prostaatcarcinoom was 100% (95% BI: 90 tot 100%).
De gepoolde specificiteit van systematische biopsie voor de diagnosestelling van ISUP graad 1 prostaatcarcinoom was 99% (95% BI: 81 tot 100%).
Samenvatting ISUP graad 1 prostaatcarcinoom.
Als we de MRI-pathway met de huidige praktijk van systematische biopsie vergelijken, zien we een toename in sensitiviteit (van 34% naar 55%; P = 0.52) met een vergelijkbare hoge specificiteit. Hieruit zou men kunnen afleiden dat met behulp van alleen MRI-pathway minder niet-agressieve kankers worden gedetecteerd dan met alleen systematische biopsie.
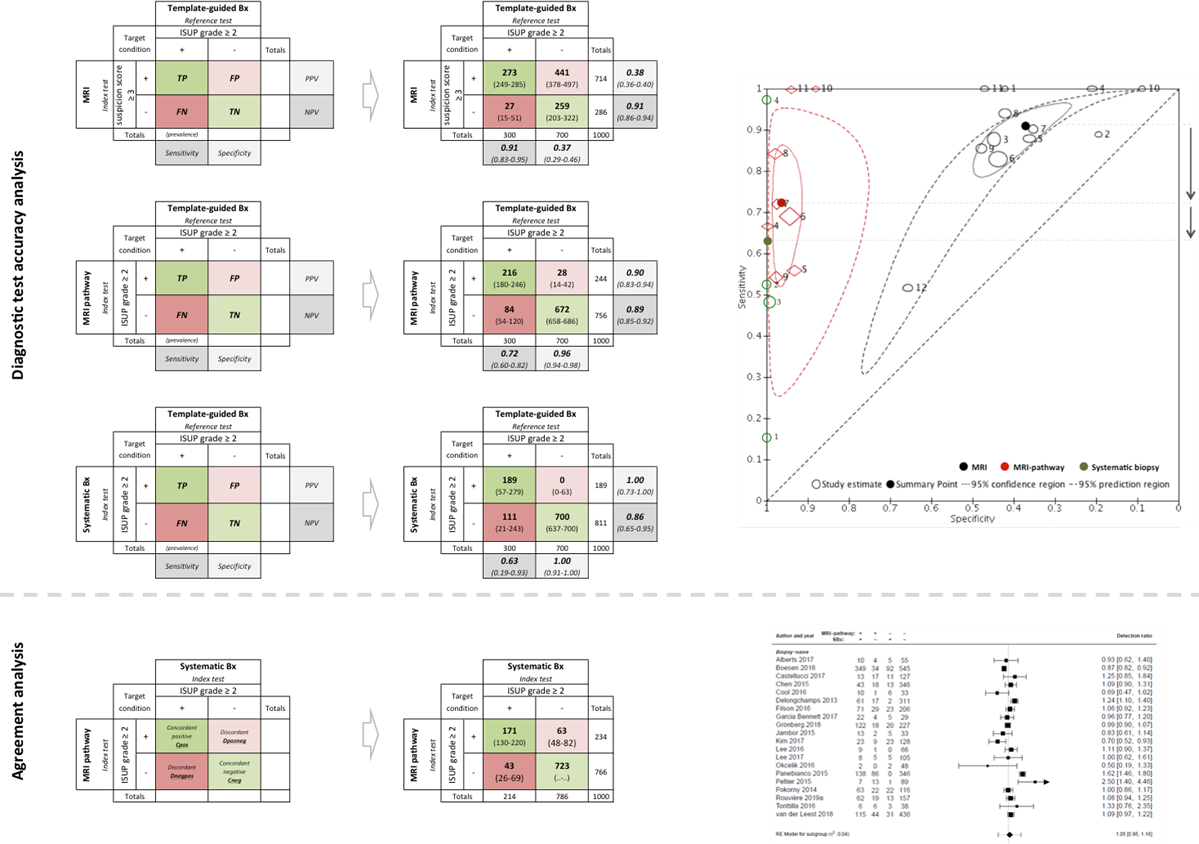
Figuur 1
a) diagnostische accuratesse analyse: 2x2 tabellen voor ISUP graad ≥ 2 prostaatcarcinoom van de index testen MRI, MRI-pathway en systematische biopsie, met template-geleide biopsie als referentie standaard. Aantallen terecht positieven, terecht negatieven, fout positieven, en fout negatieven worden weergegeven op een populatie van 1000 mannen. Tevens zijn de sensitiviteit en specificiteit gegeven. Bij een veronderstelling van een vaste prevalentie van 30% ISUP graad ≥ 2 prostaatcarcinoom in de geteste populatie, zijn ook de positief en negatief voorspellende waarden per diagnostische test gegeven. Aanvullend zijn summary receiver operating curve (ROC) plots gegeven in een figuur ter visualisatie van de 95% betrouwbaarheidsinterval (streepjeslijn) en de heterogeniteit (stippellijn).
b) agreement analyse: 2x2 tabellen voor ISUP graad ≥ 2 prostaatcarcinoom van de index testen MRI-pathway en systematische biopsie. Aantallen concordante en discordante bevindingen tussen beide index testen worden weergegeven op een populatie van 1000 biopsie-naïeve mannen. Aanvullend is een Forest plot analyse weergegeven van de kanker detectie ratio’s tussen de MRI-pathway en de systematische biopsie met als summary estimate 1.05 (95% BI: 0.95 tot 1.16).
Table 1. Diagnostic accuracy and predictive metrics of the index tests verified by template-guided biopsy as the reference standard for different target conditions
|
Target condition |
Index testa |
N participants (studies) |
Proportion negative MRI (95% CI) |
Accuracy metrics |
Prevalenceb (95% CI) |
Assumptive prevalencec |
Predictive metrics |
|||
|
Sensitivity (95% CI) |
Specificity (95% CI) |
P value |
NPVd (95% CI) |
PPVd (95% CI) |
||||||
|
ISUP G ≥ 2 prostate cancer |
MRI |
3091 (12) |
0.29 (0.22 to 0.37) |
0.91 (0.83 to 0.95) |
0.37 (0.29 to 0.46) |
P < 0.01f |
0.29 (0.22 to 0.38) |
|
0.91 (0.86 to 0.94) |
0.38 (0.36 to 0.40) |
|
MRI-pathway |
2257 (8) |
0.29 (0.24 to 0.35) |
0.72 (0.60 to 0.82) |
0.96 (0.94 to 0.98) |
P = 0.06g |
0.26 (0.18 to 0.36) |
0.30 |
0.89 (0.85 to 0.92) |
0.90 (0.83 to 0.94) |
|
|
SBx |
3421 (4) |
NA |
0.63 (0.19 to 0.93) |
1.00 (0.91 to 1.00) |
|
0.34 (0.21 to 0.51) |
|
0.86 (0.65 to 0.95) |
1.00 (0.73 to 1.00) |
|
|
ISUP G = 1 prostate cancer |
MRI |
1764 (10) |
0.28 (0.20 to 0.38) |
0.70 (0.59 to 0.80) |
0.27 (0.19 to 0.37) |
P < 0.01f |
0.20 (0.17 to 0.23) |
0.79 (0.74 to 0.82) |
0.20 (0.18 to 0.21) |
|
|
MRI-pathway |
681 (5) |
0.24 (0.16 to 0.36) |
0.34 (0.19 to 0.53) |
1.00 (0.90 to 1.00) |
P = 0.52g |
0.21 (0.18 to 0.24) |
0.20 |
0.86 (0.82 to 0.89) |
0.95 (0.37 to 1.00) |
|
|
SBx |
3421 (4) |
NA |
0.55 (0.25 to 0.83) |
0.99 (0.81 to 1.00) |
|
0.20 (0.16 to 0.25) |
|
0.90 (0.81 to 0.95) |
0.94 (0.37 to 1.00) |
|
CI: confidence interval; G: International Society of Urological Pathology grade; ID: inadequate data; MRI: magnetic resonance imaging; MRI-pathway: magnetic resonance imaging with or without magnetic resonance imaging- targeted biopsy; MRI-TBx: magnetic resonance imaging-targeted biopsy; N: number; NA: not applicable; SBx: systematic biopsy; ID, inadequate data
a) Data did not allow differentiation between the mix of included participants (biopsy-naive and prior-negative biopsy men).
b) Prevalence is pooled estimate of all detected cancer by template-guided biopsy.
c) Assumptive prevalence is an extrapolation from pooled estimates of all detected cancer by template-guided biopsy per target condition. This assumptive prevalence is necessary for adequate comparision of PPVs en NPVs between index tests.
d) Based on the Bayes’ theorem using the point estimates and 95% confidence intervals of the pooled positive and negative likelihood ratio and the point estimate of the prevalence.
e) MRI-positive men only, instead of MRI-positive + MRI-negative men, implicating a higher risk profile and increased prevalence of clinically significant prostate cancer.
f) Comparing sensitivity between MRI and the MRI-pathway.
g) Comparing sensitivity between the MRI-pathway and SBx.
Addapted from Drost et al, Cochrane Systematic Reviews Database 2019.
Interventie vergelijking
Target conditie: ISUP graad ≥2 prostaatcarcinoom
Detectieratio ISUP graad ≥2 prostaatcarcinoom
De gepoolde detectieratio voor ISUP graad ≥2 prostaatcarcinoom was 1.12 (95% BI: 1,02 tot 1,23; p< 0,01). Dit indiceert dat de MRI-pathway 12% meer ISUP graad ≥ 2 prostaatcarcinoom detecteert dan systematische biopsie. Deze getallen zijn gebaseerd op een ‘gemixte’ populatie van biopsie-naïeve mannen en mannen waarbij middels eerdere systematische biopsie geen prostaatkanker was gevonden.
Een verdere onderverdeling toonde een gepoolde detectieratio van 1.05 (95% BI: 0.95 tot 1.16); p= 0.35) bij biopsie-naïeve mannen en 1.44 (95% BI: 1.19 tot 1.75; p< 0.01) bij mannen met eerdere negatieve systematische biopten. Dit betekent dat de MRI-pathway meer agressieve kankers detecteert bij mannen na eerdere negatieve systematische biopten, dan bij biopsie-naïeve mannen. Van belang is te benadrukken dat beide testen statistisch gezien niet onder doen voor elkaar, ondanks een 5% meer gedetecteerde agressieve kankers door de MRI-pathway.
Bij mannen met een afwijkende (positieve) MRI was de gepoolde detectieratio’s 1.12 (95%BI: 1.01 tot 1.23; p= 0.35) voor biopsie-naïeve mannen en 1.49 (95% BI: 1.22 tot 1.82; p< 0,01) voor mannen met eerdere negatieve systematische biopten. Dit betekent dat de MRI-pathway meer agressieve kankers detecteert bij mannen met een afwijkende (positieve) MRI, bij zowel een biopsie-naïeve mannen als bij mannen met eerdere negatieve biopten.
Samenvattend, bij in opzet maximale detectie van ISUP graad ≥ 2 prostaatcarcinoom dient een MRI te worden vervaardigd voorafgaand aan een biopsie, bij zowel biopsie-naïeve mannen als bij mannen met eerdere negatieve biopten.
Target conditie: ISUP graad 1 prostaatcarcinoom
Detectieratio ISUP graad 1 prostaatcarcinoom
De gepoolde detectieratio voor ISUP graad 1 prostaatcarcinoom was 0.63 (95% BI: 0.54 tot 0.74; p< 0.01) bij biopsie-naïeve mannen en 0.62 (95% BI: 0,44 tot 0,88; p< 0.01) bij mannen met eerdere negatieve systematische biopten. Bij mannen met een afwijkende (positieve) MRI was de gepoolde detectieratio 0.85 (95% BI: 0.74 tot 0.98; p= 0.03) bij biopsie-naïeve mannen en 1.03 (95% BI: 0.89 tot 1.18; p= 0.71) bij mannen met eerdere negatieve systematische herhaal biopten.
Dit betekent dat de MRI-pathway minder agressieve kankers detecteert bij zowel biopsie- naïeve mannen als bij mannen met eerdere negatieve systematische biopten, en dat dit verschil afneemt bij mannen met een afwijkende (positieve) MRI.
Interventie vergelijking - toegevoegde waarde
Target conditie: ISUP graad ≥ 2 prostaatcarcinoom
Toegevoegde waarde ISUP graad ≥ 2 prostaatcarcinoom
Van het totaal (28% (95% BI: 24 tot 33%)) aan gedetecteerde ISUP graad ≥2 prostaatcarcinoom in biopsie-naïeve mannen was 17% (95% BI: 13 tot 22%) door beide testen gedetecteerd. In aanvulling hierop werd 6% (95% BI: 5 tot 8%) ISUP graad ≥ 2 prostaatcarcinoom alleen door de MRI-pathway gedetecteerd, en 4% (95% BI: 3 tot 7%) alleen door systematische biopsie.
Van het totaal (23% (95% BI: 20 tot 26%)) aan gedetecteerde ISUP graad ≥ 2 prostaatcarcinoom in mannen met een eerdere negatieve systematische biopsie werd 11% (95% BI: 9 tot 14%) door beide testen gedetecteerd. In aanvulling hierop werd 10% (95% BI: 8 tot 12%) ISUP graad ≥ 2 prostaatcarcinoom alleen door MRI-pathway gedetecteerd, en 2% (95% BI: 1 tot 4%) alleen door systematische biopsie.
Samenvattend, als bij in opzet maximale detectie van ISUP graad ≥ 2 prostaatcarcinoom wordt nagestreefd, ongeacht aantal biopten en detectie van indolente kankers, dient in zowel biopsie-naïeve mannen als in mannen met een eerdere negatieve systematische biopsie de MRI-pathway te worden toegepast en dient de systematische biopsie aanvullend te worden toegepast.
Target conditie: ISUP graad 1 prostaatcarcinoom
Toegevoegde waarde ISUP graad 1 prostaatcarcinoom
Van het totaal (21% (95% BI: 18 tot 25%)) aan gedetecteerde ISUP graad 1 prostaatcarcinoom in biopsie-naïeve mannen was 9% (95% BI: 6 tot 12%) door beide testen gedetecteerd. In aanvulling hierop werd 2% (95% BI: 1 tot 4%) ISUP graad 1 prostaatcarcinoom alleen door MRI-pathway gedetecteerd, en 10% (95% BI: 8 tot 12%) alleen door systematische biopsie.
Van het totaal (18% (95% BI: 13 tot 25%)) aan gedetecteerde ISUP graad 1 prostaatcarcinoom in mannen met een eerdere negatieve systematische biopsie was 6% (95% BI: 3 tot 10%) door beide testen gedetecteerd. In aanvulling hierop werd 4% (95% BI: 3 tot 6%) ISUP graad 1 prostaatcarcinoom alleen door MRI-pathway gedetecteerd, en 8% (95% BI: 4 tot 15%) alleen door systematische biopsie.
Samenvattend, als bij in opzet maximale detectie van ISUP graad ≥ 2 prostaatcarcinoom maar tevens ook minimale detectie van ISUP graad 1 prostaatcarcinoom wordt nagestreefd, dient in zowel biopsie-naïeve mannen als in mannen met een eerdere negatieve biopsie de MRI-pathway te worden toegepast, en dient te worden overwogen de aanvullende systematische biopsie achterwege te laten.
Bewijskracht van de literatuur
De bewijskracht van de literatuur voor de diagnostische accuratesse is met twee niveaus verlaagd gezien de beperkingen in de onderzoeksopzet t.a.v. patiëntselectie en keuze referentiestandaard (risk of bias) en grote heterogeniteit in resultaten tussen de studies (imprecisie). Voor GRADE is dit vrijwel standaard bij elke vorm van diagnostische test accuratesse analyses, waarbij randomisatie-studies tussen 2 index testen in directe vergelijking met een referentie standaard niet worden uitgevoerd. Ondanks dat de systematische review en meta-analyse van Drost (2019) de hoogste level of evidence bevat (OCEBM Levels of Evidence Working Group), toont GRADE slechts “laag” als gradering.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag: triage-
Deel 1. Diagnostische accuratesse:
Patiënten: Patiënten met een primaire of blijvende verdenking op prostaatcarcinoom Index test 1: MRI
Index test 2: MRI-pathway
Index test 3: Systematische TRUS-geleide biopten Referentie test: Template-gerichte biopten
Target condition: agressief prostaatkanker (gedefinieerd als, ISUP graad ≥ 2 (=GS ≥ 3+4 en hoger)), niet agressief prostaatkanker (gedefinieerd als, ISUP graad = 1 (=GS = 3+3), Uitkomst maten: diagnostische performance maten (sensitiviteit en specificiteit), aantal mannen die geen biopsie hoeft te ondergaan
Deel 2. Interventie vergelijking
Patiënten: Patiënten met een primaire of blijvende verdenking op prostaatcarcinoom
Interventie: MRI-pathway
Comparison: Systematische TRUS-geleide biopten
Target condition: agressief prostaatkanker (gedefinieerd als, ISUP graad ≥ 2 (=GS ≥ 3+4 en hoger)), niet agressief prostaatkanker (gedefinieerd als, ISUP graad = 1 (=GS = 3+3), Uitkomst maten: detectie ratio (DR).
Deel 3. Interventie vergelijking - additionele waarde
Patiënten: Patiënten met een primaire of blijvende verdenking op prostaatcarcinoom Interventie: MRI-pathway
Comparison: Systematische TRUS-geleide biopten
Target condition: agressief prostaatkanker (gedefinieerd als, ISUP graad ≥ 2 (=GS ≥ 3+4 en hoger)), niet agressief (indolente) prostaatkanker (gedefinieerd als, ISUP graad = 1 (=GS = 3+3),
Uitkomst maten: 1) Discordantie - positief voor MRI-pathway en negatief voor systematische biopten; 2) Discordantie - negatief voor MRI-pathway en positief voor systematische biopten.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID), Embase (via Embase.com), Central, Web of Science, Scopus, Pubmed, Google.com, Google Scholar, Cinahl, WorldCat, ProQuest, OpenGrey, ClinicalTrials, WHO register en de Cochrane Library (via Wiley) is op 31-07-2018 met relevante zoektermen gezocht naar studies over de effectiviteit en diagnostische accuratesse van MRI in diagnostiek van patiënten met een primaire verdenking op prostaatcarcinoom. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 650 treffers op. Op advies van de werkgroep is de Cochrane review van Drost et al (2019) uitgewerkt. Drost et al (2019) dekken de literatuur tot en met 31 juli 2018 en deze is als basis gebruikt voor de literatuursamenvatting. Er is één SR opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- 1 - Alberts AR, Roobol MJ, Verbeek JFM, Schoots IG, Chiu PK, Osses DF, et al. Prediction of High- grade Prostate Cancer Following Multiparametric Magnetic Resonance Imaging: Improving the Rotterdam European Randomized Study of Screening for Prostate Cancer Risk Calculators. European urology. 2018.
- 2 - Bryk DJ, Llukani E, Taneja SS, Rosenkrantz AB, Huang WC, Lepor H. The Role of Ipsilateral and Contralateral Transrectal Ultrasound-guided Systematic Prostate Biopsy in Men With Unilateral Magnetic Resonance Imaging Lesion Undergoing Magnetic Resonance Imaging-ultrasound Fusion-targeted Prostate Biopsy. Urology. 2017;102:178-82.
- 3 - Drost FJH, Osses DF, Roobol MJ, Steyerberg EW, Bangma CH, Schoots IG. Prostate MRI, with or without MRI-targeted biopsy, and systematic biopsy for detecting prostate cancer. Cochrane Database of Systematic Reviews. 2019.
- 4 - Distler FA, Radtke JP, Bonekamp D, Kesch C, Schlemmer HP, Wieczorek K, et al. The Value of PSA Density in Combination with PI-RADS for the Accuracy of Prostate Cancer Prediction. The Journal of urology. 2017;198:575-82.
- 5 - Hansen NL, Barrett T, Koo B, Doble A, Gnanapragasam V, Warren A, et al. The influence of prostate-specific antigen density on positive and negative predictive values of multiparametric magnetic resonance imaging to detect Gleason score 7-10 prostate cancer in a repeat biopsy setting. BJU international. 2017;119:724-30.
- 6 - Kasivisvanathan V, Rannikko AS, Borghi M, Panebianco V, Mynderse LA, Vaarala MH, et al. MRI-Targeted or Standard Biopsy for Prostate-Cancer Diagnosis. New England Journal of Medicine. 2018;378:1767-77.
- 7 - Lee SM, Liyanage SH, Wulaningsih W, Wolfe K, Carr T, Younis C, et al. Toward an MRI-based nomogram for the prediction of transperineal prostate biopsy outcome: A physician and patient decision tool. Urologic oncology. 2017;35:664.e11-.e18.
- 8 - Lu AJ, Syed JS, Ghabili K, Hsiang WR, Nguyen KA, Leapman MS, Sprenkle PC. Role of Core Number and Location in Targeted Magnetic Resonance Imaging-Ultrasound Fusion Prostate Biopsy. Eur Urol. 2019 Jul;76(1):14-17.
- 9 - Mehralivand S, Shih JH, Rais-Bahrami S, Oto A, Bednarova S, Nix JW, et al. A Magnetic Resonance Imaging-Based Prediction Model for Prostate Biopsy Risk Stratification. JAMA oncology. 2018;4:678-85.
- 10 - Moldovan PC, Van den Broeck T, Sylvester R, Marconi L, Bellmunt J, van den Bergh RCN, et al. What Is the Negative Predictive Value of Multiparametric Magnetic Resonance Imaging in Excluding Prostate Cancer at Biopsy? A Systematic Review and Meta- analysis from the European Association of Urology Prostate Cancer Guidelines Panel. European urology. 2017;72:250-66.
- 11 - Panebianco V, Barchetti G, Simone G, Del Monte M, Ciardi A, Grompone MD, et al. Negative Multiparametric Magnetic Resonance Imaging for Prostate Cancer: What's Next? European urology. 2018;74:48-54.
- 12 - Radtke JP, Wiesenfarth M, Kesch C, Freitag MT, Alt CD, Celik K, Distler F, Roth W, Wieczorek K, Stock C, Duensing S, Roethke MC, Teber D, Schlemmer HP, Hohenfellner M, Bonekamp D, Hadaschik BA. Combined Clinical Parameters and Multiparametric Magnetic Resonance Imaging for Advanced Risk Modeling of Prostate Cancer-Patient- tailored Risk Stratification Can Reduce Unnecessary Biopsies. Eur Urol. 2017 Dec;72(6):888-896.
- 13 - Rouvière O ea. Added value of prostate systematic and targeted biopsy based on multiparametric MRI in biopsy-naïve patients (MRI-FIRST): a prospective multicentre paired diagnostic study. . Lancet Oncol 2018.
- 14 - Rosenkrantz AB, Ginocchio LA, Cornfeld D, Froemming AT, Gupta RT, Turkbey B, Westphalen AC, Babb JS, Margolis DJ. Interobserver Reproducibility of the PI-RADS Version 2 Lexicon: A Multicenter Study of Six Experienced Prostate Radiologists. Radiology. 2016 Sep;280(3):793-804
- 15 - Schoots IG, Roobol MJ. Multivariate risk prediction tools including MRI for individualized biopsy decision in prostate cancer diagnosis: current status and future directions. World J Urol. 2019 Mar 13.PMID: 30868240. The Oxford Levels of Evidence 2. Oxford Centre for Evidence-Based Medicine.
- 16 - https://www.cebm.net/index.aspx?o=5653 (visited: 20th june 2019).
- 17 - van der Leest M, Cornel E, Israel B, Hendriks R, Padhani AR, Hoogenboom M, et al. Head-to- head Comparison of Transrectal Ultrasound-guided Prostate Biopsy Versus Multiparametric Prostate Resonance Imaging with Subsequent Magnetic Resonance- guided Biopsy in Biopsy-naive Men with Elevated Prostate-specific Antigen: A Large Prospective Multicenter Clinical Study. European urology. 2018.
Evidence table for systematic reviews of diagnostic test accuracy studies
Research question:
|
Study reference |
Study characteristics |
Patient characteristics |
Index test (test of interest) |
Reference test |
Follow-up |
Outcome measures and effect size |
Comments |
|
|
Drost, 2019
PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR (and meta- analysis)
A: Dal Moro, 2019 B:Distler, 2017 C: Hansen, 2016 D: Hansen, 2017 E: Kesch, 2017 F: Lawrence, 2014 G: Mortezavi, 2018 H: Pepe, 2013
Study design: A: Prospective cohort B: Prospective cohort C: Prospective cohort D: Prospective cohort E: Prospective cohort F: Retrospective cohort G: Prospective cohort |
Inclusion criteria SR:
Exclusion criteria SR:
8 studies included
Important patient characteristics:
Number of patients A: 123 B: 1040 C: 571 D: 487 E: 172 F: 39 G: 415 H: 14.453
Age, mean (SD) A: 62 (IQR: 57- 68) B: 65 (IQR: 60- 71) C: 65 (IQR: 59- 69) |
Describe index and comparator tests* and cut-off point(s):
A-1: MRI only +MRI- TBx +MRI-pathway: a 1.5 TeslaMRI machine was used with T2 and DWI sequences. PI- RADS version 1 was used with score 1-5 and score ≥3 for positivity. Transrectal cognitive MRI-TBx were performed from all MRI-positive lesions B: Index tests: MRI only + MRI-TBx + MRI-pathway: a 3 Tesla MRI machine (Magnetrom Prisma or Biograph mMR (Siemens Healthcare) was used, with T2, DWI and DCE sequences. The PIRADS version 1 Likert 1-5 score was used, with threshold ≥ 3 for |
Describe reference test and cut-off point(s):
A: Reference standard: transrectal 24-core saturation Bx including 8 anterior biopsies, blinded forMRI results. When a suspicious lesion was present, the operator performed first the MRI-TBx and then the saturation biopsies (unblinded) B: Reference standard: volume-based systematic transperineal grid- directed Bx with a median of 24 cores according to theGinsburg protocol. Bx operators first performed theMRI-TBx and had access to MRI data during whole procedure C: Reference standard: an 18-24 core systematic transperineal Bx |
Endpoint of follow- up: A: Not applicable B: Not applicable C: Not applicable D: Not applicable E: Not applicable F: Not applicable G: Not applicable H: Not applicable
..... |
Outcome measures and effect size (include 95%CI and p-value if available):
Outcome measure-1/2 (e.g. sensitivity / specificity (%))
|
Study quality (ROB): method used and results per individual study
Place of the index test in the clinical pathway: replacement, triage, add-on
Choice of cut-off point: influences test characteristics (sens, spec); important in relation to the clinical question (e.g. if a disease is to be ruled out, sensitivity is the critical outcome measure and more important than specificity: high sensitivity comes at the expense of low specificity and high rates of false postives, and usually those testing positive are subjected to further diagnostic tests for final diagnosis)
Facultative:
Brief description of author’s conclusion
Personal remarks on study quality, conclusions, and other issues (potentially) |
|
|
|
H: Prospective cohort
Setting and Country: A: Italy B: Germany C: UK D: Germany E: Germany F: UK G: Switzerland H: Italy |
D: 66 (IQR: 61- 72) E: 65 (IQR: 58- 71) F: 64 (range: 47-77) G: Repeat-Bx: 64 (IQR: 60 tot 69) Bx-naïve: 63 (IQR: 57-68) H: 63 (range: 49-72)
Median PSA A: 6.3 ng/mL (IQR: 4.8-8.9) B: 7.2 ng/mL (IQR: 5.3-10.4) C: 7.8 ng/mL (IQR: 4.4-83) D: 5.9 ng/mL (IQR: 4.6-8) E: 9.2 ng/mL (IQR:7.1-13.9) F: 7.2 ng/mL (IQR: 5.4-10.2) G: 10 ng/mL (range: 1.2-36) Repeat-Bx: 8.6 ng/mL (IQR: 5.7 -13) Bx-naïve: 5.8 (IQR: 4.4-8.9) H: 11 ng/ mL (range 3,7-45) |
positivity. Transperineal MRITBx were taken from all positive lesions with the Biopsee system (rigid software registration). First MRI-TBx were taken, subsequently the reference biopsies C: Index test: MRI only, MRI-TBx and MRI-pathway. A 1.5 Tesla (MR450) or a 3 Tesla (Discovery MR750 HDx) machine of GE Healthcare was used with T2, DWI and DCE sequences. The PIRADS version 1, Likert 1-5 score was used, with threshold ≥ 3 for positivity First transperineal software fusionMRI- TBx cores were taken (BiopSee platform,Medcom) of every suspicious lesion. Then the reference standard was performed D: Index tests:MRI only,MRI-TBx |
according to the Ginsburg protocol, with 1-2 cores from each of the 12 sectors, using the BiopSee MRI- TRUS fusion platform with a brachytherapy grid for guidance. Blinding of MRI results not reported D: Reference standard: a volume-based, transperineal template Bx scheme, with a median of 24 cores, according to Ginsburg protocol was performed, using the BiopSee MRI-TRUS fusion platform with brachytherapy grid for guidance. Blinding of MRI results not reported E: Reference standard: Novel, volume-based, automated core- placement method for TOP-Bx placement was performed with a needle distribution sampling each conceivable tumour lesion ≥ 0.5 mL in the complete prostate (100%), with a |
|
|
relevant to the research question
Sensitivity analyses (excluding small studies; excluding low quality studies; excluding case-control type of studies; relevant subgroup- analyses); mention only analyses which are of potential importance to the research question
Heterogeneity: clinical and statistical heterogeneity; clinical: enough similarities in patient characteristics, diagnostic tests (strategy) to allow pooling? For pooled data: assessment of statistical heterogeneity and, more importantly, assessment of the reasons for heterogeneity (if present)? Note: sensitivity and specificity depend on the situation in which the test is being used and the thresholds that have been set, and sensitivity and specificity are correlated; therefore, the use of heterogeneity statistics (p- values; I2) is problematic, and rather than testing whether heterogeneity is present, the reasons for heterogeneity should be examined. |
|
|
|
|
|
andMRI-pathway. A 3 TeslaMRI machine (Magnetron, Siemens) with T2, DWI and DCE sequences was used. The PI-RADS version 2, Likert 1-5 score was used, with threshold ≥ 3 for positivity E: index test: MRI only, a 1.5 Tesla (MR450) or a 3 Tesla (Discovery MR750 HDx) machine of GE Healthcare was used with T2, DWI and DCE sequences. The PI- RADS version 1 (until 2015) and version 2 (onwards) with a Likert 1-5 score were used, with threshold ≥ 3 for positivity. Transperineal software fusion MRI- TBx cores were taken (BiopSee system, Medcom) of every suspicious lesion, followed by template Bx. However, MRI-TBx |
median of 24 (IQR 23- 27) cores, independent of MRI F: Reference standard: 24-36 volume-based transperineal biopsieswere taken according to theGinsburg protocol,without resamplingMRI-TBx trajectories, using the Biopsee system.MRI- TBx were taken prior to the template biopsies G: Reference standard: transperineal template saturation prostate biopsies were taken according to the 20 Barzell zones (median 40 cores), not blinded for MRI results H: Reference standard: transperineal TSB with a median of 28 cores (range 26-32) including 4-6 cores in the transition and anterior zone. MRI results were not blinded during Bx procedure |
|
|
|
|
|
|
|
|
results were not reported separately F: MRI only + MRI- TBx + MRI-pathway. A 3 Tesla machine (Magnetom, Siemens) was used with T1, T2, DWI and DCE sequences. The PI- RADS version 1, Likert 1-5 scale was used, with threshold≥ 3 for positivity andMRI- TBx. Software fusion transperinealMRI-TBx were taken of all index lesions independently of the TOP-Bx, using the BiopSee MRI-TRUS fusion platform (Medcom) G: MRI only,MRI-TBx andMRI-pathway. A 1.5 or 3 TeslaMRI (MR450, GE healthcare) were used, with T1, T2 and DWI. A PI- RADS version 1 adapted sum score 1- 10 was used, with a score < 6 = no suspicion, 6 = low suspicion, 7-8 = |
|
|
|
|
|
|
|
|
|
intermediate suspicion and 9-10 = high suspicion, with threshold ≥ 6 for positivity andMRI- TBx. Transperineal software fusedMRI- TBx were taken of all positive lesions, using the Biopsee system (Medcom), prior to the Ginsburg- Bx H: MRI only, MRI-TBx and MRI-pathway. A 3 Tesla MRI (Achieva, Philips) was used, with T2, DWI, DCE and spectroscopy sequences. An in- house binary MRI score was used, with positive lesions cognitively targeted by MRI-TBx, after the performance of saturation Bx |
|
|
|
|
|
*comparator test equals the C of the PICO; two or more index/ comparator tests may be compared; note that a comparator test is not the same as a reference test (golden standard)
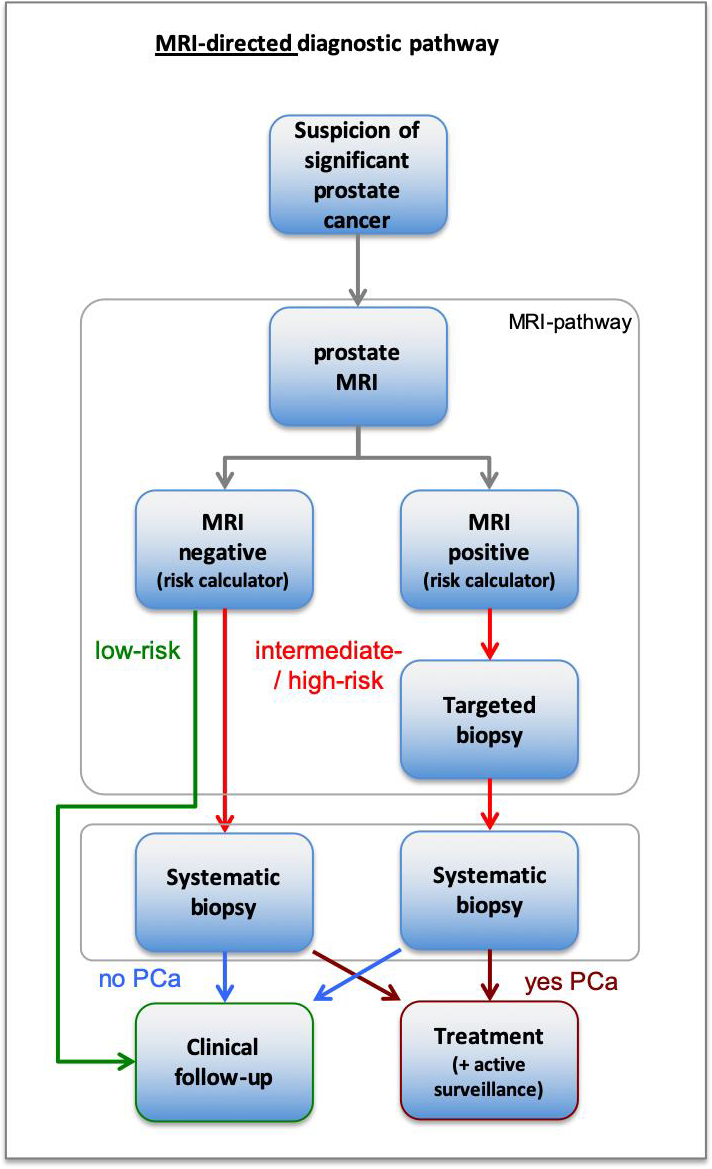
Figuur 2: Flowchart ter illustratie van de MRI-geleide prostaatkanker diagnostiek. Deze visualisatie is illustratief en dient niet als vervanging van de aanbevelingen. Lees altijd de overwegingen en aanbevelingen voor nuances, eventuele afwijkende situaties en extra achtergrondinformatie.
Table of quality assessment for systematic reviews of RCTs and observational studies
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Drost, 2019 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
YEs |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example, funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Beoordelingsdatum en geldigheid
Publicatiedatum : 18-12-2019
Beoordeeld op geldigheid : 30-01-2020
Bij het opstellen van de module heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodule komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
|
Module1 |
Regiehouder(s )2 |
Jaar van autorisati e |
Eerstvolgend e beoordeling actualiteit Richtlijn3 |
Frequentie van beoordelin g op Actualiteit4 |
Wie houdt er toezicht op actualiteit 5 |
Relevante factoren voor wijzigingen in aanbeveling6 |
|
Diagnostisch e prostaat MRI |
NVU |
2019 |
2024 |
Modulair onderhoud |
NVU |
Nieuwe wetenschappelijk e evidentie, veranderingen in de praktijk. |
1 Naam van de module
2 Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
3 Maximaal na vijf jaar
4 (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
5 regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
6 Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Patiënten participatie bij deze richtlijn werd medegefinancierd uit de Stichting Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Werkgroep
- Dr. T.M. de Reijke, uroloog, werkzaam in het Amsterdam Universitair Medische Centra, locatie AMC, NVU, voorzitter
- Prof. dr. J.O. Barentsz, radioloog, werkzaam in het RadboudUMC, NVvR
- Drs. J.L.L.M. Coenen, internist-oncoloog, werkzaam bij Isala, NIV
- Dhr. R. van der Giessen, patiënten vertegenwoordiger, Prostaatkankerstichting
- Prof. dr. J.A. Gietema, internist-oncoloog, werkzaam in het Universitair Medisch Centrum Groningen, NIV
- Prof. dr. L. Incrocci, radiotherapeut-oncoloog, werkzaam in het Erasmus Medisch centrum, NVRO
- Dr. M.J.R. Janssen, nucleair geneeskundige, werkzaam in het RadboudUMC, NVNG
- Dr. G.J.L.H. van Leenders, patholoog, werkzaam in het Erasmus Medisch Centrum, NVvP
- Prof. dr. R.J.A. van Moorselaar, uroloog, werkzaam in het Amsterdam Universitair Medische Centra, locatie VUmc, NVU
- Drs. H. Niekus, patiënten vertegenwoordiger, Prostaatkankerstichting
- Dr. I. van Oort, uroloog, werkzaam bij het RadboudUMC, NVU
- Dr. I. Schoots, radioloog, werkzaam bij het Erasmus MC, NVvR
- C. Tillier, verpleegkundig specialist urologie, V&VN
- Drs. H.A.M. Vanhauten, werkzaam in het Universitair Medisch Centrum Groningen, radiotherapeut-oncoloog, NVRO
- Dr. E. Vegt, nucleair geneeskundige, werkzaam in het Antoni van Leeuwenhoek ziekenhuis, NVNG
Met ondersteuning van:
- Dr. I. Mostovaya, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. W.J. Harmsen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
de Reijke |
Uroloog, Amsterdam UMC, locatie AMC |
Geen |
AMGEN, Ferring, Astellas, Janssen |
Geen actie |
|
van Leenders |
Patholoog, Erasmus MC, Rotterdam |
Geen |
Consulent Roche (betaald) |
Geen actie |
|
Van Oort |
Uroloog, RadboudUMC Nijmegen |
Geen |
Astellas, Janssen, Bayer, Sanofi, Mdxhealth |
Geen actie |
|
Vegt |
Nucleair geneeskundige NKI- AVL, Amsterdam |
Geen |
Geen |
Geen actie |
|
Coenen |
Internist, medisch oncoloog Isala, Zwolle |
Lid adviesraad cabazitaxel; Sanofi (betaald 1x / jaar) |
- |
Geen actie |
|
Tillier |
Verpleegkundig Specialist Urologie, NKI-AVL, Amsterdam |
Geen |
Geen |
Geen actie |
|
van Moorselaar |
Uroloog, Amsterdam UMC, locatie VUmc |
Geen |
adviescommissie: Astellas, Bayer, Janssen, Sanofi |
Geen actie |
|
Barentsz |
radioloog, RadboudUMC Nijmegen |
Geen |
- |
Geen actie |
|
Gietema |
Internist-oncoloog Universitair Medisch Centrum Groningen |
Geen |
Geen |
Geen actie |
|
Niekus |
Patiënt/Donateur PKS/lid kwaliteitscommissie PKS |
Geen |
Kapitaal in belegginsdossier in allerlei regio's. |
Geen actie |
|
Schoots |
Radioloog ErasmusMC, Rotterdam |
Geen |
Geen |
Geen actie |
|
Incrocci |
Radiotherapeut, ErasmusMC, Rotterdam |
Geen |
Geen |
Geen actie |
|
Vanhauten |
Radiotherapeut, UMC Groningen. |
Geen |
2017 spreker diversen nascholing < 10 uur op jaarbasis, vergoeding en onkostenvergoeding |
Geen actie |
|
Giessen |
Gepensioneerd. Geen bestaand dienstverband. |
Als vrijwilliger lid van: Kwaliteitscommissie ProstaatKankerStichting (PKS) Geneesmiddelencommissie NFK Onbetaalde functies |
Uitkomst richtlijnen kan geen financieel voordeel opleveren. In bezit: beperkt aantal aandelen Novartis ( geen speler in PC) |
Geen actie |
|
Janssen |
Nucleair geneeskundige, RadboudUMC Nijmegen |
-Lid onderwijscommissie NVvR, onbetaald |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door een afgevaardigde van een patiëntenvereniging, de ProstaatKankerStichting, in de werkgroep te laten participeren.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze module is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap- voor-stap beschrijving hoe een evidence-based module tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit de inventarisatie van de knelpunten door werkgroep/commissie Prostaatcarcinoom van de NVU (2017) bleek dat er een noodzaak was voor (revisie) van deze richtlijnmodule.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse is door de werkgroepleden en de adviseur een uitgangsvraag opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad Zoekverantwoording voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration:
- AMSTAR – voor systematische reviews.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Indien van toepassing: bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor: Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij één van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en welke worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE- methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de module is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die een randvoorwaarde zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur).
Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Kennislacunes
Tijdens de ontwikkeling van deze module is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de bijlage Kennislacunes. Deze bijlage is te vinden onder de aanverwante producten.
Commentaar- en autorisatiefase
De conceptmodule werd aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve module werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut via: secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit.https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html2012.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbo ok.html. 2013.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
