Chirurgische behandeling van rectum prolaps
Uitgangsvraag
- Wat is de optimale chirurgische correctie van een externe rectale prolaps?
- Wat is de optimale chirurgische correctie van een interne rectale prolaps?
Aanbeveling
Een laparoscopische ventrale rectopexie (LVR) is de eerste keus voor behandeling van een externe of interne rectum prolaps
Als een laparoscopische benadering gecontraïndiceerd is verdient de perineale benadering (de Delorme of Altemeier procedure met levatorplastiek) onder loco-regionale anesthesie de voorkeur.
Het verdient aanbeveling een patiënt met een anterieure rectocèle in combinatie met obstructief defecatie syndroom klachten te behandelen met een STARR of een LVR.
Overwegingen
Uitgangsvraag 1: Wat is de optimale chirurgische correctie van een externe rectale prolaps?
Vergelijkende studies behandeling externe rectum prolaps
Laparotomische versus laparoscopische benadering
Een grote meta-analyse met 467 patiënten en een Cochrane review tonen aan dat er geen verschil in recidieven of verbetering van functionele klachten tussen de laparotomische en laparoscopische rectopexie is. De studie van de Hoog (2009) bevestigt dit op functioneel gebied maar niet wat betreft het aantal recidieven (20 vs. 2%). Een verklaring hiervoor kan zijn dat er binnen de laparoscopie groep verschillende technieken en materialen zijn gebruikt. Zo werd bijvoorbeeld een deel geopereerd volgens de procedure van Wells (Wells 1959) en een deel volgens de techniek van D’Hoore (D’hoore 2006). De learning curve zou in deze studie ook een rol kunnen hebben gespeeld.
Aangezien de studie van de Hoog hierbij ook een zeer klein aantal patiënten behandeld met de laparoscopische benadering (n=15) beschrijft, in tegenstelling tot beide andere studies, is uiteindelijk is voor de bovenstaande conclusie gekozen. Omdat er nauwelijks verschillen bestaan in recidieven en functionele uitkomsten en omdat de laparoscopische benadering minder complicaties genereert geniet deze techniek de voorkeur bij ERP. Een bijkomend voordeel zijn de lagere kosten en het verschil in cosmetisch effect voor de patiënt.
Laparotomischeversus perineale benadering
Aangezien perineale ingrepen minder belastend zijn voor de patiënt en daarom worden voorbehouden aan patiënten met meer comorbiditeiten ligt het feit dat perineale ingrepen met minder postoperatieve complicaties zijn geassocieerd voor de hand. Zeker bij een resectie rectopexie waarbij een anastomose wordt aangelegd zijn complicaties te verwachten. De perineale benadering is echter ook geassocieerd met een hoger recidief en postoperatieve fecale incontinentie percentage. Deze conclusie is echter getrokken uit de enige, kleine (n=20) studie die er is. Bij het interpreteren van deze conclusie moet hier dus ook rekening mee worden gehouden.
Recent onderzoek toont echter aan dat abdominale technieken tegenwoordig ook veilig zijn voor ouderen met een hoge comorbiditeit. Zodoende wordt bovenstaande stelling langzaamaan meer verlaten (Mustain 2013, Lee 2011, Wijffels 2011, Fang 2012). Per patiënt zal moeten worden afgewogen of algehele anesthesie een optie is, maar (oudere) patiënten met veel comorbiditeiten hoeven niet per se perineaal geopereerd te worden. In vergelijking met laparotomische benadering geniet de perineale benadering echter wel de voorkeur bij (oudere) patiënten met veel comorbiditeiten. Over het algemeen kan gesteld worden dat de abdominale benadering betere uitkomsten wat betreft functionaliteit en recidieven heeft (zie verder richtlijn). Deze benadering krijgt dan ook de voorkeur bij jongere en gezonde patiënten. Als een intra-abdominale ingreep verantwoord is, krijgt deze dus de voorkeur.
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie
Een van de standaard stappen tijdens een rectopexie is de mobilisatie van het rectum. Er zijn in het verleden veel verschillende varianten van deze mobilisatie beschreven. Zo kan er alleen ventraal, alleen dorsaal, posterolateraal of 360 graden rondom gemobiliseerd worden. Bij veel van deze technieken worden de laterale ligamenten gekliefd. Het mag duidelijk zijn dat aan de uitkomsten van de Cochrane review betreffende deze stelling zowel voor- als nadelen zitten. De werkgroep heeft echter in de aanbeveling gekozen voor het behouden van de laterale ligamenten om de volgende redenen. Ten eerste is het klieven een onomkeerbaar proces. De verhoogde postoperatieve obstipatie wordt geweten aan de autonome rectale zenuwen die worden doorgenomen met het klieven van de laterale ligamenten. Dit kan niet meer hersteld worden. Een recidief is weliswaar erg vervelend maar kan vaak wel met een nieuwe ingreep verholpen worden. Ten tweede is veel gebeurd sinds de artikelen, waar de Cochrane review aan refereert, gepubliceerd zijn. Tegenwoordig zijn nagenoeg alle ingrepen aan de ERP in de Westerse wereld laparoscopisch en worden gelijke recidief percentages vermeld tussen technieken met en zonder posterolaterale mobilisatie. Het probleem van postoperatieve obstipatie na het klieven van de laterale ligamenten blijft echter. Om deze redenen denkt de werkgroep dat het behouden van de laterale ligamenten belangrijk is. Overigens moet ook bij dit punt rekening worden gehouden met het geringe bewijs; hoewel het drie goede vergelijkende studies betrof waren de aantallen klein.
Resectie versus geen resectie bij laparotomische rectopexie
Het bewijs voor deze onderzoeksvraag bestaat uit twee kleine trials (totaal n=48) waarvan er maar een (n=30) complicaties vermeldt. Hierbij vergelijkt een trial resectie rectopexie met mesh rectopexie en de andere trial resectie rectopexie met suture rectopexie. Zodoende zijn het dus twee trials die niet precies hetzelfde vergelijken. In combinatie met de lage patiënt getallen kan de conclusie worden getrokken dat het bewijs mager is. Desalniettemin kan wel een voorzichtige en niet onlogische afleiding worden gemaakt. Het feit dat resectie rectopexie beter is voor het reduceren van postoperatieve obstipatie is voor te stellen. Met het reseceren van het rectosigmoid wordt de knik in het distale colon opgeheven. Sommige chirurgen beschouwen dit stuk darm als een deel die zijn functie door de verzakking verloren heeft en dus als overtollig (‘redundant’) te beschouwen is (Stevenson 1998, via Caddedu). Het verwijderen hiervan zou kunnen leiden tot minder postoperatieve obstipatie, zoals deze twee trials doen vermoeden. Wanneer preoperatief de obstipatie op de voorgrond staat kan men een resectie rectopexie overwegen. Ondanks dit voordeel lijken er ook wat serieuze nadelen aan de resectie rectopexie te kleven. Zowel in de Cochrane review van Tou als in de studie van Fleming (N = 1275) kwamen er meer postoperatieve complicaties voor in de resectie groep. Dit is voor te stellen aangezien er met de resectie van het rectosigmoid een anastomose wordt aangelegd met alle risico’s van dien. Dit is een belangrijk punt in de overweging een patiënt een resectie aan te bieden. Bij een (oudere) patiënt met veel comorbiditeiten lijkt een resectie niet aangewezen. Bovendien moet een patiënt langer herstellen van een resectie dan wanneer deze niet wordt toegepast. De opnameduur zou langer zijn en daarmee de kosten hoger. Dit zijn allemaal overwegingen die er toe kunnen leiden niet voor een resectie te kiezen. Hiernaast zijn er aanwijzingen dat het postoperatieve fecale incontinentie percentage hoger is in de resectie groep. Dit is echter niet significant en zou dus in grotere trials verder uitgezocht moeten worden. Dit zou in de huidige praktijk echter eerder een vergelijke studie van LVR vs. LRR zijn.
Rectopexie versus geen rectopexie
Uit de enige geïncludeerde studie die deze vraag onderzoekt blijkt het bewijs duidelijk dat het toevoegen van een rectopexie, open of laparoscopisch, de kans op een recidief (1.5 vs. 8.6%) vermindert. Deze uitkomst is begrijpelijk. Met een rectopexie bevestigt de operateur het rectum met het promotorium en wordt zodoende de verzakking tegengegaan. De rectopexie is een hoeksteen in de behandeling van de ERP. Het wekt dan ook geen verbazing dat het uitvoeren van de rectopexie naast de gebruikelijke mobilisatie van het rectum leidt tot een lager recidief percentage. Hierbij moet wel vermeld worden dat in de studie bij de patiënten met preoperatieve obstipatie klachten een bijkomende rectosigmoid resectie werd uitgevoerd. Er is echter niet bekend (zie ook stelling hierboven) dat er een verschil bestaat in voorkomen van recidieven tussen resectie en geen resectie, dus vermoedelijk kan dit feit genegeerd worden. Wat echter wel voor een verstoring van het resultaat kan leiden zijn de verschillende gradaties, preoperatief door de chirurg bepaald, van mobilisatie die worden gebruikt. Het is bekend dat verschil in mobilisatie kan leiden tot verschillende recidief percentages in de laparotomische setting (zie behoud versus klieven). Al met al is de werkgroep van mening dat het raadzaam is een rectopexie toe te voegen aan de mobilisatie in het geval van een ERP.
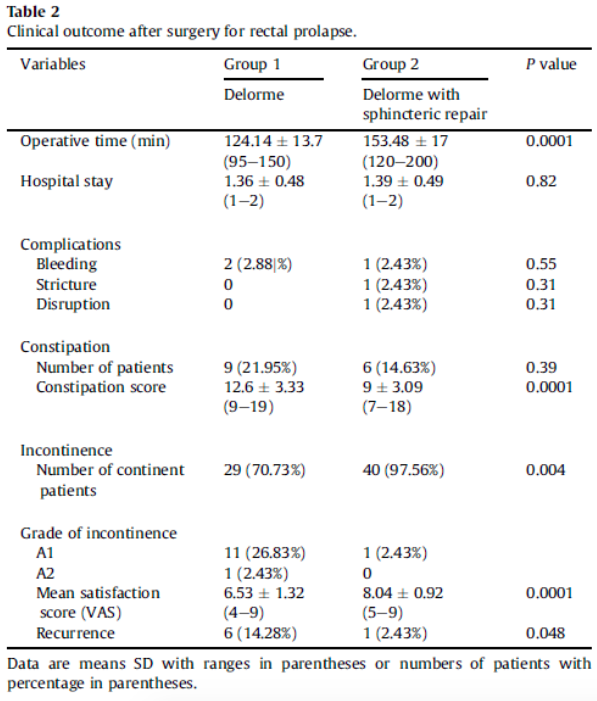
Delorme versus Delorme met levatorplastiek
Het toevoegen van een levatorplastiek aan de klassieke Delorme lijkt waardevol. Zonder verschil in complicaties maar met een betere score op functioneel gebied en in het aantal gereduceerde recidieven lijkt de additionele waarde van de levatorplastiek groot te zijn. Wanneer een Delorme procedure wordt overwogen voor de behandeling van een ERP acht de werkgroep het zinvol een levatorplastiek toe te voegen.
Altemeier versus Altemeier met levatorplastiek
Het combineren van een procedure van Altemeier met een levatorplastiek geeft veel betere resultaten dan wanneer een losse conventionele Altemeier wordt uitgevoerd. Het lijkt de werkgroep dan ook waardevol om een levatorplastiek aan de Altemeier procedure toe te voegen wanneer dit voor de behandeling van een RP wordt overwogen.
Beschrijvende studies behandeling externe rectum prolaps
Laparoscopische rectopexie
In de literatuur worden veel verschillende varianten van laparoscopische rectopexie voor de behandeling van ERP beschreven waarbij vooral de uitgebreidheid van de mobilisatie van het rectum en de plaatsing van de mat varieert. In deze richtlijn is gekozen voor, in de afwezigheid van vergelijkend onderzoek, een tweetal reviews welke de meest beschreven laparoscopische rectopexiën behandelen. De meest gebruikte techniek in Nederland is de LVR waarbij het rectum alleen ventraal wordt gemobiliseerd en de mat aan de ventrale zijde van het rectum wordt bevestigd, hiermee de laterale autonome zenuwen sparend.
In de review van Smaranayake worden de resultaten van de LVR, in de regel zonder posterieure mobilisatie, en de ventrale rectopexie (laparotomisch en laparascopisch) met posterieure mobilisatie beschreven. Beide technieken overleggen goede functionele uitkomsten maar de LVR noteerde een veel betere uitkomst wat betreft obstipatie met een gemiddelde reductie van 40.3 vs. 6.1%. Hiernaast kwam obstipatie de novo vele malen vaker voor in de groep met posterieure mobilisatie. Beide uitkomsten worden gewijd aan het klieven versus het behouden van de laterale ligamenten. Scores betreffende fecale incontinentie en complicatie percentages waren gelijkwaardig. Als laatste valt op dat het recidief percentage bij beide technieken acceptabel is, met een klein voordeel ten faveure van VRMPM. De review van Caddedu includeerde 3 studies betreffende LVR waarvan er 2 ook in de review van Smaranayake beschreven worden. De derde studie noteerde een recidief percentage van 2.75%, andere waarden werden niet genoemd.
Bij de laparoscopische Orr-Loygue rectopexie wordt het rectum zowel ventraal als posterieur gemobiliseerd met een ventrale plaatsing van de mat. Bij de posterieure benadering wordt het rectum alleen van deze zijde gemobiliseerd en wordt hier de mat geplaatst. Over het algemeen rapporteren alle studies betreffende alle verschillende technieken een verbetering van functionele klachten (met uitzondering van de posterieure benadering betreffende obstipatie) en acceptabele recidief en complicatie percentages. Wanneer men de technieken probeert te vergelijken noteren alle vier min of meer dezelfde uitkomst wat betreft fecale incontinentie. Echter met gemiddeld 40.3% reductie van de obstipatie klachten en slechts 5.5 tot 10.5% obstipatie de novo lijkt de LVR een voordeel te hebben ten opzichte van de andere technieken. De Orr-Loygue techniek toont gemiddeld 33% verbetering betreffende obstipatie klachten maar er viel ook in 3 van de 5 studies een gemiddelde van 46% aan obstipatie de novo te noteren. De posterieure benadering scoort erg slecht op obstipatie als uitkomst. De posterieure bandering scoorde wel het laagste recidief percentage met 1.7% (vs. 4.2% voor Orr-Loygue en 4.9% voor LVR, de 2 reviews gecombineerd). Hierbij moet de kortere follow-up duur wel in acht worden genomen (24 vs. 46 vs. 43 maanden). Complicaties worden door Caddedu et al. helaas niet beschreven. Voor de LVR werd een acceptabel complicatie percentage gevonden
(4.8 - 38.5%, gem. 19.2%), net als voor de ventrale rectopexie met posterieure mobilisatie (1.4 – 46.9%, gem. 19.4% (Smaranayake 2010). Een bijkomend voordeel van de LVR is dat deze ingreep gecombineerd kan worden met een abdominale gynaecologische ingreep; een gecombineerde verzakking komt immers vaak voor. De LVR is zodoende goed te combineren met een laparoscopische sarcocolpopexie, uitgevoerd door de gynaecoloog. De werkgroep acht het raadzaam om dergelijke operaties waar mogelijk gecombineerd uit te voeren.
Hoewel er geen vergelijkende studies bestaan tussen de verschillende laparoscopische rectopexiën, kan uit de bovenstaande reviews voorzichtig de conclusie worden getrokken dat op het gebied van functionele uitkomst de LVR superieur lijkt te zijn aan de ventrale rectopexie met posterieure mobilisatie, de laparoscopische Orr-Loygue rectopexie en de laparoscopische posterieure benadering. Het recidief percentage van de LVR is echter hoger dan de voornoemde technieken. De werkgroep geeft in deze de voorkeur aan de LVR. Bij de andere technieken richt men vaak schade aan de autonome zenuwen van het rectum aan, resulterend in een motiliteitsprobleem. Eventuele beschadigingen hieraan zijn niet meer te herstellen, wat een eventueel recidief wel is, hoe vervelend ook voor de patiënt. De LVR heeft in grote series aangetoond effectief en veilig te zijn en een acceptabel recidief percentage te hebben.
Wel dient aangetekend te worden dat de werkgroep voor onomstotelijk bewijs meer vergelijkend onderzoek nodig acht.
Laparoscopische resectie rectopexie
Bij de LRR wordt het rectum alleen ventraal gemobiliseerd en met hechtingen aan het promotorium bevestigd. Vanwege het risico op lekkage wordt er geen mat ingehecht. Dit heeft tot gevolg dat er geen varianten van deze techniek zijn beschreven. Uit de review van Caddedu komt naar voren dat de LRR goede functionele resultaten, een gemiddeld complicatie percentage van 15.4% en een recidief percentage van 0% laat zien. Hieruit kan geconcludeerd worden dat de LRR een adequate chirurgische behandeling voor ERP is. De behandelend arts moet zich echter wel realiseren dat bij de LRR een darm anastomose wordt aangelegd, met de risico’s van dien. De artikelen uit dit review laten een lekkage percentage van 1.6% (4/244) zien. Hierbij dient gerealiseerd te worden dat de opnameduur langer is bij een resectie dan wanneer deze niet wordt uitgevoerd en dat hier kosten aan verbonden zijn. Wanneer LRR met LVR wordt vergeleken valt op dat de LRR betere incontinentie scores en een duidelijk lager recidief percentage toont. Hierbij wordt wel aandacht gevraagd voor de gemiddeld kortere follow-up duur van de LRR (28.5 vs. 46 maanden). Verbetering in obstipatie, voorkomen van functionele klachten de novo en complicatie percentage zijn te vergelijken tussen de twee technieken.
Zo moet men dus de risico’s van de anastomose van LRR en de langere opnameduur afwegen tegen het schijnbaar betere effect op de incontinentie en het minder voorkomen van recidieven, wanneer vergeleken met de LVR. De werkgroep geeft de voorkeur aan LVR bij ERP.
Delorme procedure
Over de Delorme procedure, een van de twee meest gebruikte perineale benaderingen, wordt een goede functionele verbetering gerapporteerd in de enige geïncludeerde en beschrijvende studie. Het complicatie percentage is acceptabel. Het aantal recidieven is echter hoog, zeker wanneer dit vergeleken wordt met de abdominale technieken. Het complicatie percentage is iets hoger maar wel te vergelijken met de abdominale technieken. Het voordeel van de perineale techniek is dat de patiënt niet onder algehele anesthesie gebracht hoeft te worden. Bij (oudere) patiënten met veel comorbiditeiten waarbij dit een rol kan spelen is de Delorme procedure een uitkomst.
Altemeier procedure
De andere vaak gebruikte perineale benadering, de Altemeier procedure, laat lagere (gemiddelde) recidief en morbiditeit percentages zien in vergelijking met de Delorme. Ook vergeleken met de abdominale techniek laat de Altemeier een lager gemiddeld morbiditeit percentage zien. Er zijn echter wel veel meer recidieven te noteren bij de perineale techniek. De functionaliteit verbeterde significant na de Altemeier, maar indien vergeleken met de abdominale procedures kwamen deze laatste er beter uit. Het lijkt erop dat ook deze perineale procedure effectief is maar ondergeschikt is aan de abdominale technieken. Zodoende kan de Altemeier een rol spelen bij (oudere) patiënten met veel comorbiditeiten. Bij jongere, fitte patiënten is een abdominale procedure echter aangewezen.
Uitgangsvraag 2: Wat is de optimale chirurgische correctie van een interne rectale prolaps?
Vergelijkende studies behandeling interne rectum prolaps of rectocele (met of zonder enterocele)
Laparotomische versus laparoscopische resectie rectopexie voor interne rectum prolaps
De enige geïncludeerde studie laat duidelijk geen verschil in complicaties en postoperatieve obstipatie klachten zien tussen laparotomische en laparoscopische resectie rectopexie. Hierbij is het belangrijk dat, in zowel open als laparoscopisch, het rectum zowel ventraal als posterieur gemobiliseerd was. Er wordt beschreven dat de ‘meeste’ laterale ligamenten behouden worden. Hoewel de vergelijking laparotomische versus laparoscopische resectie rectopexie voor een IRP maar in één studie is onderzocht, is de uitslag bemoedigend en in lijn met de vergelijking laparotomische versus laparoscopische benadering voor ERP. Ook hier zal gelden dat de laparoscopische benadering goedkoper zal zijn, vooral door de kortere opnameduur. Ook zal de patient de voorkeur geven aan de minder invasieve benadering via laparoscopie die tevens een mooier cosmetisch resultaat oplevenrt. Een laparoscopische benadering geniet dan ook de voorkeur. Mits de techniek goed wordt beheerst door de operateur uiteraard.
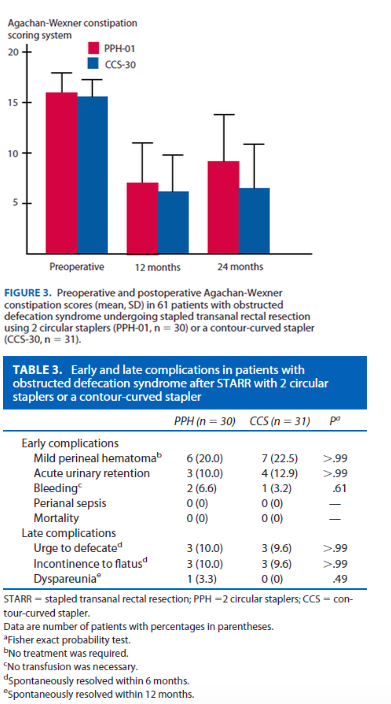
STARR versus conservatieve behandeling
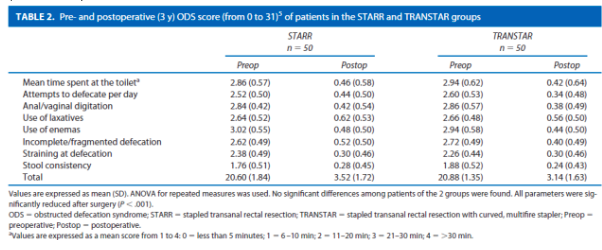
Wanneer een rectocele en/of IRP symptomatisch wordt kan chirurgie overwogen worden. STARR is een veel gebruikte operatie bij een rectocele en/of IRP in combinatie met ODS klachten. De studie geeft weer dat zowel STARR als bekkenfysiotherapie nuttig zijn bij deze groep patiënten. De STARR geeft echter betere resultaten in ODS klachten reductie. Dat bij STARR meer adverse events plaatsvonden was te verwachten. De morbiditeit viel echter mee, maar 1 ernstige complicatie waarvoor re-interventie (nabloeding) nodig was. Desalniettemin moet de behandelaar rekening houden met de mogelijke adverse events van de STARR in de keuze voor de behandeling. De werkgroep vindt het dan ook aan te bevelen bij patiënten met een kleine rectocele en/of een laaggradige IRP en ODS klachten eerst te beginnen met bekkenfysiotherapie. Wanneer de patiënt hiermee niet uit komt kan een operatie worden overwogen. Dit zou ook voor oudere patiënten met veel comorbiditeit een goede strategie zijn.
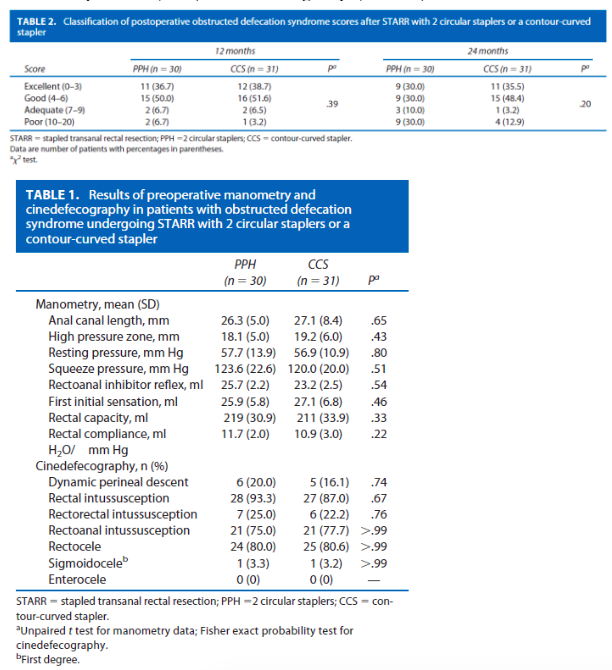
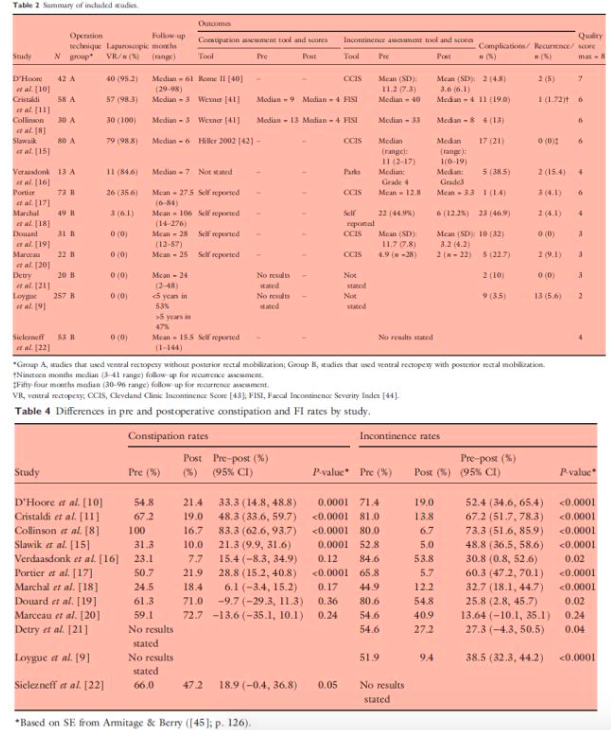
Double-stapling (PPH) STARR versus Countour Transtar
Hoewel de resultaten van de Double-stapling (PPH) STARR en de Countour Transtar (CT) staplers voor de behandeling van patiënten met ODS klachten in combinatie met een rectocele en/of IRP niet veel verschillen lijkt het er op dat de CT op de lange termijn superieur is.
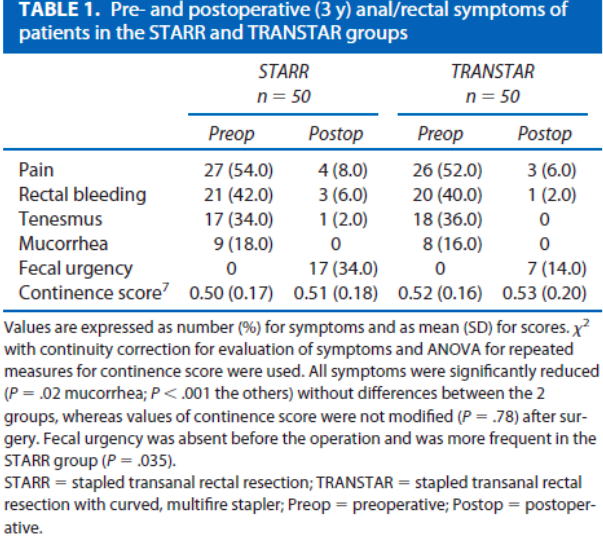
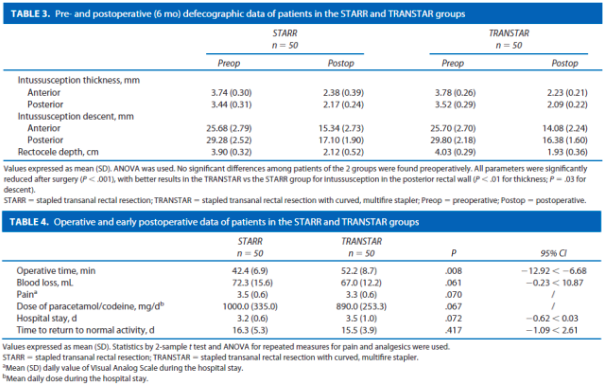
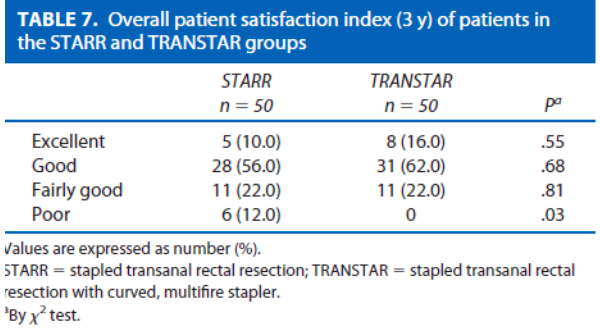
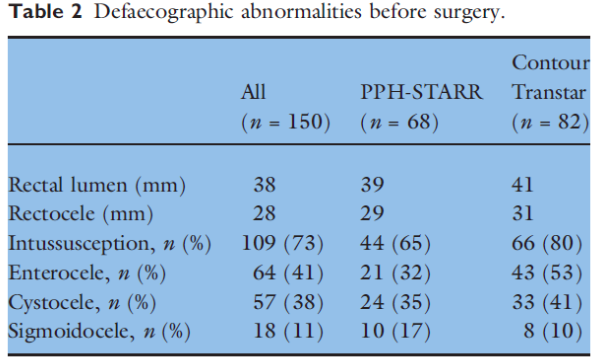
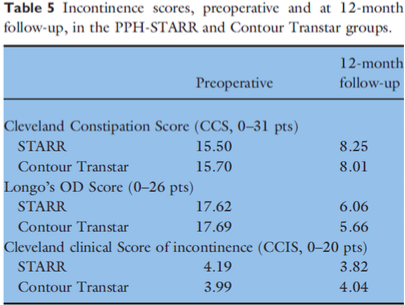
De onderzoeken van Isbert en Renzi laten geen verschillen in functionele uitkomst zien na 12 maanden. Renzi et al. beschrijft een minieme verbetering ten faveure van de CT na 24 maanden. In het cohort van Boccasanta, met een follow-up duur van 36 maanden, worden minimale functionele verschillen beschreven. In dit zelfde cohort komen klachten van fecale drang echter wel meer dan twee keer zo vaak voor in de STARR groep. Hierbij kampt van de STARR groep 12% na 3 jaar met een recidief, wat veel is in vergelijking met de 0% van de CT groep. Het lijkt alsof er vanaf 12 maanden (Renzi en Boccasanta) een verschil gemaakt wordt. Hieruit kan men concluderen dat het lijkt alsof de CT een voordelig effect heeft ten opzichte van de STARR wanneer met kijkt naar de lange termijn. Postoperatieve complicaties waren in alle drie de studies nagenoeg gelijk.
Naast het functionele aspect heeft de CT een aantal technische voordelen. Het heeft een groter reservoir dan de STARR zodoende kan er meer weefsel worden gereseceerd. Hierbij kan de CT een volledige circumferentiële resectie in een shot uitvoeren, in tegenstelling tot de PPH stapler waarbij het apparaat één maal voor de anterieure en één maal voor de posterieure zijde moet worden afgevuurd. Bij de PPH techniek blijven er vaak laterale flapjes weefsel over welke een bloeding, pijn of een partiële obstructie kunnen veroorzaken. Hiernaast heeft de CT als voordeel dat het zicht op het te reseceren weefsel veel beter is. In de literatuur wordt ook wel beschreven dat het afvuren van de PPH stapler blind gebeurd met het risico op een perforatie. Als laatste moet rekening worden gehouden met het feit dat de CT duurder is dan de conventionele STARR. Concluderend stelt de werkgroep dat door de minimale voordelen op functioneel gebied, het lagere recidief percentage en de technische voordelen de CT de voorkeur geniet boven de conventionele double stapling (PPH) STARR.
Beschrijvende studies behandeling interne rectum prolaps of rectocele met of zonder enterocele)
Laparoscopische ventrale rectopexie voor interne rectum prolaps
De twee geselecteerde studies beschrijven een positief effect van de LVR op de functionele uitkomst en goede complicatie en recidief percentages worden gerapporteerd. Na studies waarin LVR zich bewees als een goede chirurgische behandeling voor ERP volgden er steeds meer studies die hetzelfde bewijzen voor een IRP. De LVR is vooral geïndiceerd bij patiënten met een symptomatische high-grade IRP (graad 3 of 4 volgens de Oxford classificatie). Dit wordt bevestigd door een panel van experts in een recent ‘consensus’ artikel. Het panel stelt ook dat de LVR een goede chirurgische behandeling is voor de symptomatische complexe rectocele van meer dan 3-4 centimeter, doorgaans vergezeld door een hooggradige IRP en een enterocele. Bij patiënten met dergelijke problematiek kan altijd eerst biofeedback therapie geprobeerd worden, zo stelt ook het panel (Mercer-Jones, 2014).
Hoewel de LVR als indicatie voor IRP niet in vergelijkende studies is uitgezocht acht de werkgroep de LVR adequaat om patiënten die lijden aan een symptomatische IRP te helpen. Meer vergelijkend onderzoek is echter nodig om deze stelling te onderbouwen.
TRREMS (transanal repair of rectocele and rectal mucosectomy with a single circular stapler)
TRREMS is een techniek specifiek toepasbaar op patiënten met ODS klachten ten gevolge van een rectocele en een mucosa prolaps. Over deze techniek is enkel beschrijvend en geen vergelijkend onderzoek te vinden. In de enige beschrijvende studie opgenomen in deze richtlijn wordt een positief resultaat op de obstipatie en incontinentie gemeten middels gevalideerde scores. Tezamen met een acceptabel complicatie percentage lijkt het alsof deze techniek veilig en effectief is voor deze specifieke patiëntengroep. Echter het bewijs is marginaal. Meer bij voorkeur vergelijkende studies zouden moeten volgen om deze stelling kracht bij te zetten.
Algemeen
Alvorens de werkgroep haar aanbevelingen over de uitgangsvragen in deze module doet is het onderstaande van belang. Gedurende de zoektocht naar geschikt bewijs om beide uitgangsvragen te beantwoorden bleek al snel dat er weinig kwalitatief goed vergelijkend onderzoek beschikbaar was. Hierbij bleek het vergelijkende onderzoek vooral patiënten te betreffen die geopereerd waren middels een laparotomische rectopexie. Aangezien heden ten dage de laparotomische rectopexie nagenoeg niet meer in Nederland wordt uitgevoerd gaat het hier om zeer gedateerde onderzoeken. Tegenwoordig worden vrijwel alleen de laparoscopische benaderingen voor het opheffen van een RP uitgevoerd. De beweegredenen hiervoor zijn te vinden in de resultaten van de laparotomische onderzoekendie, ondersteund door losse laparoscopische series, geëxtrapoleerd worden naar de laparoscopische benadering. Zo werd het behoud versus klieven van de laterale ligamenten in de laparotomische setting onderzocht waaruit naar voren kwam dat behoud van de ligamenten de voorkeur geniet. Het review van Smaranayake laat hetzelfde resultaat zien wanneer losse laparoscopische series vergeleken worden.Hierbij werd er al lang geleden in meerdere vergelijkende studies bewezen dat de laparoscopische techniek superieur was aan de laparotomische benadering. Dit was vooral vanwege de mindere postoperatieve complicaties, lagere kosten en een verschil in het cosmetische effect. De aanbevelingen zullen daarom vooral voortkomen uit de uitkomsten van de laparotomische onderzoeken geëxtrapoleerd naar de laparoscopische benadering, op basis van losse beschrijvende series en de expert opinion van de werkgroep. Daarom raadt de werkgroep aan bij een ERP of IRP de LVR toe te passen. Eventueel kan de operateur bij een ERP voor een LRR kiezen, voornamelijk als preoperatief de obstipatie op de voorgrond staat. De LRR wordt echter nauwelijks uitgevoerd in Nederland. Het is algemeen bekend dat perineale procedures voor de behandeling van ERP inferieur zijn aan de abdominale benaderingen en dit is vooral te wijten aan het hogere recidief percentage. Er zijn voldoende aanwijzingen dat de abdominale technieken een betere functionele uitkomst hebben in vergelijking met de perineale benaderingen. Deze uitspraken zijn voornamelijk gebaseerd op losse, niet vergelijkende series. Een perineale ingreep onder loco-regionale anesthesie bij voorkeur gecombineerd met een levatorplastiek kan worden gekozen wanneer een laparoscopische benadering gecontraïndiceerd is.
Over de STARR procedure zijn veel goede recente vergelijkende onderzoeken beschikbaar. Voor rectocele met ODS klachten is vanuit chirurgisch perspectief een STARR of een LVR aangewezen. Helaas is er geen vergelijkend onderzoek tussen de twee behandelingen en op basis van ervaring kan de werkgroep geen voorkeur uitspreken. De werkgroep acht beide behandelingen adequaat voor patiënten met een symptomatische rectocele. De kundigheid en ervaring van de chirurg zullen bij de keuze voor een van de twee behandelingen leidend zijn.
Onderbouwing
De rectum prolaps (RP) kan worden onderverdeeld in een interne en een externe variant. De externe rectum prolaps (ERP) is een circumferentiële (‘full-thickness’) intussusceptie van de gehele rectumwand, die zich uitstrekt voorbij het anale kanaal. Van een interne rectum prolaps (IRP, ook wel intussusceptie genoemd) wordt gesproken wanneer deze intussusceptie zich boven het niveau van de anus (recto-recto of recto-anaal, zie aanverwacht 'Achtergrond informatie' voor gradaties RP) bevindt. RP en dan vooral de interne variant gaat vaak gepaard met andere verzakkingen van het posterieure compartiment zoals een rectocele of enterocele. Een RP moet niet verward worden met een mucosa prolaps, waarbij enkel het slijmvlies door de anus prolabeert. Een prolaps van het posterieure compartiment van de bekenbodem is geassocieerd met invaliderende klachten als obstipatie (obstructed defecation), fecale incontinentie en (chronische) pijn.
De behandeling van RP is conservatief of chirurgisch. Bij een IRP graad 1-2 wordt bekkenfysiotherapie voorgesteld; vanaf graad 3 wordt operatief ingrijpen aangeraden. Chirurgie is doorgaans gespitst op de onderliggende oorzaak. Heden ten dage wordt IRP graad 3-4 al dan niet in combinatie met een recto- of enterocele behandeld middels een laparoscopische ventrale rectopexie (LVR) of een stapled transanal rectal resection (STARR), waarvan veel verschillende varianten zijn beschreven. Voor de ERP wordt onderscheid gemaakt in perineale technieken, de Delorme- en Altemeier procedure, en abdominale technieken, verdeeld in laparoscopische rectopexie met of zonder resectie van het rectosigmoïd. Tot nu toe wordt perineale chirurgie vooral voorbehouden aan (oudere) patiënten met een hoge comorbiditeit aangezien deze procedure geen laparoscopie of laparotomie behoeft en vaak met behulp van locoregionale anesthesie kan worden uitgevoerd. Bij de operatie volgens Delorme wordt de prolaberende mucosa gestript en de spierlagen van de prolaps gepliceerd (Youssef 2013). Bij de techniek volgens Altemeier wordt de gehele prolapse full-thickness gereseceerd vanuit de perineale benadering (Ris 2012). De meest gebruikte abdominale technieken zijn LVR en laparoscopische resectie rectopexie (LRR). Bij beide technieken wordt het rectum alleen ventraal gemobiliseerd wat inhoudt dat de autonome zenuwen aan de laterale zijde worden gespaard. Bij de LVR wordt het ventrale rectum met een mat aan het promotorium bevestigd (D’Hoore 2006). Bij de LRR wordt het rectosigmoïd gereseceerd en vervolgens wordt het rectum met hechtingen (‘suture rectopexie’) aan het sacrum gefixeerd (Stevenson 1997). Met het reseceren van het rectosigmoïd wordt de knik in het distale colon opgeheven. De theorie is dat dit tot minder postoperatieve obstipatie leidt (Cadeddu 2012). Daartegenover staat het aanleggen van een anastomose met alle risico's van dien. Vanwege het risico op naadlekkage wordt geen mat gebruikt bij de LRR. De LRR en de suture rectopexie zijn de enige twee vormen van rectopexie waarbij geen mat gebruikt wordt. Bij alle overige varianten van rectopexie, zowel laparotomisch als laparoscopisch, wordt een mat gebruikt. Hoewel meer dan 100 verschillende technieken voor behandeling van RP zijn beschreven bestaan er weinig tot geen goede vergelijkende studies. Bewijs is veelal gebaseerd op losse series waarin een enkele techniek wordt beschreven. Vanwege dit feit is de richtlijn genoodzaakt betreffende dit onderwerp bewijs van dergelijke series te presenteren. In deze module worden alleen de operaties beschreven die heden ten dage vaak worden uitgevoerd en beschreven.
Uitgangsvraag 1: Wat is de optimale chirurgische correctie van een externe rectale prolaps?
|
Kwaliteit van bewijs: HOOG |
Laparotomisch versus laparoscopische rectopexie Over het algemeen zijn er geen verschillen in recidieven of verbetering van functionele klachten tussen de twee benaderingen in de behandeling van ERP. Hierbij genereert de laparoscopische benadering minder complicaties en is deze techniek goedkoper.
Cadeddu 2012, De Hoog 2009, Tou 2008 |
|
Kwaliteit van bewijs: MATIG |
Laparotomische versus perineale benadering Perineale ingrepen zijn geassocieerd met minder postoperatieve complicaties bij de behandeling van ERP. Er zijn aanwijzingen dat de perineale benadering meer recidieven en meer postoperatieve fecale incontinentie oplevert in vergelijking met de laparotomische benadering.
Fleming 2012, Tou 2008 |
|
Kwaliteit van bewijs: MATIG |
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie Bij de behandeling van ERP lijkt het klieven van de laterale ligamenten van het rectum tijdens de mobilisatie bij een laparotomische rectopexie geassocieerd te zijn met het ontwikkelen van minder recidieven maar meer postoperatieve obstipatie in vergelijking met het behouden van de laterale ligamenten.
Tou 2008 |
|
Kwaliteit van bewijs: MATIG |
Resectie versus geen resectie bij laparotomische rectopexie Er lijken aanwijzingen te zijn dat laparotomische resectie rectopexie beter is voor het reduceren van postoperatieve obstipatie bij de behandeling van ERP. Aan de andere kant lijkt laparotomische resectie rectopexie ook geassocieerd met een hoger (ernstig) complicatie percentage en verhoogde postoperatieve fecale incontinentie wanneer afgezet tegen een laparotomische rectopexie zonder rectosigmoid resectie.
Fleming 2012, Tou 2008 |
|
Kwaliteit van bewijs: MATIG |
Rectopexie versus geen rectopexie Het toevoegen van een rectopexie aan de mobilisatie van het rectum bij de behandeling van patiënten met een ERP verlaagt de kans op een recidief.
Karas 2011 |
|
Kwaliteit van bewijs: MATIG |
Delorme versus Delorme met levatorplastiek Er zijn aanwijzingen dat het toevoegen van een levatorplastiek aan de klassieke Delorme procedure voor de behandeling van ERP leidt tot een lager recidief percentage en grotere verbetering in functionele klachten dan een Delorme procedure alleen.
Youssef 2013 |
|
Kwaliteit van bewijs: ZEER LAAG |
Altemeier versus Altemeier met levatorplastiek De procedure van Altemeier gecombineerd met een levatorplastiek genereert betere functionele uitkomsten, minder complicaties en minder recidieven dan een conventionele Altemeier.
Chun 2004 |
|
Kwaliteit van bewijs: MATIG |
Laparoscopische rectopexie De LVR lijkt superieur te zijn aan de ventrale rectopexie met posterieure mobilisatie, de laparoscopische Orr-Loygue rectopexie en de laparoscopische posterieure benadering wat betreft functionele uitkomsten.
Caddedu 2012, Samaranayaka 2010 |
|
Kwaliteit van bewijs: ZEER LAAG |
Laparoscopische resectie rectopexie Voor behandeling van ERP laat de LRR goede functionele resultaten, een acceptabele complicatie en zeer lage recidief percentages zien.
Caddedu 2012 |
|
Kwaliteit van bewijs: LAAG |
Delorme en Altemeier procedure De Delorme en Altemeier zijn beide perineale technieken welke een goede functionele verbetering met een acceptabel complicatie percentage kunnen overleggen. Echter in vergelijking met de abdominale technieken komen beide perineale procedures slechter uit wat betreft recidieven en functionaliteit. Vanwege het voordeel dat de patiënt niet onder algehele anesthesie gebracht hoeft te worden bij de perineale benadering kunnen deze technieken een rol spelen bij (oudere) patiënten met veel comorbiditeiten.
Schiedeck 2005, Tsunoda 2003, Zbar 2002 |
Uitgangsvraag 2: Wat is de optimale chirurgische correctie van een interne rectale prolaps?
|
Kwaliteit van bewijs: ZEER LAAG |
Laparotomische versus laparoscopische resectie rectopexie Voor de behandeling van IRP lijkt er geen verschil te zijn tussen laparotomische en laparoscopische resectie rectopexie in termen van morbiditeit en postoperatieve obstipatie.
Johnson 2012 |
|
Kwaliteit van bewijs: MATIG |
STARR versus conservatieve behandeling Zowel STARR als bekkenfysiotherapie verbeteren ODS klachten bij patiënten met een rectocele en/of IRP. STARR genereert meer verbetering in de ODS klachten dan bekkenfysiotherapie maar is wel geassocieerd met een hogere morbiditeit.
Lehur 2008 |
|
Kwaliteit van bewijs: HOOG |
Double-stapling (PPH) STARR versus Countour Transtar Het lijkt dat de Countour Transtar stapler voor het behandelen van patiënten met ODS klachten in combinatie met een rectocele en/of IRP op lange termijn een betere uitkomst wat betreft recidieven en functionele klachten heeft in vergelijking met de conventionele Double-stapling (PPH) STARR stapler.
Boccasanta 2011, Isbert 2010, Renzi 2011 |
|
Kwaliteit van bewijs: ZEER LAAG |
TRREMS Er lijkt een aanwijzing te zijn dat TRREMS een goede uitkomst heeft op de functionele klachten bij patiënten met ODS klachten ten gevolge van een rectocele gecombineerd met een mucosa prolaps.
Leal 2010 |
|
Kwaliteit van bewijs: ZEER LAAG |
Laparoscopische ventrale rectopexie voor IRP De LVR als behandeling voor de IRP geeft goede functionele resultaten en acceptabele complicatie en recidief percentages.
Collinson 2010, Sileri 2012 |
Uitkomstmaten
Alvorens te starten met de literatuurselectie werden door de werkgroep klinisch relevante uitkomstmaten en acceptabele meetinstrumenten gedefinieerd. Ook definities voor andere relevante variabelen werden afgestemd. Bij de beoordeling van de literatuur heeft de werkgroep vooral gekeken naar studies waarbij, naar inzicht van de werkgroepleden, klinisch relevante uitkomstmaten gebruikt werden. Deze werden voorafgaand aan de literatuurselectie door de werkgroep bepaald en gedefinieerd. Ook heeft de werkgroep voorafgaand aan de search bepaald welke instrumenten voor het meten van de uitkomst zouden worden geselecteerd. Onderstaande is een overzicht van door de werkgroep opgestelde klinisch relevante uitkomstmaten en daarbij opgestelde geaccepteerde meetinstrumenten met klinisch relevante afkappunten:
|
Uitkomstmaten |
Gekozen meetinstrumenten en (klinisch relevante afkappunten) |
|
Module Anorectaal functieonderzoek en module Chirurgische behandeling van rectum prolaps |
|
|
Fecale incontinentie |
Wexner incontinence score (aanverwant ‘Scores uitkomstmaten’) (zelfde als Cleveland Clinic Incontinence Score (CCIS)) |
|
FISI - Fecal Incontinence Severity Index |
|
|
Obstipatie |
Wexner obstipatie score (aanverwant ‘Scores uitkomstmaten’) (zelfde als Cleveland Clinic Constipation Score (CCCS)) |
|
Obstructed defecation syndrome (ODS) score |
|
|
|
Rome criteria (aanverwant ‘Scores uitkomstmaten’) |
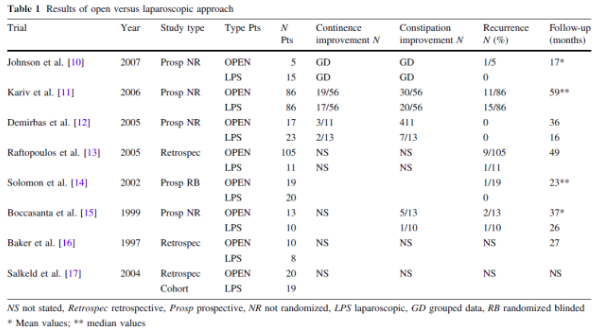
Er zijn 19 studies geselecteerd voor het beantwoorden van deze uitgangsvraag (Boccasanta 2011, Cadeddu 2012, Chun 2004, Collinson 2010, De Hoog 2009, Fleming 2012, Isbert 2010, Johnson 2012, Karas 2011, Leal 2010, Lehur 2008, Renzi 2011, Samaranayake 2010, Schiedeck 2005, Sileri 2012, Tou 2008, Tsunoda 2003, Youssef 2013, Zbar2002). Zie voor de zoekverantwoording onder het tabblad verantwoording en hieronder voor de evidencetabel.
Vergelijkende studies behandeling externe rectum prolaps
Laparotomische versus laparoscopische benadering
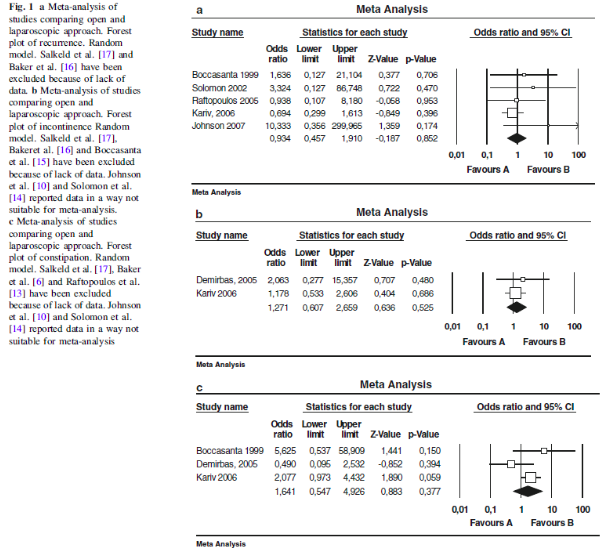
In een meta-analyse is door Cadeddu (2012) laparotomische rectopexie vergeleken met laparoscopische rectopexie voor de behandeling van ERP. In deze analyse werden acht studies geïncludeerd met in totaal 467 patiënten (275 laparotomisch, 192 laparoscopisch). De studies hadden een follow-up van 16 tot 59 maanden. Er werd tussen de twee behandelingen geen verschil gevonden in aantal recidieven en functionele uitkomst.
De Cochrane review van Tou (2008) beschrijft twee studies die een vergelijking maken tussen laparoscopische en laparotomische rectopexie bij patiënten met een ERP. Er was geen verschil in het aantal recidieven en in verbetering van incontinentie en obstipatie klachten. Het aantal postoperatieve complicaties en de kosten waren wel lager in de laparoscopie groep.
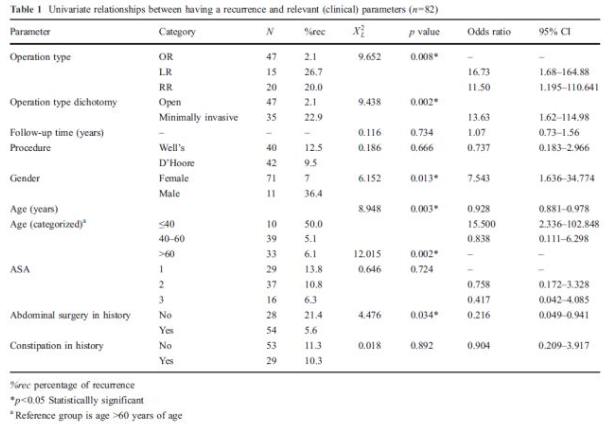
In een patiëntcontrole studie (De Hoog 2009) zijn laparoscopische (n=15), robot-geassisteerde (n=20) en laparotomische (n=47) rectopexie voor de behandeling van rectum prolaps met elkaar vergeleken. Er was bij respectievelijk vier (27%), vier (20%) en één (2%) patiënt(en) sprake van een recidief prolaps. Incontinentie en obstipatie klachten verbeterden bij alle drie de ingrepen maar onderling waren er geen verschillen.
Laparotomischeversus perineale benadering
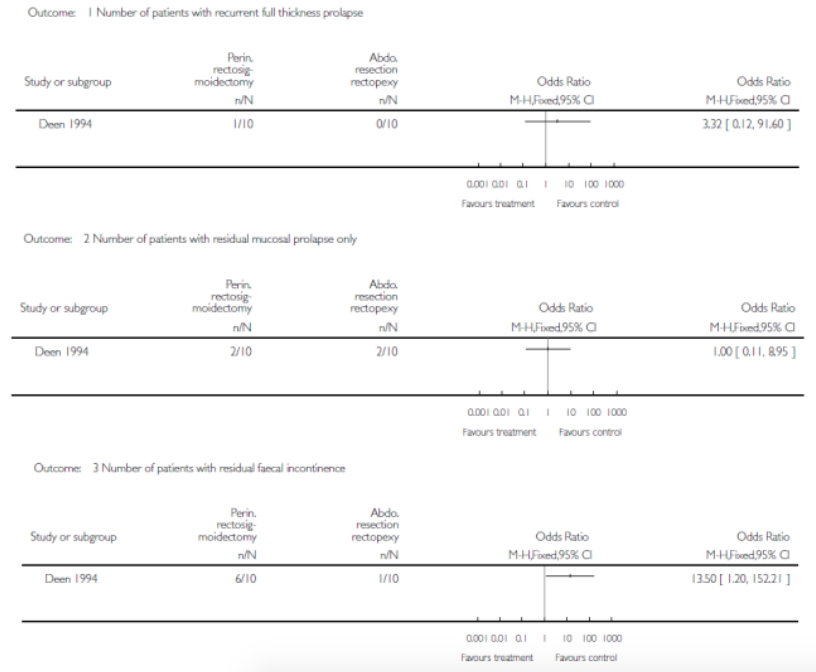
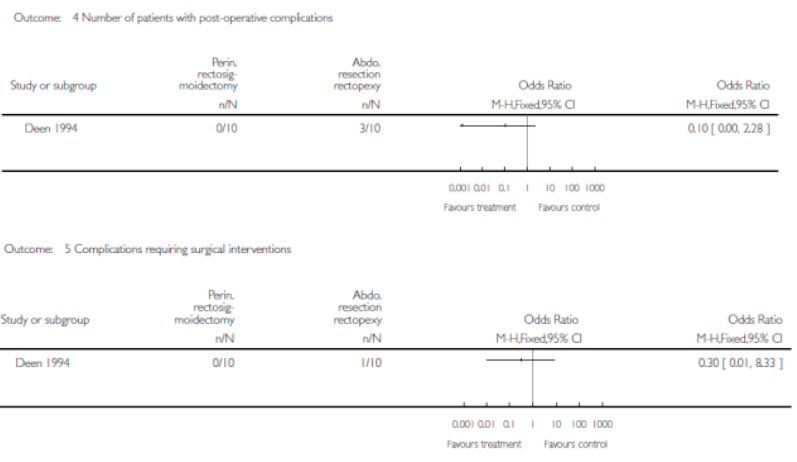
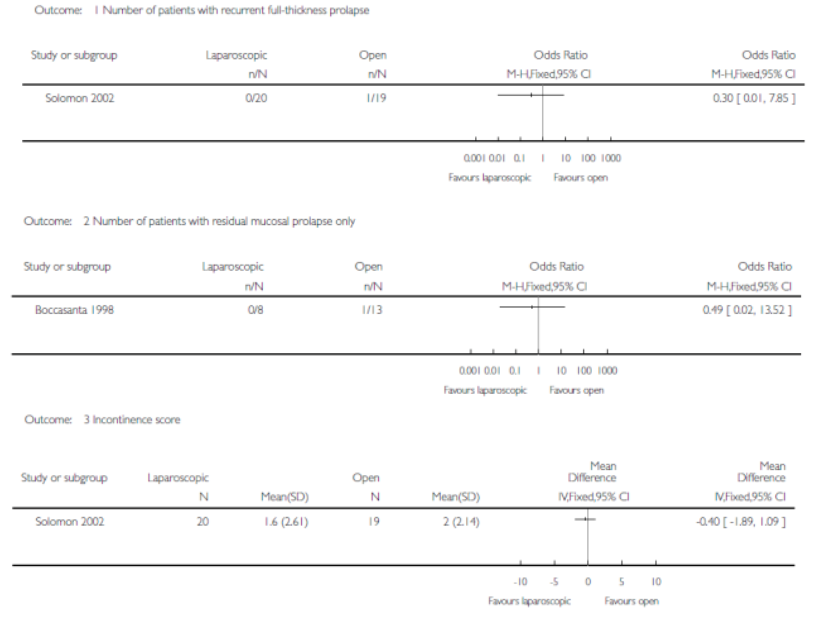
In de Cochrane review van Tou (2008) is één studie gevonden die deze vergelijking heeft onderzocht bij patiënten met een ERP. In beide behandelingsgroepen waren 10 patiënten geïncludeerd. Alleen in de perineale benadering groep was één patiënt met een recidief rectum prolaps. Zes van de 10 patiënten in de perineale groep hadden na de operatie klachten van fecale incontinentie in vergelijking met één patiënt in de laparotomie groep (OR 13.50, 95% CI 1.20-152.21). Postoperatieve complicaties waren niet significant verschillend tussen de twee groepen.
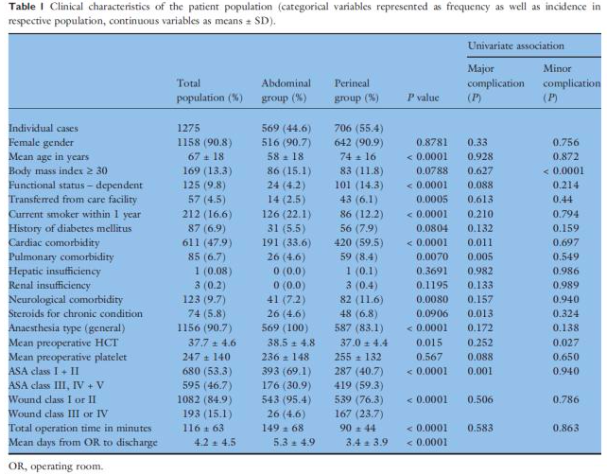
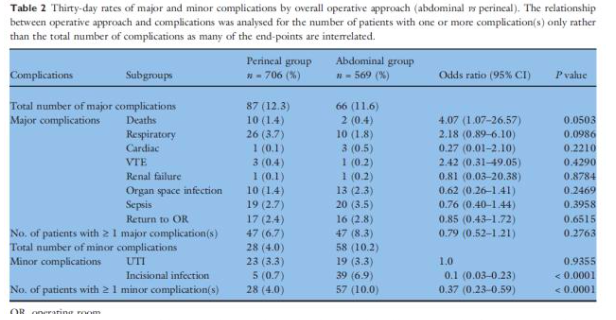
In een cohortstudie van Fleming (2012) is gekeken naar de morbiditeit en mortaliteit tot 30 dagen postoperatief bij patiënten die een laparotomie (resectie en conventionele rectopexie; n=569) danwel perineale ingreep (n=706) hebben ondergaan in verband met een rectum prolaps. Patiënten in de perineale groep waren ouder en hadden meer comorbiditeit dan de laparotomie groep. Een perineale ingreep was geassocieerd met minder postoperatieve complicaties (ernstige complicaties: OR 0.46, 95% CI 0.31-0.80; P = 0.0038) en klinisch niet significante (minor, urineweg en/of wondinfectie) complicaties: OR 0.35, 95% CI 0.20-0.60; P = 0.0002).
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie
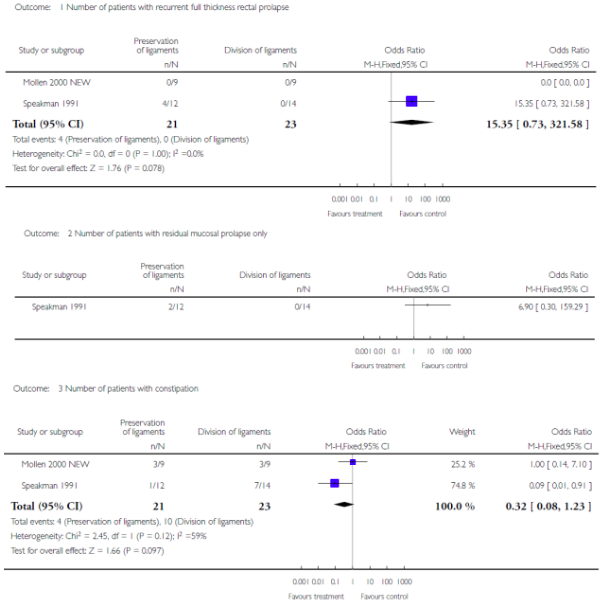
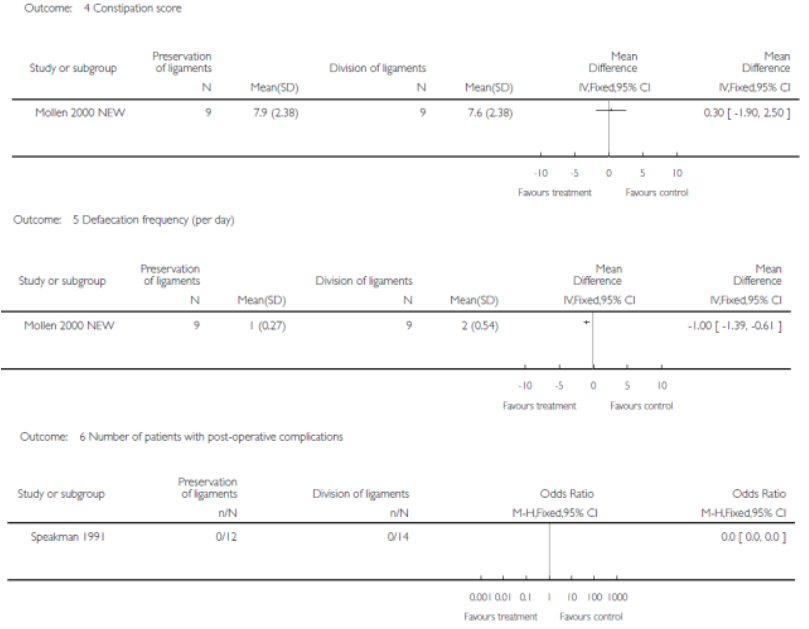
In de Cochrane review van Tou (2008) zijn twee bruikbare kleine studies gevonden die deze vergelijking (behoud versus klieven) hebben onderzocht bij patiënten met een rectum prolaps. Een recidief kwam bij vier van de 21 (19%) patiënten voor in de behoud groep en in nul van de 23 patiënten in de gekliefde groep (OR 15.35, 95% CI 0.73-321.58). Het aantal patiënten dat na de ingreep klachten had van obstipatie was vier van de 21 in de behoudende groep en 10 van de 23 in de gekliefde groep (OR 0.32, 95% CI 0.008-1.23). Er waren geen complicaties in beide groepen.
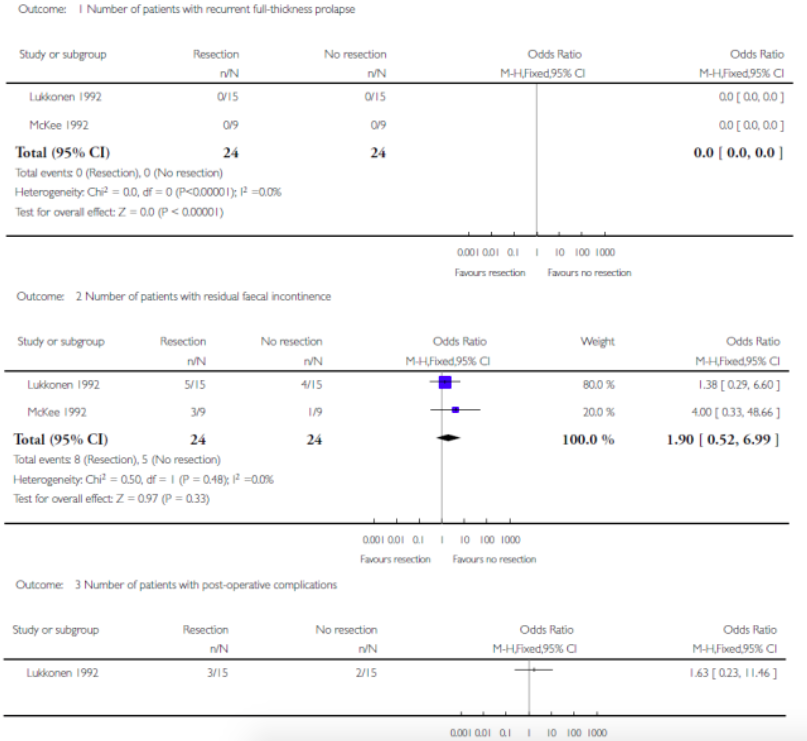
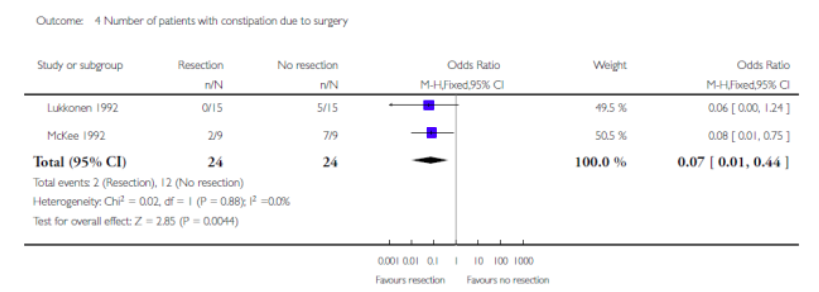
Resectie versus geen resectie bij laparotomische rectopexie
Ook heeft Tou (2008) naar deze vergelijking gekeken (2 trials, n=48) bij patiënten met een ERP. In beide groepen was geen recidief van de prolaps en een klein verschil in postoperatieve complicaties ten faveure van de ‘geen resectie’ groep (een trial, ernstige complicaties 2/15 vs. 3/15). Hoewel niet significant werd er klein verschil in postoperatieve fecale incontinentie gevonden met 8/24 (33%) incontinentie in de ‘resectie’ groep vs. 5/24 (21%) in de ‘geen resectie’ groep. De ‘resectie’ groep scoorde echter wel significant beter wat betreft obstipatie (2/24, 8% versus 12/24, 50%).
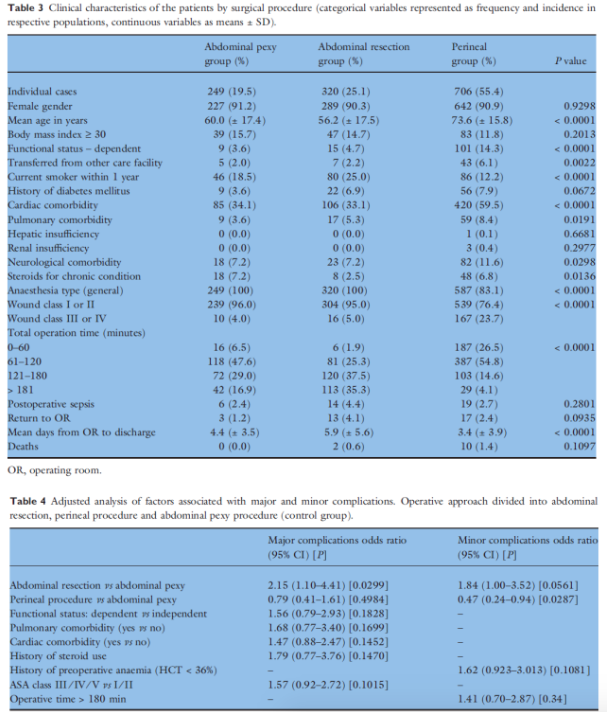
Fleming (2012) onderzocht de complicaties tussen de verschillende technieken. In de laparotomie groep werd een vergelijking gemaakt tussen een resectie en rectopexie die een significante toename van ernstige complicaties in de resectie groep liet zien (OR 2.15, 95% CI 1.10-4.41).
Rectopexie versus geen rectopexie
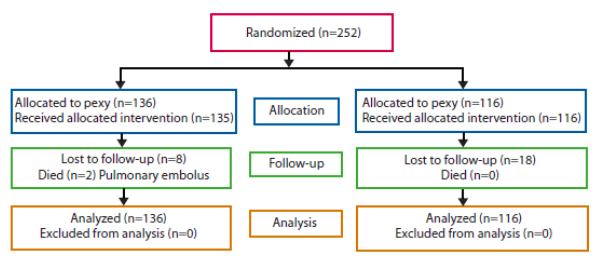
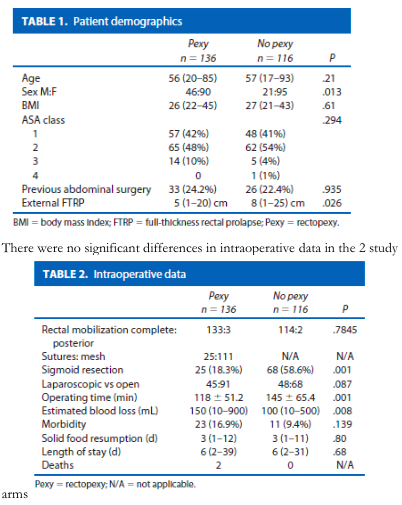
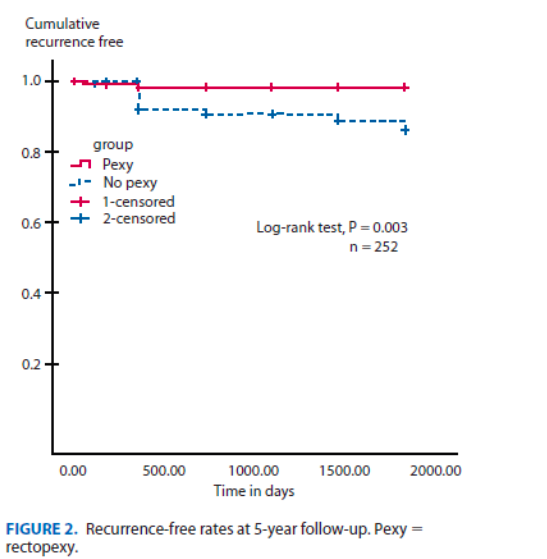
In een multicenter RCT (Karas 2011) voor patiënten met een ERP werd het rectum bij beide groepen gemobiliseerd tot aan de levator ani. Echter bij een groep werd er een mesh of suture rectopexie (n=136, 45 laparoscopisch, 91 open) uitgevoerd en vergeleken met een groep (n=116, 48 laparoscopisch, 68 open) waarbij het bleef bij mobilisatie. In hoeverre het rectum verder werd gemobiliseerd (ook posterior of 360°) werd ter plekke door de chirurg bepaald. Patiënten met preoperatie obstipatie, in welke groep dan ook, ondergingen bijkomend een rectosigmoïd resectie. Er werd geen verschil in het aantal complicaties gevonden. Na vijf jaar follow-up was het aantal recidieven in de ‘geen rectopexie’ groep hoger in vergelijking met de ‘rectopexie’ groep (8.6% vs. 1.5%, log-rank, p=0.003). In de ‘geen rectopexie’ werd in bijna 59% van de gevallen het rectosigmoïd gereseceerd, in de ‘rectopexie’ groep was dit 18.3%.
Delorme versus Delorme met levatorplastiek
In een RCT (Youssef 2013) is de Delorme procedure (n=41) vergeleken met een Delorme procedure met levatorplastiek (n=41) bij patiënten met een ERP. Patiënten die alleen een Delorme procedure ondergingen hadden één jaar postoperatief vaker een recidief prolaps (14.3% vs 2.4%, p 0.048). Obstipatie en incontinentie scores waren significant meer verbeterd in de Delorme met levatorplastiek groep. Er was onderling geen verschil in complicaties.
Altemeier versus Altemeier met levatorplastiek
Chun (2004) onderzocht deze vergelijking in een cohort met 120 patiënten (52 zonder, 68 met levatorplastiek) voor de behandeling van ERP met een gemiddelde follow-up van 28 maanden. Er werden kleine verschillen in morbiditeit gevonden (20.6% zonder, 15.3% met).
Recidief percentages verschilden nogal tussen de twee technieken, met 20.6% voor Altemeier versus 7.7% voor Altemeier met levatorplastiek. Incontinentie scores (Wexner) verbeterden het meest in de groep met levatorplastiek (12.9 preoperatief naar 5.8 postoperatief) vergeleken met de conventionele Altermeier groep (11.1 naar 7.7).
Vergelijkende studies behandeling interne rectum prolaps of rectocele (met of zonder enterocele)
Laparotomische versus laparoscopische resectie rectopexie voor interne rectum prolaps
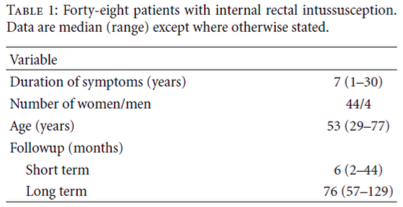
In een cohortonderzoek (Johnson 2012) is gekeken naar de korte (6 maanden) en lange termijn (76 maanden) gevolgen van (laterale ligament sparende)resectie rectopexie (25 laparoscopisch en 23 laparotomisch) in 48 patiënten met een IRP. Er waren in totaal acht gevallen (4 in beide groepen, 16.7%) van ernstige morbiditeit. Postoperatieve obstipatie klachten waren significant verbeterd in beide groepen maar er werd geen verschil gevonden tussen open of laparoscopisch.
STARR versus conservatieve behandeling
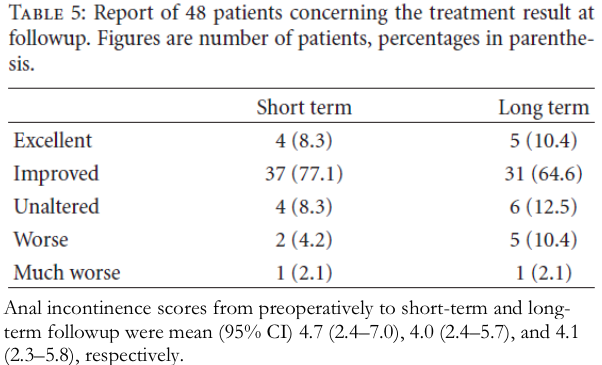
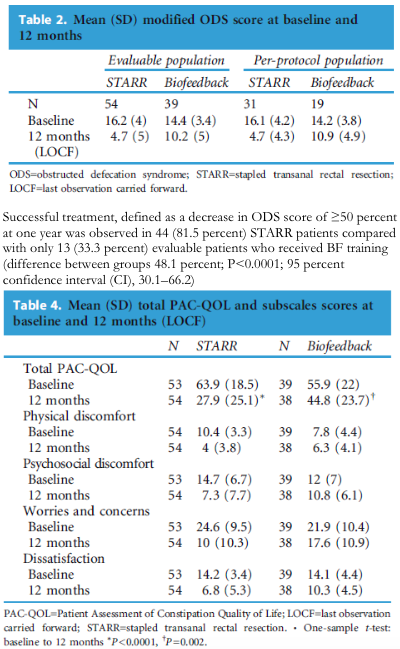
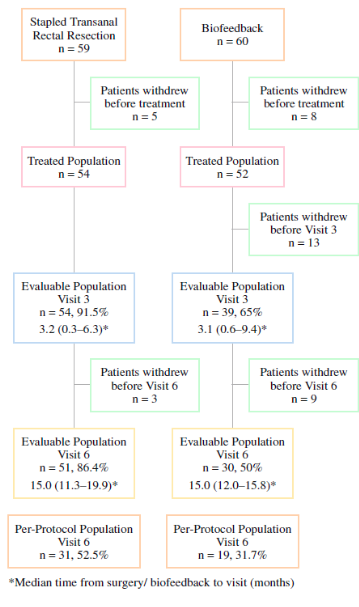
Lehur (2008) heeft in een multicenter RCT de STARR (n=59) vergeleken met bekkenfysiotherapie (n=60) bij vrouwen met het obstructief defecatie syndroom (ODS) en een rectocele en/of IRP. Van de vrouwen die voor bekkenfysiotherapie gerandomiseerd waren was na 12 maanden follow-up de helft beschikbaar. Acht (15%) van de vrouwen in de STARR groep en 1 (2%) in de bekkenfysiotherapie groep hadden een adverse event. ODS scores verbeterden in beide groepen significant maar succesvolle behandeling, gedefinieerd als een verbetering in klachten van meer dan 50%, werd significant vaker gezien in de STARR groep ten opzichte van de bekkenfysiotherapie groep (81.5% vs 33.3%, p<0.0001).
Double-stapling (PPH) STARR versus Countour Transtar
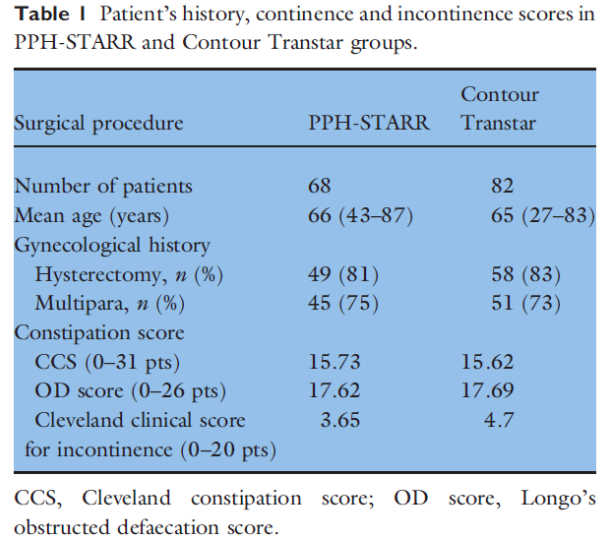
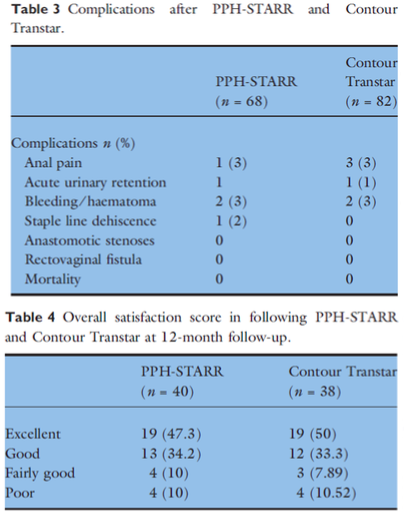
In een RCT (Boccasanta 2011) ondergingen 50 vrouwen een STARR (met dubbele PPH stapler) en 50 een Countour Transtar (CT) ingreep in verband met een rectocele of IRP gecombineerd met ODS klachten. Na een follow-up van 3 jaar had 12% in de STARR en 0% in de CT groep een recidief van de prolaps (p=0.035). Postoperatieve complicaties waren vergelijkbaar (STARR 4% vs. CT 2%). Er waren nauwelijks verschillen in klachten reductie. Echter in de STARR groep werden na 3 jaar klachten beschreven van fecale drang (‘fecale urgency’) in 34% van de gevallen versus 14% in de CT groep (p=0.035). De kosten van de CT waren hoger met een gemiddelde van 2998 euro versus 2410 euro per patiënt.
Renzi (2011) heeft in een RCT de STARR met 2 PPH staplers (n=31) en de CT (n=32) met elkaar vergeleken bij patiënten met ODS en IRP en/of rectocele. Na een follow-up van 12 maanden waren er geen verschillen in obstipatie en continentiescores. Na 24 maanden follow-up waren de functionele uitkomsten van de STARR groep wat verslechterd ten opzichte van de CT groep. Postoperatieve complicaties waren gelijk.
In een cohortonderzoek van Isbert (2010) ondergingen vrouwen een double-stapling (met PPH) STARR of CT vanwege ODS in combinatie met een rectocele met of zonder een IRP of enterocele. De technieken werden 12 maanden postoperatief met elkaar vergeleken. Postoperatieve complicaties waren niet verschillend (beide ongeveer 7.3%). Beide ingrepen lieten een flinke verbetering zien in obstipatie scores. De Wexner obstipatie (0 tot 30) score ging na de STARR van 15.5 naar 8.25 en na de CT van 15.7 naar 8.0. Er werden dus nauwelijks verschillen tussen de groepen gemeten.
Beschrijvende studies behandeling externe rectum prolaps
Laparoscopische rectopexie
In een systematisch review van Samaranayake (2010) is gekeken naar de uitkomsten van patiënten die een (laparoscopische) ventrale rectopexie (VR) met matplaatsing hebben ondergaan vanwege een ERP waarbij onderscheid werd gemaakt in studies met en zonder posterieure mobilisatie. Verdeeld over 12 studies werden er 505 (29 laparoscopisch) patiënten geïncludeerd met VR met posterieure mobilisatie (7 studies, VRMPM) en 223 (217 laparoscopisch) patiënten zonder posterieure mobilisatie (5 studies, VRZPM). VRZPM noteerde in alle studies verbetering van de obstipatie (pre-operatief min post-operatief percentage) met getallen variërend tussen 15.4 tot 83.3% en een gemiddelde van 40.3% klachten reductie. VRMPM rapporteerde -13.6 tot 28.8% klachten reductie betreffende obstipatie met een gemiddelde waarde van 6.1% (5 van de 7 studies). Obstipatie de novo wordt in 5.5 tot 10.5% voor VRZPM en in 2.7 tot 58.3% voor VRMPM vermeld. Voor de reductie van fecale incontinentie klachten worden soortgelijke getallen gevonden met een algehele (met en zonder posterieure mobilisatie) verbetering tussen 13.6 – 77.3% met een gemiddelde reductie van 44.9%. Recidief percentage varieert tussen 0 en 15.4% voor VRZPM (gemiddeld 5.5%, 4 studies) en 0 en 9.1% voor de VRMPM (gemiddeld 3.6%, 6 studies). Complicaties worden in 4.8 - 38.5% bij de VRZPM (gemiddeld 19.2%) en in 1.4 – 46.9% bij de VRMPM (gemiddeld 19.4%, 6 studies) van de gevallen beschreven. Zie tabel 1.
Tabel 1: Laparoscopische ventrale rectopexie (Bron: Samaranayake 2010)
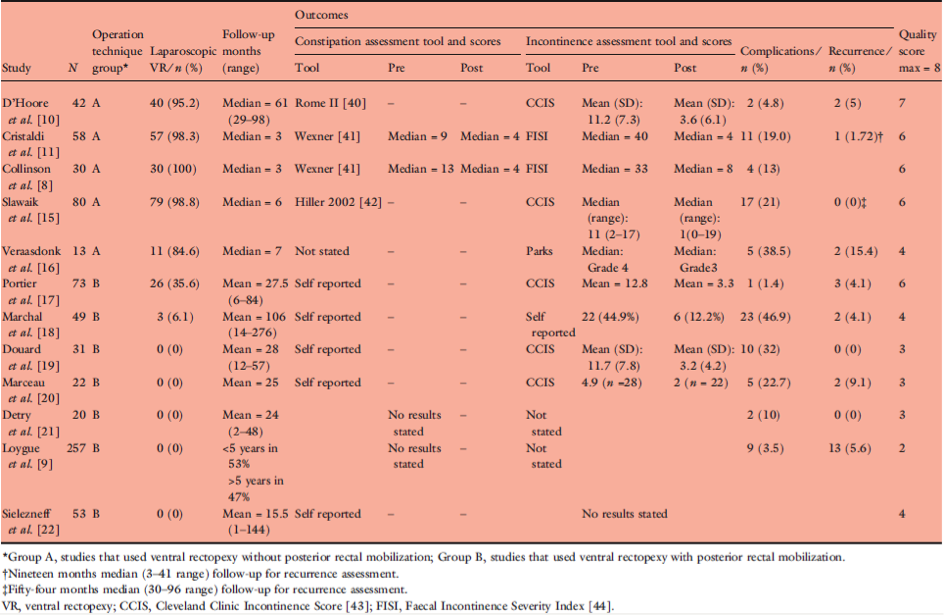
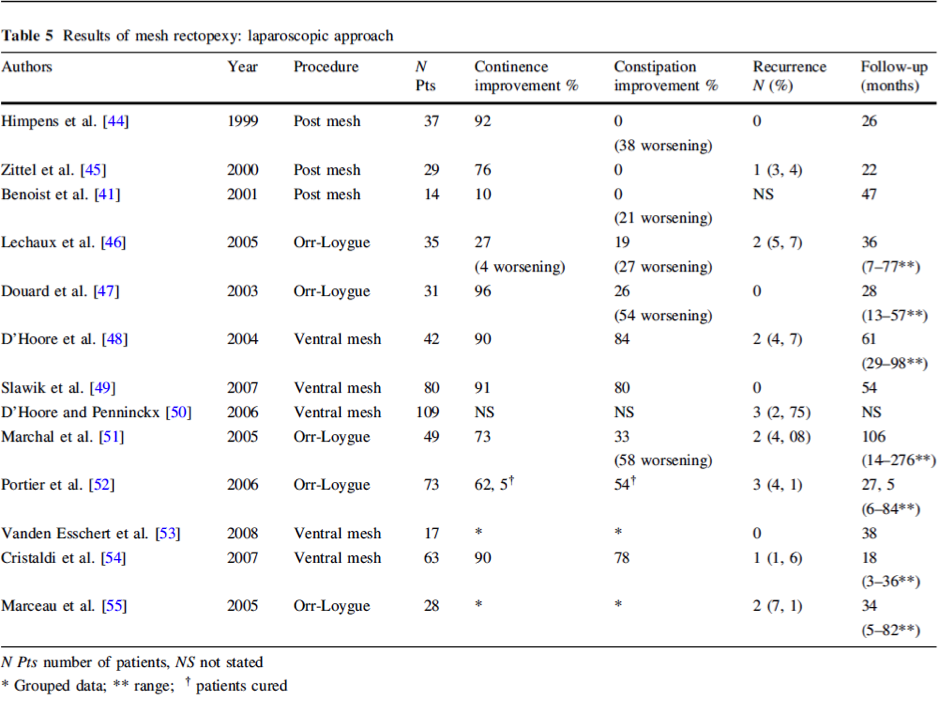
Een andere systematische review (Caddedu 2012) beschrijft uitkomsten van patiënten met een laparoscopische rectopexie met matplaatsing verdeeld in drie groepen: posterieure matplaatsing, ventrale matplaatsing en de Orr-Loygue techniek (uitleg zie overwegingen). De 3 studies (n= 80) die posterieure matplaatsing beschrijven rapporteren 10 tot 92% (gemiddeld 59%) verbetering van continentie, 0% verbetering van obstipatie en 0 tot 3.4% (gemiddeld 1.7%, 2 studies) aan recidieven na een gemiddelde follow-up van 24 maanden. In twee van de drie studies werd een verslechtering van de obstipatie gevonden: in 1 studie 38% en 1 studie 21% verslechtering. De 5 studies (n=216) betreffende Orr-Loygue noteren 27-96% (gemiddeld 65%, 4 studies) verbetering van continentie, 19-54% (gemiddeld 33%, 4 studies) verbetering van obstipatie klachten en 0-7.1% recidief percentage (gemiddeld 4.2%) met een gemiddelde follow-up van 46 maanden. De obstipatie verslechterde in drie van de vijf studies met respectievelijk 27, 54 en 58%. Caddedu (2012) includeerde 5 studies (n=311) inzake LVR met tussen de 90-91% (3 studies) aan incontinentie verbetering (gemiddeld 90%), 78-84% aan obstipatie verbetering (gemiddeld 81%) en 0-4.7% aan recidieven (gemiddeld 1.8%). De gemiddelde follow-up was 43 maanden (4 studies). De fucntionele verbetering is in dit revieuw de verhouding tussen pre en postoperatieve waarden, en niet het verschil zoals in het vorige review waardoor de getallen van Caddedu et al hoger uitvallen. Hetzelfde geld voor de laparoscopische resectie rectopexie hieronderstaand. Zie tabel 2.
Tabel 2: laparoscopische (ventale, posterieure en Orr-Loygue) rectopexie (Bron: Caddedu 2012)
Laparoscopische resectie rectopexie
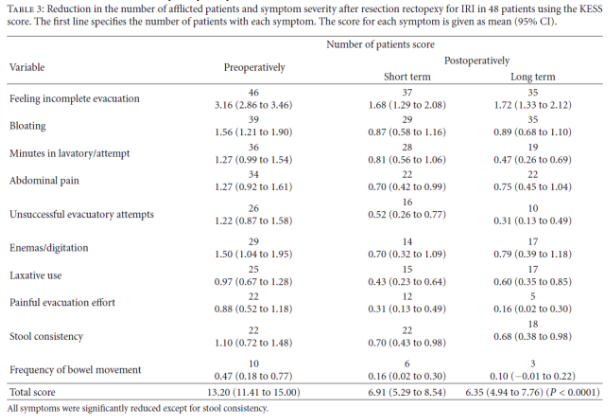
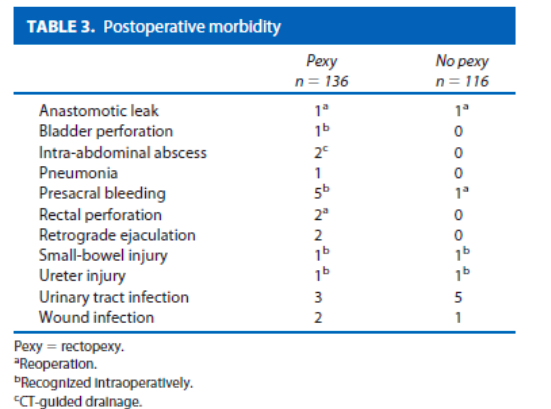
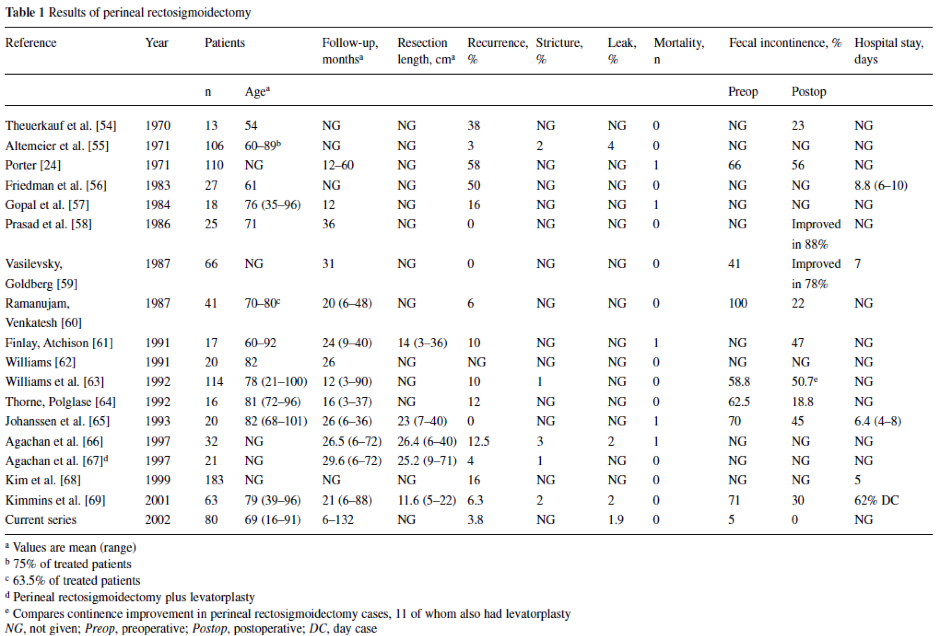
De uitkomsten van patiënten geopereerd met een laparoscopische resectie rectopexie voor ERP worden beschreven in een systematisch review van Caddedu (2012). Zes studies met 244 patiënten werden geïncludeerd. Incontinentie verbetering werd gezien in 38 tot 100% (gemiddeld 71%, 4 studies) en obstipatie verbetering in 8-76% (gemiddeld 44.8, 4 studies). Een negatief effect van de operatie werd in 8% voor zowel incontinentie als obstipatie vermeld in 1 studie. Postoperatieve morbiditeit kwam in 5 tot 30.4% voor met een gemiddelde van 15.4% (totaal 4 lekkages). Met een gemiddelde follow-up van 28.5 maanden werd een recidief percentage van 0% beschreven (5 studies). Zie tabel 3.
Tabel 3: laparoscopische resectie rectopexie voor ERP (Bron: Caddedu 2012)
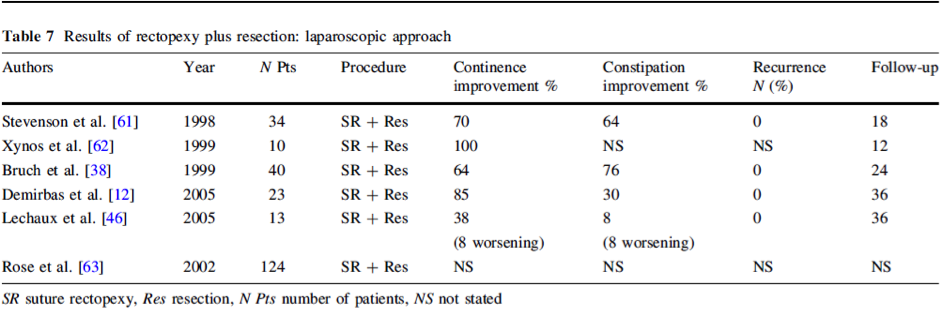
Delorme procedure
Tsunoda (2003) heeft in een cohortonderzoek gekeken naar de uitkomsten van de Delorme procedure bij 31 patenten met een ERP. Na gemiddeld 14 maanden was bij vier patiënten een recidief prolaps (12.9%). Ook was bij vier patiënten een postoperatieve complicatie. Incontinentie scores waren significant verbeterd met Wexner incontinentie scores van 11.5 (1–20) pre- en 6.0 postoperatief.
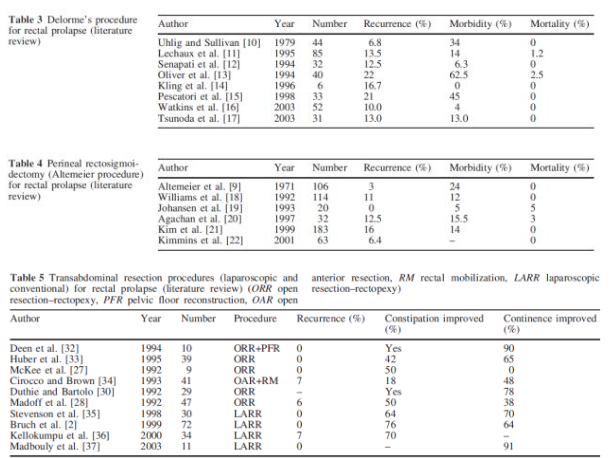
Schiedeck (2005) et al. beschrijven meerdere studies betreffende de Delorme procedure in een review. De acht geïncludeerde studies (totaal n = 323) laten een recidief percentage tussen 6.8 en 22% (gemiddeld 14.4%) zien. Het morbiditeit percentage was 0 - 62.5% (gem. 22.4%) met een mortaliteit van tussen 0 en 2.5% (gemiddeld 0.5%). Functionele uitkomsten werden niet gegeven. Zie tabel 4.
Tabel 4: Delorme procedure(Bron: Schiedeck 2005)
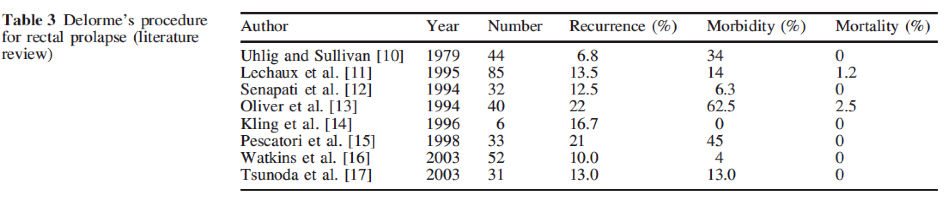
Altemeier procedure
Een review van Zbar (2002) includeerde 18 studies met een totaal van 972 patiënten. Recidief rectum prolaps vond tussen 0 en 58% (gemiddeld 14.3%, 17 studies) plaats. De fecale incontinentie was tussen 5 - 100 % preoperatief (gemiddeld 59.3%, 8 studies) en tussen 0 en 56 % postoperatief (gemiddeld 29.2%, zelfde 8 studies). Zie tabel 5.
Tabel 5: Altemeier procedure (Bron: Zbar 2002)
Beschrijvende studies behandeling interne rectum prolaps of rectocele (met of zonder enterocele)
Laparoscopische ventrale rectopexie voor interne rectum prolaps
Collinson et al. (2010) beschrijven 75 patiënten die een LVR ondergingen vanwege een symptomatische IRP met een follow-up van 12 maanden. Er werd 86% verbetering van de obstipatie klachten gevonden met een verschil in Wexner obstipatie score van 12 preoperatief vs. 5 postoperatief (mediaan). Van de patienten die met incontinentie kampten, kon in 85% van de gevallen verbetering van de continentie met een significant verschil in FISI score (mediaan preoperatief 28 vs 8 postoperatief) worden genoteerd. De algehele morbiditeit was 4% en er werd een recidief percentage van 5% beschreven.
In een soortgelijk cohort rapporteert Sileri (2012) (n=65) de uitkomsten van patiënten die een LVR kregen voor een symptomatische IRP met een gemiddelde follow-up van 12 maanden. De gemiddelde FISI incontinentie score verbeterde van 9 preoperatief naar 3 postoperatief na 6 maanden. De gemiddelde Wexner obstipatie score daalde van 16 naar 7. Complicatie percentage was 23.5%. Een (1.5%) prolaps werd niet opgeheven door de LVR en er trad een (1.5%) recidief op.
TRREMS (transanal repair of rectocele and rectal mucosectomy with a single circular stapler)
Leal (2010) heeft in een cohortstudie bestaande uit 35 vrouwen met ODS klachten ten gevolge van een rectocele en mucosa prolaps naar de uitkomst van een TRREMS procedure gekeken. Na gemiddeld 18 maanden waren obstipatie (Wexner obstipatie score 15.2 vs. 4.5) en continentie scores (Wexner incontinentie score 2.8 vs. 1.7) significant verbeterd ten opzicht van de preoperatieve metingen. Er waren vijf patiënten (14%) met een postoperatieve complicatie waarvan drie ernstig (8.6%) en waarvan 2 een re-interventie behoefden.
Grade tabel
Uitgangsvraag 1: Wat is de optimale chirurgische correctie van een externe rectale prolaps?
Beoordeling van studiekwaliteit |
Kwaliteit |
|||||||||
|
Studie ontwerp |
Studie beperkingen |
Inconsistentie |
Indirectheid |
Imprecisie |
Andere opmerkingen |
|||||
|
Laparotomisch versus laparoscopische rectopexie |
||||||||||
|
RCT 1 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
HOOG |
||||
|
Laparotomische versus perineale benadering |
||||||||||
|
RCT/observationele studie 2 |
Ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
MATIG |
||||
|
Behoud versus klieven van de laterale ligamenten van het rectum bij een laparotomische rectopexie |
||||||||||
|
RCT 3 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
MATIG |
||||
|
Resectie versus geen resectie bij laparotomische rectopexie |
||||||||||
|
RCT/observationele studie4 |
Ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
MATIG |
||||
|
Rectopexie versus geen rectopexie |
||||||||||
|
RCT 5 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
MATIG |
||||
|
Delorme versus Delorme met levatorplastiek |
||||||||||
|
RCT 6 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
MATIG |
||||
|
Altemeier versus Altemeier met levatorplastiek |
||||||||||
|
Observationele studie7 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
ZEER LAAG |
||||
|
Laparoscopische rectopexie |
||||||||||
|
Observationele studie 8 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Groot effect |
MATIG |
||||
|
Laparoscopische resectie rectopexie |
||||||||||
|
Observationele studie9 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
ZEER LAAG |
||||
|
Delorme procedure |
||||||||||
|
Observationele studie10 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
LAAG |
||||
|
Altemeier procedure |
||||||||||
|
Observationele studie11 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
LAAG |
||||
1 Twee meta-analyses (Cadeddu 2012, Tou 2008) en één patient-controle onderzoek (De Hoog 2009), aantal recidieven >300.
2 Eén meta-analyse (Tou 2008) en één cohort onderzoek (Fleming 2012). Meta-analyse heeft 20 patiënten geincludeerd, Fleming (2012) totaal 1275
3 Eén meta-analyse (Tou 2008), er is één studie geselecteerd met een totale N van 44.
4 Eén meta-analyse (Tou 2008) en één cohort onderzoek (Fleming 2012). Tou et al. heeft 48 patiënten geincludeerd en Fleming et al. in totaal 569.
5 Eén RCT (Karas 2011), totale N = 252
6 Eén RCT (Youssef 2013), totale N = 82
7 Eén cohort onderzoek (Chun 2004), totale N = 120
8 Twee systematische reviews (Caddedu 2012, Samaranayaka 2010) waarin enkel cohort onderzoeken zijn geselecteerd. Gezien grote effect van uitkomsten geüpgrade.
9 Eén systematische review (Caddedu 2012) waarin enkel cohort onderzoeken zijn geselecteerd. Totale N = 244
10 Eén systematische review (Schiedeck 2005) waarin enkel cohort onderzoeken zijn geselecteerd en één cohort onderzoek (Tsunoda 2003). Totale N van deze studies = 354
11 Twee systematische review (Schiedeck 2005, Zbar 2002) waarin enkel cohort onderzoeken zijn geselecteerd. Totale N van deze studies = 972
Uitgangsvraag 2: Wat is de optimale chirurgische correctie van een interne rectale prolaps?
|
Beoordeling van studiekwaliteit |
Kwaliteit |
||||||
|
Aantal studies |
Studie ontwerp |
Studie beperkingen |
Inconsistentie |
Indirectheid |
Imprecisie |
Andere opmerkingen |
|
|
Laparotomische versus laparoscopische resectie rectopexie |
|||||||
|
1 |
observationele studie1 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
ZEER LAAG |
|
STARR versus conservatieve behandeling |
|||||||
|
1 |
RCT 2 |
Ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
MATIG |
|
Double-stapling (PPH) STARR versus Countour Transtar |
|||||||
|
3 |
RCT/observationele studie 3 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Geen ernstige imprecisie |
Geen |
HOOG |
|
TRREMS |
|
|
|
|
|
|
|
|
1 |
observationele studie4 |
Geen ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
ZEER LAAG |
|
Laparoscopische ventrale rectopexie voor IRP |
|||||||
|
2 |
observationele studies 5 |
Ernstige beperkingen |
Geen ernstige inconsistentie |
Geen ernstige indirectheid |
Ernstige imprecisie |
Geen |
ZEER LAAG |
1 Eén cohort onderzoek (Johnson 2012), totale N = 48
2 Eén RCT (Lehur 2008), totale N = 119
3 Twee RCT’s (Boccasanta 2011, Renzi 2011) en één cohort onderzoek (Isbert 2010), totale N = 313
4 Eén cohort onderzoek (Leal 2010), totale N = 35. Tevens geen controle groep.
5 Twee cohort onderzoeken (Collinson 2010, Sileri 2012), totale N = 140. Tevens geen controle groep.
- Boccasanta, P., Venturi, M., & Roviaro, G. (2011). What is the benefit of a new stapler device in the surgical treatment of obstructed defecation? Three-year outcomes from a randomized controlled trial. Diseases of the Colon & Rectum, 54(1), 77-84.
- Cadeddu, F., Grande, M., Sileri, P., Franceschilli, L., De Luca, E., Tucci, G. et al. (2012). Focus on abdominal rectopexy for full-thickness rectal prolapse: A meta-analysis of literature. Techniques in Coloproctology, 16(1), 105.
- Chun, S. W., Pikarsky, A. J., You, S. Y., Gervaz, P., Efron, J., Weiss, E. et al. (2004). Perineal rectosigmoidectomy for rectal prolapse: role of levatorplasty. Techniques in Coloproctology, 8(1), 3-8.
- Collinson, R., Wijffels, N., Cunningham, C., & Lindsey, I. (2010). Laparoscopic ventral rectopexy for internal rectal prolapse: short-term functional results. Colorectal Disease, 12(2), 97-104.
- D'Hoore, A., & Penninckx, F. (2006). Laparoscopic ventral recto(colpo)pexy for rectal prolapse: surgical technique and outcome for 109 patients. Surg.Endosc., 20(12), 1919-1923.
- De Hoog, D. E., Heemskerk, J., Nieman, F. H., van Gemert, W. G., Baeten, C. G., & Bouvy, N. D. (2009). Recurrence and functional results after open versus conventional laparoscopic versus robot-assisted laparoscopic rectopexy for rectal prolapse: a case-control study. International Journal of Colorectal Disease, 24(10), 1201-1206.
- Fang, S. H., Cromwell, J. W., Wilkins, K. B., Eisenstat, T. E., Notaro, J. R., Alva, S. et al. (2012). Is the abdominal repair of rectal prolapse safer than perineal repair in the highest risk patients? An NSQIP analysis. Diseases of the Colon and Rectum, 55(11), 1167-1172.
- Fleming, F. J., Kim, M. J., Gunzler, D., Messing, S., Monson, J. R. T., & Speranza, J. R. (2012). It's the procedure not the patient: The operative approach is independently associated with an increased risk of complications after rectal prolapse repair. Colorectal Disease, 14(3), 362-368.
- Habr-Gama, A., Jacob, C. E., Jorge, J. M., Seid, V. E., Marques, C. F., Mantese, J. C. et al. (2006). Rectal procidentia treatment by perineal rectosigmoidectomy combined with levator ani repair. Hepatogastroenterology, 53(68), 213-217.
- Isbert, C., Reibetanz, J., Jayne, D. G., Kim, M., Germer, C. T., & Boenicke, L. (2010). Comparative study of contour transtar and STARR procedure for the treatment of obstructed defecation syndrome (ODS) - feasibility, morbidity and early functional results. Colorectal Disease, 12(9), 901-908.
- Johnson, E., Kjellevold, K., Johannessen, H. O., & Drolsum, A. (2012). Long-term outcome after resection rectopexy for internal rectal intussusception. ISRN Gastroenterology, 2012.
- Karas, J. R., Uranues, S., Altomare, D. F., Sokmen, S., Krivokapic, Z., Hoch, J. et al. (2011). No rectopexy versus rectopexy following rectal mobilization for full-thickness rectal prolapse: a randomized controlled trial. Diseases of the Colon & Rectum, 54(1), 29-34.
- Leal, V. M., Regadas, F. S. P., Regadas, S. M. M., & Veras, L. R. (2010). Clinical and functional evaluation of patients with rectocele and mucosal prolapse treated with transanal repair of rectocele and rectal mucosectomy with a single circular stapler (TRREMS). Techniques in Coloproctology, 14(4), 329-335.
- Lee, S. H., Lakhtaria, P., Canedo, J., Lee, Y. S., & Wexner, S. D. (2011). Outcome of laparoscopic rectopexy versus perineal rectosigmoidectomy for full-thickness rectal prolapse in elderly patients. Surg.Endosc., 25(8), 2699-2702.
- Lehur, P. A., Stuto, A., Fantoli, M., Villani, R. D., Queralto, M., Lazorthes, F. et al. (2008). Outcomes of stapled transanal rectal resection vs. biofeedback for the treatment of outlet obstruction associated with rectal intussusception and rectocele: a multicenter, randomized, controlled trial.[Erratum appears in Dis Colon Rectum. 2008 Nov;51(11):1739 Note: Narisetty, Prashanty [corrected to Narisetty, Prashanthi]]. Diseases of the Colon & Rectum, 51(11), 1611-1618.
- Mercer-Jones, M. A., D'Hoore, A., Dixon, A. R., Lehur, P., Lindsey, I., Mellgren, A. et al. (2014). Consensus on ventral rectopexy: report of a panel of experts. Colorectal Disease, 16(2), 82-88.
- Mustain, W. C., Davenport, D. L., Parcells, J. P., Vargas, H. D., & Hourigan, J. S. (2013). Abdominal versus perineal approach for treatment of rectal prolapse: comparable safety in a propensity-matched cohort. Am.Surg., 79(7), 686-692.
- Renzi, A., Brillantino, A., Di Sarno, G., Izzo, D., D'Aniello, F., & Falato, A. (2011). Improved clinical outcomes with a new contour-curved stapler in the surgical treatment of obstructed defecation syndrome: A mid-term randomized controlled trial. Diseases of the Colon and Rectum, 54(6), 736-742.
- Ris, F., Colin, J. F., Chilcott, M., Remue, C., Jamart, J., & Kartheuser, A. (2012). Altemeier's procedure for rectal prolapse: analysis of long-term outcome in 60 patients. Colorectal Disease, 14(9), 1106-1111.
- Samaranayake, C. B., Luo, C., Plank, A. W., Merrie, A. E., Plank, L. D., & Bissett, I. P. (2010). Systematic review on ventral rectopexy for rectal prolapse and intussusception. [Review] [49 refs]. Colorectal Disease, 12(6), 504-512.
- Schiedeck, T. H., Schwandner, O., Scheele, J., Farke, S., & Bruch, H. P. (2005). Rectal prolapse: which surgical option is appropriate? Langenbecks Archives of Surgery, 390(1), 8-14
- Sileri, P., Franceschilli, L., de, L. E., Lazzaro, S., Angelucci, G. P., Fiaschetti, V. et al. (2012). Laparoscopic ventral rectopexy for internal rectal prolapse using biological mesh: postoperative and short-term functional results. J.Gastrointest.Surg., 16(3), 622-628.
- Stevenson, A. R., Stitz, R. W., & Lumley, J. W. (1998). Laparoscopic-assisted resection-rectopexy for rectal prolapse: early and medium follow-up. Diseases of the Colon and Rectum, 41(1), 46-54.
- Tou, S., Brown, S. R., Malik, A. I., & Nelson, R. L. (2008). Surgery for complete rectal prolapse in adults. [Review] [30 refs][Update of Cochrane Database Syst Rev. 2000;(2):CD001758; PMID: 10796817]. Cochrane Database of Systematic Reviews,(4), CD001758.
- Tsunoda, A., Yasuda, N., Yokoyama, N., Kamiyama, G., & Kusano, M. (2003). Delorme's procedure for rectal prolapse: Clinical and physiological analysis. Diseases of the Colon and Rectum, 46(9), 1260-1265.
- WELLS, C. (1959). New operation for rectal prolapse. Proc.R.Soc.Med., 52, 602-603.
- Wijffels, N., Cunningham, C., Dixon, A., Greenslade, G., & Lindsey, I. (2011). Laparoscopic ventral rectopexy for external rectal prolapse is safe and effective in the elderly. Does this make perineal procedures obsolete? Colorectal Disease, 13(5), 561-566.
- Zbar, A. P., Takashima, S., Hasegawa, T., & Kitabayashi, K. (2002). Perineal rectosigmoidectomy (Altemeier's procedure): a review of physiology, technique and outcome. [Review] [78 refs]. Techniques in Coloproctology, 6(2), 109-116.
|
|
Study type |
Characteristics |
Intervention (I) |
Controls (C)
|
Outcome measures and follow-up time |
Results |
Quality assessment study |
|
Boccasanta 2011 |
Design RCT
N = 100
Country Italie |
Aim of the study: To compare the clinical and functional outcomes of the stapled transanal rectal resection, using the traditional 2 circular staplers and a new, curved stapler device in patients with obstructed defecation caused by rectal intussusception and rectocele.
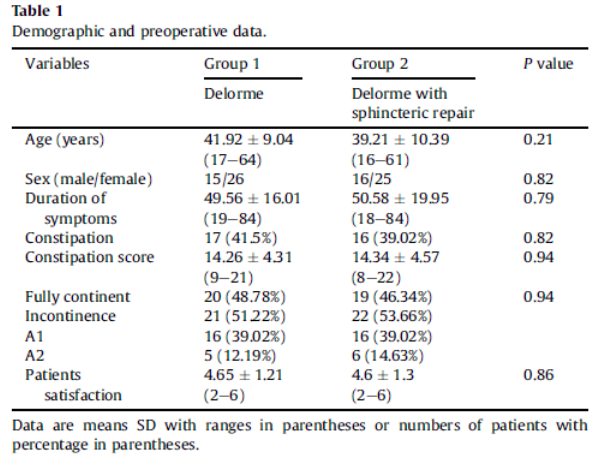
Inclusion criteria • IRP (second or third degree (Pescatori’s grading)), or rectal intussusception • Rectocele >3cm • ODS score >15 • Continence score <3 • Resting pressure >40 mm Hg, squeeze pressure >100 mm Hg
Exclusion criteria: • Previous surgery for rectal prolapse and/or rectocele • IRP first degree (Pescatori’s grading) • Rectocele _3 cm • ODS score _15 • Continence score _3 • Resting pressure _40 mm Hg, squeeze pressure _100 mm Hg • Concomitant enterocele, compressing the rectum during evacuation efforts • Concomitant cystocele, or genital prolapse • Psychiatric diseases • Absolute contraindications to surgery.
|
Intervention stapled transanal rectal resection with a new, curved multifire stapler (TRANSTAR group).
N = 50
|
Controls stapled transanal rectal resection with 2 traditional circular staplers (STARR group)
N = 50
|
Primary outcomes: rate of failure (residual mucosal rectal prolapse, with an ODS score >5)
Secundary outcomes: operative time and blood loss, complications, hospital stay, postoperative pain, time to return to normal activity, outcome of surgery on the ODS score, quality of life on the SF36 Health Survey questionnaire, costs, and patient satisfaction score.
Follow up: STARR: 36.3 ± 4.4 months TRANSTAR: 36.2 ± 4.2 |
Primary outcomes: 50 (mean age, 54.8 y; range, 27–77) underwent a conventional STARR with 2 PPH-01 staplers (STARR group) and 50 (mean age, 57.1 y; range, 31–74) had the same operation but with the new stapler CCS-30 (TRANSTAR group). Six patients from the STARR group (12.0%) and none with TRANSTAR had a prolapse recurrence at clinical examination, with an ODS score <5 (P = .035).
|
Clearly defined groups:
Selection bias:
Method of assessing the outcome appropriately:
Selective loss to follow up: No loss to follow up
Identification confounders and correction in analysis:
Funding: No financial disclosure |
|
Cadeddu 2012
|
Design meta-analysis
N = 8 studies (467 patients) |
Aim of the study: to evaluate long-term results of open and laparoscopic abdominal procedures to treat full-thickness rectal prolapse in adults.
Inclusion criteria - articles published between 1972 and 2010 on abdominal rectopexy patients with a follow-up longer than 16 months
Exclusion criteria:
|
Intervention Open procedure
N = 275
|
Controls Laparoscopic procedure
N = 192
|
Primary outcomes: recurrence of rectal prolapse
Secundary outcomes: improvement in incontinence and constipation
Follow up: 16-59 months |
Primary outcomes: Forest plot A: recurrence; plot B: incontinence; plot C: constipation
|
Clearly defined groups: Yes
Selection bias: No
Method of assessing the outcome appropriately: A literature review was performed using the National Library of Medicine’s PubMed database. All articles published between 1972 and 2010 on abdominal rectopexy patients with a follow-up longer than 16 months were considered. In the meta-analysis, both randomized and non-randomized trials comparing open and laparoscopic rectopexy with a follow-up longer than 16 months were included. Any technique for abdominal repair of rectal prolapse was considered, i.e. resection and rectopexy with either suture or mesh.
Selective loss to follow up: Not applicable
Identification confounders and correction in analysis: No
Funding: Not reported |
|
De Hoog 2009 |
Design case–control study
N = 82
Country Netherlands |
Aim of the study: to evaluate recurrence and functional outcome of three surgical techniques for rectopexy: open (OR), laparoscopic (LR), and robot-assisted (RR).
Inclusion criteria - patients who underwent a rectopexy for full thickness rectal prolapse between January 2000 and September 2006 - Patients with a “hostile abdomen” after extensive abdominal surgery were deemed eligible for an OR only.
Exclusion criteria: - age under 18 or patient unfit for surgery.
|
Intervention Laparoscopic rectopexy
N = 15
Robot-assisted rectopexy
N = 20
|
Controls Open rectopexy
N = 47
|
Primary outcomes: recurrence
Secundary outcomes: Functional results
Follow up: Median 1.95 years (mean 2.6; range 0.2–8.0). |
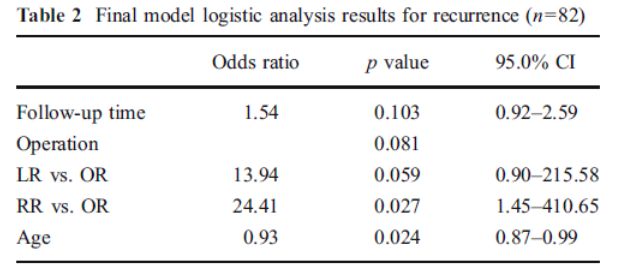
Primary outcomes: A total of 82 patients (71 females, 87%) with a mean age of 56.4 years (range, 21–88) were included and underwent an OR (n=47, 57%), LR (n=15, 18%), or RR (n=20, 24%) for rectal procidentia. Forty-one (50%) patients had fecal incontinence (including grade 4 incontinence in 35 patients). Other complaints were constipation (n=29, 35%). Nine (11%) of the 82 patients developed a recurrence. Recurrences (Table 1) were more frequent after both minimal invasive rectopexy types compared to open surgery (respectively LR 27% and RR 20% versus OR 2%; p=0.008). Recurrence occurs significantly more often in younger patients in childbearing age (p=0.003), especially below the age of 40 (50% vs. 6% above the age of 60; p=0.002). Males are more likely to get a recurrence (p=0.013), and fixation of the vaginatop (in patient with previous hysterectomy) protects against recurrence (p= 0.009). No differences were found for either decrease in Wexner score or IDL score between the three operation types Fecal incontinence was still present in 27 patients (33%). In 15 of the 42 (36%) patients the fecal incontinence improved after rectopexy. |
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: Peri-operative data were collected from patient records and functional outcome was assessed by telephonic questionnaire. In the first 42 patients, a Well’s procedure was performed. After rectal mobilization a posterior mesh rectopexy was performed (first described by Wells in 1959). Since July 2004, the general policy in our department shifted from a modified Well’s procedure towards a D’Hoore ventral mesh rectopexy. In RR, we used the four-armed DaVinci® surgical system (Intuitive Surgical Inc., CA, USA). The standardized Wexner constipation score was used to investigate the level of constipation before and after the operation. The Parks–Browning classification was used to grade fecal incontinence
Selective loss to follow up: Seventy-two (90%) patients answered the questionnaire (M–F=10:62). Reasons for not taking part were: inaccessibility (four), psychological illness (three), and unwilling (one). Two patients died during follow-up as a result of non-related causes.
Identification confounders and correction in analysis: No
Funding: Not reported |
|
Fleming 2012 |
Design Cohort study
N = 1275
Country USA |
Aim of the study: This study compares 30-day outcomes following rectal prolapse repair, examining potential surgical and patient factors associated with perioperative complications.
Inclusion criteria - The NSQIP database was examined for patients with a primary postoperative diagnosis of rectal prolapse based on the ICD-9 codes
Exclusion criteria:
|
Intervention Surgical approach: Abdominal group
(resection compared with rectopexy alone)
N = 569
|
Controls Surgical approach: Perineal group
N = 706
|
Primary outcomes: morbidity
Secundary outcomes:
Follow up: 30-day postoperative |
Primary outcomes: There were 153 major complications recorded in the 30-day postoperative period, involving 94 (7.4%) patients, and 86 minor complications in 85 (6.7%) patients.
After adjustment, a perineal approach was associated with a lower postoperative complication rate of both major (perineal vs abdominal: OR, 0.46; 95% CI, 0.31–0.80; P = 0.0038) and minor complications (perineal vs abdominal: OR, 0.35; 95% CI, 0.20–0.60; P = 0.0002).
|
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: The American College of Surgeons National Surgical Quality Improvement Program (NSQIP) comprises a clinical database with systematic data collection from hundreds of hospitals throughout the United States. the programme collects information pertaining to patient demographics, preoperative medical history, clinical findings and laboratory investigations. After discharge, follow-up data are obtained from chart review and a standardized phone interview by a certified nurse reviewer. The NSQIP database was examined for patients with a primary postoperative diagnosis of rectal prolapse (569.1) based on the International Classification of Disease, 9th Edition (ICD codes). The primary diagnosis category was then cross-referenced with the Current Procedural Terminology (CPT) codes to select for cases that specifically coded for a rectal prolapse procedure. Major complications included organ space (peritoneal) infections, cardiac events, ventilator dependence (re-intubation or failure to wean), pneumonia, venous thromboembolic events, return to the operating room (OR), renal failure, and sepsis. NSQIP uses the Center for Disease Control (CDC) definitions for septic end-points. Minor complications included surgical site infections (superficial to the fascia) and urinary tract infections.
Selective loss to follow up: No
Identification confounders and correction in analysis: Yes, operative approach, preoperative steroid use, pulmonary comorbidity, cardiac comorbidity, ASA class, functional status and preoperative platelet count
Funding: Not reported |
|
Isbert 2010 |
Design Cohort study
N = 150
Country Germany |
Aim of the study: to compare the morbidity and functional results at 12-month follow-up in patients undergoing either two circular stapling devices (PPH)-STARR or Contour Transtar (CT) for obstructive defecation syndrome (ODS).
Inclusion criteria - women with defecatory disorders who underwent a STARR from January 2006 until May 2008
Exclusion criteria:
|
Intervention PPH-STARR
N = 68
|
Controls CT-STARR
N = 82
|
Primary outcomes:
Secundary outcomes:
Follow up: 12-month postoperatively |
Primary outcomes:
Four (10%) patients following PPH-STARR and four (10.5%) patients following CT group suffered persistent obstructive defecation or pain. Five patients (10.5%) in the PPH-STARR group and two (8.3%) in the CT group complained about new onset incontinence for flatus. There was no significant difference between the preoperative and 12-month follow-up incontinence scores for either group.
|
Clearly defined groups: Yes. Initially, the conventional double stapling technique, using two PPH01 devices, was used to perform STARR. At the beginning of 2007 the CT device was used in addition. In the latter cases, the decision about whether to perform CT or PPH-STARR was made on the basis of the diameter of anal canal and the size of the rectal prolapse as assessed at operation (<3 cm after gentle dilatation); patients with larger prolapse were preferentially selected for CT.
Selection bias: Yes, see ‘clearly defined groups’
Method of assessing the outcome appropriately: Yes, 12 months postoperatively patients were referred for examination that included symptom evaluation, using the same standardized questionnaires for constipation and incontinence, clinical examination and investigation using video-rectoscopy and anal manometry.
Selective loss to follow up: Forty of the 68 (58%) patients in the PPH-STARR group and 38 of the 82 (46%) patients in the CT group attended for follow-up assessment at 12-month follow-up.
Identification confounders and correction in analysis: No
Funding: Not reported |
|
Johnson 2012 |
Design Cohort study
N = 48
Country Norway |
Aim of the study: To study the short- and long-term outcome of resection rectopexy in patients with internal rectal intussusception (IRI)
Inclusion criteria - patients with IRI who had resection rectopexy between February 1999 and June 2006.
Exclusion criteria:
|
Intervention resection rectopexy
N = 48
|
Controls No
|
Primary outcomes: morbidity, scores for constipation (KESS score) and anal incontinence, patients’ report, and health-related quality of life (HRQoL)
Secundary outcomes:
Follow up: 76 months (57-129) |
Primary outcomes: Rectopexy with suture and sigmoid resection was performed. The operation was done laparoscopically in 25 patients and by open access in 23 patients, including conversions to open operation in three patients.
Morbidity. Eight patients (16.7%) had major early morbidity. In open surgery, four patients had partial transection of ureter, reoperations for bleeding, or percutaneously drained intra-abdominal abscess. In laparoscopic surgery, four patients had rectal perforation necessitating temporary ostomy, incarcerated hernia, hematoma fromtrocar-induced lesion of inferior epigastric artery, or lung embolus. Three patients (6.3%) had delayed morbidity with operations for incisional hernia, intestinal obstruction, and anastomotic stricture including a temporary ostomy. Four patients (8.3%) had additional surgery in order to improve outcome, of whom three had operations for proctocele and transanal stapled resection ofmucosal prolapse (n = 2). One patient with a persisting enterocele had at defecation pain and incomplete evacuation of stool, that was relieved by stretching close to supine position. She underwent a laparoscopic suture of anterior rectum to anterior pelvic peritoneum that removed the enterocele and relieved her symptoms. A fifth patient improved from increased constipation after resection rectopexy, by sacral nerve stimulation.
|
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: The patients were examined in the outpatient clinic preoperatively and at short-term followup (Table 1), mainly by two consultants involved in their treatment. At long-term followup the patients were evaluated by phone interview by an unfamiliar trainee.
Selective loss to follow up: Not included in analysis (1 died, 3 didn’t respond)
Identification confounders and correction in analysis: No
Funding: No conflict of interests. |
|
Karas 2011 |
Design Multicentre RCT
N = 252
Country 21 countries |
Aim of the study: to test the hypothesis that recurrence rates following no rectopexy are not inferior to those following rectopexy for fullthickness rectal prolapse (FTRP)
Inclusion criteria All patients older than 18 years presenting at the participating centers with FTRP were candidates for inclusion in the study provided that they were medically cleared for general anesthesia and that they signed an informed consent.
Exclusion criteria: 1) failure to sign informed consent; 2) no prior surgery for rectal prolapse; 3) no medical clearance to undergo general anesthesia (these patients were considered for perineal surgery under regional anesthesia); and 4) concomitant pelvic floor descent.
|
Intervention abdominal surgery with rectal mobilization only
N = 116
|
Controls abdominal surgery with mobilization and rectopexy.
N = 136
|
Primary outcomes: recurrence rates
Secundary outcomes:
Follow up:
|
Primary outcomes:
|
Clearly defined groups: Yes, In the rectopexy study arm, rectopexy was performed using either a mesh or sutures. Sigmoid resection was added in the case of preexisting documented constipation.
Selection bias: No
Method of assessing the outcome appropriately: Constipation was defined as a Cleveland Clinic Florida score >15, whereas a score ≤15 was considered normal.11
Selective loss to follow up: 10.3% patients were lost to 5-year follow-up
Identification confounders and correction in analysis: No
Funding: This work was supported by research grants from the Western Norway Regional Health Authority, Bergen, Norway; Forde Health System, Forde, Norway; and Ethicon Endo-Surgery, Cincinnati,OH. |
|
Leal 2010 |
Design Cohort study
N = 35
Country Brazil |
Aim of the study: to make a preoperative and postoperative clinical and functional evaluation of patients who underwent transanal repair of rectocele and rectal mucosectomy with a single circular stapler (TRREMS procedure) as treatment for obstructed defecation syndrome (ODS) caused by rectocele and rectal mucosal prolapse (RMP).
Inclusion criteria - female attending the outpatient coloproctology service at Hospital Getu´lio Vargas (Teresina, Brazil) between March 2006 and April 2008. - patients were clinically diagnosed with ODS caused by rectocele grade II or grade III associated with anoscopically confirmed RMP with indications for surgery as all of them had been clinically managed (high fiber diet/laxatives) for a period of at least 4 months.
Exclusion criteria: - Patients with anismus at cinedefecography (no relaxation of the puborectal muscle during evacuation) and other compartment prolapses or fecal incontinence (score[10,0)
|
Intervention rectal mucosectomy with a single circular stapler (TRREMS procedure)
N = 35
|
Controls No
|
Primary outcomes: ODS score, Cleveland Clinic constipation score, functional continence index
Secundary outcomes:
Follow up: 18 ± 7.5 months (range 10–36 months). |
Primary outcomes: This prospective and analytical study included 35 female patients aged 47.5 ± 10.83 years (range 31–67 years). The average duration of surgery was 45 ± 8.77 min (range 33–70 min). All patients were hospitalized for 24 h with no early complications. Five patients (14.28%) experienced late postoperative complications, including three cases (8.57%) of moderate stenosis observed at 1-month followup, two of which (5.72%) resolved spontaneously (the third patient developed annular stenosis of the mucosa and was submitted to stricturotomy). One year after surgery, one patient developed a 3.0-cm granuloma on the suture line, which was resected without complications. Another patient experienced intense pelvic pain, proctalgia, hypogastralgia, sensation of pelvic heaviness and dyspareunia. CT and MRI scans revealed thickening of the anterior rectouterine pouch due to endometriosis. The average ODS score decreased from 10.63 (range 7–17) to 2.91 (range 1–6) (p = 0.001). The average functional continence score fell from 2.77 to 1.71 (p = 0.001), and the average validated Wexner constipation score decreased from 15.23 (range 8–23) to 4.46 (range 1–12) (p = 0.001) after surgery. |
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: Yes
Selective loss to follow up: Not reported
Identification confounders and correction in analysis: No
Funding: Not reported |
|
Lehur 2008 |
Design RCT
N = 119
Country France, Italy and UK |
Aim of the study: to assess the safety and outcomes achieved with stapled transanal rectal resection vs. biofeedback training in obstructed defecation patients.
Inclusion criteria - women patients, aged 18 years or older, diagnosed with ODS associated with rectal intussusception and/or rectocele and candidates for surgical treatment - A minimal ODS score of 7 on structured interviewerled Questionnaires - An adequate external sphincter function on rectal examination and evidence of anterior rectocele and/ or rectal intussusception on dynamic defecography
Exclusion criteria: - clinically evident external sphincter injury, fecal incontinence, enterocele requiring surgery and anterior defect, colpocele, or cystocele requiring a combined surgical approach.
|
Intervention STARR
N = 59
|
Controls three-month electromyographic-based BF training
N = 60
|
Primary outcomes: ODS score, PAC-QOL, continence gradeing scale
Secundary outcomes:
Follow up: 12 months |
Primary outcomes: Among the EP, the mean age (±SD) for STARR patients was 56 (±9.2; range, 34–80) years and for BF patients was 56 (±14.3; range, 24–78) years. Patients assigned to the BF group withdrew at a higher rate than the STARR group (30 (50 percent) vs. 8 (14 percent)), principally the result of high dropout rates at two centers with high enrollment. Sixteen of the 22 BF-treated patients who withdrew cited unsatisfactory results of the procedure. Three STARR and 6 BF patients were lost to follow-up and one STARR patient withdrew as a result of incontinence that needed further investigation and therapy. Safety: Adverse events, a secondary end point in the trial, were experienced by eight (15 percent) STARR patients compared with one (2 percent) BF patient who suffered from anal pain during training sessions. Adverse events included local infection, anorectal pain, incontinence, bleeding, urinary infection, or depression. Two patients who underwent the STARR procedure experienced a serious adverse event, one of which, 12-hour postoperative bleeding, was managed under general anesthesia with additional sutures at the site of hemorrhage. The second event, pain in the right upper abdominal quadrant several weeks after surgery, was considered serious because it required hospital care but was not considered to be related to the study device or study procedure.
|
Clearly defined groups: Yes
Selection bias: No
Method of assessing the outcome appropriately: Yes
Selective loss to follow up:
Identification confounders and correction in analysis: No
Funding: Supported by grants from Ethicon Endo-Surgery (Europe) GmbH, Norderstedt, Germany. |
|
Renzi 2012 |
Design RCT
N = 63
Country Italy |
Aim of the study: to compare the effectiveness and safety of the STARR with 2 circular staplers or with the contour-curved stapler in the treatment of ODS caused by rectocele or rectal intussusception.
Inclusion criteria - All patients with ODS who were candidates for STARR at the Colorectal Surgery Unit of S. Stefano Hospital from November 2005 through September 2007 - ODS score≥12; rectal intussusception (intussusception ≥10 mm) and/or rectocele extending 2 cm or more from the rectal wall contour, as shown by cinedefecography; and failure of 6 months of medical therapy (2 L of water per day and high-fiber diet).
Exclusion criteria: - previous anal and rectal surgery, intestinal inertia, anismus, associated II/III degree genital prolapse, symptomatic cystocele, or any form of anxiety or depression.
|
Intervention STARR with 2 circular staplers (PPH)
N = 31
|
Controls STARR with the contour-curved stapler. (CCS)
N = 32
|
Primary outcomes: ODS score, Wexner score
Secundary outcomes:
Follow up: 12 and 24 months |
Primary outcomes: The PPH group comprised 28 women and 2 men, with a mean age of 53 (SD, 5.2; range, 41–75) years; the CCS group comprised 29 women and 2men, with amean age of 55 (SD, 4.3; range, 38–69) years. The 2 groups did not differ with regard to preoperative ODS score: 15.2 (SD, 2.7) for PPH vs 15.5 (SD, 2.4) for CCS (2-sample T test, P = .64). The mean operative time was 28.1 (SD, 11.5) minutes in the PPH group and 33.1 (15.7) minutes in the CCS group (P=.16; 2-sample T test). The mean length of postoperative hospital stay was 28 (SD, 12.5) hours in the PPH group and 30 (12.6) hours in the CCS group (P = .53; 2-sample T test). At 24 months, an overall successful outcome as defined by ODS symptom scores was achieved in 21 patients (70.0%) in the PPH group and in 27 patients (87%) in the CCS group (P = .10).
Figure 3 shows the mean preoperative and postoperative Agachan-Wexner constipation scores in each group. At 12 months, constipation scores had improved in both groups and did not differ between the 2 groups (P= .33; 2-sample T test), whereas at 24 months constipation scores had worsened in the PPH group, resulting in a significant difference between groups (P= .03; 2-sample T test).
|
Clearly defined groups: Yes
Selection bias: No
Method of assessing the outcome appropriately: All patients underwent preoperative clinical evaluation, proctoscopy, and colonoscopy. The severity of ODS was assessed using the Obstructed Defecation Syndrome Score (ODS score). The validated Agachan-Wexner constipation scoring system was also administered. All operations (PPH and CCS groups) were performed by a single surgeon. A procedure was considered successful when ODS scores were classed as excellent, good, or adequate, defined as follows: scores of 0 to 3 were classified as excellent, 4 to 6 as good, 7 to 9 as adequate, and 10 to 20 as poor.
Selective loss to follow up: Two patients (3.2%), 1 in each study group, did not return after surgery; no postoperative data could be obtained for these patients.
Identification confounders and correction in analysis: No
Funding: This trial was not supported by any commercial company. |
|
Samaranayaka 2010
|
Design Systematic review
N = 12 articles |
Aim of the study: This systematic review assesses the effectiveness of ventral rectopexy (VR) surgery for treatment of rectal prolapse (RP) and rectal intussusception (RI) in adults.
Inclusion criteria randomized controlled trials (RCTs) or nonrandomized studies in any language; more than ten adult patients; receiving ventral mesh rectopexy surgery for RP or RI and stated outcome measures of recurrence, constipation and ⁄ or FI rates of patients.
Exclusion criteria:
|
Intervention Ventral rectopexy
N = 728 patients
|
Controls No
N =
|
Primary outcomes: recurrence, constipation and ⁄ or FI rates
Secundary outcomes:
Follow up:
|
Primary outcomes:
|
Clearly defined groups: Yes
Selection bias: Not applicable
Method of assessing the outcome appropriately: MEDLINE, EMBASE, Scopus and other relevant databases were searched to identify studies. Randomized controlled trials or nonrandomized studies with more than 10 patients receiving ventral mesh rectopexy surgery were considered for the review.
Selective loss to follow up: Not applicable
Identification confounders and correction in analysis: Not applicable
Funding: Not reported |
|
Schiedeck 2005 |
Design Cohort study
N = 150
Country Germany |
Aim of the study: Therapeutic concept for rectal prolapse at a German institution
Inclusion criteria - All patients who underwent elective laparoscopic surgery for rectal prolapse within a 10-year period (January 1993 to November 2003)
Exclusion criteria:
|
Intervention laparoscopic procedures for rectal prolapse
N = 150
|
Controls No
|
Primary outcomes: Recurrence reate
Secundary outcomes:
Follow up: mean of 38 (range 8–120) months |
Primary outcomes: Conversion to open resection was necessary in three patients (2.0%). Thus, laparoscopic operation could be completed in 147 patients (11 male, 136 female, mean age 64.4 (range 21–90) years) representing a laparoscopic completion rate of 98.0%. Most common indication for surgery was rectal prolapse II–III0 combined with sigmoidocele (n=87, 59.2%), followed by rectal prolapse III0 (n=40, 27.2%) and rectal prolapse II–III0 combined with chronic diverticulitis (n=20, 13.6%). With regard to the degree of rectal prolapse, 50 patients had rectal prolapse II0 (34.0%), 71 had rectal prolapse III0 (48.3%), and 26 patients had rectal prolapse of different stages combined with outlet-obstruction by either sigmoidocele III0 or chronic diverticulitis (17.7%). Most common procedure was laparoscopic resection–rectopexy, in 108 patients (73.3%), followed by suture rectopexy (n=32, 21.8%) and sigmoid resection (n=17, 11.9%). Intraoperatively, no complications associated with laparoscopy occurred. Overall morbidity rate was 22.4% (n=33) including 25 patients with minor complications (17.0%) and eight with major complications (5.4%). Most common major complication requiring re-operation was hemorrhage, in four patients (2.7%). In terms of late-onset complications, two porthernias were diagnosed. Follow-up study by telephone interview (90 of 150 patients available to date) showed recurrence of rectal prolapse in three of 90 patients (3.3%).
|
Clearly defined groups: In our policy, the following classification system is used: rectal prolapse I0 is defined by a rectal intussusception above the anal canal (internal or incomplete prolapse); rectal prolapse II0 is an intussusception of the rectal wall into the anal canal, diagnosed by proctoscopy, whereas a complete (“full-thickness”) rectal prolapse through the anus is represented by rectal prolapse III0
Selection bias: Not expected
Method of assessing the outcome appropriately: Prospective follow-up included recurrence and was performed by telephone interview.
Selective loss to follow up: Yes, follow-up available for 90 patients
Identification confounders and correction in analysis: No
Funding: Not reported |
|
Tsunoda 2003 |
Design Cohort study
N = 31
Country Japan |
Aim of the study: was to investigate the clinical, functional, and physiologic results of Delorme’s procedure.
Inclusion criteria - patients with external rectal prolapse were treated by Delorme’s procedure at Showa University Hospital between January 1994 and February 2002. - No patient had undergone previous surgery for rectal prolapse.
Exclusion criteria:
|
Intervention Delorme’s procedure
N = 31
|
Controls No
|
Primary outcomes: Recurrence rate
Secundary outcomes:
Follow up: median 39 (range 6–96) months. |
Primary outcomes: Their mean age was 70 (range, 14–93) years. The prolapse was full thickness, circumferential, and at least 5 cm. Prolapse recurrence was observed in four patients, with a mean recurrence time of 14 (range, 3–25) months. There were no postoperative deaths, but four patients died of nonrelated conditions six months, one, two, and three years after the procedure, respectively. Minor postoperative complications occurred in four patients (minor dehiscence, wound infection, bleeding, fever). The median (range) preoperative incontinence score in the remaining 26 patients significantly improved from 11.5 (1–20) to 6.0 (0–20) after operation (P < 0.0001) |
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: Yes
Selective loss to follow up: No
Identification confounders and correction in analysis: No
Funding: Not reported |
|
Tou 2008
|
Design Cochrane review and meta-analysis
N = 12 trials including 380 patients |
Aim of the study: To determine the effects of surgery on the treatment of rectal prolapse in adults.
Inclusion criteria - All adults with rectal prolapse (through the anus) as diagnosed and included by the trialists.
Exclusion criteria:
|
Intervention See primary outcome
N =
|
Controls See primary outcome
N =
|
Primary outcomes: - number of patients with recurrent rectal prolapse, - number of patients with residual mucosal prolapse, - number of patients with faecal incontinence or constipation.
Secundary outcomes: - Participant symptoms - Clinical end points
Follow up: 1 trial < year 11 trials 1-5 year |
Primary outcomes: Comparison 1. Surgical versus no intervention There were no trials comparing surgery with no treatment.
Comparison 3. Abdominal versus perineal approach One trial (Deen 1994) compared perineal rectosigmoidectomy and pelvic floor repair in 10 people with abdominal resection rectopexy and pelvic floor repair in another 10.
Comparison 4. Methods of performing rectopexy 4c. Preservation versus division of the lateral ligaments during open mesh rectopexy Three small trials compared the effects of preservation versus division of lateral ligaments during open mesh rectopexy (Speakman 1991; Selvaggi 1993; Mollen 2000 NEW). The Selvaggi trial was available in an abstract format and datawere insufficiently reported to allow any statistical analyses to be performed.
Comparison 6. Laparoscopic versus open mesh rectopexy procedure Laparoscopic mesh rectopexy was compared with open mesh rectopexy in two trials (Boccasanta 1998; Solomon 2002). There was a subsequent cost analysis for participants that were involved in the Solomon trial (Salkeld 2004).
Two small trials compared resection of redundant bowel in one group versus no resection in the other (both groups had a rectopexy). In one trial (Lukkonen 1992), resection was combined with suture rectopexy and compared with mesh rectopexy alone. In the other (McKee 1992), suture rectopexy was performed in both groups but resection in only one group.
|
Clearly defined groups: Yes
Selection bias: Not expected
Method of assessing the outcome appropriately: They searched the Cochrane Incontinence Group Specialised Register (searched 10 January 2008), the Cochrane Colorectal Cancer Group Trials Register (searched 10 January 2008), CENTRAL (Issue 1, 2008), PubMed (1 January 1950 to 10 January 2008) and EMBASE (1 January 1998 to 10 January 2008). The British Journal of Surgery (January 1995 to January 2008) and the Diseases of the Colon and Rectum (January 1995 to January 2008) were specifically hand searched. All randomised or quasi-randomised trials of surgery in the management of adult rectal prolapsed were selected.
Selective loss to follow up: Not applicable
Identification confounders and correction in analysis: No
Funding: Not applicable
|
|
Youssef 2013 |
Design RCT
N = 82
Country Egypt |
Aim of the study: To compare Delorme operation alone or with postanal repair and levatroplasty in treating complete rectal prolapse.
Inclusion criteria - patients, who were treated for complete rectal prolapse at the colorectal surgery unit of Mansoura University Hospital, Mansoura, Egypt, during the period from January 2007 to June 2011
Exclusion criteria: - pregnant female, any patients with previous anal surgery, pudendal nerve neuropathy, anal fistula, and sepsis, age above 80 years, vascular disease, scleroderma, malnutrition, or coagulopathy.
|
Intervention Delorme operation only (GI)
N = 41
|
Controls Delorme operation with postanal repair and levatorplasty (GII)
N = 41
|
Primary outcomes: recurrence rate
Secundary outcomes: improvement of constipation, incontinence, operative time, anal manometery and postoperative complications
Follow up:
|
Primary outcomes:
|
Clearly defined groups: Yes
Selection bias: No
Method of assessing the outcome appropriately: All assessments were conducted by investigators who were blinded to the experimental condition. A recurrence was defined as full-thickness protrusion of the neorectal bowel wall. The standardized Wexner constipation score was used to investigate the level of constipation before and after the operation. The Pescatori classification was used to grade fecal incontinence.
Selective loss to follow up: 3 women were loss to follow up
Identification confounders and correction in analysis: No
Funding: No financial disclosures |
Beoordelingsdatum en geldigheid
Publicatiedatum : 27-03-2015
Beoordeeld op geldigheid : 13-11-2014
Omdat deze richtlijn modulair is opgebouwd, kan herziening op onderdelen eenvoudig plaatsvinden. Een eerste moment zal zeker medio 2015-2016 zijn als nieuwe gegevens van, ten tijde van de richtlijnontwikkeling lopende, studies beschikbaar komen. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Obstetrie en Gynaecologie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Ook in samenwerking met:
- Nederlandse Vereniging voor Fysiotherapie bij Bekkenproblematiek en Pré- en Postpartum gezondheidszorg
De richtlijnontwikkeling werd ondersteund door de Orde van Medisch Specialisten en de richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel is om gynaecologen, maag-darm-leverartsen, urologen, bekkenfysiotherapeuten, radiologen en chirurgen te voorzien van een landelijke door de relevante beroepsverenigingen gedragen richtlijn die voldoet aan de eisen van een AGREE-instrument volgens de EBRO-methode met betrekking tot het voorkomen van prolaps en het behandelen van vrouwen met een prolaps. De te ontwikkelen richtlijn voorziet in de meest recente 'evidence based' informatie over prolaps.
Met het opstellen van een dergelijke richtlijn wordt beoogd de onduidelijkheid en onzekerheid over het voorkomen, diagnosticeren en het behandelen van een prolaps te verminderen.
De richtlijn kan worden gebruikt door alle zorgverleners die betrokken zijn bij de zorg voor vrouwen met een (verhoogd risico op een) prolaps, maar is primair geschreven voor leden van de beroepsgroepen die aan de ontwikkeling van de richtlijn hebben bijgedragen.
Doelgroep
De richtlijn geldt voor alle vrouwen die medische zorg krijgen vanwege prolaps(klachten).
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2012 een multidisciplinaire werkgroep ingesteld bestaande uit vertegenwoordigers van alle relevante beroepsgroepen die betrokken zijn bij het zorgproces in de eerste en tweede lijn van vrouwen met een (verhoogd risico op een) prolaps. De beroepsgroepen zijn de Nederlandse Vereniging voor Radiologie (NVvR), de Nederlandse Vereniging voor Urologie (NVU), de Nederlandse Vereniging van Maag-Darm-Leverartsen (MDL), de Nederlandse Vereniging Voor Heelkunde (NVvH), de Nederlandse Vereniging voor Fysiotherapie bij Bekkenproblematiek en Pré- en Postpartum gezondheidszorg (NVFB) en de Nederlandse Vereniging voor Obstetrie & Gynaecologie (NVOG). De werkgroepleden waren door de bovengenoemde wetenschappelijke verenigingen gemandateerd voor deelname aan deze werkgroep. De werkgroepleden zijn gezamenlijk verantwoordelijk voor de integrale tekst van deze conceptrichtlijn. Een partij die geen zitting had in de werkgroep maar wel voor extern advies geraadpleegd werd gezien hun mede betrokkenheid bij het onderwerp is de Vereniging van Continentie Verpleegkundigen & Verzorgenden (CV&V).
- Dhr. J.P. Roovers, uro-gynaecoloog, Academisch Medisch Centrum, Amsterdam (voorzitter)
- Mw. E. Everhardt, gynaecoloog, Medisch Spectrum Twente, Enschede
- Mw. V. Dietz, gynaecoloog, Catharina ziekenhuis, Eindhoven
- Dhr. A.L. Milani, uro-gynaecoloog, Reinier de Graaf Gasthuis, Delft
- Dhr. A.H.P. Meier, uroloog, Vie Curi, Venlo
- Mw. E.C.J. Consten, colorectaal chirurg, Meander Medisch Centrum, Amersfoort
- Dhr. J.J. Futterer, radioloog, Universitair Medisch Centrum St. Radboud, Nijmegen
- Mw. R.J.F. Felt-Bersma, maag-darm-lever arts, VU Medisch Centrum, Amsterdam
- Mw. M.C.Ph. Slieker-ten Hove, bekkenfysiotherapeut, Erasmus Medisch Centrum, Rotterdam
- Mw. T. Steenstra Touissant, AIOS gynaecologie, Kennemer Gasthuis, Haarlem
- Mw. C.A.L. van Rijn, AIOS gynaecologie, Sint Franciscus Gasthuis, Rotterdam
- Mw. F. Vlemmix, AIOS gynaecologie, Kennemer Gasthuis, Haarlem
- Mw. K. Notten, AIOS gynaecologie
- Dhr. J.J. Van Iersel, ANIOS chirurgie, Meander Medisch Centrum, Amersfoort
- Dhr. T.A. van Barneveld, klinisch epidemioloog, Orde van Medisch Specialisten, Utrecht
- Dhr. K.Y. Heida, richtlijnondersteuner Nederlandse Vereniging van Obstetrie en Gynaecologie, Utrecht
Belangenverklaringen
De belangen van de werkgroepleden werden geïnventariseerd met het door KNAW, KNMG en OMS opgestelde belangenverklaringsformulier. De gemelde belangen zijn besproken in de werkgroep en met vertegenwoordigers van het bestuur van de NVOG. Geconcludeerd werd dat de werkgroep evenwichtig was samengesteld en dat er geen bezwaren waren tegen deelname aan de werkgroep en besluitvorming (proportionaliteitsbeginsel, zie Code KNMG, KNAW, OMS).
Inbreng patiëntenperspectief
Voor ontwikkeling van een goede richtlijn is de input van patiënten nodig. Een behandeling moet immers voldoen aan de wensen en eisen van patiënten en zorgverleners. Patiënten kunnen zorgverleners die een richtlijn ontwikkelen helpen om te begrijpen hoe het is om met een ziekte of aandoening te leven of om er mee geconfronteerd te worden. Op deze manier kan bij het ontwikkelen van een richtlijn beter rekening gehouden worden met de betekenis van verschillende vormen van diagnostiek, behandeling en zorg voor patiënten. Het in kaart brengen van de behoeften, wensen en ervaringen van patiënten met de behandeling biedt tevens de gelegenheid om de knelpunten in kaart te brengen. Wat zou er volgens patiënten beter kunnen? Een patiënt doorloopt het hele zorgtraject, een behandelaar ziet vaak slechts het stukje behandeling waarin hij zich heeft gespecialiseerd. Daarom is het zinvol ook knelpunten vanuit patiëntenperspectief in kaart te brengen om de kwaliteit van de behandeling te verbeteren. In de beginfase van de ontwikkeling van deze richtlijn is een knelpuntenanalyse gedaan door middel van een groepsinterview met patiënten (focusgroep). Vanuit de poliklinieken werden patiënten, die minimaal drie maanden en maximaal vijf jaar geleden een prolaps behandeling hadden ondergaan, gevraagd om deel te nemen aan het focusgroep gesprek. Een verslag van de focusgroep is besproken in de werkgroep en de belangrijkste knelpunten zijn geadresseerd in de richtlijn. De hier voorliggende conceptrichtlijn is voor commentaar voorgelegd aan deelnemers van de focusgroep.
Verslag focusgroepbijeenkomst “Prolaps” van 13 november 2012.
In dit document worden de aandachtspunten die volgen uit het focusgroep gesprek van 13 november 2012 uitgelicht.
Doel van het focusgroep gesprek:
Vanuit patiënten inzichtelijk maken hoe de zorg aan vrouwen met een prolaps, patiëntgerichter kan.
Deelneemsters aan het focusgroep gesprek:
In samenwerking met de gynaecologen van de werkgroep richtlijnontwikkeling prolaps, werden deelnemers benaderd en geselecteerd. Er namen in totaal 11 vrouwen deel.
De gespreksstructuur:
Het gesprek werd gestructureerd door chronologisch het zorgproces door te spreken: het stellen van de diagnose prolaps, de begeleiding tot aan de ingreep, de ingreep zelf, de nazorg/follow-up. De belangrijkste aandachtspunten worden in dit verslag uitgelicht, gegroepeerd naar bovenstaande zorgmomenten.
Algemene punten, voor verbetering van het multidisciplinaire zorgproces:
De diagnose prolaps werd gesteld
Klachten en verwijzing:
- De klachten van een prolaps zijn lastig als dusdanig te herkennen en niet eenduidig. Hierdoor werden in sommige gevallen deze klachten niet door de huisarts herkend. Het heeft bij een aantal patiënten hierdoor lang geduurd alvorens de diagnose werd gesteld.
- Over het algemeen werden patiënten via de huisarts verwezen naar de gynaecoloog die vervolgens de definitieve diagnose stelde.
- In sommige gevallen werden patiënten eerst door de huisarts behandeld of verwezen naar een bekkenfysiotherapeut alvorens ze werden verwezen naar een specialist (gynaecoloog, uroloog of maag-darm-leverarts).
- Verwijzing door de huisarts verschilde per persoon en was afhankelijk van het klachtenpatroon. In een aantal gevallen werden patiënten eerst doorverwezen naar een specialist die vervolgens concludeerde dat het probleem niet op zijn/haar vakgebied ligt en patiënten werden weer retour verwezen naar de huisarts. Dit werd als vervelend ervaren. Dit zou niet nodig hoeven zijn als er in eerste instantie goed gekeken wordt.
- Door deze verwijzingen over en weer werden de patiënten door meerdere zorgverleners gezien en lichamelijk onderzocht alvorens de definitieve diagnose werd gesteld. Dit werd door een aantal patiënten als vervelend ervaren.
- Verwijzing naar een bekkenbodemcentrum/speciaal bekkenbodempoli werd ook genoemd. Niet iedereen was op de hoogte dat er zulke centra zijn in Nederland. Wellicht zijn ook de huisartsen niet goed op de hoogte van deze centra.
- Voordeel van een bekkenbodemcentrum danwel van de bekkenbodempoli is dat in één dag alle gesprekken en onderzoeken plaatsvinden (vaak in tweetallen: incontinentieverpleegkundige, gynaecoloog, uroloog, bekkenfysiotherapeut). De uitslag wordt dezelfde dag nog bekendgemaakt.
- Nadeel van deze methode is dat er weinig ruimte en aandacht is voor de emotionele en psycho-sociale impact van de verzakkingsproblemen op de patiënt.
- De emotionele aspecten konden over het algemeen wel besproken worden met de gynaecoloog, echter in het vervolgtraject was weinig aandacht voor dit aspect.
Diagnostiek:
- De onderzoeken die patiënten ondergingen werden over het algemeen niet als vervelend ervaren.
- In sommige gevallen werden door verschillende artsen dezelfde onderzoeken opnieuw gedaan. Dit werd wel als onnodig en vervelend ervaren. Het woord ‘kijkdoos’ wordt meerdere keren genoemd in dit kader van veel lichamelijk onderzoek door verschillende zorgverleners.
- Als oplossing werd gegeven de mogelijkheid van diagnostiek in een bekkenbodemcentrum/poli waarbij alle onderzoeken in één dag werden gedaan en waar de verschillende specialisten bij betrokken zijn.
- De vragenlijsten die over de bekkenbodemproblemen gaan, gaan heel beknopt in op seksuele dysfunctie, er wordt verder in het traject niet meer op dit probleem ingegaan.
Samengevat: klachten van een prolaps zijn veelal niet bekend en worden niet als dusdanig herkend, patiënten blijven lang rondlopen met klachten. Verwijzing van de huisarts naar een specialist kan meer gestructureerd (bekkenbodem centrum/poli) en communicatie tussen de zorgverleners is hierin belangrijk. Naast de medische aspecten dienen ook de emotionele aspecten van verzakkingsproblemen aandacht te krijgen.
Behandeling:
Informatie over prolaps en behandelopties
- Over het algemeen werden patiënten voorgelicht over wat voor een verzakking de patiënten hadden, de klachten van een verzakking en wat de mogelijke behandelopties zijn met de voor- en nadelen van de behandeling. Ze hadden het gevoel mee te mogen beslissen over de behandeling. Dit werd als positief ervaren.
- In een aantal gevallen was er geen mogelijkheid tot “meebeslissen” over de behandeling. Er werden geen opties besproken. Of er werden geen voor- en nadelen besproken van de ingreep. Door het gemis aan informatie hadden ze niet de mogelijkheid een weloverwogen keuze te maken.
- Er werd aangegeven dat er bijna niet wordt gesproken in de gesprekken over consequenties van een ingreep op seksueel gebied.
- Conservatieve behandelopties werden veelal niet besproken. Twee patiënten hadden een pessarium gekregen (één patiënt i.v.m. nog een kinderwens). Deze bleek in hun specifieke geval afdoende te zijn en de patiënten zijn tevreden over de behandeling met een pessarium. Voordeel is dat patiënten zelf het pessarium in en uit kunnen doen en ze hoeven geen operatie te ondergaan.
- Het overgrote deel gaf aan geen informatie te hebben gekregen over de mogelijkheid van een ‘ring’ als behandeling. Uitleg werd gegeven dat het heel erg afhankelijk is van de soort verzakking en van de ernst van de verzakking of een ‘ring’ effectief is.
- Er wordt onvrede uitgesproken over het ‘matje’, als zo’n techniek zoveel complicaties geeft, waarom gebruiken jullie het dan nog? Er werd uitleg gegeven dat het ‘matje’ in sommige gevallen de laatste behandeloptie is. Dat het niet gebruikelijk is deze als eerste behandeloptie te kiezen. Dat er verschillende soorten ‘matjes’ zijn en dat het afhankelijk is van de soort verzakking en de ernst van de verzakking welke behandeling het beste is. Daarnaast blijft de patiënt de keuze hebben of zij een ‘matje’ wil.
- Er werd aangegeven dat de mondelinge informatie ondersteunt zou moeten worden met schriftelijke informatie. Door middel van een folder met duidelijke uitleg over de verzakking en de mogelijke behandelopties (ondersteunt met plaatjes/foto’s, in begrijpelijke taal, maar ook met de Latijnse benaming voor het eventueel opzoeken op internet).
- Over het algemeen was er ruimte voor een extra gesprek een aantal dagen voorafgaand aan de operatie om nogmaals de behandeling door te spreken of om vragen te stellen. In sommige gevallen werd dit telefonisch gedaan. Telefonische informatieoverdracht werd als minder prettig ervaren dan een lijfelijk gesprek.
Instructies en procedure voorafgaand aan de ingreep
- Een enkeling is voorafgaand aan de ingreep naar een bekkenfysiotherapeut geweest voor oefeningen en training van de bekkenbodem. De oefeningen en trainingen werden als nuttig ervaren. De frequentie van de afspraken met de fysiotherapeut zou geïndividualiseerd moeten worden. Meerdere herhalingen van uitleg van de oefeningen is niet voor iedereen nodig.
Samengevat: er is behoefte aan goede en volledige informatie (evt. schriftelijk) over de verzakking, de behandelopties en de daarbij behorende voor- en nadelen, zodat een weloverwogen beslissing kan worden genomen door de patiënt samen met de behandelaar over de uiteindelijke keuze van de behandeling. Eventuele conservatieve behandelingsopties zouden overwogen moeten worden. Naast mondelinge informatie is er behoefte aan schriftelijke informatie.
De ingreep en opname:
- Over het algemeen werden er goede instructies gegeven na de ingreep (bij ontslag) over wat je allemaal wel en niet mocht doen. Er werden praktische voorbeelden gegeven, niet bukken, stofzuigen, sporten, niet hoesten/niezen, niet persen op het toilet etc.
- Geen of onvoldoende informatie werd gegeven over instructies voor het opstaan uit stoel of bed, hygiëne en schoonmaakinstructies, instructies over pijnstilling en adviezen omtrent seksuele mogelijkheden. Voorbeeld: de helft van de patiënten kreeg laxantia mee voor preventie obstipatie, de andere helft niet.
- Bij het optreden van complicaties of pijn was het niet altijd duidelijk bij wie ze terecht konden hiermee. Sommigen werden verwezen naar de huisarts, anderen naar de gynaecoloog.
- Sommige ziekenhuizen hebben folders of een hand-out met instructies. Een folder met standaardinformatie zou eigenlijk altijd meegegeven moeten worden.
- Iedereen kreeg een nacontrole ongeveer 6 weken na de operatie.
Samengevat: er is behoefte aan goede instructies na de ingreep over wat men aan fysieke activiteiten kan en mag, schoonmaakinstructies, instructies over pijnstilling en uitleg over bij wie ze terecht kunnen bij problemen (huisarts, gynaecoloog) en uitleg over mogelijkheden op seksueel gebied. Naast mondelinge instructies is er behoefte aan schriftelijke instructies.
Follow-up en nazorg:
- De meeste patiënten hebben contact gehad met een bekkenfysiotherapeut voorafgaand aan een ingreep. Er is behoefte om ook na een ingreep instructies te krijgen over oefeneningen van de spieren van de bekkenbodem om een recidief verzakking te voorkomen. Dit wordt veelal niet aangeboden.
- De kosten voor de bekkenfysiotherapie zijn onduidelijk. In hoeverre wordt dit vergoed door de verzekeraar?
- Er is behoefte aan gerichte leefregels ter voorkoming van een recidief.
- Er is behoefte aan respect van de zorgverlener voor de impact van een ingreep voor de patiënt en voor de geestelijke gesteldheid. Pijn, seksuele dysfunctie, recidief mogelijkheden moeten bespreekbaar worden gemaakt. Deze mening werd niet door alle patiënten gedeeld.
- Er wordt aangegeven dat een aantal patiënten synapause hebben gekregen voor een beter herstel, een deel heeft dit niet gehad.
Samengevat: er is behoefte aan leefregels ter voorkoming van een recidief. Dit zou idealiter via een bekkenfysiotherapeut kunnen verlopen. Die kan dan ook gerichte oefeningen geven voor versteviging van de bekkenbodem. Er moet in het nazorgtraject aandacht zijn voor eventuele problemen met betrekking tot pijn, seksuele dysfunctie en recidieven.
Samenvatting van de aanbevelingen die zouden kunnen worden gemaakt aan de hand van dit gesprek:
- Adequate kennis in de eerste lijn over klachten en diagnostiek aangaande prolaps is van belang om patiënten gericht door te kunnen verwijzen.
- Multidisciplinaire aanpak van een prolaps zal onnodig dubbel lichamelijk onderzoek kunnen voorkomen evenals foutieve of meervoudige verwijzingen. Bekkenbodemcentra/poli’s zouden hier goed bij aansluiten.
- Informatie over de verzakking en de behandelopties met de voor- en nadelen dienen met de patiënt besproken te worden.
- Patiënten moeten de mogelijkheid krijgen een weloverwogen beslissing te kunnen nemen over hun eigen behandeling, dit kan door al de behandelopties met de voor- en nadelen met de patiënt te bespreken.
- Er is behoefte aan een informatiefolder of betrouwbare informatie op het internet over verzakkingsklachten en de behandelopties.
- Er is behoefte aan (schriftelijke) instructies voor na de operatie over wat men wel en niet mag op fysiek gebied, maar ook instructies over pijnstilling, schoonmaakinstructies en seksuele instructies.
- Er dient duidelijk aangegeven te worden bij wie de patiënt terecht kan voor haar vragen in het nazorgtraject.
- Bekkenfysiotherapie zou aan iedere vrouw aangeboden moeten worden, omdat het, naast eventueel effect op de klachten, ook kan bijdragen bij het verwerkingsproces, voor het wegnemen van onzekerheden bij de vrouw en voor het geven van praktische tips.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is geprobeerd rekening te houden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
Tevens is een specifiek implementatieplan opgesteld waarin per aanbeveling barrières voor invoering zijn geïnventariseerd en wordt aangegeven op welke termijn de werkgroep de invoering van de betreffende aanbeveling realistisch acht. Ook heeft de werkgroep een inschatting gemaakt van de kostenaspecten die samenhangen met de invoering van de betreffende aanbeveling.
De richtlijn wordt verspreid onder alle relevante beroepsgroepen en ziekenhuizen. Daarnaast is een patiëntenfolder opgesteld (in ontwikkeling). Ook is de richtlijn te downloaden vanaf de websites van de Nederlandse Vereniging voor Obstetrie en Gynaecologie: www.nvog.nl.
Werkwijze
De werkgroep werkte gedurende twee jaar aan de totstandkoming van de conceptrichtlijn. De werkgroepleden zochten systematisch naar de literatuur en beoordeelden de kwaliteit en inhoud ervan. De richtlijnondersteuner maakte, in samenspraak met de subwerkgroep die voor elk hoofdstuk was aangesteld, evidencetabellen om deze vervolgens te vertalen in GRADE tabellen. Een samenvatting van de evidence met de conclusies werd teruggekoppeld aan de gehele werkgroep waarna gezamenlijk de overige overwegingen en aanbevelingen werden geformuleerd. Tijdens vergaderingen werden teksten toegelicht en werd door de werkgroepleden meegedacht en gediscussieerd. De uiteindelijke teksten vormen samen de hier voorliggende conceptrichtlijn.
Knelpuntenanalyse
De werkgroep heeft een analyse gemaakt van knelpunten die in de dagelijkse praktijk belangrijk zijn om de zorg voor vrouwen met een verzakking te verbeteren. Met name bestond er onduidelijkheid over de rol van beeldvormend onderzoek, de toegevoegde waarde van urodynamisch onderzoek, het te verwachten effect van leefstijladviezen en bekkenfysiotherapie, de afweging om een pessarium of operatie voor te stellen als behandeling, en de eerste keus operatie bij vrouwen met een interne of externe rectum prolaps. Op basis hiervan is een concept raamwerk van de in de richtlijn te bespreken onderwerpen opgesteld. Om de richtlijn zoveel mogelijk te laten aansluiten bij de dagelijkse praktijk is vervolgens een invitational conference georganiseerd. Hiervoor zijn diverse stakeholderpartijen uitgenodigd, zoals: zorgverzekeraars, Inspectie voor de Gezondheidszorg, patiëntenorganisaties, organisaties van zorginstellingen, en het College voor Zorgverzekeringen. Met deze partijen is het door de werkgroep opgestelde raamwerk besproken en nader geëxpliciteerd. Ook zijn stakeholderpartijen gevraagd aanvullingen te geven en zijn hun verwachtingen over de richtlijn en het richtlijnontwikkelingsproces geïnventariseerd. De werkgroep heeft vervolgens een prioritering aangebracht van in de richtlijn te behandelen onderwerpen en het raamwerk van de richtlijn definitief vastgesteld.
Uitgangsvragen en uitkomstmaten
Alvorens te starten met de literatuurselectie werden door de werkgroep klinisch relevante uitkomstmaten en acceptabele meetinstrumenten gedefinieerd. Ook definities voor andere relevante variabelen werden afgestemd. Bij de beoordeling van de literatuur heeft de werkgroep vooral gekeken naar studies waarbij, naar inzicht van de werkgroepleden, klinisch relevante uitkomstmaten gebruikt werden. Deze werden voorafgaand aan de literatuurselectie door de werkgroep bepaald en gedefinieerd. Ook heeft de werkgroep voorafgaand aan de search bepaald welke instrumenten voor het meten van de uitkomst zouden worden geselecteerd. Onderstaande is een overzicht van door de werkgroep opgestelde klinisch relevante uitkomstmaten en daarbij opgestelde geaccepteerde meetinstrumenten met klinisch relevante afkappunten:
|
Uitkomstmaten |
Gekozen meetinstrumenten en (klinisch relevante afkappunten) |
|
Module Anorectaal functieonderzoek en module Chirurgische behandeling van rectum prolaps |
|
|
Fecale incontinentie |
Wexner incontinence score (aanverwant ‘Scores uitkomstmaten’) (zelfde als Cleveland Clinic Incontinence Score (CCIS)) |
|
FISI - Fecal Incontinence Severity Index |
|
|
Obstipatie |
Wexner obstipatie score (aanverwant ‘Scores uitkomstmaten’) (zelfde als Cleveland Clinic Constipation Score (CCCS)) |
|
Obstructed defecation syndrome (ODS) score |
|
|
|
Rome criteria (aanverwant ‘Scores uitkomstmaten’) |
|
Module Pessarium therapie bij prolaps |
|
|
Kwaliteit van leven |
Sheffield POP scale questionnaire (SPS-Q); Pelvic Floor Distress Inventory (PFDI); Pelvic Floor Impact Questionnaire (PFIQ); Sexual Function Questionaire (SFQ) |
|
Module Chirurgische behandeling van vaginale prolaps |
|
|
Primair: subjectief |
Afwezigheid balgevoel (bulge) |
|
|
Patient tevredenheid; PGI-I (much or very much better) |
|
Primair: objectief
|
Diepste punt (punt Ba, Bp of C) van behandelde compartiment op of boven hymen (0)2 |
|
Diepste punt (Ba, Bp of C) behandelde compartiment; stadium 0 en I (dus diepste punt van prolaps ≤ -2)3 |
|
|
Leading edge (dus ‘overall prolapse’, onafhankelijk van behandelde compartiment), zoals beschreven onder I (op of boven hymen) en II (-2 of minder) |
|
|
*I is belangrijkste, als I niet wordt gerapporteerd dan II (NIH criteria), voor III geldt dezelfde prioritering. |
|
|
Secundair: subjectief |
Quality of life: mate van verbetering (met behulp van effect sizes*) in domeinscores van UDI, DDI, IIQ of PFDI-20, PFIQ-7 en overall scores PISQ-12 of domeinen van PISQ-31 |
|
Bij afwezigheid van rapportering effect sizes de statistisch significante veranderingen in de genoemde domeinscores |
|
|
* klinisch relevant is bij effect size van 0.8 of groter |
|
|
Secundair: objectief |
Heroperatie voor prolaps in zelfde compartiment |
|
|
Heroperatie wegens de novo prolaps onbehandelde compartiment (binnen een jaar) |
|
|
of heroperatie voor andere aandoening, bv (ontmaskerde) urine incontinentie, mesh exposure, of pijn (dyspareunie?) |
|
Secundair: complicaties |
Onbedoelde schade aan blaas en /of darm direct hersteld zonder re-operatie |
|
Infectie/ hematoom/ abces |
|
|
Postoperatieve pijn volgens score a t/m e:
|
|
Strategie voor zoeken en selecteren van literatuur
Per uitgangsvraag werden ten minste twee werkgroepleden aangesteld om onafhankelijk van elkaar de literatuur te beoordelen op relevantie. Bij deze selectie van titel en abstract werden de volgende exclusiecriteria gehanteerd:
- niet van toepassing op de vraagstelling;
- niet vergelijkbaar met de Nederlandse populatie;
- niet-gedefinieerde uitkomstmaat;
- minder dan 10 vrouwen in de onderzoekspopulatie (wegens imprecisie);
- niet primair onderzoek;
- case reports, case series, letters, abstracts.
Kwaliteitsbeoordeling individuele studies
Na selectie door de werkgroepleden bleven de artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De geselecteerde artikelen zijn vervolgens door minimaal twee werkgroepleden op volledige tekstinhoud beoordeeld en daarna beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs. Hierbij is de indeling gebruikt, zoals weergegeven in tabel 1.1.
Bij GRADE wordt de evidence per uitkomstmaat beoordeeld. De beoordeling wordt gedaan door het invullen van een evidenceprofiel. Alleen voor kritieke en/of belangrijke uitkomstmaten wordt een evidenceprofiel gemaakt. Er zijn in totaal vijf factoren die de kwaliteit van de evidence per uitkomstmaat kunnen verlagen en drie factoren die de kwaliteit kunnen verhogen. Per factor kan de kwaliteit met één of twee niveaus omlaag gaan. Als het om een ernstige beperking gaat, gaat de kwaliteit met één niveau omlaag; als het om een zeer ernstige beperking gaat, gaat de kwaliteit met twee niveaus omlaag.
De verschillende typen onderzoek kunnen worden ingedeeld naar mate van bewijs. RCTs zijn in beginsel van hogere methodologische kwaliteit dan observationele studies, omdat RCTs minder kans op vertekening (bias) geven. In het GRADE systeem beginnen daarom RCTs met hoge kwaliteit (4) en observationele studies met lage kwaliteit (2). Niet vergelijkende, niet-systematische studies (bijvoorbeeld case series en case reports) zijn altijd van zeer lage kwaliteit.
Een overzicht van de GRADE-indeling van kwaliteit van studies per uitkomstmaat staat in tabel 1.1.
Tabel 1.1 GRADE-indeling van kwaliteit van studies per uitkomstmaat

Samenvatten van de literatuur
De beoordeling van de verschillende artikelen vindt u in de verschillende teksten terug onder het kopje ‘Samenvatting van de literatuur’. De richtlijnondersteuner maakte in samenspraak met de subgroepen per uitgangsvraag evidencetabellen van de geselecteerde individuele studies als hulpmiddel bij het beoordelen en samenvatten van deze studies. Vervolgens wordt de kwaliteit van de evidence op het niveau van de systematische review beoordeeld. Met de kwaliteit van de evidence wordt bedoeld in hoeverre er vertrouwen is dat de aanbevelingen gebaseerd kunnen worden op de (effectschatting van de) evidence en de GRADE tabellen. Het wetenschappelijk bewijs is vervolgens kort samengevat in de ‘conclusies uit de literatuur’. De belangrijkste literatuur waarop deze conclusies zijn gebaseerd staat bij de conclusies vermeld, inclusief de GRADE gradering van bewijs.
Beoordelen van de kracht van het wetenschappelijke bewijs
Er werd gekozen om -volgens de meest recente ontwikkelingen op het gebied van richtlijnen- de methode toe te passen van The Grading of Recommendations Assessment, Development and Evaluation (GRADE) voor het graderen van de kwaliteit van bewijs en de sterkte van de aanbevelingen.
Formuleren van aanbevelingen
Nadat de gegevens uit de GRADE tabellen werden samengevat als tekst werden hieruit conclusies getrokken. Om vervolgens tot een gewogen aanbeveling te komen werden de overige overwegingen besproken en geformuleerd. Dit is van belang omdat voor een aanbeveling naast het wetenschappelijke bewijs ook andere aspecten meegewogen horen te worden, zoals voorkeur van patiënten, kosten, beschikbaarheid van voorzieningen of organisatorische aspecten. Bij de overwegingen spelen de ervaring en opvattingen van de werkgroepleden een rol. De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op zowel het beschikbare wetenschappelijke bewijs als op de belangrijkste overwegingen. De gebruikte methodiek voor richtlijnontwikkeling verhoogt de transparantie van de totstandkoming van de aanbevelingen in deze richtlijn.
Het is van belang dat het verschil tussen normerend waar mogelijk en ruimte biedend waar nodig beter tot uitdrukking komt in richtlijnen. Praktisch gezien gaat het om twee mogelijke normen: minimumnormen en streefniveau. Bij iedere aanbeveling zal in het implementatieplan worden aangegeven wat de status van de betreffende aanbeveling is: minimumnorm of streefniveau.
Verder is het van belang om helder te maken hoeveel tijd nodig is voor het realiseren van een aanbeveling. Dit geldt bijvoorbeeld voor aanbevelingen waarbij organisatorische veranderingen nodig zijn. Daarmee wordt de aanbeveling in een realistisch perspectief qua tijd gezet. Deze tijdslijnen worden opgenomen in het implementatieplan.
Zoekverantwoording
|
Onderwerp:
|
Database |
Zoekstrategie |
Aantal ref. |
|
Chirurgie van een rectum prolaps |
Medline (OVID), 1946-mei 2013 Engels, Nederlands
Embase (Elsevier)
|
1 Rectal Prolapse/ or Rectocele/ or ((rectal or anal) adj5 prolapse*).tw. or enteroc?ele*.tw. or proctoc?ele*.tw. or sigmoidoc?ele*.tw. or Intussusception/ or Intussusception*.tw. or "rectal invagination*".tw. (11378) 10 (LVR or LRR or STARR or delorme* or altemeier* or rectopex* or mucosectom* or proctosigmoidectom*).tw. (4595) 11 ((stapled adj7 transanal) or (stapled adj7 trans-anal)).tw. (148) 12 Rectocele/su or "Rectal Diseases"/su or Rectal Prolapse/su or "Digestive System Surgical Procedures"/ or "Laparoscopy"/ (66501) 13 10 or 11 or 12 (70451) 14 1 and 13 (2139) 15 Rectocele/su or "Rectal Diseases"/su or *Rectocele/su or *"Rectal Diseases"/su or *Rectal Prolapse/su or *"Digestive System Surgical Procedures"/ (8339) 16 9 and 14 (3) 17 15 and (10 or 11) (581) 18 14 or 17 (2195) 19 limit 18 to (dutch or english) (1659) 20 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or (systematic* adj review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (127085) 21 19 and 20 (31) 22 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1271329) 23 19 and 22 (170) 24 21 or 23 (182)
(((rectal OR anal) NEAR/5 prolapse*):ab,ti OR rectocele*:ab,ti OR enterocele*:ab,ti OR proctocele*:ab,ti OR sigmoidocele*:ab,ti OR intussusception*:ab,ti OR (rectal NEAR/2 invagination*):ab,ti OR 'rectum prolapse'/exp/mj AND (lvr:ab,ti OR lrr:ab,ti OR starr:ab,ti OR delorme*:ab,ti OR altemeier*:ab,ti OR rectopex*:ab,ti OR mucosectom*:ab,ti OR proctosigmoidectom*:ab,ti OR (stapled NEAR/7 transanal):ab,ti OR (stapled NEAR/7 'trans-anal'):ab,ti OR 'rectocele'/exp/mj/dm_su OR 'rectum disease'/exp/mj/dm_su OR 'rectum prolapse'/exp/mj/dm_su OR 'laparoscopy'/exp/mj) OR ('rectocele'/exp/mj/dm_su OR 'rectum disease'/exp/mj/dm_su OR 'rectum prolapse'/exp/mj/dm_su AND (lvr:ab,ti OR lrr:ab,ti OR starr:ab,ti OR delorme*:ab,ti OR altemeier*:ab,ti OR rectopex*:ab,ti OR mucosectom*:ab,ti OR proctosigmoidectom*:ab,ti OR (stapled NEAR/7 transanal):ab,ti OR (stapled NEAR/7 'trans-anal'):ab,ti))) AND ([dutch]/lim OR [english]/lim) AND [embase]/lim |
315 |