Primaire tumor onbekend - Behandeling: behandelbare subgroepen
Uitgangsvraag
Wat is de effectiviteit van locoregionale behandeling van patiënten met een metastase van (blijvend) onbekende origine wanneer gekeken wordt naar mortaliteit en kwaliteit van leven?
Aanbeveling
Lymfkliermetastase in het hoofd/hals gebied
Voor een pN1 of cN1 zonder (radiologische aanwijzing voor) extranodale groei kan men monotherapie d.w.z. een vorm van halsklierdissectie ofwel primaire radiotherapie overwegen. Bij extranodale groei en stadia N2-N3 is combinatietherapie gerechtvaardigd. Chirurgische behandeling met een curatieve intentie, een (gemodificeerd) radicale halsklierdissectie met meenemen van level I t/m V, is de behandeling van eerste keuze bij stadia N2-N3. Primaire radiotherapie kan een alternatief zijn voor chirurgie, volgens de aanbevelingen voor de behandeling van lymfkliermetastasen in de richtlijn mondholte- en orofarynxcarcinoom.
Op basis van het aantal lymfkliermetastasen, de grootte van de klier, de aanwezigheid van kapseldoorbraak en de mate van radicaliteit, is adjuvante radiotherapie van de ipsilaterale en eventueel de contralaterale hals geïndiceerd, conform de richtlijnen voor het primair plaveiselcelcarcinoom in het hoofd-halsgebied.
Controverse bestaat er over de waarde van chemoirradiatie en electieve irradiatie van de faryngelae mucosa. Weliswaar is bij behandeling van het primair plaveiselcelcarcinoom in het hoofd-halsgebied, de waarde van adjuvante chemoirradiatie bij extranodale groei bewezen, maar in de beschikbare studies over onbekende primairen geeft toevoeging van platinumverbindingen wel toename van toxiciteit doch geen verbetering van regionale controle en/of survival (1) (2) (3). Daarmee ontbreekt consensus over een aanbeveling de bestaande richtlijnen te volgen voor het primair plaveiselcelcarcinoom in het hoofd-halsgebied.
Op basis van HPV- of EBV-positiviteit van de tumor kan worden overwogen de orofarynx respectievelijk de nasofarynx electief mee te bestralen. Gezien de sensitiviteit van HPV-positieve tumoren kan in dat geval ook overwogen worden de hals middels primaire radiotherapie te behandelen. Bij EBV- en HPV-negatieve tumoren kan op indicatie electieve irradiatie van de uni- of bilaterale faryngeale mucosa worden overwogen.
Geïsoleerde lymfkliermetastasen in de lies
Primair chirurgische behandeling met een curatieve intentie wordt aanbevolen. Radiotherapie kan worden overwogen.
Overige solitaire metastasen
Bij solitaire orgaanmetastasen kan lokale behandeling worden overwogen. Met chirurgie en/of radiotherapie kan vaak langdurige respons verkregen worden. Bij solitaire botmetastasen wordt in het algemeen primaire radiotherapie aanbevolen. Chirurgie kan in zeldzame gevallen een alternatief zijn. Bij bedreiging van vitale structuren (zoals myelum) dient chirurgie eerst overwogen te worden.
Symptoombehandeling
Voor symptomatische metastasen kan lokale behandeling (o.a. chirurgie, radiotherapie, radiofrequente ablatie, embolisatie, stents) worden overwogen als onderdeel van de palliatieve behandeling.
Overwegingen
De keuze voor een vorm van lokale en/of regionale behandeling is afhankelijk van de intentie van die behandeling: curatief dan wel palliatief. Aan patiënten bij wie curatie mogelijk is, op basis van patiëntkenmerken (bijvoorbeeld leeftijd en performance status), tumorkenmerken (bijvoorbeeld uitbreiding en histologische kenmerken) en voorkeur van de patiënt, kan een meer radicale behandeling worden aangeboden.
Bij patiënten met halslymfkliermetastasen zonder bekende primaire tumor is geen goed vergelijkend onderzoek verricht waarin de waarde van postoperatieve bestraling is aangetoond of waarin radiotherapie vergeleken is met chirurgie alleen. Hetzelfde geldt voor de waarde van salvage chirurgie na (chemo)irradiatie. Eveneens ontbreken studies naar de effectiviteit en morbiditeit van uitgebreidere radiotherapieschema's (bilaterale irradiatie, inclusief de farynxmucosa). Daarmee blijft de indicatie en het doelvolume van profylactische (postoperatieve) bestraling in het hoofd-hals gebied controversieel. Gezien bovenstaande wordt geadviseerd bij de keuze voor primaire radiotherapie of primaire chirurgie met eventuele postoperatieve irradiatie van de hals, de richtlijnen voor behandeling van de hals bij (bekend) primair plaveiselcelcarcinoom in het hoofd-halsgebied te volgen. Op basis van beschikbare studies wordt algemeen aangenomen, dat electieve radiotherapie van de nasofaryngeale as waarin zich mogelijk een primaire tumor bevindt, de kans op mucosaal recidief substantieel vermindert (1) (26) (2) (27) (3). Momenteel kan deze electieve bestraling worden geïndividualiseerd op basis van virale diagnostiek. Bij een HPV positieve tumor kan worden overwogen alleen de orofarynx en bij een EBV positieve tumor alleen de nasofarynx electief mee te bestralen. De in de NICE evidence review genoemde comorbiditeit van radiotherapie (mucositis en xerostomie) is tegenwoordig beperkter (4), aangezien IMRT nu standaard is. Dat geldt met name voor het optreden van xerostomie.
Onderbouwing
Conclusies / Summary of Findings
|
|
Er is beperkt bewijs voor de effectiviteit van de uitgebreidheid van postoperatieve radiotherapie van halslymfkliermetastasen van een onbekende primaire tumor. Radiotherapie in het hoofd-halsgebied lijkt gepaard te gaan met een forse daaraan gerelateerde morbiditeit. |
|
Het gebruik van 3D-CRT of IMRT radiotherapie bij patiënten met een halslymfkliermetastase van onbekende primaire origine lijkt effectiever dan toepassing van 2D-techniek. De gerapporteerde toxiciteit na IMRT is substantieel lager dan na 2D-radiotherapie. |
| Niveau 3 |
Chirurgische behandeling van halslymfkliermetastasen van onbekende primaire origine kan leiden tot curatie, waarbij de vijfjaarsoverleving varieert van 24 tot 66%. |
| Niveau 3 |
De overleving van halslymfkliermetastasen van onbekende primaire origine wordt bepaald door de N-status en mogelijk ook kapseldoorbraak. De optimale behandeling is nog controversieel. Een combinatie van therapie-modaliteiten voor de hals lijkt de overleving niet te beïnvloeden. |
Samenvatting literatuur
Van een deel van de behandelbare entiteiten is een multidisciplinaire richtlijn voorhanden. Aanbevolen wordt deze entiteiten volgens de betreffende richtlijnen te behandelen.
Tabel 4. Behandelbare subgroepen en bijbehorende richtlijnen.
Voor onderstaande behandelbare subgroepen zijn geen richtlijnen voorhanden.
- Halslymfkliermetastasen van vooral plaveiselcelcarcinoom
- Geïsoleerde lymfkliermetastasen in de lies van met name plaveiselcelcarcinoom
- Overige solitaire metastasen
Tabel 5. Behandelbare subgroepen zonder richtlijn.
Voor deze entiteiten zijn daarom aanbevelingen gebaseerd uitgaande van de volgende vraag. Wat is de effectiviteit van locoregionale behandeling van patiënten met een metastase van (blijvend) onbekende origine wanneer gekeken wordt naar mortaliteit en kwaliteit van leven?
Wetenschappelijke onderbouwing
Vertaling ‘Short Summary' vanuit NICE richtlijn (4):
Postoperatieve behandeling van halslymfkliermetastasen van plaveiselcelcarcinoom van onbekende origine
Er waren weinig studies die geschikt waren om de effectiviteit van postoperatieve behandeling te evalueren. Het bewijs was beperkt tot observationele studies, met weinig data over patiënten die alleen chirurgisch waren behandeld. Case series suggereren dat de vijfjaars postoperatieve overleving ligt tussen 22% en 60% voor patiënten die adjuvante radiotherapie hebben gehad. In twee kleine patiëntenseries waarin patiënten alleen chirurgisch werden behandeld, varieerde de vijfjaarsoverleving van 65% tot 66%. Chirurgie met adjuvante chemoradiotherapie gaf 5-jaarsoverleving van 75%-89%.
Aan de behandeling gerelateerde comorbiditeit, inclusief mucositis en xerostomie, kwam veel voor na radiotherapie. Er was geen duidelijkheid over behandelingstoxiciteit bij patiënten zonder adjuvante therapie, maar het is aannemelijk dat deze groep patiënten enige morbiditeit bespaard is gebleven.
Lieslymfkliermetastasen van een plaveiselcelcarcinoom van onbekende primaire origine
Er was weinig relevante literatuur over patiënten met een gemetastaseerd plaveiselcelcarcinoom van onbekende origine, die zich presenteren met lieslymfadenopathie. Een aantal patiënten met inguïnale lymfkliermetastasen van onbekende origine ondergingen chirurgie met curatieve intentie. Een gemiddelde overleving van 7,7 jaar werd hierbij gerapporteerd. Het was echter niet duidelijk of minder behandeling net zo effectief zou zijn geweest. Er was een relatief hoog aandeel van geïsoleerde lymfkliermetastasen bij patiënten die chirurgisch werden behandeld (8/9 patiënten in twee patiëntenseries (89%)).
Er was één studie met gegevens over complicaties. Lymfklierdissectie was geassocieerd met lymfoedeem. Ernstige acute toxiciteit werd gezien bij 6% van de patiënten die met radiotherapie werden behandeld. 31% van de vrouwen ouder dan 50 jaar die radiotherapeutisch werden behandeld kregen een heupfractuur in het bestraalde gebied. Er was geen aan de behandeling gerelateerde mortaliteit.
Geïsoleerde levermetastasen van onbekende primaire origine
Er was schaars bewijs over lokale therapie bij geïsoleerde levermetastasen van een onbekende primaire tumor. Minder dan 10% van de patiënten met een onbekende primaire tumor en levermetastasen onderging chirurgie.
Het was onduidelijk welk effect lokale therapie voor geïsoleerde levermetastasen heeft op uitkomsten. Uit retrospectieve series blijkt duidelijk dat patiënten die chirurgisch werden behandeld voor levermetastasen van onbekende primaire origine een betere overleving hadden dan patiënten die niet werden geopereerd. De mediane overleving was 30 maanden voor patiënten die chirurgisch werden behandeld, vergeleken met 4-10 maanden voor patiënten met een onbekende primaire tumor en levermetastasen in het algemeen. Echter, patiënten die werden geselecteerd voor chirurgie hadden waarschijnlijk preoperatief een betere prognose dan patiënten die niet voor chirurgie in aanmerking kwamen.
Geïsoleerde bot-, long- of huidmetastasen van onbekende primaire origine
Er was geen direct bewijs over radicale lokale behandeling van geïsoleerde bot-, long- of huidmetastasen bij een onbekende primaire tumor.
De literatuursearch die voor de NICE richtlijn is gedaan, is geactualiseerd. Na de literatuursearch en literatuurselectie bleven 22 artikelen over die full-tekst zijn beoordeeld. Een aantal artikelen viel vervolgens af omdat deze binnen de inclusiecriteria van de NICE evidence review vielen (5) (6) (7) (8) (9) (10) (11) (12) (13) (14) (15) (16) (17) (18) (19) (20). Additioneel werd een aantal artikelen geëxcludeerd vanwege methodologische tekortkomingen of inhoudelijke redenen (omdat het artikel de uitgangsvraag niet beantwoordde) (21) (22) (23) (24).
Halslymfkliermetastasen
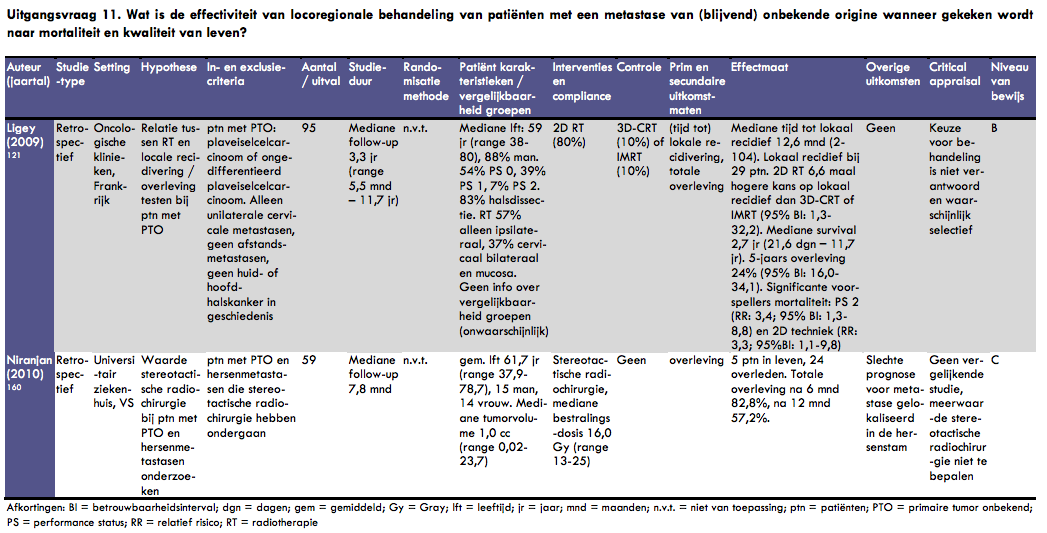
In het artikel van Ligey et al. wordt de behandeling van 95 patiënten met halslymfklier metastasen van een onbekende primaire tumor beschreven (25). In dit onderzoek werden patiënten met plaveiselcelcarcinoom of ongedifferentieerd carcinoom geïncludeerd met unilaterale halslymfklier-metastasen zonder afstandsmetastasen en zonder huid- of hoofd-halskanker in de voorgeschiedenis. De mediane leeftijd van de patiënten was 59 jaar (range 38-80 jaar); 88% was man. Van alle patiënten had 54% performance status 0, 39% performance status 1 en de rest performance status 2. De mediane lymfkliergrootte was 35 mm (range 3-80 mm). Bij 83% van de patiënten werd een halsklierdissectie uitgevoerd. Radiotherapie werd bij 57% van de patiënten alleen ipsilateraal toegepast, bij 37% werden de halslymfklieren bilateraal alsook de mucosa van de faryngeale as bestraald. Van alle patiënten kreeg 80% radiotherapie met 2D-techniek, 10% met 3D-CRT en 10% met IMRT. Chemotherapie werd gegeven aan 45% van de patiënten. De mediane follow-up bedroeg 3,3 jaar (range 6 maanden - 12 jaar). De mediane tijd tot lokale recidivering was 13 maanden (range 2 - 104 maanden). Een lokaal recidief werd gevonden bij 29 patiënten (30%). Op basis van de gevonden resultaten werd een prognostisch model ontwikkeld om de kans op lokale recidivering na behandeling met radiotherapie te kunnen voorspellen. Na univariate en multivariate analyse bleek er slechts één prognostische onderscheidende factor te zijn: het gebruik van een tweedimensionale techniek (versus 3D-CRT of IMRT) gaf een 6,6 maal hogere kans op lokale recidivering (95% BI: 1,3 - 32,2). De mediane overlevingsduur was 2,7 jaar (range 22 dagen - 12 jaar). De vijfjaars totale overleving was 24% (95% BI: 16 - 34). Significante prognostische voorspellers voor mortaliteit waren een performance status van 2 (RR = 3,4; 95% BI: 1,3 - 8,8) en het gebruik van een 2-D techniek (RR = 3,3; 95% BI: 1,1 - 9,8). De keuze voor de verschillende behandelingen is niet verantwoord en lijkt afhankelijk van de status van de patiënt.
Sinds de Franse studie van Ligey et al. zijn recent nog 5 Amerikaanse retrospectieve studies van zeer hetrogeen behandelde patiëntengroepen verschenen (1) (26) (2) (27) (3). Deze studies zijn heterogeen, zowel m.b.t. chirurgie (complete halsklierdissectie, alleen klierbiopt of niets), als m.b.t. radiotherapie (uni/bilateraal, pre/postoperatief en verschillende mucosavelden), als m.b.t. chemotherapie (inductief en/of simultaan). De overleving in deze studies was beter dan die van Ligey et al. en bedroeg in totaal 52-89% respectievelijk ziektevrij 81-88%. Daarbij werd geheel (26) (2) (27), of deels (1) (3), de IMRT-techniek toegepast. Recent is een meta-analyse verschenen en een uitgebreide review met bijdrage van vele centra (28) (29). Uit deze studies wordt geconcludeerd:
- Uni- of bilaterale electieve bestraling van de oro-nasofarynx kan de locale controle in individuele gevallen (afwegende factoren zoals stadium) mogelijk verhogen (1) (26) (2) (27) (3) (29). Door larynx en hypofarynx buiten het bestralingsveld te laten, lijkt survival niet te verslechteren (3);
- Met betrekking tot electieve RT is er met 3D-conformatie therapie en IMRT een toegenomen therapeutische ratio tov 2D-radiotherapie (29).
- Toevoeging van chemotherapie verbetert survival niet, maar geeft wel fors hogere toxiciteit in de vorm van oesofagus-stenose, tot zelfs 46% (1) (2) (3);
- Of HPV-positieve metastasen van onbekende primaire tumoren ook meer radiosensitief zijn voor radiotherapie t.o.v. HPV-negatieve metastasen, is nog niet aangetoond (29).
- De overleving wordt bepaald door het N-stadium. Bij clustering van studies en alle stadia wordt geen significant verschil in 5-jaars overleving gezien tussen behandeling met (chemo)radiotherapie alleen, versus patiënten die ook een halsklierdissectie hebben ondergaan (28).
Referenties
- 1 - Chen AM, Farwell DG, Lau DH, Li BQ, Luu Q, Donald PJ. Radiation Therapy in the Management of Head-and-Neck Cancer of Unknown Primary Origin: How Does the Addition of Concurrent Chemotherapy Affect the Therapeutic Ratio? Int J Radiat Oncol Biol Phys. 2011; 81(2): 346-52.
- 2 - Sher DJ, Balboni TA, Haddad RI, Norris CM, Jr., Posner MR, Wirth LJ, et al. Efficacy and toxicity of chemoradiotherapy using intensity-modulated radiotherapy for unknown primary of head and neck. Int J Radiat Oncol Biol Phys. 2011; 80(5): 1405-11.
- 3 - Wallace A, Richards GM, Harari PM, Kirwan JM, Morris CG, Katakam H, et al. Head and neck squamous cell carcinoma from an unknown primary site. Am J Otolaryngol. 2011; 32(4): 286-90.
- 4 - NICE. NIfHaCE. Diagnosis and management of metastatic malignant disease of unknown primary origin. Full Guideline. 2010 [cited; Available from: http://www.nice.org.uk/nicemedia/live/13044/49864/49864.pdf
- 5 - Pavlidis N, Briasoulis E, Hainsworth J, Greco FA. Diagnostic and therapeutic management of cancer of an unknown primary. Eur J Cancer. 2003; 39(14): 1990-2005.
- 6 - Ruda R, Borgognone M, Benech F, Vasario E, Soffietti R. Brain metastases from unknown primary tumour: a prospective study. J Neurol. 2001; 248(5): 394-8.
- 7 - Hainsworth JD, Fizazi K. Treatment for patients with unknown primary cancer and favorable prognostic factors. Semin Oncol. 2009; 36(1): 44-51.
- 8 - Bartelt S, Lutterbach J. Brain metastases in patients with cancer of unknown primary. J Neurooncol. 2003; 64(3): 249-53.
- 9 - D'Ambrosio AL, Agazzi S. Prognosis in patients presenting with brain metastasis from an undiagnosed primary tumor. Neurosurg Focus. 2007; 22(3): E7.
- 10 - Dova L, Pentheroudakis G, Georgiou I, Malamou-Mitsi V, Vartholomatos G, Fountzilas G, et al. Global profiling of EGFR gene mutation, amplification, regulation and tissue protein expression in unknown primary carcinomas: to target or not to target? Clin Exp Metastasis. 2007; 24(2): 79-86.
- 11 - Faure E, Riquet M, Lombe-Weta PM, Hubsch JP, Carnot F. [Malignant mediastinal lymph node tumors with unknown primary cancers]. Rev Mal Respir. 2000; 17(6): 1095-9.
- 12 - Laveau F, Picot MC, Dereure O, Guilhou JJ, Guillot B. [Metastatic melanoma of unknown primary site]. Ann Dermatol Venereol. 2001; 128(8-9): 893-8.
- 13 - Maesawa S, Kondziolka D, Thompson TP, Flickinger JC, Dade L. Brain metastases in patients with no known primary tumor. Cancer. 2000; 89(5): 1095-101.
- 14 - Mistry RC, Qureshi SS, Talole SD, Deshmukh S. Cervical lymph node metastases of squamous cell carcinoma from an unknown primary: outcomes and patterns of failure. Indian J Cancer. 2008; 45(2): 54-8.
- 15 - Nieder C, Ang KK. Cervical lymph node metastases from occult squamous cell carcinoma. Curr Treat Options Oncol. 2002; 3(1): 33-40.
- 16 - Ponce Lorenzo J, Segura Huerta A, Diaz Beveridge R, Gimenez Ortiz A, Aparisi Aparisi F, Fleitas Kanonnikoff T, et al. Carcinoma of unknown primary site: development in a single institution of a prognostic model based on clinical and serum variables. Clin Transl Oncol. 2007; 9(7): 452-8.
- 17 - Riquet M, Badoual C, le Pimpec BF, Dujon A, Danel C. Metastatic thoracic lymph node carcinoma with unknown primary site. Ann Thorac Surg. 2003; 75(1): 244-9.
- 18 - Shaw PH, Adams R, Jordan C, Crosby TD. A clinical review of the investigation and management of carcinoma of unknown primary in a single cancer network. Clin Oncol (R Coll Radiol). 2007; 19(1): 87-95.
- 19 - Zuur CL, van Velthuysen ML, Schornagel JH, Hilgers FJ, Balm AJ. Diagnosis and treatment of isolated neck metastases of adenocarcinomas. Eur J Surg Oncol. 2002; 28(2): 147-52.
- 20 - Giordana MT, Cordera S, Boghi A. Cerebral metastases as first symptom of cancer: a clinico-pathologic study. J Neurooncol. 2000; 50(3): 265-73.
- 21 - Pavlidis N, Fizazi K. Carcinoma of unknown primary (CUP). Crit Rev Oncol Hematol. 2009; 69(3): 271-8.
- 22 - Yapar Z, Kibar M, Yapar AF, Paydas S, Reyhan M, Kara O, et al. The value of 18F-fluorodeoxyglucose positron emission tomography/computed tomography in carcinoma of an unknown primary: diagnosis and follow-up. Nucl Med Commun. 2010; 31(1): 59-66.
- 23 - Thom I, Rogers C, Andritzky B, Witzel I, Schuch G, Hossfeld DK, et al. Single-center management of 136 patients with cancer of unknown primary site (CUP syndrome) over a period of 10 years. Onkologie. 2009; 32(12): 741-6.
- 24 - Penel N, Negrier S, Ray-Coquard I, Ferte C, Devos P, Hollebecque A, et al. Development and validation of a bedside score to predict early death in cancer of unknown primary patients. PLoS One. 2009; 4(8): e6483.
- 25 - Ligey A, Gentil J, Crehange G, Montbarbon X, Pommier P, Peignaux K, et al. Impact of target volumes and radiation technique on loco-regional control and survival for patients with unilateral cervical lymph node metastases from an unknown primary. Radiother Oncol. 2009; 93(3): 483-7.
- 26 - Frank SJ, Rosenthal DI, Petsuksiri J, Ang KK, Morrison WH, Weber RS, et al. Intensity-modulated radiotherapy for cervical node squamous cell carcinoma metastases from unknown head-and-neck primary site: M. D. Anderson Cancer Center outcomes and patterns of failure. Int J Radiat Oncol Biol Phys. 2010; 78(4): 1005-10.
- 27 - Shoushtari A, Saylor D, Kerr KL, Sheng K, Thomas C, Jameson M, et al. Outcomes of Patients with Head-and-Neck Cancer of Unknown Primary Origin Treated with Intensity-Modulated Radiotherapy. Int J Radiat Oncol Biol Phys. 2011.
- 28 - Balaker AE A, Elashoof D, John MA. Cancer of Unknown Primary: Does Treatment Modality Make a Difference? Laryngoscope. 2012; 122: 1279-82.
- 29 - Strojan P FA, Langendijk JA, Corry J, Woolgar JA, Rinaldo A, et al. Contemporary management of lymph node metastases from an unknown primary to the neck: II A review of therapeutic options. Head & Neck. 2011: DOI 10.1002/hed.21899.
Evidence tabellen
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 24-06-2012
Commentaar en autorisatie
Na het vaststellen van de conceptrichtlijn door de kerngroep is deze ter commentaar rondgestuurd naar de gehele werkgroep. Na verwerking van dit commentaar door de kerngroep is de richtlijn voor commentaar gestuurd naar de verenigingen aan wie ook een knelpunteninventarisatie is gestuurd. Ook hierbij werd het commentaar door de kerngroep verwerkt. Tot slot is de richtlijn ter autorisatie naar de besturen van de (wetenschappelijke) verenigingen gestuurd. Na autorisatie is de richtlijn de professionele standaard voor de leden van die verenigingen. Tijdens de bijeenkomst op 3 en 4 februari 2011 is besloten dat de richtlijn is geaccepteerd, wanneer tenminste de verenigingen die vertegenwoordigd zijn in de kerngroep, aangevuld met de Nederlandse Vereniging voor Radiotherapie en Oncologie, de richtlijn hebben geautoriseerd.
Juridische betekenis
Richtlijnen zijn geen wettelijke voorschriften, maar op ‘evidence' gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'.
Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
Herziening
De werkgroep vindt dat de richtlijn regelmatig geëvalueerd moet worden en zo nodig op onderdelen moet worden herzien, bijvoorbeeld door 1x per jaar na te gaan of er ontwikkelingen dan wel onbeantwoorde knelpunten zijn die nopen tot bijstelling van de richtlijn. Dat vereist dat de werkgroepleden door hun wetenschappelijke vereniging hiertoe zijn gemandateerd en dat de werkgroep een procedure hanteert waarbij werkgroepleden tussentijds kunnen worden vervangen indien dat wenselijk is. Een werkwijze die men hiervoor kan hanteren is bijvoorbeeld dat ieder werkgroeplid voor de duur van drie jaar wordt benoemd en dat die na drie jaar nog eens voor drie jaar kan worden herbenoemd. Een volgende benoeming kan alleen plaatsvinden indien vanuit de werkgroep door de voorzitter of door de wetenschappelijke vereniging expliciet wordt gevraagd het desbetreffende werkgroeplid nogmaals te benoemen voor drie jaar. Die wijze van herbenoeming kan daarna nog meerdere malen worden herhaald. Bij elke bijstelling is autorisatie vereist door de wetenschappelijke verenigingen die deel uitmaken van de kernwerkgroep. De bijgestelde richtlijn wordt uitgebracht via de daarvoor aangewezen kanalen. De werkgroep zal deze werkwijze proberen uit te voeren, maar is afhankelijk van structurele financiering door bijvoorbeeld de SKMS.
De werkgroep vindt het van belang dat in een revisie van deze richtlijn meer aandacht aan patiëntenvoorlichting zou moeten worden gegeven.
Doel en doelgroep
Doel van de richtlijn
Het doel van deze richtlijn is het bieden van ondersteuning aan zorgverleners bij het realiseren van een uniform en zoveel mogelijk evidence-based beleid voor nadere diagnostiek, behandeling en nazorg van patiënten met een onbekende primaire tumor. Hiermee wordt voorts beoogd diagnostiek te verminderen, samenwerkingsafspraken tussen verschillende specialismen te bevorderen en de informatieoverdracht naar de patiënt te verbeteren.
Deze richtlijn is primair geschreven voor behandelaars van deze patiënten.
Huidige tekortkomingen in het beleid bij patiënten met een onbekende primaire tumor
De diagnostiek en het behandelbeleid bij patiënten met een metastase van onbekende primaire tumor is complex, variabel en niet perfect. De tekortkomingen in het bestaande beleid kunnen worden toegeschreven aan de volgende factoren:
· Het ontbreken van een richtlijn voor deze patiënten
· Gebrek aan wetenschappelijk onderzoek
· Weinig kennis over cellulaire factoren die van belang zijn voor prognose en eventuele therapie keuzes
Samenstelling werkgroep
Om de knelpunten in de zorg voor patiënten met een onbekende primaire tumor te verbeteren is in juni 2010 een multidisciplinaire werkgroep samengesteld. Deze werkgroep bestond uit een kernwerkgroep, die de conceptaanbevelingen opstelde en een ‘schil' die betrokken was bij de inventarisatie van de knelpunten en de commentaarronde. De werkgroepleden hebben onafhankelijk gehandeld en zijn gemandateerd door hun vereniging. De werkgroep werd ondersteund door PROVA en de Nederlandse Vereniging voor Pathologie. Aan de werkgroepleden is gevraagd een belangenverklaring in te vullen, waarin hun eventuele relaties met commerciële bedrijven konden worden aangegeven (zie Belangenverklaringen).
Kerngroep
- Dr. J.J. (Joost) Oudejans, patholoog, Diakonessenhuis, Utrecht, namens de Nederlandse Vereniging voor Pathologie (voorzitter)
- Mw. drs. M.K. (Mariska) Tuut, epidemioloog, PROVA, Varsseveld (secretaris)
- Dr. M.R.W. (Marc) Engelbrecht, radioloog, Academisch Medisch Centrum, Amsterdam, namens de Nederlandse Vereniging voor Radiologie (vanaf december 2010)
- Dr. R.J.J. (Robert) van Es, kaakchirurg-oncoloog, Universitair Medisch Centrum Utrecht, namens de Nederlandse Werkgroep Hoofd-Hals Tumoren en de Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie
- Mw. dr. H.M. (Houke) Klomp, chirurgisch oncoloog, Antoni van Leeuwenhoek Ziekenhuis, Amsterdam, namens de Nederlandse Vereniging voor Chirurgische Oncologie - Nederlandse Vereniging voor Heelkunde
- Dr. J.A. (Alain) Kummer, patholoog, Antonius Ziekenhuis, Nieuwegein, namens de Nederlandse Vereniging voor Pathologie
- Mw. drs. C.A.H. (Charlotte) Lange, radioloog, Antoni van Leeuwenhoek Ziekenhuis, Amsterdam, namens de Nederlandse Vereniging voor Radiologie (tot november 2010)
- Prof. dr. H.A.M. (Henri) Marres, KNO-arts, Radboud Universitair Medisch Centrum, Nijmegen, namens de Nederlandse Vereniging van Keel-, Neus- en Oorheelkunde en Heelkunde van het Hoofd-halsgebied en de Nederlandse Werkgroep Hoofd-Hals Tumoren
- Prof. dr. J. (Hans) Morreau, patholoog, Leids Universitair Medisch Centrum, Leiden, namens de Nederlandse Vereniging voor Pathologie
- Mw. dr. A.J. (Yes) van de Wouw, internist-oncoloog, VieCuri Medisch Centrum Venlo, namens de Nederlandse Vereniging voor Medische Oncologie
Overige werkgroepleden
- Dr. J.D. (Jeroen) van Bergeijk, Maag-, Darm-, Leverarts, Gelderse Vallei, Ede, namens de Nederlandse Vereniging voor Maag-, Darm- en Leverartsen
- Mw. drs. T. (Thea) Brouwer, psycholoog, Arnhem, namens de Nederlandse Federatie van Kankerpatiëntenorganisaties
- Drs. H.M.J. (Harry) Groen, longarts, Universitair Medisch Centrum Groningen, namens de Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Dr. J.M.G. (Hans) Bonfrer, klinisch chemicus, Antoni van Leeuwenhoek Ziekenhuis, Amsterdam, namens de Nederlandse Vereniging voor Klinische Chemie
- Dr. W.V. (Wouter) Vogel, nucleair geneeskundige, Antoni van Leeuwenhoek Ziekenhuis, Amsterdam, namens de Nederlandse Vereniging voor Nucleaire Geneeskunde
- Mw. drs. E. (Eleonora) van Dorst, gynaecoloog, Universitair Medisch Centrum Utrecht, namens de Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Dr. A.P. (Adriaan) Visser, psycholoog, De Vruchtenburg, centrum voor begeleiding bij kanker, Rotterdam, namens de Nederlandse Vereniging voor Psychosociale Oncologie
- Dr. C.H.J. (Chris) Terhaard, radiotherapeut-oncoloog, Universitair Medisch Centrum Utrecht, namens de Nederlandse Vereniging voor Radiotherapie en Oncologie
Betrokken bij knelpunten en commentaarronde:
- Integraal Kankercentrum Nederland (IKNL)
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging voor Urologie
- Verpleegkundigen en Verzorgenden Nederland
Belangenverklaringen
Een overzicht van deze belangenverklaringen is opgenomen. De leden van de kerngroep, alsook de extra ondersteuners, hebben tijdens de tweedaagse op 3 en 4 februari allen een belangenverklaring ingevuld, waarin zij hebben aangegeven of en welke activiteiten zij in de laatste vier jaar hebben ontplooid op uitnodiging van of met subsidie/sponsoring van een farmaceutische industrie, in relatie tot het onderwerp van de richtlijn.
De resultaten van deze inventarisatie staan in een overzicht weergegeven.
|
Naam |
Activiteiten op uitnodiging van of met subsidie/sponsoring van een farmaceutische industrie, in relatie tot het onderwerp van de richtlijn, gedurende de laatste vier jaar |
|
Joost Oudejans (voorzitter) |
Geen |
|
Mariska Tuut (secretaris) |
Geen |
|
Marc Engelbrecht |
Geen |
|
Robert van Es |
Geen |
|
Alain Kummer |
Geen |
|
Hans Morreau |
Geen |
|
Henri Marres |
Geen |
|
Houke Klomp |
Geen |
|
Yes van de Wouw |
Geen |
|
Rinke Borgonjen (procesbegeleider tijdens tweedaagse) |
Geen |
|
Jannes van Everdingen (procesbegeleider tijdens tweedaagse) |
Geen |
|
Geert Kleinnibbelink (procesbegeleider tijdens tweedaagse) |
Geen |
Methode ontwikkeling
Evidence based
Werkwijze
Knelpunteninventarisatie
In december 2009 - januari 2010 is een knelpunteninventarisatie verricht onder verenigingen die betrokken zijn bij de zorg voor mensen met een onbekende primaire tumor. Op basis hiervan is een knelpuntenlijst door de werkgroep vastgesteld in juni 2010.
In de knelpunteninventarisatie is een brief met een voorbereide lijst met mogelijke knelpunten gestuurd naar:
- Nederlands Huisartsen Genootschap
- Nederlandse Federatie van Kankerpatiëntenverenigingen
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Nederlandse Vereniging voor Heelkunde
- Nederlandse Vereniging voor Keel-, Neus- en Oorheelkunde en Heelkunde van het Hoofd-Halsgebied
- Nederlandse Vereniging voor Klinische Chemie
- Nederlandse Vereniging voor Maag-, Darm- en Leverartsen
- Nederlandse Vereniging voor Neurologie
- Nederlandse Vereniging voor Nucleaire Geneeskunde
- Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Nederlandse Vereniging voor Pathologie
- Nederlandse Vereniging voor Psychosociale Oncologie
- Nederlandse Vereniging voor Radiologie
- Nederlandse Vereniging voor Radiotherapie en Oncologie
- Nederlandse Werkgroep voor Hoofd-Hals Tumoren
- Vereniging voor Integrale Kankercentra
- Verpleegkundigen en Verzorgenden Nederland - Oncologie
Onderstaande mogelijke knelpunten waren in deze brief opgenomen, met de vraag of de betreffende vereniging deze knelpunten onderschreef en of er aanvulling nodig was.
- Het is onduidelijk welk diagnostisch traject optimaal is om een primaire tumor aan te tonen bij patiënten die zich presenteren met een metastase van onbekende origine.
- Wat is het optimale diagnostische traject om een primaire tumor aan te tonen voor de patholoog met behulp van morfologie, immuunhistochemie,en additionele technieken (moleculaire technieken, genome profiling)
- Welke tumoren moeten in eerste instantie worden uitgesloten vanwege eventuele effectieve behandelingsopties
- Het is onduidelijk welk beeldvormend onderzoek moet worden ingezet bij welke patiënten
- Uitwendig
- Inwendig (endoscopisch)
- Het is onduidelijk wanneer en welke exploratieve chirurgische technieken moeten worden ingezet bij welke patiënten
- Het is onduidelijk welke biochemische testen bij welke patiënten moeten worden ingezet bij welke patiënten
- Het is onduidelijk of er, op basis van prognostische informatie, groepen patiënten te identificeren zijn voor wie aanvullend onderzoek geen of weinig zin heeft
- Het is onduidelijk wat het optimale traject is voor patiënten bij wie na aanvullend onderzoek geen primaire tumor wordt aangetroffen
- Het is onbekend wat de winst en de kosten zijn van systemische en locoregionale behandeling
- Het is onbekend of er valide prognostische factoren zijn voor de respons op systemische therapie
- Het optimale begeleidingstraject voor patiënten met een tumor van onbekende origine is niet duidelijk
In juni 2010 is door de werkgroep de lijst met onderstaande knelpunten vastgesteld:
- Er is behoefte aan een eenduidige definitie van het begrip ‘metastase van onbekende origine / primaire tumor onbekend';
- Het is onduidelijk welk diagnostisch traject optimaal is om een primaire tumor aan te tonen bij patiënten die zich presenteren met een metastase van onbekende origine;
- Wat is het optimale diagnostische traject om een primaire tumor aan te tonen voor de patholoog met behulp van morfologie, immuunhistochemie,en additionele technieken (moleculaire technieken, genome profiling);
- Welke tumoren moeten in eerste instantie worden uitgesloten vanwege eventuele effectieve behandelingsopties;
- Het is onduidelijk welk beeldvormend onderzoek moet worden ingezet bij welke patiënten;
- Uitwendig;
- Inwendig (endoscopisch);
- Het is onduidelijk wanneer en welke exploratieve chirurgische technieken moeten worden ingezet bij welke patiënten;
- Het is onduidelijk wat de rol is van klierextirpatie zonder een cytologische punctie vooraf;
- Het is onduidelijk welke biochemische testen bij welke patiënten moeten worden ingezet bij welke patiënten;
- Het is onvoldoende duidelijk omschreven welke groepen patiënten te identificeren zijn:
- Het is onduidelijk of er, op basis van prognostische informatie, groepen patiënten te identificeren zijn voor wie aanvullend onderzoek geen of weinig zin heeft;
- Het is onduidelijk of er, op basis van prognostische informatie, groepen patiënten te identificeren zijn met een relatief gunstige prognose;
- Het is onduidelijk wat het optimale traject is voor patiënten bij wie na aanvullend onderzoek geen primaire tumor wordt aangetroffen;
- Het is onbekend wat de winst en de kosten zijn van systemische en locoregionale behandeling;
- Het is onbekend of er valide prognostische factoren zijn voor de respons op systemische therapie;
- Het optimale begeleidingstraject (inclusief psychosociale begeleiding) voor patiënten met een tumor van onbekende origine is niet duidelijk;
- Het is onbekend hoe groot de behoefte is aan lotgenotencontact en/of psychosociale begeleiding;
- Het is onduidelijk of er een noodzaak bestaat tot het herhalen van de primaire screening bij patiënten met een langere overleving;
- Verwijzingscriteria van eerste naar tweede lijn en omgekeerd zijn niet duidelijk.
Literatuuronderzoek
Bij elk van de uitgangsvragen is uitgebreid gezocht naar literatuur. De recente richtlijn ‘Diagnosis and management of metastatic malignant disease of unknown primary origin' van NICE werd waar mogelijk als input gebruikt, waarbij de literatuur werd geactualiseerd. Voor uitgangsvragen waarbij geen overlap met de NICE richtlijn werd gevonden, is uitgebreid literatuur gezocht. De beschrijving van de literatuursearches is opgenomen in Zoekverantwoording.
Na het zoeken van de literatuur, waarbij grote lijsten met abstracts werden verkregen, is de literatuur geselecteerd. Op basis van de abstracts werd vooral geselecteerd op onderwerp. De artikelen moesten in hoofdzaak gaan over primaire tumor onbekend. Daarnaast werd geselecteerd op origineel onderzoek (bijvoorbeeld systematische reviews, gerandomiseerde klinische trial, cohortonderzoeken) en geen editorials, letters of reviews. Een overzicht van de literatuurselectie per uitgangsvraag is opgenomen in Zoekverantwoording. Daarna werd de literatuur full-tekst opgevraagd en beoordeeld op kwaliteit en inhoud. Dit leidde tot verdere selectie, omdat op basis van de full-tekst ook nog artikelen afvielen. Dit staat beschreven in de afzonderlijke hoofdstukken over de verschillende uitgangsvragen. De gebruikte literatuur is samengevat in de inhoudelijke hoofdstukken van deze richtlijn onder het kopje ‘wetenschappelijke onderbouwing'. De korte samenvattingen die gepubliceerd zijn in de evidence review van de NICE-richtlijn zijn, waar van toepassing, integraal overgenomen in het Nederlands.
De literatuur is daarnaast per uitgangsvraag samengevat in evidence tabellen volgens het format van CoCanCPG (bijlage 2). De evidence tabellen (zie Evidence tabellen) zijn ook volgens het format van CoCanCPG en gegradeerd naar mate van bewijs volgens de indeling in bijlage 3.
De literatuur uit de NICE richtlijn is niet separaat gegradeerd. Elke wetenschappelijke onderbouwing is afgesloten met één of meerdere conclusies. Ook aan deze conclusies is een niveau toegekend. Alle gebruikte literatuur is opgenomen in de referentielijst.
Het literatuuronderzoek werd uitgevoerd door een epidemioloog (M.K. Tuut) met input van de werkgroep. Voor de literatuursearches werd ondersteuning verkregen van het CBO.
Totstandkoming aanbevelingen
In een tweedaagse bijeenkomst op 3 en 4 februari 2011 hebben de leden van de kerngroep het evidence rapport (wetenschappelijke onderbouwing en conclusies) beoordeeld en vastgesteld. Op basis van de evidence zijn vervolgens aanbevelingen geformuleerd. Echter, naast de evidence uit de literatuur zijn er ook andere overwegingen die meespelen bij het formuleren van aanbevelingen. Deze zogeheten overige overwegingen zijn expliciet vermeld en zijn onder andere onderstaande overwegingen:
- Klinische relevantie
- Veiligheid
- Patiënten-perspectief
- Professioneel perspectief
- Beschikbaarheid van voorzieningen
- Zorgorganisatie
De aanbevelingen zijn gebaseerd op de evidence, de overige overwegingen en discussie in de werkgroep. De aanbevelingen zijn afgeleid van de antwoorden op de uitgangsvragen. Deze zijn niet gegradeerd. Vanwege zeer recent beschikbaar gekomen evidence is in de autorisatiefase een wijziging doorgevoerd in module over behandelbare metastasen in het hoofd-halsgebied. Hierover is consensus bereikt door de Nederlandse Werkgroep Hoofd Hals Tumoren, Nederlandse Vereniging van Keel-, Neus- en Oorheelkunde en Heelkunde van het Hoofd-halsgebied, Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie en de Nederlandse Vereniging voor Radiotherapie en Oncologie.
Zoekverantwoording
De literatuursearches zijn per uitgangsvraag weergegeven (bijlage 4). De vetgedrukte regels zijn de bestanden waarvan de abstracts zijn beoordeeld in de literatuurselectie.
Alle abstracts die gevonden zijn in de literatuursearch (bijlage 5) zijn beoordeeld op relevantie. Daarbij zijn met name artikelen die niet over onbekende primaire tumoren gingen afgevallen. Ook werd gekeken naar de methodologie. Artikelen waarbij zeker was dat het geen systematisch onderzoek betrof, werden geëxcludeerd (bijvoorbeeld narratieve reviews, letters, case reports). De referenties (ref's) die overbleven na de literatuurselectie werden full-tekst opgevraagd en beoordeeld op kwaliteit en inhoud. In de tekst per module is beschreven welke artikelen op basis van full-tekst alsnog afvielen.
