Verlaging valrisico ouderen in ziekenhuis
Uitgangsvraag
Welke (multifactoriële) valpreventieve interventies zijn effectief bij ouderen met een matig of hoog valrisico in het ziekenhuis?
Deelvraag: Wat zijn de effectieve interventiecomponenten en welke componenten zouden minimaal overwogen moeten worden in multicomponent of multifactoriële interventies?
Aanbeveling
Voer bij alle opgenomen ouderen een multifactoriële valpreventieve interventie* uit, gebaseerd op de geïdentificeerde valrisicofactoren uit de multifactoriële, (multidisciplinaire) valrisicobeoordeling ongeacht de inschatting van het valrisico.
Verwerk in de multifactoriële valpreventieve interventie de positief gescoorde valrisicofactoren en overweeg minimaal de volgende items (voor details per interventiecomponent en het complete overzicht zie tabel Aanbevelingen valpreventie interventies ouderen in het ziekenhuis):
Startend met de interventie met de hoogste bewijskracht
- Beweeginterventie met balans- en functiegerichte componenten (minimaal 1 uur per dag)
- Vitamine D-suppletie
- Behandeling van (risico op) ondervoeding en dehydratie
- Afbouw van valrisicoverhogende medicatie via een gestructureerde medicatieoptimalisatie (zie hiervoor de module beoordeling valrisicoverhogende medicatie).
- Organisatie- en omgevingsgerichte interventies
Richt de interventies tijdens de opname op risicofactoren die direct in het ziekenhuis kunnen worden aangepakt. Zorg bij ontslag voor een transmurale vervolginterventie.
*Multicomponent: alle patiënten krijgen dezelfde combinatie van interventiecomponenten. Multifactorieel: de combinatie van interventiecomponenten wordt afgestemd op de individuele patiënt.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is literatuuronderzoek uitgevoerd naar de effectiviteit van valpreventieve interventies bij ouderen in het ziekenhuis. Als deelvraag werd geformuleerd: Wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten? In de systematische literatuur analyse werd gefocust op de multicomponent en multifactoriële valpreventieve interventies (hierna: multifactoriële interventies). Multicomponent interventies worden hierbij gedefinieerd als een interventie waarbij alle deelnemers dezelfde combinatie van deelinterventies ontvangen. Bij multifactoriële interventies wordt de combinatie van deelinterventies aangepast naar de individuele patiënt.
De Cochrane review van Cameron (2018) werd als basis gebruikt voor het literatuuronderzoek en de literatuursamenvatting. Ook werd de systematische review van Morris (2022) geïncludeerd. Tenslotte werd de recent gepubliceerde RCT van Di Gennaro (2024) geïncludeerd.
Als uitkomstmaten werden, conform de Cochrane review van Cameron (2018), valrisico, valfrequentie en het risico op valgerelateerde fracturen gedefinieerd. Hierbij werd valrisico gedefinieerd als het aantal patiënten dat (éénmalig of herhaaldelijk) valt in de interventiegroep, vergeleken met het aantal patiënten dat valt in de controlegroep. Valfrequentie werd gedefinieerd als het totaal aantal valincidenten per tijdseenheid. Het risico op valgerelateerde fracturen verwijst naar het aantal patiënten met fracturen ten gevolge van een val.
De RCTs die zijn geïncludeerd in Cameron (2018), Morris (2022) en de gerandomiseerde trial van Di Gennaro (2024) suggereren dat multicomponent en multifactoriële interventies mogelijk leiden tot zowel een verlaagd valrisico als een verlaagde valfrequentie. Dit is met uitzondering van het effect van multicomponent interventies op valrisico, waarvoor geen bewijs werd gevonden. Er werden zowel voor valrisico als valfrequentie effectschattingen gevonden die een klinisch relevant effect suggereren. Voor beide uitkomstmaten geldt echter ook dat de bovengrens van het 95% betrouwbaarheidsinterval de grens van klinische besluitvorming doorkruist, wat het vertrouwen in de gevonden effecten verlaagt. Daarnaast kenden de gevonden studies beperkingen in de studieopzet, wat het vertrouwen in de gevonden effecten verlaagt. Ondanks deze beperkingen suggereert het bewijs dat multicomponent en multifactoriële interventies leiden tot een verlaging van het valrisico en valfrequentie (GRADE laag). Over het effect van multicomponent en multifactoriële interventies op het risico op valgerelateerde fracturen werd respectievelijk geen bewijs en bewijs met een zeer lage bewijskracht gevonden (GRADE zeer laag), waardoor hier geen conclusies over kunnen worden getrokken.
Om de deelvraag wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten? te kunnen beantwoorden is er gekeken naar de afzonderlijke interventiecomponenten van de multicomponent en multifactoriële interventies die beschreven werden in de literatuursamenvatting (Tabel 3). Interventiecomponenten die in meerdere studies onderdeel zijn van de multicomponent of multifactoriële interventie zijn:
- Beweeginterventies
- Medicatie interventies (medicatie review)
- Omgevingsinterventies
- Ondersteunende technologie (bijvoorbeeld bewegingsensors en hulpmiddelen)
- Educatie van personeel en patiënt
Gezien het feit dat deze deelinterventies in meerdere multicomponent en multifactoriële interventies terugkomen, lijken dit potentieel belangrijke componenten in een multifactoriële interventie.
Naast de interventie componenten van de multifactoriële en multicomponent interventies, is er ook gekeken naar de resultaten uit de Cochrane review van Cameron (2018) over enkelvoudige interventies. De belangrijkste bevindingen over enkelvoudige interventies waren zijn te vinden in tabel 4. Naast de interventies beschreven in de tabel, waren er ook studies naar de effecten van vloerbekleding, laag-laag bedden, de inzet van armbanden, de implementatie van valpreventie richtlijn, acute zorg dienst, orthogeriatrische zorg na een heup-fractuur, en educatie. Voor deze typen interventies waren geen gepoolde effecten beschikbaar, omdat de resultaten slechts afkomstig waren uit 1 studie.
Tabel 4: overzicht van de resultaten over enkelvoudige valpreventieve interventies, afkomstig uit Cameron (2018)
|
|
Valrisico (aantal patiënten dat valt) |
Valfrequentie (valincidenten per tijdseenheid) |
Risico op botbreuken |
|
Lichamelijke beweging I: lichamelijke beweging + fysiotherapie C: standard fysiotherapie |
RR: 0.36 (95% BI: 0.14 tot 0.93) N = 83, 2 studies
GRADE very low |
RaR: 0.59 (95% BI: 0.26 tot 1.34) N = 215, 2 studies
GRADE very low |
Geen informatie |
|
Medicatie review I: medicatie review (multiprofessionele medicatie review) C: standard zorg |
RR: 0.18 (95% BI: 0.01 tot 3.35) N = 114, 1 studie
Geen informatie over GRADE |
RaR: 0.14 (95% BI: 0.01 tot 6.63) N = 114, 1 studie
Geen informatie over GRADE |
Geen informatie |
|
Vitamine D I: vitamine D + calcium C: calcium |
RR: 0.82 (BI 95%: 0.59 tot 1.14) N = 203, 1 studie.
Geen informatie over GRADE |
Geen informatie |
RR: 0.34 (BI 95%: 0.04 tot 3.05) N = 203, 1 studie.
Geen informatie over GRADE |
|
Omgevingsgerichte interventies I: Bed Alarms C Usual Care
|
RR: 0.93 (95%BI: 0.38 tot 2.24) N = 28649, 2 studies
GRADE very low |
RaR: 0.60 (95% BI: 0.27 tot 1.34) N = 28649, 2 studies
GRADE very low |
Niet te berekenen. |
Voor het effect van beweeginterventies op valrisico en valfrequentie worden weliswaar effectschatters gevonden die een verlaagd risico suggereren, echter heeft het gevonden bewijs een zeer lage bewijskracht. De NICE Guideline (April 2025) adviseert, patiënten in het ziekenhuis te verzekeren dat er geen reden is lichamelijke activiteit te beperken, tenzij hen geadviseerd is, dit wel te doen. Daarbij de patiënt actief aan te moedigen, lichamelijk actief te zijn door het bed te verlaten, zich aan te kleden en regelmatig te mobiliseren. Dit alles in het kader van een op de specifieke behoeften van te patiënt toegespitst bewegingsprogramma. Het belang van een overdracht naar de eerste lijn wordt benadrukt.
Het bewijs over het effect van de inzet van een medicatiereview (zie module beoordeling valrisicoverhogende medicatie) moet ook met zorg worden geïnterpreteerd. Er werd slechts 1 studie met daarin 114 patiënten gevonden en de 95% betrouwbaarheidsintervallen zijn heel breed, waardoor er veel onzekerheid bestaat over het daadwerkelijke effect. De NICE guideline adviseert hier een multidisciplinaire medicatiereview met betrokkenheid van de ziekenhuisapotheker, gevolgd door een afweging van de noodzaak en haalbaarheid van reductie van valrisico verhogende medicatie tijdens de klinische opname. De follow up en monitoring van medicatie-aanpassingen moet worden gewaarborgd met een goede overdracht naar de eerste lijn bij ontslag. In deze overdracht moet duidelijk zijn omschreven welke medicatie om welke reden is aangepast en wie verantwoordelijk is voor de follow up.
Over de effecten van vitamine D kunnen vanwege de brede 95% betrouwbaarheidsintervallen ook geen conclusies worden getrokken. Het is niet aannemelijk dat vitamine D het valrisico in het ziekenhuis zal verlagen. Op lange termijn zijn er echter mogelijk wel positieve effecten van vitamine D op het valrisico. De NICE Guideline adviseert om patiënten te wijzen op het belang van adequate suppletie van vitamine D maar doet geen uitspraak over het starten van suppletie in de klinische setting. Het is in ieder geval belangrijk om een bepaling van de vitamine D levels te doen. Indien er sprake is van een vitamine D deficiëntie, worden het toedienen van vitamine D aanbevolen. Ga hierbij uit van een streefwaarde van 75 nmol/l suppleer volgens de vigerende richtlijn suppletie vitamine D en calcium. Naast vitamine D kunnen mogelijk ook andere voedingsinterventies zinvol zijn. Patiënten in het ziekenhuis hebben een verhoogd risico is op ondervoeding. Het is belangrijk om hier rekening mee te houden, en zo nodig en waar gezien de onderliggende ziekte gewenst bijvoorbeeld eiwitrijke voeding aan te bieden.
In het Cochrane review van Cameron (2018) werden diverse omgevingsinterventies beschreven, waaronder bed alarmen, vloerbedekking, laag-laag bedden het gebruik van armbanden. Vanwege de diversiteit in type interventie werden deze niet gepoold en de gevonden resultaten waren uiteenlopend. In de NICE guideline worden geen aanbevelingen gedaan ten aanzien van dergelijke interventies, anders dan het identificeren van omgevingsgerelateerde risicofactoren. Alleen het inzetten van omgevingsgerichte interventies wordt niet zinvol geacht.
Naast de interventies die in de literatuur worden beschreven, is de ervaring uit de praktijk dat het belangrijk is om te zorgen voor een schone en goed verlichte omgeving, voldoende (toe-) zicht op de patiënt en om een op de individuele patiënt toegesneden educatieprogramma onderdeel uit te maken van een valpreventie programma. Het is bij de kennisoverdracht aan patiënten van belang om rekening te houden met individuele patiëntkenmerken als opleidingsniveau en cognitieve status. Bij cognitieve deficits is het wenselijk dat de naasten van de patiënt hierin worden betrokken. Daarnaast is het belangrijk om zorg te dragen voor voldoende kennis bij alle disciplines die betrokken zijn bij de patiëntenzorg (verpleging, artsen, paramedici, voedingsmedewerkers, huishoudelijk).
Bij het inzetten van een valpreventieve interventies in het ziekenhuis, is het belangrijk dat in ieder geval de risicofactoren worden aangepakt die in het ziekenhuis aanpakt kunnen worden. Voor de meeste interventies geldt dat het effect op valrisico in het ziekenhuis mogelijk beperkt is, maar het is wel belangrijk dat het vervolgens thuis wordt voortgezet. Bij de follow-up na ontslag is een transmurale samenwerking en een goede overdracht naar de eerste lijn van belang.
Kwaliteit van bewijs
De overal kwaliteit van bewijs over multicomponent en multifactoriële interventies is laag. Dit betekent dat we onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege ernstige
- Risk of Bias: methodologische beperkingen, waaronder onduidelijkheid in de randomisatie procedure en toewijzing en gebrek aan blindering.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Tijdens ziekenhuisopname hebben ouderen een hoger risico om te vallen dan in de thuissituatie. Dit wordt gedeeltelijk veroorzaakt door nieuwverworven risicofactoren (zoals acute ziekte, delier, verminderde mobiliteit en medicatie) en een onbekende omgeving, waardoor de persoons-omgevingsinteractie verandert. Het inzetten van interventies om het valrisico te verlagen bij patiënten in het ziekenhuis biedt voor de patiënt een aantal belangrijke voordelen. Naast het feit dat de interventies mogelijk een lager risico op vallen en fracturen geeft, kan het ook extra letsel en extra ziekenhuisdagen voorkomen. Ook draagt het bij aan een veiliger gevoel voor zowel patiënt als zorgverlener. Er zijn echter ook nadelen, zo bestaat er het risico dat patiënten zich minder vrij voelen in hun bewegingen, wat hun zelfstandigheid en welzijn negatief kan beïnvloeden. Het is daarom van belang om interventies zorgvuldig af te stemmen op de individuele behoeften van de patiënt.
Kostenaspecten
De beschreven interventies kunnen tijd- en arbeidsintensief zijn voor het zorgpersoneel en leiden tot extra administratieve lasten. Het is aannemelijk dat de kosten van de interventies hoger zijn dan bij standaard zorg, dit betreft bijvoorbeeld materiële uitgaven en extra inzet van het personeel. Echter, wanneer er met de inzet van een multifactoriële interventie, een toekomstige val kan worden voorkomen, wegen deze extra kosten hier mogelijk tegen op.
In de RCT van Di Gennaro (2024) werd een kosteneffectiviteitanalyse gedaan. In deze studie wordt geconcludeerd dat de interventie kosteneffectief lijkt. Het is onduidelijk of deze resultaten geëxtrapoleerd kunnen worden naar andere multicomponent interventies.
Gelijkheid ((health) equity/equitable)
De interventies die worden aangeboden in het ziekenhuis, zullen worden aangeboden aan alle patiënten en hebben daarmee geen effect op de gezondheidsongelijkheid.
Mogelijk dat voor bepaalde interventies verschillende resultaten behaald kunnen worden afhankelijk van de individuele patiënt. Denk aan verschil in opleidingsniveau, culturele opvattingen en taalachterstand.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
Het inzetten van vrijheidsbeperkende maatregelen, kent mogelijk ethische bezwaren. De inzet van dit type interventie dient dan ook kritisch overwogen te worden. Voor de andere (deel)interventies, voorziet de werkgroep geen ethische bezwaren.
Duurzaamheid
Aangezien er bij de interventie meer middelen zullen moeten worden ingezet dan in bij standaard zorg, is dit een minder duurzame keuze. Echter wegen deze overwegingen niet op tegen de effectiviteit van de interventie en duurzaamheidsoverwegingen spelen daarmee geen rol.
Haalbaarheid
De haalbaarheid van de beschreven interventie hangt af van een aantal factoren. In het ziekenhuis speelt de beschikbare capaciteit een cruciale rol bij de implementatie van multicomponent of multifactoriële interventies. Een deel van de genoemde (deel)interventies, zoals de inzet van bewegingsinterventies en de adviezen ten aanzien van vitamine D suppletie zijn eenvoudig te implementeren in de praktijk of behoren al tot de standaard zorg. Er zijn met name zorgen over een adequate implementatie van het uitvoeren van een medicatiereview in de klinische setting. Dit vergt de inzet van extra personeel in het ziekenhuis, waaronder de (ziekenhuis)apotheker, iets wat nu nog zeker geen standaard zorg is in de meeste ziekenhuizen. Het implementeren van een ziekenhuisbreed educatieprogramma ten aanzien van valrisico reductie vergt een forse investering in tijd en geld.
De aanbeveling over de inzet van een multifactoriële interventie geldt voor alle oudere patiënten in het ziekenhuis die verhoogd valrisico hebben en een valrisicobeoordeling ondergaan. Dit kan door verpleegkundig personeel met bestaande instrumenten worden gedaan, maar zij hebben hier wel voldoende tijd voor nodig.
Een multifactorieel valpreventie programma wordt bij voorkeur opgesteld en uitgevoerd door een multidisciplinair team bestaande uit een arts, een verpleegkundige, een fysiotherapeut/oefentherapeut en op indicatie ook een ergotherapeut en een diëtiste. Daarnaast dient ook de follow-up van de interventie te worden uitgevoerd in transmuraal verband na ontslag.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Gezien de grote potentiële gezondheidswinst, verwachtte positieve effecten op kwaliteit van leven en functioneren evenals de aannemelijk kostenbesparing is voor ouderen in het ziekenhuis een sterke aanbeveling om een multifactoriële interventie te verrichten gericht op de geïdentificeerde valrisicofactoren vanuit de multidisciplinaire, multifactoriële valrisicobeoordeling. Vraag uitdrukkelijk na wat de wensen en doelen zijn van de patiënt en bespreek de mogelijkheden. Beslis samen met de patiënt wat de meest geschikte aanpak is in zijn/haar situatie. Dit verhoogt de therapietrouw. De focus moet liggen op de risicofactoren die tijdens de ziekenhuisopname kunnen worden aangepakt. Bij ontslag is een transmurale follow-up en adequate overdracht naar de eerste lijn van belang.
De bewijsvoering betreffende de essentiële deelinterventies binnen de multifactoriële interventie is minder eenduidig doordat er veel inhoudelijk verschil is tussen de verschillende trials. De aanbeveling over de verschillende deelinterventies zijn daarom gebaseerd op de Wereldrichtlijn Valpreventie (Montero-Odasso, 2022) en de NICE guidelines (2025).
Eindoordeel:
Sterke aanbeveling voor multifactoriële valpreventie interventies bij ouderen in het ziekenhuis.
Onderbouwing
Fall incidents are the most common reason for incident reports in hospitals. Approximately 35% of fall incidents in hospitals result in injury (Healey, 2008). These injuries can range from hematomas and bruises to head injuries and bone fractures. Especially in older adults, a fall can lead to fear of falling, which may result in reduced mobility and increased dependency, potentially leading to prolonged hospitalization. Other negative consequences may include longer hospital stays, more frequent transfers to care or nursing homes, the need for additional diagnostic procedures, and possibly even surgical interventions. All these consequences of falls also contribute to the high costs of fall incidents for the healthcare system. Therefore, it is important to prevent fall incidents in hospitals. However, it is still unclear which interventions are most effective in preventing fall incidents.
Hospital falls are a major issue worldwide, with up to 60% leading to injuries that extend hospital stays, reduce independence, and sometimes result in death. A study conducted in acute care hospitals in Australia found that patients who experienced an in-hospital fall had a mean increase in hospital length of stay (LOS) of 8 days and incurred mean additional hospital costs of $6,669 per admission (Morello, 2015). Falls, even without injury, can have significant consequences. For example, concerns about falling and reduced activity levels can impact function and quality of life, increasing the risk of more serious falls.
The incidence of falls in older adults is higher in hospitalized individuals compared to those who are not hospitalized. This indicates distinct risk factors and the need for targeted prevention strategies (Montero-Odasso, 2022). Intrinsic risk factors for in-hospital falls include advanced age (higher likelihood of falling due to factors such as impaired mobility and cognitive decline) (Heikkila, 2023) male sex (de Groot, 2020), cognitive impairment (Zhao, 2015), history of falls, comorbidity (e.g., urinary incontinence) (Brown, 2013) and orthostatic hypotension.
Many in-hospital falls are related to potentially preventable risk factors. Extrinsic risk factors include the use of certain medications (e.g., opioids, sedatives, hypnotics, neuroleptics, antipsychotics, antidepressants, benzodiazepines, and certain cardiovascular drugs and urological medication), medical devices (e.g., intravenous tubes and patient-controlled analgesia pumps). Environmental risk factors include poor lighting, slippery surfaces, and inadequate footwear. 72% of older patients in one hospital study wore ill-fitting shoes. Situational fall risk factors include poor balance and reduced mobility (de Groot, 2020; Nguyen, 2024). Hospital stays often worsen balance and mobility due to decreased activity. The hospital environment can also discourage mobility.
The original Dutch guideline on fall prevention originates from 2017. This module presents an update of this guideline. Various (inter)national guidelines on fall prevention have been published, including the World Falls Guideline (Montero-Odasso, 2022). Both the original version of the Dutch guideline and the World Falls Guideline concluded that multifactorial interventions should be applied to patients with an increased risk of falls in hospital settings. One of the key messages of the World Falls Guidelines is that older adults (aged 65 years and older) should be considered as high fall risk and have a multifactorial falls risk assessment. This module further investigates the effectiveness of multiple component and multifactorial interventions. To gain comprehensive insight into the effectiveness of multifactorial interventions, it is also important to examine the effectiveness of individual (single component) interventions
The following definitions were used for the different intervention types, similar to the definitions used in Hopewell (2018)
- Multiple component interventions: all participants receiving the same combination of interventions.
- Multifactorial interventions: the combination of interventions that is delivered, is tailored towards each individual participant.
Population: Older hospitalized patients
Intervention: Multiple component or multifactorial interventions for fall prevention
Comparator: Usual care, no intervention or another (single-component) interventions
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
|
Intervention |
Control |
||||
|
Multiple component interventions |
|||||
|
Fall risk
|
- |
- |
no GRADE (No evidence was found) |
No evidence was found regarding the effect of multiple component interventions in the hospital setting on fall risk when compared with usual care in older hospitalized patients.
|
|
|
Rate of falls
|
Rate Ratio: 0.82 (95% CI: 0.65 to 1.03). Based on data from 10371 participants in 1 study |
2,58 per 1000 bed days |
3,15 per 1000 bed days |
Low Due to serious risk of bias and serious imprecision1
|
Multiple component interventions may reduce rate of falls when compared with usual care in older hospitalized patients
(Di Gennaro, 2024) |
|
|
|||||
|
Fall related fracture risk |
- |
- |
no GRADE (No evidence was found) |
No evidence was found regarding the effect of multiple component interventions in the hospital setting on fall related fracture risk when compared with usual care in older hospitalized patients.
|
|
|
Multifactorial interventions |
|||||
|
Fall risk
|
Relative Risk: 0.82 (CI 95%: 0.62 – 1.09) Based on data from 39889 participants in 3 studies
|
- |
- |
Low Due to serious risk of bias and serious imprecision2
|
Multifactorial interventions in the hospital setting may reduce fall risk when compared with usual care in older hospitalized patients.
(Barker, 2016; Cumming, 2008; Haines, 2004) |
|
- |
|||||
|
Rate of falls
|
Rate Ratio: 0.8 (CI 95%: 0.64 – 1.01) Based on data from 44664 participants in 5 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Low Due to serious risk of bias and serious imprecision3
|
Multifactorial interventions in the hospital setting may reduce rate of falls when compared with usual care in older hospitalized patients in the hospital.
(Barker, 2016; Cumming, 2008; Haines, 2004; Healey, 2004; Hill, 2015) |
|
|
Fall related fracture risk |
Risk Ratio: 0.76 (CI 95%: 0.14 – 4.10) Based on data from 4615 participants in 2 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Very Low Due to serious risk of bias and very serious imprecision4
|
The evidence is very uncertain about the effect of multifactorial interventions in the hospital setting on fall related fracture risk in older hospitalized patients.
(Cumming, 2008; Haines, 2004) |
|
| 1. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding, risk of other bias. Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference. |
| 2. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding, risk of other bias. Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference. |
| 3. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding, risk of other bias. Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference. |
| 4. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding, risk of other bias Imprecision: very serious. Due to overlap of both limits of the 95% confidence intervals with the minimal clinically important difference. |
Description of studies
An earlier version of this guideline (2017) recommended to use multifactorial interventions to prevent falls in in patients within the hospital. Therefore, in the update of the guideline, focus of the summary of literature was on studies on multiple component and multifactorial interventions. Additionally, to be able to answer the sub-question of this module (“what are the effective intervention components which intervention components should minimally be considered in multicomponent or multifactorial interventions?”) information from systematic reviews on single-component interventions is also summarized under ‘considerations’.
Two systematic reviews, including six relevant RCTs, and one additional RCT were included in the analysis of the literature. Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Cameron (2018) performed a Cochrane systematic review to assess the effects of interventions designed to reduce the incidence of falls in older people in care facilities and in hospitals. The systematic review was an update of the Cochrane review from Cameron (2012). For this update, the Cochrane Database, MEDLINE, EMBASE and CINAHL were searched for relevant papers published until August 2017. Trials on interventions to prevent falls in older people (mean age > 65 years) in care facilities and hospitals were included. Studies on interventions that took place in emergency departments, outpatient clinics or the community were excluded. The intervention had to be any intervention designed to reduce falls in older people, compared with any other intervention, usual care, or placebo. Study designs: randomized trials, including quasi-randomised trials, cluster randomized trials, and trials in which treatment allocations was inadequately concealed. Outcomes included rate of falls, number of fallers and number of patients sustaining fall-related fractures.
In Cameron (2018), 24 studies were included that were executed in the hospital setting. For the purpose of this guideline, only studies on multiple component and multifactorial interventions executed in a hospital setting were considered relevant. In Cameron (2018) no studies were included that examined multiple component interventions in a hospital setting and five studies were included on multifactorial interventions in a hospital setting. An overview of these studies is presented in Table 2. Table 3 presents an overview of the different intervention components that were included in the multifactorial interventions. The remaining 19 studies described single component interventions and were therefore not included in the literature summary. A summary of the results of these studies is presented under the tab ‘considerations’
Morris (2022) performed a systematic review and meta-analysis to evaluate the effects of single- and multifactorial interventions on fall rates and fall risk in hospitals. A search was performed in the databases Medline, CINAHL, PsychInfo, Embase, AMED, PEDro and Cochrane electronic databases, to identify relevant papers on falls intervention in hospitals published until 31 May 2021. Inclusion criteria were: studies on falls intervention in a hospital setting, investigation falls as a primary or secondary outcome and fall data reported and included in a contemporary comparison group (RCT, quasi RCT, cluster RCT, comparative study or quasi-experimental). Studies were excluded if they only had pediatric samples, a historical comparison group, or if falls were only reported in a list of adverse events. For the purpose of this guideline, only randomized trials on multifactorial interventions were considered relevant (n = 6 studies). Of the 43 studies that were included in the systematic review of Morris (2022), six studies were on multiple component or multifactorial interventions (see Table 2). Table 3 presents an overview of the different intervention components that were included in the multifactorial interventions. The remaining 37 studies described single component interventions and were therefore not included in the literature summary. An summary of the results of these studies is presented under the tab ‘considerations’.
Baseline characteristics of the studies can be found in Cameron (2018) and Morris (2022), supplementary file Table 1. All studies that were included in Cameron (2018) were also included in Morris (2022). Additionally, Morris (2022) included four trials that were not included in Cameron (2018).
Table 2: Overview of the randomized controlled trials on multifactorial interventions in the hospital setting, papers included in Cameron (2018) and Morris (2022) (Vergroot Tabel)
|
Author |
Year |
Cameron (2018) |
Morris (2022) |
Participants |
Intervention |
|
Aizen
|
2015 |
Cameron (2018) stated that: “findings of this study were not pooled as some aspects of the study methodology and data collection could not be confirmed” |
X |
Geriatric rehabilitation N = 712 Mean age: 80.8 – 84.6 |
Multifactorial intervention consisting of environmental modification, assistive device, patient education, staff education, fall risk assessment and care plan. |
|
Barker |
2016 |
X |
X |
Acute medical and surgical wards from 6 hospitals N = 31411 Median age: 67
|
Multifactorial intervention: 6-PACK program comprising a 9 item falls risk assessment tool and delivery of one or more of six interventions to high risk patients: 1) Placement of a ‘falls alert’ sign above the patient’s bed. 2) Supervision of patients while in the bathroom. 3) Use of a low-low bed 4) Ensuring that the patient’s walking aid is within reach at all times. 5) Establishment of a toileting regimen. 6) Use of a bed/chair alarm when the patient is positioned in the bed/chair. Staff education integral to implementation. Nurses were asked to update the fall risk tool for each of their patients each shift and to apply a falls alert sign and one or more of the remaining 6-PACK interventions to patients classified as being at high risk
|
|
Cumming |
2008 |
X |
X |
Acute and subacute wards in 12 hospitals N = 3999 Mean age: 79 ± 12.8 |
Targeted multifactorial intervention: a nurse and physiotherapist each worked for 25 hours per week for 3 months in all intervention wards. Provided risk assessment of falls, staff and patient education sessions, drug review, arranged walking aids, eyewear, modification of bedside and ward environments, increased supervision, liaison with staff about confusion and foot problems, an exercise program, and sock alarms for selected patients (maximum of 2 per ward) who staff considered unsafe to walk unsupported
|
|
Haines |
2004 |
X |
X |
Subacute wards N = 626 Mean age: 80 ± 9 |
Targeted falls risk prevention program based on identified falls risk (Peter James Centre Falls Risk Assessment Tool) in additional to usual care. Potential interventions were: 1) supervised exercise program: 45-minute sessions 3 x per week from commencement of intervention until discharge. Exercises comprised gait, balance and coordination + strengthening/resistance + 3D (Tai Chi). Exercises were individually tailored. Exercises were delivered by physiotherapist 2) falls risk alert card 3) up to four educational sessions from occupational therapist (OT) at bedside to individual participants of up to 30-minute duration 4) hip protectors
|
|
Healey |
2004 |
X |
X |
Elderly care wards (acute and subacute) N = 1654 Mean age: 81.3 |
Targeted risk factor reduction care plan for patients with a history of falls or a near fall during admission. Based on assessment (and subsequent referral/action) relating to: eyesight (referral to ophthalmologist); medications check for sedatives, anti-depressants, diuretics, polypharmacy, etc (medical review of benefit vs harm); lying and standing blood pressure (advice to participant and referral to medical staff); ward urine test (mid-stream urine if positive for nitrites, blood or protein); difficulty with mobility (referral to physiotherapist); review of bed rail use; footwear safety (advice on replacement); bed height (kept at lowest height); position in ward (placing high risk patients near nurses’ station); environmental causes (act to correct); nurse call bell (explained and in reach) |
|
Hill |
2015 |
X |
X |
Wards in rehabilitation or geriatric evaluation and management units in hospitals. N = 3121 Mean age: 82 |
Individualised fall education program. Safe Recovery program for patients and staff. For patients, an individually-tailored multimedia falls prevention educational package (DVD and workbook) with further face to face follow-up education (including workbook completion and goal setting) with a health professional was provided. Aimed to alert patients to their personal risk of falls, raise their knowledge about falls epidemiology and falls prevention, and to motivate them to engage in falls prevention strategies. Patient education sessions ranged between 15 and 35 minutes with 1-4 sessions per patient. Staff training in the week of the start of the intervention on their unit and feedback to staff weekly, 56% of patients in the intervention arm were eligible to receive the intervention based on their cognitive status. |
Di Gennaro (2024) performed a randomized controlled trial to assess the effectiveness of a fall preventive care-bundle. The study was executed in twelve hospital units in Italy. Patients aged 75 years and older who were admitted to the units, with or without a fall risk, and patients younger than 75 with an ascertained risk of falls were eligible to participate in the study. Patients were randomized to receive either the care-bundle or standard medical care (in a stepped-wedge design). Groups switched from control to intervention at three fixed timepoints every five months. The care-bundle consisted of: 1) assessment of patients risk of falls at hospital admission, 2) use of alert systems on top of bed frames to increase staff awareness of patients at high risk of falls, 3) systematic communication with patients and family members/caregivers regarding fall risk, 4) application of universal strategies to ensure environmental safety, 5) conduction of rounds every two hours to assess patients’ needs (e.g. change position or drink); 6) regular re-assessment of the patients medications. Patients in the control periods received usual care. In total 10371 patients were included in the study (n = 5914 in the intervention group and n = 4457 in the control group). Outcomes included hospital-acquired falls during intervention and control periods (per bed-days of hospitalization). Costs were reported as a secondary outcome.
The guideline panel considered the intervention that was studies as a multicomponent intervention.
Table 3: overview of the intervention components included in the multiple component and multifactorial interventions studied in the included trials (Vergroot tabel)
|
|
Exercise |
Medication interventions |
Vitamin D supplementation |
Environment |
Assistive technology |
Psychological interventions |
Staff education |
Patient education |
Fall risk assessment |
other |
|
Aizen (2015)
|
|
|
|
x |
x |
|
x |
x |
|
Care plan |
|
Barker (2016) |
|
|
x
|
x |
|
x |
|
x |
Toileting Regimen |
|
|
Cumming (2008) |
x |
x |
|
x |
x |
|
x |
x |
x |
Increased supervision
Liaison with staff about confusion and foot problems |
|
Di Gennaro (2024) |
|
x |
|
x |
x |
|
|
|
x |
Systematic communication with patients family members/ care givers |
|
Haines (2004) |
x |
|
x |
x |
|
|
x |
|
|
|
|
Healey (2004) |
x |
x |
|
x |
x |
|
|
|
|
Assessment of eye sight (referral to ophthalmologist)
Lying and standing blood pressure
Ward urine test
Footwear safety |
|
Hill (2015) |
|
|
|
|
x |
x |
|
|
Results
Multiple component interventions
Fall risk
No studies were found that hat reported the effect of multiple component interventions in the hospital setting on the outcome fall risk.
Rate of falls
Di Gennaro (2024) reported the effect of a multiple component intervention in the hospital setting on rate of falls. The incident rate (IR) for falls of the multiple component intervention group was 2.58 per 1000 bed-days, compared to an in IR of 3.15 for 1000 bed days in the usual care group. The Rate Ratio was 0.82 (95% CI: 0.65 to 1.03).
Fall related fracture risk
No studies were found that reported the effect multiple component interventions in the hospital setting on the outcome fall related fracture risk.
Multifactorial interventions
Fall risk
Four studies reported the effects of multifactorial interventions in the hospital setting on fall risk (Aizen, 2015; Barker, 2016; Cumming, 2008; Haines, 2004). The results from the study of Aizen (2015) were not pooled since some aspects of the study methodology and data collection could not be confirmed.
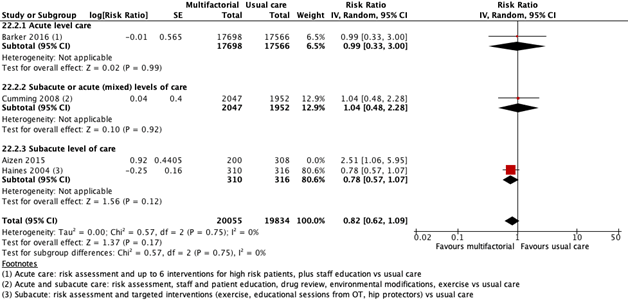
The RR between patients who received a multifactorial intervention (n = 20055) compared to patients who received usual care (n = 19834) was RR: 0.82 (95% BI: 0.62 to 1.09).
Figure 1. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome fall risk. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Falls rate
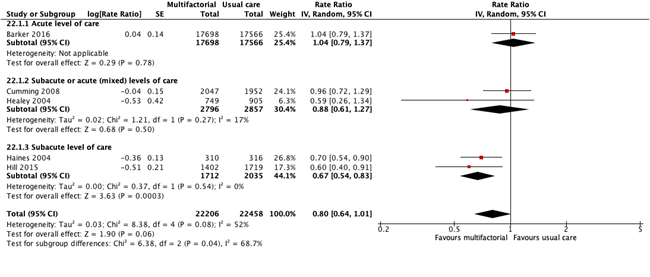
Five studies reported the effects of multifactorial interventions on fall frequency (Barker, 2016; Cumming, 2008; Haines, 2004; Healey 2014; Hill, 2015). The RR between patients who received a multifactorial intervention (n = 22206) compared to patients who received usual care (n = 22458) was RR: 0.80 (95% CI: 0.64 to 1.01). See Figure 2.
Figure 2. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome falls rate. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Fall related fracture risk
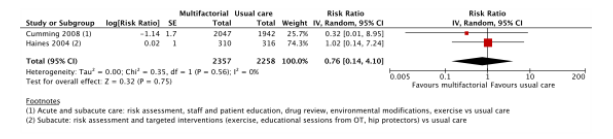
Two studies reported the effects of multifactorial interventions on fall related fracture risk (Cumming, 2008; Haines, 2004). The difference between patients who received a multifactorial intervention (n = 2357) compared to patients who received usual care (n = 2258) was RR: 0.76 (95% CI: 0.14 to 4.10). See Figure 3
Figure 3. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome fracture risk. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval
A systematic review of the literature was performed to answer the following question: What is the effectiveness of multiple component and multifactorial interventions for fall prevention, compared to usual care, no intervention or another (single component) intervention?
Table 1. PICO
|
Patients |
Older hospitalized patients |
|
Intervention |
Multiple component and multifactorial interventions for fall prevention |
|
Control |
Usual care, no intervention or another (single component) intervention |
|
Outcomes |
|
|
Other selection criteria |
Study design:
|
Relevant outcome measures
A priori, the guideline panel defined the outcomes as follows:
- Falls risk: The risk of being a faller; the number of people who fell once or more (fallers) in the intervention and control groups
- Rate of falls: falls per unit of person time (such as bed days), presented as the rate ratio
- Fall related fracture risk: the risk of fall related fractures in the intervention group, compared to the control group.
The guideline panel considered falls risk and rate of falls as a critical outcome measure for decision making; and fall related fracture risk as an important outcome measure for decision making.
The guideline panel defined a difference of 10% as a minimal clinically (patient) important difference, RR < 0.90 and RR > 1.10 for the outcomes falls risk, rate of falls and fall related fracture risk.
Search and select (Methods)
To answer this question, the Cochrane systematic review from Cameron (2018) was used as a basis for this literature analysis. In Cameron (2018), the Cochrane Bone, Joint and Muscle trauma group Register, the Cochrane Central register of Controlled trials (CENTRAL), OVID/MEDLINE, Embase and CINAHL were searched with relevant search terms, until 12-06-2017. We performed an update of this Cochrane Systematic review with the same search terms as used in Cameron (2018). The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms for articles published between 12-06-2017 until 09-08-2024. A combined search for older persons in the hospital, older persons in the community and older persons living in nursing homes was performed, as the specific research setting was not always specified in the title/abstract. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 6510 hits. Studies were selected based on the criteria described in Table 1. Titles and abstracts were screened using the ASReview software version 1.6.2. The settings TF-IDF and Naïve bayes were used. Morris (2022) was used as prior knowledge for inclusion. Park (2021), Borreli (2021), Verrusio (2018) were used as prior knowledge for exclusions.
The first 10% of references were screened by the working group and the guideline methodologist. The remaining articles were subsequently screened by the guideline methodologist, using the following stopping rule: stop after 200 subsequent exclusions.
Initially, sixteen studies were selected based on title and abstract screening using ASreview software. After reading the full text, fourteen studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and two studies were included.
- Cameron ID, Dyer SM, Panagoda CE, Murray GR, Hill KD, Cumming RG, Kerse N. Interventions for preventing falls in older people in care facilities and hospitals. Cochrane Database Syst Rev. 2018 Sep 7;9(9):CD005465. doi: 10.1002/14651858.CD005465.pub4. PMID: 30191554; PMCID: PMC6148705.
- Di Gennaro G, Chamitava L, Pertile P, Ambrosi E, Mosci D, Fila A, Alemayohu MA, Cazzoletti L, Tardivo S, Zanolin ME. A stepped-wedge randomised controlled trial to assess efficacy and cost-effectiveness of a care-bundle to prevent falls in older hospitalised patients. Age Ageing. 2024 Jan 2;53(1):afad244. doi: 10.1093/ageing/afad244. PMID: 38251740; PMCID: PMC10801830
- Montero-Odasso M, van der Velde N, Martin FC, Petrovic M, Tan MP, Ryg J, Aguilar-Navarro S, Alexander NB, Becker C, Blain H, Bourke R, Cameron ID, Camicioli R, Clemson L, Close J, Delbaere K, Duan L, Duque G, Dyer SM, Freiberger E, Ganz DA, Gómez F, Hausdorff JM, Hogan DB, Hunter SMW, Jauregui JR, Kamkar N, Kenny RA, Lamb SE, Latham NK, Lipsitz LA, Liu-Ambrose T, Logan P, Lord SR, Mallet L, Marsh D, Milisen K, Moctezuma-Gallegos R, Morris ME, Nieuwboer A, Perracini MR, Pieruccini-Faria F, Pighills A, Said C, Sejdic E, Sherrington C, Skelton DA, Dsouza S, Speechley M, Stark S, Todd C, Troen BR, van der Cammen T, Verghese J, Vlaeyen E, Watt JA, Masud T; Task Force on Global Guidelines for Falls in Older Adults. World guidelines for falls prevention and management for older adults: a global initiative. Age Ageing. 2022 Sep 2;51(9):afac205. doi: 10.1093/ageing/afac205. Erratum in: Age Ageing. 2023 Sep 1;52(9):afad188. doi: 10.1093/ageing/afad188. Erratum in: Age Ageing. 2023 Oct 2;52(10):afad199. doi: 10.1093/ageing/afad199. PMID: 36178003; PMCID: PMC9523684.
- Morris ME, Webster K, Jones C, Hill AM, Haines T, McPhail S, Kiegaldie D, Slade S, Jazayeri D, Heng H, Shorr R, Carey L, Barker A, Cameron I. Interventions to reduce falls in hospitals: a systematic review and meta-analysis. Age Ageing. 2022 May 1;51(5):afac077. doi: 10.1093/ageing/afac077. PMID: 35524748; PMCID: PMC9078046.
- National Institute for Health Care Excellence (NICE). Falls: assessment and prevention in older people and in people 50 and over at higher risk: NG249. London, NICE; 2025 Apr 29. Available from: https://www.nice.org.uk/guidance/ng249
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-04-2026
Beoordeeld op geldigheid : 30-04-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinair cluster ingesteld. Het cluster Duizeligheid, Vallen en Syncope bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden geven hun expertise, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Prof. dr. T.D. (Tjasse) Bruintjes, voorzitter cluster Duizeligheid, Vallen en Syncope, NVKNO, KNO-arts, Gelre Ziekenhuizen
- Prof. dr. N. (Nathalie) van der Velde, NVKG, klinisch geriater, Amsterdam UMC
- Dr. R.B. (Roeland) van Leeuwen, NVN, neuroloog, Gelre Ziekenhuizen
- Dr. J.H.W. (Joost) Rutten, NIV, internist, Radboud UMC
- Drs. S. (Simon) Geerse, NVKNO, KNO-arts, Treant Ziekenhuizen
- Dr. W.P.A. (Willem) Kelders, NVKNO, KNO-arts, Franciscus Gasthuis & Vlietland
- Drs. J.O. (Judella) Daal, NVKG, klinisch-geriater, Dijklander Ziekenhuis
Clusterexpertisegroep
- Drs. C.M. (Margreet) Aalten, NVKG klinisch geriater, St. Jansdal Ziekenhuis
- Ir. R.M. (Renske) Hoeben, NVKF, Klinisch Fysicus, Bernhoven
- Drs. B.S. (Birgit) Jacobs, NVZA, ziekenhuisapotheker, Catharina Ziekenhuis
- Dr. E.C.A. (Evert) Kaal, NVN, neuroloog, Maasstad Ziekhuis
- Dr. W.F. (Linde) Kok, Verenso, specialist ouderengeneeskunde bij GeriCall
- Dr. E.P. (Eveline) van Poelgeest, NIV, NVKG, internist-ouderengeneeskunde, Amsterdam UMC
- Dr. V.A. (Vincent) van Vugt, NHG, huisarts, Amsterdam UMC
- B.J.F.M. (Bart) Zwaneveld, KNGF, orofaciaal en manueel therapeut
Met ondersteuning van
- Dr. R. Zwarts - van de Putte, adviseur, Kennisinstituut van Medisch Specialisten
- Drs. D.G. Ossendrijver, adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Cluster stuurgroepleden
Tabel 1 Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Tjasse Bruintjes*
|
- KNO-arts (vrijgevestigd) Gelre ziekenhuizen Apeldoorn (0,8 fte) |
- lid beroepsgenoot Regionaal Tuchtcollege voor de Gezondheidszorg Zwolle (onkostenvergoeding) |
Geen |
Geen |
In 2022 toegekende ZonMW-subsidie voor de zgn. Predmentrial |
Geen |
Geen |
07-01-2021
18-05-2025 herbevestigd |
Geen |
|
Nathalie Van der Velde |
Staflid en hoogleraar onderafdeling Geriatrie Amsterdam UMC, lokatie AMC |
Onbetaald: |
Geen |
Geen |
Nee; alleen subsidies van onafhankelijke subsidieverstrekkers (NWO, ZonMW, Amsterdams Universiteitsfonds) |
Geen |
Geen |
07-10-2020
06-06-2025 herbevestigd |
Geen |
|
Roeland Van Leeuwen |
Neuroloog, Gelre ziekenhuizen Apeldoorn |
Lid Scheidsgerecht Gezondheidszorg. Betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
11-10-2020
18-05-2025 herbevestigd |
Geen |
|
Joost Rutten |
Internist-Vasculair Geneeskunde 0.9 FTE/Radboudumc, Nijmegen |
Consultant op projectbasis voor Volw International - project ontwikkeling screeningstool ter opsporing patiënten met lipodystrofie |
Geen |
Geen |
Principle Investigator Radboudumc CALM DIEM en CALM START studies, sponsor Vascular Dynamics (studies naar effect van specifiek type carotisstent ter verlaging van de bloeddruk) |
Geen |
Geen |
21-01-2021
23-05-2025 herbevestigd |
|
|
Simon Geerse |
KNO-arts (vrijgevestigd) Treant ziekenhuizen (0.8 fte) |
Voorzitter kerngroep Vestibulologie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
21-01-2021
26-5-2025 herbevestigd |
Geen |
|
Willem Kelders |
- KNO-arts (vrijgevestigd) Franciscus Gasthuis en Vlietland Rotterdam (0,8 fte) |
- lid kerngroep vestibulogie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
10-01-2021
17-5-2025 herbevestigd |
Geen |
|
Judella Daal |
NVKG als vereniging |
Voorzitter SIG Valpreventie NVKG/Landelijke netwerk valklinieken |
Geen |
Geen |
Geen |
Geen |
Geen |
10-04-2025
21-5-2025 herbevestigd |
Geen |
Betrokken cluster expertisegroepleden
Tabel 2 Gemelde (neven)functies en belangen expertisegroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Margreet Aalten |
Klinisch geriater Ziekenhuis St. Jansdal Harderwijk 0,6 FTE |
Lid accreditatie beoordelingscommissie NVKG onbezoldigd. |
Geen |
Geen |
Geen |
Geen |
Geen |
13-10-2021
20-05-2025 herbevestigd |
Geen |
|
Evert Kaal |
Neuroloog Maasstad Ziekenhuis 0,8 FTE |
Voorzitter Werkgroep voor Syncope en Autonome Aandoeningen, onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-10-2021
18-06-2025 herbevestigd |
Geen |
|
Linde Kok |
Specialist Ouderengeneeskunde bij GeriCall, momenteel in de 1e lijn |
Geen |
Geen |
Geen relaties met belangen |
Geen |
Geen |
Geen |
10-10-2023
16-5-2025 herbevestigd |
Geen |
|
Eveline Van Poelgeest |
Internist ouderengeneeskunde AUMC, betaald |
Kernlid Expertisecentrum farmacotherapie bij ouderen (Ephor), betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-06-2023
16-5-2025 herbevestigd
|
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door deelname van de Patiëntenfederatie Nederland in de richtlijncommissie.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Module verlaging valrisico bij thuiswonende ouderen |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.