Verlaging valrisico bij thuiswonende ouderen
Uitgangsvraag
Welke (multifactoriële) valpreventieve interventies zijn effectief bij thuiswonende ouderen met een matig of hoog valrisico?
Deelvraag: Wat zijn de effectieve interventiecomponenten en welke componenten zouden minimaal overwogen moeten worden in multicomponent of multifactoriële interventies?
Aanbeveling
Hoog valrisico:
Voer bij thuiswonende ouderen met een hoog valrisico een multifactoriële valpreventieve interventie* uit, gebaseerd op de geïdentificeerde valrisicofactoren vanuit de multidisciplinaire, multifactoriële valrisicobeoordeling.
Bespreek met de patiënt diens wensen en doelen en bepaal samen de meest geschikte aanpak om de therapietrouw te verhogen.
Neem altijd een beweeginterventie op met balans- en functiegerichte componenten.
Verwerk daarnaast in de multifactoriële valpreventieve interventie de positief gescoorde valrisicofactoren en overweeg minimaal de volgende items (voor details per interventiecomponent zie tabel Aanbevelingen valpreventieve interventies thuiswonende ouderen):
Startend met de interventie met de hoogste bewijskracht
- Afbouw van valrisicoverhogende medicatie via gestructureerde medicatieoptimalisatie (zie hiervoor de module beoordeling valrisicoverhogende medicatie)
- Persoons-omgevingsinterventies
- Management van orthostatische hypotensie (conform de module valpreventie bij orthostatische hypotensie) en cardiovasculaire aandoeningen op vergelijkbare wijze als ouderen met syncope
- Kennisoverdracht over valpreventie (beweeg-, omgevings- en alcoholadviezen)
- Behandeling van acute en chronische aandoeningen
- Optimalisatie van visus (cataract OK indien aangewezen, refractie) en gehoor
- Aanpak van voetproblemen en passend en veilig schoeisel
- Interventies gericht op bezorgdheid om te vallen (valangst)
- Vitamine D-suppletie
- Behandeling van (risico op) ondervoeding en dehydratie
- Behandeling van cognitieve stoornissen en depressie
- Behandeling van vestibulaire aandoeningen (duizeligheid)
- Management van incontinentie
- Pijnmanagement
Evalueer de uitvoering en effecten van de interventie binnen 30–90 dagen en pas het behandelplan zo nodig aan.
Matig valrisico:
Bied ouderen met een matig valrisico een multicomponent* interventie aan met minimaal de volgende onderdelen:
- Beweeginterventie met balans- en functiecomponenten
- Mondelinge en schriftelijke informatie over valpreventie (kennisoverdracht)
Overweeg daarnaast persoons-omgevingsinterventies.
*Multicomponent: alle patiënten krijgen dezelfde combinatie van interventiecomponenten; Multifactorieel: de combinatie van interventiecomponenten wordt afgestemd op de individuele patiënt.
Overwegingen
Balans tussen gewenste en ongewenste effecten en kwaliteit van bewijs
Recente richtlijnen over valpreventie, waaronder de wereldrichtlijn valpreventie (Montero-Odasso, 2022) en de NICE guideline Falls (2025), bevelen aan om multifactoriële valpreventieve interventies (hierna: multifactoriële interventies) in te zetten bij thuiswonende ouderen met een hoog valrisico.
Samenvattend wordt door deze richtlijnen aanbevolen om indien er sprake is van een hoog valrisico niet een standaard (enkelvoudige of multicomponent) interventie aan te bieden, maar een geïndividualiseerde interventie, gebaseerd op de in de uitgebreide, multidisciplinaire, multifactoriële valrisicobeoordeling geïdentificeerde modificeerbare valrisicofactoren. Dit is gebaseerd op geüpdatete literatuurreviews die onder andere een recente netwerk meta-analyse van 220 trials (Dautzenberg, 2021) bevat.
Bij matig valrisico bevelen de beide recente richtlijnen (Montero-Odasso 2022 en NICE 2025) aan om een multicomponent interventie aan te bieden, bestaande uit een beweeginterventie en kennisoverdracht (educatie). Voor deze aanpak is er sterke bewijsvoering. Uiteraard kan er in individuele gevallen sprake zijn van andere bijkomende valrisicofactoren die ook behandeling behoeven.
Ondanks de huidige aanbeveling om multifactoriële interventies in te zetten bij hoog valrisico, bestaan er over de optimale inhoud van deze interventie nog veel vragen. Daarom is er voor de update van deze module literatuuronderzoek uitgevoerd naar multifactoriële interventies ter preventie van vallen bij thuiswonende ouderen. Omdat er in de literatuur vaak geen eenduidige definitie van multifactoriële interventies wordt gehanteerd, is er ook gezocht naar multicomponent interventies. Multicomponent interventies worden hierbij gedefinieerd als een interventie waarbij alle deelnemers dezelfde combinatie van deelinterventies ontvangen. Bij multifactoriële interventies wordt de combinatie van deelinterventies aangepast naar de individuele patiënt. Redelijkerwijs kan ook worden aangenomen dat effectieve enkelvoudige interventies ook effectief zullen zijn indien onderdeel van een uitgebreide, multifactoriële interventie. Het literatuuronderzoek richtte zich op de effectiviteit van multicomponent en multifactoriële valrisicoverlagende interventies bij thuiswonende ouderen. Daarbij werd als deelvraag geformuleerd: Wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten? Er werd een netwerk meta-analyse gevonden, waarin 220 RCTs, met 104.638 patiënten waren geïncludeerd (Dautzenberg 2021). Daarnaast werden er nog zeven gerandomiseerde studies gevonden die zijn gepubliceerd na de zoekdatum van de netwerk meta-analyse.
In de netwerk meta-analyse werden veel verschillende combinaties van deelinterventies onderzocht. De volgende enkelvoudige deelinterventies werden geanalyseerd:
- Exercise (beweeginterventies)
- Medication (vitamine D)
- Surgery (operaties inclusief pacemaker plaatsing en cataract OK)
- Management of urinary incontinence (incontinentie management)
- Fluid or nutrition therapy (management dehydratie en (risico op) ondervoeding)
- Psychological interventions (psychologische interventies)
- Environmental assessment and modifications ((persoonsomgevingsinterventies)
- Assistive technology ((passend) hulpmiddelgebruik)
- Social engagement (sociale interventies)
- Quality improvement strategies (kennisoverdracht/patiënteducatie, kwaliteitsverbeteringsstrategieen)
- Management of orthostatic hypotension (management orthostatische hypotensie)
- Basic falls risk assessment (medicatiereview, cardiovasculaire interventies en fractuurpreventie)
- Whole-body vibration (trilplaat-/vibratietraining)
- Chiropractic care (chiropracter)
Deze enkelvoudige deelinterventies werden gecombineerd in verschillende multicomponent of multifactoriële interventies in Dautzenberg (2021). Voor de meerderheid van combinaties (n = 34), werd klinisch relevante verlaging gerapporteerd van het aantal patiënten met valincidenten (valrisico; cruciale uitkomstmaat) en valfrequentie (cruciale uitkomstmaat) wanneer vergeleken met gebruikelijke zorg. Over het algemeen lijken multicomponent en multifactoriële interventies het valrisico (gedefinieerd als het aantal patiënten dat valt) en valfrequentie te verlagen wanneer vergeleken met gebruikelijke zorg. Ook voor valgerelateerde botbreuken (belangrijke uitkomstmaat) was er een klinisch relevante risicoverlaging voor de meerderheid van de multicomponent en multifactoriële interventies.
Om de deelvraag ‘wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten’ te kunnen beantwoorden is gebruik gemaakt van de analyse van Dautzenberg (2021). Op basis van een component analyse wordt in Dautzenberg (2021) geconcludeerd dat de volgende veelgebruikte interventie componenten individueel geassocieerd zijn met een verlaging van het aantal patiënten dat valt, de valfrequentie en/of valgerelateerde fractuur
- Beweeginterventies
- Kennisoverdracht/patiënteducatie (kwaliteitsverbetering strategieën)
- (Passend) hulpmiddelgebruik
- Persoons-omgevingsinterventies
- Basis valpreventie strategie inclusief medicatiereview
Een trilplaat-/vibratieinterventie was ook een effectieve component, deze is echter slechts in enkele studies onderzocht, waardoor de mate van bewijskracht wat lager is.
Om de deelvraag te kunnen beantwoorden, is er daarnaast gekeken naar de resultaten uit Cochrane reviews. In de Cochrane review betreffende multifactoriële interventies bij thuiswonende ouderen (Hopewell 2018) wordt geconcludeerd dat de meest voorkomende componenten van multifactoriële interventies zijn: beweeginterventies, persoons-omgevingsinterventies, (passend) hulpmiddelgebruik, medicatiereview en psychologische interventies. De belangrijkste bevindingen betreffende enkelvoudige interventies zijn te vinden in Tabel 7.
Tabel 7: overzicht van de resultaten uit Cochrane reviews over enkelvoudige valrisicoverlagende interventies
|
|
Valrisico (aantal patiënten dat valt) |
Valfrequentie (aantal valepisoden) |
Risico op botbreuken |
|
Beweeginterventies (Sherrington, 2018) |
RR: 0,77 (95% BI: 0,71 tot 0,83) N=12.981, 59 studies |
RR: 0,85 (95% BI: 0,81 tot 0,89) N=13.518, 63 studies |
RR: 0,73 (95% BI: 0,56 tot 0,95) N=4.047, 10 studies |
|
Omgevingsfactoren (Clemson, 2023) |
RR: 0,89 (95% BI 0,82 tot 0,97) N=5.253, 12 studies |
RR: 0,74 (95% BI: 0,61 tot 0,91) N=5.293, 12 studies |
RR: 1,00 (95% BI: 0,98 tot 1,02) N=1.668, 2 studies |
|
Psychologische en educatieve interventies (Drahota, 2024)
|
|
|
|
|
Cognitieve gedragsinterventies |
RR: 0,92 (95% BI: 0,82 tot 1,02) N=1.286, 4 studies
|
Rate ratio: 0,87 (95% BI: 0,73 tot 1,03) N=NR, 4 studies |
Geen informatie |
|
Motiverende gespreksvoering |
RR: 1,44 (95% BI: 0,97 tot 2,14) N=118, 1 studie
|
Rate ratio: 1,19 (95% BI: 0,86 tot 1,64) N=119, 1 studie |
Geen informatie |
|
Andere psychologische interventies |
RR: 1,04 (95% BI: 0,70 tot 1,53) N=114, 1 studie
|
RR: 1,29 (95% BI: 0,74 tot 2,24) N=NR, 1 studie |
RR: 0,21 (95% BI: 0,01 tot 4,22) N=114, 1 studie |
|
Educatie |
RR: 0,85 (95% BI: 0,63 tot 1,14) N=3.339, 5 studies
|
Rate ratio: 0,95 (95% BI 0,77 tot 1,17) N=NR, 2 studies |
RR: 0,66 (95% BI: 0,29 tot 1,48) N=510, 2 studies |
|
Psychologische + educatieve interventies |
RR: 0,93 (95% BI 0,76 tot 1,13) N=430, 1 studie |
Rate ratio: 0,65 (95% BI 0,43 tot 0,99) N=430, 1 studie |
Geen informatie |
|
Multifactoriële interventies (Hopewell, 2018) |
|
|
|
|
Vergelijking; Gebruikelijke zorg of aandachtscontrole |
RR: 0,96 (95% BI: 0,90 tot 1,03) N=9.637, 29 studies |
RR: 0,77 (95% BI: 0,67 tot 0,87) N=5.853, 19 studies |
RR=0,73 (95% BI: 0,53 tot 1,01) N=2.850, 9 studies |
|
Vergelijking: Lichamelijke beweging |
RR=0,26 (95% BI: 0,01 tot 2,46) N=31, 1 studie |
RR: 0,13 (95%BI: 0,01 tot 2,46) N=31, 1 studie |
Geen informatie |
Cochrane publicaties over medicatie en cardiovasculaire interventies ter verlaging van het valrisico zijn nog niet gepubliceerd, waardoor deze hier niet zijn meegenomen. Daarnaast vallen population based interventions buiten de scope van deze module, daarom staan resultaten uit het Cochrane review van Lewis (2024) hier niet beschreven.
Hoewel niet voor ieder type (deel)interventie een klinisch relevante verlaging van het valrisico of de valfrequentie wordt aangetoond, impliceert dit niet dat deze interventies binnen een multifactoriële benadering eveneens ineffectief zijn. Zelfs wanneer er multifactoriële interventies worden ingezet volgens de hoogste wetenschappelijke standaarden, komt er nog geen eenduidige conclusie in welke vorm deze (het meest) effectief zijn. Dit neemt niet weg dat er grote aantallen patiënten met een verhoogd valrisico zijn die baat hebben bij dergelijke interventies. Het is belangrijk dat de interventie die wordt aangeboden aansluit bij de risicofactoren die zijn geïdentificeerd met de
multidisciplinaire, multifactoriële valrisicobeoordeling. De optimale samenstelling van een multifactoriële interventie zal per individu verschillen. Wel wordt er aanbevolen om minimaal een beweeginterventie te verwerken in een multifactoriële interventie. Dit gezien de sterke bewijskracht voor de effectiviteit van dit type interventie.
Ook is vervolg van de uitvoering (compliantie) en de effecten van de ingezette interventies van belang om te komen tot een effectieve aanpak, met zo nodig aanpassingen in het behandelplan aan op basis van de bevindingen. De wereldrichtlijn en de NICE richtlijn, adviseren hierbij een follow-up termijn van 30-90 dagen.
Aanvullend op de bewijsvoering van bovengenoemde componenten, beveelt zowel de wereldrichtlijn als de NICE richtlijn dan ook aan om het geïndividualiseerde valpreventieplan te baseren op een holistische multifactoriële valrisicobeoordeling, zoals in de betreffende module beschreven, waarbij gezamenlijke besluitvorming wordt toegepast om passende doelen en interventies vast te stellen. Dit betekent dat er aandacht besteed dient te worden aan de gehele klinische beoordeling (comprehensive geriatric assessment (CGA)) en rekening gehouden dient te worden met de prioriteiten, overtuigingen en middelen van de oudere en andere relevante personen, zoals mantelzorgers. Reden hiervoor is zodat er een haalbaar plan kan worden ontwikkeld waarin rekening wordt gehouden met individueel relevante risicofactoren in de context van andere geriatrische syndromen en aandoeningen.
De richtlijnwerkgroep is van mening interventies die worden beschreven in Dautzenberg (2024), de wereldrichtlijn valpreventie en in de NICE richtlijn ook relevant zijn voor de Nederlandse setting. Voor een overzicht van de aanbevelingen over de verschillende deelinterventies, zie tabel 9.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Bij de verschillende interventies is het belangrijk om bij de persoon zelf aandacht te hebben voor: zijn/haar autonomie, zoveel mogelijk aansluiten bij de wensen en behoefte van de oudere zelf, een goede uitleg over het belang van valpreventie en zorg te dragen voor een goede motivatie. Dit kan bijvoorbeeld behoud van zelfredzaamheid en zelfstandig functioneren betreffen, maar ook lang leven of het voorkomen van cardiovasculaire of andere events. Gezamenlijke besluitvorming is daarom essentieel om te komen tot een passend behandelplan. Betrek in de besluitvorming ook andere relevante personen zoals mantelzorgers.
Kostenaspecten
Het is aannemelijk dat de kosten van de interventies hoger zijn dan bij standaard zorg, dit betreft bijvoorbeeld materiële uitgaven, kosten voor een (extra) polikliniekbezoek en kosten voor fysiotherapie en/of ergotherapie. Echter, wanneer er met de inzet van een multifactoriële interventie een toekomstige val kan worden voorkomen, wegen deze extra kosten hier waarschijnlijk tegen op. Uit eerdere studies blijken de kosten van een valincident bij ouderen in de Nederlandse gezondheidszorgsetting te liggen tussen vierduizend en dertienduizend euro per valincident. Een recente maatschappelijke kosten-batenanalyse (MKBA) betreffende valpreventie voor thuiswonende ouderen in de Nederlandse setting liet zien dat alle scenario’s leidden tot gezondheidswinst, variërend van 90 vermeden disability-adjusted life years (DALY’s) in de informele zorg tot 300 in het eerstelijnszorgscenario. Een sensitiviteitsanalyse toonde aan dat factoren zoals een lagere leeftijdsgrens, gepaard gaande met een laag initieel valrisico voor werving, de uitkomsten van de MKBA significant (negatief) beïnvloeden.
Gelijkheid ((health) equity/equitable)
Niet elke oudere heeft dezelfde toegang tot zorg, informatie of ondersteuning, en culturele, sociale of sociaaleconomische verschillen kunnen de effectiviteit van interventies beïnvloeden. Deze factoren dienen dan ook meegenomen te worden bij de keuze voor een multifactoriële interventie. Dit onderschrijft het belang van het aanpassen van de interventie naar de wensen en behoefte van de oudere.
Mogelijk dat voor bepaalde interventies verschillende resultaten behaald kunnen worden afhankelijk van de individuele patiënt. Denk aan verschil in opleidingsniveau, culturele opvattingen en taalachterstand.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
Het inzetten van vrijheidsbeperkende maatregelen, kent mogelijk ethische bezwaren. De inzet van dit type interventie dient dan ook kritisch overwogen te worden. Voor de andere (deel)interventies, voorziet de werkgroep geen ethische bezwaren.
Duurzaamheid
Aangezien er bij de interventie meer middelen zullen moeten worden ingezet dan bij standaard zorg, is dit potentieel een minder duurzame keuze. Echter wegen deze overwegingen niet op tegen de effectiviteit van de interventie en daarnaast kan voorkomen van letsel en bijbehorende zorgconsumptie leiden tot minder middelen gebruik. Duurzaamheidsoverwegingen spelen daarmee geen rol.
Haalbaarheid
De kloof tussen onderzoek en implementatie is voor valpreventie, net als bij andere gebieden waarbij een interventie individueel gedrag betreft, substantieel. Zoals Tinetti in 2006 stelden, zijn uitdagingen zoals tijdsdruk en concurrerende klinische eisen vergelijkbaar met die van andere gezondheidszorgdiensten. Hoewel ze voor valpreventie wellicht van grotere omvang zijn vanwege het personeel intensieve karakter ervan. Bovendien is er een algemeen gebrek aan kennis, vaardigheden en coördinatie die nodig zijn voor de unieke aard van geriatrische syndromen, die niet passen in het traditionele ziektemodel van klinische zorg en vergoeding (Tinetti, 2006). Het verminderen van de incidentie van vallen wordt verder belemmerd door het gebrek aan robuust beleid op populatieniveau (WHO, 2021; van der Velde 2025).
In Nederland zijn er recent belangrijke stappen gemaakt, door middel van het Landelijk Programma Valpreventie met de bijbehorende ketenaanpak van het ministerie van Volksgezondheid, Welzijn en Sport (IGJ, 2024). Het WHO-rapport Step Safely pleit voor een systeembenadering met de wisselwerking van complexe factoren: de biologie, het gedrag, de fysieke omgeving en de culturele en sociaaleconomische omgeving van personen binnen een bio-psycho-sociaal model. Het beveelt interventies aan die een veiligere persoonlijke situatie, veiligere omgevingen, veiliger beleid en betere wetgeving omvatten. Effectief beleid vereist betrokkenheid van de juiste belanghebbenden, waaronder besluitvormers en beleidsmakers, financiers van de gezondheidszorg, professionals in de gezondheidszorg en ouderenverenigingen en -belangenbehartigers.
Een analyse van succesvolle trials en de verschillen met 2 recente, pragmatische trials met negatieve uitkomsten (van der Velde, 2022; van der Velde, 2025) laat zien dat naast studiekarakteristieken, de gekozen doelpopulatie (hoog versus matig of laag valrisico), het interventieontwerp, en de uitvoering en therapietrouw belangrijke bepalende factoren zijn. Het ideale interventieprogramma zou een multidisciplinaire CGA-benadering moeten gebruiken, die input vereist van artsen, verpleegkundigen, fysiotherapeuten en ergotherapeuten die zijn opgeleid in het beoordelen van vallen. Ook is een transmurale follow-up essentieel om de uitvoering (compliantie) en de effecten van de ingezette interventies te monitoren en bij te sturen zodat waar nodig het behandelplan aangepast kan worden op basis van de bevindingen. De NICE richtlijn beveelt aan om 30 tot 90 dagen na het starten van de interventie een vervolgonderzoek in te plannen.
Andere mogelijke belemmeringen, zoals vervoer, eigen bijdragen of verzekeringsdekking, kunnen ook hebben bijgedragen aan de lage deelname en therapietrouw.
De aanbeveling om een multifactoriële valpreventie interventie in te zetten, geldt voor alle thuiswonende oudere patiënten bij wie op basis van een multifactoriële valrisicobeoordeling een hoog valrisico is vastgesteld. Hierbij zijn transmurale samenwerkingsafspraken tussen de eerste en de tweede lijn van belang. Reden hiervoor is dat er optimaal en efficiënt gebruik gemaakt kan worden van bestaande middelen. Specifiek voor de setting van de spoedeisende hulp (SEH) geldt dat ten tijde van het SEH bezoek de focus ligt op behandeling van urgente en acute problemen. Een vervolgbehandeling die alle relevante behandelbare valrisicofactoren meeneemt, dient daarna plaats te vinden dan wel in de eerste lijn, dan wel poliklinisch, afhankelijk van regionale zorgpaden en afspraken. Voor de aanpak in lijn met de huidige IGJ-behandelaanwijzing op dit onderwerp verwijzen we naar de module Vallen als atypische uiting van een onderliggende ziekte .
De module organisatie van zorg beschrijft op welke manier de organisatie, taakverdeling en samenwerking in de keten moet worden ingericht om de multifactoriële interventies op een adequate manier te implementeren. Beperkingen in capaciteit en middelen in zowel de eerste lijn (waaronder huisartsen en apothekers) als tweede lijn zijn hierbij mogelijk een belemmerende factor voor de haalbaarheid van de interventie.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Voor patiënten met een hoog valrisico wordt een multifactoriële valpreventie interventie aanbevolen. Gezien de grote potentiële gezondheidswinst, verwachtte positieve effecten op kwaliteit van leven en functioneren evenals de aannemelijk kostenbesparing is voor thuiswonende ouderen met een hoog valrisico een sterke aanbeveling om een multifactoriële interventie te verrichten gericht op de geïdentificeerde valrisicofactoren vanuit de multidisciplinaire, multifactoriële valrisicobeoordeling. Vraag uitdrukkelijk na wat de wensen en doelen zijn van de patiënt en bespreek de mogelijkheden. Beslis samen met de patiënt wat de meest geschikte aanpak is in zijn/haar situatie. Dit verhoogt de therapietrouw.
De bewijsvoering over de essentiële deelinterventies binnen de multifactoriële interventie is minder eenduidig. Dit komt doordat er veel inhoudelijk verschil is tussen de verschillende trials. In lijn met de aanbevelingen van de wereldrichtlijn valpreventie en de NICE richtlijn is de aanbeveling dat er aandacht besteed dient te worden aan de gehele klinische beoordeling (comprehensive geriatric assessment) en rekening gehouden dient te worden met de prioriteiten, overtuigingen en middelen van de oudere en andere relevante personen, zoals mantelzorgers, om een haalbaar plan te ontwikkelen dat rekening houdt met individueel relevante risicofactoren in de context van andere geriatrische syndromen en aandoeningen. Daarnaast is de aanbeveling gebaseerd op de uitkomsten van de verschillende reviews en (netwerk) meta-analyses om in de multifactoriële interventie de focus te leggen op de positief gescoorde valrisicofactoren.
Gezien de sterke bewijskracht ten aanzien van beweeginterventies, dient een multifactoriële interventie een beweeginterventie te bevatten met op functie- en balansgerichte componenten.
Voor patiënten met en matig valrisico wordt aanbevolen om een beweeginterventie met balans- en functiecomponenten aan te bieden en hen van mondelinge en schriftelijke informatie betreffende valpreventie te voorzien (kennisoverdracht). Daarnaast dient een persoons-omgevingsinterventie met behulp van een gevalideerd instrument overwogen te worden, mogelijkerwijs uitgevoerd door ergotherapeut.
Eindoordeel:
Sterke aanbeveling voor de inzet van een multifactoriële valpreventie interventie bij thuiswonende ouderen met een hoog valrisico; Sterke aanbeveling voor de inzet van beweeginterventies en kennisoverdracht bij thuiswonende ouderen met een matig valrisico.
Onderbouwing
Fall prevention interventions for community-dwelling individuals can be categorized into single, multiple, and multifactorial interventions. Since falls generally involve multiple factors simultaneously, a multifactorial prevention program has the highest chance of success. Many studies show that the risk of falling, meaning the number of fall incidents, can be effectively reduced in older adults by approximately 20% (Dautzenberg, 2021; Hopewell, 2018; Montero-Odasso, 2022; NICE, 2025). Research indicates that, in terms of fall prevention, most measures are only effective when implemented in combination with other measures. Single interventions are sometimes used and are generally aimed at optimizing mobility. Single interventions are preferably carried out only in low and medium risk patients. There is still no certainty regarding the optimal content of the multifactorial intervention, as it varies across different studies. This variability is reflected in practice, where regional differences exist, amongst others depending on the environment where the intervention is offered (primary versus secondary care). A significant barrier to the effectiveness of the (multifactorial) intervention is compliance.
The first Dutch guideline on fall prevention originates from 2017. This module presents an update of this guideline. In the past years, various (inter)national guidelines on fall prevention have been published, including the World Falls Guideline (Montero-Odasso, 2022) and the NICE guidelines (2025). Both the first version of the Dutch guideline, NICE guidelines and the World Falls Guideline concluded that multifactorial interventions should be applied to patients with a high risk of falls in the community setting. This module further describes the effectiveness of multifactorial interventions. To gain comprehensive insight into the effectiveness of multifactorial interventions and its optimal content, it is also important to examine the effectiveness of individual (single component) interventions.
Population: Older patients living in the community
Intervention: Multiple component or multifactorial interventions for fall prevention
Comparator: Usual care, no intervention or another (single-component) interventions (with no or limited effectiveness)
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Conclusions |
|
|
Usual care, no intervention or another (single-component) interventions (with no or limited effectiveness) |
Multiple component or multifactorial interventions for fall prevention |
||||
|
Falls risk (crucial)
|
Results from network meta-analysis: Based on 192 studies with 98,388 participants |
30 combinations of interventions (clinically relevant) in favour of intervention, 7 combinations of interventions (clinically relevant) in favour of usual care |
Low Due to serious inconsistency, due to serious imprecision1 |
Multiple component/multifactorial interventions for fall prevention may reduce the number of patients with fall incidents when compared with usual care in older patients living in the community.
(Dautzenberg, 2021; Marrocco, 2023; Bischoff-Ferrari, 2022; Altamirano, 2022; Arena, 2021; Daly, 2019; Ganz, 2022; Lamb, 2020)
|
|
|
Results from additional RCTs (multiple component interventions): Based on five studies with 2,961 participants RR 0.88 (95% CI 0.76 to 1.02) |
322 Per 1000 |
283 Per 1000 |
Low Due to serious risk of bias, due to serious imprecision2 |
||
|
Difference: 39 fewer per 1000 (CI 95% 77 fewer – 6 more) |
|||||
|
Results from additional RCTs (multifactorial interventions): Based on two studies with 11,975 participants RR 0.97 (95% CI 0.94 to 1.00) |
257 Per 1000 |
249 Per 1000 |
Moderate Due to serious risk of bias3 |
||
|
Difference: 8 fewer per 1000 (CI 95% 15 fewer – 0 fewer) |
|||||
|
Rate of falls (crucial) |
Results from network meta-analysis: Based on 115 studies |
23 combinations of interventions (clinically relevant) in favour of intervention, 2 combinations of interventions (clinically relevant) in favour of usual care |
Low Due to serious inconsistency, due to serious imprecision4 |
Multiple component/multifactorial interventions for fall prevention may reduce fall frequency when compared with usual care in older patients living in the community.
(Dautzenberg; 2021; Daly, 2019; Lamb, 2020) |
|
|
Results from additional RCTs (multiple component interventions): Based on 1 study with 148 participants |
The incidence rate ratio was 1.08 (95% CI 0.70 to 1.67), in favour of the patients who received usual care. |
Low Due to very serious imprecision5 |
|||
|
Results from additional RCTs (multifactorial interventions): Based on 1 study with 6,524 participants |
The adjusted rate ratio was 1.13 (95% CI 0.98 to 1.30), in favour of the patients who received usual care. |
Low Due to serious risk of bias, due to serious imprecision6 |
|||
|
Fall-related fractures (important) |
Results from network meta-analysis: Based on 46 studies with 43,811 participants |
18 combinations of interventions (clinically relevant) in favour of intervention, 7 combinations of interventions (clinically relevant) in favour of usual care |
Low Due to serious risk of bias, due to serious inconsistency7 |
Multifactorial/multicomponent interventions for fall prevention may reduce fall-related fractures when compared with usual care in older patients living in the community.
(Dautzenberg, 2021; Marocco, 2023; Ganz, 2022; Lamb, 2020) |
|
|
Results from additional RCTs (multiple component interventions): Based on 1 study with 1,757 participants |
The risk ratio was 2.32 (95% CI 1.11 to 4.84), in favour of the patients who received usual care. |
Moderate Due to serious risk of bias8 |
|||
|
Results from additional RCTs (multifactorial interventions): Based on 2 studies with 11,975 participants RR 1.07 (95% CI 0.78 to 1.47) |
36 Per 1000 |
39 Per 1000 |
Low Due to very serious imprecision9 |
||
|
Difference: 3 more per 1000 (CI 95% 8 fewer – 17 more) |
|||||
| 1. |
Inconsistency: serious. Due to conflicting results (downgraded 1 level) Imprecesion: serious. Due to overlap of the limits of the 95% confidence interval with the minimal clinically important difference. (downgraded 1 level) |
| 2. |
Risk of Bias: serious. Due to concerns regarding randomization and allocation procedure and lack of blinding (downgraded 1 level) Inconsistency: serious. Due to overlap of upper limits of the 95% confidence interval with the minimal clinically important difference. (downgraded 1 level) |
| 3. | Risk of Bias: serious. Due to concerns regarding randomization and allocation procedure and lack of blinding (downgraded 1 level) |
| 4. |
Inconsistency: serious. Due to conflicting results (downgraded 1 level) Imprecesion: serious. Due to overlap of the limits of the 95% confidence interval with the minimal clinically important difference. (downgraded 1 level) |
| 5. | Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference (downgraded 2 levels) |
| 6. |
Risk of Bias: serious. Due to lack of blinding (downgraded 1 level) Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference. (downgraded 1 level) |
| 7. |
Inconsistency: serious. Due to conflicting results (downgraded 1 level) Imprecision: serious. Due to overlap of the limits of the 95% confidence interval with the minimal clinically important difference. (downgraded 1 level) |
| 8. | Risk of Bias: serious. Due to lack of blinding (downgraded 1 level) |
| 9. | Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference (downgraded 2 levels) |
Description of studies
One network meta-analysis was included in the analysis of the literature (Dautzenberg, 2021). Additionally, seven RCTs were included that were published after the search date in Dautzenberg (2021).
Network meta-analysis
Important study characteristics and results of the network meta-analysis are summarized in table S1 in the supplementary content of Dautzenberg (2021). The assessment of the risk of bias is summarized in the risk of bias tables in supplementary table S2 of Dautzenberg (2021).
Dautzenberg (2021) performed a network meta-analysis to evaluate the effectiveness of single, multiple, and multifactorial intervention in preventing falls and fall-related fractures among older patients living in the community. A systematic search was conducted in MEDLINE, Embase, and the Cochrane Central Register of Controlled Trials for randomized controlled trials (RCTs) assessing the effectiveness of fall prevention interventions in community-dwelling adults aged 65 years and older, from the inception of each database until February 27, 2019. Inclusion criteria were (cluster) randomized and quasi-randomized controlled trials (RCTs) published in any language that examined the effectiveness of fall prevention Interventions In community-dwelling individuals aged 65 years and older. Studies on specific conditions (e.g. stroke, Parkinson’s disease) were excluded. In total, 220 RCTs (n = 104638 patients) were included. Ninety-nine studies examined a single intervention, 75 studies had multiple interventions and 46 studies had a multifactorial intervention. An overview of the Intervention that were studied In the IIed studies Is provided In Table 2. Dautzenberg (2021) categorized the multifactorial interventions into the 14 interventions components. In order to be able to carry out analyses, it was assumed that all participants received these multifactorial intervention components. A separate analysis was performed in which all multifactorial interventions were considered as one intervention type and compared with usual care.
In a quarter of the studies (24.5%), the sample size was less than 100 patients. In 17 studies (n = 7.7%), sample size was larger than 1000 participants. In the other 149 studies, sample size varied between 100 and 1000. In 68 studies (30.9%) patients were 65-74 years old, in 128 studies (58.2%) patients were aged 75-84 years old and in 11 studies, patients were aged 85 years or older. In 33 studies (15%), only patients with a history of fall in the last 12 months were included. However, in most studies the fall history of the included patients was mixed (n = 103, 46.8%). In 84 studies (38.2%), fall history was not reported. Most studies were executed in Europe (n = 87, 39.5%), Australia/New Zealand (n = 49, 22.3%) and North America (n = 48, 21.8%). About half of the studies were executed in a multicenter setting (n = 91, 41.4%), the other half were single-center studies (n = 129, 58.6%). The majority of studies had a parallel RCT design (n = 192, 87.3%), other studies had a cluster randomized design (n = 27, 12.3%), and one study had both designs. Outcomes that were reported included number of fallers, number of repeated fallers and number of fall-related fractures. More than half of the included studies had methodological weaknesses, such as inadequate allocation concealment and a lack of blinding. Outcomes of interest were the number of fallers, fall-related fractures and falls rate.
Table 2. Overview of interventions to prevent falls (adapted from Dautzenberg 2021).
|
Intervention component (abbreviation) |
Description |
|
Exercise (exerc) |
Including gait-, balance-, and functional training, strength/resistance training, flexibility, 3D training (e.g., Tai Chi, Qigong, dance and square stepping), general physical activity (e.g.,walking groups), endurance training, and other |
|
Medication (med) |
Vitamin D (cholecalciferol, alphacalcidol, sunlight, calcitriol, and ergocalciferol) |
|
Surgery (surg) |
E.g., pacemaker implantation, hip prosthesis, or cataract removal surgery |
|
Management of urinary incontinence (incont) |
Assisted toileting, bladder retraining, medication (e.g., tamsulosin, finasteride, botox injections), surgery (e.g., colposuspension surgery, sling procedures) |
|
Fluid or nutrition therapy (nutr) |
Changes in diet, provision of supplements, nutritional therapy, protein drinks |
|
Psychological interventions (psych) |
Cognitive behavioral therapy |
|
Environmental assessment and modifications (envir) |
Assessment and correction of home environment (e.g., flooring, home check, home safety devices, home visits by occupational therapist, home furnishings and adaptations) |
|
Assistive technology (assist) |
Provision of aids for personal protection (e.g., hip protector) or personal mobility (e.g., walking aidsa, comprehensive podiatry assessment and treatment, orthosis), aids for communication/information/signaling (e.g., vision assessment and correction with glasses, personal alarm systems, hearing aids) |
|
Social engagement (social) |
Social group activities (watching films, leisure reading, singing, conversation), community activities, peer support (from peers or caregivers), seminars on non–health-related topics of general interest to older adults |
|
Quality improvement strategies (qualt) |
- Patient-level quality improvement strategies: promotion of self-management, patient education, patient reminders, and motivational interviewing - Clinic-level or care team level quality improvement strategies: case management, team changes, electronic patient registry, facilitated relay of information to clinicians, audit and feedback, staff education, and clinician reminders - Health system-level quality improvement strategies: Interventions with positive or negative financial incentives directed at clinicians (e.g., linked to adherence to some process of care or achievement of some target outcome). This strategy also includes positive or negative financial incentives directed at patients or system-wide changes in reimbursement systems |
|
Management of orthostatic hypotension (hypot) |
Wearing elastic stockings, rising slowly, sleeping in a bed with head raised, pharmacological interventions |
|
Basic falls risk assessment (brisk) |
Cardiovascular assessment (vital signs, ECG, loop recorder, pacemaker interrogation), medication review (review, modification, withdrawal/deprescribing), fracture risk screening (bone mineral density) |
|
Whole-body vibration (vibr) |
Transferring vibration of any frequency to the human body |
|
Chiropractic care (chiro) |
Improving sensorimotor function associated with fall risk |
Additional RCTs
Important study characteristics and results of the RCTs that were published after Dautzenberg (2021), are summarized in Table 3. The assessment of the risk of bias is summarized in the risk of bias table.
Marocco (2024) performed a randomized controlled trial to evaluate the effects of a multicomponent intervention for the prevention of falls in older adults (≥65 years) at high risk of falling. For inclusion in the trial, patients needed to have at least five of the following fall risk factors: history of previous falls, fear of falling, polypharmacy (at least 5 medications), treatment with medications that increase the risk of falling, impaired mobility, altered vision, social isolation, major cerebro- or cardiovascular disease, difficulty extending the knees, mental confusion, creatinine clearance < 65 mL/min and arthritis and/or arthrosis. In addition, patients required to be aged ≥ 65 years, living at home regularly and signing the informed consent. In total, 117 GPs enrolled 1757 patients
Bischoff-Ferrari (2022) performed a randomized controlled trial to test the effects of vitamin D, omega-3s fatty acids, and a simple home exercise program (SHEP) on the incidence of falls among generally healthy older adults. The inclusion criteria were: the absence of major health events in the 5 years prior to enrolment, sufficient mobility to come to the study centers, and good cognitive function, with a Mini-Mental State Exam score of at least 24. In total, 2157 patients from seven sites in five European countries were included in the trial.
Ganz (2022) reported results of a randomized controlled trial to assess intervention effects on falls, fall-related fractures, fall injuries leading to hospital admission, and fall injuries leading to medical attention. Individuals who were at risk for fall injuries and who were at least 70 years of age were eligible for trial inclusion. In total, 86 primary care practices across 10 health systems included 5451 community-dwelling older adults.
Altamirano (2022) performed a randomized controlled trial to determine the effectiveness of a preventive program in reducing falls in older adults. Community-dwelling seniors aged 65 years and older with an increased risk of physical falls. Increased risk of falls was defined as one or more falls in the past 12 months, low physical function, subjective or objective balance deficits or fear of falling. Patients were included if they had at least one of the criteria. In total, 378 patients were included in 33 general practices.
Arena (2021) performed a randomized controlled trial to examine the effects of the HOP-UP-PT program in older adults at risk for falls. The inclusion criteria were: age greater than or equal to 65 years, SCC staff identified them as ‘at-risk’ for decline in community-dwelling status due to physical, social, economic, or community-related barriers, and willing to participate in the HOP-UP-PT program. In total, 144 participants were enrolled from six senior community centers (SCC).
Lamb (2020) performed a randomized controlled trial to assess the clinical effectiveness and cost-effectiveness of a multifactorial exercise program in community-dwelling older people with an increased risk of falling. General practices contacted community-dwelling persons 70 years of age or older who were living in their own homes. In total, 63 general practices included 9803 patients.
Daly (2020) performed a randomized controlled trial to investigate whether a multifaceted osteoporosis prevention program could improve bone mineral density (BMD) and functional muscle performance in older adults at increased risk for fracture. The inclusion criteria were: community-dwelling, independently living men and women, aged ≥60 years, residing in the Western suburbs and surrounding regions of Melbourne. In total, 162 participants were included in the trial.
Table 3. Characteristics of included randomized controlled trials
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Individual studies |
||||||
|
Marrocco, 2023 |
N at baseline Intervention: 875 Control: 882
Age (mean, SD) Intervention: 77.6 years (±7.3) Control: 77.4 years (±7.2)
Sex (male/ female) Intervention: 312/563 Control: 329/553 |
Intervention: Multicomponent (medical review of treatments, recommendation of daily training sessions with gentle physical exercise, inspection of homes, followed by recommendations of home modifications)
Control: Same set of dietary recommendations and Fall Diary. |
12 months |
Fall risk Mean number of falls – frequency of falls in the last 12 months I: 0.94 (SD ±2.20) C: 1.27 (SD ±2.70) MD -0.33 (95% CI -0.56 to -0.10)
Patients falling at least once I: 158 (26.2%) C: 179 (28.8%) RR 0.89 (95% CI 0.73 to 1.08)
Fracture consequent to fall (n, %) I: 23 (3.8%) C: 10 (1.6%) OR 2.39 (95% CI 1.12 to 5.06) RR 2.32 (95% CI 1.11 to 4.84) |
Funding: no external funding.
Conflicts of interest: no conflict of interest. |
Some concerns |
|
Bischoff-Ferrari, 2022 |
N at baseline Intervention: 264 Control: 270
Age (mean, SD) Intervention: 74.8 ± 4.5 years Control: 75.2 ± 4.9 years
Sex (female/male) Intervention: 165/99 Control: 165/105 |
Intervention: Multicomponent (vitamin D + omega-3 + strength exercise)
Control: placebo |
3 years |
Fall risk Participants who sustained at least 1 fall over 3 years I: 161 (61.0%) C: 164 (60.7%) Crude incidence rate ratio of falls: 0.91 (95% CI 0.73 to 1.13)
|
Funding: funded by the Seventh Research Framework Program of the European Commission, the University of Zurich, DNP, Roche, NESTEC, Pfizer, and Streuli. The funding organizations had no role in the design and conduct of the study.
Conflicts of interest: NR |
LOW |
|
Ganz, 2022 |
N at baseline Intervention: 2802 Control: 2649
Age (mean, SD) Intervention: 79.8 ± 6.5 years Control: 79.5 ± 6.0 years
Sex (female) Intervention: 1752 (62.5%) Control: 1629 (61.5%) |
Intervention: multifactorial, patient-centered intervention
Control: usual care (including information) |
24 months |
Fall risk One or more falls (n, %) I: 1833 (65.4%) C: 1798 (67.9%) Adjusted Rate Ratio 0.99 (95% CI 0.91 to 1.08) RR 0.96 (95% CI 0.93 to 1.00)
Two or more falls (n, %) I: 1242 (44.3%) C: 1220 (46.1%) Adjusted Rate Ratio 0.97 (95% CI 0.91 to 1.04) RR 0.96 (95% CI 0.91 to 1.02)
Fall-related fractures Self-reported I: 287 (10.2%) C: 296 (11.2%) Adjusted Rate Ratio 0.94 (95% CI 0.79 to 1.12) RR 0.92 (95% CI 0.79 to 1.07)
Adjudicated I: 184 (6.6%) C: 203 (7.7%) Adjusted Rate Ratio 0.87 (95% CI 0.72 to 1.05) RR 0.86 (95% CI 0.71 to 1.04) |
Funding: multiple grants, among which NIH, NCATS (the organizations had no role in the design or conduct of the study)
Conflicts of interest: Dr. Magaziner reports board membership on the Fragility Fracture Network and Own the Bone Multi-disciplinairy Advisory Board of the American Orthopedic Association. |
HIGH |
|
Altamirano, 2022 |
N at baseline Intervention: 222 Control: 156
Age (mean, SD) Intervention: 78 ± 6 years Control: 78 ± 6 years
Sex (male/female) Intervention: 50/172 Control: 43/113 |
Intervention: patient-level intervention program (supervised physical training program (1hr/wk))
Control: usual care |
12 months |
Fall risk Number of people who fell I: 73 (32.8%) C: 70 (44.9%) OR 0.52 (95% CI 0.29 to 0.91) RR 0.73 (95% CI 0.57 to 0.95) |
Funding: NR
Conflicts of interest: NR |
HIGH |
|
Arena, 2021 |
N at baseline Intervention: 72 Control: 72
Age (mean, SD) Intervention: 76.6 ± 7.0 years Control: 77.2 ± 8.2 years
Sex (male/female) Intervention: 15/57 Control: 19/53 |
Intervention: HOP-UP-OT exercise program (with evidence that it reduces falls), motivational interviewing, home and environmental modification recommendations
Control: only assessments (instructed to continue normal level of activity) |
7 months |
Falls risk Patients reported falling since baseline I: 13.0% C: 26.8% RR 0.47 (95% CI 0.23 to 0.98) |
Funding: funded by a 2018 Michigan Health Endowment Fund-Healthy Aging Award. The funder had no role in the study design, data collection, analysis, interpretation of data, or writing of the manuscript.
Conflicts of interest: potential financial conflict for SA and CW (co-principals of HOP-UP-PT, LLC). |
LOW |
|
Lamb, 2020 |
N at baseline Intervention: 3301 Control 1: 3279 Control 2: 3223
Age (mean, SD) Intervention: 78 ± 5.7 years Control 1: 78 ± 5.7 years Control 2: 78 ± 5.7 years
Sex (female) Intervention: 1760 Control 1: 1724 Control 2: 1666 |
Intervention: advice by mail, screening, and targeted multifactorial fall prevention
Control 1: advice by mail, screening, and targeted exercise
Control 2: advice by mail |
18 months |
Number of fractures I: 173 C1: 152 C2: 133 RR I vs C2: 1.27 (95% CI 1.02 to 1.58) RR C1 vs C2: 1.12 (95% CI 0.89 to 1.41)
Number of fractures / 100 person-yr I: 3.50 C1: 3.06 C2: 2.76 Adjusted Rate Ratio I vs. C2: 1.30 (95% CI 0.99 to 1.62) Adjusted Rate Ratio C1 vs. C2: 1.20 (95% CI 0.91 to 1.59)
Fall risk Number of participants who fell I: 1301 C1: 1277 C2: 1276 RR I vs C2: 1.00 (95% CI 0.94 to 1.06) RR C1 vs C2: 0.98 (95% CI 0.93 to 1.04)
Rate of falls Number of falls per 100 person-years over 18 months I: 127.2 C1: 104.4 C2: 105.6 Adjusted Rate Ratio I vs. C2: 1.13 (95% CI 0.98 to 1.30) Adjusted Rate Ratio C1 vs. C2: 0.99 (95% CI 0.86 to 1.14) |
Funding: grant from the National Institute of Health Research Technology Assessment Programme.
Conflicts of interest: NR |
Some concerns |
|
Daly, 2019 |
N at baseline Intervention: 77 Control: 71
Age (mean, SD) Total: 67.4 (range 60-86) years
Sex (female) Total: 73% |
Intervention: Osteo-cise: multicomponent exercise program specific to osteoporosis and fall prevention (exercise program)
Control: usual care |
18 months |
Fall risk Number of participants who reported one or more falls I: 37 (45.7%) RR 1.07 (95% CI 0.57 to 2.00)
Rate of falls Number of falls per 100 person years over 18 months I: 59 (0.48) C: 53 (0.45) Incidence rate ratio 1.08 (95% CI 0.70 to 1.67) |
Funding: grant from JO & JR Wicking Trust, under auspices of Osteoporosis Australia and the Australian and New Zealand Bone and Mineral Society. RMD supported by a National Health and Medical Research Council Career Development Award.
Conflicts of interest: NR |
LOW |
*For further details, see risk of bias table in the appendix
Results
Results from the network meta-analysis and the RCTs that were additionally included could not be pooled due to the type of the analysis that was executed in Dautzenberg (2021). Therefore, results are presented separately for each outcome measure. Results from Dautzenberg (2021) are presented in figure 1, figure 2, and figure 3. Results from the additional RCTs were pooled and presented in table 4, table 5 and table 6. Results from Dautzenberg (2021) and the additional RCTs were combined in the Summary of Findings table.
Falls risk (number of people who fell once or more)
Results from network meta-analysis
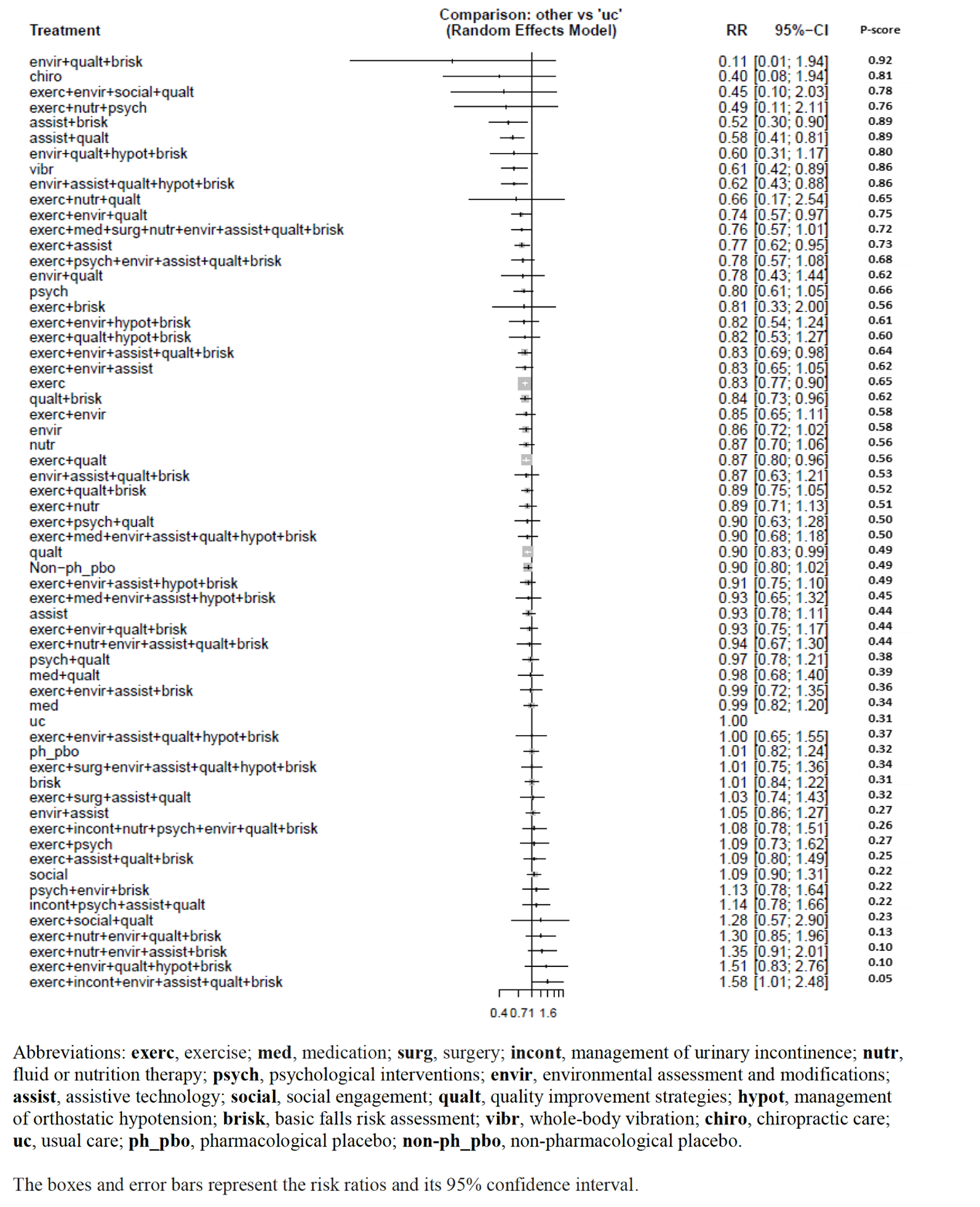
Dautzenberg (2021) included a total of 192 studies (with n = 98388 participants) that reported the number of fallers for the comparison between 63 different interventions with usual care (Figure 1). Figure 1 reports the RR for every (combination of) intervention(s) versus usual care. For 34 (combinations of) interventions, a clinically relevant difference was found, in favor of the patients who received the interventions. Six of the 30 clinically relevant interventions were single interventions, and 26 were multiple component interventions. For seven combinations of interventions, a clinically relevant difference was found, in favor of the patients who received usual care.
Dautzenberg (2021) performed an additional analysis in which all multifactorial interventions were considered as one intervention type. This analysis resulted in a risk ratio of 0.95 (95%CI 0.89 to 1.01) (188 studies; N=91,137).
Figure 1. Number of fallers (adapted from Dautzenberg 2021).
Results from additional RCTs
Of the additional RCTs that were included in the summary of the literature, five reported the number of patients with fall incidents comparing multicomponent interventions (n=1510) with usual care (n=1451) (Altamirano, 2022; Arena, 2021; Bischoff-Ferrari, 2022; Daly, 2019; Marrocco, 2023). The pooled risk ratio was 0.88 (95% CI 0.76 to 1.02), in favor of the patients who received multicomponent interventions (table 4, figure 2). This difference is considered clinically relevant.
Of the additional RCTs that were included in the summary of the literature, two reported the number of patients with fall incidents comparing multifactorial interventions (n=6103) with usual care (n=5872) (Ganz, 2022; Lamb, 2020). The pooled risk ratio was 0.97 (95% CI 0.94 to 1.00), in favor of the patients who received multifactorial interventions (table 4). This difference is not considered clinically relevant.
Table 4. Number of patients with fall incidents
|
Number of patients with fall incidents |
Intervention |
Control |
Effect measure |
|
Multiple component interventions |
|||
|
Marrocco, 2023 |
158 (26.2%) |
179 (28.8%) |
RR 0.89 (95% CI 0.73 to 1.08) |
|
Bischoff-Ferrari, 2022 |
161 (61.0%) |
164 (60.7%) |
RR 1.00 (95% CI 0.88 to 1.15) |
|
Altamirano, 2022 |
73 (32.8%) |
70 (44.9%) |
RR 0.73 (95% CI 0.57 to 0.95) |
|
Arena, 2021 |
9 (13.0%) |
19 (26.8%) |
RR 0.47 (95% CI 0.23 to 0.98) |
|
Daly, 2019 |
37 (45.7%) |
35 (43.2%) |
RR 1.07 (95% CI 0.57 to 2.00) |
|
Pooled effect |
RR 0.88 (95% CI 0.76 to 1.02) |
||
|
Multifactorial interventions |
|||
|
Ganz, 2022 |
1833 (65.4%) |
1798 (67.9%) |
RR 0.96 (95% CI 0.93 to 1.00) |
|
Lamb, 2020 |
1301 (39.4%) |
1276 (39.6%) |
RR 1.00 (95% CI 0.94 to 1.06) |
|
Pooled effect |
RR 0.97 (95% CI 0.94 to 1.00) |
||
Rate of falls (falls per unit of person time)
Results from network meta-analysis
Dautzenberg (2021) included a total of 115 studies that reported the falls rate (defined as number of falls per person-year of follow-up) (figure 2). Figure 3 reports the RR for every (combination of) intervention(s) versus usual care. For 23 (combinations of) interventions, a clinically relevant difference was found, in favor of the patients who received the interventions. Five of the 23 clinically relevant interventions were single interventions, and eighteen were multiple component interventions.
For two combinations of interventions, a clinically relevant difference was found, in favor of the patients who received usual care.
A risk ratio of 0.87 (95%CI 0.80 to 0.95) was found for multifactorial interventions, compared to usual care (111 studies; N=53,923). This indicates that the difference between multifactorial interventions and usual care was clinically relevant, in favor of the patients who received multifactorial interventions.
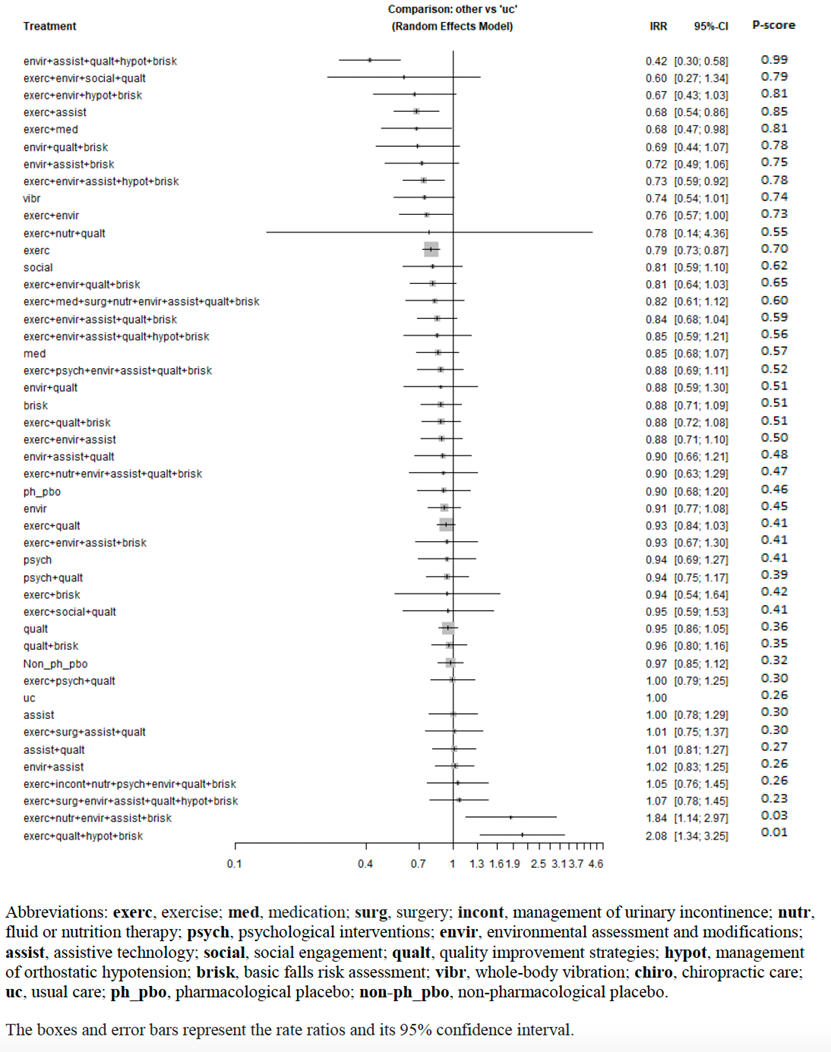
Figure 2. Falls rate (adapted from Dautzenberg 2021).
Results from additional RCTs
Of the additional RCTs that were included in the summary of the literature, one reported fall frequency comparing multicomponent interventions (n=77) with usual care (n=71) (Daly, 2019). The incidence rate ratio was 1.08 (95% CI 0.70 to 1.67), in favor of the patients who received usual care (table 5). This difference is not considered clinically relevant.
Of the additional RCTs that were included in the summary of the literature, one reported fall frequency comparing multifactorial interventions (n=3301) with usual care (n=3223) (Lamb, 2020). The adjusted rate ratio was 1.13 (95% CI 0.98 to 1.30), in favour of the patients who received usual care (table 5). This difference is not considered clinically relevant.
Table 5. Fall frequency (number of falls per 100 person years over 18 months)
|
Fall frequency |
Intervention |
Control |
Effect measure |
|
Multiple component interventions |
|||
|
Daly, 2019 |
59 (0.48) |
53 (0.45) |
Incidence rate ratio 1.08 (95% CI 0.70 to 1.67) |
|
Multifactorial interventions |
|||
|
Lamb, 2020 |
127.2 |
105.6 |
Adjusted rate ratio 1.13 (95% CI 0.98 to 1.30) |
Fall-related fractures
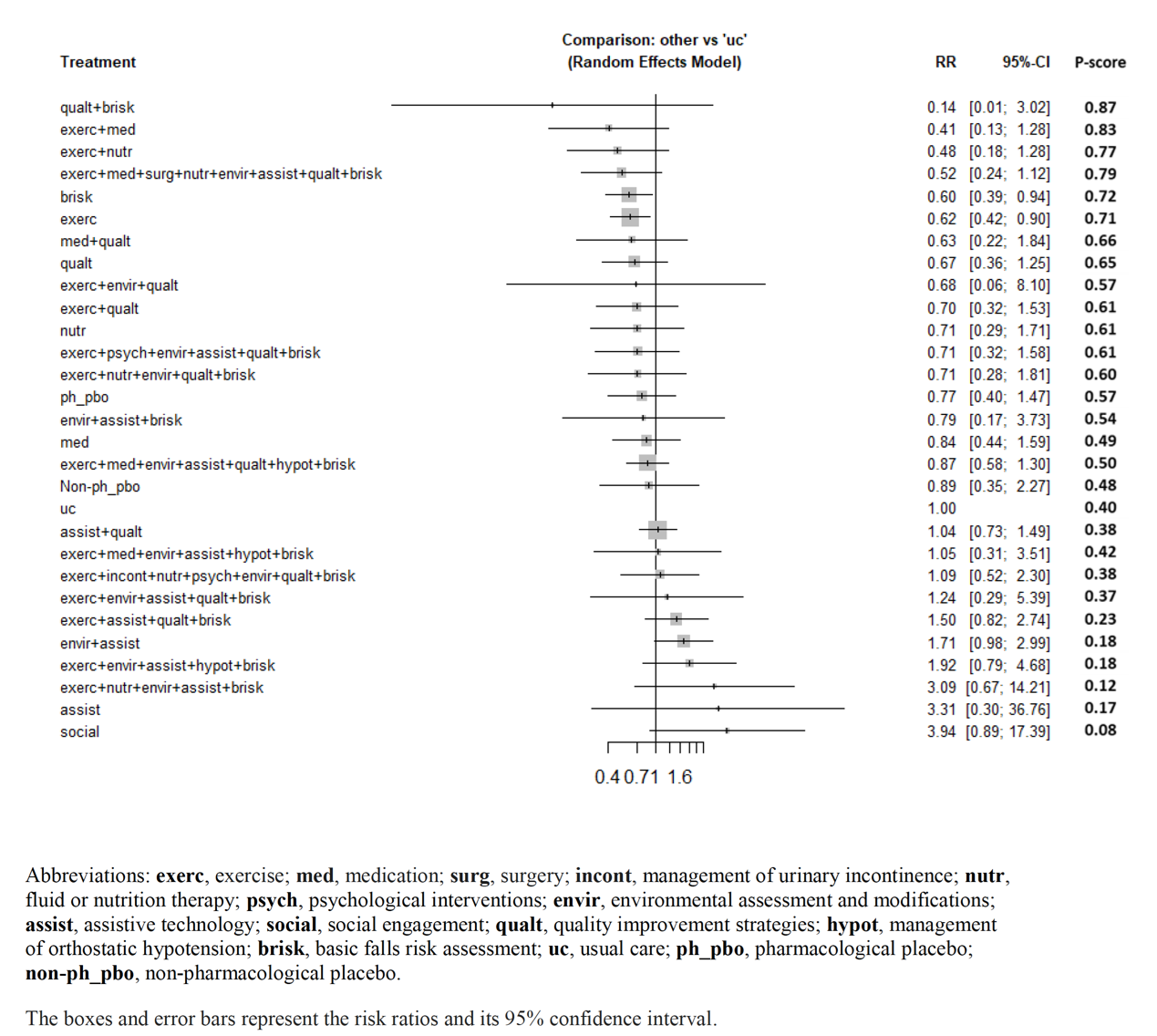
Dautzenberg (2021) included a total of 46 studies (with 43,811 participants) that reported the number of fall-related fractures for the comparison between 27 different interventions with usual care (figure 3). Figure 3 reports the RR for every (combination of) intervention(s) versus usual care. For eighteen (combinations of) interventions, a clinically relevant difference was found, in favour of the patients who received the interventions. Seven of the eighteen clinically relevant interventions were single interventions, and eleven were multiple component interventions.
For seven (combinations of) interventions, a clinically relevant difference was found, in favour of the patients who received usual care. Two of the seven clinically relevant interventions were single interventions, and five were multiple component interventions.
Figure 3. Number of fractures (adapted from Dautzenberg 2021).
Results from additional RCTs
Of the additional RCTs that were included in the summary of the literature, one reported fall frequency comparing multicomponent interventions (n=875) with usual care (n=882) (Marrocco, 2023). The risk ratio was 2.32 (95% CI 1.11 to 4.84), in favor of the patients who received usual care (table 6). This difference is considered clinically relevant.
Of the additional RCTs that were included in the summary of the literature, one reported fall frequency comparing multifactorial interventions (n=6103) with usual care (n=5872) (Ganz, 2022; Lamb, 2020). The pooled risk ratio was 1.07 (95% CI 0.78 to 1.47), in favor of the patients who received usual care (table 6). This difference is not considered clinically relevant.
Table 6. Fall-related fractures
|
Fall-related fractures |
Intervention |
Control |
Effect measure |
|
Multiple component interventions |
|||
|
Marrocco, 2023 |
23 (3.8%) |
10 (1.6%) |
RR 2.32 (95% CI 1.11 to 4.84) |
|
Multifactorial interventions |
|||
|
Ganz, 2022 |
287 (10.2%) |
296 (11.2%) |
RR 0.92 (95% CI 0.79 to 1.07) |
|
Lamb, 2020 |
173 (5.2%) |
133 (4.1%) |
RR 1.27 (95% CI 1.02 to 1.58) |
|
Pooled effect |
RR 1.07 (95% CI 0.78 to 1.47) |
||
A systematic review of the literature was performed to answer the following question: What is the effectiveness of multiple component and multifactorial interventions for fall prevention, compared to no intervention or another (single-component) intervention for older persons in the community setting?
Table 1. PICO
|
Patients |
Older patients living in the community |
|
Intervention |
Multiple component and multifactorial interventions for fall prevention |
|
Control |
Usual care, no intervention or another (single-component) intervention |
|
Outcomes |
|
|
Other selection criteria |
Study design:
|
Relevant outcome measures
A priori, the guideline panel defined the outcomes as follows:
- Falls risk: The risk of being a faller; the number of people who fell once or more (fallers) in the intervention and control groups
- Rate of falls: falls per unit of person time (such as bed days), presented as the rate ratio
- Fall related fracture risk: the risk of fall related fractures in the intervention group, compared to the control group.
The following definitions were used for the different intervention types, similar to the definitions used in Hopewell (2018)
- Multiple component interventions: all participants receiving the same combination of interventions
- Multifactorial interventions: the combination of interventions that is delivered, is tailored towards each individual participant.
The guideline panel considered falls risk and rate of falls as a critical outcome measure for decision making; and fall related fracture risk as an important outcome measure for decision making.
The guideline panel defined a difference of 10% as a minimal clinically (patient) important difference, RR ≤ 0.90 and RR ≥ 1.10 for the outcomes falls risk, rate of falls and fall related fracture risk.
Search and select (Methods)
To answer this question, the Cochrane systematic review from Hopewell (2018) was used as a basis for this literature analysis. In Hopewell (2018), the Cochrane Bone, Joint and Muscle trauma group Register, the Cochrane Central register of Controlled trials (CENTRAL), OVID/MEDLINE, Embase and CINAHL were searched with relevant search terms, until 12-06-2017. We performed an update of this Cochrane Systematic review with similar search terms as used in Hopewell (2018). The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms for articles published between 12-06-2017 until 09-08-2024. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 6510 hits. Studies were selected based on the criteria described in Table 1. For this module, only studies on older persons living in the community were included. Titles and abstracts were screened using the Asreview software version 1.6.2. The settings TF-IDF and Naïve bayes were used. Hopewell (2018) was used as prior knowledge for inclusion. Park (2021), Borreli (2021), Verrusio (2018) were used as prior knowledge for exclusions.
The first 10% of references were screened by the working group and the guideline methodologist. The remaining articles were subsequently screened by the guideline methodologist, using the following stopping rule: stop after 200 subsequent exclusions.
One network meta-analyses was identified with the literature search (Dautzenberg, 2021) and included in the summary of literature. Randomized controlled trials that were published after the search date from Datuzenberg (2021), February 27, 2019, and meeting the inclusion criteria (Table 1) were also included in the summary of literature.
Initially, 42 studies were selected based on title and abstract screening. After reading the full text, 34 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and one network meta-analysis (Dautzenberg, 2021) and seven additional RCT’s (published after the search date from Dautzenberg, 2021) were included.
- Altamirano, 2022: EFFECTIVENESS OF A PREVENTIVE PROGRAM FOR THE REDUCTION OF FALLS IN OLDER ADULTS
- Arena SK, Wilson CM, Boright L, Peterson E. Impact of the HOP-UP-PT program on older adults at risk to fall: a randomized controlled trial. BMC Geriatr. 2021 Oct 1;21(1):520. Doi: 10.1186/s12877-021-02450-0. PMID: 34598692; PMCID: PMC8485496.
- Bischoff-Ferrari HA, Freystätter G, Vellas B, Dawson-Hughes B, Kressig RW, Kanis JA, Willett WC, Manson JE, Rizzoli R, Theiler R, Hofbauer LC, Armbrecht G, da Silva JAP, Blauth M, de Godoi Rezende Costa Molino C, Lang W, Siebert U, Egli A, Orav EJ, Wieczorek M; DO-HEALTH Research Group. Effects of vitamin D, omega-3 fatty acids, and a simple home strength exercise program on fall prevention: the DO-HEALTH randomized clinical trial. Am J Clin Nutr. 2022 May 1;115(5):1311-1321. Doi: 10.1093/ajcn/nqac022. PMID: 35136915.
- Daly RM, Gianoudis J, Kersh ME, Bailey CA, Ebeling PR, Krug R, Nowson CA, Hill K, Sanders KM. Effects of a 12-Month Supervised, Community-Based, Multimodal Exercise Program Followed by a 6-Month Research-to-Practice Transition on Bone Mineral Density, Trabecular Microarchitecture, and Physical Function in Older Adults: A Randomized Controlled Trial. J Bone Miner Res. 2020 Mar;35(3):419-429. Doi: 10.1002/jbmr.3865. Epub 2019 Oct 24. PMID: 31498937.
- Dautzenberg L, Beglinger S, Tsokani S, Zevgiti S, Raijmann RCMA, Rodondi N, Scholten RJPM, Rutjes AWS, Di Nisio M, Emmelot-Vonk M, Tricco AC, Straus SE, Thomas S, Bretagne L, Knol W, Mavridis D, Koek HL. Interventions for preventing falls and fall-related fractures in community-dwelling older adults: A systematic review and network meta-analysis. J Am Geriatr Soc. 2021 Oct;69(10):2973-2984. Doi: 10.1111/jgs.17375. Epub 2021 Jul 28. PMID: 34318929; PMCID: PMC8518387.
- Ganz DA, Yuan AH, Greene EJ, Latham NK, Araujo K, Siu AL, Magaziner J, Gurwitz JH, Wu AW, Alexander NB, Wallace RB, Greenspan SL, Rich J, Volpi E, Waring SC, Dykes PC, Ko F, Resnick NM, McMahon SK, Basaria S, Wang R, Lu C, Esserman D, Dziura J, Miller ME, Travison TG, Peduzzi P, Bhasin S, Reuben DB, Gill TM. Effect of the STRIDE fall injury prevention intervention on falls, fall injuries, and health-related quality of life. J Am Geriatr Soc. 2022 Nov;70(11):3221-3229. Doi: 10.1111/jgs.17964. Epub 2022 Aug 6. PMID: 35932279; PMCID: PMC9669115.
- Hopewell S, Adedire O, Copsey BJ, Boniface GJ, Sherrington C, Clemson L, Close JC, Lamb SE. Multifactorial and multiple component interventions for preventing falls in older people living in the community. Cochrane Database Syst Rev. 2018 Jul 23;7(7):CD012221. Doi: 10.1002/14651858.CD012221.pub2. PMID: 30035305; PMCID: PMC6513234.
- Inspectie Gezondheidszorg en Jeugd (IGJ). Ketenaanpak valpreventie: stimuleren en versterken [Internet]. Den Haag: IGJ; 2024 Aug 22. Available from: https://www.igj.nl/publicaties/publicaties/2024/08/22/ketenaanpak-valpreventie-stimuleren-en-versterken
- Lamb SE, Bruce J, Hossain A, Ji C, Longo R, Lall R, Bojke C, Hulme C, Withers E, Finnegan S, Sheridan R, Willett K, Underwood M; Prevention of Fall Injury Trial Study Group. Screening and Intervention to Prevent Falls and Fractures in Older People. N Engl J Med. 2020 Nov 5;383(19):1848-1859. Doi: 10.1056/NEJMoa2001500. PMID: 33211928.
- Marrocco W, Galli A, Scotti S, Calabrese N, Misericordia P, Dalle Vedove A, Marrocco G, D’Ingianna AP, Pizzini A, Fini M, Tomino C, Bonassi S, On Behalf Of The F I M M G Research Premio Group. A Multicomponent Primary-Care Intervention for Preventing Falls in Older Adults Living in the Community: The PREMIO Study. J Clin Med. 2023 Nov 16;12(22):7134. Doi: 10.3390/jcm12227134. PMID: 38002746; PMCID: PMC10672084.
- Montero-Odasso M, van der Velde N, Martin FC, Petrovic M, Tan MP, Ryg J, Aguilar-Navarro S, Alexander NB, Becker C, Blain H, Bourke R, Cameron ID, Camicioli R, Clemson L, Close J, Delbaere K, Duan L, Duque G, Dyer SM, Freiberger E, Ganz DA, Gómez F, Hausdorff JM, Hogan DB, Hunter SMW, Jauregui JR, Kamkar N, Kenny RA, Lamb SE, Latham NK, Lipsitz LA, Liu-Ambrose T, Logan P, Lord SR, Mallet L, Marsh D, Milisen K, Moctezuma-Gallegos R, Morris ME, Nieuwboer A, Perracini MR, Pieruccini-Faria F, Pighills A, Said C, Sejdic E, Sherrington C, Skelton DA, Dsouza S, Speechley M, Stark S, Todd C, Troen BR, van der Cammen T, Verghese J, Vlaeyen E, Watt JA, Masud T; Task Force on Global Guidelines for Falls in Older Adults. World guidelines for falls prevention and management for older adults: a global initiative. Age Ageing. 2022 Sep 2;51(9):afac205. Doi: 10.1093/ageing/afac205. Erratum in: Age Ageing. 2023 Sep 1;52(9):afad188. Doi: 10.1093/ageing/afad188. Erratum in: Age Ageing. 2023 Oct 2;52(10):afad199. Doi: 10.1093/ageing/afad199. PMID: 36178003; PMCID: PMC9523684.
- National Institute for Health Care Excellence (NICE). Falls: assessment and prevention in older people and in people 50 and over at higher risk: NG249. London, NICE; 2025 Apr 29. Available from: https://www.nice.org.uk/guidance/ng249
- Tinetti ME, Gordon C, Sogolow E, Lapin P, Bradley EH. Fall-risk evaluation and management: challenges in adopting geriatric care practices. Gerontologist. 2006 Dec;46(6):717-25. Doi: 10.1093/geront/46.6.717. PMID: 17169927.
- Van der Velde N, Seppala LJ, Herrero AC, Annweiler C, Jónsdóttir AB, Blain H, Dionyssiotis Y, Duque S, Frith J, Francis BN, Grodzicki T, Hay A, Hernández-Sánchez LA, Jaatinen R, Kadane CJ, Kolsek M, Kostka T, McGarrigle L, Perkisas S, Pertinatsch C, Pettersson B, Reginster JY, Ruggiero C, Sahota O, Sibille FX, Sokhal BS, Skelton DA, Spildooren J, Stanmore E, Vankova H, Vlaeyen E, Ozturk Y, Yilmaz O, Todd C, Trevisan C, Willems H, Montero-Odasso M, Martin FC, Ryg J, Masud T; European Geriatric Medicine Society Special Interest Group on Falls, Fractures. Falls prevention in community-dwelling older adults and implementation of world falls guidelines: a call for action across Europe by the European Geriatric Medicine Society Special Interest Group on Falls and Fractures. Eur Geriatr Med. 2025 Jun 12. Doi: 10.1007/s41999-025-01206-y. Epub ahead of print. PMID: 40506658.
- World Health Organization (2021) Step safely: strategies for preventing and managing falls across the life-course. License: CC BY-NC-SA 3.0 IGO. World Health Organization, Geneva. https://www.who.int/publications/i/item/978924002191-4
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-04-2026
Beoordeeld op geldigheid : 30-04-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinair cluster ingesteld. Het cluster Duizeligheid, Vallen en Syncope bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden geven hun expertise, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Prof. dr. T.D. (Tjasse) Bruintjes, voorzitter cluster Duizeligheid, Vallen en Syncope, NVKNO, KNO-arts, Gelre Ziekenhuizen
- Prof. dr. N. (Nathalie) van der Velde, NVKG, klinisch geriater, Amsterdam UMC
- Dr. R.B. (Roeland) van Leeuwen, NVN, neuroloog, Gelre Ziekenhuizen
- Dr. J.H.W. (Joost) Rutten, NIV, internist, Radboud UMC
- Drs. S. (Simon) Geerse, NVKNO, KNO-arts, Treant Ziekenhuizen
- Dr. W.P.A. (Willem) Kelders, NVKNO, KNO-arts, Franciscus Gasthuis & Vlietland
- Drs. J.O. (Judella) Daal, NVKG, klinisch-geriater, Dijklander Ziekenhuis
Clusterexpertisegroep
- Drs. C.M. (Margreet) Aalten, NVKG klinisch geriater, St. Jansdal Ziekenhuis
- Ir. R.M. (Renske) Hoeben, NVKF, Klinisch Fysicus, Bernhoven
- Drs. B.S. (Birgit) Jacobs, NVZA, ziekenhuisapotheker, Catharina Ziekenhuis
- Dr. E.C.A. (Evert) Kaal, NVN, neuroloog, Maasstad Ziekhuis
- Dr. W.F. (Linde) Kok, Verenso, specialist ouderengeneeskunde bij GeriCall
- Dr. E.P. (Eveline) van Poelgeest, NIV, NVKG, internist-ouderengeneeskunde, Amsterdam UMC
- Dr. V.A. (Vincent) van Vugt, NHG, huisarts, Amsterdam UMC
- B.J.F.M. (Bart) Zwaneveld, KNGF, orofaciaal en manueel therapeut
Met ondersteuning van
- Dr. R. Zwarts - van de Putte, adviseur, Kennisinstituut van Medisch Specialisten
- Drs. D.G. Ossendrijver, adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Cluster stuurgroepleden
Tabel 1 Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Tjasse Bruintjes*
|
- KNO-arts (vrijgevestigd) Gelre ziekenhuizen Apeldoorn (0,8 fte) |
- lid beroepsgenoot Regionaal Tuchtcollege voor de Gezondheidszorg Zwolle (onkostenvergoeding) |
Geen |
Geen |
In 2022 toegekende ZonMW-subsidie voor de zgn. Predmentrial |
Geen |
Geen |
07-01-2021
18-05-2025 herbevestigd |
Geen |
|
Nathalie Van der Velde |
Staflid en hoogleraar onderafdeling Geriatrie Amsterdam UMC, lokatie AMC |
Onbetaald: |
Geen |
Geen |
Nee; alleen subsidies van onafhankelijke subsidieverstrekkers (NWO, ZonMW, Amsterdams Universiteitsfonds) |
Geen |
Geen |
07-10-2020
06-06-2025 herbevestigd |
Geen |
|
Roeland Van Leeuwen |
Neuroloog, Gelre ziekenhuizen Apeldoorn |
Lid Scheidsgerecht Gezondheidszorg. Betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
11-10-2020
18-05-2025 herbevestigd |
Geen |
|
Joost Rutten |
Internist-Vasculair Geneeskunde 0.9 FTE/Radboudumc, Nijmegen |
Consultant op projectbasis voor Volw International - project ontwikkeling screeningstool ter opsporing patiënten met lipodystrofie |
Geen |
Geen |
Principle Investigator Radboudumc CALM DIEM en CALM START studies, sponsor Vascular Dynamics (studies naar effect van specifiek type carotisstent ter verlaging van de bloeddruk) |
Geen |
Geen |
21-01-2021
23-05-2025 herbevestigd |
|
|
Simon Geerse |
KNO-arts (vrijgevestigd) Treant ziekenhuizen (0.8 fte) |
Voorzitter kerngroep Vestibulologie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
21-01-2021
26-5-2025 herbevestigd |
Geen |
|
Willem Kelders |
- KNO-arts (vrijgevestigd) Franciscus Gasthuis en Vlietland Rotterdam (0,8 fte) |
- lid kerngroep vestibulogie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
10-01-2021
17-5-2025 herbevestigd |
Geen |
|
Judella Daal |
NVKG als vereniging |
Voorzitter SIG Valpreventie NVKG/Landelijke netwerk valklinieken |
Geen |
Geen |
Geen |
Geen |
Geen |
10-04-2025
21-5-2025 herbevestigd |
Geen |
Betrokken cluster expertisegroepleden
Tabel 2 Gemelde (neven)functies en belangen expertisegroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Margreet Aalten |
Klinisch geriater Ziekenhuis St. Jansdal Harderwijk 0,6 FTE |
Lid accreditatie beoordelingscommissie NVKG onbezoldigd. |
Geen |
Geen |
Geen |
Geen |
Geen |
13-10-2021
20-05-2025 herbevestigd |
Geen |
|
Evert Kaal |
Neuroloog Maasstad Ziekenhuis 0,8 FTE |
Voorzitter Werkgroep voor Syncope en Autonome Aandoeningen, onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-10-2021
18-06-2025 herbevestigd |
Geen |
|
Linde Kok |
Specialist Ouderengeneeskunde bij GeriCall, momenteel in de 1e lijn |
Geen |
Geen |
Geen relaties met belangen |
Geen |
Geen |
Geen |
10-10-2023
16-5-2025 herbevestigd |
Geen |
|
Eveline Van Poelgeest |
Internist ouderengeneeskunde AUMC, betaald |
Kernlid Expertisecentrum farmacotherapie bij ouderen (Ephor), betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-06-2023
16-5-2025 herbevestigd
|
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door deelname van de Patiëntenfederatie Nederland in de richtlijncommissie.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Module verlaging valrisico bij thuiswonende ouderen |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.