Preoperatief verwijderen van haar
Uitgangsvraag
1a. Wat is de plaats van preoperatief verwijderen van haar in het operatiegebied bij de preventie
van postoperatieve wondinfecties (POWIs)?1
1b. Indien preoperatief verwijderen van haar noodzakelijk is, welke methode heeft dan de voorkeur?1
2. Indien preoperatief verwijderen van haar noodzakelijk is, welk moment heeft dan de voorkeur?1
Disclaimer: Dit is een adaptatie van een origineel werk ‘Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.’ (https://www.who.int/publications/i/item/9789241550475). Deze adaptatie is niet uitgevoerd door de WHO. De WHO is niet verantwoordelijk voor de inhoud of nauwkeurigheid van deze adaptatie. De originele uitgave is de bindende en authentieke uitgave.
1 De WHO-richtlijn beschrijft geen uitgangsvragen. De uitgangsvragen voor deze module zijn opgesteld in overeenstemming met de standaardprocedures van het Kennisinstituut van de Federatie Medisch Specialisten.
Aanbeveling
1a. Preoperatief verwijderen van haar
Verwijder geen haar in het operatiegebied voorafgaand aan de operatie, tenzij dit om chirurgisch technische redenen noodzakelijk is.
[Aangepast van WHO 2018]
Informeer de patiënt over de mogelijke risico’s van preoperatief ontharen en instrueer de patiënt om niet zelf voorafgaand aan de operatie haar in het operatiegebied te verwijderen. [De novo]
1b. Methoden van preoperatief verwijderen van haar
Indien het verwijderen van haar in het operatiegebied om chirurgisch technische redenen noodzakelijk is:
- gebruik een (medische) tondeuse met wegwerp tondeusekop;
[Aangepast van WHO 2018] - gebruik geen scheermes;
[WHO 2018] - gebruik geen ontharingscrème.
[De novo]
2. Moment van preoperatief verwijderen van haar
Indien het verwijderen van haar in het operatiegebied om chirurgisch technische redenen noodzakelijk is:
- verwijder haar op de dag van operatie;
[De novo] - verwijder haar bij voorkeur niet in de operatiekamer, maar in een andere daarvoor geschikte ruimte in het operatiekamercomplex.
[De novo]
Disclaimer: Dit is een adaptatie van een origineel werk ‘Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.’ (https://www.who.int/publications/i/item/9789241550475). Deze adaptatie is niet uitgevoerd door de WHO. De WHO is niet verantwoordelijk voor de inhoud of nauwkeurigheid van deze adaptatie. De originele uitgave is de bindende en authentieke uitgave.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is systematisch literatuuronderzoek verricht naar het effect van preoperatief verwijderen van haar bij patiënten die chirurgische procedures ondergaan. Daarnaast is het effect onderzocht van verschillende ontharingsmethodes (scheren, tondeuse, ontharingscrème) en het moment van ontharen (de dag voorafgaand aan de operatie, de dag van operatie). Postoperatieve wondinfectie (POWI’s) werden als cruciale uitkomstmaat gedefinieerd en POWI-attributieve sterfte als belangrijke uitkomstmaat. Een relatief verschil van 25% (relatief risico kleiner dan 0.80 of groter dan 1.25) in het optreden van POWI’s en 5% (relatief risico kleiner dan 0.95 of groter dan 1.05) in het optreden van POWI-attributieve sterfte tussen beide interventies werd als klinisch relevant beschouwd.
1. Preoperatief ontharen versus niet ontharen
a. Scheren versus niet ontharen
Zeven gerandomiseerde gecontroleerde studies die het effect van preoperatief scheren hebben vergeleken met niet ontharen bij volwassen chirurgische patiënten werden geïncludeerd. Analyse liet een klinisch relevant verschil zien in het optreden van POWI’s tussen scheren (4.2%) en niet ontharen (2.3%) (RRgepoold 1.69; 95% CI 0.95 tot 2.98 / RDgepoold 0.010; 95% CI -0.001 tot 0.021). Vanwege studiebeperkingen (risk of bias) en het overschrijden van de bovengrens voor klinische relevantie (imprecisie) is de bewijskracht met twee niveaus afgewaardeerd van ‘hoog’ tot ‘laag’. Dit betekent dat er lage zekerheid is dat het ware effect van preoperatief scheren vergeleken met niet ontharen dicht bij het geschatte effect ligt.
b. Tondeuse versus niet ontharen
Eén gerandomiseerde gecontroleerde studie die het effect van preoperatief ontharen met een tondeuse heeft vergeleken met niet ontharen bij volwassen chirurgische patiënten werd geïncludeerd. Analyse liet geen klinisch relevant verschil zien in het optreden van POWI’s tussen het ontharen met een tondeuse (1.5%) en het niet ontharen (1.5%) (RR 1.00; 95% CI 0.06 tot 15.65 / RD 0.000; 95% CI -0.042 tot 0.042). Vanwege studiebeperkingen (risk of bias) en het overschrijden van beide grenzen van klinische relevantie (imprecisie) is de bewijskracht met drie niveaus afgewaardeerd van ‘hoog’ tot ‘zeer laag’. Dit betekent dat er zeer lage zekerheid is dat het ware effect van preoperatief ontharen met een tondeuse vergeleken met niet ontharen dicht bij het geschatte effect ligt.
c. Ontharingscrème versus niet ontharen
Eén gerandomiseerde gecontroleerde studie die het effect van preoperatief ontharen met een ontharingscrème heeft vergeleken met niet ontharen bij volwassen chirurgische patiënten werd geïncludeerd. Analyse liet geen klinisch relevant verschil zien in het optreden van POWI’s tussen ontharen met een ontharingscrème (7.9%) en niet ontharen (7.8%) (RR 1.02; 95% CI 0.45 tot 2.31 / RD 0.001; 95% CI -0.063 tot 0.066). Vanwege studiebeperkingen (risk of bias) en het overschrijden van beide grenzen van klinische relevantie (imprecisie) is de bewijskracht met drie niveaus afgewaardeerd van ‘hoog’ tot ‘zeer laag’. Dit betekent dat er zeer lage zekerheid is dat het ware effect van preoperatief ontharen met ontharingscrème vergeleken niet ontharen dicht bij het geschatte effect ligt.
Er is geen conclusie te trekken met betrekking tot het effect van preoperatief ontharen op POWI-attributieve sterfte, omdat geen van de geïncludeerde studies POWI-attributieve sterfte als uitkomst heeft gerapporteerd.
Er zijn geen studies gevonden die het effect van preoperatief ontharen hebben onderzocht bij kinderen die een chirurgische ingreep ondergingen.
2. Methoden van preoperatief ontharen
a. Tondeuse versus scheren
Vier gerandomiseerde gecontroleerde studies die het effect van preoperatief ontharen met een tondeuse hebben vergeleken met scheren bij volwassen chirurgische patiënten werden geïncludeerd. Analyse liet een klinisch relevant verschil zien in het optreden van POWI’s tussen ontharen met een tondeuse (2.4%) en scheren (4.7%) (RRgepoold 0.52; 95% CI 0.30 tot 0.91 / RDgepoold -0.018; 95% CI -0.035 tot -0.001). Vanwege studiebeperkingen (risk of bias) en het overschrijden van de ondergrens van klinische relevantie (imprecisie) is de bewijskracht met twee niveaus afgewaardeerd van ‘hoog’ tot ‘laag’. Dit betekent dat er lage zekerheid is dat het ware effect van preoperatief ontharen met een tondeuse vergeleken met scheren dicht bij het geschatte effect ligt.
b. Tondeuse of niet ontharen versus scheren
Tien gerandomiseerde gecontroleerde studies die het effect van preoperatief ontharen met een tondeuse of niet ontharen hebben vergeleken met scheren bij volwassen chirurgische patiënten werden geïncludeerd. Analyse liet een klinisch relevant verschil zien in het optreden van POWI’s tussen ontharen met een tondeuse of niet ontharen (2.4%) en scheren (5.0%) (RRgepoold 0.54; 95% CI 0.36 tot 0.80 / RDgepoold -0.020; 95% CI -0.035 tot -0.006). Vanwege studiebeperkingen (risk of bias) is de bewijskracht met één niveau afgewaardeerd van ‘hoog’ tot ‘redelijk’. Dit betekent dat er redelijke zekerheid is dat het ware effect van preoperatief ontharen met een tondeuse of niet ontharen vergeleken met scheren dicht bij het geschatte effect ligt.
c. Ontharingscrème versus scheren
Zes gerandomiseerde gecontroleerde studies die het effect van preoperatief ontharen met ontharingscrème hebben vergeleken met scheren bij volwassen chirurgische patiënten werden geïncludeerd. Analyse liet een klinisch relevant verschil zien in het optreden van POWI’s tussen ontharen met ontharingscrème (4.0%) en scheren (11.3%) (RRgepoold 0.39; 95% CI 0.13 tot 1.18 / RDgepoold -0.050; 95% CI -0.114 tot 0.014). Vanwege studiebeperkingen (risk of bias), statistische heterogeniteit (inconsistentie) en het overschrijden van beide grenzen van klinische relevantie (imprecisie) is de bewijskracht met drie niveaus afgewaardeerd van ‘hoog’ tot ‘zeer laag’. Dit betekent dat er zeer lage zekerheid is dat het ware effect van preoperatief ontharen met ontharingscrème vergeleken met scheren dicht bij het geschatte effect ligt.
Er is geen conclusie te trekken met betrekking tot het effect van verschillende ontharingsmethoden op POWI-attributieve sterfte, omdat geen van de geïncludeerde studies POWI-attributieve sterfte als uitkomst heeft gerapporteerd.
Er zijn geen studies gevonden die verschillende methoden van preoperatief ontharen hebben vergeleken bij kinderen die een chirurgische ingreep ondergingen.
3. Moment van preoperatief ontharen
Eén gerandomiseerde gecontroleerde studie die het effect van het moment van preoperatief ontharen heeft onderzocht bij volwassen chirurgische patiënten werd geïncludeerd. Analyse liet verschillende resultaten zien voor scheren en ontharen met een tondeuse. Voor scheren werd geen klinisch relevant verschil zien in het optreden van POWI’s tussen scheren op de dag voorafgaand aan de operatie (5.2%) en scheren op de dag van operatie (6.4%) (RR 0.81; 95% CI 0.41 tot 1.61 / RD -0.012; 95% CI -0.052 tot 0.027). Echter, voor ontharen met een tondeuse werd wel een klinisch relevant verschil gevonden tussen de dag voorafgaand aan de operatie (4.0%) en de dag van operatie (1.8%) (RR 2.26; 95% CI 0.72 tot 7.11 / RD 0.022; 95% CI -0.008 tot 0.052).
Vanwege studiebeperkingen (risk of bias) en het overschrijden van beide grenzen van klinische relevantie (imprecisie) is de bewijskracht (voor zowel scheren als ontharen met een tondeuse) met drie niveaus afgewaardeerd van ‘hoog’ tot ‘zeer laag’. Dit betekent dat er zeer lage zekerheid is dat het ware effect van preoperatief ontharen op de dag voorafgaand aan de operatie (scheren of tondeuse) vergeleken met de dag van operatie dicht bij het geschatte effect ligt. Hier ligt een kennislacune.
Er is geen conclusie te trekken met betrekking tot het effect van het moment van preoperatief ontharen (scheren of tondeuse) op POWI-attributieve sterfte, omdat de geïncludeerde studie POWI-attributieve sterfte niet als uitkomst heeft gerapporteerd.
Er zijn geen studies gevonden die het moment van preoperatief ontharen hebben onderzocht bij kinderen die een chirurgische ingreep ondergingen.
4. Ruimte voor preoperatief ontharen
In geen van de 15 geïncludeerde studies naar preoperatief ontharen bij volwassen chirurgische patiënten is het effect van de ruimte waar preoperatief ontharen wordt uitgevoerd (operatiekamer, voorbereidingsruimte, holding, verpleegafdeling) onderzocht.
Internationale richtlijnen
Internationale richtlijnen voor de preventie van POWI’s zijn unaniem in de aanbeveling om haar in het operatiegebied niet routinematig te verwijderen (Tabel 1) (Berríos-Torres, 2017; NICE, 2019; Calderwood, 2023; WHO, 2009; WHO, 2018A). Scheren wordt ontraden (NICE, 2019; WHO, 2009; WHO, 2018A) en, indien ontharen noodzakelijk is, wordt geadviseerd een elektrische tondeuse te gebruiken (Berríos-Torres, 2017; NICE, 2019; WHO, 2009; WHO, 2018A). NICE beveelt hierbij een tondeuse kop voor éénmalig gebruik aan (NICE, 2019).
Het CDC beveelt aan om haar, indien noodzakelijk, direct voorafgaand aan de operatie te verwijderen (Berríos-Torres, 2017), de WHO binnen 2 uur voorafgaand aan de operatie (WHO, 2009), en NICE op de dag van operatie (NICE, 2019).
Tabel 1. Internationale richtlijnen voor de preventie van postoperatieve wondinfecties.
|
Richtlijn |
Aanbeveling(en) |
|
CDC (Berríos-Torres, 2017) |
|
|
NICE (NICE, 2019) |
|
|
SHEA/IDSA/APIC/AHA (Calderwood, 2023) |
|
|
WHO – Safe surgery (WHO, 2009) |
|
|
WHO (WHO, 2018A) |
|
AHA = American Hospital Association
APIC = Association for Professionals in Infection Control
CDC = Centers for Disease Prevention and Control
IDSA = Infectious Diseases Society of America
NICE = National Institute for Health and Care Excellence
SHEA = Society for Healthcare Epidemiology of America
WHO = World Health Organization
Overige effecten van de interventie
Ontharen met een scheermes vergroot de kans op beschadigingen van de huid, doordat het (scherpe) mes direct over de huid wordt getrokken (Alexander 1983, Balthazar 1982). Naast een verhoogd risico op POWI’s is er bij scheren ook meer kans op het infecteren van de hechtingen (Alexander, 1983).
Tondeuses knippen het haar dicht bij de huid zonder de huid echt aan te raken, waardoor er minder risico is op beschadigingen van de huid. Het nadeel van het gebruik van een tondeuse zijn het verspreiden van (losse) haardeeltjes, huidschilfers en huidbacteriën in het operatiegebied (Edmiston, 2016). Recent ontwikkelde tondeuses met vacuümsysteem verminderen mogelijk het vrijkomen van haardeeltjes, wat van belang kan zijn bij ontharen op de operatiekamer. De wetenschappelijke onderbouwing hiervoor is echter beperkt. Hier ligt een kennislacune. Het reinigen en desinfecteren van herbruikbare tondeusekoppen is arbeidsintensief en wordt beperkt toegepast. Om kruisbesmetting tussen patiënten te voorkomen wordt daarom een tondeusekop voor éénmalig gebruik geadviseerd (NICE, 2019).
Ontharingscrèmes bevatten chemicaliën. Naast praktische bezwaren aan het gebruik van een ontharingscrème (inwerktijd en noodzaak om af te spoelen) zijn dergelijke crèmes niet toepasbaar in het urogenitale gebied en bestaat de kans op overgevoeligheidsreacties.
In de huidige Nederlandse praktijk vindt het preoperatief ontharen van het operatiegebied, indien geïndiceerd, vaak plaats in de operatiekamer. Dit heeft als voordeel dat de chirurg ter plaatse de noodzaak van ontharen en het te ontharen gebied kan beoordelen, maar vergroot aan de andere kant de kans op het verspreiden van haardeeltjes, huidschilfers en huidbacteriën in de operatiekamer. Bij ontharen in een andere ruimte op het operatiekamercomplex, zoals de voorbereidingsruimte of de holding, blijft beoordeling door de chirurg direct voorafgaand aan de operatie mogelijk. Dit is niet het geval bij preoperatief ontharen op de verpleegafdeling, waarbij beoordeling door de chirurg al eerder op de verpleegafdeling moet plaatsvinden en het moment van preoperatief ontharen ook verder voor de start van de operatie ligt dan bij ontharen op de operatiekamer.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Er is weinig bekend over waarden en voorkeuren van patiënten met betrekking tot preoperatief ontharen. Waarden en voorkeuren van patiënten zijn niet als uitkomst gerapporteerd in de studies die zijn geïncludeerd in de literatuuranalyse van de WHO. In een studie naar voorkeuren van patiënten en chirurgen bij maxillofaciale chirurgie, gaven patiënten de voorkeur aan ‘niet ontharen’ boven ‘scheren’, en rapporteerden chirurgen geen verschil in het gemak van sluiten van de operatiewond tussen ‘niet ontharen’ en ‘scheren’ (Ilankovan, 1992).
Het is belangrijk dat de patiënt goed geïnformeerd wordt over de mogelijke risico’s van preoperatief ontharen met daarbij het advies om de huid in het operatiegebied niet zelf te ontharen. Enerzijds omdat ontharen mogelijk niet nodig is, anderzijds omdat ontharen, indien noodzakelijk, het liefst zo kort mogelijk voor de operatie en met een tondeuse met wegwerpkop wordt uitgevoerd. Het is van belang dat instructies voor de patiënt ook geschikt zijn voor kwetsbare patiënten en patiënten met een cognitieve beperking.
Kosten (middelenbeslag)
POWI’s behoren tot de meest voorkomende zorggerelateerde infecties (PREZIES, 2023A; ECDC, 2023). In nationale en internationale studies zijn POWI’s consequent geassocieerd met een toename in zorgkosten ten opzichte van patiënten zonder infectie door verlenging van de opnameduur, heropnames, en heroperaties (Badia, 2017; Broex, 2009; Eckmann, 2022; Gantz, 2019; Koek, 2019; Lewis, 2013; Purba, 2020; VandenBergh, 1996).
‘Niet ontharen’ brengt geen kosten met zich mee en vormt geen belasting voor patiënt en zorgmedewerkers. De personele en materiele kosten van preoperatief ontharen met een (medische) tondeuse zijn gering. De kosten van het gebruik van wegwerp tondeusekoppen zijn hoger dan die van het gebruik van herbruikbare tondeusekoppen.
Kosteneffectiviteit was geen uitkomst in de studies die zijn geïncludeerd in de WHO-literatuuranalyse en er is niet aanvullend naar gezocht.
Aanvaardbaarheid, haalbaarheid en implementatie
De aanbeveling om alleen op chirurgisch technische redenen preoperatief te ontharen is overeenkomstig de huidige klinische praktijk. Datzelfde geldt voor de aanbeveling om, indien ontharen noodzakelijk is, niet te scheren maar een (medische) tondeuse te gebruiken met wegwerp tondeusekop. In de aanbevelingen wordt met betrekking tot de locatie van preoperatief ontharen, indien noodzakelijk, een voorkeur uitgesproken voor een ruimte binnen het operatiekamercomplex anders dan de operatiekamer. Met deze aanbeveling wordt zorginstellingen de ruimte gelaten om zelf te bezien of er een geschikte ruimte is binnen het operatiekamercomplex anders dan de operatiekamer.
De werkgroep verwacht dat de meeste patiënten in staat zijn de instructies voor het niet zelf preoperatief ontharen van het operatiegebied op te volgen.
Duurzaamheid
Duurzaamheid is niet benoemd in de WHO-richtlijn en er is niet aanvullend naar gezocht.
De aanbeveling om alleen op chirurgisch technische redenen preoperatief te ontharen beperkt het gebruik van (medische) tondeuses (R2-Reduce). In Nederland worden voornamelijk wegwerp tondeusekoppen gebruikt. Het is niet onderzocht of deze minder duurzaam zijn dan de herbruikbare tondeusekoppen. Het gebruik van wegwerp tondeusekoppen is mogelijk minder duurzaam dan herbruikbare tondeusekoppen, maar dit is niet onderzocht.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
1a/b. Preoperatief verwijderen van haar, incl. methoden
Preoperatief ontharen van het operatiegebied kan nodig zijn om preoperatieve markering en toegankelijkheid van de huid voor incisie te vergemakkelijken. Bovendien kan het hechten en het aanbrengen van wondverband bemoeilijkt worden door de aanwezigheid van haar.
Ontharen met een scheermes vergroot de kans op beschadigingen van de huid en bewijs van redelijke kwaliteit laat zien dat scheren het risico op postoperatieve wondinfecties (POWI’s) vergroot in vergelijking tot preoperatief niet ontharen òf ontharen met een tondeuse.
Bewijs van zeer lage kwaliteit laat geen duidelijk effect zien van preoperatief ontharen met een ontharingscrème op het optreden van POWI’s in vergelijking tot niet ontharen of scheren. Wel kunnen bij het gebruik van ontharingscrèmes overgevoeligheidsreacties optreden, zijn dergelijke crèmes niet toepasbaar in het urogenitaal gebied en zijn er ook praktische bezwaren aan het gebruik (inwerktijd en noodzaak om af te spoelen).
Bewijs van zeer lage kwaliteit laat geen duidelijk verschil zien in het POWI-risico tussen preoperatief ontharen met een tondeuse en niet ontharen. Wel is er een verschil in kosten en duurzaamheid in het voordeel van niet ontharen.
Het gebruik van wegwerp tondeusekoppen is mogelijk minder duurzaam dan het gebruik van herbruikbare tondeusekoppen, maar voorkomt de kans op kruisbesmetting tussen patiënten en de arbeidsintensieve en risicovolle handelingen die nodig zijn voor het adequaat reinigen en desinfecteren van herbruikbare tondeusekoppen.
De werkgroep is daarom van mening dat haar in het operatiegebied alleen om chirurgisch technische redenen verwijderd mag worden. Als ontharen noodzakelijk is, is het gebruik van een (medische) tondeuse met wegwerp tondeusekop de aanbevolen methode. Preoperatief scheren en het gebruik van ontharingscrème wordt afgeraden, evenals het preoperatief ontharen door de patiënt zelf.
Hoewel er geen studies in kinderen zijn gevonden, is de werkgroep van mening dat de aanbevelingen ook voor kinderen van toepassing zijn.
2. Moment van preoperatief verwijderen van haar
Bewijs van zeer lage kwaliteit laat geen duidelijk verschil zien in het POWI-risico tussen preoperatief ontharen op de dag voorafgaand aan de operatie en ontharen op de dag van operatie. Internationale richtlijnen bevelen aan om niet eerder dan de dag van operatie te ontharen. De werkgroep volgt deze aanbeveling, omdat ontharen van het operatiegebied kort voor de ingreep op theoretische gronden de minste kans op besmetting geeft en daarnaast het meest praktisch is.
Er is geen wetenschappelijk bewijs dat de ruimte waar het ontharen plaatsvindt van invloed is op het POWI-risico. Om logistieke redenen heeft het de voorkeur preoperatief ontharen uit te voeren op het operatiekamercomplex en niet op de verpleegafdeling. Vanwege de kans op verspreiding van haardeeltjes, huidschilfers en huidbacteriën tijdens het preoperatief ontharen met een tondeuse is de werkgroep van mening dat het ontharen bij voorkeur niet in de operatiekamer dient plaats te vinden, maar in een andere daarvoor geschikte ruimte in het operatiekamercomplex.
De werkgroep is van mening dat de aanbevelingen ook voor kinderen van toepassing zijn.
Disclaimer: Dit is een adaptatie van een origineel werk ‘Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.’ (https://www.who.int/publications/i/item/9789241550475). Deze adaptatie is niet uitgevoerd door de WHO. De WHO is niet verantwoordelijk voor de inhoud of nauwkeurigheid van deze adaptatie. De originele uitgave is de bindende en authentieke uitgave.
Onderbouwing
Deze module betreft een adaptatie van de module ‘Preoperative hair removal’ van de World Health Organization (WHO)-richtlijn ‘Global guidelines for the prevention of surgical site infection, second edition. 2018’ (WHO, 2018A; WHO, 2018B). Voor een toelichting op de procedure van adapteren wordt verwezen naar de Startpagina en de Bijlage Adapteren.
Postoperatieve wondinfecties (POWI’s) behoren tot de meest voorkomende zorggerelateerde infecties (PREZIES, 2023A; ECDC, 2023). In maart 2023, werd bij 6,9% (prevalentie) van de patiënten die op dat moment in een Nederlands ziekenhuis waren opgenomen een zorggerelateerde infectie vastgesteld; 30% hiervan waren POWI’s (PREZIES, 2023A). In de periode 2017-2021, werd bij 1,9% (cumulatieve incidentie) van de patiënten die in deze periode een operatie ondergingen in een Nederlands ziekenhuis een POWI vastgesteld, variërend van 0.8% voor knieprothese ingrepen tot 16.3% voor open colonchirurgische ingrepen (PREZIES, 2023B).
Het verwijderen van haar van de beoogde plaats van chirurgische incisie maakt traditioneel deel uit van de routine preoperatieve voorbereiding van patiënten die een operatie ondergaan. Het verwijderen van haar kan nodig zijn om preoperatieve markering en toegankelijkheid van de huid voor incisie te vergemakkelijken. Bovendien kan het hechten en het aanbrengen van wondverband bemoeilijkt worden door de aanwezigheid van haar. Het is onduidelijk of de aanwezigheid van haar of juist het verwijderen van haar (met als gevolg microscopische trauma van de huid), de kans op een POWI vergroten. Daarnaast is onduidelijk wat het effect is van verschillende ontharingsmethoden (scheren, tondeuse, ontharingscrème), het moment van ontharen en de ruimte waar het ontharen wordt uitgevoerd op de incidentie van POWI’s.
Disclaimer: Dit is een adaptatie van een origineel werk ‘Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.’ (https://www.who.int/publications/i/item/9789241550475). Deze adaptatie is niet uitgevoerd door de WHO. De WHO is niet verantwoordelijk voor de inhoud of nauwkeurigheid van deze adaptatie. De originele uitgave is de bindende en authentieke uitgave.
- Hair removal versus no hair removal1
|
Low GRADE |
Preoperative shaving may increase the occurrence of surgical site infections when compared with no hair removal in patients undergoing surgical operations (any type of procedure).
Sources: Abouzari, 2009; Celik, 2007; Court-Brown, 1981; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992 |
|
Very low GRADE |
The evidence is very uncertain about the effect of preoperative clipping on the occurrence of surgical site infections when compared with no hair removal in patients undergoing surgical operations (any type of procedure).
Sources: Abouzari, 2009 |
|
Very low GRADE |
The evidence is very uncertain about the effect of preoperative depilatory cream on the occurrence of surgical site infections when compared with no hair removal in patients undergoing surgical operations (any type of procedure).
Sources: Court-Brown, 1981 |
|
No GRADE |
No evidence was found about the effect of preoperative shaving, clipping or depilatory cream on surgical site infection attributable mortality when compared with no hair removal in patients undergoing surgical operations (any type of procedure).
Sources: - |
- Comparison of methods of hair removal1
|
Low GRADE |
Preoperative clipping may reduce the occurrence of surgical site infections when compared with shaving in patients undergoing surgical operations (any type of procedure).
Sources: Abouzari, 2009; Alexander, 1983; Balthazar, 1982, Grober, 2013 |
|
Moderate GRADE |
Preoperative clipping or no hair removal likely reduces the occurrence of surgical site infections when compared with shaving in patients undergoing surgical operations (any type of procedure).
Sources: Abouzari, 2009; Alexander, 1983; Balthazar, 1982; Celik, 2007; Court-Brown, 1981; Grober, 2013; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992 |
|
Very low GRADE |
The evidence is very uncertain about the effect of preoperative depilatory cream on the occurrence of surgical site infections when compared with shaving in patients undergoing surgical operations (any type of procedure).
Sources: Adisa, 2011; Court-Brown, 1981; Goëau-Brisonnière, 1987; Powis, 1976; Seropian, 1971; Thur de Koos, 1983 |
|
No GRADE |
No evidence was found about the effect of preoperative clipping, clipping or no hair removal or depilatory cream on surgical site infection attributable mortality when compared with shaving in patients undergoing surgical operations (any type of procedure).
Sources: - |
- Timing of hair removal1
|
Very low GRADE |
The evidence is very uncertain about the effect of hair removal (shaving or clipping) on the night before surgery on the occurrence of surgical site infections when compared with hair removal (shaving or clipping) on the day of surgery in patients undergoing surgical operations (any type of procedure).
Sources: Alexander, 1983 |
|
No GRADE |
No evidence was found about the effect of hair removal (shaving or clipping) on the night before surgery on the occurrence of surgical site infection attributable mortality when compared with hair removal (shaving or clipping) on the day of surgery in patients undergoing surgical operations (any type of procedure).
Sources: - |
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 The conclusions of the literature were formulated in accordance with the standard procedures of the Knowledge Institute of the Federation of Medical Specialists.
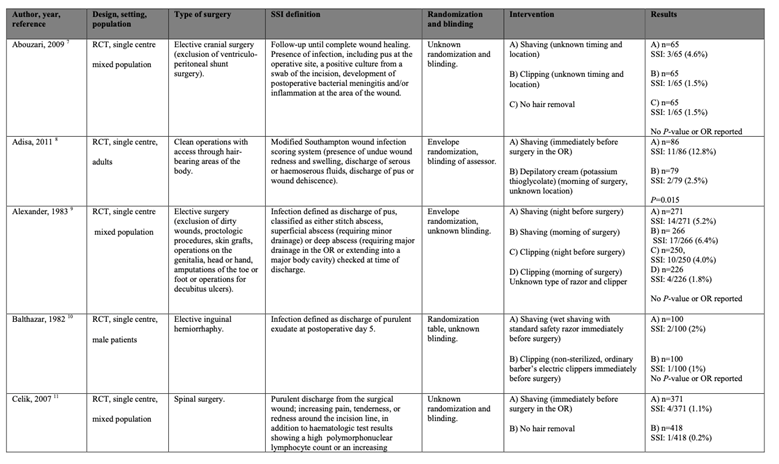
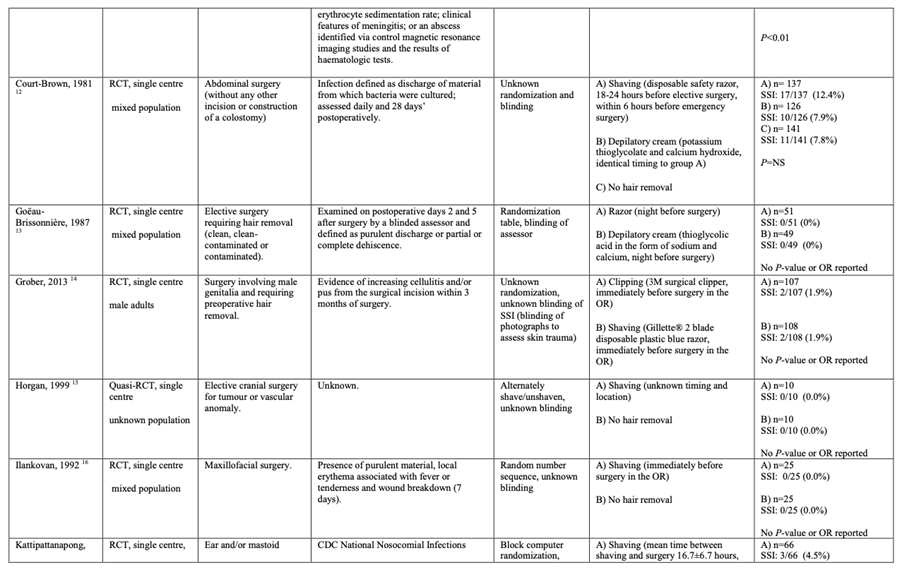
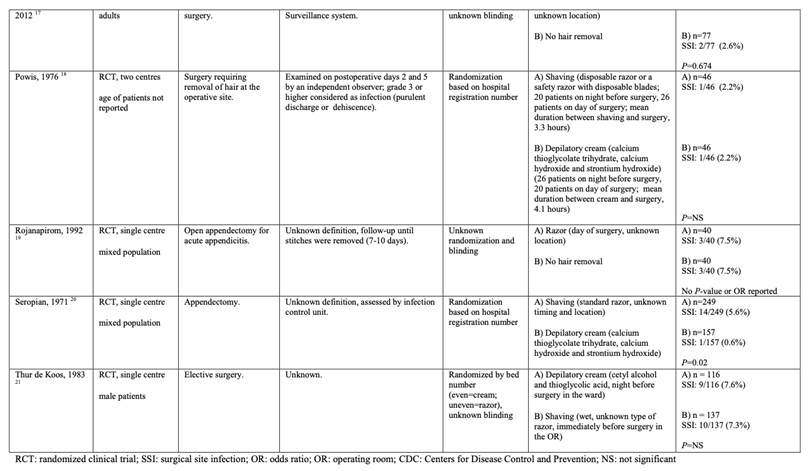
Description of studies
- Hair removal versus no hair removal
Seven randomized controlled trials (RCT) (Abouzari, 2009; Celik, 2007; Court-Brown, 1981; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992) comparing shaving with no hair removal were identified with surgical site infection (SSI) as an outcome. In addition, one RCT comparing clipping with no hair removal (Abouzari, 2009) and one RCT comparing depilatory cream with no hair removal (Court-Brown, 1981) were identified with SSI as an outcome. Included patients were adults undergoing several types of surgical procedures (cranial, maxillofacial, and abdominal surgery).
No studies were identified that investigated the effect of hair removal in children undergoing surgery.
- Comparison of methods of hair removal
Four RCTs comparing clipping with shaving (Abouzari, 2009; Alexander, 1983; Balthazar, 1982; Grober, 2013), ten RCTs (Abouzari, 2009; Alexander, 1983; Balthazar, 1982; Celik, 2007; Court-Brown, 1981; Grober, 2013; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992) comparing clipping or no hair removal with shaving, and 6 RCTs comparing depilatory cream with shaving (Adisa, 2011; Court-Brown, 1981; Goëau-Brisonnière, 1987; Powis, 1976; Seropian, 1971; Thur de Koos, 1983) were identified with SSI as the outcome. Included patients were adults undergoing several types of surgical procedures (general, cranial, maxillofacial, inguinal and abdominal surgery).
No studies were identified that compared different methods of hair removal in children undergoing surgery.
- Timing of hair removal
One RCT comparing hair removal the night before surgery and hair removal on the day of surgery was identified with SSI as an outcome (Alexander, 1983).
No studies were identified that investigated the effect of timing of hair removal in children undergoing surgery.
Results
- Hair removal versus no hair removal
a. Shaving versus no hair removal
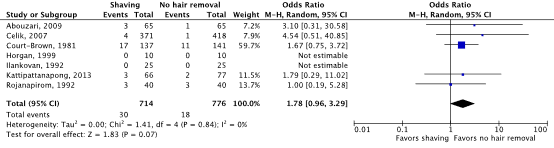
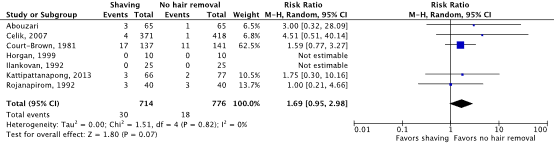
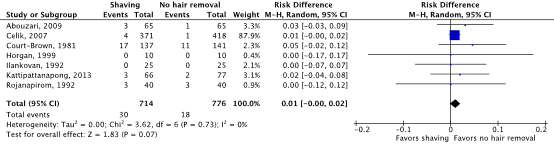
Meta-analyses of the seven RCTs comparing shaving with no hair removal showed a clinically relevant difference in the incidence of SSIs in favor of no hair removal (4.2% vs. 2.3%) (ORpooled 1.78; 95% CI 0.96 to 3.29 / RRpooled 1.69; 95% CI 0.95 to 2.98 / RDpooled 0.010; 95% CI -0.001 to 0.021) (Figure 1a; Comparisons) (Abouzari, 2009; Celik, 2007; Court-Brown, 1981; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992). SSI-attributable mortality was not reported.
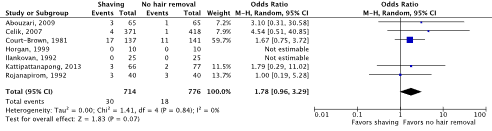
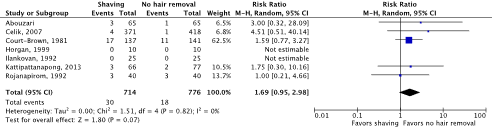
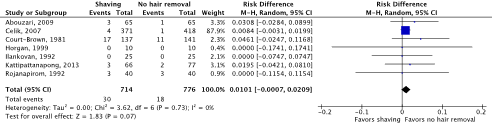
Figure 1a. Forest plot of surgical site infections for preoperative shaving versus no hair removal (pooled odds ratio, risk ratio, and risk difference; random effects model).
b. Clipping versus no hair removal
The RCT comparing clipping with no hair removal showed no clinically relevant difference in the incidence of SSIs between clipping (1.5%) and no hair removal (1.5%) (OR 1.00; 95% CI 0.06 to 16.34 / RR 1.00; 95% CI 0.06 to 15.65 / RD 0.000; 95% CI -0.042 to 0.042) (Abouzari, 2009). SSI-attributable mortality was not reported.
c. Depilatory cream versus no hair removal
The RCT comparing depilatory cream with no hair removal showed no clinically relevant difference in the incidence of SSIs between depilatory cream (7.9%) and no hair removal (7.8%) (OR 1.02; 95% CI 0.42 to 2.49 / RR 1.02; 95% CI 0.45 to 2.31 / RD 0.001; 95% CI -0.063 to 0.066) (Court-Brown, 1981). SSI-attributable mortality was not reported.
2. Comparison of methods of hair removal
a. Clipping versus shaving
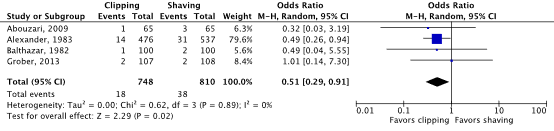
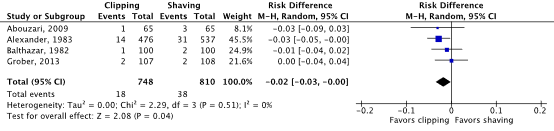
Meta-analyses of the four RCTs comparing clipping with shaving showed a clinically relevant difference in the incidence of SSIs in favor of clipping (2.4% vs. 4.7%) (ORpooled 0.51; 95% CI 0.29 to 0.91 / RRpooled 0.52; 95% CI 0.30 to 0.91 / RDpooled -0.018; 95% CI -0.035 to -0.001) (Figure 2a; Comparisons) (Abouzari, 2009; Alexander, 1983; Balthazar, 1982; Grober, 2013). SSI-attributable mortality was not reported.
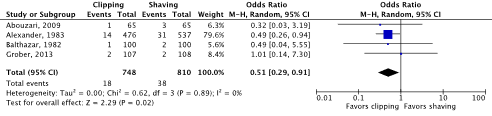
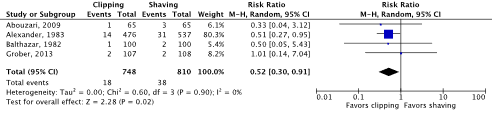
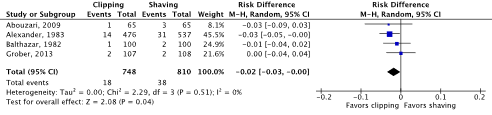
Figure 2a. Forest plot of surgical site infections for preoperative clipping versus shaving (pooled odds ratio, risk ratio, and risk difference; random effects model).
b. Clipping or no hair removal versus shaving
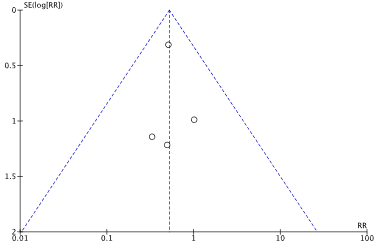
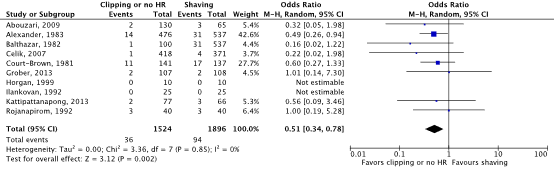
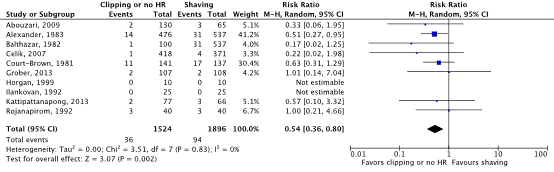
Meta-analyses of the ten RCTs comparing clipping or no hair removal with shaving showed a clinically relevant difference in the incidence of SSIs in favor of clipping or no hair removal (2.4% vs. 5.0%) (ORpooled 0.51; 95% CI 0.34 to 0.78 / RRpooled 0.54; 95% CI 0.36 to 0.80 / RDpooled -0.020; 95% CI -0.035 to -0.006) (Figure 2b; Comparisons) (Abouzari, 2009; Alexander, 1983; Balthazar, 1982; Celik, 2007; Court-Brown, 1981; Grober, 2013; Horgan, 1999; Ilankovan, 1992; Kattipattanapong, 2013; Rojanapirom, 1992). SSI-attributable mortality was not reported.
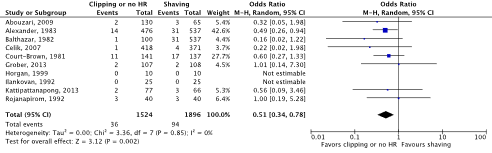
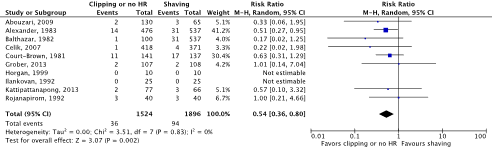
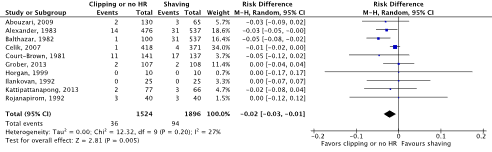
Figure 2b. Forest plot of surgical site infections for preoperative clipping or no hair removal (HR) versus shaving (pooled odds ratio, risk ratio, and risk difference; random effects model).
c. Depilatory cream versus shaving
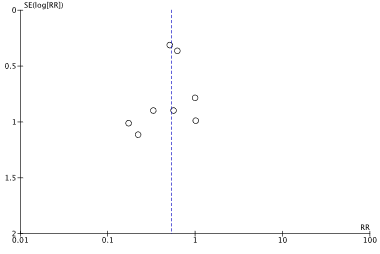
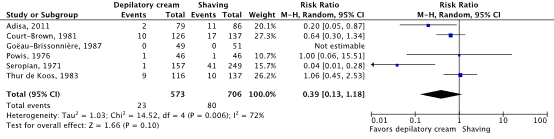
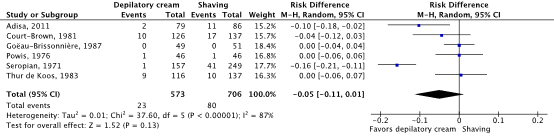
Meta-analyses of the six studies comparing depilatory cream with shaving showed a clinically relevant difference in the incidence of SSIs in favor of depilatory cream (4.0% vs. 11.3%) (ORpooled 0.36; 95% CI 0.11 to 1.17 / RRpooled 0.39; 95% CI 0.13 to 1.18 / RDpooled -0.050; 95% CI -0.114 to 0.014) (Figure 2c; Comparisons) (Adisa, 2011; Court-Brown, 1981; Goëau-Brisonnière, 1987; Powis, 1976; Seropian, 1971; Thur de Koos, 1983). SSI-attributable mortality was not reported.
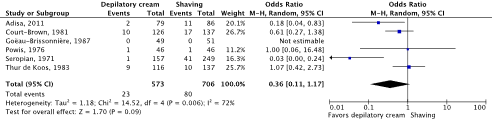
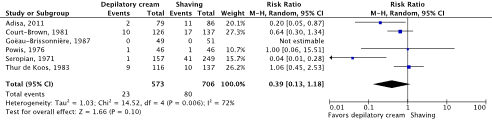
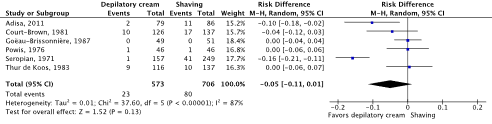
Figure 2c. Forest plot of surgical site infections for depilatory cream versus shaving (pooled odds ratio, risk ratio, and risk difference; random effects model).
3.Timing of hair removal
The study comparing hair removal the night before surgery with hair removal on the day of surgery showed inconsistent results for shaving and clipping (Alexander, 1983).1
a. Shaving
For shaving, no clinically relevant difference was shown in the incidence of SSIs between shaving on the night before surgery (5.2%) and shaving on the day of surgery (6.4%) (OR 0.80; 95% CI 0.39 to 1.65 / RR 0.81; 95% CI 0.41 to 1.61 / RD -0.012; 95% CI -0.052 to 0.027). SSI-attributable mortality was not reported.
b. Clipping
For clipping, a clinically relevant difference was shown in the incidence of SSIs in favor of clipping on the day of surgery (4.0% vs. 1.8%) (OR 2.31; 95% CI 0.71 to 7.48 / RR 2.26; 95% CI 0.72 to 7.11 / RD 0.022; 95% CI -0.008 to 0.052). SSI-attributable mortality was not reported.
Level of evidence of the literature
- Hair removal versus no hair removal
- Shaving versus no hair removal
For SSIs, the level of evidence, based on seven RCTs, started at high and was downgraded with two levels to low because of study limitations, including inadequate allocation concealment, lack of blinding and selective outcome reporting (risk of bias; -1), and the 95% confidence interval of the risk ratio crossing the upper boundary of clinical relevance (imprecision; -1) (GRADE tables). Downgrading for imprecision was not based on the WHO-criterium of meeting the optimal information size, but on the 95% confidence interval of the effect estimate crossing the boundaries of clinical relevance.
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Clipping versus no hair removal
For SSIs, the level of evidence, based on one RCT, started at high and was downgraded with three levels to very low because of study limitations, including lack of blinding (risk of bias; -1), and the 95% confidence interval of the effect estimate crossing both boundaries of clinical relevance (imprecision; -2) (GRADE tables).
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Depilatory cream versus no hair removal
For SSIs, the level of evidence, based on one RCT, started at high and was downgraded with three levels to very low because of study limitations, including lack of blinding and selective outcome reporting (risk of bias; -1), and the 95% confidence interval of the effect estimate crossing both boundaries of clinical relevance (imprecision; -2) (GRADE tables).
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Comparison of methods of hair removal
- Clipping versus shaving
For SSIs, the level of evidence, based on four RCTs, started at high and was downgraded with two levels to low because of study limitations, including lack of blinding (risk of bias; -1), and the 95% confidence interval of the effect estimate crossing the lower boundary of clinical relevance (imprecision; -1) (GRADE tables).
Downgrading for imprecision was not based on the WHO-criterium of meeting the optimal information size, but on the 95% confidence interval of the effect estimate crossing the boundaries of clinical relevance.
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Clipping or no hair removal versus shaving
For SSIs, the level of evidence, based on ten RCTs, started at high and was downgraded with one level to moderate because of study limitations, including inadequate allocation concealment, lack of blinding, and selective outcome reporting (risk of bias; -1) (GRADE tables). For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Depilatory cream versus shaving
For SSIs, the level of evidence, based on six RCTs, started at high and was downgraded with three levels to very low because of study limitations, including inadequate sequence generation, lack of blinding, and selective outcome reporting (risk of bias; -1), inconsistent direction of effect estimates, non-overlapping 95% confidence intervals and an I2 representing substantial statistical heterogeneity (inconsistency; -1), and the 95% confidence interval of the effect estimate crossing the lower boundary of clinical relevance (imprecision; -1) (GRADE tables).
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Timing of hair removal
- Shaving
For SSIs, the level of evidence, based on one RCT, started at high and was downgraded with three levels to very low because of study limitations, including lack of blinding (risk of bias; -1), and the 95% confidence interval of the effect estimate crossing both boundaries of clinical relevance (imprecision; -2) (GRADE tables).
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
- Clipping
For SSIs, the level of evidence, based on one RCT, started at high and was downgraded with three levels to very low because of study limitations, including lack of blinding (risk of bias; -1), and the 95% confidence interval of the effect estimate crossing both boundaries of clinical relevance (imprecision; -2) (GRADE tables).
For SSI-attributable mortality, the level of evidence could not be assessed due to the absence of relevant studies.
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 The WHO performed a meta-analysis and pooled the results for both shaving and clipping. Because of inconsistent results, the working group decided not to present the pooled results.
The World Health Organization (WHO) performed a systematic review of the literature to answer the following (search) questions:
- What is the effect of preoperative hair removal on the incidence of surgical site infections (SSIs) and SSI-attributable mortality1 in surgical patients when compared to no hair removal?
- What is the effect of different hair removal methods on the incidence of surgical site infections (SSIs) and SSI-attributable mortality1 in surgical patients?
- What is the effect of different timing of hair removal on the incidence of surgical site infections (SSIs) and SSI-attributable mortality1 in surgical patients when compared to no hair removal?
P: Adult patients undergoing any type of surgical procedure
I: No hair removal
C: Hair removal (different methods and timing)
O: SSI, SSI-attributable mortality
Relevant outcome measures
The working group considered surgical site infections as a critical outcome and SSI-attributable mortality as an important outcome for decision making.2
The working group defined a 25% relative difference (RR<0.8 or >1.25) in SSI rate and a 5% relative difference (RR<0.95 or >1.05) in SSI-attributable mortality as minimal clinically (patient) important difference.2
Search and select (Methods)
The WHO searched the following databases: Medline (PubMed); Excerpta Medica database (EMBASE); Cumulative Index to Nursing and Allied Health Literature (CINAHL); Cochrane Central Register of Controlled Trials (CENTRAL); and WHO regional medical databases. The time limit for the review was between 1 January 1900 and 15 January 2014. Of note, the usual time limit of 1990 for the systematic reviews conducted for the WHO SSI prevention guidelines was extended to include important relevant literature published prior to this date. Language was restricted to English, French and Spanish. A comprehensive list of search terms was used, including Medical Subject Headings (MeSH) (Search strategy).
Two independent WHO-reviewers screened the titles and abstracts of retrieved references for potentially relevant studies. The full text of all potentially eligible articles was obtained and then reviewed independently by two WHO authors for eligibility based on inclusion criteria. Duplicate studies were excluded. Data were extracted data in a predefined evidence table (Evidence tables) and retrieved studies were critically appraised. Quality was assessed using the Cochrane Collaboration tool to assess the risk of bias of randomized controlled trials (RCTs) (Higgins, 2011) (Risk of bias tables). Any disagreements were resolved through discussion or after consultation with the senior WHO-author, when necessary. Publication bias was assessed using a funnel plot (Egger, 1997).
Meta-analyses of available comparisons were performed using Review Manager version 5.3 as appropriate (Cochrane Collaboration, 2014) (Comparisons). The WHO extracted and pooled odds ratios (OR) with 95% confidence intervals (CI) for each comparison with a random effects model. In addition to the WHO meta-analyses, risk ratios (RR) and risk differences (RD) with 95% CI were extracted and pooled with a random effects model and included in the current literature analysis.3
The WHO used the Grading of Recommendations Assessment, Development and Evaluation (GRADE) methodology (GRADE Pro software) (GRADE Working Group, 2015; Guyatt, 2011) to assess the quality of the body of retrieved evidence (GRADE tables).
The WHO systematic literature search resulted in 609 (non-duplicate) hits. Forty-four studies were initially selected based on title and abstract screening; after reading the full text, 29 studies were excluded, and 15 studies were included in the analysis (Study selection).
Results
Fifteen RCTs were included in the current analysis of the literature (Summary of literature). Important study characteristics and results are summarized in the evidence tables (Evidence tables). The assessment of the risk of bias is summarized in the risk of bias tables (Risk of bias tables). The WHO considered no hair removal and clipping similar in terms of reduced potential to cause microscopic skin trauma. Based on these considerations, the WHO made the following comparisons:
- Hair removal versus no hair removal
a. Shaving versus no hair removal
b. Clipping versus no hair removal
c. Depilatory cream versus no hair removal - Comparisons of methods of hair removal
a. Clipping versus shaving
b. Clipping or no hair removal versus shaving
c. Depilatory cream versus shaving - Timing of hair removal
a. Night before versus day of surgery
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 The working group modified the WHO-search question by including all WHO-defined outcomes.
2 The WHO-guideline did not distinguish between crucial and important outcome measures and did not define thresholds for clinical decision making.
3 The WHO-guideline did not report risk ratios and risk differences.
- Abouzari M, Sodagari N, Hasibi M, Behzadi M, Rashidi A. Re: Nonshaved cranial surgery in black Africans: a short-term prospective preliminary study (Adeleye and Olowookere, Surg Neurol 2008;69-72) Effect of hair on surgical wound infection after cranial surgery: a 3-armed randomized clinical trial. Surg Neurol. 2009 Feb;71(2):261-2; author reply 262. doi: 10.1016/j.surneu.2008.01.059. Epub 2008 Apr 28. PMID: 18440617.
- Adisa AO, Lawal OO, Adejuyigbe O. Evaluation of two methods of preoperative hair removal and their relationship to postoperative wound infection. J Infect Dev Ctries. 2011 Oct 13;5(10):717-22. doi: 10.3855/jidc.1527. PMID: 21997940.
- Alexander JW, Fischer JE, Boyajian M, Palmquist J, Morris MJ. The influence of hair-removal methods on wound infections. Arch Surg. 1983 Mar;118(3):347-52. doi: 10.1001/archsurg.1983.01390030079013. PMID: 6824435.
- Badia JM, Casey AL, Petrosillo N, Hudson PM, Mitchell SA, Crosby C. Impact of surgical site infection on healthcare costs and patient outcomes: a systematic review in six European countries. J Hosp Infect. 2017 May;96(1):1-15. doi: 10.1016/j.jhin.2017.03.004. Epub 2017 Mar 8. PMID: 28410761.
- Balthazar ER, Colt JD, Nichols RL. Preoperative hair removal: a random prospective study of shaving versus clipping. South Med J. 1982 Jul;75(7):799-801. PMID: 7089645.
- Berríos-Torres SI, Umscheid CA, Bratzler DW, Leas B, Stone EC, Kelz RR, Reinke CE, Morgan S, Solomkin JS, Mazuski JE, Dellinger EP, Itani KMF, Berbari EF, Segreti J, Parvizi J, Blanchard J, Allen G, Kluytmans JAJW, Donlan R, Schecter WP; Healthcare Infection Control Practices Advisory Committee. Centers for Disease Control and Prevention Guideline for the Prevention of Surgical Site Infection, 2017. JAMA Surg. 2017 Aug 1;152(8):784-791. doi: 10.1001/jamasurg.2017.0904. Erratum in: JAMA Surg. 2017 Aug 1;152(8):803. PMID: 28467526.
- Broex EC, van Asselt AD, Bruggeman CA, van Tiel FH. Surgical site infections: how high are the costs? J Hosp Infect. 2009 Jul;72(3):193-201. doi: 10.1016/j.jhin.2009.03.020. Epub 2009 May 31. PMID: 19482375.
- Calderwood MS, Anderson DJ, Bratzler DW, Dellinger EP, Garcia-Houchins S, Maragakis LL, Nyquist AC, Perkins KM, Preas MA, Saiman L, Schaffzin JK, Schweizer M, Yokoe DS, Kaye KS. Strategies to prevent surgical site infections in acute-care hospitals: 2022 Update. Infect Control Hosp Epidemiol. 2023 May;44(5):695-720. doi: 10.1017/ice.2023.67. Epub 2023 May 4. PMID: 37137483.
- Celik SE, Kara A. Does shaving the incision site increase the infection rate after spinal surgery? Spine (Phila Pa 1976). 2007 Jul 1;32(15):1575-7. doi: 10.1097/BRS.0b013e318074c39f. PMID: 17621202.
- Cochrane Collaboration 2014. The Nordic Cochrane Centre TCC. Review Manager (RevMan). Version 5.3. Copenhagen: The Cochrane Collaboration 2014.
- Court-Brown CM. Preoperative skin depilation and its effect on postoperative wound infections. J R Coll Surg Edinb. 1981 Jul;26(4):238-41. PMID: 7021812.
- Eckmann C, Kramer A, Assadian O, Flessa S, Huebner C, Michnacs K, Muehlendyck C, Podolski KM, Wilke M, Heinlein W, Leaper DJ. Clinical and economic burden of surgical site infections in inpatient care in Germany: A retrospective, cross-sectional analysis from 79 hospitals. PLoS One. 2022 Dec 28;17(12):e0275970. doi: 10.1371/journal.pone.0275970. PMID: 36576894; PMCID: PMC9797083.
- Edmiston CE Jr, Griggs RK, Tanner J, Spencer M, Seabrook GR, Leaper D. Perioperative hair removal in the 21st century: Utilizing an innovative vacuum-assisted technology to safely expedite hair removal before surgery. Am J Infect Control. 2016 Dec 1;44(12):1639-1644. doi: 10.1016/j.ajic.2016.03.071. Epub 2016 Jun 30. PMID: 27375061.
- Egger M, Davey Smith G, Schneider M, Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ. 1997 Sep 13;315(7109):629-34. doi: 10.1136/bmj.315.7109.629. PMID: 9310563; PMCID: PMC2127453.
- European Centre for Disease Prevention and Control. Point prevalence survey of healthcareassociated infections and antimicrobial use in European acute care hospitals, 2016-2017. Stockholm: ECDC; 2023. (https://www.ecdc.europa.eu/sites/default/files/documents/healthcare-associated--infections-antimicrobial-use-point-prevalence-survey-2016-2017.pdf, accessed 25 August 2023).
- Gantz O, Zagadailov P, Merchant AM. The Cost of Surgical Site Infections after Colorectal Surgery in the United States from 2001 to 2012: A Longitudinal Analysis. Am Surg. 2019 Feb 1;85(2):142-149. PMID: 30819289.
- Goëau-Brissonnière O, Coignard S, Merào AP, Haicault G, Sasako M, Patel JC. Préparation cutanée à la chirurgie. Etude prospective comparant un agent dépilatoire au rasage [Preoperative skin preparation. A prospective study comparing a depilatory agent in shaving]. Presse Med. 1987 Sep 26;16(31):1517-9. French. PMID: 2958817.
- GRADE Working Group. GRADEpro Guideline Development Tool. Summary of findings tables, health technology sssessment and guidelines. GRADE Working Group, Ontario: McMaster University and Evidence Prime Inc.; 2015 (http://www.gradepro.org, accessed 5 May 2016).
- Grober ED, Domes T, Fanipour M, Copp JE. Preoperative hair removal on the male genitalia: clippers vs. razors. J Sex Med. 2013 Feb;10(2):589-94. doi: 10.1111/j.1743-6109.2012.02904.x. Epub 2012 Aug 21. PMID: 22908852.
- Guyatt G, Oxman AD, Akl EA, Kunz R, Vist G, Brozek J, Norris S, Falck-Ytter Y, Glasziou P, DeBeer H, Jaeschke R, Rind D, Meerpohl J, Dahm P, Schünemann HJ. GRADE guidelines: 1. Introduction-GRADE evidence profiles and summary of findings tables. J Clin Epidemiol. 2011 Apr;64(4):383-94. doi: 10.1016/j.jclinepi.2010.04.026. Epub 2010 Dec 31. PMID: 21195583.
- Higgins JP, Altman DG, Gøtzsche PC, Jüni P, Moher D, Oxman AD, Savovic J, Schulz KF, Weeks L, Sterne JA; Cochrane Bias Methods Group; Cochrane Statistical Methods Group. The Cochrane Collaboration's tool for assessing risk of bias in randomised trials. BMJ. 2011 Oct 18;343:d5928. doi: 10.1136/bmj.d5928. PMID: 22008217; PMCID: PMC3196245.
- Horgan MA, Kernan JC, Schwartz MS, Kellogg JX, McMenomey SO, Delashaw JB. Shaveless brain surgery: safe, well tolerated, and cost effective. Skull Base Surg. 1999;9(4):253-8. doi: 10.1055/s-2008-1058134. PMID: 17171113; PMCID: PMC1656773.
- Ilankovan V, Starr DG. Preoperative shaving: patient and surgeon preferences and complications for the Gillies incision. J R Coll Surg Edinb. 1992 Dec;37(6):399-401. PMID: 1283411.
- Kattipattanapong W, Isaradisaikul S, Hanprasertpong C. Surgical site infections in ear surgery: hair removal effect; a preliminary, randomized trial study. Otolaryngol Head Neck Surg. 2013 Mar;148(3):469-74. doi: 10.1177/0194599812472297. Epub 2013 Jan 2. PMID: 23283828.
- Koek MBG, van der Kooi TII, Stigter FCA, de Boer PT, de Gier B, Hopmans TEM, de Greeff SC; Burden of SSI Study Group. Burden of surgical site infections in the Netherlands: cost analyses and disability-adjusted life years. J Hosp Infect. 2019 Nov;103(3):293-302. doi: 10.1016/j.jhin.2019.07.010. Epub 2019 Jul 19. PMID: 31330166.
- Lewis SS, Moehring RW, Chen LF, Sexton DJ, Anderson DJ. Assessing the relative burden of hospital-acquired infections in a network of community hospitals. Infect Control Hosp Epidemiol. 2013 Nov;34(11):1229-30. doi: 10.1086/673443. PMID: 24113613; PMCID: PMC3977691.
- National Institute for Health and Care Excellence. NICE guideline. Surgical site infections: prevention and treatment. 2019 (last update 2020). (https://www.nice.org.uk/guidance/ph36/resources/healthcareassociated-infections-prevention-and-control-pdf-1996300832965), accessed 24 August 2023).
- Powis SJ, Waterworth TA, Arkell DG. Preoperative skin preparation: clinical evaluation of depilatory cream. Br Med J. 1976 Nov 13;2(6045):1166-8. doi: 10.1136/bmj.2.6045.1166. PMID: 791444; PMCID: PMC1689580.
- PREventie van ZIEkenhuisinfecties door Surveillance (PREZIES). Jaarcijfers 2023: alle ziekenhuizen. 2023. (https://www.rivm.nl/documenten/po-jaarcijfers-algemeen, accessed 26 August 2023). A
- PREventie van ZIEkenhuisinfecties door Surveillance (PREZIES). Referentiecijfers 2017-2021: Postoperatieve wondinfecties. RIVM, 2023. (https://www.rivm.nl/documenten/referentiecijfers-powi-2021, accessed 10 October 2023). B
- Purba AKR, Luz CF, Wulandari RR, van der Gun I, Dik JW, Friedrich AW, Postma MJ. The Impacts of Deep Surgical Site Infections on Readmissions, Length of Stay, and Costs: A Matched Case-Control Study Conducted in an Academic Hospital in the Netherlands. Infect Drug Resist. 2020 Sep 30;13:3365-3374. doi: 10.2147/IDR.S264068. PMID: 33061483; PMCID: PMC7533242.
- Rojanapirom S, Danchaivijitr S. Pre-operative shaving and wound infection in appendectomy. J Med Assoc Thai. 1992 Mar;75 Suppl 2:20-3. PMID: 1402495.
- Seropian R, Reynolds BM. Wound infections after preoperative depilatory versus razor preparation. Am J Surg. 1971 Mar;121(3):251-4. doi: 10.1016/0002-9610(71)90199-1. PMID: 5546329.
- Spencer M, Barnden M, Johnson HB, Fauerbach LL, Graham D, Edmiston CE Jr. Perioperative hair removal: A review of best practice and a practice improvement opportunity. J Perioper Pract. 2018 Jun;28(6):159-166. doi: 10.1177/1750458918767592. Epub 2018 May 4. PMID: 29726808.
- Thur de Koos P, McComas B. Shaving versus skin depilatory cream for preoperative skin preparation. A prospective study of wound infection rates. Am J Surg. 1983 Mar;145(3):377-8. doi: 10.1016/0002-9610(83)90205-2. PMID: 6837864.
- VandenBergh MF, Kluytmans JA, van Hout BA, Maat AP, Seerden RJ, McDonnel J, Verbrugh HA. Cost-effectiveness of perioperative mupirocin nasal ointment in cardiothoracic surgery. Infect Control Hosp Epidemiol. 1996 Dec;17(12):786-92. doi: 10.1086/647237. PMID: 8985764.
- World Health Organization. Guidelines for safe surgery. Geneva: World Health Organization; 2009 (http://apps.who.int/iris/bitstream/10665/44185/1/9789241598552_eng.pdf, accessed 24 August 2023).
- World Health Organization. Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. (https://www.who.int/publications/i/item/global-guidelines-for-the-prevention-of-surgical-site-infection-2nd-ed/, accessed 11 July 2023). A
- World Health Organization. Global Guidelines for the Prevention of Surgical Site Infection. Geneva: World Health Organization; 2018. Web Appendix 7, Summary of a systematic review on the effectiveness and optimal method of hair removal. (https://www.ncbi.nlm.nih.gov/books/NBK536407/, accessed 11 July 2023). B
Evidence tables
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
Risk of bias tables
|
Author, year |
Sequence generation |
Allocation concealment |
Participants blinded |
Care providers blinded |
Outcome assessors blinded |
Incomplete outcome data |
Selective outcome reporting |
Other sources of bias |
|
Abouzari, 2009 |
Unclear |
Unclear |
High |
High |
Unclear |
Unclear |
Low |
- |
|
Adisa, 2011 |
Low |
Low |
High |
Low |
Low |
Low |
Low |
- |
|
Alexander, 1983 |
Low |
Unclear |
High |
Unclear |
Unclear |
Low |
Low |
- |
|
Balthazar, 1982 |
Low |
Unclear |
High |
Unclear |
Unclear |
Low |
Low |
- |
|
Celik, 2007 |
Low |
Unclear |
High |
High |
Unclear |
High |
Low |
- |
|
Court-Brown, 1981 |
Unclear |
Unclear |
High |
High |
Unclear |
Unclear |
High |
- |
|
Goëau-Brisonnière, 1987 |
Low |
Unclear |
High |
High |
Unclear |
Unclear |
Unclear |
- |
|
Grober, 2013 |
Unclear |
Unclear |
Low |
High |
Unclear |
Unclear |
Low |
- |
|
Horgan, 1999 |
Unclear |
High |
High |
High |
Unclear |
Low |
Low |
- |
|
Ilankovan, 1992 |
Low |
Unclear |
Low |
High |
Unclear |
Low |
High |
- |
|
Kattipattanapong, 20131 |
Low |
Low |
High |
High |
Unclear |
Low |
Low |
- |
|
Powis, 1976 |
High |
Unclear |
High |
Unclear |
Low |
Low |
Low |
- |
|
Rojanapirom, 1992 |
Unclear |
Unclear |
High |
High |
Unclear |
Low |
Low |
- |
|
Seropian, 1971 |
High |
Unclear |
High |
Unclear |
Unclear |
Low |
High |
- |
|
Thur de Koos, 1983 |
High |
Unclear |
High |
Unclear |
Unclear |
Low |
Unclear |
- |
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 Correction to WHO-guideline, webappendix 7.
Comparisons
In addition to the odds ratios (OR) reported by the WHO, risk ratios (RR) and risk differences (RD) with 95% confidence intervals (CI) were extracted and pooled with a random effects model and included in the current literature analysis.1
1. Hair removal versus no hair removal
1a. Shaving versus no hair removal
Forest plots
Funnel plot

2. Comparison of methods of hair removal
2a. Clipping versus shaving
Forest plots

Funnel plot
2b. Clipping or no hair removal versus shaving
Forest plots
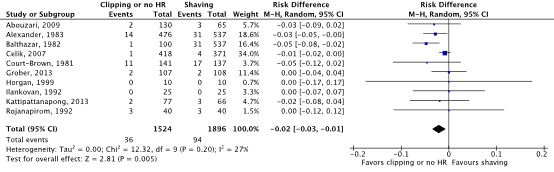
Funnel plot
2c. Depilatory cream versus shaving
Forest plots

Funnel plot

Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 The WHO-guideline does not report risk ratios and risk differences.
GRADE tables
1. Hair removal versus no hair removal
1a. Shaving versus no hair removal
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Shaving |
No hair removal |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
7 |
RCTs |
Seriousa |
Not serious |
Not serious |
Seriousb |
None |
30/714 (4.2%) |
18/776 (2.3%) |
OR 1.78 (0.96 to 3.29)
RR 1.69 (0.95 to 2.98) |
RD 0.010 (-0.001 to 0.021) |
⨁⨁◯◯ LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of selection bias (inadequate allocation concealment), performance bias (lack of blinding of participants/health care providers), and reporting bias (selective outcome reporting).
b 95% confidence interval of the risk ratio crosses the upper boundary of clinical relevance.2
1b. Clipping versus no hair removal
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Clipping |
No hair removal |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
1 |
RCT |
Seriousa |
Not serious |
Not serious |
Very seriousb |
None |
1/65 (1.5%) |
1/65 (1.5%) |
OR 1.00 (0.06 to 16.34)
RR 1.00 (0.06 to 15.65) |
RD 0.000 (-0.042 to 0.042) |
⨁◯◯◯ VERY LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of performance bias (lack of blinding of participants/health care providers).
b 95% confidence interval of the risk ratio crosses both boundaries of clinical relevance.
1c. Depilatory cream versus no hair removal
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Depilatory cream |
No hair removal |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
1 |
RCT |
Seriousa |
Not serious |
Not serious |
Very seriousb |
None |
10/126 (7.9%)3 |
11/141 (7.8%) |
OR 1.02 (0.42 to 2.49)
RR 1.02 (0.45 to 2.31) |
RD 0.001 (-0.063 to 0.066) |
⨁◯◯◯ VERY LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of performance bias (lack of blinding of participants/health care providers) and reporting bias (selective outcome reporting).
b 95% confidence interval of the risk ratio crosses both boundaries of clinical relevance.
2. Comparison of methods of hair removal
2a. Clipping versus shaving.
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Clipping |
Shaving |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
4 |
RCTs |
Seriousa |
Not serious |
Not serious |
Seriousb |
None |
18/748 (2.4%) |
38/810 (4.7%)3 |
OR 0.51 (0.29 to 0.91)
RR 0.52 (0.30 to 0.91) |
RD -0.018 (-0.035 to -0.001) |
⨁⨁◯◯ LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of performance bias (lack of blinding of participants/health care providers).
b 95% confidence interval of the risk ratio crosses the lower boundary of clinical relevance.2
2b. Clipping or no hair removal versus shaving
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Clipping or no hair removal |
Shaving |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
10 |
RCTs |
Seriousa |
Not serious |
Not serious |
Not serious |
None |
36/1,524 (2.4%) |
94/1,896 (5.0%) |
OR 0.51 (0.34 to 0.78)
RR 0.54 (0.36 to 0.80) |
RD -0.020 (-0.035 to -0.006) |
⨁⨁⨁◯ MODERATE
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of selection bias (inadequate allocation concealment), performance bias (lack of blinding of participants/health care providers) and reporting bias (selective outcome reporting).
2c. Depilatory cream versus shaving
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Depilatory cream |
Shaving |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
6 |
RCTs |
Seriousa |
Seriousb |
Not serious |
Seriousc |
None |
23/573 (4.0%) |
80/706 (11.3%) |
OR 0.36 (0.11 to 1.17)
RR 0.39 (0.13 to 1.18) |
RD -0.050 (-0.114 to 0.014) |
⨁⨁⨁◯ VERY LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of selection bias (inadequate sequence generation), performance bias (lack of blinding of participants/health care providers) and reporting bias (selective outcome reporting).
b Inconsistent direction of effect estimates, non-overlapping 95% confidence intervals and a I representing substantial statistical heterogeneity.4
c 95% confidence interval of the risk ratio crosses lower boundary of clinical relevance.
3. The night before surgery versus the day of surgery
|
Outcome |
Quality assessment |
Number of patients |
Effect1 |
Quality |
||||||||
|
Number of studies |
Study design |
Risk of bias |
Inconsistency |
Indirectness |
Imprecision |
Other considerations |
Night before surgery |
Day of surgery |
Relative (95% CI) |
Absolute (95% CI) |
|
|
|
SSI |
1 |
RCT |
Seriousa |
Not serious |
Not serious |
Very seriousb |
None |
Shaving 14/271 (5.2%)
Clipping 10/250 (6.4%) |
Shaving 17/266 (4.0%)
Clipping 4/226 (1.8%) |
Shaving OR 0.80 (0.39 to 1.65)
RR 0.81 (0.41 to 1.61)
Clipping OR 2.31 (0.71 to 7.48)
RR 2.26 (0.72 to 7.11) |
Shaving RD -0.012 (-0.052 to 0.027)
Clipping RD 0.022 (-0.008 to 0.052) |
⨁◯◯◯ VERY LOW
|
|
SSI-attributable mortality |
0 |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
Not applicable |
No GRADE |
CI=confidence interval; OR=odds ratio; RCT=randomized controlled trial; RD=risk difference; RR=risk ratio; SSI=surgical site infection
a Risk of performance bias (lack of blinding of participants/health care providers).
b 95% confidence interval of the risk ratio crosses both boundaries of clinical relevance.
c WHO reported overall data. As effect estimates for shaving and clipping were in opposite directions, the working group decided to report stratified data.
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
1 In addition to the odds ratios reported by WHO, risk ratios and risk differences with 95% confidence intervals were extracted and pooled with a random effects model.
2 Downgrading for imprecision was not based on the WHO-criterium of meeting the optimal information size but on the 95% confidence interval of the risk ratio crossing the boundaries of clinical relevance.
3 Correction to WHO-guideline, webappendix 7.
4 In addition to an I2 representing substantial heterogeneity, as reported by WHO, the working group noted inconsistent directions of effect estimates and non-overlapping 95% confidence intervals.
Study selection
Flow chart of the study selection
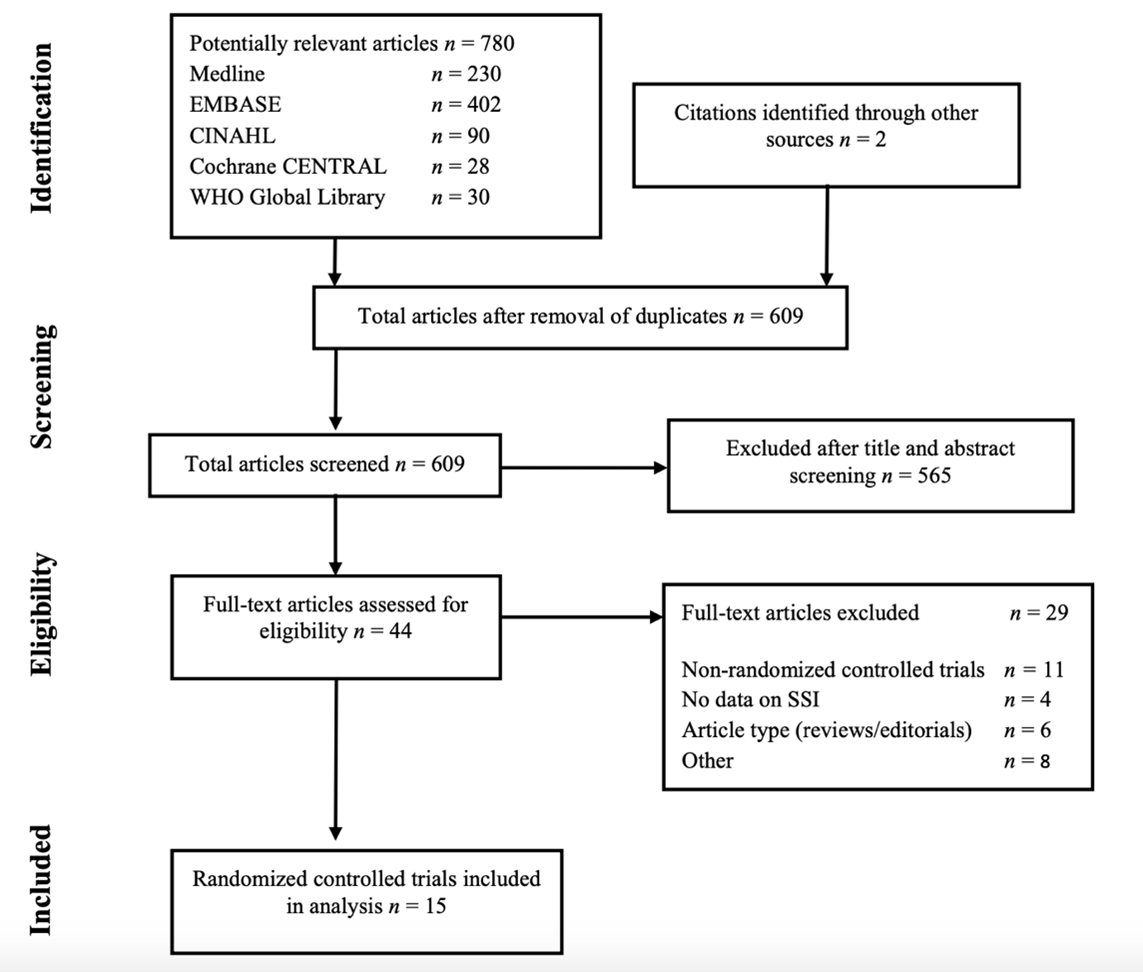
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
Search strategy
Medline
1. surgical wound infection/ or (surgical site infection* or SSI or SSIs or surgical wound infection* or surgical infection* or post-operative wound infection* or postoperative wound infection*).ti,ab,kw.
2. wound infection.mp. or exp wound infection/
3. hair removal/ or (hair remov* or shaving or shave).ti,ab,kw. 4. 1 or 2
5. 3 and 4
8. limit 5 to yr="1900 -current"
EMBASE
1. esthetic surgery/ or (hair remov* or shaving or shave).ti,ab,kw.
2. surgical infection/ or (surgical site infection* or SSI or SSIs or surgical wound infection* or surgical infection* or post-operative wound infection* or postoperative wound infection*).ti,ab,kw.
3. exp wound infection/
4. 2 or 3
5. 1 and 4
6. limit 5 to yr="1990 -current"
CINAHL
1. (MH "wound infection+")
2. (MH "surgical wound infection") 3. ("wound infection")
4. (MH "hair removal")
5. ("hair removal")
6. 1 or 2 or 3
7. 4 or 5
8. 6 and 7
Cochrane CENTRAL
1. wound infection:ti,ab,kw
2. surgical wound infection:ti,ab,kw 3. hair removal:ti,ab,kw
4. shaving:ti,ab,kw
5. 1 or 2
6. 3 or 4
7. 5 and 6
WHO regional medical databases
1. (ssi)
2. (surgical site infection)
3. (surgical site infections)
4. (wound infection)
5. (wound infections)
6. (postoperative wound infection) 7. (hair removal)
8. (shaving)
African Index Medicus
1. infection [Key Word] 2. surgical [Key Word] 3. surgery [Key Word] 4. 2 or 3
5. 1 and 4
ti: title; ab: abstract; kw: key word.
Disclaimer: This is an adaptation of an original work “Global guidelines for the prevention of surgical site infection, second edition. Geneva: World Health Organization; 2018. License: CC BY-NC-SA 3.0 IGO.” (https://www.who.int/publications/i/item/9789241550475). This adaptation was not created by WHO. WHO is not responsible for the content or accuracy of this adaptation. The original edition shall be the binding and authentic edition.
Beoordelingsdatum en geldigheid
Publicatiedatum : 17-12-2024
Beoordeeld op geldigheid : 01-12-2024
Algemene gegevens
De richtlijnontwikkeling is ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten. De SRI-modules zijn gefinancierd door het ministerie van VWS (Ministerie van Volksgezondheid, Welzijn en Sport). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodules 2 tot 16 is in 2020 op initiatief van de NVvH een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor preventie van postoperatieve wondinfecties. Daarnaast is in 2022 op initiatief van het Samenwerkingsverband Richtlijnen Infectiepreventie (SRI) een separate multidisciplinaire werkgroep samengesteld voor de herziening van de WIP-richtlijn over postoperatieve wondinfecties: module 17-22. De ontwikkelde modules van beide werkgroepen zijn in deze richtlijn samengevoegd.
Werkgroep
- Mw. prof. dr. M.A. (Marja) Boermeester, Nederlandse Vereniging voor Heelkunde (NVvH), voorzitter
- Mw. M. (Marloes) van de Biezen - Brinkman, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- Dhr. dr. M. (Michel) Cromheecke, Nederlandse Vereniging voor Plastische Chirurgie (NVPC)
Dhr. dr. J.H.M. (Jon) Goosen, Nederlandse Orthopaedische Vereniging (NOV) - Dhr. dr. N.G. (Nico) Hartwig, Nederlandse Vereniging voor Kindergeneeskunde (NVK)
- Mw. G.M. (Gini) van der Heijden, Verpleegkundigen & Verzorgenden Nederland (V&VN)
- Mw. MSc. E.A. (Elise) van den Helder, Verpleegkundigen & Verzorgenden Nederland (V&VN)
- Dhr. dr. R.R. (Rogier) Jansen, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Mw. dr. E (Etelka) Moll, Nederlandse Vereniging voor Obstetrie en Gynaecologie (NVOG)
- Mw. dr. M.G.H.C. (Marieke) Reinders, Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV)
- Dhr. R.R. (Roald) Schaad, Nederlandse Vereniging voor Anesthesiologie (NVA)
- Mw. drs. K. (Klaartje) Spijkers, Patiëntenfederatie Nederland (PFNL)
- Mw. K.J. (Klaske) Vliegenthart-Jongbloed, Nederlandse Internisten Vereniging (NIV), Nederlandse Vereniging van Internist-Infectiologen (NVII)
Met ondersteuning van
- Mw. dr. H. (Haitske) Graveland, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mw. dr. M.F.Q. (Marjolein) Kluijtmans-van den Bergh, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoek financiering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Mevr. prof. dr. M.A. Boermeester |
Chirurg |
* Medisch Ethische Commissie, Amsterdam UMC, locatie AMC * Antibiotica Commissie, Amsterdam UMC |
Persoonlijke financiële belangen Hieronder staan de beroepsmatige relaties met bedrijfsleven vermeld waarbij eventuele financiële belangen via de AMC Research B.V. lopen, dus institutionele en geen persoonlijke gelden zijn: Skillslab instructeur en/of spreker (consultant) voor KCI/3M, Smith&Nephew, Johnson&Johnson, Gore, BD/Bard, TELABio, GDM, Medtronic, Molnlycke.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Institutionele grants van KCI/3M, Johnson&Johnson en New Compliance.
Intellectuele belangen en reputatie Ik maak me sterk voor een 100% evidence-based benadering van maken van aanbevelingen, volledig transparant en reproduceerbaar. Dat is mijn enige belang in deze, geen persoonlijk gewin.
Overige belangen Geen.
|
Geen restrictie |
|
Dhr. R.R. Schaad |
Anesthesioloog |
Geen |
Geen |
Geen restrictie |
|
Dhr. dr. J.H.M. Goosen |
Orthopedisch Chirurg |
Inhoudelijke presentaties voor Smith&Nephew en Zimmer Biomet. Deze worden vergoed per uur |
Geen |
Geen restrictie |
|
Dhr. dr. N. Hartwig |
Kinderarts-infectioloog |
Freelance: Medisch adviseur Veduma Medisch Advies te Zaltbommel. Betaald per uitgebracht advies
Lid-beroepsgenoten Regionaal Tuchtcollege te Amsterdam Betaald per zitting
Commissies: Commissie-lid: commissie Vaccinaties van de Gezondheidsraad Commissie-lid: commissie Vaccinaties voor werknemers van de Gezondheidsraad Commissie-lid: commissie Vaccinaties COVID-19 van de Gezondheidsraad Betaald: volgens vaccatie-regeling |
Geen |
Geen restrictie |
|
Dhr. Dr. R. Jansen |
Arts Microbioloog |
Geen |
Geen |
Geen restrictie |
|
Mevr. dr. M. Reinders |
Dermatoloog |
Geen |
Geen |
Geen restrictie |
|
Mevr. E. van de Helder-Vreugdenhil, MSc. |
Verpleegkundig specialist Wondzorg |
Geen |
Geen |
Geen restrictie |
|
Mevr. M. van de Biezen-Brinkman |
Deskundige infectiepreventie |
Geen |
Geen |
Geen restrictie |
|
Mevr. dr. K. Vliegenthart |
Internist-infectioloog |
Onbetaald: Commissie Kwaliteit voor de NVII, comissielid ter beoordeling van richtlijnen en ondersteunen van kwaliteitsinitiatieven, tevens notulist Internationaal co-assistenten begeleider (Haydom Lutheran Hospital) Minor Global Health, begeleider voor Tanzania (Erasmus MC) Medisch Team, lid, World Servants |
Geen |
Geen |
|
Mevr. dr. E. Moll |
Gynacoloog-perinatoloog |
MOET cursus docent, onbetaald, wel onkostenvergoeding SAVER cursus docent, onbetaald, wel onkostenvergoeding Lid van werkgroep NVOG, Gynaecoloog en Recht. Vanuit die functie schrijven van expertiserapporten, betaald. |
Geen |
Geen restrictie |
|
Dhr. dr. M. Cromheecke |
Plastisch chirurg |
Geen |
Geen |
Geen restrictie |
|
Mevr. G. v.d. Heijden, MSc. |
Verpleegkundig specialist (wondzorg en vaatchirurgie) |
Geen |
Geen |
Geen restrictie |
|
Mevr. K. Spijkers |
Adviseur Patiëntfederatie Nederland |
Voorzitter Ervaringsraad SKILZ (afgevaardigd Patientenfederatie). Bestuurslid Stichting Revalidatie Impact (afgevaardigd Patientenfederatie). |
Geen |
Geen restrictie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van de Patiëntenfederatie Nederland voor de invitational conference. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptmodules zijn tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt. Voor de modules 17-22 was de patiëntfederatie vertegenwoordigd in de werkgroep.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn.
Voor module 8 (Negatieve druktherapie) geldt dat uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000 - 40.000 patiënten). Tevens volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
Voor de overige modules en aanbevelingen geldt dat uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten). Tevens volgt uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet en het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Ook wordt geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners verwacht of een wijziging in het opleidingsniveau van zorgpersoneel. Er worden daarom geen substantiële financiële gevolgen verwacht.
Methode ontwikkeling
Evidence based
Implementatie
Zie voor de implementatie het implementatieplan in het tabblad 'Bijlagen'.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroepen de knelpunten in de zorg voor patiënten die chirurgie ondergaan. Tevens zijn er knelpunten aangedragen door middel van een invitational conference. De verslagen hiervan zijn opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Adaptatie
Een aantal modules van deze richtlijn betreft een adaptatie van modules van de World Health Organization (WHO)-richtlijn ‘Global guidelines for the prevention of surgical site infection’ (WHO, 2018), te weten:
- Module Normothermie
- Module Immunosuppressive middelen
- Module Glykemische controle
- Module Antimicrobiële afdichtingsmiddelen
- Module Wondbeschermers bij laparotomie
- Module Preoperatief douchen
- Module Preoperatief verwijderen van haar
- Module Chirurgische handschoenen: Vervangen en type handschoenen
- Module Afdekmaterialen en operatiejassen
Methode
- Uitgangsvragen zijn opgesteld in overeenstemming met de standaardprocedures van het Kennisinstituut van de Federatie Medisch Specialisten.
- De inleiding van iedere module betreft een korte uiteenzetting van het knelpunt, waarbij eventuele onduidelijkheid en praktijkvariatie voor de Nederlandse setting wordt beschreven.
- Het literatuuronderzoek is overgenomen uit de WHO-richtlijn. Afhankelijk van de beoordeling van de actualiteit van de richtlijn is een update van het literatuuronderzoek uitgevoerd.
- De samenvatting van de literatuur is overgenomen van de WHO-richtlijn, waarbij door de werkgroep onderscheid is gemaakt tussen ‘cruciale’ en ‘belangrijke’ uitkomsten. Daarnaast zijn door de werkgroep grenzen voor klinische besluitvorming gedefinieerd in overeenstemming met de standaardprocedures van het Kennisinstituut van de Federatie Medisch Specialisten, en is de interpretatie van de bevindingen primair gebaseerd op klinische relevantie van het gevonden effect, niet op statistische significantie. In de meta-analyses zijn naast odds-ratio’s ook relatief risico’s en risicoverschillen gerapporteerd.
- De beoordeling van de mate van bewijskracht is overgnomen van de WHO-richtlijn, waarbij de beoordeling is gecontroleerd op consistentie met de standaardprocedures van het Kennisinstituut van de Federatie Medisch Specialisten (GRADE-methode; http://www.gradeworkinggroup.org/). Eventueel door de WHO gerapporteerde bewijskracht voor observationele studies is niet overgenomen indien ook gerandomiseerde gecontroleerde studies beschikbaar waren.
- De conclusies van de literatuuranalyse zijn geformuleerd in overeenstemming met de standaardprocedures van het Kennisinstituut van de Federatie Medisch Specialisten.
- In de overwegingen heeft de werkgroep voor iedere aanbeveling het bewijs waarop de aanbeveling is gebaseerd en de aanvaardbaarheid en toepasbaarheid van de aanbeveling voor de Nederlandse klinische praktijk beoordeeld. Op basis van deze beoordeling is door de werkgroep besloten welke aanbevelingen ongewijzigd zijn overgenomen, welke aanbevelingen niet zijn overgenomen, en welke aanbevelingen (mits in overeenstemming met het bewijs) zijn aangepast naar de Nederlandse context. ‘De novo’ aanbevelingen zijn gedaan in situaties waarin de werkgroep van mening was dat een aanbeveling nodig was, maar deze niet als zodanig in de WHO-richtlijn was opgenomen. Voor elke aanbeveling is vermeld hoe deze tot stand is gekomen, te weten: ‘WHO’, ‘aangepast van WHO’ of ‘de novo’.
Voor een verdere toelichting op de procedure van adapteren wordt verwezen naar de Bijlage Adapteren.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
World Health Organization. Global guidelines for the prevention of surgical site infection,
second edition. Geneva: World Health Organization; 2018. (https://www.who.int/publications/i/item/9789241550475, accessed 12 June 2023).
Zoekverantwoording
Zie voor de zoekstrategie het tabblad 'Evidence tabellen'.
