Behandeling en preventie van complicaties na poliepectomie
Uitgangsvraag
Welke preventieve maatregelen kunnen het optreden en de ernst van postpoliepectomie complicaties gunstig beïnvloeden en hoe kunnen postpoliepectomie complicaties worden behandeld?
Aanbeveling
Behandel een intraprocedurele bloeding met thermische therapie (snaartip soft coagulatie, coagulatie forceps) of mechanische therapie (clips, endoloop) met of zonder gecombineerd gebruik van adrenaline.
Overweeg endoscopische coagulatie met snaar tip of forceps een intraprocedurele bloeding die tijdens een piecemeal resectie optreedt, omdat gebruik van clips de resterende resectie kunnen bemoeilijken.
Overweeg het gebruik van mechanische profylaxe middels clip(s) of endoloop na resectie van grote gesteelde poliepen ≥ 20 mm, indien voorafgaand aan de resectie alleen preventief adrenaline injectie is gebruikt.
Overweeg het gebruik van mechanische profylaxe middels clip(s) of endoloop na resectie van grote gesteelde poliepen ≥ 20 mm, indien voorafgaand aan de resectie alleen preventief adrenaline injectie is gebruikt.
Bij presentatie van een patiënt met een postprocedurele bloeding wordt in principe een conservatief en ondersteunend beleid geadviseerd. Alleen bij persisterend bloedverlies of niet te stabiliseren hemodynamiek wordt een re-interventie aanbevolen. Als eerste keus re-interventie in gestabiliseerde patiënt wordt een coloscopie geadviseerd.
Bij noodzakelijke interventie in het geval van een postprocedurele bloeding wordt forceps coagulatie of mechanische therapie met of zonder gecombineerd gebruik van adrenaline geadviseerd in geval van actieve bloeding of andere high-risk stigmata.
Het gebruik van contact thermische probes (Gold ProbeTM) wordt afgeraden gezien het risico op transmurale schade.
Overweeg bij EMR toevoeging van indigokarmijn of methyleenblauw aan de injectievloeistof om het demarqueren van de laesie te vergemakkelijken. Daarnaast kan het resectievlak beter te worden op eventuele diepe schade van de wand.
Inspecteer EMR resectievlak nauwkeurig om tekenen of risicofactoren voor perforatie zoals bij een vastgesteld “target sign” te herkennen en dit defect direct te sluiten met clips.
Overweeg het endoscopisch sluiten van een perforatie in gereinigde darm indien deze direct of binnen 4 uur herkend wordt. Dit is afhankelijk van type, grootte en lokale expertise. Het eventueel wisselen naar CO2, het afzuigen van darminhoud en eventueel decompressie van spanning pneumoperitoneum moet hierbij verricht worden.
Maak bij klinische verdenking op een late perforatie een CT-scan (eventueel met oraal en/of rectaal contrast) om geen diagnostisch delay op te lopen.
Bij verdenking op een postpoliepectomie syndroom wordt aanbevolen om laagdrempelig een CT-scan met eventueel oraal en/of rectaal contrast te maken om differentiatie met perforatie adequaat te maken, en geen diagnostisch delay op te lopen.
Overwegingen
Literatuur omtrent de preventie en behandeling van complicaties na poliepectomie is beperkt. Bloeding en perforatie na poliepectomie zijn relatief zeldzame complicaties en daardoor is er weinig prospectief vergelijkend onderzoek beschikbaar ten aanzien van eventuele superioriteit van een specifieke behandeling of te volgen beleid. Veel adviezen en aanbevelingen zijn dan ook vaak gebaseerd op “low tot moderate quality evidence” en met name gebaseerd op ervaring en expert opinion. De “strong recommendations” in de internationale richtlijnen (ESGE, BSG) zijn dan ook vaak gebaseerd op consensus van de verschillende ervaringsdeskundigen. De onderstaande aanbevelingen van de werkgroep sluiten daar grotendeels bij aan.
Onderbouwing
Achtergrond
Poliepectomie van het colon reduceert de incidentie en mortaliteit van het colorectaal carcinoom, maar is geassocieerd met mogelijke complicaties zoals bloeding, perforatie en postpoliepectomie syndroom. Het risico op complicaties bij endoscopische verwijdering van poliepen neemt toe naarmate de grootte en complexiteit van de verwijderde poliepen toeneemt. Complicaties/adverse events van poliepectomie dienen te worden geregistreerd in de DRCE (Dutch Registration of Complications in Endoscopy). Overigens is niet iedere onbedoelde gebeurtenis een complicatie of adverse event. Alleen als een onbedoelde gebeurtenis tijdens het zorgproces leidt tot een onbedoelde uitkomst (schade voor de patiënt, zodanig ernstig dat aanpassing van het (be)handelen noodzakelijk is dan wel dat sprake is van onherstelbare schade) is sprake van een complicatie of adverse event. Er is sprake van een incident/event of near miss indien een onbedoelde gebeurtenis niet leidt tot het voortijdig beëindigen van de procedure en/of tot aanpassing van het beleid (Wagner, 2005; Cotton, 2010). Voorbeelden van incidenten zijn een intraprocedurele bloeding die spontaan of met endoscopische therapie tot stand komt en niet heeft geleid tot aanpassing van het beleid of een near-perforatie die tijdens de scopie wordt behandeld met clips zonder dat het beleid peri procedureel voor de patiënt wordt aangepast (bijv. geen antibiotica, geen opname en geen nieuwe geplande interventie omdat procedure niet compleet is volbracht). Incidenten/events worden niet geregistreerd in de DRCE.
- Adverse event: Een onbedoelde uitkomst die is ontstaan door het (niet) handelen van een zorgverlener en/of door het zorgsysteem met schade voor de patiënt, zodanig ernstig dat er sprake is van tijdelijke of permanente beperking, verlenging of verzwaring van de behandeling dan wel overlijden van de patiënt.
- Complicatie: Een onbedoelde en ongewenste uitkomst tijdens of volgend op het handelen van een zorgverlener, die voor de gezondheid van de patiënt zodanig nadelig is dat aanpassing van het (be)handelen noodzakelijk is dan wel dat sprake is van onherstelbare schade.
- Incident = event: Een onbedoelde gebeurtenis tijdens het zorgproces die tot schade aan de patiënt heeft geleid, had kunnen leiden of (nog) kan leiden.
- Near miss: Een onbedoelde gebeurtenis die a. voor de patiënt geen nadelen oplevert omdat de gevolgen ervan op tijd zijn onderkend en gecorrigeerd, of b. waarvan de gevolgen niet van invloed zijn op het fysiek, psychisch of sociaal functioneren van de patiënt.
Conclusies / Summary of Findings
|
No GRADE |
Mechanische profylaxe middels clip(s) of endoloop lijkt superieur aan alleen adrenaline injectie bij gesteelde poliepen ≥ 20 mm.
Bronnen: Paspatis, 2006; Kouklakis, 2009 |
|
No GRADE |
Er is onvoldoende bewijs voor het routinematig preventief dichtclippen van het postpoliepectomie defect ter preventie van een postprocedurele bloeding.
Bronnen: Shioji, 2003; Parikh, 2013 |
|
No GRADE |
Het preventief coaguleren van niet-bloedende vaten in het resectievlak na poliepectomie is niet effectief in het voorkomen van een postprocedurele bloeding.
Bronnen: Bahin, 2014 |
|
No GRADE |
Een postprocedurele bloeding vereist in de meeste gevallen geen endoscopische re-interventie en kan meestal conservatief worden behandeld.
Bronnen: Sonnenberg, 2012; Burgess, 2014 |
|
No GRADE |
Een (dreigende) perforatie met partiële of diepe schade aan de muscularis propria kan worden geïdentificeerd door herkenning van het zogenaamd “target sign”. Door dit defect direct te sluiten met clips kan een late perforatie met fecale peritonitis en noodzaak tot chirurgische interventie worden voorkomen.
Bronnen: Swan, 2011; Burgess, 2017 |
|
No GRADE |
Het vroeg endoscopisch sluiten van een “target sign” of perforatie < 20 mm, door gebruik van TTS (Through-The-Scope) clips of OTS (Over-The-Scope) clips laat goede technische en klinische succes percentages zien van respectievelijk 93% en 89%.
Bronnen: Paspatis, 2014; Magdeburg, 2008; Byeon, 2013 |
|
No GRADE |
In geval van technisch gefaald (incompleet) endoscopisch sluiten van een perforatie en in geval van klinische achteruitgang van de patiënt is klinische opname en chirurgische consultatie geïndiceerd.
Bronnen: Paspatis, 2014 |
Samenvatting literatuur
Bloeding
Er bestaat in de literatuur geen consensus over de definitie van een postpoliepectomie bloeding. Omdat deze richtlijn als basis de Europese (ESGE) richtlijn “Colorectal polypectomy and EMR” gebruikt, worden in deze richtlijn dezelfde definities gebruikt, waarbij onderscheid wordt gemaakt tussen een intraprocedurele (directe) en een postprocedurele (late) poliepectomie bloeding:
- Intraprocedurele bloeding (IPB) is een bloeding die optreedt gedurende de procedure en langer dan 60 seconden persisteert of endoscopische interventie behoeft.
- Postprocedurele bloeding (PPB) is een bloeding die optreedt na de procedure, tot 30 dagen postpoliepectomie en resulteert in een niet gepland SEH bezoek, klinische opname of re-interventie (re-scopie, angiografie of chirurgie).
Intraprocedurele bloeding (IPB)
Risicofactoren
Gerapporteerde incidentie van IPB varieert van 2,8% in standaard poliepectomie tot 11,8% in patiënten die EMR ondergaan voor vlakke of sessiele poliepen > 20 mm en is zelden klinisch relevant. Een IBP is dan ook meestal geen complicatie, maar eerder een event of near miss. Risicofactoren voor IPB zijn grootte, morfologie (gesteeld en Paris 0-IIa+Is), (tubulo)villeuze histologie en laag volume endoscopisten (Kim, 2006; Burgess, 2014). Intraprocedurele bloeding is ook geassocieerd met late bloeding (OR 2,16) en met recidief (RR 1,7) (Burgess, 2014).
Behandeling
Literatuur ten aanzien van de effectiviteit en veiligheid van beschikbare technieken ter verkrijging van intraprocedurele hemostase zijn nauwelijks beschikbaar. IPB kan mechanisch worden behandeld met clips, of thermisch met een coagulatie forceps (SOFT COAG TM op 80 W Effect 5, ERBE) of met snaartip soft coagulatie(STSC) (SOFT COAG TM op 80 W Effect 4, ERBE). In een groot prospectief cohortonderzoek verricht in een tertiair verwijscentrum in Australië bleek snaar tip soft coagulatie (STSC) voor IPB in EMR voor poliepen > 20 mm effectieve hemostase te leveren in 40 van de 44 gevallen (91%). Er was geen verschil in optreden van late bloedingen of complicaties in vergelijking met de groep zonder IBP (Fahrtash-Bahin, 2013). Adrenaline-injectie (1:10000 of 1:20000) kan gebruikt worden om beter overzicht te krijgen over de acute bloeding maar zal bij voorkeur gecombineerd moeten worden met een tweede mechanische of thermische hemostatische modaliteit om een late postprocedurele bloeding te voorkomen (Dobrowolski, 2004). In het geval van een bloeding tijdens piecemeal resectie kunnen clips het completeren van de resterende resectie in de weg staan en wordt in het algemeen thermische coagulatie aanbevolen.
Preventie bij gesteelde poliepen
Na een poliepectomie van gesteelde poliepen bestaat er een verhoogd risico op een bloeding wanneer de diameter van de steel groter is dan 5 mm of de kop > 20 mm (Dobrowolski, 2006). Het is echter onbekend vanaf welke diameter van steel en/of grootte van de kop er preventieve maatregelen getroffen dienen te worden om een bloeding te voorkomen. Zowel mechanische hemostase door endoloop of clips als injectie van de steel met 1:10000 adrenaline zijn effectief gebleken voor preventie van een (na)bloeding voor gesteelde poliepen > 10 mm, maar vooral voor poliepen > 20 mm. De kans op een (na)bloeding voor poliepen > 20 mm was ongeveer gelijk met preventief endoloop gebruik of gebruik van adrenaline (2,7% respectievelijk 2,9%) versus 15,1% in de controlegroep in een gerandomiseerde studie (Di Giorgio, 2004). Voor poliepen > 20 mm is mechanische profylaxe middels endoloop of clips mogelijk superieur aan alleen adrenaline-injectie. Twee RCT’s laten een significante afname zien in (na)bloeding als mechanische profylaxe wordt gebruikt, alleen of in combinatie met adrenaline, in vergelijking met alleen adrenaline gebruik (Paspatis, 2006; Kouklakis, 2009).
Postprocedurele bloeding (PPB)
Risicofactoren
Een postprocedurele (ofwel late) bloeding komt minder vaak voor dan een IPB, maar kan significante gevolgen hebben voor de patiënt inclusief heropname, re-interventie en bloedtransfusie. De incidentie van PPB varieert van 0,3 tot 2%, maar kan oplopen tot meer dan 10% in hoog risico groepen. Veel (overwegend retrospectief) onderzoek is gedaan naar risicofactoren voor PPB met wisselende en soms inconsistente conclusies, onderzoek blijkt uitdagend gezien de lage incidentie in algemene praktijk en tevens ontbreken van uniforme definities. Consistente risicofactoren voor PPB zijn onder te verdelen in poliep gerelateerde factoren, patiënt gerelateerde factoren en endoscopist gerelateerde factoren. Consistente poliep gerelateerde factoren zijn voornamelijk grootte en rechtszijdige locatie met in het bijzonder het coecum (Buddingh, 2011; Consolo, 2008; Heldwein, 2005; Kim, 2013; Sawhney, 2008). Er is een direct verband tussen poliepgrootte en het risico op PPB in vrijwel alle studies. In een meta-analyse werd een 3.4 maal verhoogd risico gezien op PPB in poliepen vanaf 10 mm (Jaruvongvanich, 2017). Poliepgrootte van > 40 mm werd als major risicofactor (OR= 43.0) geïdentificeerd in een studie naar 493 poliepectomieën (Kim, 2012). In een studie naar 167208 poliepectomieën in het Engelse darmkanker screeningsprogramma kwam eveneens grootte > 40 mm (OR 3.9) als sterke risicofactor naar voren (Rutter, 2014). Een Australische studie liet zien dat rechtszijdige locatie een belangrijke risicofactor was voor PPB (OR =4.4) met hoogste incidentie in het coecum (Metz, 2011). Dezelfde resultaten liet een retrospectieve analyse zien waarbij rechtszijdige locatie een 5 maal verhoogd risico gaf op PPB (OR=4.7) met in univariate analyse locatie in het coecum als hoogste risicofactor (OR= 13.8) (Buddingh, 2011). Consistente patiënt gerelateerde risicofactoren zijn voornamelijk thienopyridine (clopidogrel en prasugrel) en anticoagulantia gebruik en hypertensie (OR=1,5). In een meta-analyse kwam een significant verhoogd risico (RR= 4,66) op PPB naar voren bij gecontinueerd clopidogrel gebruik (Gandhi, 2013). In een andere studie was het risico op PPB driemaal hoger (3,5% versus 1%) in de clopidogrel groep (Singh, 2010). Van de endoscopist gerelateerde factoren kwam poliepectomie uitgevoerd door laagvolume endoscopisten (ongeveer < 300 coloscopieën/jaar) ook als risicofactor naar voren in meerdere studies (Rabeneck, 2008; Singh, 2009). Ook het niet gebruiken van een microprocessor gecontroleerde stroom (Endocut), leidt tot een significant verhoogd risico op PPB (OR 2.03) in een prospectief onderzoek bij EMR > 20 mm (Fahrtash-Bahin, 2013).
Preventie
Het profylactisch sluiten van resectievlak in ongeselecteerde poliepen < 10 mm blijkt ineffectief in reduceren van kans op PPB (Shioji, 2003). In een ongecontroleerde retrospectieve studie in 524 ongeselecteerde poliepen > 20 mm blijkt clippen effectief in het reduceren van PPB van 9,7% naar 1,8%.(27) Een meta-analyse en kosteneffectiviteitsanalyse tonen dat het profylactisch clippen in poliepen > 10 mm alleen kosteneffectief kan zijn in patiënten die plaatjesremmers of anticoagulantia gebruiken (Parikh, 2013). Toekomstig gerandomiseerd onderzoek is noodzakelijk om over de (kosten)effectiviteit van profylactisch clippen een sterke aanbeveling te kunnen doen.
Het routinematig preventief zichtbare niet-bloedende vaten in EMR vlak coaguleren na grote EMR (> 20 mm) is niet effectief gebleken in het reduceren van PPB in een prospectief gerandomiseerd onderzoek in 347 patiënten. Opvallend was tevens in dit onderzoek dat de meeste en grootste bloedvaten zichtbaar waren na resectie in het distale colon, maar dat de meeste PPB proximaal waren gelokaliseerd (OR 3,1) (Bahin, 2014).
Behandeling
Niet elke PPB vereist endoscopische re-interventie. Adviezen ten aanzien van het te voeren beleid voor patiënten met een PPB zijn voornamelijk gebaseerd op expert opinion. In een “decision model” werd berekend dat een endoscopische re-interventie voor het identificeren en behandelen van een PPB slechts nuttig is in 22% van de patiënten, wat een NNT betekent van 4,5 (Sonnenberg, 2012) In een multicenter, prospectief onderzoek naar 1039 EMR’s voor poliepen > 20 mm bleek PPB voor te komen in 62 patiënten (6%). 34 patiënten konden conservatief worden behandeld (55%). In 21 van de 27 patiënten (44%) die een re-interventie nodig hadden, werd endoscopische therapie toegepast (Burgess, 2014). Een uit deze data voortgekomen algoritme voor het beleid ten aanzien van PPB is hieronder bijgesloten. De optimale techniek voor het verkrijgen van hemostase is niet goed bepaald in beschikbare literatuur en is afhankelijk van kenmerken van de laesie, voorkeur van de endoscopist en beschikbare devices. Meest gangbaar is het gebruik van clips of coagulatie forceps met of zonder het gecombineerd gebruik van adrenaline (Burgess, 2015: Metz, 2011; Parra-Blanco, 2000; Paspatis, 2008;). Voorzichtigheid wordt in het algemeen geadviseerd voor het gebruik van thermische modaliteiten omdat coagulatie het weefsel verder kan beschadigen met risico op transmurale schade (Metz, 2011). Over het gebruik van hemostatisch poeder (Hemospray, Endoclot et cetera) als primaire behandeling of “salvage” therapie bij PPB is weinig beschikbare literatuur voorhanden. Meeste data komen van case reports en kleine retrospectieve en prospectieve case series waarbij onmiddellijk succespercentages van 88 tot 100% worden genoemd met recidief boedingspercentages van 3 tot 13%. Alhoewel mogelijk een aantrekkelijk alternatief in lastig te controleren bloedingen is toekomstig gerandomiseerd onderzoek noodzakelijk om plaats te kunnen bepalen van hemostatisch poeder ten opzichte van conventionele hemostatische therapie (Mourad, 2018).
Figuur 1 Behandelingsalgoritme voor postprocedurele bloeding na poliepectomie* (Burgess, 2014)
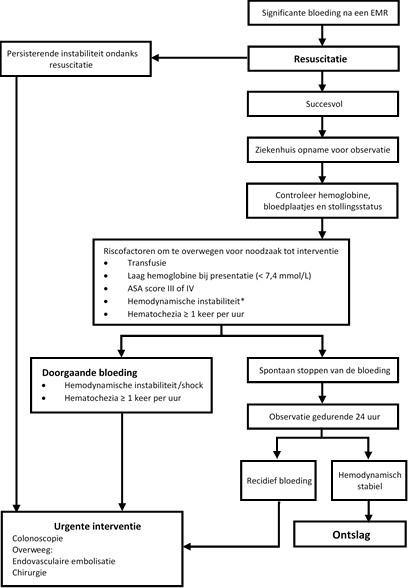
Hemodynamische instabiliteit wordt gedefinieerd als polsslag ≥ 100/min, systolische bloeddruk (SBP) ≤ 100 mm Hg, of orthostatische verlaging in SBP ≥20 mm Hg
* figuur gebruikt met toestemming van de uitgever
Tips and Tricks
- Een waterpomp is essentieel om exacte locatie van bloeding vast te stellen. Bijkomend voordeel: waterpomp infiltreert ook de submucosa wat een tamponnerend effect geeft. Gebruik van een transparante korte cap kan behulpzaam zijn, onder andere door lokale compressie van de cap, waardoor beter overzicht verkregen kan worden over de exacte bloedingsplaats.
- Snaartip soft coagulatie (kleine vaatjes): laat tip van de snaar 2 tot 3 mm uit de sheath steken. Raak met de tip voorzichtig de bloedingsplek aan en gebruik soft coagulatie (SOFT COAG TM op 80 W Effect 4, ERBE).
- Coagulation forceps (vaten ≥ 0,5 mm): pak het vat met de forceps (Coagrasper, Olympus, Tokyo, Japan) vast en tent deze voorzichtig weg van het resectievlak. Geef kort 1 tot 3 pulsen van een halve seconde met soft coagulatie (SOFT COAG TM op 80 W Effect 5, ERBE)
- Gebruik het effect van de zwaartekracht en dus positiewisseling van patiënt om bloed van resectievlak af te houden om beter overzicht te krijgen over exacte locatie van bloeding.
Perforatie
Preventie
Perforatie is de meest zeldzame en meest gevreesde complicatie van endoscopische resectie. Het risico op perforatie bij poliepectomie in algemene praktijk varieert van 0,2 tot 1,1% (Heldwein, 2005; Panteris, 2009; Singh, 2009), maar incidentie kan oplopen tot 1,5% in resectie van poliepen ≥ 20 mm (Hassan, 2015). Adviezen ten aanzien van diagnose en management van iatrogene colonperforaties zijn in deze richtlijn gebaseerd op het in 2014 uitgebrachte “ESGE position statement diagnosis and management of iatrogenic endoscopic perforations” (Paspatis, 2015). Het is van groot belang dat een (dreigende) perforatie tijdig wordt herkend gedurende de procedure om de potentieel ernstige gevolgen van een late perforatie met fecale peritonitis en noodzaak tot chirurgische interventie te voorkomen. Risicofactoren voor diepe schade aan de muscularis propria zijn locatie in het colon transversum, en bloc resectie van sessiele of vlakke laesies ≥ 25 mm en histologisch hooggradige dysplasie of submucosaal invasief carcinoom (Burgess, 2017). Nauwkeurige inspectie van het post EMR resectievlak is een essentieel onderdeel van poliepectomie waarbij beschadiging van de muscularis propria tijdig herkend kan worden en preventief behandeld kan worden met clips (Swan, 2011). Door toevoeging van een blauwe kleurstof aan de submucosale injectievloeistof (indigokarmijn of methyleenblauw) kan partiële of diepe schade aan de muscularis propria worden herkend als het zogenaamd “target sign”, te herkennen als een witte schijf in de blauwe submucosa aan de onderkant van het gereseceerde specimen of als een concentrische witte ring in het blauwe post EMR resectievlak. In een grote retrospectieve analyse uit Australië naar 911 sessiele en vlakke poliepen ≥ 20 mm werd in 3% een target sign gevonden en in alle gevallen direct succesvol geclipt. In slechts 0,2% in deze serie trad een klinisch significante perforatie op (klinische tekenen van peritonitis met noodzaak chirurgische interventie) (Burgess, 2017).
Behandeling
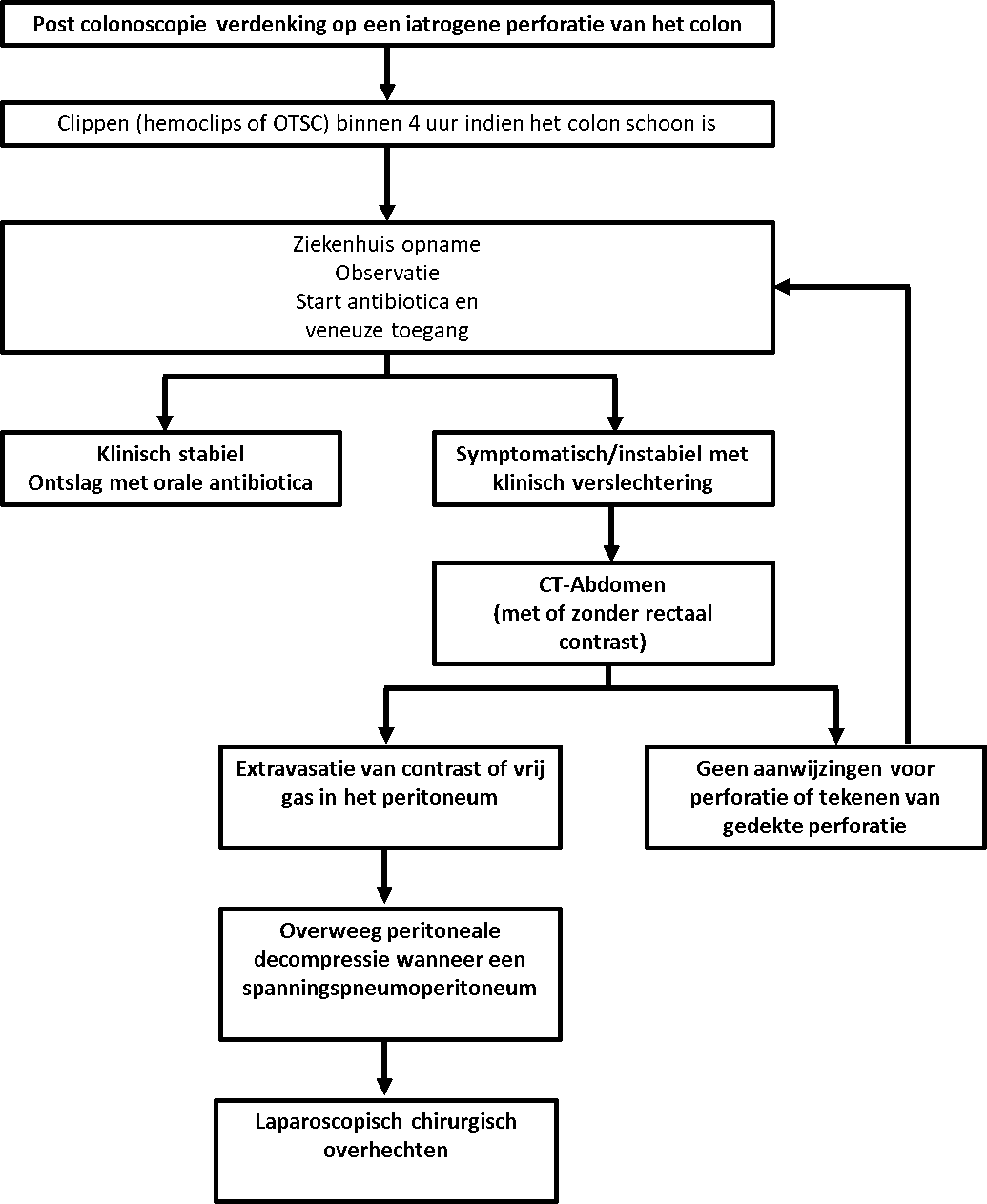
Vrij lucht intra-abdominaal is een klassieke bevinding bij iatrogene colonperforatie maar hoeft niet tot klinisch significante peritonitis te leiden, tenzij er tevens sprake is van vrij vocht (darminhoud). Het herkennen van een perforatie kan direct procedureel zijn, maar kan ook laat optreden tot 3 dagen postprocedureel, in dat laatste geval is meestal sprake van een fecale peritonitis en is chirurgische interventie geïndiceerd. Alleen een direct of vroeg gediagnostiseerde perforatie kan eventueel conservatief worden behandeld door endoscopische sluiten van de perforatie met clips, gebruik van CO2, afzuigen van darminhoud en antibiotica (Bassan, 2013; La Torre, 2012). Aanbevelingen ten aanzien van de manier waarop en welke perforaties endoscopisch gesloten kunnen worden is voornamelijk gebaseerd op case series. Het vroeg endoscopisch sluiten van perforaties kleiner dan 20 mm door TTS clips of OTSC laat technische en klinische succespercentages zien van respectievelijk 93% en 89% (Byeon, 2013). Het gebruik van TTS (Through-The-Scope) clips lijkt meer effectief voor het sluiten van perforaties < 10 mm, terwijl OTSC (Over-The-Scope-Clip) mogelijk meer geschikt is voor diagnostische (scoop-) perforaties of grotere perforaties (Jovanovic, 2011; Magdeburg, 2013). Het falen van endoscopisch sluiten van een perforatie met fecale peritonitis is een harde indicatie voor chirurgie.
Figuur 2 Behandeling algoritme (Panteris, 2009)
Tips and Tricks
Perforatie
Geen paniek, een perforatie is nooit direct levensbedreigend, check gebruik van CO2, minimaliseer insufflatie en controleer eventueel aanwezigheid van een spanning pneumoperitoneum. Vraag altijd een collega endoscopist erbij om te reflecteren. Bij twijfel: verwijder de endoscoop, start iv antibiotica en maak rustig een plan. Belangrijke vragen zijn:
- Kan deze perforatie endoscopisch worden gesloten of is chirurgie geïndiceerd?
- Is er een andere onderliggende reden om chirurgie te prefereren (carcinoom, polyposis et cetera)?
- Zijn de juiste materialen beschikbaar? (TTS clips/OTSC)?
- Is voldoende expertise beschikbaar?
Decompressie spanning pneumoperitoneum
Positioneer patiënt in rugligging, hoofdeinde plat. Overweeg de maag te desuffleren met een neus-maagsonde. Pas handhygiëne toe en desinfecteer de huid van het abdominaal linker boven kwadrant. Gebruik bij voorkeur een dikke (16G) infuusnaald (grijze Venflon) met een 20 cc spuit welke 10 CC NaCl bevat. Prik de infuusnaald circa 20 tot 30 mm subcostaal links in de midclaviculair lijn (Palmer’s point) in een hoek van circa 90° al aspirerend door de huid en subcutis heen tot in de peritoneaal holte waarbij men lucht/CO2 aspireert. Trek vervolgens de opvoernaald (met spuit) terug en schuif de canule volledig op. Sluit vervolgens de spuit halfgevuld met NaCl aan op de canule en verwijder de zuiger van de spuit. De ontsnapte lucht/CO2 geeft een zogenaamd “jacuzzi” effect. Verwijder de canule zodra er geen lucht/CO2 meer ontsnapt.
Postprocedurele buikpijn en postpoliepectomie syndroom (PPS)
Pijn na poliepectomie/EMR is gerelateerd aan distentie van het colon. Koolstofdioxide (CO2) wordt bij voorkeur gebruikt als insufflatie gas omdat het postprocedurele pijn significant verlaagt en kans op spanning pneumoperitoneum in geval van perforatie verkleint (Bassan, 2013). Het postpoliepectomie syndroom (PPS), ook bekend als postpoliepectomie coagulatie syndroom of transmural burn syndrome wordt gedefinieerd als serositis veroorzaakt door poliepectomie met elektrocoagulatie in afwezigheid van perforatie (vrij lucht intra/retroperitoneaal op beeldvorming). PPS wordt gekenmerkt door lokale pijn en peritonitis, koorts en verhoogde infectie parameters optredend 1 tot 5 dagen postpoliepectomie en is zonder aanvullend beeldvormend onderzoek niet goed te onderscheiden van een perforatie. Incidentie varieert sterk van 0,5% tot 2,8%. PPS heeft een uitstekende prognose met conservatief beleid (Cha, 2013; Waye, 1996).
Referenties
- Bahin, F. F., Naidoo, M., Williams, S. J., Hourigan, L. F., Ormonde, D. G., Raftopoulos, S. C.,... & Bourke, M. J. (2015). Prophylactic endoscopic coagulation to prevent bleeding after wide-field endoscopic mucosal resection of large sessile colon polyps. Clinical Gastroenterology and Hepatology, 13(4), 724-730.
- Bassan, M. S., Holt, B., Moss, A., Williams, S. J., Sonson, R., & Bourke, M. J. (2013). Carbon dioxide insufflation reduces number of postprocedure admissions after endoscopic resection of large colonic lesions: a prospective cohort study. Gastrointestinal endoscopy, 77(1), 90-95.
- Buddingh, T. K., Herngreen, T., Haringsma, J., Van Der Zwet, W. C., Vleggaar, F. P., Breumelhof, R., & Ter Borg, F. (2011). Location in the right hemi-colon is an independent risk factor for delayed post-polypectomy hemorrhage: a multi-center case–control study. Official journal of the American College of Gastroenterology| ACG, 106(6), 1119-1124.
- Burgess, N. G., Metz, A. J., Williams, S. J., Singh, R., Tam, W., Hourigan, L. F.,... & Bourke, M.J. (2014). Risk factors for intraprocedural and clinically significant delayed bleeding after wide-field endoscopic mucosal resection of large colonic lesions. Clinical Gastroenterology and Hepatology, 12(4), 651-661.
- Burgess, N. G., Williams, S. J., Hourigan, L. F., Brown, G. J., Zanati, S. A., Singh, R.,... & Bourke, M. J. (2014). A management algorithm based on delayed bleeding after wide-field endoscopic mucosal resection of large colonic lesions. Clinical Gastroenterology and Hepatology, 12(9), 1525-1533.
- Burgess, N. G., Bahin, F. F., & Bourke, M. J. (2015). Colonic polypectomy (with videos). Gastrointestinal endoscopy, 81(4), 813-835.
- Burgess, N. G., Bassan, M. S., McLeod, D., Williams, S. J., Byth, K., & Bourke, M. J. (2017). Deep mural injury and perforation after colonic endoscopic mucosal resection: a new classification and analysis of risk factors. Gut, 66(10), 1779-1789.
- Byeon, J. S. (2013). Colonic perforation: can we manage it endoscopically?. Clinical endoscopy, 46(5), 495.
- Cha, J. M., Lim, K. S., Lee, S. H., Joo, Y. E., Hong, S. P., Kim, T. I.,... & Shin, J. E. (2013). Clinical outcomes and risk factors of post-polypectomy coagulation syndrome: A multicenter, retrospective, case–control study. Endoscopy, 45(03), 202-207.
- Consolo, P., Luigiano, C., Strangio, G., Scaffidi, M. G., Giacobbe, G., Di Giuseppe, G.,... & Familiari, L. (2008). Efficacy, risk factors and complications of endoscopic polypectomy: ten year experience at a single center. World journal of gastroenterology: WJG, 14(15), 2364.
- Cotton, P. B., Eisen, G. M., Aabakken, L., Baron, T. H., Hutter, M. M., Jacobson, B. C.,... & Vargo, J. J. (2010). A lexicon for endoscopic adverse events: report of an ASGE workshop. Gastrointestinal endoscopy, 71(3), 446-454.
- Di Giorgio, P., De Luca, L., Calcagno, G., Rivellini, G., Mandato, M., & De Luca, B. (2004).Detachable snare versus epinephrine injection in the prevention of postpolypectomy bleeding: a randomized and controlled study. Endoscopy, 36(10), 860-863.
- Dobrowolski, S., Dobosz, M., Babicki, A., Dymecki, D., & Hać, S. (2004). Prophylactic submucosal saline–adrenaline injection in colonoscopic polypectomy: prospective randomized study. Surgical endoscopy, 18(6), 990-993.
- Dobrowolski, S., Dobosz, M., Babicki, A., Głowacki, J., & Nałęcz, A. (2006). Blood supply of colorectal polyps correlates with risk of bleeding after colonoscopic polypectomy. Gastrointestinal endoscopy, 63(7), 1004-1009.
- Fahrtash-Bahin, F., Holt, B. A., Jayasekeran, V., Williams, S. J., Sonson, R., & Bourke, M. J. (2013). Snare tip soft coagulation achieves effective and safe endoscopic hemostasis during wide-field endoscopic resection of large colonic lesions (with videos). Gastrointestinal endoscopy, 78(1), 158-163.
- Ferlitsch, M., Moss, A., Hassan, C., Bhandari, P., Dumonceau, J. M., Paspatis, G.,... & Bourke, M. J. (2017). Colorectal polypectomy and endoscopic mucosal resection (EMR): European Society of Gastrointestinal Endoscopy (ESGE) clinical guideline. Endoscopy, 49(03), 270-297.
- Gandhi, S., Narula, N., Mosleh, W., Marshall, J. K., & Farkouh, M. (2013). Meta‐analysis: colonoscopic post‐polypectomy bleeding in patients on continued clopidogrel therapy. Alimentary pharmacology & therapeutics, 37(10), 947-952.
- Hassan, C., Repici, A., Sharma, P., Correale, L., Zullo, A., Bretthauer, M.,... & Rex, D. K. (2016). Efficacy and safety of endoscopic resection of large colorectal polyps: a systematic review and meta-analysis. Gut, 65(5), 806-820.
- Heldwein, W., Dollhopf, M., Rösch, T., Meining, A., Schmidtsdorff, G., Hasford, J.,... & Schmitt, W. (2005). The Munich Polypectomy Study (MUPS): prospective analysis of complications and risk factors in 4000 colonic snare polypectomies. Endoscopy, 37(11), 1116-1122.
- Jaruvongvanich, V., Prasitlumkum, N., Assavapongpaiboon, B., Suchartlikitwong, S., Sanguankeo, A., & Upala, S. (2017). Risk factors for delayed colonic post-polypectomy bleeding: a systematic review and meta-analysis. International journal of colorectal disease, 32(10), 1399-1406.
- Jovanovic, I., Zimmermann, L., Fry, L. C., & Mönkemüller, K. (2011). Feasibility of endoscopic closure of an iatrogenic colon perforation occurring during colonoscopy. Gastrointestinal endoscopy, 73(3), 550-555.
- Kim, H. S., Kim, T. I., Kim, W. H., Kim, Y. H., Kim, H. J., Yang, S. K.,... & Song, J. S. (2006). Risk Factors for Immediate Postpolypectomy Bleeding of the Colon: A Multicenter Study: CME. Official journal of the American College of Gastroenterology| ACG, 101(6), 1333-1341.
- Kim, H. H., Kim, J. H., Park, S. J., Park, M. I., & Moon, W. (2012). Risk factors for incomplete resection and complications in endoscopic mucosal resection for lateral spreading tumors. Digestive Endoscopy, 24(4), 259-266.
- Kim, J. H., Lee, H. J., Ahn, J. W., Cheung, D. Y., Kim, J. I., Park, S. H., & Kim, J. K. (2013). Risk factors for delayed post‐polypectomy hemorrhage: a case‐control study. Journal of gastroenterology and hepatology, 28(4), 645-649.
- Kouklakis, G., Mpoumponaris, A., Gatopoulou, A., Efraimidou, E., Manolas, K., & Lirantzopoulos, N. (2009). Endoscopic resection of large pedunculated colonic polyps and risk of postpolypectomy bleeding with adrenaline injection versus endoloop and hemoclip: a prospective, randomized study. Surgical endoscopy, 23(12), 2732-2737.
- La Torre, M., Velluti, F., Giuliani, G., Di Giulio, E., Ziparo, V., & La Torre, F. (2012). Promptness of diagnosis is the main prognostic factor after colonoscopic perforation. Colorectal Disease, 14(1), e23-e26.
- Magdeburg, R., Collet, P., Post, S., & Kaehler, G. (2008). Endoclipping of iatrogenic colonic perforation to avoid surgery. Surgical endoscopy, 22(6), 1500-1504.
- Magdeburg, R., Sold, M., Post, S., & Kaehler, G. (2013). Differences in the endoscopic closure of colonic perforation due to diagnostic or therapeutic colonoscopy. Scandinavian journal of gastroenterology, 48(7), 862-867.
- Metz, A. J., Bourke, M. J., Moss, A., Williams, S. J., Swan, M. P., & Byth, K. (2011). Factors that predict bleeding following endoscopic mucosal resection of large colonic lesions. Endoscopy, 43(06), 506-511.
- Mourad, F. H., & Leong, R. W. (2018). Role of hemostatic powders in the management of lower gastrointestinal bleeding: A review. Journal of gastroenterology and hepatology, 33(8), 1445-1453.
- Panteris, V., Haringsma, J., & Kuipers, E. J. (2009). Colonoscopy perforation rate, mechanisms and outcome: from diagnostic to therapeutic colonoscopy. Endoscopy, 41(11), 941-951.
- Parikh, N. D., Zanocco, K., Keswani, R. N., & Gawron, A. J. (2013). A cost-efficacy decision analysis of prophylactic clip placement after endoscopic removal of large polyps. Clinical Gastroenterology and Hepatology, 11(10), 1319-1324.
- Parra-Blanco, A., Kaminaga, N., Kojima, T., Endo, Y., Uragami, N., Okawa, N.,... & Fujita, R. (2000). Hemoclipping for postpolypectomy and postbiopsy colonic bleeding. Gastrointestinal endoscopy, 51(1), 37-41.
- Paspatis, G. A., Paraskeva, K., Theodoropoulou, A., Mathou, N., Vardas, E., Oustamanolakis,.,... & Karagiannis, I. (2006). A prospective, randomized comparison of adrenaline injection in combination with detachable snare versus adrenaline injection alone in the prevention of postpolypectomy bleeding in large colonic polyps: CME. Official journal of the American College of Gastroenterology| ACG, 101(12), 2805-2809.
- Paspatis, G. A., Vardas, E., Theodoropoulou, A., Manolaraki, M. M., Charoniti, I., Papanikolaou, N.,... & Chlouverakis, G. (2008). Complications of colonoscopy in a large public county hospital in Greece. A 10-year study. Digestive and Liver Disease, 40(12), 951-957.
- Paspatis, G. A., Dumonceau, J. M., Barthet, M., Meisner, S., Repici, A., Saunders, B. P.,... & Hassan, C. (2014). Diagnosis and management of iatrogenic endoscopic perforations: European Society of Gastrointestinal Endoscopy (ESGE) Position Statement. Endoscopy, 46(08), 693-711.
- Rabeneck, L., Paszat, L. F., Hilsden, R. J., Saskin, R., Leddin, D., Grunfeld, E.,... & Stukel, T. A. (2008). Bleeding and perforation after outpatient colonoscopy and their risk factors in usual clinical practice. Gastroenterology, 135(6), 1899-1906.
- Rutter, M. D., Nickerson, C., Rees, C. J., Patnick, J., & Blanks, R. G. (2014). Risk factors for adverse events related to polypectomy in the English Bowel Cancer Screening Programme. Endoscopy, 46(02), 90-97.
- Sawhney, M. S., Salfiti, N., Nelson, D. B., Lederle, F. A., & Bond, J. H. (2008). Risk factors for severe delayed postpolypectomy bleeding. Endoscopy, 40(02), 115-119.
- Shioji, K., Suzuki, Y., Kobayashi, M., Nakamura, A., Azumaya, M., Takeuchi, M.,... & Narisawa, R. (2003). Prophylactic clip application does not decrease delayed bleeding after colonoscopic polypectomy. Gastrointestinal endoscopy, 57(6), 691-694.
- Singh, H., Penfold, R. B., DeCoster, C., Kaita, L., Proulx, C., Taylor, G.,... & Moffatt, M. (2009). Colonoscopy and its complications across a Canadian regional health authority. Gastrointestinal endoscopy, 69(3), 665-671.
- Singh, M., Mehta, N., Murthy, U. K., Kaul, V., Arif, A., & Newman, N. (2010). Postpolypectomy bleeding in patients undergoing colonoscopy on uninterrupted clopidogrel therapy. Gastrointestinal endoscopy, 71(6), 998-1005.
- Sonnenberg, A. (2012). Management of delayed postpolypectomy bleeding: a decision analysis. Official journal of the American College of Gastroenterology| ACG, 107(3), 339-342.
- Swan, M. P., Bourke, M. J., Moss, A., Williams, S. J., Hopper, A., & Metz, A. (2011). The target sign: an endoscopic marker for the resection of the muscularis propria and potential perforation during colonic endoscopic mucosal resection. Gastrointestinal endoscopy, 73(1), 79-85.
- Wagner, C., & Wal, V. D. G. (2005). Voor een goed begrip: bevordering patiëntveiligheid vraagt om heldere definitie.
- Waye, J. D., Kahn, O., & Auerbach, M. E. (1996). Complications of colonoscopy and flexible sigmoidoscopy. Gastrointestinal endoscopy clinics of North America, 6(2), 343-377.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-02-2022
Beoordeeld op geldigheid : 02-02-2022
Uiterlijk in 2026 bepaalt het bestuur van de NVMDL of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVMDL is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
De voorliggende richtlijn betreft een herziening van de NVMDL richtlijn Endoscopische poliepectomie van het colon uit 2019. Alle modules zijn beoordeeld op actualiteit. Vervolgens is een prioritering aangebracht welke modules een daadwerkelijke update zouden moeten krijgen. Hieronder staan de modules genoemd met de wijzigingen. Tevens is per module een inschatting gemaakt voor de beoordeling voor herziening.
|
Uitgangsvraag/onderwerpen |
Wijzigingen richtlijn 2021 |
Uiterlijk jaar voor herziening |
|
Randvoorwaarden voor poliepectomie |
Minimale (tekstuele) aanpassingen |
2026 |
|
Minuscule poliepen ≤ 5 mm en poliepen tussen 10 en 20 mm |
Minimale (tekstuele) aanpassingen |
2026 |
|
Poliepen 6 – 9 mm |
Gereviseerd |
2026 |
|
Sessiele en vlakke poliepen > 20 mm |
Gereviseerd |
2026 |
|
Herkenning van een potentieel maligne poliep |
Gereviseerd |
2026 |
|
Verwijdering van een potentieel maligne poliep |
Wordt behandeld in de CRC richtlijn |
- |
|
Behandeling en preventie van complicaties |
Minimale (tekstuele) aanpassingen |
2026 |
|
Preventief dichtclippen van wondvlak |
Nieuw ontwikkeld |
2026 |
|
Lokaal recidief na poliepectomie |
Gereviseerd |
2026 |
|
Behandeling van lokaal recidief |
Nieuw ontwikkeld |
2026 |
|
Pathologie: biopteren |
Nieuw ontwikkeld |
2026 |
|
Pathologie: weefselverwerking |
Minimale (tekstuele) aanpassingen |
2026 |
|
Prestatie indicatoren |
Minimale (tekstuele) aanpassingen |
2026 |
Belangrijkste wijzigingen ten opzichte van vorige versie
In de gereviseerde modules is de literatuur opnieuw systematisch gezocht en/of is de literatuursamenvatting aangepast. De strekking van de aanbevelingen is nagenoeg hetzelfde gebleven. Tevens zijn er drie nieuwe modules aan de richtlijn toegevoegd. De overige modules zijn opnieuw beoordeeld waarbij er minimale (tekstuele) aanpassingen gedaan. De module 'Verwijderen van een potentieel maligne poliep' is teruggetrokken. Dit onderwerp komt terug in de richtlijn Colorectaal carcinoom.
Algemene gegevens
De ontwikkeling en herziening van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in het voorjaar van 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die direct betrokken zijn bij de zorg voor patiënten met poliepen in het rectum en colon.
Werkgroep
- Dr. L.M.G. (Leon) Moons (voorzitter), MDL-arts UMC Utrecht, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. T. (Tom) Seerden (vice-voorzitter), MDL-arts Amphia Breda, Nederlandse Vereniging van Maag-Darm-Leverartsen
- B.A.J. (Barbara) Bastiaansen, MDL-arts Amsterdam UMC, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. J.J. (Jurjen) Boonstra, MDL-arts, LUMC Leiden, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. A.D. (Arjun) Koch, MDL-arts, Erasmus MC Rotterdam, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. B.W.M. (Marcel) Spanier, MDL-arts, Rijnstate ziekenhuis, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. Y. (Yara) Backes, MDL-arts i.o., Meander Medisch Centrum Amersfoort, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. L. (Lindsey) Oudijk, patholoog Erasmus MC Rotterdam, Nederlandse Vereniging voor Pathologie
- Dr. M.M. (Miangela) Laclé, patholoog UMC Utrecht, Nederlandse Vereniging voor Pathologie
- C. (Christiaan) Hoff, chirurg Medisch Centrum Leeuwarden, Nederlandse Vereniging voor Heelkunde
- R. (Ruud) Blankenburgh, Internist-Oncoloog Saxenburgh Hardenberg, Nederlandse Internisten Vereniging
Klankbordgroep
- J.J. (Jan) Meeuse, NIV
- S. (Silvie) Dronkers, Stichting Darmkanker
- J. (Jannie) Verheij - van der Wiel, Stomavereniging
- J.H.M.A. (Ans) Dietvorst, Stichting Lynch Polyposis
Met ondersteuning van
- Dr. A.N. (Anh Nhi) Nguyen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Dr. E.V. (Ekaterina) van Dorp-Baranova, adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Restrictie (zie ook tekst onder de tabel) |
|
Moons (voorzitter) |
MDL-arts, interventie endoscopist, UMC Utrecht, Utrecht, Nederland |
Geen |
Consultant Boston Scientific |
Geen |
|
Seerden (vice-voorzitter) |
MDL arts, Medisch specialistisch bedrijf Amphia te Breda |
Geen |
Geen |
Geen |
|
Bastiaansen |
MDL-arts Amsterdam UMC |
Geen |
Geen |
Geen |
|
Boonstra |
MDL-arts, LUMC, Leiden |
Geen |
Consultant Boston Scientific |
Geen |
|
Koch |
MDL-arts, Erasmus MC, Universitair Medisch Centrum Rotterdam |
Geen |
Consultant Boston Scientific. Pentax Medical, ERBE Elektromedizin, DrFalk Pharma |
Geen |
|
Spanier |
Als vrijgevestigd MDL-arts in dienst bij Cooperatie Medisch Specialisten Rijnstate u.a. (CMSR) |
Bestuurslid CMSR, 4 dagdelen, betaald, vergoeding naar vakgroep MDL Rijnstate |
Geen |
Geen |
|
Backes |
aios MDL, Meander Medisch Centrum Amersfoort |
Geen |
Geen |
Geen |
|
Oudijk |
Patholoog, Erasmus MC Rotterdam |
PPM patholoog Palga: Motiveren gebruik PALGA protocollen, contactpersoon voor PALGA rapportage gebruik protocollen, mede-pathologen en MDO-leden, clinici. Onbetaald. Lid wetenschappelijke commissie Dutch Thyroid Cancer Group: onbetaald. Lid wetenschappelijke adviescommissie Stichting Bijniernetwerk Nederland: onbetaald |
Geen |
Geen |
|
Laclé |
Patholoog UMC Utrecht |
Geen |
Geen |
Geen |
|
Hoff |
Chirurg Medisch Centrum Leeuwarden (via Heelkunde Friesland Groep) (0,6) medisch cobestuurder MCL 0,4) |
Geen |
Geen |
Geen |
|
Blankenburgh |
Internist-Oncoloog, Saxenburgh te Hardenberg |
Geen |
Geen |
Geen |
Het Kennisinstituut in zijn rol als methodologisch ondersteuner, de NVMDL als initiërende vereniging en de richtlijnwerkgroep zijn zich bewust van de belangen die spelen binnen de richtlijnwerkgroep, maar het werd toch noodzakelijk geacht om de betreffende inhoudelijk experts op dit gebied bij de richtlijn te betrekken. Tijdens de commentaarfase werd de NVMDL verzocht om bij het aanleveren van commentaar kritisch te zijn op de gemelde belangen en geformuleerde aanbevelingen en onderbouwing en om experts, vrij van belangen, expliciet te verzoeken om de richtlijn te beoordelen.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden vanuit patiëntenverenigingen in de klankbordgroep met de conceptrichtlijn mee te laten lezen. De commentaren zijn besproken in de werkgroep en verwerkt. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland, Stichting Darmkanker, Stomavereniging en Stichting Lynch Polyposis.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijnmodules en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden in de bijlagen. De werkgroep heeft ook interne kwaliteitsindicatoren ontwikkeld.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijn (Nederlandse Vereniging van Maag-Darm-Leverartsen, 2019) op noodzaak tot revisie. Op basis van de geprioriteerde knelpunten zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, en bijkomende aspecten van de organisatie van zorg worden behandeld in de module Randvoorwaarden.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html
Zoekverantwoording
("Endoscopic Mucosal Resection"(Mesh) OR "Colonic Polyps"(Mesh) OR polypectom*(tiab) OR p-EMR(tiab) OR piecemeal EMR(tiab) OR endoscopic mucosal resection*(tiab) OR therapeutic colonoscopy(tiab) OR endoscopic resection(tiab))
AND
("Colon"(Mesh) OR "Rectum"(Mesh) OR colon*(tiab) OR rectum(tiab) OR colorectum(tiab) OR rectal(tiab) OR colorectal(tiab))
AND
("Postoperative Complications"(Mesh) OR "Hemostasis, Endoscopic"(Mesh) OR "Hemorrhage"(Mesh) OR "Intestinal Perforation"(Mesh) OR "Abdominal Pain"(Mesh) OR "Serositis"(Mesh) OR hemorrhage*(tiab) OR haemorrhage*(tiab) OR bleeding*(tiab) OR perforat*(tiab) OR target sign(tiab) OR complication*(tiab) OR postpolypectom*(tiab) OR post-polypectom*(tiab) OR transmural burn syndrome*(tiab) OR serositis(tiab))
