Remifentanil vs Epidurale analgesie, Pethidine of Tramadol
Uitgangsvraag
Wat is de plaats van remifentanil vergeleken met epiduraal, pethidine of tramadol bij zwangere vrouwen met het verzoek tot behandelen van de baringspijn?
Aanbeveling
Geef de voorkeur aan epidurale analgesie boven remifentanil en pethidine bij zwangeren met een verzoek om medicamenteuze pijnbehandeling tijdens de baring.
Geef de voorkeur aan remifentanil boven pethidine wanneer epidurale analgesie niet mogelijk is.
Overwegingen
De onderstaande overwegingen gelden in principe voor de gehele patiëntenpopulatie zoals geformuleerd in de uitgangsvraag.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Epidurale analgesie is superieur aan remifentanil waar het de effectiviteit van pijnbehandeling en patiënttevredenheid (gerapporteerd door middel van een AUC-waarde) ten aanzien van de pijnstilling betreft. Daarnaast is de cross-over naar andere vormen van pijnbehandeling significant hoger bij gebruik van remifentanil versus epidurale analgesie.
Remifentanil lijkt een goed alternatief in specifieke situaties, bijvoorbeeld in geval van een falende epidurale analgesie of onmogelijkheid tot het prikken van een epiduraal (medisch of logistiek), en heeft zeker de voorkeur boven pethidine. Tevens lijkt remifentanil naar mening van de werkgroep een goed alternatief voor zwangeren die naar verwachting slechts een korte periode van pijnbehandeling nodig hebben. Hierbij kan gedacht worden aan multiparae met al ver gevorderde ontsluiting.
Voor welke groepen zwangeren remifentanil de voorkeur zou kunnen hebben boven epidurale analgesie, onder andere ook in het kader van de tevredenheid, zou onderwerp voor verder onderzoek moeten zijn.
Potentieel nadelige effecten van epidurale analgesie zijn een hoger risico op maternale koorts. De belangrijkste nadelige effecten van maternale koorts zijn een verhoogde kans op opname van de neonaat voor antibiotische behandeling, omdat er differentiaal diagnostisch altijd gedacht moet worden aan een intra-uteriene infectie als oorzaak voor de koorts bij moeder.
Remifentanil geeft meer saturatiedalingen dan epidurale analgesie. Het is onzeker of er sprake is van meer respiratoire insufficiëntie. Echter, dit is een weinig voorkomende complicatie die zeer waarschijnlijk ondergerapporteerd wordt, maar wel ernstige consequenties kan hebben. Om deze reden was een doseringsadvies onderdeel van de in 2014 uitgebrachte SOP. Echter, deze komt na aanname van deze richtlijn te vervallen. De timing en hoogte van de bolusdosering, het wel of niet geven van achtergrondinfusie en de lock out time zijn van invloed op het risico op optreden van respiratoire insufficientie. Er zijn aanwijzingen dat het geven van achtergrond infusie risico op apnoe en saturatiedalingen vergroot. (Logtenberg, 2019) Het alleen geven van een bolus lijkt even effectieve pijnstilling te geven als de combinatie met achtergrond infusie, maar juist bij achtergrondinfusie is de kans op respiratoire complicaties groter (Blair, 2001). Bij een inventarisatie van de “serious adverse events” bij remifentanil gebruik in Nederland werden 6 casus van apnoe gerapporteerd, waarbij in 5 gevallen achtergrond infusie werd gegeven (Logtenberg 2019). Daarnaast is er een vijftal case reports van ernstige maternale morbiditeit bij remifentanil gebruik, waarbij in 3 gevallen achtergrondinfusie werd gegeven (O’Kinney, 2012; Waring, 2007; Aaronson, 2017). De werkgroep adviseert remifentanil PCA toe te passen in bolusvorm zonder achtergrondinfusie. Als bolusdosis wordt 30 microgram geadviseerd met een lockout tijd van 3 minuten. Bij een bolus dosis van 30 microgram was de tevredenheid gelijk aan een bolus van 40 microgram met minder respiratoire bijwerkingen (Melber 2019). Verder is de voorwaarde dat zwangeren die remifentanil krijgen intensief gemonitord worden (zie voorbeeldmodel).
Hoewel het onzeker is of remifentanil betere pijnstilling geeft dan pethidine, geeft het wel een hogere mate van tevredenheid en minder cross-over naar andere vormen van pijnbehndeling, en heeft derhalve de voorkeur.
Uit de meta-analyse komt geen duidelijk verschil in misselijkheid en braken tussen pethidine en remifentanil. De studie van Wilson (2018) is hier echter niet in meegenomen, deze rapporteert niet misselijkheid en braken, maar wel het anti-emetica gebruik in beide groepen, waarbij er in de pethidine groep significant meer anti-emetica worden voorgeschreven dan in de remifentanil groep (68% versus 21%, RR 0,31, 95% BI 2,23 tot 0,41, p<0.0001).
Voor de vergelijking remifentanil en tramadol is er geen literatuur beschikbaar. Er kan derhalve geen conclusie met betrekking tot de cruciale en belangrijke uitkomstmaten worden getrokken. Derhalve zullen er ook geen aanbevelingen gedaan worden. Hier ligt een kennislacune.
Waarden en voorkeuren van patiënten
Een belangrijke voorwaarde voor het gebruik zowel epidurale analgesie als remifentanil is dat de zwangere vrouw adequaat geïnformeerd wordt over de voor- en nadelen en mogelijke risico’s van beide methoden.
Het zelf toedienen van remifentanil met behulp van een pomp, het gevoel van controle en regie wordt als een belangrijk voordeel voor de bevallende vrouw ervaren. Echter, met de toepassing van PCEA komt dit argument deels te vervallen.
Daarnaast wordt de procedure rondom remifentanil door veel zwangeren ervaren als minder invasief. Anderzijds wordt de sedatie die bij remifentanil optreedt door een aantal zwangeren als onprettig ervaren. Het verdient aanbeveling de remifentanil te stoppen bij de start van de uitdrijving, vanwege het sedatieve effect dat remifentanil heeft.
In de meldactie van de Patiëntenfederatie geven zwangere vrouwen net zo vaak aan de wens voor een epidurale analgesie te hebben als remifentanil. Dit terwijl een hoger percentage zwangeren uiteindelijk de epidurale analgesie krijgt. Echter, de epidurale analgesie werd vaker besproken dan remifentanil (92% versus 65%) in de voorlichting. Het verschil in voorlichting kan mogelijk verklaard worden door het feit dat niet overal remifentanil beschikbaar is, en dit laatste kan ook voor een deel verklaren waarom minder zwangeren daadwerkelijk remifentanil krijgen tijdens de bevalling. Een andere reden voor het feit dat er vaker toch epidurale analgesie wordt gegeven kan zijn dat de overwegingen van de zwangere tijdens de zwangerschap anders kunnen zijn dan op het moment van de daadwerkelijke bevalling. Deze veranderde overwegingen ingegeven door de omstandigheden tijdens de bevalling kunnen ertoe leiden dat er vaker gekozen wordt voor epidurale analgesie in plaats van voor remifentanil. Overigens kan dit fenomeen zich ook andersom voordoen. Het lijkt daarom extra belangrijk alle mogelijke opties te bespreken met de zwangere. Zwangere vrouwen willen al tijdens de zwangerschap informatie over de verschillende vormen van pijnbehandeling, de voor- en de nadelen en wat dit betekent in hun situatie en willen hierover samen beslissen. Uit de meldactie blijkt dat dit nog onvoldoende in de praktijk gebeurt en vastgelegd wordt. Zie voor wijze van counselen en de vergelijking van de verschillende opties de module ‘Counseling: Samen beslissen‘.
Kosten (middelenbeslag)
Epidurale analgesie lijkt duurder dan parenterale opioïden in het algemeen. Er is 1 studie die gekeken heeft naar kosten van epidurale analgesie versus parenteraal toegediende opioïden (dus niet alleen pethidine/remifentanil) (Macario, 2000). Extra kosten voor zwangeren die epidurale analgesie kregen werden berekend op basis van literatuuronderzoek naar complicaties en extra kosten die gemaakt werden voor betrokkenheid van een anesthesioloog. De resultaten toonden totaal extra kosten van $338 ($228 voor betrokkenheid van de anesthesioloog en $118 voor behandeling van complicaties). Of deze cijfers op de Nederlandse situatie van toepassing zijn is de vraag aangezien de betrokkenheid van anesthesioloog berekend wordt op een lager bedrag. Data van de RAVEL-trial laten geen verschil in kosten van pijnstilling inclusief betrokkenheid van de anesthesioloog zien, tussen de groep zwangeren die gerandomiseerd was voor remifentanil versus epidurale analgesie (Freeman, 2018). In deze studie werden echter ook zwangeren die geen pijnstilling hadden meegenomen. Vanuit economisch perspectief is er dan ook geen voorkeur voor remifentanil of epidurale analgesie en wordt aanbevolen voor de meest effectieve pijnbehandeling te kiezen als eerste keuze.
Aanvaardbaarheid voor de overige relevante stakeholders
Het aanbieden van epidurale analgesie vereist betrokkenheid en beschikbaarheid van een anesthesioloog. Hoewel formeel de aanbeveling is om in alle ziekenhuizen 24/7 deze mogelijkheid beschikbaar te hebben, lukt dit in de praktijk niet altijd mede vanwege andere spoedingrepen op het OK complex waarbij de betrokkenheid van de anesthesioloog vereist is. Voor het aanbieden van remifentanil moet aan de bewakingsvoorwaarden zoals geformuleerd voldaan kunnen worden (zie de module ‘Monitoring van moeder en kind’). Hiervoor is één-op-één begeleiding door een geschoolde zorgverlener ten minste in het eerste uur een vereiste. Daarnaast is aandacht voor scholing van belang (Convenant Medische Technologie, 2016).
Haalbaarheid en implementatie
De werkgroep is van mening dat epidurale analgesie beschikbaar moet zijn voor alle barende vrouwen die dat willen, 7 dagen per week 24 uur per dag. Dit houdt in dat in alle centra waar zwangeren bevallen 24/7 een anesthesioloog beschikbaar moet zijn voor het plaatsen van een epiduraal als de vrouw dat wenst. Dit vraagt voldoende formatie van alle betrokken zorgverleners. Daarnaast is er een groep zwangeren met een verzoek om pijnbehandeling die geen epidurale analgesie meer krijgen doordat de bevalling te vlot vordert. De studies van Howell (2000) en Logtenberg (2016) onderschrijven dat. In deze studies kreeg een aanzienlijk percentage zwangeren, welke gerandomiseerd was voor epidurale analgesie geen pijnstilling meer ondanks een verzoek daarom. Ook is er een groep zwangeren die om verscheidene redenen (bijvoorbeeld stollingsstoornissen) geen epidurale analgesie kan krijgen, het is belangrijk om deze zwangeren een alternatief te kunnen bieden.
Op grond van de tevredenheid heeft voor deze groep zwangeren remifentanil de voorkeur boven pethidine.
Vanzelfsprekend is goede voorlichting aan de zwangere over voor- en nadelen van de beschikbare methoden van pijnbehandeling een vereiste. Een voorwaarde voor het gebruik van remifentanil is adequate maternale bewaking. De maternale bewakingsmethode bij de epidurale analgesie is gestandaardiseerd geregeld.
Zoals eerder beschreven kan het indicatiegebied voor remifentanil wellicht uitgebreid worden, echter dan zijn de eisen voor maternale bewaking en gepast gebruik remifentanil wel een voorwaarde (zie de modules ‘Monitoring van moeder en kind’ en ‘Voorbeeldmodel bij gebruik remifentanil’).
Aanbeveling-1
Rationale/ balans tussen voor- en nadelen van de interventie
Het superieure effect van epidurale analgesie ten opzichte van remifentanil op de pijnintensiteit lijkt over het algemeen aanwezig met een lagere cross-over naar andere pijnmedicatie. Daarbij lijken de ongewenste effecten weinig ernstig of zeldzaam te zijn. Op basis hiervan wordt door de werkgroep ingeschat dat de gewenste effecten de ongewenste effecten van epidurale analgesie ten opzichte van remifentanil overstijgen, indien er een wens en indicatie is voor epidurale analgesie.
Aanbeveling-2
Rationale/ balans tussen voor- en nadelen van de interventie
In een aantal gevallen bestaat er een absolute of relatieve contra-indicatie voor het geven van epidurale analgesie. Ook kan er een ongewenste vertraging zijn in de beschikbaarheid van epidurale anesthesie of is er onvoldoende of geen effect van epidurale anesthesie. In al deze gevallen kan het wenselijk zijn een alternatieve vorm van pijnstilling aan te grijpen. Remifentanil lijkt dan een logischer keuze dan pethidine, daar pethidine veel meer een sedatief dan een pijnstillend effect heeft.
Onderbouwing
Hoewel epidurale analgesie de gouden standaard is voor het behandelen van baringspijn kunnen er redenen zijn om alternatieve medicamenteuze methoden toe te passen. Bijvoorbeeld logistieke redenen, voorkeur van de barende vrouw of zorgverleners of het bestaan van een contra-indicatie voor epidurale analgesie. Er is grote praktijkvariatie in het gebruik van opioïden tijdens de baring. De vraag is hoe de effectiviteit, de tevredenheid en de veiligheid van de epiduraal, pethidine en tramadol zich verhoudt tot die van remifentanil. Remifentanil is een lichte vorm van sedatie, voor aanbevelingen ten aanzien van sedatie zie de NVA richtlijn sedatie.
Remifentanil versus epidurale analgesie
|
Laag GRADE |
Epidurale analgesie lijkt een grotere mate van pijnstilling te geven op 1 uur en 2 uur na start analgesie tijdens de baring in vergelijking tot behandeling met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Redelijk GRADE |
Epidurale analgesie geeft gemiddeld over de gehele baring een grotere mate van pijnstilling in vergelijking tot behandeling met remifentanil PCA.
Bronnen: (Logtenberg, 2016; Freeman, 2015) |
|
Redelijk GRADE |
Behandeling met epidurale analgesie tijdens de baring geeft waarschijnlijk een lagere cross-over naar andere pijnmedicatie in vergelijking tot behandeling met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Laag GRADE |
Er lijkt geen verschil in tevredenheid ten aanzien van pijnstilling wanneer gemeten op verschillende tijdspunten na start analgesie of direct na de baring tussen zwangeren behandeld met epidurale analgesie in vergelijking tot behandeling met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Redelijk GRADE |
Epidurale analgesie geeft gemiddeld over de gehele baring wanneer gemeten als AUC-waarde een klinisch relevante grotere mate van tevredenheid in vergelijking tot behandeling met remifentanil PCA.
Bronnen: (Logtenberg, 2016; Freeman, 2015) |
|
Redelijk GRADE |
Er is waarschijnlijk geen verschil in het risico op een sectio caesarea tussen zwangeren behandeld met epidurale analgesie en zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Laag GRADE |
Er lijkt geen verschil in het risico op een vaginale kunstverlossing tussen zwangeren behandeld met epidurale analgesie en zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Redelijk GRADE |
Behandeling met remifentanil PCA geeft waarschijnlijk een hoger risico op desaturatie tijdens de baring in vergelijking tot behandeling met epidurale analgesie.
Bronnen: (Weibel, 2017, Logtenberg, 2016) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in de incidentie van ademhalingsdepressie (gedefinieerd als < 9 en/of < 8 ademhalingen/min) tijdens de baring bij behandeling met remifentanil PCA in vergelijking tot behandeling met epidurale analgesie.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in de incidentie van hypotensie tijdens de baring bij behandeling met remifentanil PCA in vergelijking tot behandeling met epidurale analgesie.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Zwangeren behandeld met remifentanil PCA tijdens de baring lijken een lager risico op temperatuurverhoging te hebben in vergelijking tot zwangeren behandeld met epidurale analgesie. Het is onzeker of dit verschil een klinisch relevant verschil reflecteert.
Bronnen: (Logtenberg, 2016; Douma, 2015; Evron, 2008) |
|
Laag GRADE |
Zwangeren behandeld met epidurale analgesie tijdens de baring lijken een lager risico op misselijkheid en braken te hebben in vergelijking tot zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Laag GRADE |
Er lijkt geen verschil in het risico op jeuk tussen zwangeren behandeld met epidurale analgesie en zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Laag GRADE |
Er lijkt geen verschil in het risico op een Apgarscore < 7 bij 5 minuten tussen neonaten van zwangeren behandeld met epidurale analgesie en neonaten van zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op foetale CTG-afwijkingen van zwangeren behandeld met remifentanil PCA in vergelijking tot neonaten van zwangeren behandeld met epidurale analgesie.
Bronnen: (Weibel, 2017) |
|
GRADE |
Er lijkt geen (klinisch of patiënt relevant) verschil in pH. a. umbilicalis tussen zwangeren behandeld met epidurale analgesie en zwangeren behandeld met remifentanil PCA.
Bronnen: (Weibel, 2017) |
Remifentanil versus pethidine
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in pijnintensiteit tijdens de baring bij behandeling met remifentanil PCA in vergelijking tot behandeling met pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017; Günes, 2014) |
|
Redelijk GRADE |
Behandeling met remifentanil PCA tijdens de baring geeft waarschijnlijk een klinisch relevante lagere cross-over naar andere pijnmedicatie in vergelijking tot behandeling met pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Laag GRADE |
Remifentanil PCA lijkt een klinisch relevante grotere mate van tevredenheid ten aanzien van de pijnstilling te geven in vergelijking tot behandeling met pethidine IM
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het starten van borstvoeding na behandeling met remifentanil PCA in vergelijking tot behandeling met pethidine IM.
Bronnen: (Wilson, 2018) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op een sectio caesarea tussen zwangeren behandeld met remifentanil PCA en zwangeren behandeld met pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Laag GRADE |
Zwangeren behandeld met remifentanil lijken een lager risico op vaginale kunstverlossing te hebben in vergelijking tot zwangeren behandeld met pethidine IM. Het is onzeker of dit verschil een klinisch relevant verschil reflecteert.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in ademhalingsdepressie tussen zwangeren behandeld met remifentanil PCA en zwangeren behandeld met pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Redelijk GRADE |
Remifentanil PCA geeft waarschijnlijk een groter risico op zuurstofdesaturatie (gedefinieerd als PO2 < 94% of < 95%) in vergelijking tot pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op hypotensie tussen zwangeren behandeld met remifentanil PCA en zwangeren behandeld met pethidine IM, de bijwerking hypotensie kwam in beide groepen niet voor in de onderzochte literatuur.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op misselijkheid, braken en jeuk tussen zwangeren behandeld met remifentanil PCA en zwangeren behandeld met pethidine IM.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op een Apgarscore < 7 bij 5 minuten bij neonaten van zwangeren behandeld met remifentanil PCA en neonaten van zwangeren behandeld met pethidine IM.
Bronnen: (Wilson, 2018; Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het risico op foetale CTG-afwijkingen tussen zwangeren behandeld met remifentanil PCA in vergelijking tot pethidine IM.
Bronnen: (Weibel, 2017) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in de pH a. umbilicalis bij neonaten van zwangeren behandeld met remifentanil PCA in vergelijking tot pethidine IM.
Bronnen: (Wilson, 2018) |
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in NICU opnamen van neonaten van zwangeren behandeld met remifentanil PCA en zwangeren behandeld met pethidine IM.
Bronnen: (Wilson, 2018) |
Remifentanil versus tramadol
|
- GRADE |
Niet van toepassing. Er werden geen studies geïncludeerd naar aanleiding van de literatuursearch.
Bronnen: - |
De literatuuranalyse is gebaseerd op de Cochrane review van Weibel (2017) en geüpdatet met relevante recente RCT’s (Wilson, 2018; Logtenberg, 2017; Günes, 2014). De meta-analyse van Weibel (2017) includeerde enkel RCT’s waarbij cross-over studies of quasi-RCT’s werden geëxcludeerd. De studiepopulatie betrof zwangere vrouwen met een geplande vaginale bevalling en een verzoek om pijnbehandeling (inclusief eventuele risicogroepen zoals inductie of vroeggeboorte). Studies waarbij de populatie een geplande sectio caesarea betrof, werden geëxcludeerd. Geïncludeerde studies vergeleken behandeling met remifentanil PCA versus een controle groep zoals placebo, geen behandeling of enige andere vorm van pijnbehandeling. Voor het beantwoorden van deze uitgangsvraag werden enkel de resultaten van de studies geëxtraheerd waarbij remifentanil PCA vergeleken werd met epidurale analgesie of remifentanil PCA vergeleken werd met opioïden (pethidine of tramadol). Indien meerdere studiearmen waren gepoold in de meta-analyse van Weibel, werd de individuele publicatie geraadpleegd om de relevante data te extraheren (Douma, 2010; Evron, 2008; Ismail, 2012).
Remifenanil versus Epidurale analgesie
Beschrijving studies
De Cochrane-review van Weibel (2017) includeerde 10 RCT’s waarbij remifentanil (PCA) werd vergeleken met toediening van epidurale analgesie (Douma, 2010 Douma, 2015; Evron, 2008; El-Kerdawy, 2010; Freeman, 2015; Stocki, 2014; Stourac, 2014; Tveit, 2012; Ismail, 2012; Volmanen, 2008). De studie van Ismail (2012) vergeleek remifentanil met zowel epidurale analgesie als Combined Spinal Epidural (CSE). Uit deze studie, werden enkel de resultaten van de epidurale analgesie groep meegenomen. De CSE-groep werd buiten beschouwing gelaten. Uit de studie van Evron (2008) werden enkel de data van de ropivacaïne-groep en remifentanil-groep meegenomen in de analyse (de remifentanil + ropivacaïne en ropivacaïne + paracetamol-groep werden buiten beschouwing gelaten). De individuele publicatie werd geraadpleegd om de relevante data te extraheren.
De uitkomstmaten van deze review werden geüpdatet en waar mogelijk gepoold met de resultaten van één recente RCT (Logtenberg, 2016) waarin tevens de effectiviteit en veiligheid van remifentanil PCA vergeleken werd met epidurale analgesie tijdens de baring. De RCT van Logtenberg (2016) includeerde 418 zwangere vrouwen > 32 weken amenorroe met een laag obstetrisch risicoprofiel (ongecompliceerde zwangerschap) die onder behandeling waren van een 1e lijns verloskundige. Zwangeren met een verzoek om pijnstilling of met medische complicaties voorafgaand aan of tijdens de baring werden doorverwezen van de 1e lijns naar 2e lijns zorg.
Zowel de geïncludeerde RCT van Freeman (2015) als de studie van Logtenberg (2016) beschrijven een populatie die gerandomiseerd werd voorafgaand aan de start van de bevalling. In beide studies had een groot deel van de populatie uiteindelijk geen verzoek om de pijn te behandelen. Zo ontving in de studie van Freeman (2015) respectievelijk 65% en 52% van de zwangeren in de remifentanil en epidurale analgesie groep daadwerkelijk pijnbehandeling. In de studie van Logtenberg (2016) ontving 46% in de remifentanil groep en 37% in de epidurale analgesie groep daadwerkelijk pijnbehandeling. In de Cochrane-review van Weibel (2017) werden enkel data van de subgroepen met een verzoek tot pijnbehandeling meegenomen in de analyse. Dit werd ook voor de aanvullende studie van Logtenberg (2016) zo uitgevoerd.
Resultaten
Pijnintensiteit - gemeten op 1 en 2 uur na start analgesie
De Cochrane review van Weibel (2017) includeerde 6 studies (n=235 zwangeren) waarin de pijnintensiteit gerapporteerd werd (Douma, 2011; Douma, 2015; El-Kerdawy, 2010; Stocki, 2014; Stourac, 2014; Tveit, 2012). Pijnintensiteit werd gemeten 1-uur na start van analgesie middels een VAS-schaal of een NRS-schaal. In 4 van deze studies (Douma, 2011; Douma, 2015; Stocki, 2014; Tveit, 2012) werd de pijnintensiteit ook 2 uur na start van analgesie gemeten (n=143 zwangeren).
De pijnintensiteit 1-uur na start van analgesie bleek significant lager in de groep behandeld met een epidurale analgesie in vergelijking met remifentanil (PCA) (gestandaardiseerd gemiddeld verschil 0,57, 95% BI 0,31 tot 0,84). Er was geen sprake van heterogeniteit (I2 0%). Ook 2 uur na start van analgesie werd een significant grotere afname in pijnintensiteit waargenomen in de epidurale analgesie groep versus de remifentanil groep (gestandaardiseerd gemiddeld verschil 1,46, 95% BI 0,66 tot 2,26). Er was sprake van een grote mate van heterogeniteit (I2 71%).
Figuur 1 Pijnintensiteit 1-u na start analgesie remifentanil versus epidurale analgesie
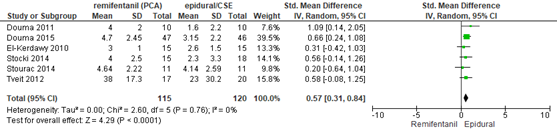
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Figuur 2 Pijnintensiteit 2-u na start analgesie remifentanil versus epidurale analgesie
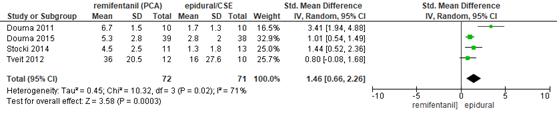
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pijnintensiteit 1 uur en 2 uur na start analgesie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Pijnintensiteit -over de gehele bevalling gemeten als AUC-waarde na start analgesie
De RCT van Logtenberg (2016) en Freeman (2015) rapporteerden de pijnintensiteit (VAS-schaal) middels een AUC (Area Under the Curve) gemeten over herhaalde metingen nadat pijnbehandeling gestart werd (n=964). De AUC-waarde reflecteert een pijnscore over de gehele bevallingsduur, waarbij de bevallingsduur niet significant verschilde tussen de groepen. Logtenberg (2016) rapporteerde een significant lagere pijnintensiteit gedurende analgesie in de groep behandeld met epidurale analgesie in vergelijking met remifentanil met een gemiddelde AUC-waarde van 29 in de remifentanil groep en 17 in de epidurale-groep (gemiddeld verschil AUC-waarde 12; 95% BI 3,0 tot 21). Ook de studie van Freeman (2015) rapporteerde een significant lagere pijnintensiteit in de groep behandeld met epidurale analgesie in vergelijking tot remifentanil met een gemiddelde AUC-waarde van 27 in de remifentanil groep en 20 in de epidurale groep (gemiddeld verschil AUC-waarde 6,4; 95% BI 3,5 tot 9,4).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pijnintensiteit na start analgesie gemeten als AUC-waarde is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Cross-over naar andere/ aanvullende pijnmedicatie
De meta-analyse van Weibel (2017) beschrijft 6 studies (n=988 zwangeren) waarin cross-over naar de andere groep bij een verzoek om additionele pijnbehandeling gerapporteerd werd (escape analgesia) (Douma, 2011; Douma, 2015; Evron, 2008; Freeman, 2015; Stocki, 2014; Tveit, 2012). De data werd aangevuld met de studie van Logtenberg (2016). De cross-over naar andere pijnmedicatie was significant hoger in de remifentanil groep in vergelijking met de epidurale analgesie groep (RR 8,69, 95% BI 3,89 tot 19,41). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 3 Cross-over naar andere pijnmedicatie remifentanil versus epidurale analgesie
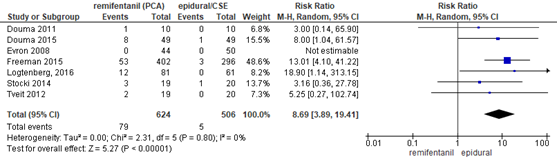
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat cross-over naar andere pijnmedicatie is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias door ontbreken van blindering). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Tevredenheid ten aanzien van pijnstilling
Tevredenheid ten aanzien van pijnstilling wordt in de literatuur op verschillende tijdstippen (na start pijnstilling en na de baring) gemeten en op verschillende manieren (losse tijdspunten en als Area Under the Curve (AUC)-waarde) gerapporteerd. De AUC-waarde is een waarde die naar de mening van de werkgroep de overall tevredenheid met pijnstilling beter en zuiverder weergeeft dan wanneer gemeten op een enkel tijdstip na toediening pijnstilling of postpartum omdat deze gebruik maakt van alle verkregen tevredenheidsscores.
Tevredenheid ten aanzien van pijnstilling - gedurende of direct na de bevalling
In 7 studies (n=1755 zwangeren) van de meta-analyse van Weibel (2017) werd tevredenheid ten aanzien van pijnstilling gerapporteerd (Douma, 2011; Douma, 2015; El-Kerdawy, 2010; Freeman, 2015; Ismail, 2012; Stocki, 2014; Volmanen, 2008). Tevredenheid ten aanzien van pijnstilling werd gemeten middels een VAS-schaal, NRS-schaal of VRS-schaal. Er werd geen significant verschil waargenomen in tevredenheid ten aanzien van de pijnstilling tussen zwangeren behandeld met remifentanil PCA versus epidurale analgesie (gestandaardiseerd gemiddeld verschil -0,01, 95% BI -0,27 tot 0,025). Er was sprake van substantiële heterogeniteit (I2 75%). Met uitzondering van de studie van Volmanen (2008) werden in deze meta-analyse tevredenheidsscores gebruikt die na de bevalling nagevraagd werden.
Figuur 4 Tevredenheid ten aanzien van pijnstilling remifentanil versus epidurale analgesie
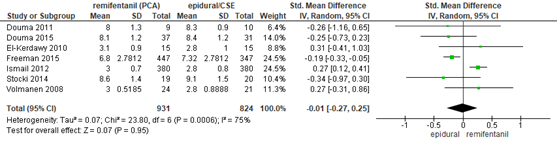
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
In 4 studies van de meta-analyse van Weibel (2017) (Douma, 2001; Freeman, 2015; Stocki 2014; Volmanen, 2008; n=618) werd naast tevredenheid ten aanzien van pijnstilling na de baring ook tevredenheid gemeten op verschillende tijdspunten na toediening van pijnstilling tijdens de baring. Douma (2001) rapporteerde tevredenheid op respectievelijk 1, 2 en 3 uur na start pijnstilling. Tevredenheid was op geen van de tijdstippen verschillend tussen de groepen, met een VAS-score voor tevredenheid van 8,6 (SD 1,1) 7,4 (SD 1,8) en 7,3 (SD 0,8) in de remifentanil groep en gerapporteerd en 8,3 (SD 1,5), 8,6 (SD 0,9) en 7,3 (SD 0,8) in de groep behandeld met epidurale analgesie. Stocki, 2014 rapporteerde tevredenheid (NRS score) op 30 minuten na toediening pijnstilling en vond geen verschil tussen remifentanil (8,4, SD 2,3) en epidurale analgesie (8,4, SD 2,5 p=0,93).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat tevredenheid ten aanzien van pijnstilling gedurende of direct na de bevalling is met twee niveaus verlaagd gezien sterke beperkingen in de onderzoeksopzet (risk of bias) en de inconsistentie van de puntschatters. Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Tevredenheid ten aanzien van pijnstilling - gemeten door middel van AUC-waarde na start analgesie
De RCT van Logtenberg (2016) en Freeman (2015) rapporteerden de tevredenheid (VAS-schaal) middels een AUC gemeten over herhaalde metingen nadat pijnstilling toegediend werd (n=684). De AUC-waarde reflecteert een tevredenheidsscore over de gehele bevallingsduur, waarbij de bevallingsduur niet significant verschilde tussen de groepen. Logtenberg (2016) rapporteerde een significant hogere tevredenheid gedurende analgesie in de groep behandeld met epidurale analgesie in vergelijking tot remifentanil met een gemiddelde AUC-waarde van 23 in de remifentanil-groep en 35 in de epidurale-groep (gemiddeld verschil AUC-waarde -12; 95% BI -22,0 tot -1,5). Ook de studie van Freeman (2015) rapporteerde een significant hogere tevredenheid in de groep behandeld met epidurale analgesie in vergelijking tot remifentanil met een gemiddelde AUC-waarde van 25,6 in de remifentanil groep en 36,1 in de epidurale groep (gemiddeld verschil AUC-waarde -10,4; 95% BI -13,9 tot -7,0). Dit verschil is ook klinisch relevant.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat tevredenheid ten aanzien van pijnstilling gemeten als AUC-waarde is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Hoewel in de studie van Logtenberg (2016) het betrouwbaarheidsinterval van het gemiddelde verschil van de AUC-waarde de grens van klinische relevantie aan één zijde overschrijdt, is er niet afgewaardeerd voor imprecisie. Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Modus partus - sectio caesarea
In 9 studies (n=1149 zwangeren) van de meta-analyse van Weibel (2017) werd de incidentie van een sectio caesarea gerapporteerd (Douma, 2011; Douma, 2015; El-Kerdawy, 2010; Evron, 2008; Ismail, 2012; Stocki, 2014; Stourac, 2014; Tveit, 2012; Volmanen, 2008). Er werd geen significant verschil waargenomen in het risico op een sectio caesarea tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 0,93, 95% BI 0,0,75 tot 1,17). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 5 Modus partus - sectio caesarea remifentanil versus epidurale analgesie
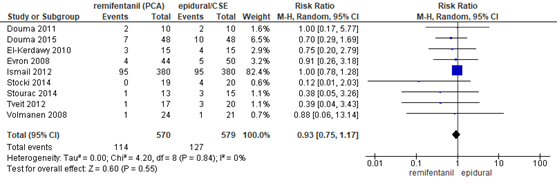
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat sectio caesarea is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Modus partus - vaginale kunstverlossing
In 8 studies (n=1121 zwangeren) van de meta-analyse van Weibel (2017) werd de incidentie van een vaginale kunstverlossing gerapporteerd. Één van de studies rapporteerde het gebruik van de forceps (Evron, 2008), één studie rapporteerde zowel de partus middels forceps als middels vacuüm (Tveit, 2012), 2 studies rapporteerden enkel het gebruik van de vacuüm (Stocki, 2014; Volmanen, 2008) en 4 studies gaven geen definitie van vaginale kunstverlossing (Douma, 2011; Douma, 2015; El-Kerdawy, 2010; Isamail, 2012). Er werd geen significant verschil waargenomen in het risico op een vaginale kunstverlossing tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 0,93, 95% BI 0,65 tot 1,33). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 6 Modus partus - vaginale kunstverlossing remifentanil versus epidurale analgesie
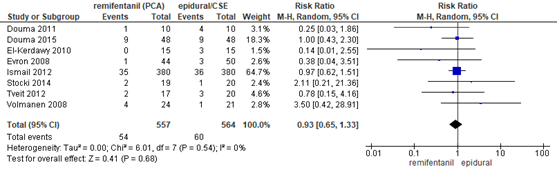
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat vaginale kunstverlossing is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het geringe aantal events (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Ademhalingsproblemen
Zuurstofsaturatie
De meta-analyse van Weibel (2017) includeerde 5 studies waarin zuurstofsaturatie (SpO2) werd gerapporteerd als uitkomstmaat. Deze data werden aangevuld met de resultaten van de studie van Logtenberg (2016). Vier studies (n=944 zwangeren) rapporteerden de saturatie <92% (Logtenberg, 2016; Douma, 2015; Freeman, 2015; Tveit, 2012) en 4 studies (n=970 zwangeren) rapporteerden de saturatie <94% of 95% (Logtenberg, 2016; Freeman, 2015; Stocki, 2014; Volmanen, 2008). Zwangeren behandeld met epidurale analgesie hadden een betere zuurstofsaturatie in vergelijking met zwangeren behandeld met remifentanil PCA zowel bij een afkapwaarde <92% (RR 2,65, 95% BI 1,64 tot 4,30) als een afkwapwaarde <95% of <94% (RR 2,82, 95% BI 1,69 tot 4,72). Er was sprake van substantiële heterogeniteit (I2 55 tot 65%).
Figuur 7 Zuurstof saturatie <92% remifentanil versus epidurale analgesie
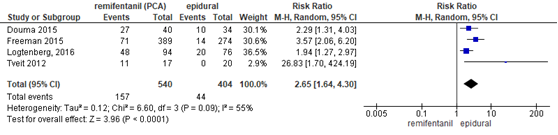
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Figuur 8 Zuurstof saturatie <95%, <94% remifentanil versus epidurale analgesie
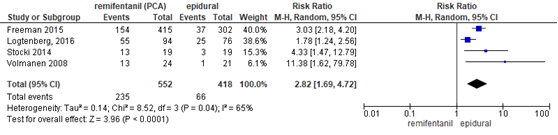
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat zuurstofsaturatie is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Ademhalingsdepressie
In 3 studies (n=687 zwangeren) van de meta-analyse van Weibel (2017) werd de incidentie van ademhalingsdepressie gerapporteerd. Één van de studies definieerde ademhalingsdepressie als < 9 ademhalingen/min (Tveit, 2012) en de overige 2 studies als < 8 ademhalingen/min (Freeman, 2015; Stocki, 2014). Er werden geen events waargenomen in beide groepen in de studie van Tveit (2012) en geen events in de epidurale analgesie groep van de studie van Freeman (2015). Er werd geen significant verschil waargenomen in het risico op ademhalingsdepressie tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 1,52, 95% BI 0,66 tot 1,27). Er was sprake van substantiële heterogeniteit (I2 50%).
Figuur 9 Ademhalingsdepressie (< 9, < 8 ademhalingen/min) remifentanil versus epidurale analgesie
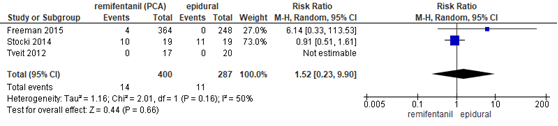
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ademhalingsdepressie is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: blindering en attrition bias) en het geringe aantal patiënten en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Hypotensie
In 4 studies (n=823 zwangeren) van de meta-analyse van Weibel (2017) werd de incidentie van hypotensie gerapporteerd. Één van de studies definieerde hypotensie als een systolische bloeddruk < 90 mmHg (Freeman, 2015) of als > 25% verlaging van de baseline systolische bloeddruk (Stourac, 2014). De overige 2 studies gaven geen definitie voor hypotensie (Douma, 2011; El-Kerdawy, 2010). Er werden geen events waargenomen in beide groepen in de studie van Douma (2011), geen events in de remifentanil groep van de studie van El-Kerdway (2010) en geen events in de epidurale analgesie groep van de studie van Freeman (2015). Er werd geen significant verschil waargenomen in het risico op hypotensie tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 0,58, 95% BI 0,22 tot 1,49). Er was sprake van lage heterogeniteit (I2 17%).
Figuur 10 Hypotensie remifentanil versus epidurale analgesie
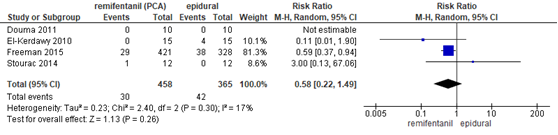
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypotensie is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: blindering), het geringe aantal patiënten en events (imprecisie) en de inconsistentie van de puntschatters (heterogeniteit). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Temperatuur
De RCT’s van Logtenberg (2016), Douma (2015) en Evron (2008) rapporteerden het percentage zwangeren met een temperatuur ≥ 38⁰C. Er werd een significant lager risico op temperatuurverhogingen waargenomen bij zwangeren behandeld met remifentanil PCA in vergelijking met epidurale analgesie (RR 0,45, 95% BI 0,25 tot 0,82). Er was sprake van substantiële heterogeniteit (I2 66%). Echter, er is onzekerheid of dit verschil ook een klinisch relevant verschil reflecteert aangezien het betrouwbaarheidsinterval de grens van klinische besluitvorming overschrijdt.
Figuur 11 Temperatuur remifentanil versus epidurale analgesie
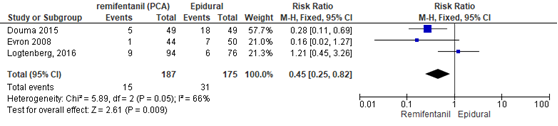
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat temperatuur is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het geringe aantal patiënten en events (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Misselijkheid en braken
Misselijkheid
De meta-analyse van Weibel, 2017 includeerde 8 studies (n=1529 zwangeren) waarin de klacht misselijkheid werd gerapporteerd (Douma, 2011; Douma, 2015; Freeman, 2015; El-Kerdawy, 2010; Ismail, 2012; Stocki, 2014; Tveit, 2012; Volmanen, 2008). Zwangeren behandeld met remifentanil PCA rapporteerden vaker klachten van misselijkheid in vergelijking met zwangeren behandeld met epidurale analgesie (RR 1,53, 95% BI 1,121 tot 1,93). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 12 Misselijkheid remifentanil versus epidurale analgesie
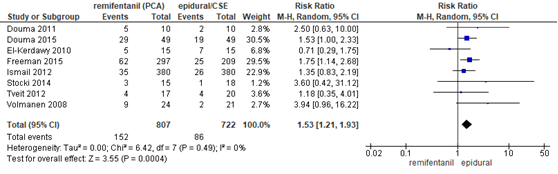
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Braken
De meta-analyse van Weibel (2017) includeerde 6 studies (n=1460 zwangeren) waarin de incidentie van braken werd gerapporteerd (Douma, 2011; Douma, 2015; Freeman, 2015; El-Kerdawy, 2010; Ismail, 2012; Tveit, 2012). Zwangeren behandeld met remifentanil PCA hadden een hoger risico op braken in vergelijking met zwangeren behandeld met epidurale analgesie (RR 1,66, 95% BI 1,25 tot 2,20). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 13 Braken remifentanil versus epidurale analgesie
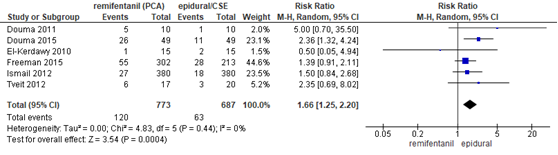
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat misselijkheid en braken is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: blindering en attrition bias), het geringe aantal patiënten en events (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Jeuk
De meta-analyse van Weibel (2017) includeerde 7 studies (n=1472 zwangeren) waarin de klacht jeuk werd gerapporteerd (Douma, 2011; Douma, 2015; Freeman, 2015; El-Kerdawy, 2010; Ismail, 2012; Stocki, 2014; Tveit, 2012). Er werd geen significant verschil waargenomen in het risico op jeuk tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 0,72, 95% BI 0,47 tot 1,11). Er was sprake van een relatief lage heterogeniteit (I2 19%).
Figuur 14 Jeuk remifentanil versus epidurale analgesie
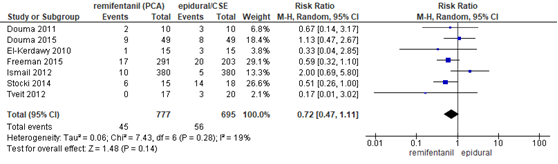
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat jeuk is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Apgarscore
In 5 studies (n=942 neonaten) van de meta-analyse van Weibel (2017) werd de incidentie van een Apgarscore <7 bij 5 minuten gerapporteerd. In de studie van Stocki (2014) en El-Kerdawy (2010) werden geen events gerapporteerd in beide groepen. In de studies van Douma (2011 en 2015) werden geen events waargenomen in resp. de remifentanil of epidurale analgesie groep. Er werd geen significant verschil waargenomen in het risico op een Apgarscore < 7 bij 5 minuten tussen neonaten van zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 1,22, 95% BI 0,57 tot 2,65). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 15 Apgarscore < 7 bij 5 minuten remifentanil versus epidurale analgesie
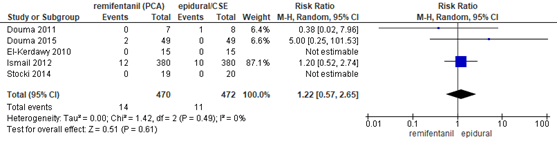
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat Apgarscore is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Foetale hartslag afwijkingen
De meta-analyse van Weibel (2017) rapporteert van 5 studies (n=900 neonaten) de uitkomstmaat FHR/CTG afwijkingen of non-reassuring fetal status. Er werd geen significant verschil waargenomen in het risico op FHR/CTG afwijkingen of non-reassuring fetal status tussen neonaten van zwangeren behandeld met remifentanil PCA of epidurale analgesie (RR 1,48, 95% BI 0,44 tot 5,04). Er was sprake van substantiële heterogeniteit (I2 52%).
Figuur 16 FHR/CTG afwijkingen, non-reassuring fetal status remifentanil versus epidurale analgesie
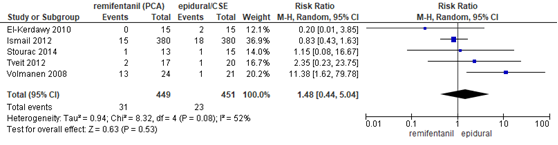
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat FHR/CTG afwijkingen of non-reassuring fetal status is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), de heterogeniteit in de puntschatters (inconsistentie) en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
pH a. umbilicalis
In 6 studies van de meta-analyse van Weibel (2017) werd de pH. a. umbilicalis gerapporteerd. In 5 studies (n=865 zwangeren) werd de arteriële pH. a. umbilicalis bepaald (Douma, 2011; El-Kerdawy, 2010; Ismail, 2012; Stocki, 2014; Tveit, 2012) en in 4 studies (n=919 zwangeren) werd de veneuze pH. a. umbilicalis bepaald (Douma, 2015; El-Kerdawy, 2010; Ismail, 2012; Tveit, 2012).
Er werden significant lagere arteriële pH. a. umbilicalis waarden waargenomen bij zwangeren behandeld met remifentanil PCA versus epidurale analgesie (gemiddeld verschil: -0,01, 95% BI -0,02 tot -0,00). Er was geen sprake van heterogeniteit (I2 0%). Echter, de bovengrens van het betrouwbaarheidsinterval bereikt de grens van een nul-effect en een gemiddeld verschil van -0.01 wordt niet als een klinische relevant of patiënt relevant verschil beschouwd. Er werd geen significant verschil waargenomen in veneuze pH. a. umbilicalis tussen zwangeren behandeld met remifentanil PCA of epidurale analgesie (gemiddeld verschil: 0,01, 95% BI -0,01 tot 0,02). Er was sprake van substantiële heterogeniteit (I2 57%).
Figuur 17 Arteriële pH. a. umbilicalis remifentanil versus epidurale analgesie
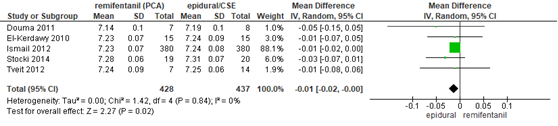
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Figuur 18 Veneuze pH. a. umbilicalis remifentanil versus epidurale analgesie
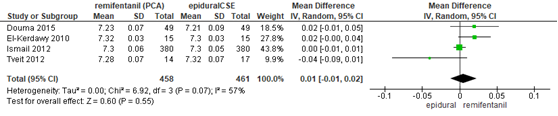
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met epidurale analgesie geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pH. a. umbilicalis is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en de heterogeniteit in de puntschatters (inconsistentie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
De volgende uitkomstmaten werden niet gerapporteerd of niet specifiek gerapporteerd voor de subgroep met een pijnbehandelingsverzoek: angst ten aanzien van pijn, borstvoeding, convulsie/eclamptisch insult, fluxus postpartum, bevallingsduur, urineretentie, motorisch blok, postspinale hoofdpijn, epidurale analgesie abces/hematoom, opname NICU, mortaliteit of negatieve uitkomsten voor de baby op lange termijn.
Remifentanil versus pethidine
Beschrijving studies
De Cochrane-review van Weibel (2017) includeerde 3 RCT’s (n=128 zwangeren) waarbij remifentanil (PCA) werd vergeleken met pethidine/meperidine (IM) (Calderon, 2006; Ng, 2011; Thurlow, 2002). De uitkomstmaten van deze review werden geüpdatet en waar mogelijk gepoold met de resultaten van twee RCT’s (Wilson, 2018; Günes, 2014) waarin tevens de effectiviteit en veiligheid van remifentanil met pethidine tijdens de baring vergeleken werd. De RCT van Wilson (2018) includeerde 401 zwangeren in partu met een pijnbehandelingswens. De zwangeren werden gerandomiseerd over een groep remifentanil (PCA) en een groep intramusculair (IM) pethidine. De RCT van Günes (2014) includeerde 90 zwangere vrouwen met een geplande vaginale baring. De zwangeren werden gerandomiseerd over de volgende 3 groepen 1) pethidine IM 2) remifentanil PCA bolus 3) remifentanil PCA bolus + infusie. De data van beide remifentanil groepen werden voor de analyse van deze uitgangsvraag gecombineerd.
Resultaten
Pijnintensiteit remifentanil PCA versus pethidine IM
De Cochrane review van Weibel (2017) includeerde 2 studies (n=92 zwangeren) waarin de pijnintensiteit gerapporteerd werd (Calderon, 2006; Ng, 2011). Deze data werden aangevuld met de resultaten van de RCT van Günes (2014) (n=90). Pijnintensiteit werd gemeten 1-uur na start van analgesie middels een VAS of VRS-schaal. Er werd geen significant verschil waargenomen tussen behandeling met remifentanil PCA en pethidine IM in de pijnintensiteit 1-uur na start van analgesie, met een gepoold gestandaardiseerd gemiddeld verschil van -0,76 (95% BI: -1,94 tot 0,42). In 2 studies (Ng, 2011; Günes, 2014) werd pijnintensiteit gerapporteerd 2 uur na start van analgesie. Hierbij werd geen significant verschil waargenomen tussen de remifentanil PCA en pethidine IM groep (gestandaardiseerd gemiddeld verschil -1,58, 95% BI -3,25 tot 0,10). Er was in beide gevallen sprake van een grote mate van heterogeniteit (I2 91-95%). Een mogelijke verklaring voor deze grote mate van heterogeniteit is waarschijnlijk een fout in de rapportage in de studie van Günes (2014). De gepoolde resultaten zouden bij excluderen van deze studie opschuiven ten faveure van remifentanil. In de studie van Wilson, 2018 werd elke 30 minuten de VAS-score gemeten. De mediaan van deze VAS-scores, gemeten over de gehele bevallingsduur, werd getoetst en was significant lager in de remifentanil-groep dan in de pethidine-groep. De studie rapporteerde de gemiddelde ± SD VAS-score per groep (remifentanil-groep: 50,8 ± 29,4; pethidine-groep: 64,6 ± 32,6) met een gemiddeld verschil van -13,9, 95% BI -21,4 tot -6.4, p=0,0003).
Figuur 19 Pijnintensiteit 1-h na start analgesie remifentanil PCA versus pethidine IM
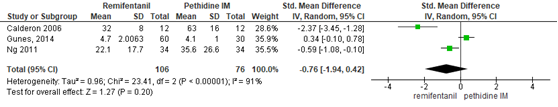
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd) aangevuld met RCT van Günes (2014)
Figuur 20 Pijnintensiteit 2-h na start analgesie remifentanil PCA versus pethidine IM
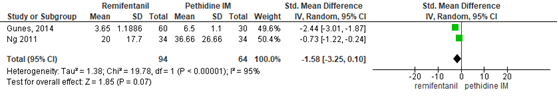
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd) aangevuld met RCT van Günes (2014)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pijnintensiteit (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), heterogeniteit van de puntschatters (inconsistentie) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Cross-over naar andere/aanvullende pijnmedicatie remifentanil PCA versus pethidine IM
De meta-analyse van Weibel (2017) rapporteerde 2 studies waarin de uitkomstmaat additionele pijnbehandeling werd meegenomen. In één van de studies werd als ‘escape’ medicatie pethidine IM en Entonox aangeboden (Ng, 2011) en in één studie eerst Entonox en vervolgens een epidurale analgesie (Thurlow, 2002). In de aanvullende RCT van Wilson (2018) werd het percentage epiduralen gerapporteerd. Behandeling met remifentanil PCA resulteerde in een lager verzoek voor additionele pijnbehandeling in vergelijking tot pethidine IM (gepoold RR 0,55, 95% CI 0,45 tot 0,69). Er was geen sprake van heterogeniteit (I2 0%). Zwangeren in de remifentanil PCA-groep hadden gemiddeld een 45% lagere kans op cross-over naar andere/aanvullende pijnmedicatie dan patiënten in de pethidine IM-groep.
Figuur 21 Cross-over naar andere pijnmedicatie remifentanil PCA versus pethidine IM
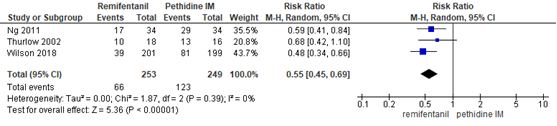
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd) aangevuld met de RCT van Wilson (2018)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat cross-over naar andere pijnmedicatie (remifentanil PCA versus pethidine IM) is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Tevredenheid ten aanzien van pijnstilling - remifentanil PCA versus pethidine IM
De Cochrane review van Weibel (2017) includeerde 3 studies (Calderon, 2006; Ng, 2011; Thurlow, 2002) waarbij tevredenheid ten aanzien van de pijnstilling vergeleken werd tussen remifentanil PCA en pethidine IM (n=128 zwangeren). De aanvullende RCT van Günes (2014) rapporteerde ook de uitkomstmaat tevredenheid (n=90). De resultaten van deze studies zijn gepoold. Tevredenheid werd gemeten middels een VAS/NRS-schaal. Behandeling met remifentanil PCA resulteerde in een klinisch relevant grotere tevredenheid ten aanzien van de pijnstilling in vergelijking met pethidine IM, met een gepoold gestandaardiseerd gemiddeld verschil van 1,53 (95% BI: 1,00 tot 2,06). Er was sprake van een substantiële mate van heterogeniteit (I2 62%), echter het effect is in alle studies ten faveure van remifentanil PCA. In de studie van Wilson (n=401) werd de tevredenheid ten aanzien van pijnstilling gemeten op een 5-punts categoriale schaal. Significant meer zwangeren in de remifentanil groep dan in de pethidine groep gaven aan zeer tevreden of tevreden te zijn over hun pijnstilling (RR 1,15, 95% BI 1,04 tot 1,27). Dit verschil is ook klinisch relevant.
Figuur 22 Tevredenheid ten aanzien van pijnstilling remifentanil PCA versus pethidine IM
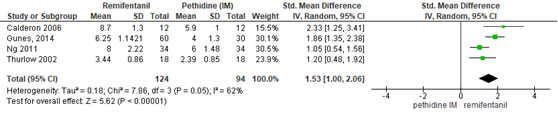
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd)aangevuld met RCT van Günes (2014)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat tevredenheid ten aanzien van pijnstilling (remifentanil PCA versus pethidine IM) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Borstvoeding - remifentanil PCA versus pethidine IM
De RCT van Wilson (2018) rapporteerde het percentage zwangeren dat startte met borstvoeding in het eerste uur na de geboorte. Er werd geen verschil tussen de remifentanil groep en pethidine IM groep waargenomen (RR 0,99, 95% BI 0,80 tot 1,22).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat borstvoeding (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Sectio caesarea - remifentanil PCA versus pethidine IM
De Cochrane review van Weibel (2017) includeerde 3 studies (n=127 zwangeren) waarbij de sectio caesarea als uitkomstmaat werd meegenomen. In de RCT Wilson (2018) werd de uitkomst sectio ook meegenomen (n=401). De resultaten van deze studies zijn gepoold. Het risico op een sectio caesarea bleek niet significant te verschillen tussen zwangeren gerandomiseerd naar de remifentanil PCA en pethidine IM-groep (RR 0,97, 95% BI: 0,68 tot 1,36). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 23 Modus partus - sectio caesarea remifentanil PCA versus pethidine IM
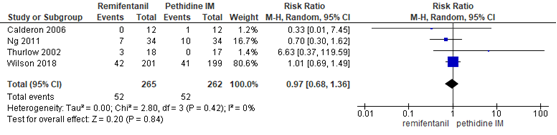
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd) , aangevuld met de RCT van Wilson (2018)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat sectio caesarea (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), het geringe aantal patiënten en brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Modus partus - vaginale kunstverlossing - remifentanil PCA versus pethidine IM
De Cochrane review van Weibel (2017) includeerde 3 studies (n= 127 zwangeren) waarbij vaginale kunstverlossing als uitkomstmaat werd meegenomen. Deze uitkomstmaat werd niet gerapporteerd in de studie van Günes (2014). Twee studies uit de review rapporteerden het voorkomen van bevalling middels vacuüm extractie (Ng, 2011; Thurlow, 2002 en in één studie werd type vaginale kunstverlossing niet gedefinieerd (Calderon, 2006). In de studie van Wilson (2018) (n=401) werd de uitkomst vaginale kunstverlossing gerapporteerd als het voorkomen van vacuüm extractie en forcipale extractie. Het risico op een vaginale kunstverlossing bleek significant lager te zijn bij zwangeren gerandomiseerd naar remifentanil PCA in vergelijking tot pethidine IM (RR 0,62, 95% BI 0,43 tot 0,90). Er is onzekerheid of dit verschil ook een klinisch relevant verschil reflecteert aangezien het betrouwbaarheidsinterval de grens van klinische besluitvorming overschrijdt.
Figuur 24 Modus partus - vaginale kunstverlossing remifentanil PCA versus pethidine IM
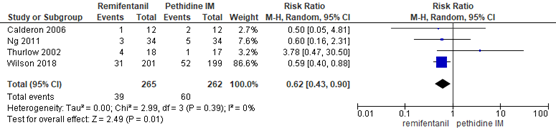
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd), aangevuld met de studie van Wilson (2018)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat vaginale kunstverlossing (remifentanil PCA versus pethidine IM) is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), en het overschrijden van de grens van klinische relevantie (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Ademhalingsproblemen
Ademhalingsdespressie - remifentanil PCA versus pethidine IM
Één studie in de meta-analyse van Weibel (2017) rapporteerde de incidentie van ademhalingsdepressie (< 8 ademhalingen/minuut) (Thurlow, 2002, n=36). Drie van de 18 zwangeren in de remifentanil (PCA) groep en geen van de 18 zwangeren in de pethidine IM groep hadden een respiratoire depressie tijdens de bevalling. In de studie van Wilson (2018) werd bij één van de 187 zwangeren in de remifentanil groep en geen van de 152 zwangeren in de pethidine groep ademhalingsdepressie (< 8 ademhalingen/minuut) gerapporteerd. Er was geen sprake van een significant verschil in het risico op ademhalingsdepressie tussen zwangeren behandeld met remifentanil PCA en pethidine IM (RR 4,35, 95%BI 0,51 tot 37,17).
Figuur 25 Ademhalingsdepressie -remifentanil PCA versus pethidine IM
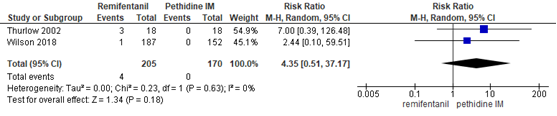
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd)., aangevuld met de RCT van Wilson (2018)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat ademhalingsdepressie (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), het geringe aantal patiënten en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Zuurstofdesaturatie - remifentanil PCA versus pethidine IM
De meta-analyse van Weibel (2017) includeerde 1 studie (n=36 zwangeren) waarin zuurstofdesaturatie (SpO2 <95%) werd gerapporteerd (Thurlow, 2002). In de studie van Wilson (2018) werd zuurstofdesaturatie gerapporteerd als een SPO2 <94%. Er werd een significant verschil waargenomen in zuurstofdesaturatie in het voordeel van de pethidine IM groep (RR 2,82, 95% BI 1,44 tot 5,52). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 26 Zuurstofdesaturatie <95%, <94% -remifentanil PCA versus pethidine IM
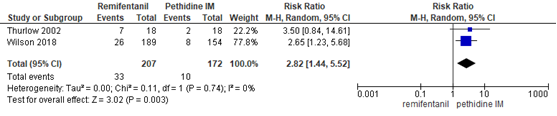
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd), aangevuld met de RCT van Wilson (2018)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat zuurstofdesaturatie (remifentanil PCA versus pethidine IM) is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias). Het niveau van bewijskracht wordt gegradeerd als ‘redelijk’.
Hypotensie - remifentanil PCA versus pethidine IM
De meta-analyse van Weibel (2017) rapporteerde dat geen van de geïncludeerde RCT’s hypotensie als uitkomstmaat meenamen. De RCT van Günes (2014) (n=90 zwangeren) definieerde hypotensie als een systolische bloeddruk <100 mmHg of een verlaging van 30% ten opzichte van baseline. Geen van de zwangeren in beide groepen kregen hypotensie.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypotensie (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), het zeer geringe aantal patiënten en ontbreken van events (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Misselijkheid en braken - remifentanil PCA versus pethidine IM
Weibel (2017) includeerde 3 studies waarin de combinatie misselijkheid en braken (Calderon, 2006; Thurlow, 2002) of afzonderlijk misselijkheid of braken (Ng 2011) vergeleken werd tussen remifentanil PCA en pethidine IM (n=128 zwangeren). Zwangeren in de remifentanil-groep hadden geen significant lager risico op misselijkheid (en braken) in vergelijking met de pethidine IM-groep (RR 0,56, 95% BI 0,30 tot 1,04). Er was sprake van een lage mate van heterogeniteit (I2=0%). Daarnaast rapporteerde de studie van Ng (2011) afzonderlijk over braken, waarbij 1/34 en 2/34 van de zwangeren braakten in respectievelijk de remifentanil en pethidine groep (RR 0,50, 95% BI 0,05 tot 5,26, p=0,55).
Figuur 27 Misselijkheid en braken remifentanil PCA versus pethidine IM
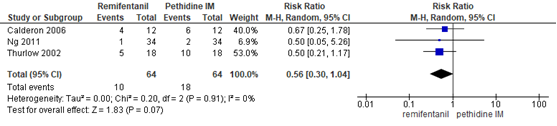
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Weibel (2017) (interventies met pethidine/meperidine geselecteerd)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat misselijkheid en braken (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Jeuk - remifentanil PCA versus pethidine IM
Weibel (2017) includeerde één studie (n=68 zwangeren) waarin jeuk tussen de remifentanil PCA en pethidine IM-groep vergeleken werd (Ng, 2011). Geen van zwangeren in beide groepen had last van jeuk.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat jeuk (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Apgarscore - remifentanil PCA versus pethidine IM
De RCT van Wilson rapporteerde de Apgarscore < 7 bij 5 minuten. Er werd 1 event in de remifentanil-groep en 2 events in de pethidine-groep gerapporteerd (RR 0,50 95% BI 0,05 tot 5,42). De meta-analyse van Weibel (2016) includeerde geen studies waarin de Apgarscore < 7 bij 5 minuten gerapporteerd werd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat Apgarscore (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
Foetale hartslag afwijkingen - remifentanil PCA versus pethidine IM
De meta-analyse van Weibel (2017) includeerde 1 studie (n=68 neonaten) die de uitkomstmaat ‘foetale nood’ met verminderde variabiliteit op het CTG (Ng, 2011) rapporteerde. Er werd geen verschil waargenomen in neonaten van zwangeren behandeld met remifentanil PCA in het risico op CTG-afwijkingen in vergelijking tot behandeling met pethidine IM met 1 event in beide groepen ((RR 1,0 95% BI 0,07 tot 15,34).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat foetale hartslagafwijkingen (remifentanil PCA versus pethidine IM) is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias), het geringe aantal patiënten en brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
pH a. umbilicalis - remifentanil PCA versus pethidine IM
In de RCT van Wilson werd geen verschil waargenomen in de pH a umbilicalis (n=188). De gemiddelde pH waarde was 7,24 (SD 0,09) in beide groepen.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pH a umbilicalis is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en een zeer gering aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
NICU opname - remifentanil PCA versus pethidine IM
De RCT van Wilson (2018) rapporteerde geen verschillen tussen de groepen in het aantal opnames. In de remifentanil groep werden 8 (4%) neonaten opgenomen en in de pethidine IM-groep 9 (5%) (RR= 0,88 95%BI 0,35 tot 2,23).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat NICU opnamen (remifentanil PCA versus pethidine IM) is met twee niveaus verlaagd gezien de beperkingen in onderzoeksopzet (risk of bias), het geringe aantal patiënten en het brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘zeer laag’.
De volgende uitkomstmaten werden niet gerapporteerd: convulsie/eclamptisch insult, fluxus post-partum, bevallingsduur, temperatuur, urineretentie, motorisch blok, postspinale hoofdpijn, epidurale analgesie abces/hematoom, mortaliteit of negatieve uitkomsten voor de baby op lange termijn.
Remifentanil versus Tramadol
Beschrijving studies
Niet van toepassing. Er werden geen studies geïncludeerd naar aanleiding van de literatuursearch.
Resultaten
Niet van toepassing. Er werden geen studies geïncludeerd naar aanleiding van de literatuursearch.
Bewijskracht van de literatuur
Niet van toepassing. Er werden geen studies geïncludeerd naar aanleiding van de literatuursearch.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat zijn de (on)gunstige effecten van remifentanil vergeleken met epiduraal, pethidine of tramadol bij zwangere vrouwen met een verzoek tot behandelen van de baringspijn?
P: zwangere vrouwen met een verzoek tot behandelen van de baringspijn;
I: remifentanil;
C: epiduraal/ pethidine (IM)/ tramadol (parenterale toediening);
O: zie onderstaand:
- Pijnintensiteit (VAS/ NRS-schaal of ander gevalideerd instrument).
- Cross-over naar andere/aanvullende pijnmedicatie.
- Tevredenheid ten aanzien van pijnstilling(rapportcijfer/ VAS/ NRS-schaal of een ander gevalideerd instrument).
- Borstvoeding.
- Modus partus (vaginale kunstverlossing, sectio caesarea).
- Maternale complicaties: convulsie/ eclamptisch insult, fluxus postpartum, ademhalingsdepressie/problemen, bevallingsduur, hypotensie, temperatuur, urineretentie, misselijkheid/braken, jeuk, mate van motorisch blok, postspinale punctie hoofdpijn, epiduraal abces/ hematoom.
- Neonatale complicaties: opname NICU, Apgarscore < 7 bij 5 min, foetale hartslag afwijkingen, temperatuur, pH a. umbilicalis, mortaliteit, negatieve uitkomsten voor de baby op lange termijn.
- Kosten.
Relevante uitkomstmaten
De werkgroep achtte pijnintensiteit, tevredenheid en maternale en neonatale sterfte voor de besluitvorming kritieke uitkomstmaten; en de modus partus, temperatuur en respiratoire complicaties voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde de uitkomstmaten als volgt: pijnintensiteit (VAS/ NRS-schaal of een ander gevalideerd instrument) en tevredenheid (rapportcijfer/ VAS/ NRS-schaal of een ander gevalideerd instrument), waarbij scores door de patiënt zelf gedurende of direct na de bevalling gerapporteerd werden. Voor neonatale Apgarscore wordt de definitiescore van < 7 bij 5 min aangehouden. Voor de overige uitkomstmaten definieerde de werkgroep niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Naast significantie wordt de klinische besluitvorming vooral bepaald door de klinische relevantie van de waargenomen verschillen tussen behandelopties. Voor dichotome uitkomstmaten definieerde de werkgroep een minimaal klinisch (patiënt) relevant verschil volgens de grenzen van de GRADE working group, namelijk een verschil in relatief risico van 25%. Voor de continue kritieke uitkomstmaten definieerde de werkgroep een verschil van 10% op pijnintensiteit of tevredenheid als een klinisch (patiënt) relevant verschil.
Zoeken en selecteren (Methode)
Het betreft een literatuurzoekactie gebaseerd op de Cochrane systematische review van Weibel (2017). In de databases Medline (OVID), Embase (via Embase.com) en de Cochrane Library (via Wiley) is op 18 december 2017 met relevante zoektermen gezocht naar studies die pijnbehandeling middels remifentanil vergeleken met epidurale analgesie, pethidine of tramadol bij zwangere vrouwen met baringspijn. In verband met het verschijnen van een recente relevante RCT werd met dezelfde search-string op 13 september 2018 een update van de zoekactie uitgevoerd. Studies gepubliceerd tot 13 september 2018 werden hierin meegenomen. Deze aanvullende zoekactie leverde, na ontdubbelen, 10 nieuwe treffers op.
De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 41 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- Studiedesign RCT.
- Gepubliceerd tussen 1 januari 2013 en 13 augustus 2018.
- Voldoet aan de PICO.
- Beschrijven van minimaal één van de bovengenoemde uitkomstmaten.
Op basis van titel en abstract werden in eerste instantie 25 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 21 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en 4 studies definitief geselecteerd. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Blair JM, Hill DA, Fee JP. Patient-controlled analgesia for labour using remifentanil: a feasibility study. Br J Anaesth. 2001;87(3):415–420. doi:10.1093/bja/87.3.415
- Freeman L, Middeldorp J, van den Akker E, Oudijk M, Bax C, van Huizen M, et al. (2018) An economic analysis of patient controlled remifentanil and epidural analgesia as pain relief in labour (RAVEL trial); a randomised controlled trial. PLoS ONE 13(10): e0205220. https://doi.org/10.1371/journal.pone.0205220.
- Güneş S, Türktan M, Güleç ÜK, Hatipoğlu Z, Ünlügenç H, Işık G. The Comparison of Patient-Controlled Remifentanil Administered by Two Different Protocols (Bolus and Bolus+Infusion) and Intramuscular Meperidine for Labor Analgesia. Turk J Anaesthesiol Reanim. 2014 Oct;42(5):264-9. doi: 10.5152/TJAR.2014.77045. Epub 2014 Jul 9. PMID: 27366433.
- Kinney MA, Rose CH, Traynor KD, et al. Emergency bedside cesarean delivery: lessons learned in teamwork and patient safety. BMC Res Notes. 2012;5:412. Published 2012 Aug 6. doi:10.1186/1756-0500-5-412
- Logtenberg S, Oude Rengerink K, Verhoeven CJ, Freeman LM, van den Akker E, Godfried MB, van Beek E, Borchert O, Schuitemaker N, van Woerkens E, Hostijn I, Middeldorp JM, van der Post JA, Mol BW. Labour pain with remifentanil patient-controlled analgesia versus epidural analgesia: a randomised equivalence trial. BJOG. 2017 Mar;124(4):652-660. doi: 10.1111/1471-0528.14181. Epub 2016 Jun 27. PMID: 27348853.
- Logtenberg SLM, Vink ML, Godfried MB, et al. Serious adverse events attributed to remifentanil patient-controlled analgesia during labour in The Netherlands. Int J Obstet Anesth. 2019;39:22–28. doi:10.1016/j.ijoa.2018.10.013
- Macario A, Scibetta WC, Navarro J, Riley E. Analgesia for labor pain: a cost model. Anesthesiology. 2000 Mar;92(3):841-50. PMID: 10719963.
- Waring J, Mahboobi SK, Tyagaraj K, Eddi D. Use of remifentanil for labor analgesia: the good and the bad. Anesth Analg. 2007;104(6):1616–1617.doi:10.1213/
- Weibel S, Jelting Y, Afshari A, Pace NL, Eberhart LH, Jokinen J, Artmann T, Kranke P. Patient-controlled analgesia with remifentanil versus alternative parenteral methods for pain management in labour. Cochrane Database Syst Rev. 2017 Apr 13;4:CD011989. doi:10.1002/14651858.CD011989.pub2. Review. PMID: 28407220.
- Wilson MJA, MacArthur C, Hewitt CA, Handley K, Gao F, Beeson L, Daniels J; RESPITE Trial Collaborative Group. Intravenous remifentanil patient-controlled analgesia versus intramuscular pethidine for pain relief in labour (RESPITE): an open-label, multicentre, randomised controlled trial. Lancet. 2018 Aug 25;392(10148):662-672. doi: 10.1016/S0140-6736(18)31613-1. Epub 2018 Aug 13. PMID: 30115484.
- Convenant Medische Technologie, 2016: https://www.vmszorg.nl/wp-content/uploads/2017/11/Convenantmedische-technologie-tweede-druk-2016.pdf.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: Wat is de effectiviteit van remifentanil in vergelijking met epiduraal, pethidine of tramadol in de pijnstilling bij zwangere vrouwen met het verzoek tot behandelen van de baringspijn?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Weibel, 2017
Study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of RCTs
Literature search up to December 2015
Remifentanil versus Pethidine A: Calderon, 2006 B: Ng, 2011 C: Thurlow, 2002 D: Evron, 2005 E: Blair, 2005 F: Douma, 2010 G: Volikas, 2001
Remifentanil versus epidural/CSE H: Douma, 2011 I: Douma, 2015 J: Evron, 2008 K: El-Kerdawy, 2010 L: Freeman, 2015 M: Ismail, 2012 N: Stocki, 2014 O: Stourac, 2014 P: Tveit, 2012 Q: Volmanen, 2008
Study design: RCTs
Setting and Country: A: unclear, Spain B: unclear, China C: unclear, UK D: unclear, Israel E: unclear, UK F: unclear, Netherlands G: unclear, UK H: unclear, Netherlands I: Leiden University Medical Center, Netherlands J: Wolfson Medical Center affiliated to Tel-Aviv University K: unclear, Egypt/Saudi Arabia L: 15 hospitals, the Netherlands M: TAIBA Hospital in Kuwait N: Jerusalem tertiary hospital O: unclear, Czech Republic P: unclear, Norway Q: unclear, Finland
Source of funding: None of the trials was funded by industry
|
Inclusion criteria SR: RCTs and cluster RCTs. Trials incl women in labour with planned vaginal delivery, incl high risk groups, e.g. pre-term labour or following induction of labour were eligible.
Exclusion criteria SR: cross-over trials and quasi-RCTs. Trials involving women scheduled for caesarean delivery were excluded
7 studies included that describe comparison with Pethidine, 10 studies included that describe comparison with epidural (studies using other interventions were not described)
Important patient characteristics at baseline:
N, population randomized I/C; N, receiving treatment I/C: A: 12/12; 12/12 B: 34/34; 34/34 C: 18/18; 18/18 D: 43/45; 43/45 E: 20/20; 20/20 F: 60/60; 52/53 G: 9/8; 9/8 H: 14/12; 14/11 I: 57/59; 49/49 J: unclear (analysed 44/50 K: unclear (analysed 15/15) L: 709/705; 402/296 M: 380/760; 380/760 (epidural and spinal-epidural arms combined) N: 20/20; 19/20 O: 13/15; 13/15 P: 19/20; 19/20 Q: 27/25; 27/24
Groups comparable at baseline? Yes |
Describe intervention: Reminfentanil
A: infusor with a capacity of 250 mL was filled with 2.5mg remifentanil and a 12 mL/h was started (average infusion of 0.025 μg/(kg*min) and boluses of 5 mL with a time of closing of 30 min) B: 50 mL syringe remifentanil 20 μg/mL. For each successful PCA demand, an IV bolus of 1.25 mL remifentanil 25μg was delivered to parturients weighing < 60 kg and 1.5 mL (remifentanil 30 μg) for those weighing ≥ 60 kg. The bolus was delivered at a rate of 20 mL/h. Lockout interval was 3.75 - 4.50 min with an hourly limit of 25 mL. C: PCA: starting with a 5 μg bolus, an increasing dose of remifentanil was given at the beginning of each painful contraction until the contraction was pain-free D: Remifentanil: 20μg as a starting doseand a 3 min lockout interval without basal infusion. The dose was increased by the attending anaesthesiologist every 15 to 20 min by 5 μg increments, on woman’s request, to a maximum dose limit of 1500 μg/h. If any parturie E: remifentanil PCA using 40 μg remifentanil with a lockout of 2 min. bolus dose and lockout period for the remifentanil PCA were based on an average maternal weight (80 kg) and a bolus of 0.5 μg/kg F: 40μg loading dose and remifentanil 40μg per bolus with a lockout of 2min and a max dose limit 1200ug/h G: PCA with remifentanil bolus of 0.5 μg/kg, a lockout period of 2 min and no hourly maximum limit
H: IVremifentanil PCA, 40μg loading dose and boluses of 40μg with a 2min lockout time and bolus duration of 36s using a Graseby 3300 syringe pump I: remifentanil (PCA) 40 μg bolus (lockout 2 min, bolus duration 36 s) using a Graseby 3300 syringe pump J: Remifentanil: 0.025 μg/(kg*min) combined with 20 μg bolus doses with a lockout of 3 min. The dose was increased by 25% every 15 to 20 min as required. K: remifentanil: 50μg/mL (3mg diluted to 60mL of normal saline). The PCA was set to deliver 0.5μg/kg as a loading bolus infused over 10 s, lockout time of 5min, PCA bolus of 0.25 μg/kg, continuous background infusion of 0.05μg/(kg*min), and maximum dose was 3mg in 4 h. L: 30μg remifentanil (solution 20μg/mL) on request with a lockout time of 3min. The dose could be increased to 40μg in case of insufficient pain relief or decreased to 20μg in case of excessive side effects. M: remifentanil: 0.1μg/kg, diluted with saline and given as a solution of 25μg/mL as a bolus infused during a period of 1min, with a lockout time of 1min, into an IV catheter providing continuous infusion of saline at approximately 100mL/h. IV PCIA bolus was increased following scheme (0.1 - 0.2 - 0.3 - 0.5 - 0.7 - 0.9 μg/kg) N: bolus dose was titrated to effect from 20 μg up to a max of 60 μg as required; the lockout interval was initially set at 2 min O: Remifentanil via PCA device from a 50 mL syringe in a concentration of 20 μg/mL. On demand, the parturient received an IV bolus of 20μg (1 mL) of remifentanil. Lockout interval was set to 3 min P: remifentanil 50 μg/mL, given as stepwise bolusses. starting bolus dose was 0.15 μg/kg, with increasing dose steps of 0.15 μg/kg. Q: remifentanil: 0.1 mg/kg diluted with saline as a solution of 25 μg/mL as a bolus infused during a period of 1 min, with a lockout time of 1 min, into an IV catheter attached to a 1-way line providing continuous infusion of saline at approx. 100 mL/h. IV PCA bolus scheme (0.1 - 0.2 - 0.33 - 0.5 - 0.7 - 0.9 μg/kg)
|
Describe control: Pethidine/meperidine
A: meperidine IM, 1 mg/kg B: A single IM injection of pethidine 50 mg diluted to 1.5 mL with saline was given to parturients weighing < 60 kg and pethidine 75 mg in 1.5 mL to those weighing ≥ 60 kg C: IM Meperidine 100 mg D: 75mg of meperidine in 100mL of normal saline over 30min (approximately 1 mg/kg in a single bolus). In case of insufficient analgesia, another dose of 75mg, followed by 50mg. E: Control participants received PCA using pethidine 15 mg with a lockout of 10 min F: meperidine PCA 49.5mg loading dose and 5 mg boluses with a lockout of 10 min and a maximum overall dose limit of 200 mg G: PCA with a pethidine bolus 10 mg, a lockout period of 5 min and a maximum limit of 100 mg per h
H: epidural: loading dose of 0.2% ropivacaine 12.5mL was given through the epidural catheter, followed by a continuous infusion of 0.1% ropivacaine with sufentanil 0.5μg/mL at 10mL/h. If analgesia was inadequate, additional boluses of the epidural solution were given. I: loading dose of ropivacaine 25mg (0.2% ropivacaine 12.5 mL), followed by a continuous infusion of 0.1% ropivacaine and sufentanil 0.5μg/mL at 10mL/h. In case of inadequate analgesia, additional 10mL boluses given. J: Epidural: test dose of 3mL lidocaine (2% without epine-phrine) was followed by increments of 5mL to 10mL of 0.2% ropivacaine; maintenance was provided with the same solution via patient-controlled epidural analgesia (PCEA) with a background infusion of 10 mg/h and a 10 mg patient-activated bolus with 20 min lockout. K: Epidural: bolus of 10mL to 15mL of 0.25% bupivacaine plus 1 μg/kg fentanyl. Analgesia was maintained by continuous infusion of 0.125% bupivacaine plus 2μg/mL fentanyl at a rate of 10mL to 12mL per hour aiming to obtain a T-10 sensory level L: Women randomised to epidural received this when they requested pain relief,according to local protocol M: epidural: 8mL dose of 0.125% levobupivacaine with 2 μg/mL fentanyl was administered through the epidural catheter. Then an electronic pump delivered continuous infusion of 8 mL/h of 0.125% levobupi and 2 μg/mLfentanyl. Further boluses of 5 mL to 10 mL of 0.125% levobupi given upon request Spinal-epidural: needle-through-needle technique was performed with 2mg levobupi and 15μg fentanyl injected intrathecally and the spinal needle was removed. Epi catheter connected to an electronic pump set to deliver the same previously mentioned mixture N: incremental initial loading dose of 15mL of 0.1% bupi with 50μg fentanyl administered followed by PCA epidural analgesia infusion of 0.1% bupi with 2μg/mL fentanyl: basal infusion of 5 mL/h, PCA bolus 10 mL, and lockout interval 20 min. O: induction dose of 12.5mg of bupi and 5μg of sufentanil in 10 mL of normal saline; top-up boluses of half-size dose were repeated in 60 to 90min intervals P: epidural infusion of ropi 1mg/mL and fentanyl 2μg/mL (‘walking epidural’). An initial bolus dose of 10mL, followed by a 5mL top-up after 5 min (total 15 mL) was given before the start of infusion (10 mL/h). Thereafter, the midwife was allowed to adjust the infusion dose (5 mL/h to 15 mL/h) and give rescue doses (5 mL) if needed Q: epidurally 20 mL of levobupi (0.625 mg/mL) and fentanyl 2 μg/mL in saline divided into 2 10mL boluses given by the researcher manually with a 5-min interval IV saline was used for blinding in the epidural group. |
End-point of follow-up: Up until delivery for all RCTs
For how many participants were no complete outcome data available? (intervention/control) A: No missing outcome data after randomisation. B: No missing outcome data after randomisation C: 0% dropout. However, some outcome data (additional analgesia, mode of delivery) incomplete, without reasons D: 0% dropout. 2%/22% of outcome data (AE for women: SpO2) not reported and imbalanced between groups. No reasons given. E: 0%/5% dropout. F: 15%/12% drop-out, 21 excluded due to delivery 1h after randomisation. Up to 50% missings (satisfaction, AE newborn, AE mother, rate CS, rate of assisted birth, umbilical blood pH). No reasons reported. G: No missing outcome data after randomisation. H: 29%/17% dropout. Only 10 in each group completed study. N=5 excluded because delivery within 1hr of randomisation and 1 because of incorrect placement of epidural catheter. 30%/20% of for neonatal outcomes not reported. I: 14%/17% dropout. No reasons declared for exclusion of 5 women. J: 10% dropout. Reasons for missing outcome data were described (12 delivered quickly without requirement for analgesia and 9 with labour < 2 h were excluded) K: No missing outcome data after randomisation L: 3%/5% dropout. 5.5% to 41.5) of data for maternal side effects and neonatal data were missing. No reasons reported. Only 65% and 52% received an analgesic intervention in the remi/ epi group. Only 57% in remi group, 42% in epi group received allocated intervention M: No missing outcome data after randomisation N: 5%/0% dropout. O: 8%/20% dropout. N=4 caesarean sections excluded from analaysis. P: 10%/0% dropout. Missing outcomes 15 to 70% regarding neonatal outcomes, without reasons Q: 11%/16% dropout. unclear from the description why and how many women in each group were excluded
|
Outcome measures as defined in this research question are extracted from the systematic review for the following comparisons:
Remifentanil versus Pethidine
Remifentanil versus epidural
Remifentanil versus tramadol (no data)
The outcome measures and effect sized can be found in the forrest plots (figures) of the literature analysis. |
Risk of bias: Incomplete outcome data (attrition bias): Other bias:
|
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
Research question: Wat is de effectiviteit van remifentanil in vergelijking met epiduraal, pethidine of tramadol in de pijnstilling bij zwangere vrouwen met het verzoek tot behandelen van de baringspijn?
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Risk of bias tables
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
Study Question: Wat is de effectiviteit van remifentanil in vergelijking met epiduraal, pethidine of tramadol in de pijnstilling bij zwangere vrouwen met het verzoek tot behandelen van de baringspijn?
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Weibel, 2017 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
Yes |
Unclear |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Risk of bias table for intervention studies (randomized controlled trials)
Research question: Wat is de effectiviteit van remifentanil in vergelijking met epiduraal, pethidine of tramadol in de pijnstilling bij zwangere vrouwen met het verzoek tot behandelen van de baringspijn?
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Wilson, 2018 |
Women were randomly assigned (1:1) to either intravenous remifentanil PCA (ie, the intervention group) or intramuscular pethidine (ie, the control group), via a web-based central service or a 24-h, 7-day interactive telephone-based service. A minimisation algorithm was used to avoid chance imbalances in four variables: parity (nulliparous versus multiparous), maternal age (<20 years, 20 to <30 years, 30 to <40 years, and ≥40 years), ethnicity (south Asian versus other), and onset of labour (induced versus spontaneous). |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely
|
Unlikely |
|
Logtenberg 2016 |
Randomisation was performed using a web-based program stratified for midwifery practice and parity. Randomisation was performed before the onset of labour. |
Likely (open label) |
Likely (open label) |
Likely |
Likely |
unlikely |
Likely, only 48% en 51% received allocated intervention. |
unlikely |
|
Gunes, 2014 |
computer based randomization method in the way that each group would include 15 primiparous and 15 multiparous pregnant women |
Likely |
Likely |
Likely |
Likely, only assessment of apgar scores blinded |
unlikely |
No drop-out reported |
unlikely |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules.
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear.
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Jelting, 2017 |
Is een verkorte versie van de Cochrane Review van Weibel 2017 |
|
Lee, 2017 |
Systematische review, alle relevante trials zitten ook in Weibel, 2017 |
|
Stourac, 2016 |
Systematische review, alle relevante trials zitten ook in Weibel, 2017 |
|
Liu, 2014 |
Systematische review, alle relevante trials zitten ook in Weibel, 2017 |
|
Devabhakthuni, 2013 |
Geen systematische review |
|
Van de Velde, 2013 |
Narrative review |
|
Wilson, 2017 |
Conference abstract |
|
Boterenbrood, 2016 |
Conference abstract |
|
Chetty, 2016 |
Conference abstract |
|
Koyyalamudi, 2016 |
Narrative paper |
|
Anonymus ,2015 |
Abstract beschrijft studie van Douma, 2015. Deze RCT is al geïncludeerd via Weibel, 2017 |
|
Douma, 2015 |
RCT zit al in Weibel, 2017 |
|
Frauenfelder, 2015 |
Observationele studie |
|
Freeman, 2015 |
RCT zit al in Weibel, 2017 |
|
Birnbach, 2014 |
Editorial stuk |
|
Freeman, 2014 |
Conference abstract |
|
Logtenberg, 2014 |
Conference abstract |
|
Stocki, 2014 |
RCT zit al in Weibel, 2017 |
|
Stourac, 2014 |
RCT zit al in Weibel, 2017 |
|
Lim, 2013 |
Review, onduidelijk of systematisch is gezocht |
|
Tveit, 2013 |
RCT zit al in Weibel, 2017 |
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-07-2020
Beoordeeld op geldigheid : 03-07-2020
Bij het opstellen van de modules heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodules komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De andere aan deze richtlijnmodule deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijnmodule delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Remifentanil versus epidurale analgesie, pethidine of tramadol |
NVA/ NVOG |
2019 |
2024 |
Eens in de 5 jaar |
Regiehouder en relevante wetenschappelijke verenigingen. |
literatuur welke de aanbeveling mogelijk doet veranderen. |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Patiëntenfederatie Nederland
De ontwikkeling van de richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodules.
Samenstelling werkgroep
- Dr. W.L.M.C.M. Schellekens, extern voorzitter
- Drs. I.C.M. Beenakkers, anesthesioloog, werkzaam in het UMC Utrecht, NVA
- Drs. F.A. Klerk, anesthesioloog, werkzaam in het Diakonessenhuis Utrecht, NVA
- Drs. C.E. Kam-Endtz, anesthesioloog, werkzaam in het Haaglanden Medisch Centrum, NVA
- Dr. F.T.H. Lim, gynaecoloog, werkzaam in het IJssellandziekenhuis, NVOG
- Dr. L.M. Freeman, gynaecoloog, werkzaam in het Ikazia Ziekenhuis Rotterdam, NVOG
- Dr. J.M. Middeldorp, gynaecoloog, werkzaam in het Leids Universitair Medisch Centrum, NVOG
- Drs. A.G. Kaspers, kinderarts, werkzaam in het Medisch Spectrum Twente, NVK
- Drs. L.A.M. Moll, klinisch verloskundige, werkzaam in het St. Antonius Ziekenhuis Nieuwegein, KNOV
- Dr. J. de Boer, beleidsmedewerker bij KNOV
- Drs. S. Ratsma-Wesselius, Obstetrisch verpleegkundige, werkzaam bij het Amsterdam UMC, Locatie AMC, V&VN
- Dr. J.E. Nagtegaal, Ziekenhuisapotheker, werkzaam in het Meander Medisch Centrum, NVZA
- Dr. A.M.D.E. Timmerman, Klinisch Fysicus, werkzaam in het UMC Utrecht, NVKF
- Drs. J.C. Mooij, adviseur patiëntenbelang, Patiëntenfederatie Nederland.
Met ondersteuning van
- Dr. E.M.E. den Breejen, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Dr. W.J. Harmsen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Schellekens |
gepensioneerd, ZZP: strategisch adviseur |
Lid RvT Diakonessenhuis, Utrecht |
Geen |
Geen |
|
Klerk |
Staf Anesthesiologie Diakonessenhuis Utrecht. |
bestuurslid Obst. Anesth. onbetaald |
Geen |
Geen |
|
Ratsma Wesselius |
Senior verpleegkundige Verloscentrum AMC |
Gastdocent VU Amstel Academie verpleegkundige vervolgopleidingen Obstetrie, betaald |
Geen |
Geen |
|
Beenakkers |
Anesthesioloog WKZ/UMCU |
Voorzitter sectie obstetrische anesthesie van de NVA. Onbetaald |
Echtgenoot werkzaam bij GSK |
Geen |
|
Nagtegaal |
Ziekenhuisapotheker Meander Medisch Centrum |
Beroepenveldcommissie Farmakunde Hogeschool Utrecht, onbetaald |
Geen |
Geen |
|
Timmerman |
Staffunctionaris Klinische Fysica & Patiëntveiligheid |
Lid NIVEL expertgroep infuustechnologie - advies maken kennistoets voor verpleegkundigen – onbetaald Lid ondernemingsraad UMC Utrecht - onbetaald |
EMRP Researcher Grant Metrology for Drug Delivery HLT07- REG1 €120,422.88 USPTO Applicaton #: #20160106909 Apparatus for simultaneous multiple medicament administration |
Geen |
|
Kam-Endtz |
Anesthesioloog Haaglanden MC |
Geen |
Geen |
Geen |
|
Middeldorp |
Gynaecoloog-perinatoloog |
Geen |
Geen |
Geen |
|
Moll |
Klinisch verloskundige/research verloskundige in het St. Antoniusziekenhuis in Nieuwegein |
Geen |
Geen |
Geen |
|
Freeman |
Gynaecoloog |
voorzitter multidiciplinaire werkgroep obstetrische anesthesie
|
Mijn promotieonderzoek naar epidurale analgesie en remifentanil is gesubsidieerd door ZonMw. Dit onderzoek is afgerond maar de resultaten zullen gebruikt worden in deze richtlijn |
Geen |
|
Mooij |
Beleidsmedewerker Patiëntenvereniging Nederland |
Vrijwilligerswerk (onbetaald) patiëntenorganisatie CCUVN |
Geen |
Geen |
|
Kaspers |
Kinderarts-neonatoloog, MST Enschede |
Geen |
Geen |
Geen |
|
De Boer |
Beleidsmedewerker richtlijnontwikkeling |
Geen nevenwerkzaamheden |
Geen |
Geen |
|
Lim |
gynaecoloog |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de Patientenfederatie Nederland in de werkgroep te laten deelnemen. De conceptmodule is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland. Daarnaast is door de Patiëntenfederatie Nederland een achterbanraadpleging verricht, waarvan de uitkomsten zo veel mogelijk meegenomen zijn in de overwegingen van de modules.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze modules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, (2010)), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based module tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit inventarisatie van de knelpunten door de commissie van de NVA bleek dat er een noodzaak was voor revisie van deze richtlijnmodules. Tevens zijn tijdens een fysieke knelpunteninventarisatie knelpunten aangedragen door aanpalende stakeholders inclusief patiëntenorganisaties. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroepleden en de adviseur uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad ‘Zoekverantwoording’ voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de modules is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Indicatorontwikkeling
Indicatoren over zwangerschap en geboorte zijn reeds onderdeel van de vervaardigde indicatoren bij de zorgstandaard integrale geboortezorg. Derhalve zijn er bij deze modules geen indicatoren ontwikkeld.
Kennislacunes
Tijdens de ontwikkeling van deze modules is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de Kennislacunes. Deze zijn te vinden onder de aanverwante producten.
Commentaar- en autorisatiefase
De conceptmodules werden aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werden de conceptmodules aangepast en definitief vastgesteld door de werkgroep. De definitieve modules werden aan de deelnemende (wetenschappelijke) verenigingen en de Patiëntenfederatie Nederland voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut via secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|||||||||||||||||||||||||||
|
Medline (OVID)
(jaartal)
|
|
na ontdubbelen: 41 |
|||||||||||||||||||||||||||
|
Embase (Elsevier) |
|
||||||||||||||||||||||||||||
|
Cochrane library |
(labor:ab,ti or labour:ab,ti or childbirth:ab,ti or birth*:ab,ti or delivery:ab,ti or parturient*:ab,ti) and (remifentanil:ab,ti or ultiva:ab,ti) and (epidural*:ab,ti or cse:ab,ti or pcea:ab,ti or meperidin*:ab,ti or pethidin*:ab,ti or isonipecain:ab,ti or dolsin:ab,ti or dolosal:ab,ti or dolin:ab,ti or perindine:ab,ti or dolantin:ab,ti or dolargan:ab,ti or lidol:ab,ti or lydol:ab,ti or demerol:ab,ti or dolcontral:ab,ti or (parenteral* next/2 opioid*):ab,ti or (tramado* or tramal or tramundin or biodalgic or jutadol or nobligan or prontofort or zytram or takadol or theradol or tiral or topalgic or tradol or tradonal or tralgiol or trama or biokanol or tramadin or ranitidin or trasedal or ultram or xymel or zamudol or zumalgic or zydol or tramadura or tramagetic or tramagit or tramake or tramex or adolonta or contramal or amadol):ab,ti) |
Zoekverantwoording - update search
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
September 2018 |
Zoekstrategie zie originele search
= 17 |
10 (nieuw na ontdubbelen) |
|
Embase (Elsevier) |
((('labor'/exp OR 'obstetric delivery'/exp OR 'labor pain'/exp OR 'obstetric analgesia'/exp OR labor:ab,ti OR labour:ab,ti OR childbirth:ab,ti OR birth*:ab,ti OR delivery:ab,ti OR parturient*:ab,ti) AND ('remifentanil'/exp OR remifentanil:ab,ti OR ultiva:ab,ti) AND ('epidural anesthesia'/exp OR epidural*:ab,ti OR cse:ab,ti OR pcea:ab,ti OR 'pethidine'/exp OR meperidin*:ab,ti OR pethidin*:ab,ti OR isonipecain:ab,ti OR dolsin:ab,ti OR dolosal:ab,ti OR dolin:ab,ti OR perindine:ab,ti OR dolantin:ab,ti OR dolargan:ab,ti OR lidol:ab,ti OR lydol:ab,ti OR demerol:ab,ti OR dolcontral:ab,ti OR ((parenteral* NEXT/2 opioid*):ab,ti) OR tramado*:ab,ti OR tramal:ab,ti OR tramundin:ab,ti OR biodalgic:ab,ti OR jutadol:ab,ti OR nobligan:ab,ti OR prontofort:ab,ti OR zytram:ab,ti OR takadol:ab,ti OR theradol:ab,ti OR tiral:ab,ti OR topalgic:ab,ti OR tradol:ab,ti OR tradonal:ab,ti OR tralgiol:ab,ti OR trama:ab,ti OR biokanol:ab,ti OR tramadin:ab,ti OR ranitidin:ab,ti OR trasedal:ab,ti OR ultram:ab,ti OR xymel:ab,ti OR zamudol:ab,ti OR zumalgic:ab,ti OR zydol:ab,ti OR tramadura:ab,ti OR tramagetic:ab,ti OR tramagit:ab,ti OR tramake:ab,ti OR tramex:ab,ti OR adolonta:ab,ti OR contramal:ab,ti OR amadol:ab,ti) AND ((dutch)/lim OR (english)/lim) AND (2013-2018)/py)
Gebruikte filters: Systematische reviews: ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
RCT’s: ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it = 39 (26 uniek) |

