Optoppen epiduraal
Uitgangsvraag
Wat is de beste strategie voor optoppen van een zittende epiduraal om een adequaat chirurgisch blok voor een sectio te verkrijgen met de minste kans op complicaties/ bijwerkingen?
Aanbeveling
Overweeg bij een secundaire sectio met hoge urgentie, waarbij de barende al een epiduraal in situ heeft een top-up van lidocaïne + adrenaline (met of zonder additief) vanwege het sneller bereiken van chirurgische diepte van het blok ten opzichte van ropivacaïne of bupivacaïne.
Overweeg in geval van een sectio ropivacaïne in plaats van bupivacaïne wanneer de urgentie nog niet te hoog is.
Overweeg spinale anesthesie bij een niet goed zittende epiduraal wanneer er een sectio verricht moet worden.
Overwegingen
De onderstaande overwegingen gelden in principe voor de gehele patiëntenpopulatie zoals geformuleerd in de uitgangsvraag.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In bovenstaande onderzoeken worden veel verschillende regimes qua optoppen van epiduralen voor sectio’s beschreven. In de vergelijking bupivacaïne/ropivacaïne versus lidocaïne + adrenaline incl. fentanyl wordt een significant verschil ten faveure van lidocaïne + adrenaline (eventueel met fentanyl) waargenomen in tijd tot chirurgisch blok namelijk 3,13 minuten. Dit kan op ongeveer 10 minuten tot chirurgisch blok als klinisch relevant worden beschouwd vanwege de mogelijkheid sneller te kunnen starten met opereren en daarmee een grotere kans op goede uitkomst voor het kind. Daarnaast geeft dit ook geringe kans op onvoldoende pijnstilling bij de zwangere (Visser, 2009).
Bij de zwangeren die lidocaïne + adrenaline kregen als oplossing om de epiduraal op te toppen duurde de tijd tot chirurgisch blok gemiddeld 1.66 minuten korter (95% BI -2,40 tot -0,91 minuten) vergeleken met (levo)bupivacaïne of ropivacaïne. Ook dit reflecteert een mogelijk klinisch relevant verschil. Er werd heterogeniteit waargenomen tussen de RCT’s in de effectgrootte, welke voornamelijk toe te schrijven was aan de RCT van Sng (2008). Indien de RCT van Sng (2008) geëxcludeerd wordt uit de meta-analyse, dan reduceerde dit de tijd tot chirurgisch blok met gemiddeld 4,51 minuten (95% BI -5,89 tot -3,31 minuten).
Daarnaast werd een significant kortere tijd tot chirurgisch blok waargenomen bij zwangeren die een oplossing met fentanyl ontvingen dan zwangeren die een oplossing zonder fentanyl ontvingen. Dit resulteerde in een gemiddeld 2,02 minuten kortere tijd tot chirurgisch blok (95% BI -3,31 tot -0,73 minuten) vergeleken met oplossingen zonder fentanyl. Dit is een mogelijk klinisch relevant verschil.
De overige uitkomstmaten, zoals maternale en neonatale complicaties laten geen klinische relevante verschillen zien tussen de groepen. Door de opzet van deze richtlijn is ook bij deze uitgangsvraag het motorisch blok als uitkomstmaat meegenomen. Aangezien het hier om het verkrijgen van een chirurgisch blok gaat met daarbij automatisch een motorisch blok, is deze uitkomstmaat hier van geen waarde. De overall bewijskracht van de uitkomstmaten varieerde van zeer laag tot laag.
Waarden en voorkeuren van patiënten
Een goed werkende epiduraal kan vaak opgetopt worden. Mocht de epiduraal niet goed werken, dan zal overgegaan worden op spinale anesthesie of algehele anesthesie. Het is van belang dit van te voren met de zwangere te bespreken.
Kosten (middelenbeslag)
Het niet doen van een extra handeling en het gebruik van extra materialen bij een spinaal of algehele anesthesie kan kostenbesparend zijn. kostenbesparend werken.
Aanvaardbaarheid voor de overige relevante stakeholders
Voor de gynaecoloog is een snel zittend blok soms een voorwaarde voor goede zorg, met name in een spoedsituatie waarbij het kind zo snel mogelijk geboren moet worden. Dan kan wachten op het inwerken van de verdoving te lang duren. Het toevoegen van additieven (bijvoorbeeld adrenaline, bicarbonaat, opioïden, clonidine en dexmedetomidine) kan dan extra zinvol zijn. Voor voorbeelden van doseringen van adrenaline bij lidocaïne en fentanyl zie de module ‘Epidurale analgesie: doseringsstrategieën’.
Haalbaarheid en implementatie
Bij een goedzittende epiduraal kan er, wanneer de tijd toereikend is, opgetopt worden. In gevallen van extreme spoed zal men eerder overgaan op spinale anesthesie of algehele anesthesie.
Aanbeveling-1
Rationale/ balans tussen voor- en nadelen van de interventie
Zwangere vrouwen die lidocaïne + adrenaline ontvangen als oplossing om de epiduraal op te toppen hebben mogelijk een kortere tijd tot chirurgisch blok ten opzichte van ropivacaïne en bupivacaïne, dit terwijl er geen verschillen in beschreven bijwerkingen of complicaties worden waargenomen.
Een epidurale oplossing met fentanyl geeft mogelijk sneller chirurgisch blok vergeleken met oplossingen zonder fentanyl, dit terwijl er geen verschillen in bijwerkingen of complicaties worden waargenomen. De toevoeging van een opiaat aan de epidurale oplossing voor het optoppen van epiduralen is dan ook te adviseren. In de Nederlandse setting wordt met zowel fentanyl als met sufentanil gewerkt (zie ook de module ‘Epidurale analgesie: Opioïden’). Meerdere additieven zijn onderzocht met allen een effect op de snelheid en duur van het blok. Het voorheen toegevoegde bicarbonaat is niet meer gebruikelijk, vanwege risico’s op fouten bij mixen van medicatie en onvoldoende effect op snelheid van inwerken bij alkaliniseren van lokaal anesthetica voor epiduraal gebruik.
Aanbeveling-2
Rationale/ balans tussen voor- en nadelen van de interventie
In Sanders en Sng lijkt er een trend naar beter chirurgisch blok door ropivacaïne te bestaan dan bij bupivacaïne. Dit uit zich in een hogere kans op suppletie door middel van iv opioïden, epidurale top-up of lachgas bij bupivacaïne. Sanders geeft als mogelijke verklaring dat de hogere concentratie van ropivacaïne daar wellicht een rol bij speelt.
Aanbeveling-3
Rationale/ balans tussen voor- en nadelen van de interventie
Bij elke sectio is het streven om geen algehele anesthesie te geven. Wanneer er een epiduraal in situ is, zal dit de eerste keus zijn om een chirurgische blok te bewerkstelligen. Echter, wanneer een epiduraal niet goed heeft gezeten op de afdeling (geen of halfzijdig blok, meerdere interventies/top-ups door zorgverleners op de afdeling of ondanks recente extra bolus nog klachten van pijn bij parturiënt bij aankomst op OK) is de kans groot dat het bereiken van een chirurgisch blok door middel van het optoppen van de epiduraal niet of niet voldoende lukt (Mankowitz, 2016). De beste strategie is dan om primair voor een SSS (Single Shot Spinal) of CSE te kiezen. Als er recent (binnen 30 min) nog een bolus via de epiduraal gegeven is het raadzaam de spinale dosis lokaal anestheticum met 20-30% te reduceren (Depuydt, 2013). Dit is ook afhankelijk van gebruikelijke dosering spinaal, gebruik van additiva en lichaamshabitus van de vrouw. Als de laatste bolus via de epiduraal langer dan 30 minuten geleden is of er is geen aantoonbaar blok volstaat een normale spinale dosering (Dahl,2009). In alle gevallen dient natuurlijk rekening gehouden te worden met een spoed intubatie vanwege te hoog spinaal blok of total spinal.
Onderbouwing
Bij zwangeren die epidurale pijnbehandeling tijdens de baring hebben en alsnog een sectio caesarea moeten ondergaan kan, indien de epiduraal goed gewerkt heeft, deze ‘opgetopt’ worden. De resultaten hiervan wat betreft chirurgisch blok zijn wisselend (Bauer, 2012). Er is een gerede kans dat het blok onvoldoende werkt en extra pijnbehandeling via het infuus nodig is, een spinaal bijgezet moet worden of overgegaan moet worden op algehele anesthesie. De vraag is met welke combinatie van een lokaal anestheticum en additief een goed en snel anesthetisch blok bereikt wordt met de minste kans op complicaties of bijwerkingen.
Tijd tot chirurgisch blok
Vergelijking lokaal anesthetica
|
Laag GRADE |
De tijd tot chirurgisch blok lijkt significant korter na optoppen van de epiduraal met lidocaïne + adrenaline (eventueel plus fentanyl) vergeleken met (levo)bupivacaïne/ ropivacaïne.
Bronnen: (Balaji, 2009; Goring-Morris, 2006; Lucas, 1999; Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Tijd tot chirurgisch blok lijkt significant korter na het optoppen van een epiduraal met lidocaïne/ levobupivacaïne met additief versus zonder additief (fentanyl).
Bronnen: (Hong, 2010; Malhotra, 2007) |
|
Laag GRADE |
Er lijkt geen verschil in tijd tot chirurgisch blok na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016) |
Blokhoogte
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen klinisch relevant verschil in blokhoogte na het optoppen van een epiduraal met bupivacaïne versus lidocaïne plus adrenaline.
Bronnen: (Lucas, 1999) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen klinisch relevant verschil in blokhoogte na het optoppen van een epiduraal met lidocaïne met additief versus zonder additief (fentanyl).
Bronnen: (Hong, 2010) |
|
Laag GRADE |
Er lijkt geen klinisch relevant verschil in blokhoogte na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016) |
Pijnintensiteit
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in pijnintensiteit na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (eventueel met fentanyl).
Bronnen: (Allam, 2008; Lucas, 1999; Balaji, 2009; Goring-Morris, 2007; Sng, 2008) |
|
Laag GRADE |
Er lijkt geen verschil in pijnintensiteit na het optoppen van een epiduraal met levobupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in pijnscore na het optoppen van een epiduraal met levobupivacaïne met of zonder additief fentanyl.
Bronnen: (Malhotra, 2007) |
Cross-over naar andere pijnmedicatie/ aanvullende pijnmedicatie
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in aanvullende pijnmedicatie of algehele anesthesie na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (eventueel met fentanyl).
Bronnen: (Allam, 2008; Lucas, 1999; Balaji, 2009; Goring-Morris, 2007; Sng, 2008) |
|
Laag GRADE |
Er lijkt geen verschil in aanvullende pijnmedicatie of algehele anesthesie na het optoppen van een epiduraal met levobupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008; Sanders, 2004) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in aanvullende pijnmedicatie of algehele anesthesie na het optoppen van een epiduraal met lidocaïne met versus zonder additief fentanyl.
Bronnen: (Hong, 2010, Malhotra, 2007) |
|
Laag GRADE |
Er lijkt geen verschil in aanvullende pijnmedicatie na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016)) |
Hypotensie
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in het risico op hypotensie na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (evt. met fentanyl).
Bronnen: (Sng, 2008; Goring-Morris, 2006) |
|
Laag GRADE |
Er lijkt geen verschil in het risico op hypotensie na het optoppen van een epiduraal met (levo)bupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in het risico op hypotensie na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016) |
Motorisch blok
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in de mate van motorisch blok na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (met fentanyl).
Bronnen: (Sng, 2008) |
|
Laag GRADE |
Er lijkt geen verschil in de mate van motorisch blok na het optoppen van een epiduraal met (levo)bupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in de mate van motorisch blok na het optoppen van een epiduraal met levobupivacaïne met of zonder additief fentanyl.
Bronnen: (Malhotra, 2007) |
Misselijkheid/ braken
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in de mate van misselijkheid/braken na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (eventueel met fentanyl).
Bronnen: (Allam, 2008; Balaji, 2008; Goring-Morris, 2006; Sng, 2008) |
|
Laag GRADE |
Er lijkt geen verschil in de mate van misselijkheid/braken na het optoppen van een epiduraal met (levo)bupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in de mate van misselijkheid/braken na het optoppen van een epiduraal met lidocaïne/ levobupivacaïne met of zonder additief fentanyl.
Bronnen: (Hong, 2010; Malhotra, 2007) |
|
Laag GRADE |
Er lijkt geen verschil in het risico op misselijkheid na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016) |
Jeuk
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in jeuk na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (zonder fentanyl).
Bronnen: (Sng, 2008) |
|
Laag GRADE |
Er lijkt geen verschil in jeuk na het optoppen van een epiduraal met (levo)bupivacaïne versus ropivacaïne.
Bronnen: (Sng, 2008) |
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in jeuk na het optoppen van een epiduraal met lidocaïne/ levobupivacaïne met of zonder additief fentanyl.
Bronnen: (Sng, 2008 |
pH a. umbilicalis
Vergelijking lokaal anesthetica
|
Laag GRADE |
Er lijkt geen verschil in pH a. umbilicalis na het optoppen van een epiduraal met (levo)bupivacaïne versus lidocaïne + adrenaline (zonder fentanyl).
Bronnen: (Allam, 2008 |
Apgarscore
Vergelijking additieven
|
Laag GRADE |
Er lijkt geen verschil in het risico op Apgarscores < 7 bij 5 minuten bij neonaten na het optoppen van een epiduraal met lidocaïne + adrenaline versus lidocaïne + dexmedetomidine.
Bronnen: (Hasanein, 2016) |
Beschrijving studies
De meta-analyse van Hillyard (2011) is geïncludeerd en als uitgangspunt genomen. Hillyard (2011) includeerde 11 RCT’s met zwangere vrouwen die epidurale pijnbehandeling tijdens de baring kregen en alsnog een sectio caesarea moesten ondergaan. Twee van deze studies zijn alleen gepubliceerd als conference abstract en worden buiten beschouwing gelaten in deze literatuursamenvatting. Daarnaast vergeleek 1 studie epidurale pijnbehandeling met en zonder bicarbonaat (HCO3).
De 8 overige RCT’s includeerden totaal 615 zwangere vrouwen. De zwangeren kregen verschillende oplossingen van een lokaal anestheticum eventueel met additief om de epiduraal ‘op te toppen’ voor een sectio caesarea. De oplossingen werden door Hillyard (2011) in 3 groepen onderverdeeld: (1) 0,5% bupivacaïne of levobupivacaïne; (2) 1 of 2% lidocaïne en adrenaline, met of zonder fentanyl en (3) 0,75% ropivacaïne.
Aanvullend is de RCT van Hasanein (2016) geïncludeerd. Hasanein (2016) vergeleek lidocaïne/ adrenaline versus lidocaïne/ dexmedetomidine bij 60 zwangere vrouwen die epidurale pijnbehandeling tijdens de baring kregen en alsnog een sectio caesarea moesten ondergaan.
Tabel 1 Top-up oplossingen epidurale analgesie per geïncludeerde studie
|
Auteur, jaartal |
Top-up groep 1 |
Top-up groep 2 |
Top-up groep 3 |
|
Sanders 2004 |
0,5% bupivacaïne (20 ml) |
|
0.75% ropivacaïne (20 ml) |
|
Sng 2008 |
0,5% levobupivacaïne (15 ml) |
2% lidocaïne/ adrenaline (1:200.000) and 50 µg fentanyl (total: 15 ml) |
0.75% ropivacaïne (15 ml) |
|
Balaji 2009 |
0,5% levobupivacaïne (20 ml) |
2% lidocaïne/ 100 μg adrenaline and 100 µg fentanyl (total: 22,1 ml) |
|
|
Goring-Morris 2006 |
0,5% bupivacaïne (20 ml) |
2% lidocaïne (20 ml)/ 100 μg adrenaline and 100 µg fentanyl (total: 22,1 ml) |
|
|
Lucas 1999 |
0,5% bupivacaïne |
2% lidocaïne/ adrenaline (1:200.000) |
0.5% bupivacaïne and 2% lidocaïne/ adrenaline (1:200.000) |
|
Allam 2008 |
0,5% levobupivacaïne (20 ml) |
1.8% lidocaïne (20 ml)/ 0,1 ml adrenaline (1:1000) and 8,4% HCO3 (2 ml) |
|
|
Hong 2010 |
|
2% lidocaïne (20 ml)/ adrenaline (1:200.000) |
2% lidocaïne (20 ml)/ adrenaline (1:200:000) and 100 µg fentanyl (2 ml) |
|
Malhotra 2007 |
0,5% levobupivacaïne (20 ml) |
0.5% levobupivacaïne (20 ml) + 75 µg fentanyl (1,5 ml) |
|
|
Hasanein 2016 |
2% lidocaïne (19 ml)/ adrenaline 5 μg (1 ml) (1:200.000) |
2% lidocaïne (19 ml)/ dexmedetomidine 1 μg/kg (1 ml) |
|
Nb. Lidocaïne 1,8% komt door de verdunning van 18cc lidocaïne2% met 2 cc HCO3 erbij. Officieel zou 19 cc lidocaïne2% met 1 cc adrenaline dan ook 20 cc 0,19% zijn. Deze concentratie verschillen zijn te verwaarlozen
Op basis van de geïncludeerde studies worden de volgende vergelijkingen in een literatuuranalyse uitgewerkt:
Vergelijking lokaal anesthetica
- (Levo)bupivacaïne versus lidocaïne plus adrenaline (evt. plus fentanyl).
- (Levo)bupivacaïne versus ropivacaïne.
Vergelijking additieven
- Lidocaïne/ levobupivacaïne plus fentanyl versus lidocaïne/ levobupivacaïne zonder fentanyl
- Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Resultaten
Tijd tot chirurgisch blok
Negen studies rapporteerden de tijd tot chirurgisch blok, welke op verschillende manieren werd gedefinieerd: Sanders 2004; Sng, 2008; Lucas, 1999; Allam, 2008; Hong, 2010; Malhotra, 2007; rapporteerden de tijd vanaf het eind van de top-up tot koude blok T4. Balaji (2009) rapporteerde de tijd vanaf het eind van de top-up tot diepe tastzin T7 en Goring-Morris (2006) rapporteerde de tijd vanaf het starten van de top-up tot diepe tastzin T7. Hasanein (2016) rapporteerde de tijd vanaf het eind van de top-up tot koude blok T4 aan beide kanten gemeten.
Vergelijking lokaal anesthetica
Lidocaïne plus adrenaline (eventueel plus fentanyl) versus (levo)bupivacaïne/ ropivacaïne
De meta-analyse van Hillyard includeerde 5 studies (de studie van Sng twee maal vanwege het feit dat twee van de drie armen voldoenaan deze vergelijking) die lidocaïne plus adrenaline (eventueel plus fentanyl) (n= 170) vergeleken met (levo)bupivacaïne of ropivacaïne (n= 176). Bij de zwangeren die lidocaïne + adrenaline kregen als oplossing om de epiduraal op te toppen duurde de tijd tot chirurgisch blok gemiddeld 1.66 minuten korter (95% BI -2,40 tot -0,91) vergeleken met (levo)bupivacaïne of ropivacaïne. Dit is een klinisch relevant verschil. Er was sprake van grote mate van heterogeniteit (I2 83%).
Figuur 1 Tijd tot chirurgisch blok (minuten) vergelijking lidocaïne plus adrenaline (eventueel plus fentanyl) versus (levo)bupivacaïne/ ropivacaïne
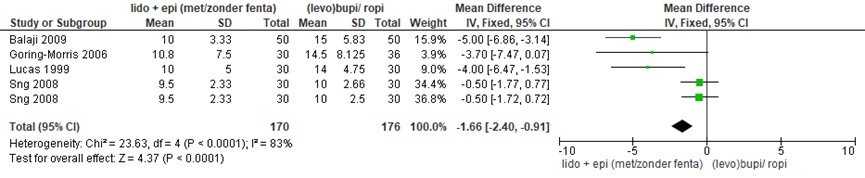
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Hillyard (2011)
Vergelijking additieven
Lidocaïne/ levobupivacaïne met fentanyl versus lidocaïne/ levobupivacaïne zonder fentanyl Twee studies vergeleken oplossingen met fentanyl (n= 82) met oplossingen zonder fentanyl (n= 84). Bij de zwangeren die een oplossing met fentanyl kregen was tijd tot chirurgisch blok gemiddeld 2,02 minuten korter (95% BI -3,31 tot -0,73) vergeleken met oplossingen zonder fentanyl. Dit is een klinisch relevant verschil. Er was geen sprake van heterogeniteit (I2 11%).
Figuur 2 Tijd tot chirurgisch blok (minuten) vergelijking oplossing met en zonder fentanyl
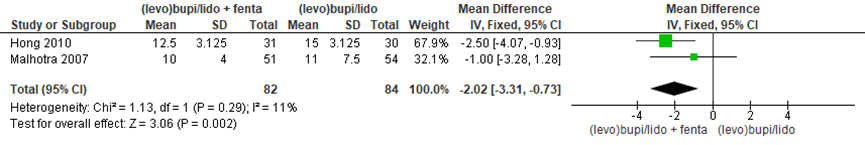
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval. Bron: Hillyard (2011)
Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Hasanein (2016) rapporteerde de tijd vanaf het eind van de top-up tot verlies van koud sensatie T4 aan beide kanten bij 30 zwangeren per behandelarm. Dit was in beide groepen 10 minuten (SD=1 in de lidocaïne/ adrenaline versus SD=0 in de lidocaïne/ dexmedetomidine groep).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat tijd tot chirurgisch blok is met twee niveaus verlaagd gezien heterogeniteit tussen de studies, zoals het gebruik van verschillende oplossingen van lokaal anestheticum/additieven (indirectheid) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Blokhoogte
Drie studies rapporteerden de blokhoogte bij 181 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline
Lucas (1999) vond een mediane blokhoogte van T3 in beide groepen, de interkwartielrange (IQR) varieerde van IQR T3 tot T4 bij 30 zwangeren die een 0,5% bupivacaïne oplossing kregen versus IQR T2 tot T4 bij 30 zwangeren die 2% lidocaïne/ adrenaline oplossing kregen.
Vergelijking additieven
Lidocaïne met fentanyl versus lidocaïne zonder fentanyl
Hong (2010) rapporteerde een mediane blokhoogte van T1 (range C8 tot T3) bij 31 zwangeren die een lidocaïne plus adrenaline oplossing met fentanyl kregen versus een mediaan van T3 (range T2 tot T4) in de groep met 30 zwangeren die deze oplossing zonder fentanyl kreeg.
lidocaïneplus adrenaline versus lidocaïneplus dexmedetomidine
Hasanein (2016) rapporteerde de blokhoogte. In de lidocaïne plus adrenaline-groep (n=30) was het mediane niveau/dermatoom T3 (range T1 tot T4) versus T3 (range T2 tot T4) in de groep (n=30) die lidocaïne plus dexmedetomidine kregen.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat niveau/ blokhoogte is met twee niveaus verlaagd gezien heterogeniteit tussen de studies, zoals het gebruik van verschillende oplossingen van lokaal anestheticum/additieven (indirectheid) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Pijnintensiteit
De pijnintensiteit (VAS) tijdens de sectio caesarea werd in 8 studies bij 539 zwangeren gerapporteerd. De meeste studies rapporteerden de mediane VAS-score met interkwartielrange (IQR) waardoor de data niet gepoold is.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (eventueel met fentanyl)
Twee studies (Allam, 2008; Lucas, 1999) rapporteerden de VAS pijnscores. Allam (2008) vergeleek levobupivacaïne versus lidocaïne plus epineprine (n= 46) en rapporteerde een mediane VAS-score van 1 in beide groepen (IQR 1-1 versus 1-1,3). Lucas (1999) rapporteerde een VAS-score voor kwaliteit van het blok, waarbij 0= ernstige pijn en 10 = geen pijn. De mediane VAS-score van 9,2 (IQR 2-10) in de groep met 0,5% bupivacaïne oplossing versus 8,9 (IQR 8,1-10) in de groep met 2% lidocaïne plus adrenaline (n= 60).
Drie studies (Balaji, 2009; Goring-Morris, 2007; Sng, 2008) rapporteerden de VAS-score bij zwangeren die (levo)bupivacaïne kregen versus zwangeren die een oplossing van lidocaïne plus adrenaline en fentanyl kregen. Sng (2008) rapporteerden een mediane VAS-score van 3,5 (IQR 3 tot 4) versus 3 (IQR 3 tot 4) en de studie van Goring-Morris (2007) rapporteerde een VAS-score van 0 (IQR 0 tot 0,25) versus 0 (IQR 0 tot 0,023). De studie van Balaji (2009) rapporteerde een gemiddelde VAS-score van 0,28 (SD 0,89) in de groep met (levo)bupivacaïne versus 0,11 (SD 0,44) in de groep met lidocaïne plus adrenaline en fentanyl. De waargenomen verschillen zijn niet significant of klinisch relevant.
Levobupivacaïne versus ropivacaïne
Sng (2008) rapporteerde een mediane VAS-score van 3 (IQR 3 tot 4) in de groep met levobupivacaïne versus 3,5 (IQR 3 tot 4) in de groep met ropivacaïne. Dit is geen klinisch relevant verschil.
Vergelijking additieven
Levobupivacaïne met fentanyl versus levobupivacaïne zonder fentanyl
Malhotra (2007) rapporteerde de pijnintensiteit bij 105 zwangeren behandeld met levobupivacaïne met versus zonder fentanyl. De mediane VAS-score was 0 (IQR 0 tot 1) in de groep met fentanyl versus 0 (IQR 0 tot 0) in de groep zonder fentanyl. Dit is geen klinisch relevant verschil.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pijnintensiteit is met twee niveaus verlaagd gezien heterogeniteit tussen de studies, zoals het gebruik van verschillende oplossingen van lokaal anestheticum/additieven (indirectheid) en het geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Cross-over naar andere pijnmedicatie/ aanvullende pijnmedicatie
Negen studies rapporteerden intra-operatieve bloksuppletie bij 599 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (eventueel met fentanyl)
Vijf studies (n= 299) vergeleken (levo)bupivacaïne versus lidocaïne + adrenaline (met/ zonder fentanyl) en rapporteerden het aantal zwangeren waarbij intra-operatieve bloksuppletie nodig was. Er werd geen significant verschil waargenomen tussen de groepen (RR 1,58 (95% BI 0,91 tot 2,76)). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 3 Intra-operatieve bloksuppletie (Levo)bupivacaïne versus Lidocaïne/ adrenaline (met en zonder fentanyl)
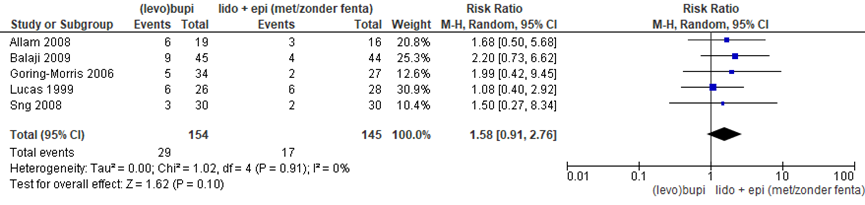
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Daarnaast hadden 3 (1,9%) zwangeren behandeld met (levo)bupivacaïne algehele anesthesie nodig versus 4 (2,8%) zwangeren met lidocaïne + adrenaline, waarbij geen significant verschil tussen de groepen (risico verschil -0,01 (95% BI -0,05 tot 0,04)). Er was sprake van enige heterogeniteit (I2 33%).
Figuur 4 Algehele anesthesie (Levo)bupivacaïne versus lidocaïne/ adrenaline (met en zonder fentanyl)
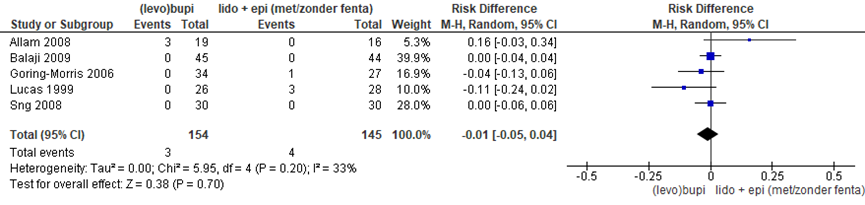
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
(Levo)bupivacaïne versus ropivacaïne
Twee studies vergeleken (levo)bupivacaïne met ropivacaïne en rapporteerden intra-operatieve bloksuppletie. Er werd geen significant verschil waargenomen tussen de groepen (RR 3,01 (95% BI 0,95 tot 9,53)). Er was geen sprake van heterogeniteit (I2 10%).
Daarnaast had één zwangere in de (levo)bupivacaïne groep algehele anesthesie nodig (risico verschil 0,01 (95% BI -0,05 tot 0,07)).
Figuur 5 Intra-operatieve bloksuppletie (levo)bupivacaïne versus ropivacaïne
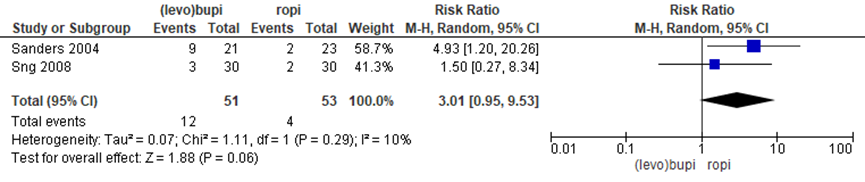
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Vergelijking additieven
Lidocaïne of levobupivacaïne met fentanyl versus lidocaïne of levobupivacaïne zonder fentanyl
Twee studies rapporteerden het aantal zwangeren dat aanvullende pijnmedicatie kreeg wanneer lidocaïne/ levobupivacaïne + fentanyl versus zonder fentanyl gegeven werd. Er werd geen significant verschil waargenomen tussen de groepen (RR 0,56 (95% BI 0,04 tot 0,73)). Er was sprake van grote mate van heterogeniteit (I2 85%).
Figuur 6 Aanvullende pijnmedicatie met fentanyl versus zonder fentanyl
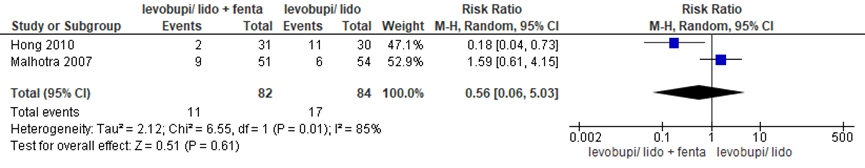
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Daarnaast hadden 2 zwangeren (2,4%) in de fentanyl groep versus 3 (3,6%) zwangeren in de groep zonder fentanyl algehele anesthesie nodig (RD -0,01 (95% BI -0,07 tot 0,04). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 7 Algehele anesthesie met fentany versus zonder fentanyl
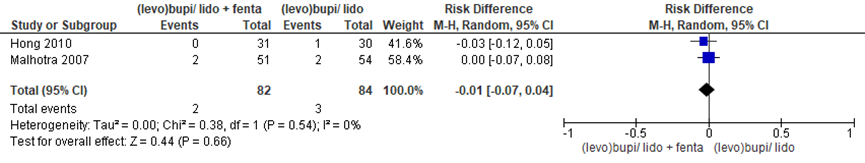
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Hasanein (2016) rapporteerde hoeveel zwangeren aanvullend intraveneus fentanyl nodig hadden. In de lidocaïne/ adrenaline groep hadden 11 (33,3%) van de 30 zwangeren aanvullend fentanyl nodig versus 4 (13,3%) van de 30 zwangeren in de lidocaïne plus dexmedetomidine groep (RR 2,50 (95% BI 0,88 tot 7,10)). Hasanein (2016) rapporteerde niet over algehele anesthesie.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat cross-over naar andere pijnmedicatie/ aanvullende pijnmedicatie is met twee niveaus verlaagd gezien de geringe studiepopulatie, het zeer geringe aantal events en/of brede betrouwbaarheidsintervallen (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Maternale complicaties
Hypotensie
Vier studies rapporteerden hypotensie bij 272 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (eventueel met fentanyl)
Sng (2008) rapporteerde geen significant verschil in hypotensie tussen de levobupivacaïne versus de lidocaïne + adrenaline groep (RR 0,78 (95% BI 0,33, 1,82)). Ook de studie van Goring-Morris (2006) rapporteerde geen significant verschil in systolisch druk (<100 mmHg) tussen de bupivacaïne groep versus de lidocaïne + adrenaline-groep (RR 0,91 (95% BI 0,60 tot 1,40)).
(Levo)bupivacaïne versus ropivacaïne
Sng (2008) rapporteerde geen significant verschil in hypotensie tussen de levobupivacaïne versus de ropivacaïne groep (RR 0,88 (95% BI 0,36 tot 2,11)).
Vergelijking additieven
Lidocaïne met fentanyl versus lidocaïne zonder fentanyl
Hong (2010) rapporteerde geen significant verschil in hypotensie tussen de groep met fentanyl versus de groep zonder fentanyl (RR 0,24 (95% BI 0,06 tot 1,05)).
Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Hasanein (2016) rapporteerde geen significant verschil in hypotensie tussen de lidocaïne + adrenaline groep versus de lidocaïne + dexmedetomidine groep (RR 0,60 (95% BI 0,16 tot 2,29)).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypotensie is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Motorisch blok
Twee studies rapporteerden de Bromage score bij 202 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (met fentanyl)
Sng (2008) rapporteerde geen verschil in Bromage score, met een mediane score van 2 (alleen de voet kunnen bewegen) met een interkwartielrange (IQR) van 1-2 (in staat om knie en voet te bewegen) in beide groepen.
(Levo)bupivacaïne versus ropivacaïne
Sng (2008) rapporteerde een mediane Bromage score van 2 (alleen de enkel kunnen bewegen) met een interkwartielrange van 1 tot 2 (in staat om knie en enkel op te heffen) in de levobupivacaïne groep versus een mediane Bromage score van 1 (IQR 1 tot 2) in de ropivacaïne-groep.
Vergelijking additieven
Levobupivacaïne met fentanyl versus levobupivacaïne zonder fentanyl
Malhotra (2007) rapporteerde dezelfde mediane Bromage score en interkwartielafstand in de groep zwangeren met en zonder fentanyl (1 (IQR 1 tot 2)) bij totaal 105 zwangeren.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat motorisch blok is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Misselijkheid/ braken
Vijf studies namen misselijkheid en/of braken mee als uitkomstmaat bij totaal 412 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (eventueel met fentanyl)
In de (levo)bupivacaïne had 26,3% van de zwangeren last van misselijkheid/ braken versus 24,4% van de in de lidocaïne/ adrenaline groep, waarbij geen significant verschil tussen de groepen (RR 1,06 (95% BI 0,69 tot 1,62)). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 8 Misselijkheid (levo)bupivacaïne versus lidocaïne/ adrenaline (met en zonder fentanyl)
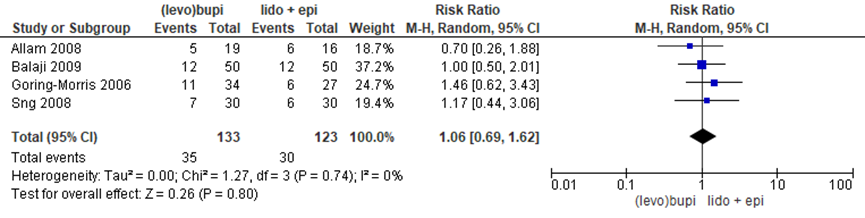
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
(Levo)bupivacaïne versus ropivacaïne
Sng (2008) rapporteerde misselijkheid/ braken bij 23,3% van de zwangeren in de levobupivacaïne versus 20% van de zwangeren in de ropivacaïne groep, waarbij geen significant verschil tussen de groepen (RR 1,17 (95% BI 0,44 tot 3,06)).
Vergelijking additieven
Lidocaïne of levobupivacaïne met fentanyl versus lidocaïne of levobupivacaïne zonder fentanyl
Twee studies die oplossingen met en zonder fentanyl vergeleken rapporteerden misselijkheid/ braken. In de fentanyl-groep had 34,1% van de zwangeren last van misselijkheid/ braken versus 21,4% in de groep zonder fentanyl, waarbij geen significant verschil tussen de groepen (RR 0,91 (95% BI 0,08 tot 10,62)). Er was sprake van een grote mate van heterogeniteit (I2 90%).
Figuur 9 Misselijkheid (met versus zonder fentanyl)
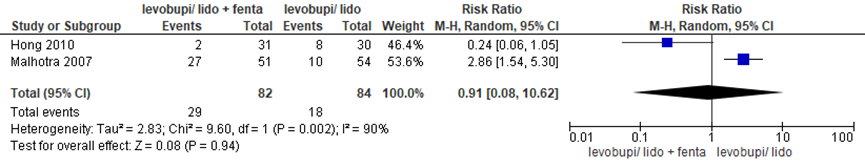
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Hasanein (2016) rapporteerde bij 10% van de zwangeren misselijkheid of braken in de lidocaïne + adrenaline-groep versus 13,3% in de lidocaïne + dexmedetomidine-groep, waarbij geen significant verschil tussen de groepen (RR 0,75 (95% BI 0,18 tot 3,07)).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat misselijkheid/ braken is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten en brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Jeuk
Vier studies namen jeuk mee als uitkomstmaat bij totaal 356 zwangeren.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (zonder fentanyl)
Geen van de zwangeren binnen de studie van Sng (2008) (n= 60) rapporteerden jeuk. In de studie van Balaji (2009) (n=100) werd geen significant verschil in jeuk waargenomen tussen de levobupivacaïne groep versus de lidocaïne + adrenaline-groep (RR 0,40 (95% BI 0,13 tot 1,19)) of postoperatieve jeuk (RR 0,31 (95% BI 0,11 tot 0,88)).
(Levo)bupivacaïne versus ropivacaïne
Geen van de zwangeren binnen de studie van Sng (2008) n= 60) rapporteerden jeuk.
Vergelijking additieven
Lidocaïne of levobupivacaïne met fentanyl versus lidocaïne of levobupivacaïne zonder fentanyl
Er werden geen significante verschillen waargenomen in jeuk tussen de fentanyl-groep versus de groep zonder fentanyl (RR 0,95 (95% BI 0,35 tot 10,91)). Er was geen sprake van heterogeniteit (I2 0%).
Figuur 10 Jeuk (met versus zonder fentanyl)
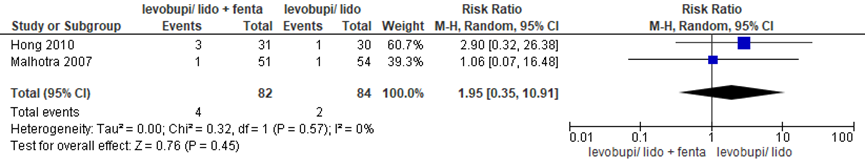
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat jeuk is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten en brede betrouwbaarheidsinterval (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Neonatale complicaties
pH a. umbilicalis
Eén studie rapporteerde de pH a. umbilicalis bij totaal 46 neonaten.
Vergelijking lokaal anesthetica
(Levo)bupivacaïne versus lidocaïne plus adrenaline (zonder fentanyl)
Allam (2008) rapporteerde een pH a. umbilicalis gemiddelde van 7,3 (SD 0,1) in beide groepen met totaal 35 zwangeren.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat pH a. umbilicalis is met twee niveaus verlaagd gezien het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Apgarscore
Eén studie rapporteerde het aantal neonaten met een Apgarscore < 7 bij 5 minuten (n=60).
Vergelijking additieven
Lidocaïne plus adrenaline versus lidocaïne plus dexmedetomidine
Geen van de zwangeren binnen de studie van Hasanein (2016) (30 zwangeren per arm) rapporteerden neonaten met een Apgarscore < 7.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat Apgarscore < 7 bij 5 minuten is met twee niveaus verlaagd het zeer geringe aantal patiënten (imprecisie). Het niveau van bewijskracht wordt gegradeerd als ‘laag’.
Geen van de studies naar combinaties van lokaal anestheticum en additief rapporteerden de uitkomstmaten: tevredenheid ten aanzien van pijnstilling, borstvoeding, maternale complicaties: convulsie/ eclamptisch insult, fluxus post-partum, postspinale punctie hoofdpijn, urineretentie, epiduraal abces/ hematoom, neonatale complicaties: opname NICU, foetale hartslag afwijkingen, temperatuur, mortaliteit, negatieve uitkomsten voor de baby op lange termijn en kosten.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Middels welke combinatie van lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) evt. met additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl) wordt snel en voldoende anesthetisch blok bereikt met de minste kans op complicaties of bijwerkingen?
P: zwangere vrouwen met een epiduraal in situ waarvoor optoppen noodzakelijk is vanwege conversie naar een sectio-caesarea;
I: De volgende combinaties van lokaal anestheticum (LA) evt. met additief worden onderling vergeleken (bij comparison staan dus dezelfde middelen genoteerd):
- Lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) zonder additief.
- Lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) met additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl)*.
C:
- Lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) zonder additief.
- Lokaal anestheticum (lidocaine of ropivacaïne of (levo)bupivacaïne) met additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl)*.
*NB: uitzondering is de combinatie ropivacaïne met epineprine, wordt niet gezamenlijk toegediend.
O: zie onderstaand:
- Tijd tot chirurgisch blok.
- oogte van het blok.
- Pijnintensiteit (VAS/ NRS-schaal of een ander gevalideerd instrument).
- Cross-over naar andere pijnmedicatie/aanvullende pijnmedicatie.
- Tevredenheid ten aanzien van pijnstilling (rapportcijfer/ VAS/ NRS-schaal of een ander gevalideerd instrument).
- Borstvoeding.
- Maternale complicaties: convulsie/ eclamptisch insult, fluxus postpartum, ademhalingsdepressie, bevallingsduur, hypotensie, temperatuur, urineretentie, misselijkheid/braken, jeuk, mate van motorisch blok, postspinale punctie hoofdpijn, epiduraal abces/ hematoom.
- Neonatale complicaties: opname NICU, Apgarscore < 7 bij 5 min, foetale hartslag afwijkingen, temperatuur, pH a. umbilicalis, negatieve uitkomsten voor de baby op lange termijn.
- Maternale/ neonatale sterfte.
- Kosten.
Relevante uitkomstmaten
De werkgroep definieerde pijnintensiteit, tevredenheid ten aanzien van pijnstilling en maternale/ neonatale sterfte als kritieke uitkomstmaten voor de besluitvorming. De uitkomstmaat tijd tot chirurgisch blok is voor de besluitvorming een belangrijke uitkomstmaat.
De werkgroep definieerde de uitkomstmaten als volgt: pijnintensiteit (VAS-schaal 3 tot 5-10/ NRS schaal 100) en tevredenheid (rapportcijfer 1 tot 10) gemeten volgens gevalideerde instrumenten, waarbij scores door de patiënt zelf gedurende of direct na de bevalling gerapporteerd (vragenlijsten achteraf werden geëxcludeerd). De werkgroep definieerde niet a priori de genoemde overige uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Naast significantie wordt de klinische besluitvorming vooral bepaald door de klinische relevantie van de waargenomen verschillen tussen behandelopties. Minuten verschil in tijd tot chirurgisch blok kunnen het verschil tussen leven en dood betekenen voor de neonaat tijdens een spoed sectio. Hiernaast zal het verschil voor de parturïent op dat moment betekenen dat ze wel of geen pijn bij incisie heeft. Voor dichotome uitkomstmaten definieerde de werkgroep een minimaal klinisch (patiënt) relevant verschil volgens de grenzen van de GRADE-working group, namelijk een verschil in relatief risico van 25%. Voor de continue uitkomstmaten definieerde de werkgroep een verschil van 10% op pijnintensiteit of tevredenheid als een klinisch (patiënt) relevant verschil.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID), Embase (via Embase.com) en de Cochrane Library (via Wiley) is op 30 april 2018 met relevante zoektermen gezocht naar Engelstalige systematische reviews, gerandomiseerde gecontroleerde studies (RCT’s), gecontroleerde klinische studie (CCTs) en vergelijkend observationeel onderzoek studies gepubliceerd vanaf 1946 die een combinatie van lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaine) en additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl) onderzochten voor het bereiken van een anesthetisch blok wanneer zwangeren epidurale pijnbehandeling tijdens de baring hebben en alsnog een sectio caesarea moeten ondergaan. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 84 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- Studiedesign RCT.
- Voldoet aan de PICO.
- Beschrijven van minimaal één van de bovengenoemde uitkomstmaten.
Op basis van titel en abstract werden in eerste instantie 23 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 21 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 1 systematisch review en 1 RCT definitief geselecteerd. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Bauer ME, Kountanis JA, Tsen LC, Greenfield ML, Mhyre JM. Risk factors for failed conversion of labor epidural analgesia to cesarean delivery anesthesia: a systematic review and meta-analysis of observational trials. Int J Obstet Anesth. 2012 Oct;21(4):294-309. doi: 10.1016/j.ijoa.2012.05.007. Epub 2012 Aug 20. Review. PubMed PMID: 22918030.
- Visser, WA, Dijkstra, A, Albayrak M, Gielen MJ, Boersma E, Vonsée HJ. Spinal anesthesia for intrapartum Cesarean delivery following epidural labor analgesia: a retrospective cohort study. Canadian Journal of Anesthesia/Journal canadien d'anesthésie, 2009, 56.8: 577-583.
- Depuydt E, Van de Velde M. Unplanned cesarean section in parturients with an epidural catheter in-situ: how to obtain surgical anesthesia. Acta Anaesthesiol Belg, 2013, 64.2: 61-74.
- Dahl V, Spreng UJ. Anaesthesia for urgent (grade 1) caesarean section. Current Opinion in Anesthesiology, 2009, 22.3: 352-356.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: Middels welke combinatie van lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) en additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl) wordt snel en voldoende anesthethisch blok bereikt?
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Hillyard, 2011 |
Yes |
Yes |
Included: yes, excluded: no |
No* |
Not applicable |
Yes |
Yes |
Yes |
SR: yes, included studies: unclear |
*Patient characteristics are not described
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy - otherwise the evidence table for studies of diagnostic test accuracy should be used.
Research question: Middels welke combinatie van lokaal anestheticum (lidocaïne of ropivacaïne of (levo)bupivacaïne) en additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl) wordt snel en voldoende anesthethisch blok bereikt?
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Hasanein, 2016 |
Type of study: RCT
Setting: Saad Specialist Hospital, Alkhobar, Saudi Arabia
Country: Saudi Arabia
Source of funding: not reported |
Inclusion criteria: Emergency cesarean section in the absence of maternal or fetal compromise (category 2, 3), well-functioning epidural catheter (required 2 or less intra-partum supplementation with bupivacaine 0.125%), and uncomplicated pregnancy with singleton pregnancy P36 weeks of gestation.
Exclusion criteria: Emergency caesarean section with maternal or fetal compromise (category 1), a poorly functioning epidural catheter during the labor, if narcotics or alpha 2 agonists rather than our regimen was given within the previous 4 h, last intrapartum supplementation of epidural catheter less than 2 h and if the parturient had preeclampsia or eclampsia, bleeding, liver impairment, renal impairment, diabetes mellitus or cardiac disease.
N total at baseline: Intervention: 30 Control: 30
Important prognostic factors2: Age, mean (SD): I: 28 (3) C: 28 (1)
Gestational age (weeks): I: 39 (2) C: 39 (2)
Pre-existing VAS I: 2.5 (2-3) C: 2 (2-3)
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test):
The routine method used for epidural labor analgesia was the administration of a bolus of 10 ml 0.125% bupivacaine with 50 µg fentanyl followed by a continuous infusion at a constant rate (10–12 ml/h) of 0.125% bupivacaine with 2 µg/ml fentanyl. An additional bolus of 5 ml 0.125% bupivacaine was supplemented when required aiming to have adequate analgesia for labor up to T10 level.
Lidocaine adrenaline 19 ml of lidocaine 2% and 1 ml containing 5 µg (1:200.000) adrenaline (Daihan Pharm Co., Seoul, Korea)
|
Describe control (treatment/procedure/test):
The routine method used for epidural labor analgesia was the administration of a bolus of 10 ml 0.125% bupivacaine with 50 µg fentanyl followed by a continuous infusion at a constant rate (10–12 ml/h) of 0.125% bupivacaine with 2 µg/ml fentanyl. An additional bolus of 5 ml 0.125% bupivacaine was supplemented when required aiming to have adequate analgesia for labor up to T10 level.
Lidocaine dexmedetomidine 19 ml of lidocaine and 1 ml containing 1 µg/kg dexmedetomidine (Precedex, Hospira, Lake Forest, IL, USA) |
Length of follow-up: after deliveru
Loss-to-follow-up: 0
Incomplete outcome data: 0
|
Outcome measures and effect size (include 95%CI and p-value if available):
Degree of sedation Fully awake (I/C): 19 (63.3%)/ 2 (6.7%) Calm: 8 (26.7)/ 5 (16.7%) Awake on verbal commands: 3 (10%)/ 9 (30%) Awake on gentle tactile stimulation: 0/ 14 (46.6%) P<0.001
Max block height, median (range) I: T3 (T1-T4) C: T3 (T2-T4) NS
Time to maximum block (min), mean (SD) I: 12 (1) C: 12 (1) NS
Time to loss of cold sensation to T4 on both sides (min), mean (SD) I: 10 (1) C: 10 (0) NS
Patients requiring fentanyl supplementation (n) I: 11 (33.3%) C:4 (13.3%) P<0.05
Mean total fentanyl used (µg) I: 34 (13) C: 25 (0) P<0.001
Time to delivery (min), mean (SD) I: 16 (1) C: 15 (1) NS
Maternal complications Hypotension (I/C): 3 (10%)/ 5 (16.6%) NS
Bradycardia (I/C): 0/ 9 (30%) P<0.001
Nausea, vomiting (I/C): 3 (10%)/ 4 (13.3%) NS
Dizziness (I/C): 0/ 0
Respiratory depression (I/C): 0/ 0
Neonatal outcomes Apgarscore < 7 (I/C): 0/ 0 |
Author’s conclusion: Epidural dexmedetomidine is comparable to adrenaline as an adjuvant to epidural lidocaine in fastening the onset of surgical anesthesia and resulted in better intraoperative analgesia and in longer duration of sensory and motor block in the settings of converting labor epidural analgesia for emergency caesarean section. |
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Risk of bias table for intervention studies (randomized controlled trials)
Research question: Middels welke combinatie van lokaal anestheticum (lidocaine of ropivacaine of (levo)bupivacaïne) en additief (adrenaline of clonidine of dexmedetomidine of bicarbonaat of sufentanil of fentanyl) wordt snel en voldoende anesthethisch blok bereikt?
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Hasanein, 2016 |
Patients were randomly assigned by computer-generated random numbers using sealed envelopes to one of two groups. |
Unlikely |
Unlikely |
Unlikely |
Unclear |
Unlikely |
Unlikely |
Unlikely |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules.
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Anonymous, Obstetric Anaesthetists' Association 2012 |
Conference abstracts |
|
Eley 2015 |
Vergelijking voldoet niet aan de PICO (failure rate extending labour BMI>40 versus BMI<40) |
|
Ismail 2015 |
Voldoet niet aan PICO (gaat over risicofactoren voor slagen conversie, CS rate of assisted delibery rate bij epiduraal) |
|
Varón 2015 |
Voldoet niet aan PICO (gaat over voorspellende factoren falen epiduraal) |
|
Hong 2010 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Balaji 2009 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Allam 2008 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Regan 2008 |
Beschrijvende survey studie |
|
Sng 2008 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Allam 2007 |
Conference abstract |
|
Balaji 2007 |
Conference abstract |
|
Malhotra 2007 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Goring-Morris 2006 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Bolad 2005 |
Conference abstract |
|
Rho 2005 |
Artikel in Koreaans |
|
Sanders 2004 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Sanders 2004 |
Conference abstract |
|
Lam 2001 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Lucas 1999 |
Geïncludeerd in meta-analyse Hillyard 2011 |
|
Lucas 1999 |
Conference abstract |
|
Gaiser 1998 |
Geïncludeerd in meta-analyse Hillyard 2011 |
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-07-2020
Beoordeeld op geldigheid : 03-07-2020
Bij het opstellen van de modules heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodules komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De andere aan deze richtlijnmodule deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijnmodule delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Optoppen epiduralen |
NVA |
2019 |
2024 |
5-jaarlijks |
NVA |
Nieuwe evidence/inzichten |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Patiëntenfederatie Nederland
De ontwikkeling van de richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodules.
Samenstelling werkgroep
- Dr. W.L.M.C.M. Schellekens, extern voorzitter
- Drs. I.C.M. Beenakkers, anesthesioloog, werkzaam in het UMC Utrecht, NVA
- Drs. F.A. Klerk, anesthesioloog, werkzaam in het Diakonessenhuis Utrecht, NVA
- Drs. C.E. Kam-Endtz, anesthesioloog, werkzaam in het Haaglanden Medisch Centrum, NVA
- Dr. F.T.H. Lim, gynaecoloog, werkzaam in het IJssellandziekenhuis, NVOG
- Dr. L.M. Freeman, gynaecoloog, werkzaam in het Ikazia Ziekenhuis Rotterdam, NVOG
- Dr. J.M. Middeldorp, gynaecoloog, werkzaam in het Leids Universitair Medisch Centrum, NVOG
- Drs. A.G. Kaspers, kinderarts, werkzaam in het Medisch Spectrum Twente, NVK
- Drs. L.A.M. Moll, klinisch verloskundige, werkzaam in het St. Antonius Ziekenhuis Nieuwegein, KNOV
- Dr. J. de Boer, beleidsmedewerker bij KNOV
- Drs. S. Ratsma-Wesselius, Obstetrisch verpleegkundige, werkzaam bij het Amsterdam UMC, Locatie AMC, V&VN
- Dr. J.E. Nagtegaal, Ziekenhuisapotheker, werkzaam in het Meander Medisch Centrum, NVZA
- Dr. A.M.D.E. Timmerman, Klinisch Fysicus, werkzaam in het UMC Utrecht, NVKF
- Drs. J.C. Mooij, adviseur patiëntenbelang, Patiëntenfederatie Nederland.
Met ondersteuning van
- Dr. E.M.E. den Breejen, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Dr. W.J. Harmsen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Schellekens |
gepensioneerd, ZZP: strategisch adviseur |
Lid RvT Diakonessenhuis, Utrecht |
Geen |
Geen |
|
Klerk |
Staf Anesthesiologie Diakonessenhuis Utrecht. |
bestuurslid Obst. Anesth. onbetaald |
Geen |
Geen |
|
Ratsma Wesselius |
Senior verpleegkundige Verloscentrum AMC |
Gastdocent VU Amstel Academie verpleegkundige vervolgopleidingen Obstetrie, betaald |
Geen |
Geen |
|
Beenakkers |
Anesthesioloog WKZ/UMCU |
Voorzitter sectie obstetrische anesthesie van de NVA. Onbetaald |
Echtgenoot werkzaam bij GSK |
Geen |
|
Nagtegaal |
Ziekenhuisapotheker Meander Medisch Centrum |
Beroepenveldcommissie Farmakunde Hogeschool Utrecht, onbetaald |
Geen |
Geen |
|
Timmerman |
Staffunctionaris Klinische Fysica & Patiëntveiligheid |
Lid NIVEL expertgroep infuustechnologie - advies maken kennistoets voor verpleegkundigen – onbetaald Lid ondernemingsraad UMC Utrecht - onbetaald |
EMRP Researcher Grant Metrology for Drug Delivery HLT07- REG1 €120,422.88 USPTO Applicaton #: #20160106909 Apparatus for simultaneous multiple medicament administration |
Geen |
|
Kam-Endtz |
Anesthesioloog Haaglanden MC |
Geen |
Geen |
Geen |
|
Middeldorp |
Gynaecoloog-perinatoloog |
Geen |
Geen |
Geen |
|
Moll |
Klinisch verloskundige/research verloskundige in het St. Antoniusziekenhuis in Nieuwegein |
Geen |
Geen |
Geen |
|
Freeman |
Gynaecoloog |
voorzitter multidiciplinaire werkgroep obstetrische anesthesie
|
Mijn promotieonderzoek naar epidurale analgesie en remifentanil is gesubsidieerd door ZonMw. Dit onderzoek is afgerond maar de resultaten zullen gebruikt worden in deze richtlijn |
Geen |
|
Mooij |
Beleidsmedewerker Patiëntenvereniging Nederland |
Vrijwilligerswerk (onbetaald) patiëntenorganisatie CCUVN |
Geen |
Geen |
|
Kaspers |
Kinderarts-neonatoloog, MST Enschede |
Geen |
Geen |
Geen |
|
De Boer |
Beleidsmedewerker richtlijnontwikkeling |
Geen nevenwerkzaamheden |
Geen |
Geen |
|
Lim |
gynaecoloog |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de Patientenfederatie Nederland in de werkgroep te laten deelnemen. De conceptmodule is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland. Daarnaast is door de Patiëntenfederatie Nederland een achterbanraadpleging verricht, waarvan de uitkomsten zo veel mogelijk meegenomen zijn in de overwegingen van de modules.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze modules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, (2010)), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based module tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit inventarisatie van de knelpunten door de commissie van de NVA bleek dat er een noodzaak was voor revisie van deze richtlijnmodules. Tevens zijn tijdens een fysieke knelpunteninventarisatie knelpunten aangedragen door aanpalende stakeholders inclusief patiëntenorganisaties. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroepleden en de adviseur uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad ‘Zoekverantwoording’ voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de modules is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Indicatorontwikkeling
Indicatoren over zwangerschap en geboorte zijn reeds onderdeel van de vervaardigde indicatoren bij de zorgstandaard integrale geboortezorg. Derhalve zijn er bij deze modules geen indicatoren ontwikkeld.
Kennislacunes
Tijdens de ontwikkeling van deze modules is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de Kennislacunes. Deze zijn te vinden onder de aanverwante producten.
Commentaar- en autorisatiefase
De conceptmodules werden aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werden de conceptmodules aangepast en definitief vastgesteld door de werkgroep. De definitieve modules werden aan de deelnemende (wetenschappelijke) verenigingen en de Patiëntenfederatie Nederland voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut via secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
|
1 (exp Cesarean Section/ or (cesarean* or caesarean* or (abdominal adj1 deliver*) or (c adj1 section*)).ti,ab.) and (Emergency treatment/ or emergency medical services/ or (emergenc* or unplanned or unscheduled or 'non-elective' or urgent).ti,ab.) 5513 2 exp Analgesia, obstetric/ or exp Analgesia, Epidural/ or (analges* or epidural*).ti,ab. 135871 3 1 and 2 501 4 exp Anesthetics, Local/ or exp Lidocaine/ or exp Bupivacaine/ or (lidocain* or bupivacain* or levobupivacain* or ropivacain*).ti,ab. or (local adj2 (anesthe* or anaesthe*)).ti,ab. 129881 5 exp Adrenaline/ or Clonidine/ or Dexmedetomidine/ or exp Sufentanil/ or Fentanyl/ or (adrenaline or adrenalin* or clonidine or dexmedetomidine or bicarbonate or sufenta* or sulfentan* or fentan*).ti,ab. 143185 6 (convert* or convers* or extending or extension or prolong* or adjuvant or supplement* or additiv* or 'top-up' or 'topped-up' or adding).ti,ab. 1483425 7 4 or 5 or 6 1720188 8 3 and 7 183 9 limit 8 to (dutch or english) 148 10 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) 339986 11 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) 1719386 14 9 and (10 or 11) 38 |
(na ontdubbeling) 84 |
|
Embase (Elsevier) |
#14 #11 AND (#9 OR #10) 53 #11 #8 AND ((dutch)/lim OR (english)/lim) 420 #10 ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it 2,093,391 #9 ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT 'conference abstract':it 309,942 #8 #6 AND #7 480 #7 #3 OR #4 OR #5 2,349,396 #6 #1 AND #2 968 #5 convert*:ab,ti OR convers*:ab,ti OR extending:ab,ti OR extension:ab,ti OR prolong*:ab,ti OR adjuvant:ab,ti OR supplement*:ab,ti OR additiv*:ab,ti OR 'top-up':ab,ti OR 'topped-up':ab,ti OR adding:ab,ti 1,918,284 #4 'adrenaline'/exp OR 'clonidine'/exp OR 'dexmedetomidine'/exp OR 'sufentanil'/exp OR 'fentanyl'/exp OR adrenaline:ab,ti OR adrenalin*:ab,ti OR clonidine:ab,ti OR dexmedetomidine:ab,ti OR bicarbonate:ab,ti OR sufenta*:ab,ti OR sulfentan*:ab,ti OR fentan*:ab,ti 259,557 #3 'local anesthetic agent'/exp OR lidocain*:ab,ti OR bupivacain*:ab,ti OR levobupivacain*:ab,ti OR ropivacain*:ab,ti OR ((local NEAR/2 (anesthe* OR anaesthe*)):ab,ti) 251,299 #2 'obstetric analgesia'/exp OR 'epidural analgesia'/exp OR analges*:ab,ti OR epidural*:ab,ti 191,056 #1 ('cesarean section'/exp OR cesarean*:ab,ti OR caesarean*:ab,ti OR ((abdominal NEXT/1 deliver*):ab,ti) OR ((c NEXT/1 section*):ab,ti)) AND ('emergency treatment'/de OR 'emergency care'/de OR 'emergency health service'/exp OR emergenc*:ab,ti OR unplanned:ab,ti OR unscheduled:ab,ti OR 'non-elective':ab,ti OR urgent:ab,ti) 9965 |
|
|
Cochrane library - CENTRAL |
(cesarean*:ab,ti or caesarean*:ab,ti) and (emergenc* or unplanned or unscheduled or 'non-elective' or urgent):ab,ti and (analges* or epidural*):ab,ti and (lidocain* or bupivacain* or levobupivacain* or ropivacain* or (local near/2 (anesthe* or anaesthe*)) or adrenaline or adrenalin* or clonidine or dexmedetomidine or bicarbonate or sufenta* or sulfentan* or fentan* or convert* or convers* or extending or extension or prolong* or adjuvant or additiv* or 'top-up' or 'topped-up' or adding):ab,ti 58 |
