Antitrombotische therapie na chirurgische en/of endovasculaire interventie
Uitgangsvraag
Wat is de optimale antitrombotische therapie na chirurgische en/of endovasculaire interventie bij perifeer arterieel vaatlijden?
De uitgangsvraag bevat de volgende deelvragen:
- Wat is de optimale antitrombotische therapie na endovasculaire interventie?
- Wat is de optimale antitrombotische therapie na chirurgische interventie?
Aanbeveling
Endovasculaire interventies
Behandel patiënten na endovasculaire interventies met acetylsalicylzuur 80 tot 100 milligram eenmaal daags of clopidogrel 75 milligram eenmaal daags.
Overweeg na complexe endovasculaire* interventies behandeling middels clopidogrel 75 milligram eenmaal daags plus acetylsalicylzuur eenmaal daags 80 tot 100 milligram voor minimaal zes maanden en maximaal twaalf maanden.*
Chirurgische interventies
Behandel patiënten na veneuze bypasschirurgie gedurende minimaal twee jaar met een VKA.
Behandel patiënten na kunststof bypasschirurgie minimaal drie jaar met rivaroxaban 2,5 milligram tweemaal daags plus acetylsalicylzuur 80 tot 100 milligram eenmaal daags.
Behandel patiënten na kunststof bypasschirurgie met een verhoogd bloedingsrisico** met acetylsalicylzuur 80 tot 100 milligram eenmaal daags of clopidogrel 75 milligram eenmaal daags.
*Complexe endovasculaire interventies zijn bijvoorbeeld cumulatieve stentplaatsing van tenminste tien centimeter en multi-level procedures, uitgebreide procedures van arteriën onder de knie.
**Actieve bloeding, trauma, maligniteit, hemorragisch of ischemisch CVA, leverziekte geassocieerd met coagulopathie, aanwezigheid van afwijkingen met een verhoogd bloedingsrisico (ulcus tractus digestivus, oesophagus varices, aneurysmata en spinale of intracraniele vasculaire malformaties) (VOYAGER criteria).
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek uitgevoerd naar het effect van behandeling met verschillende antitrombotica bij patiënten met perifeer arterieel vaatlijden. MACE en MALE werden gedefinieerd als cruciale uitkomstmaten. Bloedingen, compliantie, kosten en complicaties werden als belangrijke uitkomstmaten aangemerkt.
Er werd één netwerk meta-analyse geïncludeerd, waaruit 24 individuele gerandomiseerde onderzoeken werden geïncludeerd.
De geïncludeerde studies bevatten over het algemeen kleine cohorten waardoor slechts een enkele studie goed gepowerd was. Ook waren de studies veelal heterogeen in hun methodes. Zo verschilden de definities van MACE, MALE en majeure bloedingen. Door deze majeure limitatie is het vergelijken van de verschillende antitrombotische therapieën zeer lastig.
Ook moet meegewogen worden dat er meerdere factoren invloed hebben op MACE, MALE en majeure bloedingen zoals therapietrouw, type interventies, behandeltechnieken, behandel trajecten en gebruikte materialen, zoals bijvoorbeeld stents. Hierom is ervoor gekozen de literatuur niet te graderen, maar beschrijvend weer te geven.
Endovasculaire behandeling
Bij endovasculaire behandelingen is het wachten op de uitkomsten van de trials die op dit moment lopen zoals CLEAR-PATH (Wegerif, 2024). Tot die tijd is het advies om monotherapie acetylsalicylzuur of clopidogrel te volgen. De VOYAGER-trial onderzocht ASA plus lage dosering rivaroxaban vergeleken met ASA-monotherapie. Deze studie laat een hogere mortaliteit zien met 2% ARR in MALE uitkomsten (Rymer, 2023). Ook in hun subanalyse laten ze geen voordeel zien in effectiviteit voor ASA plus lage dosering rivaroxaban in de groep die een endovasculaire behandeling onderging. In deze landmark studie is weliswaar het effect van acetylsalicylzuur met of zonder rivaroxaban onderzocht, maar op basis van de CAPRIE-trial zou clopidogrel effectiever zijn dan acetylsalicylzuur. Een combinatie van clopidogrel en acetylsalicylzuur kan ook worden overwogen bij endovasculaire behandeling van complexe laesies, alleen is de winst hiervan niet onomstotelijk aangetoond. Onder endovasculaire behandeling van complexe laesies valt de behandeling van bijvoorbeeld cumulatieve stentplaatsing van tenminste 10cm, multi-level procedures en uitgebreide procedures van arteriën onder de knie. De studie van Cho (2019) laat wel zien dat indien DAPT gegeven wordt er minimaal zes maanden clopidogrel en ascal gegeven moet worden. Na zes tot twaalf maanden wordt geadviseerd de acetylsalicylzuur te staken en de clopidogrel te continueren. Voor patienten die een endovasculaire interventie ondergaan en al ingesteld zijn op een andere bloedverdunner, zoals een DOAC of VKA, kan bij gebrek aan wetenschappelijke onderbouwing geen aanbeveling gedaan worden. In de praktijk wordt de DOAC of VKA veelal gecontinueerd.
Veneuze bypass
De BOA-trial en de VOYAGER-PAD-trial zijn beiden verreweg de grootste trials, die het gebruik van antitrombotische therapie na veneuze bypasschirurgie hebben geëvalueerd. De BOA trial toont na twee jaar een betere patency in veneuze bypasses bij gebruik van een VKA ten opzichte van ASA. De VOYAGER PAD subanalyse van bypassoperaties toont na drie jaar een voordeel in MACE en MALE voor rivaroxaban en ASA ten opzichte van placebo en ASA. Het risico op bloedingen is na gebruik van VKA mogelijk wat groter dan na gebruik van Rivaroxaban en ASA, echter de definities in de studies verschillen en zijn daarom niet goed te vergelijken. Ook werd in de BOA trial een streef INR van 3.0-4.5 aangehouden, hetgeen tegenwoordig als relatief hoog wordt geduid. Een groot nadeel van het gebruik van rivaroxaban en ASA is de beperkte therapietrouw. In Nederland hebben we daarentegen een goed georganiseerde trombosedienst, die bij patiënten die een VKA gebruiken, de INR controleert. Deze INR-controles werken therapietrouw in de hand. Een tweede nadeel van rivaroxaban is de prijs. De kosten zijn momenteel nog aanmerkelijk hoger dan de kosten van het gebruik van een VKA. Dit kan in de toekomst veranderen na het verlopen van het patent.
Op basis van bovenstaande argumenten gaat in Nederland vooralsnog de voorkeur uit naar het gebruik van een VKA na aanleg van een veneuze perifere bypass.
Kunststof bypass
In de BOA-trial werd bij patiënten met een perifere kunststof bypass na gebruik van ASA een betere patency gevonden dan na gebruik van een VKA. In de CASPAR trial werd in patiënten met een infragenuale kunststof bypass een betere patency gevonden na gebruik van clopidogrel en ASA dan na gebruik van alleen ASA. In supragenuale kunststof bypass werd geen verschil in patency gevonden. Echter, de beschreven patency rates in de CASPAR trial zijn aanmerkelijk lager dan in de BOA-trial en VOYAGER-PAD-trial. In de VOYAGER PAD trial leidt het gebruik van Rivaroxaban en ASA tot een lagere MALE dan na gebruik van alleen ASA. Vanwege het lage risico op occlusie van de bypass in de VOYAGER PAD trial lijken patiënten met een kunststof bypass het meest gebaat bij een behandelstrategie met rivaroxaban en ASA. Zoals eerder beschreven zijn de nadelen van deze behandeling de therapietrouw, de kosten en het verhoogde risico op bloedingscomplicaties.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het doel van antistolling na een endovasculaire of chirurgische revascularisatie is het verlagen van de trombo-embolische events (MALE en MACE) met daarbij aanvaardbare bloedingsrisico’s. Het lijkt erop dat meer of betere bloedverdunning leidt tot minder trombo-embolische events. Alleen dit gaat ten koste van het bloedingsrisico, in sommige studies leidt tot maar liefst 20% meer majeure bloedingen. Ook therapieontrouw is een veel voorkomend probleem. Patiënten met ernstig perifeer arterieel vaatlijden zijn vaak ouder en kwetsbaar. Er is dan ook vaak sprake van polyfarmacie. Polyfarmacie leidt tot verminderde therapietrouw in het medicijn gebruik van de patiënten. Meer pillen betekent minder gebruik hiervan. In Nederland hebben we daarentegen een goed georganiseerde trombosedienst, die bij patiënten die een VKA gebruiken de INR controleert. Deze INR-controles hebben op basis van ervaringen van de werkgroep mogelijk een positieve invloed op de therapietrouw van patiënten.. Op basis van bovenstaande overwegingen kan in goed overleg met de patiënt voor de beste individuele antitrombotische behandeling gekozen worden.
Kosten (middelenbeslag)
De meeste antistollingsmedicatie bestaat al jaren en de kosten ervan zijn laag. Rivaroxaban heeft een ietwat hogere prijs. Wanneer alle kosten worden meegenomen, waaronder de kosten van de trombosedienst, wordt dit verschil mogelijk tenietgedaan.
Aanvaardbaarheid, haalbaarheid en implementatie
Op dit moment worden alle soorten antistollingsregimenten in Nederland door elkaar gebruikt en is er geen eenduidigheid (Ipema, 2020). De aanbevelingen kunnen hierin meer eenduidigheid creëren.
Rationale van de aanbeveling
Na een revascularisatie zijn verschillende antithrombotische strategieën mogelijk. Hierbij wordt het risico op trombo-embolische complicaties enerzijds afgewogen tegen het risico op een bloedingscomplicatie anderzijds. De definities van deze eindpunten verschillen nogal in de beschikbare studies, waardoor onderlinge vergelijking niet altijd mogelijk is. Ook therapietrouw wordt meegenomen in de overweging om voor een bepaald medicamenteus regime te kiezen. Polyfarmacie leidt tot een mindere therapietrouw, regelmatige controle via de trombosedienst lijkt juist de therapietrouw te verbeteren.
In principe worden alle patiënten met perifeer arterieel vaatlijden levenslang ingesteld op clopidogrel 75 milligram eenmaal daags in het kader van secundaire preventie, zie de module [LINK na publicatie]. Na een endovasculaire interventie dient deze behandeling gecontinueerd te worden. In meerdere studies over endovasculaire interventies wordt acetylsalicylzuur 80 tot 100 milligram gebruikt, hetgeen tot vergelijkbare resultaat leidt. Er zijn aanwijizngen dat bij complexere endovasculaire behandelingen DAPT voor een periode van zes tot twaalf maanden tot betere resultaten leidt.
Na veneuze bypasschirurgie leidt het gebruik van VKA in de eerste twee jaar na de operatie tot een beter patency dan na gebruik van ASA. De combinatie Rivaroxaban en ASA leidt ook tot betere patencies dan ASA, maar op basis van het nadelig effect van polyfarmacie op therapietrouw en de vermeende betere therapietrouw bij controle door de trombosedienst, gaat in de Nederlandse situatie de voorkeur uit naar VKA. Bij patiënten met een perifere kunststof bypass resulteert gebruik van ASA juist tot een betere patency dan na gebruik van een VKA. Gebruik van clopidogrel resulteert in vergelijkbare resultaten als gebruik van ASA. De combinatie van Rivaroxaban en ASA leidt in de eerste drie jaar na de operatie zelfs tot nog betere patencies dan alleen ASA en krijgt derhalve de voorkeur. Echter, deze combinatie resulteert in een verhoogd risico op bloedingscomplicaties en wordt derhalve niet geadviseerd bij patiënten met een verhoogd bloedingsrisico. Er is geen wetenschappelijke onderbouwing om patiënten na een bypassoperatie langer dan twee jaar met een VKA te behandelen of langer dan drie jaar met de combinatie Rivaroxaban en ASA. Na deze periodes kan overwogen de patiënt levenslang in te stellen clopidogrel 75 milligram eenmaal daags
Onderbouwing
Despite antithrombotic therapy, patients with peripheral arterial disease (PAD) continue to develop atherothrombotic events (Peripheral Arterial Diseases Antiplatelet Consensus Group, 2003; Antithrombotic Trialists' Collaboration, 2002). Particularly after intervention. In patients with peripheral arterial disease (PAD), 18.2% experienced myocardial infarction (MI), stroke and/or cardiovascular death after one-year follow-up. Compared with patients with primary coronary artery disease (CAD), it is 13.3% and cerebrovascular disease (CVD) 10% (Steg, 2007).
Another major problem remains the patency rates after intervention. These are lower in PAD patients compared with cardiac interventions. Restenosis after percutaneous transluminal angioplasty (PTA) of the arteria femoralis superior (AFS) is around 25% during the first year of follow-up (Krankenberg, 2009). For below-knee revascularisation, patency rates are much lower with restenosis rates (approximately 60%) (Schwarzwalder, 2009). This suggests that (mono) platelet aggregation inhibitor(s) are less effective in preventing atherosclerosis of the peripheral arteries especially after intervention. To further reduce atherothrombotic events, several antiplatelet therapies have been investigated, including dual antiplatelet therapies. In CAD and CVD patients, the benefit of dual antiplatelet therapy has been demonstrated in two large, randomised trials (Steinhubl, 2002; Wang, 2013). The striking difference in incidence rates between PAD, CAD and CVD patients receiving monotherapy with platelet aggregation inhibitors suggests that the outcomes of DAPT studies in CAD and CVD patients cannot be extrapolated to PAD patients. Finally, several new platelet aggregation inhibitors and antithrombotics have become available. The aim is to determine the optimal antithrombotic treatment after both endovascular and surgical treatment in patients with PAD.
A network meta-analysis is the most appropriate study design to answer the research question of this guideline module. Therefore, we searched the electronic databases for network meta-analyses on the optimal antithrombotic therapy after surgical and/or endovascular treatment. None of the network meta-analyses captured by the literature search met the PICO criteria of this guideline module. Although the systematic review by Willems (2022) did not fully comply, the study still included several individual randomized controlled trials answering the research question of this module. The description of the studies and the results of each study were presented descriptively in the ‘description of studies and ‘results’ section.
Description of studies
One network meta-analysis (Willems (2022) was included in the analysis of the literature. Willems (2022) searched the electronic databases for randomized controlled trials (RCTs) published between the 1st of January 1995 up to the 31st of December 2021. Studies on patients with symptomatic lower extremity PAD, based on a clinical presentation of intermittent claudication or chronic limb-threatening ischaemia that either was related to an ankle-brachial index below 0.9 and in the need for peripheral revascularization, were considered eligible for this guideline if (1) two or more antithrombotic treatment strategies were compared, (2) patients were followed for clinical outcome measurements. Clinical outcome measurements included death, myocardial infarction, stroke, acute limb ischaemia (ALI), need for revascularization, major amputation, and bleeding events. Study reports meeting one or more of the following criteria were excluded: (1) studies on patients using anticoagulant therapy for venous thromboembolic disease, (2) studies on patients using anti- coagulant therapy for the prevention of systemic embolism in atrial fibrillation, (3) studies on patients with known congenital bleeding or thrombotic disorders, (4) studies with intravenous or intra-arterial antithrombotic treatment as intervention, (5) studies in which the clinical outcomes were described for a follow-up period that was twice or more the duration of the intervention period, (6) animal studies, (7) in vitro studies, and (8) non-revascularized cohorts.
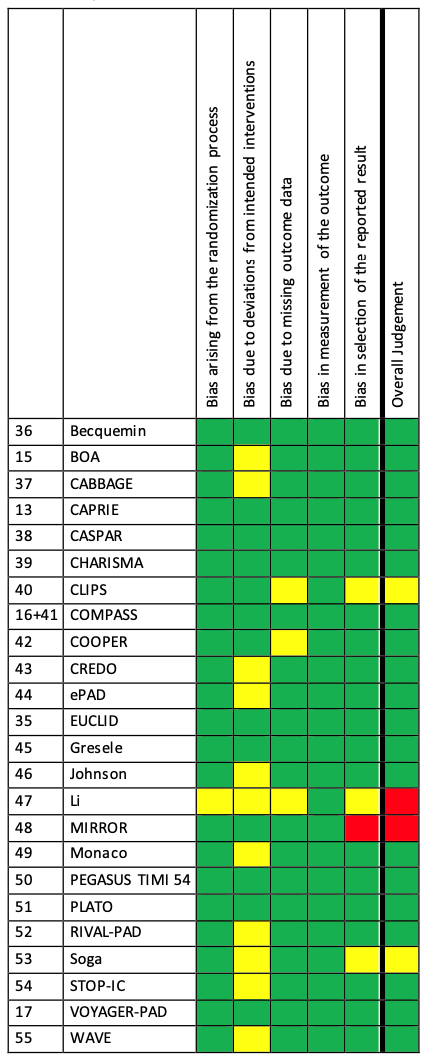
In total, 24 RCTs were included. Important study characteristics and results are summarized in Table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tab’).
Table 2. Characteristics of included studies
|
Study |
Participants (number, age, other important characteristics) |
Comparison |
Follow-up |
Outcome measures |
Risk of bias (adopted from the network meta-analysis of Willems (2022))* |
|
Included in the systematic review of Willems (2022) |
|||||
|
Becquimin (1997) |
N total: N = 243
Age 67.0 years
Sex % (male) 77% male
Population Infrainguinal saphenous-vein bypass grafts |
Intervention: TP2
Control: P |
24 months |
MACE |
Low risk |
|
BOA (2000) |
N total: N = 2690
Age 69.0 years
Sex % (male) 64% male
Population Infrainguinal bypass graft vein, biograft, prosthetic, composite |
Intervention: A
Control: VKA2 |
21 months |
MACE MALE
|
Low risk |
|
CABBAGE (2017) |
N total: N = 50
Age 73.0 years
Sex % (male) 74% male
Population EVR, balloonangioplasty infrapopliteal |
Intervention: A
Control: A+CI |
3 months |
MACE MALE |
Low risk |
|
CAPRIE (1996) |
N total: N = 6452
Age 64.0 years
Sex % (male) 72% male
Population PAD |
Intervention: A
Control: C |
23 months |
MACE |
Low risk |
|
CASPAR (2010) |
N total: N = 851
Age 66.0 years
Sex % (male) 76% male
Population Bypass graft (venous and prosthetic) below the knee |
Intervention: A
Control: A + C |
12 months |
MALE MB |
Low risk |
|
CHARISMA (2009) |
N total: N = 3096
Age 60.0 years
Sex % (male) 70% male
Population PAD |
Intervention: A
Control: A + C |
26 months |
MACE MB |
Low risk |
|
CLIPS (2007) |
N total: N = 366
Age 66.0
Sex % (male) 77% male
Population PAD |
Intervention: A
Control: P
|
21 months |
MACE
|
|
|
COMPASS (2018) |
N total: N = 7470
Age 68.0
Sex % (male) 72% male
Population PAD |
Intervention: A
Control: A + R1
Control: R2
|
21 months |
MACE MALE MB ALI
|
Some concerns |
|
COOPER (2012) |
N total: N = 431
Age 71.0
Sex % (male) 88% male
Population PAD |
Intervention: C
Control: TPI |
3 months |
MACE
|
Low risk |
|
CREDO (2006) |
N total: N = 272
Age 67.0
Sex % (male) 66% male
Population CAD |
Intervention: A
Control: A + C |
12 months |
MACE |
Low risk |
|
ePAD (2018) |
N total: N = 203
Age 67.0
Sex % (male) 29% male
Population EVR, femoropopliteal |
Intervention: A + C
Control: A + E |
2.7 months |
MACE MB |
Low risk |
|
EUCLID (2017) |
N total: N = 13,885
Age 66.0
Sex % (male) 72% male
Population PAD |
Intervention: C
Control: TG2 |
30 months |
MACE MB ALI
|
Low risk |
|
Gresele (2000) |
N total: N = 159
Age 66.0
Sex % (male) 86% male
Population PAD |
Intervention: A
Control: A + CC |
6 months |
MACE |
Low risk |
|
Johnson (2002) |
N total: N = 831
Age 64.0
Sex % (male) Not reported.
Population Infrainguinal bypass graft (venous and prosthetic) |
Intervention: A
Control: A + VKA1 |
38 months |
MB |
Low risk |
|
Li (2013) |
N total: N = 50
Age 74.0
Sex % (male)
Population EVR femoropopliteal |
Intervention: C
Control: C + VKA1 |
12 months |
MACE MB
|
High risk |
|
MIRROR (2011) |
N total: N = 80
Age 70.0
Sex % (male) 66% male
Population EVR femoropopliteal |
Intervention: A
Control: A + C |
6 months |
MACE |
High risk |
|
Monaco (2012) |
N total: N = 318
Age 67.0
Sex % (male) 53% male
Population Femoropopliteal bypass (venous and prosthetic) |
Intervention: A + C
Control: C + VKA1 |
77 months |
MACE MB |
Low risk |
|
PEGASUS TIMI 54 (2016) |
N total: N = 1143
Age 66.0
Sex % (male) 70% male
Population CAD |
Intervention: A
Control: A + TGI
Control: A + TG2 |
36 months |
MACE MALE MB ALI |
Low risk |
|
PLATO (2015) |
N total: N = 1144
Age 66.0
Sex % (male) 78% male
Population CAD |
Intervention: A + C
Control: A + TG2 |
9 months |
MACE MB |
Low risk |
|
RIVAL-PAD (2020) |
N total: N = 20
Age 67.0
Sex % (male) 60% male
Population EVR, balloon angioplasty infrainguinal |
Intervention: A + C
Control: A + R1 |
3 months |
MB |
Low risk |
|
Soga (2009) |
N total: N = 80
Age 71.0
Sex % (male) 83% male
Population EVR femoropopliteal |
Intervention: A + TP1
Control: A + TP1 + CI |
24 months |
MACE MB |
Some concerns |
|
STOP-IC (2013) |
N total: N = 200
Age 73.0
Sex % (male) 59% male
Population EVR femoropopliteal |
Intervention: A
Control: A + CI |
12 months |
MACE MALE |
Low risk |
|
VOYAGER-PAD (2020) |
N total: N = 6564
Age 67.0
Sex % (male) 74% male
Population Bypass and EVR femoropopliteal |
Intervention: A
Control: A + R1 |
28 months |
MACE MALE MB ALI
|
Low risk |
|
WAVE (2007) |
N total: N = 2161
Age 64.0
Sex % (male) 74% male
Population PAD |
Intervention: A
Control: A + VKA1 |
35 months |
MACE MB ALI |
Low risk |
*The risk of bias assessment was adopted from the systematic network meta-analysis from Willems (2022).
Antithrombotic regimen: A acetylsalicylic acid 75–325 mg daily, C clopidogrel 75 mg once daily, , CI cilostazol 200 mg once daily, E edoxaban 60 mg once daily, P placebo only, R1 rivaroxaban 2.5 mg twice daily, TP1 ticlopidine 200 mg twice daily, TP2 ticlopidine 250 mg twice daily, VKA1 vitamin K antagonist with target INR between 1.4 and 3, VKA2 vitamin K antagonist with target INR between 3 and 4.5
Population: EVR femoropopliteal studies on patients who underwent a peripheral vascular intervention for peripheral arterial disease
Outcomes: ALI acute limb event, INR international normalized ratio, MACE major adverse cardiovascular events, MALE major adverse limb events, MB major bleeding, Nx number of patients in group x PAD peripheral arterial disease, Tx treatment in group x.
Table 3: Definitions of outcome measurements
|
Author |
MACEa |
MALEb |
Major bleedingc |
|
Becquemin (1997) |
1, 3, 4 |
- |
- |
|
BOA (2000) |
2, 3, 4, 6 |
- |
1, 2, 3 |
|
CABBAGE (2017) |
1, 3, 4 |
1, 2, 3 |
1, 2, 3, 4 |
|
CAPRIE (1996) |
2, 3, 4 |
- |
- |
|
CASPAR (2010) |
- |
1, 3, 4 |
GUSTOd |
|
CHARISMA (2009) |
1, 3, 4 |
- |
GUSTOd |
|
CLIPS (2007) |
1, 3, 4 |
- |
- |
|
COMPASS (2018) |
2, 3, 4 |
1, 3, 5 |
Modified ISTHe |
|
COOPER (2012) |
2, 3, 4 |
- |
- |
|
CREDO (2006) |
1, 3, 4 |
- |
- |
|
ePAD (2018) |
2, 3, 4 |
- |
TIMIf |
|
EUCLID (2017) |
2, 3, 5 |
1, 5 |
TIMIf |
|
Gresele (2000) |
2, 3, 4 |
- |
- |
|
Johnson (2002) |
- |
- |
- |
|
Li (2013) |
1, 3, 4 |
- |
- |
|
MIRROR (2011) |
NS |
- |
- |
|
Monaco (2012) |
2, 3, 4, 7 |
- |
- |
|
PEGASUS TIMI 54 (2016) |
2, 3, 4 |
1, 5 |
TIMIf |
|
PLATO (2015) |
2, 3, 4 |
- |
TIMIf |
|
RIVAL-PAD (2020) |
- |
- |
TIMIf |
|
Soga (2009) |
1, 3, 4 |
- |
5, 6, 9 |
|
STOP-IC (2013) |
1, 3, 4 |
3, 4, 5, 6 |
- |
|
VOYAGER-PAD (2020) |
1, 3, 4, 6, 8 |
1, 3, 5 |
ISTHe |
|
WAVE (2007) |
2, 3, 4 |
- |
1, 2, 5, 6, 10 |
aMACE: 1 = death; 2 = cardiovascular death; 3 = myocardial infarction; 4 = stroke; 5 = ischaemic stroke; 6 = amputation; 7 = urgent revascularization; 8 = acute limb event.
bMALE: 1 = peripheral revascularization; 2 = any revascularization; 3 = major amputation; 4 =re-occlusion/revascularization of target lesion after intervention; 5 = acute limb event; 6 = death.
cMB: 1 = fatal bleeding; 2 = intracranial haemorrhage; 3 = bleeding requiring hospitalization; 4 = gastro-intestinal haemorrhage; 5 = bleeding requiring intervention; 6 = bleeding requiring blood product transfusion; 7 = hematoma with diameter > 5 cm; 8 = haemoglobin reduction of > 4 g/dL; 9 = hypotension requiring inotropic support; 10 = intraocular haemorrhage. GUSTO = major bleeding defined as intracranial haemorrhage and/or haemodynamic compromise. ISTH = major bleeding including (1) fatal bleeding, (2) symptomatic bleeding into a critical organ, or (3) bleeding causing a fall in haemoglobin level of 2 g/dL (1.24 mmol/L) or more or leading to transfusion of two or more units of whole blood or red cells. Modi- fied ISTH = major bleeding including (1) symptomatic bleeding into a critical organ, (2) surgical site bleeding requiring reoperation, or (3) any bleeding requiring hospitalization (including presentation to an acute care facility without an overnight stay). TIMI = major bleeding including (1) any intracranial bleeding, (2) clinically overt signs of haemorrhage associated with a drop in haemoglobin of ≥ 5 g/dL or a ≥ 15% absolute decrease in haematocrit, and (3) fatal bleeding.
cMALE: 1 = peripheral revascularization; 2 = any revascularization; 3 = major amputation; 4 =re-occlusion / re-vascularization of target lesion after intervention; 5 = acute limb event; 6 = death.
dGUSTO Global Use of Strategies to Open Occluded Arteries.
eISTH International Society on Thrombosis and Haemostasis, MACE major adverse cardiovascular events, MALE major adverse limb events, MB major bleeding, NS not specified.
fTIMI Thrombolysis In Myocardial Infarction.
Table 4: Number of events per study, sorted by study population
|
Author |
Antithrombotic regimen |
Sample size |
MACE |
Major bleeding |
Male |
||||||||||
|
|
T1 |
T2 |
T3 |
N1 |
N2 |
N3 |
N1 |
N2 |
N3 |
N1 |
N2 |
N3 |
N1 |
N2 |
N3 |
|
Studies on patients who are solely selected for PAD |
|||||||||||||||
|
CAPRIE (1996) |
A |
C |
|
3229 |
3223 |
|
277 |
215 |
|
|
|
|
|
|
|
|
CHARISMA (2009) |
A |
A + C |
|
1551 |
1545 |
|
138 |
117 |
|
27 |
26 |
|
|
|
|
|
CLIPS (2007) |
A |
P |
|
185 |
181 |
|
9 |
19 |
|
|
|
|
|
|
|
|
COMPASS (2018) |
A |
A + R1 |
R2 |
2504 |
2492 |
|
174 |
126 |
149 |
42 |
68 |
66 |
56 |
32 |
40 |
|
COOPER (2012) |
C |
TP1 |
|
215 |
216 |
|
0 |
2 |
|
|
|
|
|
|
|
|
EUCLID (2017) |
C |
TG2 |
|
6955 |
6930 |
|
740 |
751 |
|
109 |
113 |
|
|
|
|
|
Gresele (2000) |
A |
A + CC |
|
73 |
74 |
|
0 |
0 |
|
|
|
|
|
|
|
|
WAVE (2007) |
A |
A = VKA1 |
|
1081 |
1080 |
|
144 |
132 |
|
24 |
74 |
|
|
|
|
|
Studies on patients who underwent a peripheral vascular intervention for PAD |
|||||||||||||||
|
Becquimin (1997) |
P |
TP2 |
|
121 |
122 |
|
31 |
28 |
|
|
|
|
|
|
|
|
BOA (2000) |
A |
VKA2 |
|
1324 |
1326 |
|
275 |
248 |
|
56 |
107 |
|
|
|
|
|
CABBAGE (2017) |
A |
A + CI |
|
25 |
25 |
|
2 |
1 |
|
0 |
1 |
|
2 |
3 |
|
|
CASPAR (2010) |
A |
A + C |
|
426 |
425 |
|
|
|
|
5 |
9 |
|
151 |
149 |
|
|
ePAD (2018) |
A + C |
A + E |
|
101 |
100 |
|
1 |
3 |
|
2 |
0 |
|
|
|
|
|
Johnson (2002) |
A |
A = VKA1 |
|
413 |
418 |
|
|
|
|
15 |
35 |
|
|
|
|
|
Li (2013) |
C |
C + VKA1 |
|
25 |
25 |
|
2 |
1 |
|
0 |
1 |
|
|
|
|
|
MIRROR (2011) |
A |
A + C |
|
40 |
40 |
|
15 |
12 |
|
|
|
|
|
|
|
|
Monaco (2012) |
A + C |
C + VKA1 |
|
157 |
161 |
|
5 |
7 |
|
13 |
15 |
|
|
|
|
|
RIVAL-PAD (2020) |
A + C |
A + R1 |
|
11 |
9 |
|
|
|
|
0 |
0 |
|
|
|
|
|
Soga (2009) |
A + TP1 |
A + TP1 + CI |
|
39 |
39 |
|
3 |
1 |
|
0 |
0 |
|
|
|
|
|
STOP-IC (2013) |
A |
A + CI |
|
98 |
93 |
|
9 |
11 |
|
|
|
|
28 |
16 |
|
|
VOYAGER-PAD (2020) |
A |
A + R1 |
|
3278 |
3286 |
|
588 |
514 |
|
100 |
140 |
|
770 |
687 |
|
|
Studies on patients with coronary artery disease who coincide with PAD |
|||||||||||||||
|
CREDO (2006) |
A |
A + C |
|
140 |
132 |
|
24 |
12 |
|
|
|
|
|
|
|
|
PEGASUS TIMI 54 (2016) |
A |
A + TG1 |
A + TG2 |
404 |
368 |
|
71 |
47 |
54 |
4 |
4 |
5 |
26 |
23 |
17 |
|
PLATO (2015) |
A + C |
A + TG2 |
|
578 |
566 |
|
112 |
93 |
|
46 |
58 |
|
|
|
|
Results
Multiple studies in the network meta-analysis of Willems (2022) reported data regarding the optimal antithrombotic treatment in patients with peripheral arterial disease who underwent surgical and/or endovascular treatment. However, a few studies in the network meta-analysis included patients with peripheral arterial disease who did not undergo surgical and/or endovascular treatment and therefore, we were unable to grade the level of evidence of the included studies.
For this guideline, we followed the results from the network meta-analysis of Willems (2022).
1. Major adverse cardiac events (MACE) (critical)
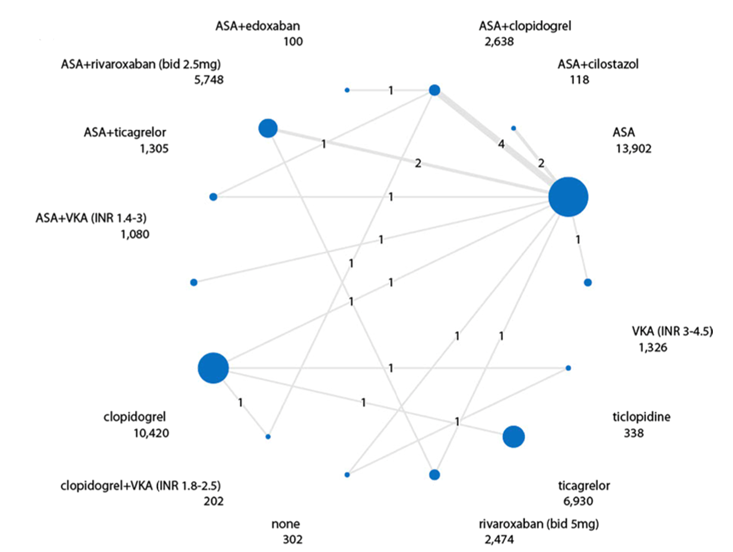
The network meta-analysis of Willems (2022) investigated the effect of different antithrombotic treatments on MACE. In total, 21 studies with 46,961 patients reported MACE (Becquimin, 1997; BOA, 2000; CABBAGE, 2017; CAPRIE, 1996; CHARISMA, 2009; CLIPS, 2007; COMPASS, 2018; COOPER, 2012; CREDO, 2006; ePAD, 2018; EUCLID, 2017; Gresele, 2000; Li, 2013; MIRROR, 2011; Monaco, 2012; PEGASUS TIMI 54, 2016; PLATO, 2015; Soga, 2009; STOP-IC, 2013; VOYAGER-PAD, 2020; WAVE, 2007). One study (Soga, 2009) with 78 patients is not part of the network graph, since its treatment regimens did not connect to other studies. A network graph for MACE, is presented in figure 1.
Compared to acetylsalicylic acid (ASA), clopidogrel, ticagrelor, ASA plus ticagrelor, and ASA plus low-dose rivaroxaban were more effective in reducing MACE. None of these four antithrombotic regimens were superior to one another (see table 4).
Figure 1. Network graph of all studies for outcome MACE in network meta-analysis (Willems, 2022). The values on the line in the graph represent the number of studies between two treatments. The values under each antithrombotic treatment represent the number of patients.
1. Major adverse limb events (MALE) (critical)
The network meta-analysis of Willems (2022) investigated the effect of different antithrombotic treatments on MALE. In total, seven studies with 29,015 patients reported MALE. A network graph could be built of six studies (COMPASS, 2018; VOYAGER-PAD, 2020; CABBAGE, 2017; CASPAR, 2010; PEGASUS-TIMI 54, 2016; STOP-IC, 2013). The EUCLID (2017) trial was left out since its treatment options did not connect to other studies. ASA plus clopidogrel, ASA plus ticagrelor, rivaroxaban 5 milligram twice daily, ASA plus low-dose rivaroxaban, and ASA plus cilostazol were compared to ASA, but none was superior in preventing MALE (see table 5).
2. Major bleeding (important)
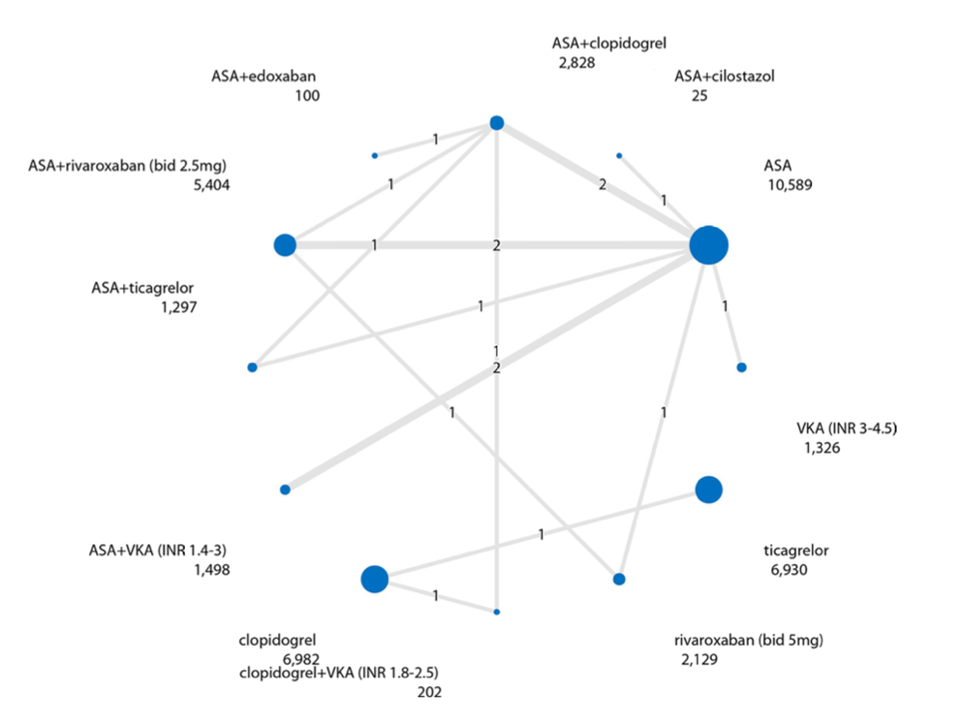
The network meta-analysis of Willems (2022) investigated the effect of different antithrombotic treatments on major bleeding. In total, sixteen studies with 39,388 patients reported major bleeding (BOA, 2000; CABBAGE, 2017; CASPAR, 2010; CHARISMA, 2009; COMPASS, 2018; ePAD, 2018; EUCLID, 2017; Li, 2013; Monaco, 2012; PEGASUS TIMI 54, 2016; PLATO, 2015; RIVAL-PAD, 2020; Soga, 2009; VOYAGER-PAD, 2020; WAVE, 2007). One study (Soga, 2009) with 78 patients is not part of the network graph. A network graph for MACE, is presented in figure 2.
High-intensity VKA, rivaroxaban 5 milligram twice daily, ASA plus low-intensity VKA, and ASA plus low-dose rivaroxaban all significantly increased the risk of major bleeding compared to ASA monotherapy. No antithrombotic regimen or placebo reduced the risk of major bleeding (see table 6).
Figure 2. Network graph of all studies for outcome major bleeding in network meta-analysis (Willems, 2022). The values on the line in the graph represent the number of studies between two treatments. The values under each antithrombotic treatment represent the number of patients.
3. Compliance (important)
None of the studies in the network meta-analysis of Willems (2022) reported information regarding compliance.
4. Costs (important)
None of the studies in the network meta-analysis of Willems (2022) reported information regarding costs.
5. Complications (important)
None of the studies in the network meta-analysis of Willems (2022) reported information regarding complications.
A systematic review of the literature was performed to answer the following question(s): What are the benefits and harms of different antithrombotic treatments after both endovascular and/or surgical treatment in patients with peripheral arterial disease?
Table 1. PICO
|
Patients |
Patients with peripheral arterial disease who underwent endovascular and/or surgical treatment. |
|
Intervention |
Antithrombotic treatment. |
|
Control |
Different antithrombotic treatments compared to each other. |
|
Outcomes |
Major adverse cardiac events (MACE), major adverse limb events (MALE), major bleeding, compliance, costs. |
|
Other selection criteria |
Study design: randomized controlled trials. |
Relevant outcome measures
The guideline panel considered MACE and MALE as critical outcome measures for decision making; and major bleeding, compliance, and costs as important outcome measure for decision making.
The guideline panel considered a relative risk <0.80 or >1.25 and a difference of 10% of the maximum score for continuous outcome measures as a minimal clinically (patient) important difference. In case of inclusion of a network meta-analysis, the definition of minimally important difference of that publication was followed.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until the 22nd of April 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 29 hits. Studies were selected based on the following criteria: network meta-analyses on the effects of various antithrombotic treatments in patients with peripheral arterial disease. Four studies were initially selected based on title and abstract screening. After reading the full text, three studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and one study was included for descriptive purposes but this study was not suitable for GRADE conclusions.
- Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ. 2002 Jan 12;324(7329):71-86. doi: 10.1136/bmj.324.7329.71. Erratum in: BMJ 2002 Jan 19;324(7330):141. PMID: 11786451; PMCID: PMC64503.
- Becquemin JP. Effect of ticlopidine on the long-term patency of saphenous-vein bypass grafts in the legs. Etude de la Ticlopidine après Pontage Fémoro-Poplité and the Association Universitaire de Recherche en Chirurgie. N Engl J Med. 1997 Dec 11;337(24):1726-31. doi: 10.1056/NEJM199712113372404. PMID: 9392698.
- Belch JJ, Dormandy J; CASPAR Writing Committee; Biasi GM, Cairols M, Diehm C, Eikelboom B, Golledge J, Jawien A, Lepäntalo M, Norgren L, Hiatt WR, Becquemin JP, Bergqvist D, Clement D, Baumgartner I, Minar E, Stonebridge P, Vermassen F, Matyas L, Leizorovicz A. Results of the randomized, placebo-controlled clopidogrel and acetylsalicylic acid in bypass surgery for peripheral arterial disease (CASPAR) trial. J Vasc Surg. 2010 Oct;52(4):825-33, 833.e1-2. doi: 10.1016/j.jvs.2010.04.027. Epub 2010 Aug 1. Erratum in: J Vasc Surg. 2011 Feb;53(2):564. Biasi, B M [corrected to Biasi, G M]. PMID: 20678878.
- Bonaca MP, Bhatt DL, Braunwald E, Cohen M, Steg PG, Storey RF, Held P, Jensen EC, Sabatine MS. Design and rationale for the Prevention of Cardiovascular Events in Patients With Prior Heart Attack Using Ticagrelor Compared to Placebo on a Background of Aspirin-Thrombolysis in Myocardial Infarction 54 (PEGASUS-TIMI 54) trial. Am Heart J. 2014 Apr;167(4):437-444.e5. doi: 10.1016/j.ahj.2013.12.020. Epub 2014 Jan 6. PMID: 24655690.
- Bonaca MP, Bauersachs RM, Anand SS, Debus ES, Nehler MR, Patel MR, Fanelli F, Capell WH, Diao L, Jaeger N, Hess CN, Pap AF, Kittelson JM, Gudz I, Mátyás L, Krievins DK, Diaz R, Brodmann M, Muehlhofer E, Haskell LP, Berkowitz SD, Hiatt WR. Rivaroxaban in Peripheral Artery Disease after Revascularization. N Engl J Med. 2020 May 21;382(21):1994-2004. doi: 10.1056/NEJMoa2000052. Epub 2020 Mar 28. PMID: 32222135.
- Debus ES, Nehler MR, Govsyeyev N, Bauersachs RM, Anand SS, Patel MR, Fanelli F, Capell WH, Brackin T, Hinterreiter F, Krievins D, Nault P, Piffaretti G, Svetlikov A, Jaeger N, Hess CN, Sillesen HH, Conte M, Mills J, Muehlhofer E, Haskell LP, Berkowitz SD, Hiatt WR, Bonaca MP. Effect of Rivaroxaban and Aspirin in Patients With Peripheral Artery Disease Undergoing Surgical Revascularization: Insights From the VOYAGER PAD Trial. Circulation. 2021 Oct 5;144(14):1104-1116. doi: 10.1161/CIRCULATIONAHA.121.054835. Epub 2021 Aug 12. PMID: 34380322.
- Efficacy of oral anticoagulants compared with aspirin after infrainguinal bypass surgery (The Dutch Bypass Oral Anticoagulants or Aspirin Study): a randomised trial. Lancet. 2000 Jan 29;355(9201):346-51. Erratum in: Lancet 2000 Mar 25;355(9209):1104. PMID: 10665553.
- Johnson WC, Williford WO; Department of Veterans Affairs Cooperative Study #362. Benefits, morbidity, and mortality associated with long-term administration of oral anticoagulant therapy to patients with peripheral arterial bypass procedures: a prospective randomized study. J Vasc Surg. 2002 Mar;35(3):413-21. doi: 10.1067/mva.2002.121847. PMID: 11877686.
- Krankenberg H, Tübler T, Sixt S, Fischer M, Schmiedel R, Schulte KL, Balzer JO, Kieback A, Fiehn E, Wittenberg G, Ali T, Tiefenbacher C, Jahnke T, Steinkamp HJ, Wegscheider K, Treszl A, Ingwersen M, Zeller T. German multicenter real-world registry of stenting for superficial femoral artery disease: clinical results and predictive factors for revascularization. J Endovasc Ther. 2014 Aug;21(4):463-71. doi: 10.1583/13-4625R.1. PMID: 25101571.
- Li H, Zhang F, Liang G, Luo X, Zhang C, Feng Y, Guo M. A prospective randomized controlled clinical trial on clopidogrel combined with warfarin versus clopidogrel alone in the prevention of restenosis after endovascular treatment of the femoropopliteal artery. Ann Vasc Surg. 2013 Jul;27(5):627-33. doi: 10.1016/j.avsg.2012.07.011. Epub 2013 Mar 26. PMID: 23540665.
- Iida O, Yokoi H, Soga Y, Inoue N, Suzuki K, Yokoi Y, Kawasaki D, Zen K, Urasawa K, Shintani Y, Miyamoto A, Hirano K, Miyashita Y, Tsuchiya T, Shinozaki N, Nakamura M, Isshiki T, Hamasaki T, Nanto S; STOP-IC investigators. Cilostazol reduces angiographic restenosis after endovascular therapy for femoropopliteal lesions in the Sufficient Treatment of Peripheral Intervention by Cilostazol study. Circulation. 2013 Jun 11;127(23):2307-15. doi: 10.1161/CIRCULATIONAHA.112.000711. Epub 2013 May 7. PMID: 23652861.
- Moll F, Baumgartner I, Jaff M, Nwachuku C, Tangelder M, Ansel G, Adams G, Zeller T, Rundback J, Grosso M, Lin M, Mercur MF, Minar E; ePAD Investigators. Edoxaban Plus Aspirin vs Dual Antiplatelet Therapy in Endovascular Treatment of Patients With Peripheral Artery Disease: Results of the ePAD Trial. J Endovasc Ther. 2018 Apr;25(2):158-168. doi: 10.1177/1526602818760488. PMID: 29552984; PMCID: PMC5862321.
- Monaco M, Di Tommaso L, Pinna GB, Lillo S, Schiavone V, Stassano P. Combination therapy with warfarin plus clopidogrel improves outcomes in femoropopliteal bypass surgery patients. J Vasc Surg. 2012 Jul;56(1):96-105. doi: 10.1016/j.jvs.2012.01.004. Epub 2012 May 1. PMID: 22551909.
- Patel MR, Becker RC, Wojdyla DM, Emanuelsson H, Hiatt WR, Horrow J, Husted S, Mahaffey KW, Steg PG, Storey RF, Wallentin L, James SK. Cardiovascular events in acute coronary syndrome patients with peripheral arterial disease treated with ticagrelor compared with clopidogrel: Data from the PLATO Trial. Eur J Prev Cardiol. 2015 Jun;22(6):734-42. doi: 10.1177/2047487314533215. Epub 2014 May 15. PMID: 24830710.
- Peripheral Arterial Diseases Antiplatelet Consensus Group. Antiplatelet therapy in peripheral arterial disease. Consensus statement. Eur J Vasc Endovasc Surg. 2003 Jul;26(1):1-16. doi: 10.1053/ejvs.2002.1927. PMID: 12819642.
- Qureshi MI, Li HL, Ambler GK, Wong KHF, Dawson S, Chaplin K, Cheng HY, Hinchliffe RJ, Twine CP. Antiplatelet and Anticoagulant Use in Randomised Trials of Patients Undergoing Endovascular Intervention for Peripheral Arterial Disease: Systematic Review and Narrative Synthesis. Eur J Vasc Endovasc Surg. 2020 Jul;60(1):77-87. doi: 10.1016/j.ejvs.2020.03.010. Epub 2020 Apr 4. PMID: 32265113.
- Rymer J, Anand SS, Sebastian Debus E, Haskell LP, Hess CN, Jones WS, Muehlhofer E, Berkowitz SD, Bauersachs RM, Bonaca MP, Patel MR. Rivaroxaban Plus Aspirin Versus Aspirin Alone After Endovascular Revascularization for Symptomatic PAD: Insights From VOYAGER PAD. Circulation. 2023 Dec 12;148(24):1919-1928. doi: 10.1161/CIRCULATIONAHA.122.063806. Epub 2023 Oct 18. PMID: 37850397.
- SCHWARZWALDER U, ZELLER T. Below-the-knee revascularization. Advanced techniques. J Cardiovasc Surg (Torino). 2009 Oct;50(5):627-34. PMID: 19741578.
- Shigematsu H, Komori K, Tanemoto K, Harada Y, Nakamura M. Clopidogrel for Atherothrombotic Event Management in Patients with Peripheral Arterial Disease (COOPER) Study: Safety and Efficacy of Clopidogrel versus Ticlopidine in Japanese Patients. Ann Vasc Dis. 2012;5(3):364-75. doi: 10.3400/avd.oa.12.00039. PMID: 23555538; PMCID: PMC3595857.
- Soga Y, Yokoi H, Kawasaki T, Nakashima H, Tsurugida M, Hikichi Y, Nobuyoshi M. Efficacy of cilostazol after endovascular therapy for femoropopliteal artery disease in patients with intermittent claudication. J Am Coll Cardiol. 2009 Jan 6;53(1):48-53. doi: 10.1016/j.jacc.2008.09.020. PMID: 19118724.
- Soga Y, Takahara M, Iida O, Yamauchi Y, Hirano K, Fukunaga M, Zen K, Suzuki K, Shintani Y, Miyashita Y, Tsuchiya T, Yamaoka T, Ando K. Efficacy of CilostAzol for Below-the-Knee Artery Disease after Balloon AnGioplasty in PatiEnts with Severe Limb Ischemia (CABBAGE Trial). Ann Vasc Surg. 2017 Nov;45:22-28. doi: 10.1016/j.avsg.2017.05.029. Epub 2017 Jun 6. PMID: 28600024.
- Steg PG, Bhatt DL, Wilson PW, D'Agostino R Sr, Ohman EM, Röther J, Liau CS, Hirsch AT, Mas JL, Ikeda Y, Pencina MJ, Goto S; REACH Registry Investigators. One-year cardiovascular event rates in outpatients with atherothrombosis. JAMA. 2007 Mar 21;297(11):1197-206. doi: 10.1001/jama.297.11.1197. PMID: 17374814.
- 10.1001/jama.288.19.2411. Erratum in: JAMA. 2003 Feb 26;289(8):987. PMID: 12435254.
- Sterne JA, Sutton AJ, Ioannidis JP, Terrin N, Jones DR, Lau J, Carpenter J, Rücker G, Harbord RM, Schmid CH, Tetzlaff J, Deeks JJ, Peters J, Macaskill P, Schwarzer G, Duval S, Altman DG, Moher D, Higgins JP. Recommendations for examining and interpreting funnel plot asymmetry in meta-analyses of randomised controlled trials. BMJ. 2011 Jul 22;343:d4002. doi: 10.1136/bmj.d4002. PMID: 21784880.
- Tepe G, Bantleon R, Brechtel K, Schmehl J, Zeller T, Claussen CD, Strobl FF. Management of peripheral arterial interventions with mono or dual antiplatelet therapy--the MIRROR study: a randomised and double-blinded clinical trial. Eur Radiol. 2012 Sep;22(9):1998-2006. doi: 10.1007/s00330-012-2441-2. Epub 2012 May 10. PMID: 22569995.
- Wang Y, Wang Y, Zhao X, Liu L, Wang D, Wang C, Wang C, Li H, Meng X, Cui L, Jia J, Dong Q, Xu A, Zeng J, Li Y, Wang Z, Xia H, Johnston SC; CHANCE Investigators. Clopidogrel with aspirin in acute minor stroke or transient ischemic attack. N Engl J Med. 2013 Jul 4;369(1):11-9. doi: 10.1056/NEJMoa1215340. Epub 2013 Jun 26. PMID: 23803136.
- Wegerif ECJ, Ünlü Ç, Generaal MI, van den Bor RM, van de Ven PM, Bots ML, de Borst GJ. Rationale and design for the randomized placebo-controlled double-blind trial studying the effect of single antiplatelet therapy (clopidogrel) versus dual antiplatelet therapy (clopidogrel/acetylsalicylic acid) on the occurrence of atherothrombotic events following lower extremity peripheral transluminal angioplasty (CLEAR-PATH). Am Heart J. 2024 Jul;273:121-129. doi: 10.1016/j.ahj.2024.04.001. Epub 2024 Apr 10. PMID: 38608997.
Evidence tabel
|
Study |
Participants (number, age, other important characteristics) |
Comparison |
Follow-up |
Outcome measures |
Risk of bias (adopted from the network meta-analysis of Willems (2022))* |
|
Included in the systematic review of Willems (2022) |
|||||
|
Becquimin (1997) |
N total: N = 243
Age 67.0 years
Sex % (male) 77% male
Population PVI |
Intervention: TP2
Control: P |
24 months |
MACE |
Low risk |
|
BOA (2000) |
N total: N = 2690
Age 69.0 years
Sex % (male) 64% male
Population PVI |
Intervention: A
Control: VKA2 |
21 months |
MACE MALE
|
Low risk |
|
CABBAGE (2017) |
N total: N = 50
Age 73.0 years
Sex % (male) 74% male
Population PVI |
Intervention: A
Control: A+CI |
3 months |
MACE MALE |
Low risk |
|
CAPRIE (1996) |
N total: N = 6452
Age 64.0 years
Sex % (male) 72% male
Population PAD |
Intervention: A
Control: C |
23 months |
MACE |
Low risk |
|
CASPAR (2010) |
N total: N = 851
Age 66.0 years
Sex % (male) 76% male
Population PVI |
Intervention: A
Control: A + C |
12 months |
MALE MB |
Low risk |
|
CHARISMA (2009) |
N total: N = 3096
Age 60.0 years
Sex % (male) 70% male
Population PAD |
Intervention: A
Control: A + C |
26 months |
MACE MB |
Low risk |
|
CLIPS (2007) |
N total: N = 366
Age 66.0
Sex % (male) 77% male
Population PAD |
Intervention: A
Control: P
|
21 months |
MACE
|
|
|
COMPASS (2018) |
N total: N = 7470
Age 68.0
Sex % (male) 72% male
Population PAD |
Intervention: A
Control: A + R1
Control: R2
|
21 months |
MACE MALE MB ALI
|
Some concerns |
|
COOPER (2012) |
N total: N = 431
Age 71.0
Sex % (male) 88% male
Population PAD |
Intervention: C
Control: TPI |
3 months |
MACE
|
Low risk |
|
CREDO (2006) |
N total: N = 272
Age 67.0
Sex % (male) 66% male
Population CAD |
Intervention: A
Control: A + C |
12 months |
MACE |
Low risk |
|
ePAD (2018) |
N total: N = 203
Age 67.0
Sex % (male) 29% male
Population PVI |
Intervention: A + C
Control: A + E |
2.7 months |
MACE MB |
Low risk |
|
EUCLID (2017) |
N total: N = 13,885
Age 66.0
Sex % (male) 72% male
Population PAD |
Intervention: C
Control: TG2 |
30 months |
MACE MB ALI
|
Low risk |
|
Gresele (2000) |
N total: N = 159
Age 66.0
Sex % (male) 86% male
Population PAD |
Intervention: A
Control: A + CC |
6 months |
MACE |
Low risk |
|
Johnson (2002) |
N total: N = 831
Age 64.0
Sex % (male) Not reported.
Population PVI |
Intervention: A
Control: A + VKA1 |
38 months |
MB |
Low risk |
|
Li (2013) |
N total: N = 50
Age 74.0
Sex % (male)
Population PVI |
Intervention: C
Control: C + VKA1 |
12 months |
MACE MB
|
High risk |
|
MIRROR (2011) |
N total: N = 80
Age 70.0
Sex % (male) 66% male
Population PVI |
Intervention: A
Control: A + C |
6 months |
MACE |
High risk |
|
Monaco (2012) |
N total: N = 318
Age 67.0
Sex % (male) 53% male
Population PVI |
Intervention: A + C
Control: C + VKA1 |
77 months |
MACE MB |
Low risk |
|
PEGASUS TIMI 54 (2016) |
N total: N = 1143
Age 66.0
Sex % (male) 70% male
Population CAD |
Intervention: A
Control: A + TGI
Control: A + TG2 |
36 months |
MACE MALE MB ALI |
Low risk |
|
PLATO (2015) |
N total: N = 1144
Age 66.0
Sex % (male) 78% male
Population CAD |
Intervention: A + C
Control: A + TG2 |
9 months |
MACE MB |
Low risk |
|
RIVAL-PAD (2020) |
N total: N = 20
Age 67.0
Sex % (male) 60% male
Population PVI |
Intervention: A + C
Control: A + R1 |
3 months |
MB |
Low risk |
|
Soga (2009) |
N total: N = 80
Age 71.0
Sex % (male) 83% male
Population PVI |
Intervention: A + TP1
Control: A + TP1 + CI |
24 months |
MACE MB |
Some concerns |
|
STOP-IC (2013) |
N total: N = 200
Age 73.0
Sex % (male) 59% male
Population PVI |
Intervention: A
Control: A + CI |
12 months |
MACE MALE |
Low risk |
|
VOYAGER-PAD (2020) |
N total: N = 6564
Age 67.0
Sex % (male) 74% male
Population PVI |
Intervention: A
Control: A + R1 |
28 months |
MACE MALE MB ALI
|
Low risk |
|
WAVE (2007) |
N total: N = 2161
Age 64.0
Sex % (male) 74% male
Population PAD |
Intervention: A
Control: A + VKA1 |
35 months |
MACE MB ALI |
Low risk |
Risk of bias tabel
Exclusie tabel
|
Reference |
Reason for exclusion |
|
De Carlo M, Di Minno G, Sayre T, Fazeli MS, Siliman G, Cimminiello C. Efficacy and Safety of Antiplatelet Therapies in Symptomatic Peripheral Artery Disease: A Systematic Review and Network Meta-Analysis. Curr Vasc Pharmacol. 2021;19(5):542-555. doi: 10.2174/1570161118666200820141131. PMID: 32819249; PMCID: PMC8573731.
|
A more recent published NMA was included. |
|
Katsanos K, Spiliopoulos S, Saha P, Diamantopoulos A, Karunanithy N, Krokidis M, Modarai B, Karnabatidis D. Comparative Efficacy and Safety of Different Antiplatelet Agents for Prevention of Major Cardiovascular Events and Leg Amputations in Patients with Peripheral Arterial Disease: A Systematic Review and Network Meta-Analysis. PLoS One. 2015 Aug 14;10(8):e0135692. doi: 10.1371/journal.pone.0135692. PMID: 26274912; PMCID: PMC4537264. |
A more recent published NMA was included. |
|
Liang X, Wang Y, Zhao C, Cao Y. Systematic review the efficacy and safety of cilostazol, pentoxifylline, beraprost in the treatment of intermittent claudication: A network meta-analysis. PLoS One. 2022 Nov 1;17(11):e0275392. doi: 10.1371/journal.pone.0275392. PMID: 36318524; PMCID: PMC9624404. |
A more recent published NMA was included. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 02-04-2025
Beoordeeld op geldigheid : 01-04-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg rondom patiënten met (chronisch) perifeer arterieel vaatlijden van de onderste extremiteit(en).
Werkgroep
- Dr. B. (Bram) Fioole (voorzitter), Nederlandse Vereniging voor Heelkunde
- Dr. C. (Çagdas) Ünlü, Nederlandse Vereniging voor Heelkunde
- Drs. J.L. (Jorg) de Bruin, Nederlandse Vereniging voor Heelkunde
- Prof. dr. B.M.E. (Barend) Mees, Nederlandse Vereniging voor Heelkunde
- Drs. D.A.F. (Daniel) van den Heuvel, Nederlandse Vereniging voor Radiologie
- Dr. S.W. (Sanne) de Boer, Nederlandse Vereniging voor Radiologie
- Dr. R. (Rinske) Loeffen), Nederlandse Internisten Vereniging
- Dr. M.E.L. (Marie-Louise) Bartelink, Nederlands Huisartsen Genootschap
- E. (Emilien) Wegerif, Nederlandse Vereniging voor Heelkunde
- J. (Jenny) Zwiggelaar, Koninklijk Nederlands Genootschap voor Fysiotherapie / Vereniging van Oefentherapeuten Cesar en Mensendieck
- G. (Gilaine) Kleian, Harteraad
- P.A.H. (Patricia) van Mierlo – van den Broek, MANP, Verpleegkundigen & Verzorgenden Nederland / VS Vaatchirurgie Netwerk
Met ondersteuning van:
- Dr. W. (Wouter) Harmsen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot 2023)
- Dr. R. (Romy) Zwarts - van de Putte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot 2023)
- Dr. M.S. (Matthijs) Ruiter, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf 2023)
- M. (Mitchel) Griekspoor, MSc, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf 2023)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Hoofdfunctie |
Project Tekstveld |
Nevenwerkzaamheden |
Persoonlijke Financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intell. Belangen en reputatie |
Overige belangen |
Ondernomen actie |
|
Bram Fioole (vz.) |
Vaatchirurg |
Richtlijn Perifeer arterieel vaatlijden |
Opleider vaatchirurgie en algemene heelkunde Maasstadziekenhuis, onbetaald
Secretaris Stichting DEAll (stichting ter bevordering van wetenschappelijk onderzoek op het gebied van de vaatchirurgie en interventieradiologie), onbetaald.
|
Geen. |
Geen. |
Stichting DEAll/FOREST trial/projectleider-> ja Getinge/DISCOVER trial/projectleider-> ja Cook/Zephyr registry/ projectleider -> ja |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Marie-Louise Bartelink |
* 80% huisartsdocent en -onderzoeker, associate professor * 20% huisartsdocent
|
Richtlijn Perifeer arterieel vaatlijden |
Geen. |
Geen. |
Geen. |
ZonMw - EBM-leren in de huisartspraktijk, kwalittatieve studies - Projectleider |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Patricia van Mierlo – van den Broek |
Verpleegkundig Specialist in het specialisme Algemene Gezondheidszorg werkzaam bij de afdeling Vaatchirurgie.
|
Richtlijn Perifeer arterieel vaatlijden |
Als vrijwilliger werkzaam (onbetaald) als collectant voor een aantal goede doelen (KWF en dierenbescherming) |
Geen. |
Geen. |
Betrokken bij de "FOREST"-trial (randomized comparison of FemORal drug-Eluting balloons and Stents), een gerandomiseerd prospectief multicenter onderzoek waarbij de langere termijn resultaten van drug-eluting ballonnen en stents in het AFS traject onderzocht wordt (NL57055.101.16). Deze trial wordt gesponsord door de stichting DEAII (Dutch Endovascular Alliance).
|
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Emilien Wegerif |
Arts onderzoeker |
Richtlijn Perifeer arterieel vaatlijden
|
Eigenaresse Caro-Jo Amsterdam, eenmanszaak betaald Caro-Jo Amsterdam is een Chaar sierraden merk
|
Ik heb geen financiële belangen bij de uitkomsten van de publicaties |
Geen. |
Geen. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Jenny Zwiggelaar |
*Fysiotherapeut, hart-vaat-long gespecialiseerd
*Projectmedewerker Chronisch ZorgNet
Beide functies in loondienst |
Richtlijn Perifeer arterieel vaatlijden
|
Geen. |
Geen, enkel de bekende werkrelaties. |
Geen. |
Geen. |
Geen persoonlijk belangen of reputatiegewin. Ik treed in deze werkgroep als afgevaardigde van de beroepsgroep KNGF en zal enkel de kennis vanuit ChronischZorgnet (voorheen ClaudicatioNet) meebrengen.
|
Chronisch ZorgNet is op de hoogte en ondersteund de inbreng in deze werkgroep. Vanuit KNGF is de duidelijke opdracht om alle fysiotherapeuten met de specialisatie PAV te vertegenwoordigen. Dit zal naar verwachting ook beter zichtbaar worden bij het invoeren van het aantekenregister Vaat (als onderdeel van deelregistratie hart-vaat-long-fysiotherapeut). Er is een open en prettige communicatie onderling en geen belangenverstrengeling.
|
Geen restricties voor deelname aan de richtlijn. |
|
Rinske Loeffen |
Internist vasculair geneeskundige |
Richtlijn Perifeer arterieel vaatlijden
|
* Redactielid Focus Vasculair (onbetaald) * Werkgroep Tabaksontmoediging NVALT (onbetaald) * Werkgroep SKMS project Stop met Roken Zorg (onbetaald) * Werkgroep Acute boekje vasculaire geneeskunde (onbetaald).
|
Geen. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Sanne de Boer |
Interventieradioloog |
Richtlijn Perifeer arterieel vaatlijden |
* Verschillende wetenschappelijke en beleidscommissies binnen de NVIR (onbetaald) * Institutioneel contract met Brainlab voor consultant werkzaamheden * Institutioneel contract met MUMC/CTCM * Incidenteel consultant werkzaamheden voor Philips, ook via institutioneel contract.
|
Zie nevenwerkzaamheden. |
Geen. |
|
Geen. |
Geen. |
Geen restricties. Onderwerp van advieswerk valt buiten de afbakening van de richtlijn. |
|
Çagdas Ünlü |
Vaatchirurg |
Richtlijn Perifeer arterieel vaatlijden
|
Projectleider CLEARPATH, studie na antistolling na endovasculaire behandeling ZonMw subsidie |
Geen. |
Geen. |
ZonMw (Clearpath) |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Daniel van den Heuvel |
Interventie Radioloog |
Richtlijn Perifeer arterieel vaatlijden
|
Proctor voor bedrijf LimFlow SA, Parijs. Betaald. Adjudicator voor Bioreact studie, Biotronic. Betaald. |
Zie nevenwerkzaamheden. Verder geen persoonlijke financiële belangen. |
Geen. |
Philips/Illumenate BTK PMS. Effectiviteit en veiligheid van de Stellarex .014 Ballon bij patiënten met kritieke ischemie ->ja. Micromedical/Heal study, PMS. Effectiviteit en veiligheid van de Microstent bij patiënten met kritieke ischemie -> ja. Philips/REPEAT study. Reproduceerbaarheid van 2D perfusie angiografie-> ja. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Jorg de Bruin |
Vaatchirurg |
Richtlijn Perifeer arterieel vaatlijden
|
EMC; Klinisch en wetenschappelijk werk vaatchirurgie in academisch ziekenhuis |
Geen conflict of specifiek belang. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn. |
|
Ilse Verstraaten |
Beleidsadviseur Harteraard (betaald) |
Richtlijn Perifeer arterieel vaatlijden
|
Geen. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn.
|
|
Gilaine Kleian |
Junior projectmedewerker, Harteraad |
Richtlijn Perifeer arterieel vaatlijden
|
Geen. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen. |
Geen restricties voor deelname aan de richtlijn.
|
|
Barend Mees |
Vaatchirurg |
Richtlijn Perifeer arterieel vaatlijden
|
* Secretaris bestuur Nederlandse Vereniging voor Vaatchirurgie * Lid Commissie Richtlijnen NVvH * Council Member European Society for Vascular Surgery * Member ESVS Steering Guideline Committee * Director European Vascular Course. * Bestuur Stichting Drie Lichten * Lid Onderzoekspijler Dutch Cardiovascular Alliance * Lid adviesraad Marfan patienten * Consultancy werkzaamheden voor Philips, Bentley Innomed. |
Geen. |
Geen. |
* Regmed XB: Cardiovascular Moonshot (Moonshot leader) * EU-Horizon 2020: PAPA-ARTIS (local PI) * InScIte: XS-graft (onderzoeksleider) * Philips: SAVER-registry (National PI) * ID3: Supersurg trial (local PI) * Cook: Zephyr registry (local PI) * Philips: FORS registry (local co-PI) * ZonMw: GENPAD study (local PI) |
*Ontwikkelaar van de mazeBox, een training tool voor endovasculaire technieken. |
Geen. |
Geen restricties voor deelname aan richtlijn. Genoemde onderzoek valt buiten de afbakening van de richtlijn. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van Harteraad voor de schriftelijke knelpuntenanalyse. Het verslag hiervan is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de deelnemers van de schriftelijke knelpuntenanalyse en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst.
|
Module |
Uitkomst raming |
Toelichting |
|
Module: Antitrombotische therapie na chirurgische en/of endovasculaire interventie |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn, volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van het zorgpersoneel betreft. Toediening van duurdere medicatie betreft een beperkt aantal patiënten. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met (chronisch) perifeer arterieel vaatlijden van de onderste extremiteit(en). Tevens zijn er knelpunten aangedragen via een schriftelijke knelpuntenanalyse. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. [Review Manager 5.4] werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in module 14 en 15.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: Perifeer arterieel vaatlijden – UV2 Antitrombotische therapie na chirurgische en/of endovasculaire interventie |
|
|
Uitgangsvraag/modules: Wat zijn de (on)gunstige effecten van verschillende antitrombotica bij patiënten met perifeer arterieel vaatlijden die een endovasculaire of chirurgische interventie ondergingen? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 22 april 2024 |
|
Periode: vanaf 2000 |
Talen: geen restrictie |
|
Literatuurspecialist: Esther van der Bijl |
Rayyan review: https://rayyan.ai/reviews/1007290 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen perifeer arterieel vaatlijden EN antitrombotica.
Deze zoekstrategie is opgebouwd naar het artikel van Willems et al (2022). Zoals afgesproken worden alleen de Netwerk meta-analyses aangeboden in Rayyan.
à De volgende sleutelartikelen worden vanwege het studiedesign niet gevonden met deze search:
Het volgende sleutelartikel valt uit op de P, er wordt in titel, abstract of keywords niet over arterie gesproken:
|
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op 22 april 2024 systematisch gezocht naar netwerk meta-analyses over de effecten van verschillende antitrombotica bij patiënten met perifeer arterieel vaatlijden. De literatuurzoekactie leverde 29 unieke treffers op. |
|
Zoekopbrengst 22 april 2024
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
Netwerk meta-analyse |
28 |
16 |
29 |
|
Totaal |
|
|
29* |
*in Rayyan
Zoekstrategie Embase.com 22 april 2024
|
No. |
Query |
Results |
|
#1 |
'peripheral arterial disease'/exp OR 'intermittent claudication'/exp OR 'critical limb ischemia'/exp OR 'peripheral arterial occlusion'/exp OR 'iliac artery occlusion'/exp OR 'femoral artery disease'/exp OR 'popliteal artery occlusion'/exp OR 'femoropopliteal occlusive disease'/exp OR 'femoropopliteal occlusion'/exp OR ((('arter* peripheral' OR 'peripheral arter*' OR 'peripheral vascular') NEAR/3 disease*):ti,ab,kw) OR ((claudicatio* NEAR/3 intermitten*):ti,ab,kw) OR (((limb* OR leg*) NEAR/3 (ischaemia OR ischemia)):ti,ab,kw) OR (((aortic* OR iliac* OR femoral OR popliteal OR femoropopliteal) NEAR/3 'occlus*'):ti,ab,kw) OR ((('aortic arter*' OR 'iliac* arter*' OR 'femor* arter*' OR 'popliteal arter*' OR 'femoropopliteal arter*') NEAR/3 disease*):ti,ab,kw) |
188686 |
|
#2 |
'anticoagulant agent'/exp OR 'antithrombocytic agent'/exp OR 'thienopyridine derivative'/exp OR 'acetylsalicylic acid'/exp OR 'acetylsalicylic acid 3 (nitroxymethyl)phenyl ester'/exp OR 'clopidogrel'/exp OR 'prasugrel'/exp OR 'satigrel'/exp OR 'elinogrel'/exp OR 'ticagrelor'/exp OR 'cangrelor'/exp OR 'carbasalate calcium'/exp OR 'dipyridamole'/exp OR 'ticlopidine'/exp OR 'picotamide'/exp OR 'triflusal'/exp OR 'cilostazol'/exp OR 'vorapaxar'/exp OR 'indobufen'/exp OR 'blood clotting factor 10a'/exp OR 'rivaroxaban'/exp OR 'apixaban'/exp OR 'edoxaban'/exp OR 'otamixaban'/exp OR 'betrixaban'/exp OR 'darexaban'/exp OR 'argatroban'/exp OR 'melagatran'/exp OR 'inogatran'/exp OR 'terutroban'/exp OR 'dabigatran'/exp OR 'ximelagatran'/exp OR 'lepirudin'/exp OR 'desulfatohirudin'/exp OR 'bivalirudin'/exp OR 'idraparinux'/exp OR 'idrabiotaparinux'/exp OR 'fondaparinux'/exp OR 'antivitamin k'/exp OR 'coumarin'/exp OR 'warfarin'/exp OR 'acenocoumarol'/exp OR 'phenprocoumon'/exp OR 'phenindione'/exp OR 'fluindione'/exp OR 'difenacoum'/exp OR 'dicoumarol'/exp OR 'heparin'/exp OR 'heparinoid'/exp OR 'tinzaparin'/exp OR 'reviparin'/exp OR 'parnaparin'/exp OR 'nadroparin'/exp OR 'enoxaparin'/exp OR 'danaparoid'/exp OR 'dalteparin'/exp OR 'certoparin'/exp OR 'ardeparin'/exp OR 'bemiparin'/exp OR anticoagula*:ti,ab,kw OR 'anti coagula*':ti,ab,kw OR antithrombo*:ti,ab,kw OR 'anti thrombo*':ti,ab,kw OR 'platelet aggregation inhibitor*':ti,ab,kw OR 'platelet inhibitor*':ti,ab,kw OR antiplatelet*:ti,ab,kw OR 'anti platelet*':ti,ab,kw OR p2y12:ti,ab,kw OR thienopyridine*:ti,ab,kw OR aspirin:ti,ab,kw OR 'acetylsalicylic acid*':ti,ab,kw OR nitroaspirin:ti,ab,kw OR asa:ti,ab,kw OR clopidogrel:ti,ab,kw OR prasugrel:ti,ab,kw OR satigrel:ti,ab,kw OR pyragrel:ti,ab,kw OR elinogrel:ti,ab,kw OR ticagrelor:ti,ab,kw OR cangrelor:ti,ab,kw OR 'carbasalate calcium':ti,ab,kw OR dipyridamole:ti,ab,kw OR ticlopidine:ti,ab,kw OR picotamide:ti,ab,kw OR triflusal:ti,ab,kw OR cilostazol:ti,ab,kw OR vorapaxar:ti,ab,kw OR indobufen:ti,ab,kw OR (('factor xa' NEAR/1 (antagon* OR inhibit*)):ti,ab,kw) OR rivaroxaban:ti,ab,kw OR apixaban:ti,ab,kw OR edoxaban:ti,ab,kw OR otamixaban:ti,ab,kw OR betrixaban:ti,ab,kw OR darexaban:ti,ab,kw OR argatroban:ti,ab,kw OR melagatran:ti,ab,kw OR inogatran:ti,ab,kw OR terutroban:ti,ab,kw OR dabigatran:ti,ab,kw OR ximelagatran:ti,ab,kw OR lepirudin:ti,ab,kw OR desirudin:ti,ab,kw OR bivalirudin:ti,ab,kw OR idraparinux:ti,ab,kw OR idrabiotaparinux:ti,ab,kw OR fondaparinux:ti,ab,kw OR (('vitamin k' NEAR/1 (antagon* OR inhibit*)):ti,ab,kw) OR coumarin:ti,ab,kw OR warfarin:ti,ab,kw OR acenocoumarol:ti,ab,kw OR phenprocoumon:ti,ab,kw OR phenindione:ti,ab,kw OR fluindione:ti,ab,kw OR difenacoum:ti,ab,kw OR dicumarol:ti,ab,kw OR heparin:ti,ab,kw OR lmwh:ti,ab,kw OR lmh:ti,ab,kw OR heparinoids:ti,ab,kw OR tinzaparin:ti,ab,kw OR reviparin:ti,ab,kw OR parnaparin:ti,ab,kw OR nadroparin:ti,ab,kw OR enoxaparin:ti,ab,kw OR danaparoid:ti,ab,kw OR dalteparin:ti,ab,kw OR certoparin:ti,ab,kw OR bemiparin:ti,ab,kw OR ardeparin:ti,ab,kw |
1022673 |
|
#3 |
#1 AND #2 |
32572 |
|
#4 |
#3 AND [2000-2024]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
21017 |
|
#5 |
'network meta-analysis'/exp OR ((network NEAR/3 ('meta analys*' OR metaanalys*)):ti,ab,kw) – Netwerk meta-analyses |
15256 |
|
#6 |
#4 AND #5 |
28 |
Zoekstrategie Ovid/Medline 22 april 2024
|
# |
Searches |
Results |
|
1 |
exp Peripheral Arterial Disease/ or exp Intermittent Claudication/ or exp Chronic Limb-Threatening Ischemia/ or ((arter* peripheral or peripheral arter* or peripheral vascular) adj3 disease*).ti,ab,kf. or (claudicatio* adj3 intermitten*).ti,ab,kf. or ((limb* or leg*) adj3 (ischaemia or ischemia)).ti,ab,kf. or ((aortic* or iliac* or femoral or popliteal or femoropopliteal) adj3 occlus*).ti,ab,kf. or ((aortic arter* or iliac* arter* or femor* arter* or popliteal arter* or femoropopliteal arter*) adj3 disease*).ti,ab,kf. |
60861 |
|
2 |
exp Anticoagulants/ or exp Thienopyridines/ or exp Clopidogrel/ or exp Prasugrel Hydrochloride/ or exp Ticagrelor/ or exp Dipyridamole/ or exp Ticlopidine/ or exp Cilostazol/ or exp Rivaroxaban/ or exp Dabigatran/ or exp Fondaparinux/ or exp Coumarins/ or exp Warfarin/ or exp Acenocoumarol/ or exp Phenprocoumon/ or exp Phenindione/ or exp Dicumarol/ or exp Heparin/ or exp Heparinoids/ or exp Tinzaparin/ or exp Nadroparin/ or exp Enoxaparin/ or exp Dalteparin/ or anticoagula*.ti,ab,kf. or anti coagula*.ti,ab,kf. or antithrombo*.ti,ab,kf. or anti thrombo*.ti,ab,kf. or platelet aggregation inhibitor*.ti,ab,kf. or platelet inhibitor*.ti,ab,kf. or antiplatelet*.ti,ab,kf. or anti platelet*.ti,ab,kf. or p2y12.ti,ab,kf. or thienopyridine*.ti,ab,kf. or aspirin.ti,ab,kf. or acetylsalicylic acid*.ti,ab,kf. or nitroaspirin.ti,ab,kf. or asa.ti,ab,kf. or clopidogrel.ti,ab,kf. or prasugrel.ti,ab,kf. or satigrel.ti,ab,kf. or pyragrel.ti,ab,kf. or elinogrel.ti,ab,kf. or ticagrelor.ti,ab,kf. or cangrelor.ti,ab,kf. or carbasalate calcium.ti,ab,kf. or dipyridamole.ti,ab,kf. or ticlopidine.ti,ab,kf. or picotamide.ti,ab,kf. or triflusal.ti,ab,kf. or cilostazol.ti,ab,kf. or vorapaxar.ti,ab,kf. or indobufen.ti,ab,kf. or (factor xa adj1 (antagon* or inhibit*)).ti,ab,kf. or rivaroxaban.ti,ab,kf. or apixaban.ti,ab,kf. or edoxaban.ti,ab,kf. or otamixaban.ti,ab,kf. or betrixaban.ti,ab,kf. or darexaban.ti,ab,kf. or argatroban.ti,ab,kf. or melagatran.ti,ab,kf. or inogatran.ti,ab,kf. or terutroban.ti,ab,kf. or dabigatran.ti,ab,kf. or ximelagatran.ti,ab,kf. or lepirudin.ti,ab,kf. or desirudin.ti,ab,kf. or bivalirudin.ti,ab,kf. or idraparinux.ti,ab,kf. or idrabiotaparinux.ti,ab,kf. or fondaparinux.ti,ab,kf. or (vitamin k adj1 (antagon* or inhibit*)).ti,ab,kf. or coumarin.ti,ab,kf. or warfarin.ti,ab,kf. or acenocoumarol.ti,ab,kf. or phenprocoumon.ti,ab,kf. or phenindione.ti,ab,kf. or fluindione.ti,ab,kf. or difenacoum.ti,ab,kf. or dicumarol.ti,ab,kf. or heparin.ti,ab,kf. or lmwh.ti,ab,kf. or lmh.ti,ab,kf. or heparinoids.ti,ab,kf. or tinzaparin.ti,ab,kf. or reviparin.ti,ab,kf. or parnaparin.ti,ab,kf. or nadroparin.ti,ab,kf. or enoxaparin.ti,ab,kf. or danaparoid.ti,ab,kf. or dalteparin.ti,ab,kf. or certoparin.ti,ab,kf. or bemiparin.ti,ab,kf. or ardeparin.ti,ab,kf. |
499722 |
|
3 |
1 and 2 |
5659 |
|
4 |
limit 3 to yr="2000 -Current" |
4646 |
|
5 |
4 not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
4350 |
|
6 |
exp Network Meta-Analysis/ or (network adj3 ('meta analys*' or metaanalys*)).ti,ab,kf. – Netwerk meta-analyses |
11107 |
|
7 |
5 and 6 |
16 |