Elektrostimulatie bij dysfagie
Uitgangsvraag
Wat is de meerwaarde van (functionele) elektrostimulatie in de behandeling van patiënten met dysfagie?
Aanbeveling
Aanbeveling-1
Bekijk of neuromusculaire (oppervlakte) elektrostimulatie in individuele gevallen de slikrevalidatie van patiënten met dysfagie als gevolg van spierzwakte door niet-aangeboren hersenletsel, zoals een cerebrovasculair accident, kan ondersteunen. Gebruik neuromusculaire (oppervlakte) elektrostimulatie in goed overleg met de patiënt en mantelzorger.
Pas elektrostimulatie alleen toe na scholing in het gebruik ervan.
Aanbeveling-2
Gebruik geen elektrostimulatie bij patiënten met dysfagie als gevolg van de ziekte van Parkinson of door chirurgische/radiotherapeutische behandeling voor hoofd-halskanker.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is literatuuronderzoek verricht naar het effect van neuromusculaire elektrostimulatie (NMES) in verschillende patiëntengroepen (cerebrovasculair accident (CVA), hoofd-halskanker en patiënten met de ziekte van Parkinson).
Patiënten met dysfagie als gevolg van een CVA
Bij patiënten met dysfagie als gevolg van een CVA kan NMES bovenop reguliere logopedische sliktherapie vs alleen reguliere logopedische sliktherapie mogelijk leiden tot een klinisch relevante verbetering van de cruciale uitkomstmaten functionele orale voedselinname en slikgerelateerde kwaliteit van leven. De kwaliteit van bewijs loopt uiteen van zeer laag tot laag door risico op bias (gebrek aan blindering van patiënten), imprecisie (de grenzen van het betrouwbaarheidsinterval overschrijden de grens van klinisch relevantie) en inconsistentie (grote variatie in puntschatters). Voor de belangrijke uitkomstmaat functioneel slikvermogen is mogelijk een gunstig effect gevonden in het voordeel van NMES bovenop reguliere sliktherapie. Ook is hier is echter de kwaliteit van bewijs laag. Er werd mogelijk weinig tot geen verschil gevonden voor de belangrijke uitkomstmaat aspiratie.
Voor patiënten met een CVA is er ook gekeken naar aanpalende literatuur. In de zelf-gecontroleerde crossover studie van Zhang (2022), werden de effecten van NMES op de initiatie van het slikken onderzocht. Patiënten kwamen in aanmerking voor de studie indien zij tussen de 18 en 80 jaar oud waren en een CVA hadden doorgemaakt volgens de criteria van de Chinese Society of Neurology (2018). Patiënten bij wie tijdens het klinisch onderzoek tevens dysfagie werd vastgesteld, ondergingen een videofluoroscopisch slikonderzoek (VFSS). Een vertraagde initiatie van het slikken werd vastgesteld op basis van de score op item 6 van het Modified Barium Swallow Impairment Profile (MBSImP). Patiënten met een MBSImP-6-score lager dan niveau 3 kwamen in aanmerking voor inclusie. Patiënten met ernstige aandoeningen van hart, lever, longen, nieren of andere vitale organen, een voorgeschiedenis van epilepsie na een CVA, nasofarynxcarcinoom of hoofd-hals-tumoren na radiotherapie, evenals ernstige gehoor- of begripsstoornissen, werden geëxcludeerd. In totaal werden 35 patiënten met vertraagde slikinitiatie geïncludeerd; 17 patiënten ontvingen eerst echte NMES, terwijl de overige 18 patiënten eerst sham-NMES ontvingen. De studie concludeerde dat NMES aspiratie kan verlagen.
Patiënten met hoofd-halskanker gerelateerde dysfagie
Bij patiënten met dysfagie als gevolg van (de radiotherapeutische behandeling van) hoofd-halskanker is het bewijs voor een gunstig additioneel effect van NMES naast reguliere logopedische sliktherapie op functionele orale voedselinname zeer beperkt en erg onzeker. Dit komt mede doordat het gebaseerd is op slechts één RCT met een zeer breed betrouwbaarheidsinterval. Er werd eveneens geen verschil gevonden voor de cruciale uitkomstmaat slikgerelateerde kwaliteit van leven. Ook hier is de kwaliteit van bewijs laag door methodologische beperkingen in studie opzet en imprecisie (breed betrouwbaarheidsinterval). Het bewijs liet zien dat functioneel slikvermogen mogelijk met een klinisch relevant verschil verbetert na behandeling met NMES naast reguliere logopedische sliktherapie vs sham NMES en reguliere logopedische sliktherapie, maar de kwaliteit van bewijs is laag doordat er geen intention-to-treat analyse is verricht en het betrouwbaarheidsinterval overschrijdt de grens van klinisch relevantie. Tot slot is ook het bewijs zeer onzeker voor de uitkomstmaat aspiratie.
Patiënten met dysfagie als gevolg van de ziekte van Parkinson
In patiënten met de ziekte van Parkinson is het bewijs zeer beperkt. De cruciale uitkomstmaten functioneel orale voedselinname en slikgerelateerd kwaliteit van leven waren niet gerapporteerd. Er werd slechts één studie gevonden dat wel rapporteerde over de belangrijke uitkomstmaten functioneel slikvermogen en aspiratie. Het bewijs is echter zeer onzeker, mede door ernstige imprecisie (zeer breed betrouwbaarheidsinterval, laag aantal patiënten). Eerder werd er al geen bewijs voor een additioneel effect van NMES naast logopedie gevonden door Heijnen et al (2012) en Baijens et al (2013).
Voor alle drie de patiëntengroepen werd de belangrijke uitkomstmaat aantal patiënten dat teruggaat naar een normaal dieet niet gerapporteerd.
Uit theoretisch oogpunt is het te verklaren waarom patiënten met dysfagie als gevolg van een CVA een additioneel positief effect kunnen krijgen van NMES. NMES berust op het passief aanspannen van spieren om spierzwakte en atrofie te compenseren. Er zou een herstel kunnen optreden van motorische en sensorische banen in het perifere en centrale zenuwstelsel met een mogelijk herstel van spiercontractiepatronen. Bij patiënten met een status na (radiotherapie als gevolg van) hoofd-halskanker of een progressieve neurodegeneratieve aandoening zoals de ziekte van Parkinson is dit herstel minder te verwachten.
Kwaliteit van bewijs
Patiënten met dysfagie als gevolg van een CVA
Over het algemeen is de kwaliteit van bewijs zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege (zeer) ernstige:
- Risk of bias: methodologische beperkingen binnen het randomisatieproces, gebrek aan blindering van patiënten en personeel.
- Inconsistentie: grote variatie in puntschatters.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grenzen van klinisch relevantie overschrijdt.
Patiënten met hoofd-halskanker gerelateerde dysfagie
Over het algemeen is de kwaliteit van bewijs zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege (zeer) ernstige:
- Risk of bias: methodologische beperkingen binnen het randomisatieproces, gebrek aan blindering van patiënten en personeel.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grenzen van klinisch relevantie overschrijdt.
Patiënten met dysfagie als gevolg van de ziekte van Parkinson
De kwaliteit van bewijs werd niet gegradeerd, omdat er geen bewijs is gevonden voor de twee cruciale uitkomstmaten.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
NMES in de hals regio wordt veelal goed verdragen door patiënten. De therapiebelasting voor de patiënt neemt toe door NMES, omdat het een aanvulling is op reguliere logopedische behandeling, echter indien er additionele verlichting ontstaat van klachten door NMES kan het op de langere termijn voor minder belasting zorgen.
De bijwerkingen van NMES, zoals lokale huidirritatie door het gebruik van de plakkers of door de elektrische pulsen, zijn beperkt.
Kostenaspecten
De apparatuur moet eenmalig worden aangeschaft en het personeel moet eenmalig worden geschoold. Ook de kosten van de pleisters zijn relatief laag. Gezien de lage kwaliteit van het wetenschappelijke bewijs is niet duidelijk te stellen of de mogelijke ziektewinst bij patiënten met slikklachten door een CVA opweegt ten opzichte van de kosten die gemaakt worden.
Gelijkheid ((health) equity/equitable)
NMES wordt niet standaard in ziekenhuizen of revalidatieklinieken aangeboden. Daarmee is de plek waar iemand is opgenomen bepalend voor de toegankelijkheid tot NMES. Dit geldt eveneens voor de poliklinische toegang, aangezien er een verwijzing gemaakt moet worden naar een centrum die NMES aanbiedt. Gezien het beperkte wetenschappelijk bewijs voor NMES leidt dit slechts beperkt tot ongelijkheid van zorg.
Aanvaardbaarheid
Ethische aanvaardbaarheid
NMES is aanvaardbaar voor de betrokkenen. Er zijn geen ethische bezwaren.
Duurzaamheid
Bij NMES lijken duurzaamheidsaspecten beperkt. Bij gebruik van NMES naast reguliere logopedische sliktherapie worden disposable plakkers gebruikt voor de elektroden, maar de pleisters kunnen ook hergebruikt worden.
Haalbaarheid
De apparatuur om NMES uit te voeren is commercieel verkrijgbaar. Er zijn verschillende apparaten op de markt met verschillende stimulatieparameters. Op basis van de literatuur is niet goed vast te stellen welke parameters het meest geschikt zijn voor slikklachten. Daarnaast is NMES niet in elk ziekenhuis of revalidatiecentrum beschikbaar en dus ook niet voor elke patiënt gemakkelijk beschikbaar. Enige ervaring en scholing is vereist voor het gebruik van NMES bij patiënten met slikklachten.
Rationale van aanbeveling-1: weging van argumenten voor en tegen de interventies
Voor niet-aangeboren hersenletsel zoals een CVA is er enig bewijs voor een additioneel positief effect van NMES. De mate van bewijs is echter van lage kwaliteit. Er is een theoretische basis waarop NMES een additioneel positief effect zou kunnen hebben voor niet-aangeboren hersenletsel, echter de literatuur is voornamelijk gericht op CVA. Het gebruik van NMES voor niet-aangeboren hersenletsel moet derhalve in goed overleg met patiënt en naasten worden gemaakt en bekeken worden of het in individuele gevallen de slikrevalidatie kan ondersteunen. Patiënten dienen hiervoor cognitief voldoende sterk te zijn en voldoende belastbaar om de extra inspanning te kunnen dragen en deze inspanning om te zetten naar een betere of efficiënter beoogde resultaat. Dit kan ook al in een vroeg stadium na de CVA worden gestart.
Eindoordeel:
Zwakke aanbeveling voor (doen).
Rationale van aanbeveling-2: weging van argumenten voor en tegen de interventies
Voor patiënten met slikklachten door (de chirurgische of radiotherapeutische behandeling van) hoofd-halskanker of met de ziekte van Parkinson is geen bewijs gevonden van een additioneel effect van NMES en wordt derhalve niet geadviseerd.
Eindoordeel:
Sterke aanbeveling tegen (niet doen).
Onderbouwing
Neuromuscular electrical stimulation (NMES) during swallowing training is a technique aimed at strengthening the suprahyoid muscles in particular. This is intended to enhance hyolaryngeal elevation and thereby promote a more efficient and safer pharyngeal swallowing physiology (Humbert, 2012). However, it remains unclear whether and under which conditions the application of electrical stimulation provides added value, and as a result, its use remains limited.
Summary of Findings
PICO (1.1)
Population: Stroke patients
Intervention: NMES+TDT
Comparator: TDT
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|
|
TDT |
NMES+TDT |
||||
|
Functional oral intake of food experienced by the patient (crucial) Follow-up FOIS: 1-8 weeks MASA:3-4 weeks DOSS: 2 weeks |
Measured by: FOIS Scale: 1-7, higher is better Based on data from 298 participants in 10 studies |
MD 0.87 higher (95% CI, 0.41 higher to 1.33 higher) |
Low Due to serious risk of bias, Due to serious imprecision1 |
NMES+TDT may improve functional oral intake of food experienced by the patient (measured by FOIS) when compared with TDT only in stroke patients with dysphagia. (Bucyana, 2019; Cakmak, 2022; Cola, 2021; Huang, 2014; Lee, 2014; Matos, 2022; Permsirivanich, 2009; Simonelli, 2019; Sproson, 2018; Zhang, 2016) |
|
|
Measured by: MASA Scale: 38-200, higher is better
|
MD 1.00 higher (95% CI, 10.61 lower to 12.61 higher) (Carnaby, 2020) MD 23.46 higher (95% CI, 11.77 higher to 35.15 higher) (Umay, 2017) |
Very low Due to serious risk of bias, Due to serious inconsistency, Due to serious imprecision2 |
The evidence is very uncertain about the effect of NMES+TDT on functional oral intake of food experienced by the patient (measured by MASA) when compared with TDT only in stroke patients with dysphagia. (Carnaby, 2020; Umay, 2017) |
||
|
Measured by: DOSS Scale: 1-7, higher is better Based on data from 20 participants in 1 study |
MD 0.30 higher (95% CI, 0.80 lower to 1.40 higher)
|
Very low Due to serious risk of bias, Due to very serious imprecision3 |
The evidence is very uncertain about the effect of NMES+TDT on functional oral intake of food experienced by the patient (measured by DOSS) when compared with TDT only in stroke patients with dysphagia. (Meng, 2017) |
||
|
Swallowing-related quality of life (crucial) Follow-up SWAL-QOL: 2-12 weeks EAT-10: 3 weeks
|
Measured by: SWAL-QOL Scale: 0-220, higher is better Based on data from 1414 participants in 17 studies
|
MD 23.31 higher (95% CI, 17.23 higher to 29.93 higher) |
Low Due to serious risk of bias, Due to serious imprecision4 |
NMES+TDT may improve swallowing-related quality of life (measured by SWAL-QOL questionnaire) when compared with TDT only in stroke patients with dysphagia. (Chang, 2020; Chen, 2017; Chen, 2021; Cui, 2018; Dong, 2017; Gu, 2021; Guo, 2019; Lei, 2020; Li, 2021; Mo, 2022; Shi, 2021; Sproson, 2018; Wang, 2009; Wang, 2021; Wang, 2021(b), Wen, 2020) |
|
|
Measured by: EAT-10 Scale: 0-40, lower is better Based on data from 34 participants in 1 study |
MD 3.80 lower (95% CI, 9.42 lower to 1.82 higher) |
Low Due to serious risk of bias, Due to serious imprecision5 |
NMES+TDT may improve swallowing-related quality of life (measured by EAT-10) when compared with TDT only in stroke patients with dysphagia. (Cakmak, 2022) |
||
|
Functional swallowing ability (important) Follow-up: FDS: 2-6 weeks ?: 2 weeks
|
Measured by: FDS Scale: 0-100, lower is better Based on data from 104 participants in 3 studies
|
MD 8.81 lower (95% CI, 16.48 lower to 1.15 lower) |
Low Due to serious risk of bias, Due to serious imprecision6 |
NMES+TDT may improve functional swallowing ability (measured by FDS) when compared with TDT only in stroke patients with dysphagia. (Huang, 2014; Lim, 2014; Park, 2016) |
|
|
Number or percentage of patients who return to a normal diet (important) |
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of NMES+TDT on number or percentage of patients who return to a normal diet when compared with TDT only in stroke patients with dysphagia. |
|
|
Aspiration (important) Follow-up: 2-8 weeks
|
Measured by: PAS Scale: 1-8, lower is better Based on data from 252 participants in 7 studies
|
MD 0.52 lower (95% CI, 1.07 lower to 0.04 higher) |
Low Due to serious risk of bias, Due to serious imprecision7 |
NMES+TDT may result in little to no difference in aspiration (measured by PAS) when compared with TDT only in stroke patients with dysphagia. (Arreola, 2021; Cakmak, 2022; Huang, 2014; Lim, 2014; Park, 2016; Simonelli, 2019; Sproson, 2018) |
|
1. Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias; Imprecision: serious. Left boundary of the 95% CI cross the threshold of clinical relevance;
2. Risk of Bias: serious. No information about concealment of allocation during randomization process in one study; Inconsistency: serious. Point estimates vary widely; Imprecision: serious. The lower boundary of the 95% CI overlaps with clinical relevance threshold;
3. Risk of Bias: serious. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Deviation from the intended interventions; Imprecision: very serious. Wide confidence intervals (threshold of clinical relevance overlaps with both boundaries of the 95% CI);
4. Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Other bias ; Imprecision: serious. Wide confidence intervals (left boundary of the 95% CI crosses the border of clinical relevance);
5. Risk of Bias: serious. Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Deviation from the intented intervention; Imprecision: serious. Wide confidence intervals (left boundary of the 95% CI crosses border of clinical relevance);
6. Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Other bias; Imprecision: serious. Wide confidence intervals (left boundary of 95% CI crosses the threshold of clinical relevance);
7.Risk of Bias: serious. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias; Imprecision: serious. Wide confidence intervals (left boundary of the 95% CI crosses threshold of clinical relevance).
PICO (1.2)
Population: head and neck cancer patients with dysphagia
Intervention: NMES+TT or NMES only
Comparator: sham NMES+exercises or exercises only
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|
|
Sham NMES+exercises or exercises only |
NMES+TT or NMES only |
||||
|
Functional oral intake of food experienced by the patient (crucial) FOIS: 4 weeks ASHA NOMS: 2 weeks |
Measured by: FOIS Scale: 1-7, higher is better Based on data from 65 participants in 1 study |
MD 0.14 higher
|
No GRADE (SDs not reported) |
Due to lack of data, it was not possible to draw conclusions regarding the effect of TNMES on functional oral intake of food experienced by the patient measured by FOIS when compared with exercises only in HNC patients with dysphagia. (Ku, 2023) |
|
|
Measured by: ASHA NOMS Scale: 0-7, higher is better Based on data from 26 participants in 1 study
|
MD 0.19 higher (95% CI, 1.33 lower to 1.71 higher)
|
Very low Due to very serious risk of bias, Due to serious imprecision1 |
The evidence is very uncertain about the effect of NMES+exercises on functional oral intake of food experienced by the patient (measured by ASHA NOMS) when compared with sham NMES+exercises in HNC patients with dysphagia. (Ryu, 2009) |
||
|
Swallowing-related quality of life (crucial) Up to 15 weeks |
Measured by: HNCI, MDADI and FACT-NP All: higher is better Based on data from 231 participants in 4 studies
|
SMD 0.09 higher (95% CI, 0.20 lower to 0.39 higher) |
Low Due to serious risk of bias, Due to serious imprecision2 |
NMES+TT or NMES only may result in little to no difference in swallowing-related quality of life (measured by HNCI, MDADI and FACT-NP) when compared with sham NMES+exercises or exercises only in HNC patients with dysphagia. (Ku, 2023; Langmore, 2016; Lin, 2011; Ryu, 2009) |
|
|
Functional swallowing ability (important) 2 weeks
|
Measured by: FDS Scale: 0-100, lower is better Based on data from 26 participants in 1 study
|
MD 12.90 lower (95% CI, 25.13 lower to 0.67 lower) |
Low Due to serious risk of bias, Due to serious imprecision3 |
NMES+exercises may improve functional swallowing ability (measured by FDS) when compared with sham NMES+exercises in HNC patients with dysphagia. (Ryu, 2009) |
|
|
Number or percentage of patients who return to a normal diet (important) |
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of NMES+TDT on number or percentage of patients who return to a normal diet when compared with TDT only in HNC patients with dysphagia. |
|
|
Aspiration (important) 4-15 weeks
|
Measured by: PAS Scale: 1-8, lower is better Based on data from 210 participants in 3 studies
|
MD 0.30 lower (95% CI, 1.25 lower to 0.64 higher) |
Very low Due to serious risk of bias, Due to very serious imprecision4
|
The evidence is very uncertain about the effect of NMES+exercises or TNMES only on aspiration (measured by PAS) when compared with sham NMES+exercises or exercises only in HNC patients with dysphagia. (Ku, 2023; Langmore, 2016; Lin, 2011) |
|
1. Risk of Bias: very serious. Bias arising from the randomization process; Imprecision: serious. Both boundaries of the 95% CI cross the threshold of clinical relevance;
2. Risk of Bias: serious. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias; Imprecision: serious. Wide confidence interval;
3. Risk of Bias: serious. Missing intention-to-treat analysis; Imprecision: serious. Left boundary of the 95% CI crosses the threshold of clinical relevance;
4. Risk of Bias: serious. Imprecision: very serious. Low number of patients (<200), Wide confidence intervals (left boundary of the 95% CI crosses the threshold of clinical relevance).
PICO (1.3)
Population: Parkinson’s Disease patients
Intervention: NMES+exercises
Comparator: sham NMES+exercises
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|
|
Sham NMES+exercises |
NMES+exercises |
||||
|
Functional oral intake of food experienced by the patient (crucial) |
- |
-
|
No GRADE (no evidence was found |
No evidence was found regarding the effect of NMES+exercises on number or percentage of patients who return to a normal diet when compared with sham NMES+exercises in Parkinson’s Disease patients with dysphagia. |
|
|
Swallowing-related quality of life (crucial) |
-
|
- |
No GRADE (no evidence was found |
No evidence was found regarding the effect of NMES+exercises on number or percentage of patients who return to a normal diet when compared with sham NMES+exercises only in Parkinson’s Disease patients with dysphagia. |
|
|
Functional swallowing ability (important) 4 weeks |
Measured by: VDS Scale: 0-100, lower is better Based on data from 18 participants in 1 study
|
MD 0.83 higher (95% CI, 6.78 lower to 8.44 higher) |
Very low Due to serious risk of bias, Due to very serious imprecision1 |
The evidence is very uncertain about the effect of NMES+exercises on functional swallowing ability (measured by FDS) when compared with sham NMES+exercises in Parkinson’s Disease patients with dysphagia. (Park, 2018) |
|
|
Number or percentage of patients who return to a normal diet (important) |
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of NMES+exercises on number or percentage of patients who return to a normal diet when compared with sham NMES+exercises in Parkinson’s Disease patients with dysphagia. |
|
|
Aspiration (important) 4 weeks
|
Measured by: PAS Scale: 1-8, lower is better Based on data from 18 participants in 1 study
|
MD 1.34 lower (95% CI, 2.32 lower to 0.36 lower) |
Very low Due to serious risk of bias, Due to very serious imprecision1 |
The evidence is very uncertain about the effect of NMES+exercises on aspiration (measured by PAS) when compared with sham NMES+exercises in Parkinson’s Disease patients with dysphagia. (Park, 2018) |
|
1. Risk of Bias: serious. Imprecision: very serious. Wide confidence intervals, Low number of patients (<200), Only data from one study.
Description of studies
A total of five studies were included in the analysis of the literature (n=2 for post-stroke patients, n=2 for head and neck cancer (HNC) patients, and n=1 for Parkinson’s Disease patients). Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Post-stroke dysphagia patients and traumatic brain injury
Wang (2023) conducted a systematic review (SR) and meta-analysis (MA) to compare the efficacy of neuromuscular electrostimulation (NMES) on top of swallowing therapy (ST) with ST alone in patients with post-stroke dysphagia. Eight databases were systematically searched up to 9 June 2022 (CNKI, Wanfang, VIP, SinoMed, PubMed, Embase, Cochrane Library, and Web of Science). Fourty-six randomized controlled trials (RCTs) with patients diagnosed with post-stroke dysphagia (no other neurological disease) and the same ST intervention performed in the experimental and control groups except the experimental group that received NMES, were eligible for inclusion. Outcomes relevant for the purpose of this guideline included swallowing-related quality of life (measured by the Swallowing Quality of Life questionnaire [SWAL-QOL]), swallowing function (measured by FOIS and FDS), and aspiration (measured by PAS).
Additionally, Banda (2023) conducted a network meta-analysis to evaluate the comparative effectiveness of combined and single neurostimulation and traditional dysphagia therapies (TDT) for post-stroke dysphagia. In august 2022, a systematic search was conducted across six databases (Embase, PubMed, Ovid-Medline, CINAHL, Cochrane Library, Web of Science). Additionally, reference lists of published systematic reviews and meta-analyses were searched. Eligible studies were RCTs involving adults with post-stroke dysphagia comparing the effect of different neurostimulation therapies on swallowing function and aspiration. Both standalone and combination therapies were analyzed.
HNC dysphagia patients
Paim (2023) conducted a SR and MA to evaluate the effectiveness of NMES in the rehabilitation of dysphagia following treatment for HNC. A comprehensive search was performed in MEDLINE/PubMed, Embase, Cochrane CENTRAL, SciELO, and PEDro, from database inception to September 2021. Clinical and quasi-clinical trials involving adult patients (>18y) with objectively confirmed dysphagia after radiotherapy for HNC, comparing NMES (either as standalone treatment or combined with swallowing exercises) with sham stimulation, usual care or exercises alone, were included. Outcomes relevant for the purpose of this guideline included functional oral intake of food as experienced by the patient (measured by the American speech-language-hearing association national outcome measurement system swallowing level scale, ASHA NOMS), swallowing-related quality of life (measured by the Head and Neck Cancer Inventory [HNCI], MD Anderson Dysphagia Inventory [MDADI], and the functional assessment after cancer therapy-nasopharyngeal [FACT-NP]), functional swallowing ability (measured by the functional dysphagia scale [FDS]), and aspiration (measured by the Penetration-Aspiration-Scale [PAS]).
Ku (2023) conducted an RCT to compare the effects of transcutaneous neuromuscular electrical stimulation (TNMES) and exercise-based swallowing training (EBST) when administered early after radiotherapy for nasopharyngeal carcinoma (NPC). Eligible patients were adults (>18y) of Chinese ethnicity with a histological diagnosis of NPC who had completed primary radiotherapy or chemoradiotherapy ≤3 months prior and were confirmed to be in remission by negative biopsy. Patients with a history of other head and neck cancers treated with radiotherapy/chemotherapy/surgery, synchronous malignancies, residual or recurrent NPC, other causes of dysphagia, preexisting dysphagia before radiotherapy, contraindications to electrical stimulation, neurological disorders, poor cognitive function, inability to attend training or follow-up were excluded. A total of 111 eligible patients were randomized to receive either TNMES (n = 50) or EBST (n = 57). Both interventions consisted of 12 supervised 40-minute sessions over four weeks, without home-based exercises during the study period. Swallowing function was assessed at baseline, immediately after treatment, and at 6 and 12 months. Relevant outcomes for the purpose of this guideline included PAS, FOIS and QoL (measured by FACT-NP).
Patients with Parkinson’s Disease
Cheng (2023) conducted a SR and MA to evaluate the effectiveness of dysphagia interventions in patients with Parkinson’s Disease. Comprehensive searches were performed in PubMed, EMBASE (Ovid), CINAHL, Web of Science, and Cochrane Library from database inception to April 2022. Reference lists of relevant papers were also screened. Eligible studies were RCTs with parallel or crossover designs, involving adults with Parkinson’s Disease and clinically confirmed dysphagia, comparing any form of dysphagia treatment (including behavioral therapy, stimulation treatment, or pharmacological therapy) with sham, no treatment or conventional dysphagia therapy. Nine RCTs involving 286 patients with Parkinson’s Disease met the inclusion criteria, of which one study covered NMES and was relevant for the purpose of this guideline. Relevant outcomes included PAS.
Table 2. Characteristics of included studies
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Post-stroke dysphagia patients |
||||||
|
Relevant studies in systematic review of Wang (2023)
|
||||||
|
Additional relevant studies on top of Wang (2023) in NMA of Banda (2023)
|
||||||
|
Head and neck cancer patients |
||||||
|
Relevant studies in systematic review of Paim (2023)
|
||||||
|
Additional individual studies |
||||||
|
Ku, 2023 |
N at baseline Intervention: 31 Control: 34
Age (mean, SD) Intervention: 53.77y (12.25) Control: 49.75y (11.32)
Sex (m/f) Intervention: 18/13 Control: 25/9
|
Intervention VitalStim® electrical stimulation therapy, twelve 40-min training sessions over a 4-week period
Control Shaker Exercise, Masako maneuver, effortful swallows and Mendelsohn maneuver, twelve 40-min training sessions over a 4-week period |
Up to 12 months |
PAS FACT-NP (QoL) |
This study was supported by research funds from the Research Grants Council, Hong Kong Special Administrative Region, China (RGC reference number: 475210).
The authors declare that they have no competing interests or financial relationships to disclose |
Some concerns (all outcomes) |
|
Parkinson Disease patients |
||||||
|
Relevant studies in systematic review of Cheng (2023)
|
||||||
*For further details, see risk of bias table in the appendix
Results
Stroke patients
Comparison: NMES+TDT vs. TDT only
Functional oral intake of food as experienced by the patient (crucial)
Thirteen studies reported the outcome measure functional oral intake of food as experienced by the patient.
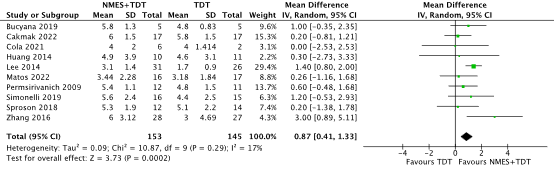
Five RCTs included in the SR of Wang (2023) reported the outcome using the Functional Oral Intake Scale (FOIS) (scale 1-7, higher is better) (Huang, 2014; Lee, 2014; Simonelli, 2019; Sproson, 2018; Zhang, 2016). Five RCTs included in the NMA of Banda (2023) were added (Bucyana, 2019; Cakmak, 2022; Cola, 2021; Matos, 2022; Permsirivanich, 2009). In total, 153 patients received NMES on top of TDT, and 145 patients received TDT only (Figure 1). The MD was 0.87 points higher (95% CI 0.41 higher to 1.33 higher), in favor of the NMES+TDT group and clinically relevant.
Figure 1. Functional oral intake (measured with the functional oral intake scale, FOIS) in stroke patients receiving NMES+TDT versus TDT
Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation
Two RCTs included in the NMA of Banda (2023) reported the outcome using the Mann Assessment of Swallowing Ability (MASA) up to four weeks posttreatment (scale 38-200, higher is better) (Carnaby, 2020; Umay, 2017). Carnaby (2020) reported a mean of 172.7 (SD 16.7) points in the NMES+TDT group (n=17) vs. 171.7 (SD 17.3) points in the TDT only group (n=16). This corresponded to a calculated MD of 1.00 point higher (95% CI, 10.61 lower to 12.61 higher) in favor of the NMES+TDT group, but not clinically relevant. Umay (2017) reported a mean of 181.27 (SD 20.66) points in the NMES+TDT group (n=58) vs. 157.81 (SD 33.58) points in the TDT only group (n=40). This corresponded to a calculated MD of 23.46 points higher (95% CI, 11.77 higher to 35.15 higher) in favor of the NMES+TDT group and clinically relevant.
One RCT included in the NMA of Banda (2023) reported the outcome using the Dysphagia Outcome and Severity Scale (DOSS) up to two weeks (scale 1-7, higher is better) (Meng, 2017; Zhang, 2021). Meng (2017) reported a mean of 5.2 (SD 1.4) points in the NMES+TDT group (n=10) vs. 4.9 (SD 1.1) points in the TDT only group (n=10). This corresponded to a calculated MD of 0.30 points higher (95% CI, 0.80 lower to 1.40 higher) in favor of the NMES+TDT group, but not clinically relevant.
Swallowing-related quality of life (crucial)
Eighteen studies reported the outcome measure swallowing-related quality of life.
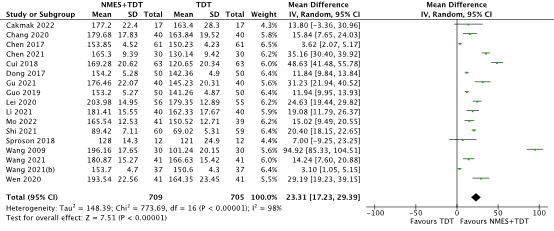
Sixteen RCTs included in the SR and MA of Wang (2023) reported the outcome using the Swallowing Quality of Life Questionnaire (SWAL-QOL) (scale 0-220, higher is better) (Chang, 2020; Chen, 2017; Chen, 2021; Cui, 2018; Dong, 2017; Gu, 2021; Guo, 2019; Lei, 2020; Li, 2021; Mo, 2022; Shi, 2021; Sproson, 2018; Wang, 2009; Wang, 2021; Wang, 2021(b), Wen, 2020). One RCT included in the NMA of Banda (2023) was added (Cakmak, 2022). In total 709 patients received NMES on top of TDT, and 705 patients received TDT only (Figure 2). The MD was 23.31 points higher (95% CI 17.23 higher to 29.39 higher), in favor of the NMES+TDT group and clinically relevant.
Figure 2. Swallowing-related quality of life (measured with the swallowing quality of life questionnaire, SWAL-QOL) in stroke patients receiving NMES+TDT versus TDT Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation
Cakmak (2022) also reported the outcome dysphagia symptom severity using the Eating Assessment Tool-10 (EAT-10) up to three months (scale 0-40, lower is better). The EAT-10 is used as a surrogate outcome of swallowing-related quality of life in the current guideline. Cakmak (2022) reported a mean of 7.7 (SD 7.9) points in the NMES+TDT group (n=17) vs. 11.5 (SD 8.8) points in the TDT only group (n=17). This corresponded to a calculated MD of 3.80 points lower (95% CI, 9.42 lower to 1.82 higher) in favor of the NMES+TDT group, but not clinically relevant.
Functional swallowing ability (important)
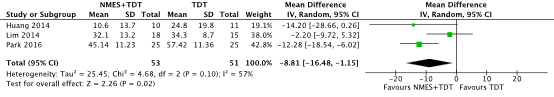
Three RCTs included in the SR and MA of Wang (2023) reported the outcome using the Functional Dysphagia Scale (FDS) (scale 0-100, lower is better) (Huang, 2014; Lim, 2014; Park, 2016). In total, 53 patients received NMES on top of TDT, and 53 patients received TDT only (Figure 3). The MD was 8.81 points lower (95% CI 16.48 lower to 1.15 lower), in favor of the NMES+TDT group, but not clinically relevant.
Figure 3. Functional Swallowing Ability (measured with the Functional Dysphagia Scale, FDS) in stroke patients receiving NMES+TDT versus TDT
Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation
Number or percentage of patients who return to a normal diet (important)
The outcome measure number or percentage of patients who return to a normal diet was not reported.
Aspiration (important)
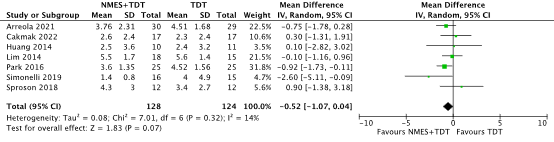
Six RCTs included in the SR and MA of Wang (2023) reported the outcome aspiration with the use of the Penetration-Aspiration Scale (PAS) (scale 1-8, lower is better) (Arreola, 2021; Huang, 2014; Lim, 2014; Park, 2016; Simonelli, 2019; Sproson, 2018). One RCT included in the NMA of Banda (2023) was added (Cakmak, 2022). In total, 128 patients received NMES on top of TDT, and 124 patients received TDT only (Figure 4). The MD was 0.52 points lower (95% CI 1.07 lower to 0.04 higher), in favor of the NMES+TDT group, but not clinically relevant.
Figure 4. Aspiration (measured with the Penetration-Aspiration Scale) in stroke patients receiving NMES+TDT versus TDT
Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation
HNC patients
Comparison: NMES+TT or NMES only vs sham NMES+exercises or exercises only
Functional oral intake of food as experienced by the patient (crucial)
Two studies reported the outcome measure functional oral intake of food as experienced by the patient.
One RCT reported the outcome using the FOIS (scale 1-7, higher is better) four weeks posttreatment (Ku, 2023). Ku (2023) reported a mean of 6.52 points in the NMES group (n=31) vs. 6.38 points in the EBST group (n=34). This corresponded to a MD of 0.14 points higher in the TNMES group, which is not clinically relevant. SDs were not reported, and a GRADE assessment could not be performed.
One RCT included in the SR and MA of Paim (2023) reported the outcome using the American speech-language-hearing association national outcome measurement system swallowing level scale (ASHA NOMS) (scale 0-7, higher is better) posttreatment (Ryu, 2009). Ryu (2009) reported a mean ASHA NOMS score of 3.86 (SD 1.80) in the NMES+TDT group (n=14) vs. 3.67 (SD 2.10) in the sham NMES+TDT only group (n=12). This corresponded to a calculated MD of 0.19 points higher (95% CI, 1.33 lower to 1.71 higher) in favor of the NMES+TDT group, but not clinically relevant.
Swallowing-related quality of life (crucial)
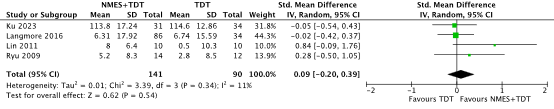
Three studies included in the SR and MA of Paim (2023) reported the outcome swallowing-related quality of life (Lin, 2011; Langmore, 2016; Ryu, 2009). One study used the Head and Neck Cancer Inventory (HNCI, scale 0-100, higher is better) (Langmore, 2016) and two studies used the MD Anderson Dysphagia Inventory (MDADI, scale 20-100, higher is better) (Lin, 2011; Ryu, 2009). One additional study published after the search date of the Paim (2023) was added (Ku, 2023). Ku (2023) reported the outcome using the functional assessment after cancer therapy-nasopharyngeal (FACT-NP, scale 0-172, higher is better). In total, 141 patients received TNMES alone or on top of TDT and 90 patients received sham NMES on top of TDT or TDT only (Figure 5). The calculated SMD was 0.09 points higher (95% CI, 0.20 lower to 0.39 higher), which is not clinically relevant.
Figure 5. Quality of life (measured with the HNCI, MDADI and FACT-NP) in HNC patients receiving TNMES alone or on top of TDT versus sham NMES on top of TDT or TDT only
Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation; HNC, head and neck cancer
Functional swallowing ability (important)
One RCT included in the SR and MA of Paim (2023) reported the outcome functional swallowing ability using the FDS (scale 0-100, lower is better) posttreatment (Ryu, 2009). Ryu (2009) reported a mean FDS score of 22.4 (SD 13.4) in the NMES+TDT group (n=14) vs. 35.3 (SD 17.7) in the sham NMES+TDT only group (n=12). This corresponded to a MD of 12.90 points lower (95% CI, 25.13 lower to 0.67 lower), in favor of the NMES+TDT group, and clinically relevant.
Number or percentage of patients who return to a normal diet (important)
The outcome measure number or percentage of patients who return to a normal diet was not reported.
Aspiration (important)
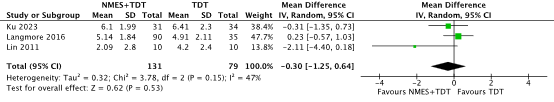
Two studies included in the SR and MA of Paim (2023) reported the outcome aspiration using the PAS (scale 1-8, lower is better) (Lin, 2011; Langmore, 2016). One additional study published after the search date of the Paim (2023) also reporting on the PAS was added (Ku, 2023). In total, 131 patients received NMES on top of TDT or TNMES only and 79 patients received sham NMES on top of TDT or EBST only (Figure 6). The calculated MD was 0.30 points lower (95% CI, 1.25 lower to 0.64 higher), in favor of the NMES+TDT or TNMES only group, but not clinically relevant.
Figure 6. Aspiration (measured with the Penetration-Aspiration Scale) in HNC patients receiving NMES on top of TDT or TNMES only versus sham NMES on top of TDT or EBST only
Abbreviations: NMES, neuromuscular electrical stimulation; TDT, traditional dysphagia therapy; SD, standard deviation; HNC, head and neck cancer
Parkinson's disease patients
Comparison: NMES + exercises vs. sham + exercises
Functional oral intake of food as experienced by the patient (crucial)
The outcome measure functional oral intake of food as experienced by the patient was not reported.
Swallowing-related quality of life (crucial)
The outcome measure swallowing-related quality of life was not reported.
Functional swallowing ability (important)
One RCT included in the SR and MA of Cheng (2023) reported the outcome functional swallowing ability using the Videofluoroscopic Dysphagia Scale (VDS) (scale 0-100, lower is better) four weeks posttreatment (Park, 2018). Park (2018) reported a mean VDS score of 54.11 (SD 5.62) in the NMES+exercises group (n=9) vs. 53.28 (SD 10.21) in the sham NMES+exercises group (n=9). This corresponded to a MD of 0.83 points higher (95% CI, 6.78 lower to 8.44 higher), in favor of the sham NMES+exercises group, but not clinically relevant.
Number or percentage of patients who return to a normal diet (important)
The outcome measure number or percentage of patients who return to a normal diet was not reported.
Aspiration (important)
One RCT included in the SR and MA of Cheng (2023) reported the outcome aspiration using the PAS (scale 1-8, lower is better) four weeks posttreatment (Park, 2018). Park (2018) reported a mean PAS score of 2.33 (SD 0.71) in the NMES+exercises group (n=9) vs. 3.67 (SD 1.32) in the sham NMES+exercises group (n=9). This corresponded to a MD of 1.34 points lower (95% CI, 2.32 lower to 0.36 lower), in favor of the NMES+exercises group, and clinically relevant.
A systematic review of the literature was performed to answer the following question(s):
What is the effectiveness of neuromuscular electrical stimulation and conventional swallowing therapy as treatment for patients with dysphagia compared to placebo electrical stimulation or no electrical stimulation and conventional swallowing therapy?
Table 1. PICO
| Patients | Patients with oropharyngeal dysphagia |
| Intervention | Neuromuscular electrical stimulation and conventional swallowing therapy |
| Control | Placebo electrical stimulation or no electrical stimulation and conventional swallowing therapy |
| Outcomes | The functional oral intake of food as experienced by the patient (measured with FOIS or FOAMS), swallowing-related quality of life (measured with the Swal-QoL, Visual Analogue Scale (VAS), MD Anderson Dysphagia Inventory (MDADI), and other questionnaires with a dysphagia domain), functional swallowing ability; the number or percentage of patients who return to a normal diet, aspiration |
| Other selection criteria | Study design: systematic reviews and randomized controlled trials (RCTs) |
Relevant outcome measures
The guideline panel considered the functional oral intake of food as experienced by the patient and swallowing-related quality of life as a critical outcome measure for decision making; and functional swallowing ability, the number or percentage of patients who return to a normal diet and aspiration as an important outcome measure for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel used the GRADE standard limits of 25% (a relative risk (RR) of <0.80 and >1.25) for dichotomous outcomes and 10% for continuous outcomes as a minimal clinically (patient) important difference. For dichotomous outcomes with very few events, a risk difference of 25% was used as a minimal clinically (patient) important difference.
Search and select (Methods)
A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched from 2015 to the 4th of April 2025 for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords. The overall search strategy was derived from two primary search concepts: (1) dysphagia; (2) electric stimulation. Duplicates were removed using EndNote software. After deduplication a total of 1481 records were imported for title/abstract screening. Studies were selected based on the criteria described in Table 1. Titles and abstracts were screened using the ASReview software version 1.6.2. The settings TF-IDF and Naïve bayes were used. One study was used as prior knowledge for inclusion (Terré, 2015; Gandhi, 2022). One study was used as prior knowledge for exclusions (Chen, 2022; Baroni, 2024).
The first 10% of references were screened by the working group and the guideline methodologist. The remaining articles were subsequently screened by the guideline methodologist, using the following stopping rule: stop after 200 subsequent exclusions.
Initially, 60 studies were selected based on title and abstract screening. After reading the full text, 41 studies were excluded for post-stroke patients, four for head and neck cancer (HNC) patients, four for neurodegenerative patients, and seven for other patient groups (see the exclusion table under the tab ‘Evidence tabellen’). In total, five studies were included.
The included studies are described separately per disease category in the results section. These categories comprise post-stroke patients, patients with Parkinson’s Disease, and patients with head and neck cancer (HNC).
- Baijens LW, Speyer R, Passos VL, Pilz W, van der Kruis J, Haarmans S, Desjardins-Rombouts C. Surface electrical stimulation in dysphagic Parkinson patients: a randomized clinical trial. Laryngoscope. 2013 Nov;123(11):E38-44. doi: 10.1002/lary.24119. Epub 2013 Apr 17. PMID: 23595549.
- Banda KJ, Wu KC, Jen HJ, Chu H, Pien LC, Chen R, Lee TY, Lin SK, Hung SH, Chou KR. Comparative Effectiveness of Combined and Single Neurostimulation and Traditional Dysphagia Therapies for Post-Stroke Dysphagia: A Network Meta-Analysis. Neurorehabil Neural Repair. 2023 Apr;37(4):194-204. doi: 10.1177/15459683231166940. Epub 2023 Apr 20. PMID: 37078600.
- Cheng I, Sasegbon A, Hamdy S. Dysphagia treatments in Parkinson's disease: A systematic review and meta-analysis. Neurogastroenterol Motil. 2023 Aug;35(8):e14517. doi: 10.1111/nmo.14517. Epub 2022 Dec 22. Erratum in: Neurogastroenterol Motil. 2025 Jun 5:e70094. doi: 10.1111/nmo.70094. PMID: 36546568.
- Heijnen BJ, Speyer R, Baijens LW, Bogaardt HC. Neuromuscular electrical stimulation versus traditional therapy in patients with Parkinson's disease and oropharyngeal dysphagia: effects on quality of life. Dysphagia. 2012 Sep;27(3):336-45. doi: 10.1007/s00455-011-9371-z. Epub 2011 Nov 13. PMID: 22081122; PMCID: PMC3417093.
- Humbert IA, Michou E, MacRae PR, et al. Electrical Stimulation and Swallowing: How Much Do We Know Semin Speech Lang. 2012; 33(3):203-216.
- Ku PKM, Vlantis AC, Wong RWM, Hui TSC, Law T, Ng LKY, Wong EWY, Chang WT, Johnson DR, Mok FST, Wong KH, Abdullah V, van Hasselt A, Lee KYS, Tong MCF. Quality of life and swallowing outcomes after early proactive swallowing rehabilitation by either transcutaneous neuromuscular electrical stimulation or exercise-based swallowing training in patients with nasopharyngeal carcinoma after radiotherapy. Laryngoscope Investig Otolaryngol. 2023 Oct 14;8(6):1532-1546. doi: 10.1002/lio2.1162. PMID: 38130249; PMCID: PMC10731556.
- Paim ÉD, Sugueno LA, Martins VB, Zanella VG, Macagnan FE. Electrical Stimulation for Treatment of Dysphagia Post Head Neck Cancer: A Systematic Review and Meta-Analysis. Int Arch Otorhinolaryngol. 2023 Sep 14;28(2):e339-e349. doi: 10.1055/s-0043-1761175. PMID: 38618607; PMCID: PMC11008950.
- Wang Y, Xu L, Wang L, Jiang M, Zhao L. Effects of transcutaneous neuromuscular electrical stimulation on post-stroke dysphagia: a systematic review and meta-analysis. Front Neurol. 2023 May 9;14:1163045. doi: 10.3389/fneur.2023.1163045. PMID: 37228409; PMCID: PMC10203701.
- Zhang Q, Wu S. Effects of Synchronized Neuromuscular Electrical Stimulation (NMES) on the Submental Muscles During Ingestion of a Specified Volume of Soft Food in Patients with Mild-to-Moderate Dysphagia Following Stroke. Med Sci Monit. 2021 Mar 29;27:e928988. doi: 10.12659/MSM.928988. PMID: 33780432; PMCID: PMC8018178.
- Zhang YW, Dou ZL, Zhao F, Xie CQ, Shi J, Yang C, Wan GF, Wen HM, Chen PR, Tang ZM. Neuromuscular electrical stimulation improves swallowing initiation in patients with post-stroke dysphagia. Front Neurosci. 2022 Nov 14;16:1011824. doi: 10.3389/fnins.2022.1011824. PMID: 36452336; PMCID: PMC9704362.
Risk of Bias tables
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
|
Ku, 2023 |
Definitely yes;
Reason: computer generated random numbers |
No information;
|
Probably no;
Reason: outcome assessors were blinded, but no information regarding blinding of patients, healthcare providers and data-analysts |
Probably yes;
Reason: large loss to follow-up in both groups, but drop-out probably not related to the intervention. |
Definitely yes
Reason: All relevant outcomes were reported; |
Definitely yes;
Reason: No other problems noted |
Some concerns (lack of blinding) |
|
|
The risk of bias for the other articles can be found in the systematic reviews of Wang (2023), supplementary material of Banda (2023), Paim (2023), and Cheng (2023) |
||||||||
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Stroke patients |
|
|
Alamer A, Melese H, Nigussie F. Effectiveness of Neuromuscular Electrical Stimulation on Post-Stroke Dysphagia: A Systematic Review of Randomized Controlled Trials. Clin Interv Aging. 2020 Sep 3;15:1521-1531. doi: 10.2147/CIA.S262596. PMID: 32943855; PMCID: PMC7481288. |
More recent SR available |
|
Assoratgoon I, Shiraishi N, Tagaino R, Ogawa T, Sasaki K. Sensory neuromuscular electrical stimulation for dysphagia rehabilitation: A literature review. J Oral Rehabil. 2023 Feb;50(2):157-164. doi: 10.1111/joor.13391. Epub 2022 Nov 28. PMID: 36357332; PMCID: PMC10286766. |
Wrong I (most suggested application parameters of NMES) and no control group |
|
Balcerak P, Corbiere S, Zubal R, Kägi G. Post-stroke Dysphagia: Prognosis and Treatment-A Systematic Review of RCT on Interventional Treatments for Dysphagia Following Subacute Stroke. Front Neurol. 2022 Apr 25;13:823189. doi: 10.3389/fneur.2022.823189. PMID: 35547370; PMCID: PMC9082350. |
More recent SR and NMA available |
|
Bath PM, Lee HS, Everton LF. Swallowing therapy for dysphagia in acute and subacute stroke. Cochrane Database Syst Rev. 2018 Oct 30;10(10):CD000323. doi: 10.1002/14651858.CD000323.pub3. PMID: 30376602; PMCID: PMC6516809. |
More recent SR and NMA available |
|
Carnaby GD, LaGorio L, Silliman S, Crary M. Exercise-based swallowing intervention (McNeill Dysphagia Therapy) with adjunctive NMES to treat dysphagia post-stroke: A double-blind placebo-controlled trial. J Oral Rehabil. 2020 Apr;47(4):501-510. doi: 10.1111/joor.12928. Epub 2020 Jan 19. PMID: 31880338; PMCID: PMC7067660. |
Included in NMA of Banda (2023) |
|
Chen YW, Chang KH, Chen HC, Liang WM, Wang YH, Lin YN. The effects of surface neuromuscular electrical stimulation on post-stroke dysphagia: a systemic review and meta-analysis. Clin Rehabil. 2016 Jan;30(1):24-35. doi: 10.1177/0269215515571681. Epub 2015 Feb 19. PMID: 25697453. |
More recent SR available |
|
Chiang CF, Lin MT, Hsiao MY, Yeh YC, Liang YC, Wang TG. Comparative Efficacy of Noninvasive Neurostimulation Therapies for Acute and Subacute Poststroke Dysphagia: A Systematic Review and Network Meta-analysis. Arch Phys Med Rehabil. 2019 Apr;100(4):739-750.e4. doi: 10.1016/j.apmr.2018.09.117. Epub 2018 Oct 21. PMID: 30352222. |
More recent SR and NMA available |
|
Diéguez-Pérez I, Leirós-Rodríguez R. Effectiveness of Different Application Parameters of Neuromuscular Electrical Stimulation for the Treatment of Dysphagia after a Stroke: A Systematic Review. J Clin Med. 2020 Aug 12;9(8):2618. doi: 10.3390/jcm9082618. PMID: 32806675; PMCID: PMC7463982. |
More recent SR available |
|
Doan TN, Ho WC, Wang LH, Chang FC, Tran TTQ, Chou LW. Therapeutic Effect and Optimal Electrode Placement of Transcutaneous Neuromuscular Electrical Stimulation in Patients with Post-Stroke Dysphagia: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Life (Basel). 2022 Jun 10;12(6):875. doi: 10.3390/life12060875. PMID: 35743906; PMCID: PMC9225155. |
More recent SR and NMA available |
|
Guillén-Solà A, Messagi Sartor M, Bofill Soler N, Duarte E, Barrera MC, Marco E. Respiratory muscle strength training and neuromuscular electrical stimulation in subacute dysphagic stroke patients: a randomized controlled trial. Clin Rehabil. 2017 Jun;31(6):761-771. doi: 10.1177/0269215516652446. Epub 2016 Jun 7. PMID: 27271373. |
Wrong C (sham IEMT) |
|
Güleç A, Albayrak I, Erdur Ö, Öztürk K, Levendoglu F. Effect of swallowing rehabilitation using traditional therapy, kinesiology taping and neuromuscular electrical stimulation on dysphagia in post-stroke patients: A randomized clinical trial. Clin Neurol Neurosurg. 2021 Dec;211:107020. doi: 10.1016/j.clineuro.2021.107020. Epub 2021 Nov 6. PMID: 34781221. |
Wrong C (kinesiotaping) |
|
Jamil A, Imtiaz M, Muhammad A, Rahat A, Obaid HB, Jarral J, Imran R. Evidence based therapeutic and assessment techniques to rehabilitate post stroke dysphagia patients-A systematic review. Eur Arch Otorhinolaryngol. 2025 Jan;282(1):1-10. doi: 10.1007/s00405-024-08874-9. Epub 2024 Aug 6. PMID: 39105791. |
Lack of data relevant for the guideline |
|
Jing, Q, Yang X, Reng Q. Effect of Neuromuscular Electrical Stimulation in Patients with Post-Stroke Dysphagia. Med Sci Tech 2016; 57:1-5. doi: 10.12659/MST.895042 |
Poor methodological quality |
|
Konecny P, Elfmark M. Electrical stimulation of hyoid muscles in post-stroke dysphagia. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub. 2018 Mar;162(1):40-42. doi: 10.5507/bp.2017.043. Epub 2017 Nov 2. PMID: 29097820. |
Included in NMA of Banda (2023) |
|
Koneěný P, Elfmark M, Rosolová M, Bastlová P, Lerchová I, Můěková A. Electrical stimulation of the suprahyoid muscles in post stroke patients with dysphagia. Ceska a Slovenska Neurologie a Neurochirurgie. 2017. https://doi.org/10.14735/amcsnn2017578 |
Wrong I (only NMES, standard care not included) |
|
Kumaresan A, Manoj Abraham M, Arunachalam Ramachandran. Effects of Neuro Muscular Electrical Stimulation on Swallowing Function and Quality of Life in Subjects with Post Stroke Dysphagia. Research Journal of Pharmacy and Technology. 2018 May;11;12. DOI: 10.5958/0974-360X.2018.01011.9 |
No control group (quasi-experimental design) |
|
Kushner DS, Johnson-Greene D, Cordero MK, Thomashaw SA, Rodriguez J. Swallowing Outcomes and Discharge Destinations in Acute Stroke Tube-Feeding Dependent Dysphagia Patients Treated With Neuromuscular Electrical Stimulation During Inpatient Rehabilitation. Am J Phys Med Rehabil. 2020 Jun;99(6):487-494. doi: 10.1097/PHM.0000000000001353. PMID: 31764228. |
Wrong study design (retrospective case-control study)
|
|
Kwon DI, Villegas BC, Ouyoung LM, Sinha UK. Improved Swallow Outcomes with Early Intervention using Combined Swallow Therapy in Advanced Oropharyngeal Carcinoma. J Laryngol Otol. 2021 Oct 27:1-22. doi: 10.1017/S0022215121003212. Epub ahead of print. PMID: 34702385. |
Wrong study design (cohort study) and wrong comparison |
|
Lee SY, Park D, Jang J, Jang EG, Lee JC, Park Y, Cho S, Kim WS, Park J, Kim BR, Seo KH, Park S, Ryu JS. Compensatory Effects of Sequential 4-Channel Neuromuscular Electrical Stimulation for the Treatment of Acute, Subacute, and Chronic Dysphagia in a Prospective, Double-Blinded Randomized Clinical Trial. Neurorehabil Neural Repair. 2021 Sep;35(9):801-811. doi: 10.1177/15459683211029891. Epub 2021 Jul 4. PMID: 34218702. |
Wrong comparison (no traditional swallowing therapy in intervention and control group) |
|
Liang Y, Lin J, Wang H, Li S, Chen F, Chen L, Li L. Evaluating the Efficacy of VitalStim Electrical Stimulation Combined with Swallowing Function Training for Treating Dysphagia following an Acute Stroke. Clinics (Sao Paulo). 2021 Nov 8;76:e3069. doi: 10.6061/clinics/2021/e3069. PMID: 34755758; PMCID: PMC8552953. |
Wrong O (method to measure QoL does not include a dysphagia domain + other outcomes don’t match the PICO) |
|
Li L, Li Y, Huang R, Yin J, Shen Y, Shi J. The value of adding transcutaneous neuromuscular electrical stimulation (VitalStim) to traditional therapy for post-stroke dysphagia: a randomized controlled trial. Eur J Phys Rehabil Med. 2015 Feb;51(1):71-8. Epub 2014 Jul 23. Retraction in: Eur J Phys Rehabil Med. 2015 Apr;51(2):237. PMID: 25052012. |
Article is retracted, for reasons of redundancy |
|
Li, Lejun, Li, Yumei; Wu, Xiaohong; Wang, Guohua; Yi, Xiaojing; Zhao, Yichun; Guo, Mingjie; Pan, Muzhi; Tang, Chunlin. The Value of Adding Transcutaneous Neuromuscular Electrical Stimulation (VitalStim) to Traditional Therapy for Poststroke Dysphagia: A Randomized Controlled Trial. Topics in Geriatric Rehabilitation 34(3):p 200-206, July/September 2018. | DOI: 10.1097/TGR.0000000000000195 |
Wrong O (PTT and OTT) |
|
Matos KC, de Oliveira VF, de Oliveira PLC, Carvalho FA, de Mesquita MRM, da Silva Queiroz CG, Marques LM, Lima DLN, Carvalho FMM, Braga-Neto P. Combined conventional speech therapy and functional electrical stimulation in acute stroke patients with dyphagia: a randomized controlled trial. BMC Neurol. 2022 Jun 22;22(1):231. doi: 10.1186/s12883-022-02753-8. PMID: 35733098; PMCID: PMC9215026. |
Included in NMA of Banda (2023) |
|
Meng P, Zhang S, Wang Q, Wang P, Han C, Gao J, Yue S. The effect of surface neuromuscular electrical stimulation on patients with post-stroke dysphagia. J Back Musculoskelet Rehabil. 2018;31(2):363-370. doi: 10.3233/BMR-170788. PMID: 29278871. |
Included in NMA of Banda (2023) |
|
Miller S, Diers D, Jungheim M, Schnittger C, Stürenburg HJ, Ptok M. Studying effects of neuromuscular electrostimulation therapy in patients with dysphagia: which pitfalls may occur? A translational phase I study. Ger Med Sci. 2021 Jun 1;19:Doc07. doi: 10.3205/000294. PMID: 34194290; PMCID: PMC8204381. |
Wrong P (healthy subjects) |
|
Park D, Suh JH, Kim H, Ryu JS. The Effect of Four-Channel Neuromuscular Electrical Stimulation on Swallowing Kinematics and Pressures: A Pilot Study. Am J Phys Med Rehabil. 2019 Dec;98(12):1051-1059. doi: 10.1097/PHM.0000000000001241. PMID: 31180928. |
Wrong study design (case-control study) |
|
Park JS, Oh DH, Hwang NK, Lee JH. Effects of neuromuscular electrical stimulation combined with effortful swallowing on post-stroke oropharyngeal dysphagia: a randomised controlled trial. J Oral Rehabil. 2016 Jun;43(6):426-34. doi: 10.1111/joor.12390. Epub 2016 Mar 9. PMID: 26969528. |
Included in SR of Wang (2023) |
|
Simonelli M, Ruoppolo G, Iosa M, Morone G, Fusco A, Grasso MG, Gallo A, Paolucci S. A stimulus for eating. The use of neuromuscular transcutaneous electrical stimulation in patients affected by severe dysphagia after subacute stroke: A pilot randomized controlled trial. NeuroRehabilitation. 2019;44(1):103-110. doi: 10.3233/NRE-182526. PMID: 30714980. |
Included in SR of Wang (2023) |
|
Tan Z, Wei X, Tan C, Wang H, Tian S. Effect of neuromuscular electrical stimulation combined with swallowing rehabilitation training on the treatment efficacy and life quality of stroke patients with dysphagia. Am J Transl Res. 2022 Feb 15;14(2):1258-1267. PMID: 35273727; PMCID: PMC8902560. |
Wrong study design (retrospective cohort study) |
|
Tarihci Cakmak E, Sen EI, Doruk C, Sen C, Sezikli S, Yaliman A. The Effects of Neuromuscular Electrical Stimulation on Swallowing Functions in Post-stroke Dysphagia: A Randomized Controlled Trial. Dysphagia. 2023 Jun;38(3):874-885. doi: 10.1007/s00455-022-10512-7. Epub 2022 Aug 20. PMID: 35986170. |
Included in NMA of Banda (2023) |
|
Terré R, Mearin F. A randomized controlled study of neuromuscular electrical stimulation in oropharyngeal dysphagia secondary to acquired brain injury. Eur J Neurol. 2015 Apr;22(4):687-e44. doi: 10.1111/ene.12631. Epub 2015 Jan 9. PMID: 25573027. |
Wrong P (mixture of populations, stroke and traumatic brain injury) |
|
Umay EK, Yaylaci A, Saylam G, Gundogdu I, Gurcay E, Akcapinar D, Kirac Z. The effect of sensory level electrical stimulation of the masseter muscle in early stroke patients with dysphagia: A randomized controlled study. Neurol India. 2017 Jul-Aug;65(4):734-742. doi: 10.4103/neuroindia.NI_377_16. PMID: 28681742. |
Included in NMA of Banda (2023) |
|
Wang T, Dong L, Cong X, Luo H, Li W, Meng P, Wang Q. Comparative efficacy of non-invasive neurostimulation therapies for poststroke dysphagia: A systematic review and meta-analysis. Neurophysiol Clin. 2021 Dec;51(6):493-506. doi: 10.1016/j.neucli.2021.02.006. Epub 2021 Sep 15. PMID: 34535361. |
More recent SR and NMA available |
|
Wang Z, Xiao Z, Shen Q, Zhao N, Zhang W. Neuromuscular Electrical Stimulation for Post-Stroke Dysphagia Treatment: A Systemic Evaluation and Meta-Analysis of Randomized Controlled Trials. Dysphagia. 2024 Jun;39(3):424-432. doi: 10.1007/s00455-023-10626-6. Epub 2023 Nov 1. PMID: 37914887. |
The search date of the SR by Wang (2023) is more recent |
|
Yuan H, Yu LJ, Xie S, Zha Y, Deng BQ, Wu T. Effectiveness of neuromuscular electrical stimulation combined with swallowing training for dysphagia after acute ischemic stroke. Academic Journal of Second Military Medical University. 2018. https://doi.org/10.16781/j.0258-879x.2018.09.1052 |
Wrong O |
|
Zeng Y, Yip J, Cui H, Guan L, Zhu H, Zhang W, Du H, Geng X. Efficacy of neuromuscular electrical stimulation in improving the negative psychological state in patients with cerebral infarction and dysphagia. Neurol Res. 2018 Jun;40(6):473-479. doi: 10.1080/01616412.2018.1451015. Epub 2018 May 4. PMID: 29726748. |
Wrong O (negative effect disorders) |
|
Zhang M, Tao T, Zhang ZB, Zhu X, Fan WG, Pu LJ, Chu L, Yue SW. Effectiveness of Neuromuscular Electrical Stimulation on Patients With Dysphagia With Medullary Infarction. Arch Phys Med Rehabil. 2016 Mar;97(3):355-62. doi: 10.1016/j.apmr.2015.10.104. Epub 2015 Nov 19. PMID: 26606872. |
Included in NMA of Banda (2023) |
|
Zhang Q, Wu S. Effects of Synchronized Neuromuscular Electrical Stimulation (NMES) on the Submental Muscles During Ingestion of a Specified Volume of Soft Food in Patients with Mild-to-Moderate Dysphagia Following Stroke. Med Sci Monit. 2021 Mar 29;27:e928988. doi: 10.12659/MSM.928988. PMID: 33780432; PMCID: PMC8018178. |
Wrong comparison (conventional swallowing training + NMES vs. conventional swallowing training + ET soft food vs. conventional swallowing training + IST tongue hold swallow + NMES) |
|
Zhang YW, Dou ZL, Zhao F, Xie CQ, Shi J, Yang C, Wan GF, Wen HM, Chen PR, Tang ZM. Neuromuscular electrical stimulation improves swallowing initiation in patients with post-stroke dysphagia. Front Neurosci. 2022 Nov 14;16:1011824. doi: 10.3389/fnins.2022.1011824. PMID: 36452336; PMCID: PMC9704362. |
Wrong study design (crossover trial) |
|
Zhu ZZ, Cui LL, Yin MM, Yu Y, Wang HT. Effects of swallowing training combined with low -frequency electrical stimulation on dysphagia after ischemic stroke. Chinese Journal of Contemporary Neurology and Neurosurgery. 2015. https://doi.org/10.3969/j.issn.1672-6731.2015.04.007 |
Article in Chinese |
|
Zhuang Y, Wang X, Yin X, Li X, Liu W. Exploration of treatment methods for patients with post-stroke dysphagia: a network meta-analysis. Biotechnol Genet Eng Rev. 2024 Apr;40(1):436-453. doi: 10.1080/02648725.2023.2184044. Epub 2023 Mar 26. PMID: 36966378. |
SR and NMA with more recent search date available |
|
Head and neck cancer patients |
|
|
Bhatt AD, Goodwin N, Cash E, Bhatt G, Silverman CL, Spanos WJ, Bumpous JM, Potts K, Redman R, Allison WA, Dunlap NE. Impact of transcutaneous neuromuscular electrical stimulation on dysphagia in patients with head and neck cancer treated with definitive chemoradiation. Head Neck. 2015 Jul;37(7):1051-6. doi: 10.1002/hed.23708. Epub 2015 Apr 6. PMID: 24710791. |
Wrong study design (retrospective review of a prospectively maintained database) |
|
Costa DR, Santos PSDS, Fischer Rubira CM, Berretin-Felix G. Immediate effect of neuromuscular electrical stimulation on swallowing function in individuals after oral and oropharyngeal cancer therapy. SAGE Open Med. 2020 Dec 14;8:2050312120974152. doi: 10.1177/2050312120974152. PMID: 33403111; PMCID: PMC7739140. |
Sample size too small (n=10) |
|
Kwon DI, Villegas BC, Ouyoung LM, Sinha UK. Improved Swallow Outcomes with Early Intervention using Combined Swallow Therapy in Advanced Oropharyngeal Carcinoma. J Laryngol Otol. 2021 Oct 27:1-22. doi: 10.1017/S0022215121003212. Epub ahead of print. PMID: 34702385. |
Wrong study design (cohort study) |
|
Langmore SE, McCulloch TM, Krisciunas GP, Lazarus CL, Van Daele DJ, Pauloski BR, Rybin D, Doros G. Efficacy of electrical stimulation and exercise for dysphagia in patients with head and neck cancer: A randomized clinical trial. Head Neck. 2016 Apr;38 Suppl 1(Suppl 1):E1221-31. doi: 10.1002/hed.24197. Epub 2015 Oct 15. PMID: 26469360; PMCID: PMC4833725. |
Included in SR of Paim (2023) |
|
Neurodegenerative patients |
|
|
Alali D, Ballard K, Bogaardt H. Treatment Effects for Dysphagia in Adults with Multiple Sclerosis: A Systematic Review. Dysphagia. 2016 Oct;31(5):610-8. doi: 10.1007/s00455-016-9738-2. Epub 2016 Aug 4. PMID: 27488370. |
No control group |
|
Gandhi P, Steele CM. Effectiveness of Interventions for Dysphagia in Parkinson Disease: A Systematic Review. Am J Speech Lang Pathol. 2022 Jan 18;31(1):463-485. doi: 10.1044/2021_AJSLP-21-00145. Epub 2021 Dec 10. PMID: 34890260; PMCID: PMC9159671. |
Wrong O and qualitative SR |
|
Kim JY, Kim H. Effects of behavioural swallowing therapy in patients with Parkinson's disease: A systematic review. Int J Speech Lang Pathol. 2023 Apr;25(2):269-280. doi: 10.1080/17549507.2022.2045356. Epub 2022 Mar 13. PMID: 35282718. |
SR and MA available with more recent search date |
|
Park JS, Oh DH, Hwang NK, Lee JH. Effects of neuromuscular electrical stimulation in patients with Parkinson's disease and dysphagia: A randomized, single-blind, placebo-controlled trial. NeuroRehabilitation. 2018;42(4):457-463. doi: 10.3233/NRE-172306. PMID: 29660951. |
Included in SR of Cheng (2023) |
|
Other populations |
|
|
Chen L, Liu C, Yuan M, Yin X, Niu S, Tang J, Chen H, Xiong B, Feng X. Interventions for Postextubation Dysphagia in Critically Ill Patients: A Systematic Review and Meta-analysis. Dysphagia. 2024 Dec;39(6):1013-1024. doi: 10.1007/s00455-024-10695-1. Epub 2024 Apr 1. PMID: 38558176. |
Only one study relevant, but this study has a wrong control group (acid ice stimulation) |
|
Frost J, Robinson HF, Hibberd J. A comparison of neuromuscular electrical stimulation and traditional therapy, versus traditional therapy in patients with longstanding dysphagia. Curr Opin Otolaryngol Head Neck Surg. 2018 Jun;26(3):167-173. doi: 10.1097/MOO.0000000000000454. PMID: 29553959. |
Wrong study design (narrative review + prospective case series) |
|
Li XW, Li LY. Efficacy of neuromuscular electrical stimulation on Wilson's disease patients with dysphagia. J Phys Ther Sci. 2019 Dec;31(12):971-974. doi: 10.1589/jpts.31.971. Epub 2019 Dec 3. PMID: 32038066; PMCID: PMC6893162. |
Disease is too rare |
|
Maeda K, Koga T, Akagi J. Interferential current sensory stimulation, through the neck skin, improves airway defense and oral nutrition intake in patients with dysphagia: a double-blind randomized controlled trial. Clin Interv Aging. 2017 Nov 7;12:1879-1886. doi: 10.2147/CIA.S140746. PMID: 29158670; PMCID: PMC5683771. |
Wrong I (TESS) |
|
Miller S, Peters K, Ptok M. Review of the effectiveness of neuromuscular electrical stimulation in the treatment of dysphagia - an update. Ger Med Sci. 2022 Jun 14;20:Doc08. doi: 10.3205/000310. PMID: 35875244; PMCID: PMC9284430. |
Population too broad and lack of numerical data, which is reported in the SR of Wang (2023) |
|
Speyer R, Sutt AL, Bergström L, Hamdy S, Heijnen BJ, Remijn L, Wilkes-Gillan S, Cordier R. Neurostimulation in People with Oropharyngeal Dysphagia: A Systematic Review and Meta-Analyses of Randomised Controlled Trials-Part I: Pharyngeal and Neuromuscular Electrical Stimulation. J Clin Med. 2022 Jan 31;11(3):776. doi: 10.3390/jcm11030776. PMID: 35160228; PMCID: PMC8836998. |
More recent SR and NMA available |
|
Sun Y, Chen X, Qiao J, Song G, Xu Y, Zhang Y, Xu D, Gao W, Li Y, Xu C. Effects of Transcutaneous Neuromuscular Electrical Stimulation on Swallowing Disorders: A Systematic Review and Meta-Analysis. Am J Phys Med Rehabil. 2020 Aug;99(8):701-711. doi: 10.1097/PHM.0000000000001397. PMID: 32209833; PMCID: PMC7343179. |
More recent SR and NMAs specifically on stroke patients, HNC patients and PD patients available |
Beoordelingsdatum en geldigheid
Publicatiedatum : 12-03-2026
Beoordeeld op geldigheid : 12-03-2026
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire cluster ingesteld. Dit cluster bestaat uit vertegenwoordigers van alle relevante organisaties die betrekking hebben op de zorg voor patiënten met stem- en slikklachten.
Het cluster Laryngologie bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden worden indien nodig gevraagd om hun expertise in te zetten voor een specifieke richtlijnmodule. Het cluster Laryngologie bestaat uit de volgende personen:
Clusterstuurgroep
- Dhr. drs. R.N.P.M. (Rico) Rinkel
- Mevr. drs. M.M.G.E.C. (Margaret) de Jong
- Mevr. dr. E.M.J.M. (Emke) van den Broek
- Dhr. dr. D.A. (Derrek) Heuveling
- Mevr. drs. M.J. (Marieke) Hazewinkel
Clusterexpertisegroep
- Dhr. dr. M.R.A. (Michel) van Hooren
- Mevr. C. (Carine) Roos
- Mevr. Y.G.J. (Yvonne) Hendrick
- Mevr. drs. M.M. (Masja) van het Hoofd
- Mevr. P.S. (Petra) Verdouw
Met ondersteuning van
- Mevr. drs. B.L. (Babette) Gal-de Geest, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. dr. A.C. (Anniek) van ‘t Veld, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. E. (Esther) van der Bijl, informatiespecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterstuurgroepleden en actief betrokken expertisegroepsleden (fungerend als schrijver en/of meelezer bij tenminste één van de geprioriteerde richtlijnmodules) hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een richtlijnmodule worden wijzigingen in belangen aan de projectleider doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase. Een overzicht van de belangen van de clusterleden en betrokken expertisegroepsleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Clusterstuurgroep
Tabel Gemelde (neven)functies en belangen stuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Rico Rinkel (voorzitter) |
KNO-arts laryngoloog Amsterdam UMC |
Plv Regionaal Tuchtcollege |
Geen |
Geen restricties |
|
Emke van den Broek |
Laryngoloog UMC Utrecht |
Voorzitter kerngroep laryngologie, lid werkgroep chronische hoest, MAR larynxpapillomatose, bezoekend docent/KNO-arts opleiding logopedie Hogeschool Utrecht |
Geen |
Geen restricties |
|
Marieke Hazewinkel |
Radioloog bij MRON (Maatschap Radiologie Oost Nederland)
|
MRI trekker radioloog MST (Medisch Spectrum Twente) |
Geen |
Geen restricties |
|
Derrek Heuveling
|
KNO-arts Meander Medisch Centrum |
Lid Kerngroep Laryngologie Lid werkgroep Standpuntnota benigne speekselklierpathologie |
Geen |
Geen restricties |
|
Margaret de Jong
|
HumanCapitalCare arbodienst verlener
|
Lid klachtencommissie Sexuele Intimidatie en Geweld sociale werkvoorziening; onkostenvergoeding per zitting |
Geen |
Geen restricties |
Clusterexpertisegroep
Tabel Gemelde (neven)functies en belangen expertisegroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Michel van Hooren |
KNO-arts te Maasziekenhuis Pantein |
PhD candidate te UM: dysfonie en OD bij M. Parkinson |
Geen |
Geen restricties |
|
Carine Roos |
Logopedist slikteam, De Hoogstraat Revalidatie |
Axon docent slikproblematiek |
Geen |
Geen restricties |
|
Yvonne Hendrick |
Logopedist slikteam, De Hoogstraat Revalidatie |
Geen |
Geen |
Geen restricties |
|
Masja van het Hoofd |
Beleidsmedewerker Parkinson Vereniging |
Redacteur bij het parkinsonplatform in oprichting (informatieplatform vergelijkbaar met bijv ms.nl, diabetes.nl) |
Geen |
Geen restricties |
|
Petra Verdouw |
Patiëntenvereniging |
Geen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van relevante patiëntenorganisaties aan de need-for-update en/of prioritering. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijnmodule is tevens ter commentaar voorgelegd aan alle relevante patiëntenorganisaties in de stuur- en expertisegroep (zie ‘Samenstelling cluster’ onder ‘Verantwoording’). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
| Module |
Uitkomst raming |
Toelichting |
|
Elektrostimulatie bij dysfagie |
Geen financiële gevolgen |
Uitkomst 2 |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Need-for-update, prioritering en uitgangsvragen
Tijdens de need-for-update fase (november, 2023) inventariseerde het cluster de geldigheid van de richtlijnmodules binnen het cluster. Naast de partijen die deelnemen aan de stuur- en expertisegroep zijn hier ook andere stakeholders voor benaderd. Per richtlijnmodule is aangegeven of deze geldig is, herzien moet worden, kan vervallen of moet worden samengevoegd. Ook was er de mogelijkheid om nieuwe onderwerpen aan te dragen die aansluiten bij één (of meerdere) richtlijn(en) behorend tot het cluster. De richtlijnmodules waarbij door één of meerdere partijen werd aangegeven herzien te worden, werden doorgezet naar de prioriteringsronde. Ook suggesties voor nieuwe richtlijnmodules werden doorgezet naar de prioriteringsronde. Afgevaardigden vanuit de partijen in de stuur- en expertisegroep werden gevraagd om te prioriteren (zie ‘Samenstelling cluster’ onder ‘Verantwoording’). Hiervoor werd de RE-weighted Priority-Setting (REPS) – tool gebruikt. De uitkomsten (ranklijst) werd gebruikt als uitgangspunt voor de discussie. Voor de geprioriteerde richtlijnmodules zijn door de het cluster concept-uitgangsvragen herzien of opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd indien mogelijk gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
Tabel Gradaties voor de kwaliteit van wetenschappelijk bewijs
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in een richtlijnmodule volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Tabel Sterkte van de aanbevelingen
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de richtlijnmodule Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd voorgelegd aan alle partijen die benaderd zijn voor de need-for-update fase. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd ter autorisatie of goedkeuring voorgelegd aan de partijen die beschreven staan bij ‘Initiatief en autorisatie’ onder ‘Verantwoording’.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 3.0 (2023). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: Laryngologie - Module electrostimulatie |
|
|
Uitgangsvraag/modules: Wat is de meerwaarde van (functionele) elektrostimulatie in de behandeling van patiënten met dysfagie? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 4 april 2025 |
|
Periode: vanaf 2015 |
Talen: geen restrictie |
|
Literatuurspecialist: Esther van der Bijl |
|
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Deduplication: voor het ontdubbelen is gebruik gemaakt van http://dedupendnote.nl:9777/ |
|
|
Toelichting:
Het sleutelartikel wordt gevonden met deze search.
Vanwege de grote opbrengst wordt de search in AS Review uitgevoerd.
|
|
|
Te gebruiken voor richtlijntekst: A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched from 2015 to the 4th of April 2025 for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords. The overall search strategy was derived from two primary search concepts: (1) dysphagia; (2) electric stimulation. Duplicates were removed using EndNote software. After deduplication a total of 1481 records were imported for title/abstract screening. |
|
Zoekopbrengst - 4 april 2025
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
292 |
102 |
|
|
RCT |
433 |
218 |
|
|
Observationele studies |
623 |
209 |
|
|
Totaal |
1348 |
529 |
1481* |
*voor AS Review
Zoekstrategie - 4 april 2025
Embase.com
|
No. |
Query |
Results |
|
#1 |
'dysphagia'/exp OR 'oropharyngeal dysphagia'/exp OR 'regurgitation'/exp OR 'swallowing'/exp OR 'cricopharyngeal dysfunction'/exp OR aphagopraxia:ti,ab,kw OR dysphag*:ti,ab,kw OR disphag*:ti,ab,kw OR dysfag*:ti,ab,kw OR disfag*:ti,ab,kw OR regurgitat*:ti,ab,kw OR swallow*:ti,ab,kw |
247628 |
|
#2 |
'electrotherapy'/exp OR 'neuromuscular electrical stimulation'/exp OR 'nerve stimulation'/exp OR 'transcutaneous electrical nerve stimulation'/exp OR 'vitalstim'/exp OR (((neuromuscular OR nerve*) NEAR/3 stimulat*):ti,ab,kw) OR ((electr* NEAR/3 stimulat* NEAR/3 therap*):ti,ab,kw) OR ((electr* NEAR/3 (therap* OR treatment*)):ti,ab,kw) OR electrotherap*:ti,ab,kw OR electrostimulat*:ti,ab,kw OR electricostimulat*:ti,ab,kw OR nmes:ti,ab,kw OR 'nerve stimulus':ti,ab,kw OR neurostimulat*:ti,ab,kw OR tens:ti,ab,kw OR 'percutaneous electr* nerve stimulat*':ti,ab,kw OR 'transcutaneous electr* nerve stimulat*':ti,ab,kw OR vitalstim:ti,ab,kw OR 'functional electr* stimulat*':ti,ab,kw |
435191 |
|
#3 |
#1 AND #2 |
6624 |
|
#4 |
#3 AND [2015-2025]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
2472 |
|
#5 |
'meta analysis'/exp OR 'systematic review'/exp OR 'scoping review'/exp OR 'rapid review'/exp OR 'umbrella review'/exp OR 'cochrane database of systematic reviews'/jt OR 'network meta-analysis'/exp OR 'networkmeta analy*':ti,ab,kw OR 'networkmetaanaly*':ti,ab,kw OR metaanaly*:ti,ab,kw OR 'meta analy*':ti,ab,kw OR metanaly*:ti,ab,kw OR prisma:ti,ab,kw OR prospero:ti,ab,kw OR metaanali*:ti,ab,kw OR 'meta anali*':ti,ab,kw OR metanali*:ti,ab,kw OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab,kw) OR (((structured OR systemic*) NEAR/3 (review* OR overview* OR synth*) NEAR/3 literature):ti,ab,kw) OR ((systemic* NEAR/1 review*):ti,ab,kw) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab,kw) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab,kw) OR (((literature NEAR/3 (review* OR overview*)):ti,ab,kw) AND (search*:ti,ab,kw OR database*:ti,ab,kw OR 'data base*':ti,ab,kw)) OR (('data extraction*':ti,ab,kw OR 'data source*':ti,ab,kw) AND ('study selection*':ti,ab,kw OR 'studies selection*':ti,ab,kw)) OR ('search strateg*':ti,ab,kw AND 'selection criteria*':ti,ab,kw) OR ('data source*':ti,ab,kw AND 'data synth*':ti,ab,kw) OR medline*:ti,ab,kw OR pubmed*:ti,ab,kw OR 'pub med*':ti,ab,kw OR embase:ti,ab,kw OR cochrane*:ti,ab,kw OR (((critical* OR rapid*) NEAR/2 (review* OR overview* OR synth*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synth*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynth*:ti,ab,kw OR 'meta synth*':ti,ab,kw OR 'review* of review*':ti,ab,kw |
1097437 |
|
#6 |
'randomized controlled trial'/exp OR 'clinical trial'/exp OR 'randomization'/de OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'triple blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ti,ab OR ((random* NEAR/2 (trial OR study)):ti,ab) OR ((random* NEAR/10 (trial OR trail OR 'clinical trial' OR 'clinical trail' OR 'clinical study' OR 'multicenter study' OR crossover OR 'cross over')):ti) OR (((randomised OR randomized) NEXT/6 study):ti) OR 'random* control* clinical trial':ti,ab OR 'random* control* clinical trail':ti,ab OR 'random* control* clinical study':ti,ab OR ((('single blind*' OR 'double blind*' OR 'triple blind*' OR 'quadruple blind*') NEAR/4 (study OR trial OR trail OR design)):ti,ab) OR placebo*:ti,ab OR ((randomly NEAR/1 assign*):ti,ab) OR ((random* NEAR/3 distribut* NEAR/7 group*):ti,ab) OR (((pragmatic OR practical) NEXT/1 ('clinical trial' OR 'clinical trail')):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEXT/3 (trial OR trail)):ti,ab) OR ((random* NEAR/4 ('cross over*' OR crossover*)):ti,ab) OR ((phase NEAR/5 ('clinical trial' OR 'clinical trail' OR randomized OR randomised)):ti) OR ((random* NEAR/3 phase NEAR/3 (trial OR trail OR study)):ti,ab) OR 'random* divid*':ti,ab,kw OR 'control* group':ti,ab,kw |
3955407 |
|
#7 |
'major clinical study'/de OR 'clinical study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR 'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
17974506 |
|
#8 |
#4 AND #5 - SR |
292 |
|
#9 |
#4 AND #6 NOT #8 - RCT |
433 |
|
#10 |
#4 AND #7 NOT (#8 OR #9) - Observationeel |
623 |
|
#11 |
#8 OR #9 OR #10 - Totaal |
1348 |
|
#12 |
'effectiveness of interventions for dysphagia in parkinson disease':ti |
1 |
|
#13 |
#11 AND #12 |
1 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Deglutition Disorders/ or exp Deglutition/ or aphagopraxia.ti,ab,kf. or dysphag*.ti,ab,kf. or disphag*.ti,ab,kf. or dysfag*.ti,ab,kf. or disfag*.ti,ab,kf. or regurgitat*.ti,ab,kf. or swallow*.ti,ab,kf. |
160497 |
|
2 |
exp Electric Stimulation Therapy/ or exp Electric Stimulation/ or exp Transcutaneous Electric Nerve Stimulation/ or ((neuromuscular or nerve*) adj3 stimulat*).ti,ab,kf. or (electr* adj3 stimulat* adj3 therap*).ti,ab,kf. or (electr* adj3 (therap* or treatment*)).ti,ab,kf. or electrotherap*.ti,ab,kf. or electrostimulat*.ti,ab,kf. or electricostimulat*.ti,ab,kf. or nmes.ti,ab,kf. or nerve stimulus.ti,ab,kf. or neurostimulat*.ti,ab,kf. or tens.ti,ab,kf. or percutaneous electr* nerve stimulat*.ti,ab,kf. or transcutaneous electr* nerve stimulat*.ti,ab,kf. or vitalstim.ti,ab,kf. or functional electr* stimulat*.ti,ab,kf. |
302492 |
|
3 |
1 and 2 |
2175 |
|
4 |
limit 3 to yr="2015 -Current" |
934 |
|
5 |
4 not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
825 |
|
6 |
exp Meta-Analysis/ or exp Network Meta-Analysis/ or exp Systematic Review/ or (networkmeta analy* or networkmetaanaly* or metaanaly* or meta analy* or metanaly* or prisma or prospero or metaanali* or meta anali* or metanali*).ti,ab,kf. or ((systemati* or scoping or umbrella or structured literature) adj3 (review* or overview*)).ti,ab,kf. or ((structured or systemic*) adj3 (review* or overview* or synth*) adj3 literature).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 (review* or overview*)) and (search* or database* or data base*)).ti,ab,kf. or ((data extraction* or data source*) and (study selection* or studies selection*)).ti,ab,kf. or (search strateg* and selection criteria*).ti,ab,kf. or (data source* and data synth*).ti,ab,kf. or (medline* or pubmed* or pub med* or embase or cochrane*).ti,ab,kf. or cochrane.jw. or ((critical* or rapid*) adj2 (review* or overview* or synth*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synth*)) and (search* or database* or data base*)).ab. or metasynth*.ti,ab,kf. or meta synth*.ti,ab,kf. |
816855 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2864789 |
|
8 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or exp cohort studies/ or epidemiologic studies/ or ((multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ |
7970102 |
|
9 |
5 and 6 - SR |
102 |
|
10 |
(5 and 7) not 9 - RCT |
218 |
|
11 |
(5 and 8) not (9 or 10) - Observationeel |
209 |
|
12 |
9 or 10 or 11 - Totaal |
529 |