Timing weke delen behandeling bij open onderbeenfractuur
Uitgangsvraag
Op welk moment dient definitieve reconstructie van het weke delen letsel van patiënten met een open onderbeenfractuur plaats te vinden?
Aanbeveling
Verricht de definitieve reconstructie van de weke delen van een open onderbeenfractuur zo snel mogelijk, het liefst binnen drie dagen en uiterlijk binnen één week, indien de conditie van de patiënt dat toelaat.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek verricht naar het effect van vroeg sluiten van de weke delen versus vertraagd sluit van de weke delen bij patiënten met open fracturen aan de onderste extremiteiten. Infecties werden gedefinieerd als cruciale uitkomstmaat. Complicaties (zoals non-union, amputaties en fractuur gerelateerde infecties) werden als belangrijke uitkomstmaten gedefinieerd.
Voor de cruciale uitkomstmaat infectie werd een klinisch relevant verschil gevonden in het aantal infecties na sluiten van de weke delen binnen drie dagen vergeleken met sluiten van de weke delen na drie dagen, binnen een week versus na een week en binnen twee weken versus na twee weken. Echter, voor alle drie de PICO’s werd de bewijskracht als zeer laag gegradeerd. Dit wil zeggen dat de literatuur erg onzeker is over de gevonden effecten. De zeer lage bewijskracht kan worden verklaard door een gebrek aan informatie met betrekking tot het corrigeren van confounders en het kleine aantal events in de geïncludeerde studies. Ditzelfde geldt voor de belangrijke uitkomstmaat. Voor de belangrijke uitkomstmaat complicaties, waaronder (secundaire) amputatie, non-union en fractuur gerelateerde infecties werden klinisch relevante verschillen gevonden voor amputatie bij sluiten van de weke delen binnen drie dagen ten opzichte van sluit van de weke delen na drie dagen en sluiten van de weke delen binnen een week versus sluiten van de weke delen na een week. De literatuur liet geen verschil zien in het aantal amputaties tussen sluiting binnen twee weken en sluiting na twee weken. De bewijskracht voor deze vergelijkingen werd echter ook op zeer laag gegradeerd. De uitkomst non-union werd in één geïncludeerde studie gerapporteerd, maar hier bleek geen verschil te bestaan tussen sluiten van de wond binnen een week versus sluiten van de wond na een week. De bewijskracht hiervoor was zeer laag.
De International Lower Limb Collaborative studie werd gepubliceerd na de literatuursearch voor de herziening van deze module en is derhalve niet in de literatuuranalyse opgenomen. Dit is een internationale retrospectieve studie met één jaar follow-up, waarin in totaal 2694 patiënten werden geïncludeerd. De resultaten laten zien dat een weke delen bedekking na 72 uur zorgt voor een significante toename van het aantal diepe infecties, non-unions en amputaties. Deze complicaties gaan gepaard met forse toename van persoonlijke en maatschappelijke kosten.
De publicatie van de richtlijn van de ‘British Orthopedic Association (BOA)’ en de ‘British Association of Plastic, Reconstructive and Aesthetic Surgeons (BAPRAS) (2017)’ streeft eenzelfde beleid na op dezelfde gronden.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het aanbieden van een letsel met een fractuur die al meer dan een week blootligt is niet meer van deze tijd. De patiënt wacht dan nodeloos, vaak zelfs op een overplaatsing, waarbij de risico’s op korte en lange termijn complicaties significant toenemen.
Kosten (middelenbeslag)
In de Lower Limb Collaborative studie komt naar voren dat behandeling van weke delen bedekking na 72 uur zorgt voor een significante toename van het aantal diepe infecties, non-unions en amputaties. Deze complicaties gaan gepaard met een frose toename van persoonlijke en maatschappelijke kosten.
Aanvaardbaarheid, haalbaarheid en implementatie
Uiteindelijk maakt het type weke delen bedekking niet uit zolang deze maar adequaat is. Ook maakt het niet uit voor de bedekking of het een fasciocutane lap of een spierlap betreft. Voor de hoogenergetische letsels is de bedekking met een vrije lap toch vaak de beste keuze vanwege de bekende zone of injury. Dit is zeker zo voor de letsels in het distale derde deel van de tibia, de enkel en de voet. Echter, de organisatie van een vrije lap is gezien de operatieduur lastiger en de planning daarvan legt een belasting op de reconstructieve afdelingen.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Zowel de resultaten van de systematische literatuur search als de recent gepubliseerde INTELLECT trial laten zien dat er minder diepe infectie, non-unions en amputaties optreden indien de definitieve weke delen bedekking zo vroeg mogelijk wordt verricht.
Onderbouwing
In het geval van een open fractuur is het van groot belang dat de weke delen goed verzorgd worden. Het initieel debridement is hierin noodzakelijk en dient te worden uitgevoerd door een ervaren team, wat kan betekenen dat de patiënt moet worden overgeplaatst of dat het debridement in de dienst wordt uitgesteld tot de volgende ochtend, alleen bij een fors gecontamineerde dient dit direct te worden uitgevoerd.
Na het debridement moet besloten worden of de wond primair gesloten kan worden, een weke delen reconstructie nodig heeft of dat een amputatie de beste optie is. In deze besluitvorming dient de mening van de orthopedisch-traumachirurg, plastisch chirurg, revalidatiearts en patiënt gewogen te worden.
Als een weke delen reconstructie noodzakelijk wordt geacht en dit niet direct na het debridement gedaan kan worden is het noodzakelijk dit op korte termijn te plannen om diepe infecties en de hiermee gepaard gaande complicaties te voorkomen.
Hoe snel deze definitieve bedekking precies gedaan dient te worden is onduidelijk, echter is onnodig uitstellen omdat er geen plastisch chirurg beschikbaar obsoleet in deze tijd, een snelle verwijzing is dan noodzakelijk.
PICO 1: Soft tissue coverage within three days versus soft tissue coverage after three days
- Infections
|
Very low GRADE |
Soft tissue coverage within three days may result in less infections when compared with soft tissue coverage after more than three days in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Godina (1986); Gopal (2000); Gopal (2004); Wood (2012). |
- Complications
- Amputation
|
Very low GRADE |
Soft tissue coverage within three days may result in less amputations when compared with soft tissue coverage after more than three days in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Gopal (2000); Wood (2012). |
-
- Non-union
|
No GRADE |
Because of a lack of data in the included studies of this guideline, it was not possible to draw any conclusions regarding the outcome non-union in patients with open fractures of the lower limbs undergoing soft tissue coverage within three days compared with patients who underwent soft tissue coverage after more than three days.
Sources: - |
-
- Fracture related infection
|
No GRADE |
Because of a lack of data in the included studies of this guideline, it was not possible to draw any conclusions regarding the outcome fracture related infection in patients with open fractures of the lower limbs undergoing soft tissue coverage within three days compared with patients who underwent soft tissue coverage after more than three days.
Sources: - |
PICO 2: Soft tissue coverage within one week versus soft tissue coverage after one week
- Infections
|
Very low GRADE |
Soft tissue coverage within one week may result in less infections when compared with soft tissue coverage after more than one week in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Cierny (1983); Wood (2012). |
- Complications
- Amputation
|
Very low GRADE |
Soft tissue coverage within one week may result in less amputations when compared with soft tissue coverage after more than one week in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Cierny (1983); Wood (2012). |
-
- Non-union
|
Very low GRADE |
Soft tissue coverage within one week may result in less non-unions when compared with soft tissue coverage after more than one week in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Cierny (1983); Wood (2012). |
-
- Fracture related infection
|
No GRADE |
Because of a lack of data in the included studies of this guideline, it was not possible to draw any conclusions regarding the outcome fracture related infection in patients with open fractures of the lower limbs undergoing soft tissue coverage within one week compared with patients who underwent soft tissue coverage after more than one week.
Sources: - |
PICO 3: Soft tissue coverage within two weeks versus soft tissue coverage after two weeks
- Infections
|
Very low GRADE |
Soft tissue coverage within two weeks may result in less infections when compared with soft tissue coverage after more than two weeks in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Fischer (1991); Wood (2012). |
- Complications
- Amputation
|
Very low GRADE |
Soft tissue coverage within two weeks may result in little to no difference in the number of amputations when compared with soft tissue coverage after more than two weeks in patients with open fractures of the lower limbs. However, the evidence is very uncertain.
Sources: Fischer (1991); Wood (2012). |
-
- Non-union
|
No GRADE |
Because of a lack of data in the included studies of this guideline, it was not possible to draw any conclusions regarding the outcome non-union in patients with open fractures of the lower limbs undergoing soft tissue coverage within two weeks compared with patients who underwent soft tissue coverage after more than two weeks.
Sources: - |
-
- Fracture related infection
|
No GRADE |
Because of a lack of data in the included studies of this guideline, it was not possible to draw any conclusions regarding the outcome fracture related infection in patients with open fractures of the lower limbs undergoing soft tissue coverage within two weeks compared with patients who underwent soft tissue coverage after more than two weeks.
Sources: - |
Description of studies
The systematic review of Wood (2012) investigated the timing of flap coverage in open fractures. Wood (2012) searched the electronic databases of Cochrane Database of Systematic Reviews, Cochrane Central Register of Controlled Trials, MEDLINE, CINAHL, and EMBASE between January 1950 and July 2010. The Orthopaedic Trauma Association (2003-2010) were also examined. Studies were eligible for inclusion if they met the following inclusion criteria: (I) studies that followed patients who had surgical repair of an open fracture requiring flap coverage; (II) review articles or comparative studies evaluating the timing of wound coverage for open fractures including randomized controlled trials and observational studies; (III) studies that used a clinical outcome marker to evaluate timing of wound coverage in management of open fractures, and (IV) unpublished data from studies fulfilling criteria I or II. Articles exclusively examining nonliving populations or animal studies, articles examining management using primary closure methods, articles which used non-surgical methods for fracture management, or articles that studied other variables outside of timing of flap coverage in open fracture injuries were excluded. In total, twenty observational studies were included in Wood (2012). Of these, six studies met the inclusion criteria of this guideline (Cierny, 1983; Fischer, 1991; Francel, 1992; Godina, 1986; Gopal, 2000; Gopal, 2004), involving 753 participants. Gopal (2000) and Gopal (2004) compared soft tissue coverage within three days with soft tissue coverage after three days (PICO 1). Cierny (1985) compared soft tissue coverage within zero to seven days with soft tissue coverage between seven and 30 days (PICO 1). Fischer (1991) compared soft tissue coverage within ten days with soft tissue coverage between ten days and six weeks or after six weeks and Francel (1992) compared soft tissue coverage within fifteen days with soft tissue coverage between fifteen and 30 days or after more than 31 days (both studies were included for PICO 3). The risk of bias was assessed with the Newcastle-Ottawa Scale for Cohort Studies. The reported outcomes in the study of Wood (2012) were infections and complications.
Results
PICO 1: Soft tissue coverage within three days versus soft tissue coverage after more than three days
- Infections
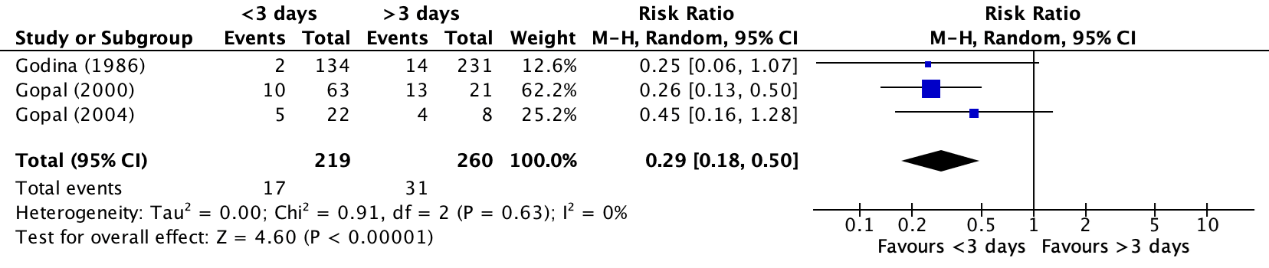
Infections were reported in three studies derived from the systematic review of Wood (2012) (Godina, 1986; Gopal, 2000; Gopal, 2004). The results were pooled in a meta-analysis. The pooled number of patients who experienced infections when soft tissue was covered within three days was 17/219 (7.8%), compared to 31/260 (11.9%) infections when soft tissue was covered after more than three days. This resulted in a pooled relative risk ratio of 0.29 (95% CI 0.18 to 0.50) and a number needed to treat (NNT) of 24.4, in favor of covering of soft tissue within three days (figure 1). This was considered as a clinically relevant difference.
Figure 1. Forest plot showing the comparison between soft tissue coverage within three days and soft tissue coverage after more than three days for infections. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
- Complications
- Amputation
Amputations were reported in one study, derived from the systematic review of Wood (2012) (Gopal, 2000). The number of amputations when soft tissue was covered within three days was 2/63 (3.1%), compared to 2/21 (9.5%) amputations when the soft tissue was covered after more than three days. This resulted in a pooled relative risk of 0.33 (95% CI 0.05 to 2.22) and a number needed to treat (NNT) of 15.6, in favor of covering soft tissue within three days. This was considered as a clinically relevant difference.
-
- Non-union
None of the included studies reported information regarding non-union for wound closure within three days compared with wound closure after more than three days in patients with open fractures of the lower limbs.
-
- Fracture related infection
None of the included studies reported information regarding fracture related infection for wound closure within three days compared with wound closure after more than three days in patients with open fractures of the lower limbs.
PICO 2: Soft tissue coverage within one week versus soft tissue coverage after one week
- Infections
Infections were reported in one study derived from the systematic review of Wood (2012) (Cierny, 1983). The number of patients who experienced infections when soft tissue was covered within one week was 3/24 (12.5%), compared to 8/12 (66.7%) infections when soft tissue was covered after more than one week. This resulted in a relative risk ratio of 0.19 (95% CI 0.06 to 0.58) and a number needed to treat (NNT) of 1.8, in favor of covering of soft tissue within one week. This was considered as a clinically relevant difference.
- Complications
- Amputation
Amputations were reported in one study derived from the systematic review of Wood (2012) (Cierny, 1983). The number of patients who experienced amputation when soft tissue was covered within one week was 1/24 (4.2%), compared to 4/12 (33.3%) amputations when soft tissue was covered after more than one week. This resulted in a relative risk ratio of 0.13 (95% CI 0.02 to 1.00) and a number needed to treat (NNT) of 3.4, in favor of covering of soft tissue within one week. This was considered as a clinically relevant difference.
-
- Non-union
Non-unions were reported in one study derived from the systematic review of Wood (2012) (Cierny, 1983). The number of patients who experienced non-union when soft tissue was covered within one week was 1/24 (4.2%), compared to 2/12 (16.7%) non-unions when soft tissue was covered after more than one week. This resulted in a relative risk ratio of 0.25 (95% CI 0.03 to 2.49) and a number needed to treat (NNT) of 8.0, in favor of covering soft tissue within one week. This was considered as a clinically relevant difference.
-
- Fracture related infection
None of the included studies reported information regarding fracture related infection for wound closure within one week compared with wound closure after one week in patients with open fractures of the lower limbs.
PICO 3: Soft tissue coverage within two weeks versus soft tissue coverage after two weeks
- Infections
Infections were reported in one study derived from the systematic review of Wood (2012) (Fischer, 1991). The number of patients who experienced infections when soft tissue was covered within two weeks was 3/11 (27.3%), compared to 13/13 (100%) infections when soft tissue was covered after more than two weeks. This resulted in a relative risk ratio of 0.30 (95% CI 0.12 to 0.73) and a number needed to treat (NNT) of 1.4, in favor of covering soft tissue within two weeks. This was considered as a clinically relevant difference.
- Complications
- Amputation
Amputations were reported in one study derived from the systematic review of Wood (2012) (Fischer, 1991). The number of patients who experienced amputation when soft tissue was covered within two weeks was 1/11 (9.1%), compared to 1/13 (7.7%) when soft tissue was covered after more than two weeks. This resulted in a relative risk ratio of 1.18 (95% CI 0.08 to 16.78) and a number needed to treat (NNT) of 71.4, in favor of covering of soft tissue after two weeks. This was not considered as a clinically relevant difference.
-
- Non-union
None of the included studies reported information regarding non-union infection for wound closure within two weeks compared with wound closure after two weeks in patients with open fractures of the lower limbs.
-
- Fracture related infection
None of the included studies reported information regarding fracture related infection for wound closure within two weeks compared with wound closure after two weeks in patients with open fractures of the lower limbs.
Level of evidence of the literature
PICO 1: Soft tissue coverage within three days versus soft tissue coverage after three days
- Infections
The level of evidence regarding the outcome infections was derived from observational studies and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1) and the small number of events (imprecision, -1). The level of evidence was considered as very low.
- Complications
- Amputation
The level of evidence regarding the outcome amputation was derived from an observational study and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1), the wide confidence interval crossing the lower and upper boundaries of clinical relevance, and the small number of events (both imprecision, -2). The level of evidence was considered as very low.
-
- Non-union
None of the included studies reported information regarding the predefined outcome non-union in patients with open fractures in the lower limbs who underwent soft tissue coverage within three days compared with patients who underwent soft tissue coverage after more than three days.
-
- Fracture related infection
None of the included studies reported information regarding the predefined outcome fracture related infection in patients with open fractures in the lower limbs who underwent soft tissue coverage within three days compared with patients who underwent soft tissue coverage after more than three days.
PICO 2: Soft tissue coverage within one week versus soft tissue coverage after one week
- Infections
The level of evidence regarding the outcome infections was derived from observational studies and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1) and the small number of events (imprecision, -1). The level of evidence was considered as very low.
- Complications
- Amputation
The level of evidence regarding the outcome amputation was derived from an observational study and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1), the wide confidence interval crossing the lower boundary of clinical relevance, and the small number of events (both imprecision, -2). The level of evidence was considered as very low.
-
- Non-union
The level of evidence regarding the outcome non-union was derived from an observational study and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1), the wide confidence interval crossing the lower and upper boundaries of clinical relevance, and the small number of events (both imprecision, -2). The level of evidence was considered as very low.
-
- Fracture related infection
None of the included studies reported information regarding the predefined outcome fracture related infection in patients with open fractures in the lower limbs who underwent soft tissue coverage within one week compared with patients who underwent soft tissue coverage after more than one week.
PICO 3: Soft tissue coverage within two weeks versus soft tissue coverage after two weeks
- Infections
The level of evidence regarding the outcome infections was derived from observational studies and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1) and the small number of events (imprecision, -1). The level of evidence was considered as very low.
- Complications
- Amputation
The level of evidence regarding the outcome amputation was derived from an observational study and therefore started low. The level of evidence was downgraded by one level because of a lack of information regarding confounding (risk of bias, -1), the wide confidence interval crossing the lower and upper boundaries of clinical relevance, and the small number of events (both imprecision, -2). The level of evidence was considered as very low.
-
- Non-union
None of the included studies reported information regarding the predefined outcome non-union in patients with open fractures in the lower limbs who underwent soft tissue coverage within two weeks compared with patients who underwent soft tissue coverage after more than two weeks.
-
- Fracture related infection
None of the included studies reported information regarding the predefined outcome fracture related infection in patients with open fractures in the lower limbs who underwent soft tissue coverage within two weeks compared with patients who underwent soft tissue coverage after more than two weeks.
PICO 1: Soft tissue coverage within three days versus soft tissue coverage after three days
A systematic review of the literature was performed to answer the following question: What are the (un)beneficial effects of soft tissue coverage within three days versus after more than three days in patients with an open fracture of the lower limbs.
P: Patients with open fractures of the lower limbs
I: Soft tissue coverage within three days
C: Soft tissue coverage after three days
O: Chronic infection; infection; non-union; fracture related infection; (secondary) amputation
PICO 2: Soft tissue coverage within one week versus soft tissue coverage after one week
A systematic review of the literature was performed to answer the following question: What are the (un)beneficial effects of soft tissue coverage within one week versus after more than one week in patients with an open fracture of the lower limbs.
P: Patients with open fractures of the lower limbs
I: Soft tissue coverage within one week
C: Soft tissue coverage after one week
O: Chronic infection; infection; non-union; fracture related infection; (secondary) amputation
PICO 3: Soft tissue coverage within two weeks versus soft tissue coverage after two weeks
A systematic review of the literature was performed to answer the following question: What are the (un)beneficial effects of soft tissue coverage within two weeks versus after more than two weeks in patients with an open fracture of the lower limbs.
P: Patients with open fractures of the lower limbs
I: Soft tissue coverage within two weeks
C: Soft tissue coverage after two weeks
O: Chronic infection; infection; non-union; fracture related infection; (secondary) amputation
Relevant outcome measures
The guideline development group considered infections as a critical outcome for decision making; and non-union, (secondary) amputation, and fracture related infection as important outcomes for decision making.
The working group defined a threshold of 10% for continuous outcomes and a relative risk (RR) for dichotomous outcomes of <0.80 and >1.25 as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2010 until the 26th of June 2022. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 742 hits. Studies were selected based on the following criteria: systematic reviews, RCTs and observational studies on when definitive reconstruction of the soft tissue lesion in patients with an open lower leg fracture should take place. Four studies were initially selected based on title and abstract screening. After reading the full text, one study met the inclusion criteria and was therefore included in the analysis of the literature.
Results
One study (a systematic review) was included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Berner JE, Chan JKK, Gardiner MD, Navia A, Tejos R, Ortiz-Llorens M, Ortega-Briones A, Rakhorst HA, Nanchahal J, Jain A; INTELLECT Collaborative. International Lower Limb Collaborative (INTELLECT) study: a multicentre, international retrospective audit of lower extremity open fractures. Br J Surg. 2022 Aug 16;109(9):792-795. doi: 10.1093/bjs/znac105. PMID: 35470389.
- Cierny G 3rd, Byrd HS, Jones RE. Primary versus delayed soft tissue coverage for severe open tibial fractures. A comparison of results. Clin Orthop Relat Res. 1983 Sep;(178):54-63. PMID: 6349899.
- Francel TJ, Vander Kolk CA, Hoopes JE, Manson PN, Yaremchuk MJ. Microvascular soft-tissue transplantation for reconstruction of acute open tibial fractures: timing of coverage and long-term functional results. Plast Reconstr Surg. 1992 Mar;89(3):478-87; discussion 488-9. PMID: 1741471.
- Fischer MD, Gustilo RB, Varecka TF. The timing of flap coverage, bone-grafting, and intramedullary nailing in patients who have a fracture of the tibial shaft with extensive soft-tissue injury. J Bone Joint Surg Am. 1991 Oct;73(9):1316-22. PMID: 1918113.
- Godina M. Early microsurgical reconstruction of complex trauma of the extremities. Plast Reconstr Surg. 1986 Sep;78(3):285-92. doi: 10.1097/00006534-198609000-00001. PMID: 3737751.
- Gopal S, Majumder S, Batchelor AG, Knight SL, De Boer P, Smith RM. Fix and flap: the radical orthopaedic and plastic treatment of severe open fractures of the tibia. J Bone Joint Surg Br. 2000 Sep;82(7):959-66. doi: 10.1302/0301-620x.82b7.10482. PMID: 11041582.
- Gopal S, Giannoudis PV, Murray A, Matthews SJ, Smith RM. The functional outcome of severe, open tibial fractures managed with early fixation and flap coverage. J Bone Joint Surg Br. 2004 Aug;86(6):861-7. doi: 10.1302/0301-620x.86b6.13400. PMID: 15330028.
- Wood T, Sameem M, Avram R, Bhandari M, Petrisor B. A systematic review of early versus delayed wound closure in patients with open fractures requiring flap coverage. J Trauma Acute Care Surg. 2012 Apr;72(4):1078-85. doi: 10.1097/TA.0b013e31823fb06b. PMID: 22491630.
Evidence table for systematic reviews
Research question: Op welk moment dient definitieve reconstructie van het weke delen letsel van patiënten met een open onderbeenfractuur plaats te vinden?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
|
Wood (2012) |
SR and meta-analysis of cohort studies
Literature search between 1950 and July 2010.
A: Cierny (1983) B: Francel (1992) C: Fischer (1991) D: Godina (1986) E: Gopal (2000) F: Gopal (2004)
Study design: A: Prospective cohort study B: Retrospective cohort study C: Retrospective cohort study. D: Prospective cohort study E: Retrospective cohort study F: Retrospective cohort study
Setting and Country: A: Not reported. B: Not reported. C: Not reported. D: Not reported. E: Not reported. F: Not reported.
Source of funding Not stated.
Conflicts of interest: The authors declare no conflicts of interest.
|
Inclusion criteria SR:
Exclusion criteria SR:
Two studies included
Important patient characteristics at baseline:
N A: N=36 B: N=72 C: N=43 D: N=532 (of which N = 231 >6 weeks) E: N=80 N=33
Type of fractures A: Open tibial type III/IIIa fractures B: Open tibial type IIIb fractures C: Open tibial type IIIb fractures D: Complex trauma of extremities E: Open tibial type iiib/IIIc fractures F: Open tibial type iiib/IIIc fractures
Groups comparable at baseline? Yes. |
Describe intervention:
A: Early flap coverage 0-7 days
B: <15 days
C: Early flap coverage 0-10 days
D: Coverage within 72 hours
E1: < 24h E2: 24-72h Both groups combined: <3 days.
F1: < 24h F2: 24-72h Both groups combined: <3 days.
|
Describe control:
A: Late flap coverage >7 days
B1: 15-30 days B2: >30 days Both groups combined: >2 weeks
C: Late flap coverage >6 weeks
D1: Coverage between >72 hours and 3 months. ( N = 301); D2: coverage after 3 months (N = 231)
E: >72h (>3 days).
F: >72h (>3 days). |
End-point of follow-up: A: 7 weeks
B: 42 months
C: Mean 104 weeks
D: Not reported.
E: N/A
F: 46 months
|
< 3 days versus > 3 days
Outcome measure: infection, n/N (%) D (Godina, 1986) I: 2/134 (1.5%) C: 14/231 (6%)
E (Gopal, 2000) I: 10/63 (15.9%) C: 13/21 (61.9%)
F (Gopal, 2004) I: 5/22 (22.7%) C: 4/8 (50%)
Outcome measure: amputations, n/N (%) E (Gopal, 2000) I: 2/63 (3.2%) C: 2/21 (9.5%)
< 1 week versus > 1 week
Outcome measure: infection, n/N (%) A (Cierny, 1983) I: 3/24 (12.5%) C: 8/12 (66.7%)
Outcome measure: amputation, n/N (%) A (Cierny, 1983) I: 1/24 (4.2%) C: 4/12 (33.3%)
Outcome measure: Non-union, n/N (%) A (Cierny, 1983) I: 1/24 (4.2%) C: 2/12 (16.7%)
< 2 weeks versus > 2 weeks
Outcome measure: major complications such as reexploration, loss of free flap, and chronic osteomyelitis, n/N (%)
B (Francel, 1982) I: 1/28 (3.6%) C: 14/44 (31.8%)
Outcome measure: minor complications such as superficial infections, partial los of skin graft, n/N (%) B (Francel, 1982) I: 10/28 (3.6%) C: 7/44 (15.9%)
Outcome measure: total complications, n/N (%) B (Francel, 1982) I: 11/28 (39.3%) C: 21/44 (47.7%)
Outcome measure: infection, n/N (%) C (Fischer, 1991) I: 3/11 C: 13/13
Outcome measure: amputation, n/N (%) C (Fischer, 1991) I: 1/11 C: 1/13
|
Quality assessment for single studies retrieved from the systematic review of Wood (2012)
Research question: Op welk moment dient definitieve reconstructie van het weke delen letsel van patiënten met een open onderbeenfractuur plaats te vinden?
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure?
|
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study?
|
Confounding-assessment
Can we be confident in the assessment of confounding factors?
|
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables?
|
Assessment of outcome
Can we be confident in the assessment of outcome?
|
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias
|
|
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Low, Some concerns, High |
|
|
Cierny (1983) |
Probably yes
Reason: -
|
Definitely yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Probably yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
Some concerns |
|
Francel (1992) |
Definitely yes
Reason: Eighty-three Gustilo grade IIIB tibial fractures required free-muscle-flap coverage of the Maryland Institute for Emergency Medical Services Systems between January of 1983 and June of 1988.
|
Probably yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Probably yes
Reason: -
|
Definitely yes
Reason: -
|
No information
Reason: -
|
Some concerns |
|
Godina (1986) |
Probably yes
Reason: Between 1976 and 1983, 532 patients underwent microsurgical reconstruction of posttraumatic defects of the extremities performed by the Microsurgery Service of the University Department for Plastic Surgery and Burns in Ljubljana.
|
Probably yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Probably yes
Reason: The bone-healing time was based on a clinical evaluation. In the lower extremity, the bone was considered to be healed when full weight-bearing commenced; in the upper extremity, when the patients was permitted unrestricted use without splints. With respect to hospitalization time, this included all time in the hospital following the injury.
|
No information
Reason: -
|
No information
Reason: -
|
High
|
|
Gopal (2000) |
Definitely yes
Reason: We retrospectively reviewed the records of 84 patients who had been seen primarily or referred to our department between 1990 and 1998 with an open fracture of the tibia graded OIIIb or OIIIc.
|
Probably yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Some concerns |
|
Gopal (2004) |
Definitely yes
Reason:
|
Probably yes
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Probably yes
Reason: -
|
No information
Reason: -
|
No information
Reason: -
|
Some concerns |
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
D’Alleyrand (2014) |
Does not match PICO: Wrong outcomes. |
|
Jenkinson (2014) |
Does not match PICO: Wrong comparison. |
|
Liu (2012) |
Does not match PICO: Wrong outcomes. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-04-2024
Beoordeeld op geldigheid : 02-10-2023
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2020 een multidisciplinaire cluster ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van het cluster) die betrokken zijn bij de zorg voor patiënten met een letsel na een ongeval.
Deze module is herzien binnen het cluster letsel na ongeval. Het cluster letsel na ongeval bestaat uit twaalf richtlijnen. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden worden indien nodig gevraagd om hun expertise in te zetten voor een specifieke richtlijnmodule. De samenstelling van de clusterstuur- en expertisegroep is als volgt:
Clusterstuurgroep
- Dhr. dr. M.F. Termaat, chirurg, Leids Universitair Medisch Centrum, Leiden; NVvH (voorzitter)
- Dhr. drs. H. Amghar, radioloog, Saxenburgh Medisch Centrum, Hardenberg; NVvR
- Mevr. E.C. Cingir – Doganer, junior projectmanager, Stichting Kind en Ziekenhuis, Utrecht
- Dhr. dr. G.J. van Geffen, anesthesioloog, Radboudumc, Nijmegen; NVA
- Dhr. drs. R.P.T.C.G. Groetelaers, chirurg, Maxima Medisch Centrum, Eindhoven; NVvH
- Dhr. dr. T. de Jong, plastisch chirurg, Radboudumc, Nijmegen; NVPC
- Dhr. dr. J. van Oldenrijk, orthopedisch chirurg, Erasmus MC, Rotterdam; NOV
- Dhr. prof. dr. V.A. de Ridder, chirurg, Wilhelmina Kinderziekenhuis, Utrecht; NVvH
- Dhr. dr. J.P.H.J. Rutges, orthopedisch chirurg, Erasmus MC, Rotterdam; NOV
- Mevr. A. Swinkels, junior projectmanager en beleidsmedewerker, Stichting Kind & Ziekenhuis, Utrecht (vervanger van mevr. Doganer tijdens zwangerschapsverlof)
- Mevr. drs. P.V. ter Wengel, neurochirurg, Haaglandenmc, Den Haag; NVvN
- Dhr. drs. H.H. Wijnen, klinisch geriater, Rijnstate, Arnhem; NVKG
- Mevr. dr. S. Woltz, chirurg, Spaarne Gasthuis, Haarlem; NVvH
- Dhr. dr. G. Zemack, revalidatiearts, Libra Revalidatie & Audiologie, Eindhoven; VRA
- Dhr. prof. dr. J.N. Doornberg, orthopedisch chirurg, Universitair Medisch Centrum Groningen, Groningen; NOV (tot november 2021)
- Mevr. R. Uitzinger, junior projectmanager, Stichting Kind en Ziekenhuis, Utrecht (tot juni 2022)
- Mevr. dr. D. Vos, chirurg, Amphia Ziekenhuis, Breda; NVvH (tot januari 2022)
- Dhr. dr. B.P. Vierhout, chirurg, Wilhelmina Ziekenhuis Assen, Assen; NVvH (tot februari 2023)
Clusterexpertisegroep
- Dhr. dr. J. Alexandridis, SEH-arts KNMG; NVSHA
- Dhr. drs. B.F.M. Blok, uroloog, ErasmusMC, Rotterdam; NVU
- Dhr. drs. G.P.G. Boots, bedrijfsarts; NVAB
- Dhr. H.J.G. van den Broek, voorzitter, Osteoporose Vereniging, Haarlem
- Mevr. drs. N.N. Cheung, arts-microbioloog, HAGA ziekenhuis, Den Haag; NVMM
- Dhr. dr. J. Deunk, chirurg, Amsterdam UMC, Amsterdam; NVvH
- Mevr. dr. J.A.M.C. Dirks, arts-microbioloog, Maastricht Universitair Medisch Centrum; NVMM
- Mevr. drs. M.H.G. Dremmen, radioloog, Erasmus MC, Rotterdam; NVvR
- Dhr. dr. A.W.J.M. Glaudemans, nucleair geneeskundige, Universitair Medisch Centrum Groningen, Groningen; NVNG
- Mevr. drs. M. Hartog, AIOS Klinische Geriatrie, Eramsus MC, Rotterdam; NVKG
- Mevr. K.D. den Hertog, gipsverbandmeester, Alrijne Ziekenhuis, Leiden; VGN
- Dhr. dr. D.J. Hofstee, orthopedisch chirurg, Noordwest Ziekenhuisgroep, Alkmaar; NOV
- Mevr. G. Hoitinga, verpleegkundige, Amsterdam UMC, Amsterdam; NVSHV
- Dhr. dr. H.R. Holtslag, revalidatiearts, Amsterdam UMC, Amsterdam; VRA
- Dhr. dr. J. Hoogendoorn, chirurg, Haaglanden MC, den Haag; NVvH
- Dhr. M.J.M. Hospers, ambulance verpleegkundige, V&VN, Utrecht
- Dhr. D.J.W. Hulsen, klinisch fysicus, Jeroen Bosch Ziekenhuis, ‘s Hertogenbosch; NVKF
- Dhr. drs. D. van Iersel, radioloog, VieCuri Medisch Centrum, Venlo; NVvR
- Dhr. T. Jonkergouw, adviseur patiëntenbelangen, Patiëntenfederatie Nederland, Utrecht
- Mevr. V. Kleijn-Vis, physician assistant (trauma)chirurgie, Francisus Gasthuis & Vlietland, Rotterdam; NAPA
- Mevr. S.K. Koster †, handtherapeut, Alrijne Ziekenhuis, Leiden; NVHT
- Dhr. dr. N.D. Kruyt, neuroloog, Leids Universitair Medisch Centrum, Leiden; NVN
- Dhr. dr. C. van der Leij, radioloog, Maastricht Universitair Medisch Centrum, Maastricht; NVvR
- Dhr. dr. M.P.A. van Meer, arts-microbioloog, Rijnstate, Arnhem; NVMM
- Mevr. dr. B.L. van Meer, sportarts, St Antonius Ziekenhuis, Nieuwegein; VSG
- Dhr. dr. B. van Minnen, kaakchirurg, Universitair Medisch Centrum Groningen, Groningen; NVMKA
- Dhr. dr. F.C. Öner, orthopedisch chirurg, Universitair Medisch Centrum Utrecht, Utrecht; NOV
- Dhr. F. Penninx, Dwarslaesie Organisatie Nederland, Nijkerk
- Dhr. dr. M.C.G. van der Poll, chirurg-intensivist, Maastricht Universitair Medisch Centrum, Maastricht; NVIC
- Dhr. dr. H. Rakhorst, plastisch chirurg, Medisch Spectrum Twente, Enschede; NVPC
- Mevr. drs. M.J. Scheerder, radioloog, Amsterdam UMC, Amsterdam; NVvR
- Dhr. drs. H. Scheper, internist, Leids Universitair Medisch Centrum, Leiden; NIV
- Dhr. drs. J. van Schuppen, radioloog, Amsterdam UMC, Amsterdam; NVvR
- Dhr. R.R. Smit Duijzentkunst, bestuurslid, Korter maar Krachtig, Enschede
- Dhr. I. Spin, medior medewerker kwaliteit, KNGF, Amersfoort
- Dhr. drs. R.S. de Wijn, plastisch chirurg, Spaarne Gasthuis, Haarlem; NVPC
- Dhr. drs. M.J. Elzinga, chirurg, Medisch Centrum Leeuwaarden, Leeuwarden; NVvH (tot november 2022)
Met ondersteuning van
- M. Griekspoor, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.N. Hofstede, senior adviseur en teamleider, Kennisinstituut van de Federatie Medisch Specialisten
- A.L.J. Kortlever – van der spek, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Clusterstuurgroep
Tabel 1. Gemelde (neven)functies en belangen stuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Termaat (voorzitter) |
|
|
Geen
|
Geen restricties |
|
Amghar |
|
Geen |
Geen
|
Geen restricties |
|
Doganer |
|
Geen |
Geen
|
Geen restricties |
|
van Geffen |
|
Geen |
Geen
|
Geen restricties |
|
Groetelaers |
|
|
Geen
|
Geen restricties |
|
de Jong |
|
|
Geen |
Geen restricties |
|
van Oldenrijk |
|
|
Geen
|
Geen restricties |
|
de Ridder |
|
(Alle genoemde nevenwerkzaamheden zijn onbetaald.)
|
Geen
|
Geen restricties |
|
Rutges |
|
|
Extern gefinancierd onderzoek:
Organiseren van AO spine events in Nederland. |
Geen restricties |
|
Swinkels |
|
Geen |
Geen
|
Geen restricties |
|
Ter Wengel |
|
|
Persoonlijke financiële belangen:
Persoonlijke relaties:
Extern gefinancierd onderzoek:
|
Geen restricties; geen relatie tussen extern gefinancierd onderzoek en de te herziene modules |
|
Wijnen |
|
Geen |
Overige belangen:
|
Geen restricties; er is geen relatie tussen het bedrijf en de te herziene modules. |
|
Woltz |
|
|
Geen
|
Geen restricties |
|
Zemack |
|
|
Geen
|
Geen restricties |
|
Doornberg (per november 2021 gestopt)
|
|
Geen |
Geen
|
Geen restricties |
|
Uitzinger (per juni 2021 gestopt) |
|
Geen |
Geen
|
Geen restricties |
|
Vierhout (per februari 2023 gestopt) |
|
|
Extern gefinancierd onderzoek:
|
Geen restricties; geen relatie tussen extern gefinancierd onderzoek en de te herziene modules. |
|
Vos (per januari 2022 gestopt) |
|
|
Geen |
Geen restricties |
Richtlijn Open onderbeenfractuur:
- Module ‘Debridement’
- Module ‘Weke delenletsel bij open onderbeenfractuur’
- Module ‘Timing weke delen behandeling bij open onderbeenfractuur’
(Vanuit de stuurgroep waren dhr. Vierhout en dhr. de Jong betrokken om het perspectief van de stuurgroep te vertegenwoordigen.)
Tabel 3. Gemelde (neven)functies en belangen expertisegroep modules richtlijn Open onderbeenfractuur
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Alexandridis |
|
|
Geen |
Geen restricties |
|
Hartog |
|
|
Geen |
Geen restricties |
|
Hofstee |
|
Geen |
Geen |
Geen restricties |
|
Holtslag |
|
|
Geen |
Geen restricties |
|
Hoogendoorn |
|
Geen |
Geen |
Geen restricties |
|
van Meer |
|
Geen |
Geen |
Geen restricties |
|
Rakhorst |
|
|
Intellectuele belangen en reputatie:
|
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door de participatie van Stichting Kind en Ziekenhuis in de stuurgroep en diverse organisaties in de expertisegroep (zie samenstelling van de stuur- en expertisegroep). De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptmodule is tevens te commentaar voorgelegd aan alle patiëntenorganisaties in de stuur- en expertisegroep. De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema).
Uit de kwalitatieve raming blijkt dat er [waarschijnlijk geen/ mogelijk] substantiële financiële gevolgen zijn, zie onderstaande tabel.
Tabel 4. Uitkomsten kwalitatieve raming
|
Module |
Uitkomst raming |
Toelichting |
|
Module ‘Debridement’ |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten). De aanbevelingen zullen daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module ‘Weke delenletsel bij open onderbeenfractuur’ |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten). De aanbevelingen zullen daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module ‘Timing weke delen behandeling bij open onderbeenfractuur’ |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten). De aanbevelingen zullen daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Need-for-update, prioritering en uitgangsvragen
Tijdens de need-for-update fase (april, 2021) inventariseerde het cluster de geldigheid van de modules binnen het cluster. Naast de partijen die deelnemen aan de stuur- en expertisegroep zijn hier ook andere stakeholders voor benaderd, zie onderstaande tabel.
Tabel 5. Partijen need-for-update.
|
Partijen need-for-update |
||
|
Nederlands Huisartsen Genootschap |
Nederlandse Vereniging voor Handchirurgie |
Patiëntenvereniging Complex Regionaal Pijn Syndroom
|
|
Revalidatie Nederland |
Ambulancezorg Nederland
|
Inspectie Gezondheidszorg en Jeugd
|
|
Nederlandse Vereniging voor Kindergeneeskunde
|
Nederlands Vereniging van Rugpatiënten de ‘Wervelkolom’
|
Nederlandse Federatie van Universitair Medische Centra
|
|
Nederlandse Vereniging van Ziekenhuizen |
Samenwerkende Topklinische Ziekenhuizen
|
Zorginstituut Nederland |
|
Zelfstandige Klinieken Nederland |
Zorgverzekeraars Nederland
|
Vereniging van Specialisten Ouderengeneeskunde
|
|
Ergotherapie Nederland |
Nederlands Instituut van Psychologen |
Nederlandse Wetenschappelijke Vereniging voor Seksuologie |
|
Nederlandse Vereniging van Diëtisten |
Nederlandse Vereniging voor Arthroscopie
|
Nederlandse Vereniging voor Reumatologie |
|
Nederlandse Vereniging van Ziekenhuisapothekers |
Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose |
Nederlandse Vereniging van Anesthesiemedewerkers |
|
Reumafonds |
ReumaZorg Nederland |
|
Per module is aangegeven of deze geldig is, kan worden samengevoegd met een andere module, obsoleet is en kan vervallen of niet meer geldig is en moet worden herzien. Ook was er de mogelijkheid om nieuwe onderwerpen voor modules aan te dragen die aansluiten bij één (of meerdere) richtlijn(en) behorend tot het cluster. De modules die uit de need-for-update naar voren kwamen zijn besproken en geprioriteerd door leden van de stuur- en expertisegroep.
Voor de geprioriteerde modules zijn door de het cluster concept-uitgangsvragen herzien of opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd zo nodig gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Hultcrantz, 2017; Schünemann, 2013).
Tabel 6. Gradaties voor de kwaliteit van wetenschappelijk bewijs
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Tabel 7. Sterkte van de aanbevelingen
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd ter commentaar voorgelegd aan alle partijen die benaderd zijn voor de need-for-update fase. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd voorgelegd ter autorisatie aan de partijen die beschreven staan onder het kopje geldigheid en onderhoud (zie verantwoording).
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Literature search strategy
Algemene informatie
|
Richtlijn: Open onderbeenfracturen |
|
|
Uitgangsvraag: Op welk moment dient definitieve reconstructie van het weke delen letsel van patiënten met een open onderbeenfractuur plaats te vinden? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 26-06-2022 |
|
Periode: >2010 |
Talen: Engels, Nederlands |
|
Literatuurspecialist: Laura Boerboom |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
→ Voor deze vraag is gezocht op de elementen open onderbeenfractuur (in het blauw) en soft tissue coverage (in het groen).
à Het genoemde sleutelartikel van Wood (2012) zit in de zoekopbrengst.
à Resultaten staan in Rayyan.
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 26-06-2022 met relevante zoektermen gezocht vanaf 2010 naar systematische reviews, RCT’s en observationele studies over op welk moment de definitieve reconstructie van het weke delen letsel van patiënten met een open onderbeenfractuur dient plaats te vinden. De literatuurzoekactie leverde 742 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
39 |
54 |
64 |
|
RCTs |
128 |
145 |
208 |
|
Observationele studies |
268 |
412 |
470 |
|
Totaal |
435 |
611 |
742 |
Zoekstrategie
|
Database |
Zoektermen |
|||||||||||||||||||||||||||||||||||||||
|
Embase
|
|
|||||||||||||||||||||||||||||||||||||||
|
Medline (OVID)
|
1 exp *Fractures, Open/ or ((open or 'long-bone' or tibia* or 'lower limb') adj3 fracture*).ti,ab,kf. (23026) 2 exp *Wound Healing/ or ('wound healing' or 'tissue coverage' or 'tissue closure' or 'wound closure' or 'wound coverage' or fix or flap).ti,ab,kf. (215812) 3 1 and 2 (2982) 4 limit 3 to ((english or dutch) and yr="2013-Current") (1554) 5 (meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) (573240) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (2273358) 7 Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) (5185679) 8 4 and 5 (54) – SRs 9 (4 and 6) not 8 (145) - RCTs 10 (4 and 7) not 8 not 9 (412) – Observationele studies 11 8 or 9 or 10 (611) |