Aanvullend onderzoek naar micrometastasen bij lymfeklieronderzoek
Uitgangsvraag
Welke aanvullende lymfeklieronderzoeken zijn nodig voor adequate stadiering?
Aanbeveling
Gebruik geen aanvullende technieken voor het detecteren van (micro)metastasen in regionale lymfeklieren.
Overwegingen
Het toevoegen van aanvullende immuunhistochemische en/of pcr technieken aan de standaard HE-gebaseerde diagnostiek voor het herkennen van metastasen in mediastinale lymfeklieren bij NSCLC leidt tot een toename van het aantal gevonden micrometastasen. Deze patiënten hebben een verminderde kans op overleving (HR=2.46). Prospectieve predictieve data met betrekking tot overleving naar aanleiding van het instellen van adjuvante therapie op basis van deze bevindingen ontbreken echter.
De bewijskracht van de bevindingen is laag.
Het vaststellen, verslaan en acteren op basis van middels aanvullende technieken in schildwachtklieren aangetroffen (micro)metastasen behoort in Nederland inmiddels tot de standaard voor mammacarcinoom en melanoom patiënten met een verhoogde a priori kans op metastasering op basis van de tumorkenmerken. Dit type factoren (met name grootte van de tumor, tumortype en differentiatiegraad) zou mogelijk ook in NSCLC patiënten de positieve voorspellende waarde voor het aantreffen van micrometastasen in mediastinale lymfeklieren met immuunhistochemie en/of pcr kunnen verhogen. Totdat dit echter op basis van prospectieve studies (zoals ook bij mammacarcinoom en melanoom) de besluitvorming omtrent aanvullende therapie informeert, is het twijfelachtig of de onrust veroorzaakt bij de patiënt door aangetroffen micrometastasen en de kosten en personeelsbelasting voor de pathologie laboratoria door een hierop aangepaste werkwijze opwegen tegen de voordelen van mogelijk betere prognostische accuratesse.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Zie boven.
Kosten (middelenbeslag)
Zie boven.
Haalbaarheid en implementatie
Zie boven.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Gezien het ontbreken van adequate klinische interventie studies is er, ondanks de aangetoonde prognostische waarde van de detectie van micrometastasen, tot dusverre geen bewijs voor de toegevoegde predictieve waarde van aanvullende technieken voor het detecteren van (micro)metastasen in regionale lymfeklieren.
Onderbouwing
In de huidige praktijk van NSCLC worden mediastinale lymfeklierstations pre-operatief en/of peri-operatief gesampled ten behoeve van stagering en beslissingen omtrent de modaliteit van (in opzet) curatieve behandeling dan wel (neo-)adjuvante therapie. De beoordeling van het middels EUS/EBUS/mediastinoscopie/chirurgie verkregen lymfekliermateriaal is daarbij gebaseerd op puur morfologische herkenning van tumorcellen en dan met name van macrometastasen. Het is onduidelijk in hoeverre het herkennen van lymfeklier macro- en micrometastasen met behulp van een sentinel node procedure/immuunhistochemie/seriële coupes/RT-PCR leidt tot klinisch significante additionele prognostische of predictieve bevindingen naast de huidige stand van de praktijk.
Prevalence micrometastases
|
- GRADE |
The detection rate of lymph node micrometastases in patients with pathological N0 non-small cell lung cancer ranged from 3.8% to 68.8%
Sources: (Jeong, 2018; Dai, 2017; Gwozdz, 2018; Ren, 2018) |
Overall survival
|
Low GRADE |
The presence of lymph node micrometastases in patients with pathological N0 non-small cell lung cancer possibly leads to a higher risk of death (HR=2.46, 95%CI 1.87 to 3.25).
Sources: (Jeong, 2018; Dai, 2017; Gwozdz, 2018; Ren, 2018) |
Description of studies
Jeong (2018) reported the results of a systematic review and meta-analysis of observational studies. They searched for relevant studies until 2016 and included 16 studies and 2026 patients (Dai, 2013; Dobashi, 1997; Goldstein, 2000; Gu, 2002; Izbicki, 1996; Kawano, 2002; Li, 2008; Martin, 2016; Nosotti, 2005; Osaki, 2002; Rena, 2007; Roh, 2004; Rusch, 2011; Wu, 2001; Yamashita, 2010; Yasumoto, 2003.) All these studies included stage I–IIB NSCLC. Most studies included T1, N0, M0 NSCLC patients. Sometimes, pathologic N1 or N2 patients were also included, but the results were separately reported for the pathological N0 patients. The included studies reported the number of patients with micrometastases in patients with negative regional lymph nodes which were negative by conventional means. All studies also compared the overall survival between patients with micrometastases en patients without micrometastases, mostly based on 5-year survival data. 14 studies reported the hazard ratio for overall survival and were included in the meta-analysis. The original publications were studies to obtain detailed information on the results of the individual studies.
Additionally, 3 recent studies reporting on the overall survival with or without micrometastases were included (Dai, 2017; Gwozdz, 2018; Ren 2018).
Dai (2017) reported the results of an observational, retrospective, study including 235 patients with pathologically confirmed primary T1a-2aN0M0 adenocarcinoma (stage I). Lymph node micrometastasis was detected with immunohistochemical staining for cytokeratin (AE1/AE3) and thyroid transcription factor-1 (TTF-1). Lymph node micrometastasis was defined as isolated tumor cells or cellular clusters ≤ 0.2mm in greatest dimension. The average number of resected lymph nodes: 14.1±6.7.
Gwozdz (2018) reported the results of an observational retrospective including 148 stage I/II NSCLC patients. Patients with neoadjuvant therapy or early postoperative death were excluded. 4810 mediastinal lymph nodes were determined as metastasis-free by hematoxylin and eosin staining. Occult micrometastases in mediastinal lymph nodes were detected using 1. hematoxylin and eosin, 2. immunohistochemical stains for cytokeratin AE1/AE3/PCK26, and 3. BerEp4.
Ren (2018) reported on an observational study in 589 patients. It clinically and pathologically confirmed primary T1-2aN0M0 (c-stage 1) adenocarcinoma in patients who had undergone surgery. 7892 removed lymph nodes were analysed. The average number of resected lymph nodes was 13.3 ± 6.5. Micrometastases were detected using IHC staining with anti-CK antibody (AE1/AE3; Dako, Carpinteria, CA, USA) and anti-TTF1 antibody (8G7G3/1; Dako). Micrometastases were defined as all metastases smaller than 2 mm in greatest dimension.
The search did not reveal prospective clinical studies using the presence of micrometastases as triage point for additional treatment.
Results
Number of patients with micrometastases
The detection rates for lymph node micrometastases by ancillary techniques in routine pathological N0 (patients without LN metastasis using histologic examination)) patients ranged from 3.8% to 68.8% (Jeong, 2018; Dai, 2017; Gwozdz, 2018; Ren, 2018). Jeong (2018) reported an overall detection rate of LNMM in patients without nodal disease of 25.3% (95%CI 20-32%); Using IHC, the detection rate of lymph node micrometastases was 23.1% (95% CI 18-29%). Using PCR, the detection rate was 33.7% (95% CI 26-43%). The recent studies reported slightly lower detection rates (Dai, 2017: 15%; Gwozdz, 2018: 9.5%; Ren, 2018: 9.3%).
Overall survival
For the meta-analysis of the prognostic value of micrometastases on the overall survival, the data of the meta-analyses by Jeong (2018) and the three more recent observational studies were combined (Figure 1). Patients with pathological N0 and micrometastases in lymph nodes have a higher risk of death as compared to patients with pathological N0 without micrometastases in lymph nodes (HR=2.46 (95%CI 1.87 to 3.25)).
Figure 1 Forrest plot overall survival between patients with or without micrometastases
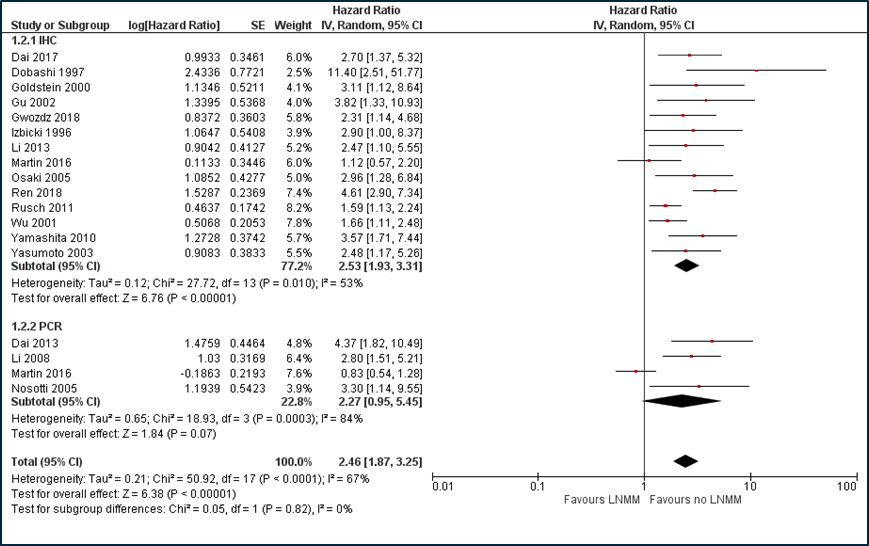
Martin (2016) reported no difference in overall survival between patients with or without micrometastases. In this study, however, two separate comparisons were made: 1. between patients with N1 micrometastases versus patients without micrometastases and 2. between patients with N2 micrometastases versus patients without micrometastases. In most studies, both N1 and N2 micrometastases were combined. In this meta-analysis (Figure 1) we included the data of the comparison N1 versus N0 from the study by Martin (2016). For both IHC and PCR, the HRs reported by Martin (2016) were low as compared to the remaining studies. If we excluded these results of Martin (2016) in a sensitivity analysis, the overall hazard ratio would be slightly higher (HR=2.75 (95%CI 2.19 to 3.46)).
Level of evidence of the literature
For the outcome detection rate, no comparative studies were included. Therefore, no GRADE rating is available.
The level of evidence regarding the outcome measure overall survival was downgraded by two levels because of study limitations (risk of bias; retrospective study design: selection of patients and adequate correction for confounding variables).
A systematic review of the literature was performed to answer the following question:
Does detection of lymph node micrometastasis by immunohistochemistry or PCR affect patients’ overall survival in patients with respectable NSCLC?
P: patients with resectable NSCLC;
I: immunohistochemistry or PCR for detecting lymph node micrometastasis;
C: routine lymph node examination;
O: number of patients with micrometastases in lymph nodes, overall survival.
Relevant outcome measures
The guideline development group considered overall survival as a critical outcome measure for decision making; and the detection rate as an important outcome measure for decision making. A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until March 2019. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 347 hits. Studies were selected based on the following criteria: systematic review or observational study, reporting on the detection rate of micometastases and the overall survival in patients with or without lymph node micrometastasis (detected by immunohistochemistry or PCR). 22 studies were initially selected based on title and abstract screening. After reading the full text, we included the most recent of three relevant meta-analyses (Jeong, 2018) and added three relevant observational studies that had been published after the date until which had been searched in the systematic review.
Results
One systematic review and three more recent original studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- 1 - Dai C, Xie H, Kadeer X, Su H, Xie D, Ren Y, She Y, Zhu E, Fan Z, Chen T, Qin L, Zheng H, Zhang L, Jiang G, Wu C, Chen C. Relationship of Lymph Node Micrometastasis and Micropapillary Component and Their Joint Influence on Prognosis of Patients With Stage I Lung Adenocarcinoma. Am J Surg Pathol. 2017 Sep;41(9):1212-1220. doi: 10.1097/PAS.0000000000000901.
- 2 - Gwóźdź P, Pasieka-Lis M, Kołodziej K, Pankowski J, Banaś R, Wiłkojć M, Zieliński M. Prognosis of Patients With Stages I and II Non-Small Cell Lung Cancer With Nodal Micrometastases. Ann Thorac Surg. 2018 May;105(5):1551-1557. doi: 10.1016/j.athoracsur.2017.12.006.
- 3 - Jeong JH, Kim NY, Pyo JS. Prognostic roles of lymph node micrometastasis in non-small cell lung cancer. Pathol Res Pract. 2018 Feb;214(2):240-244. doi: 10.1016/j.prp.2017.11.005.
- 4 - Ren Y, Zhang L, Xie H, She Y, Su H, Xie D, Zheng H, Zhang L, Jiang G, Wu C, Dai C, Chen C. Lymph Node Micrometastasis Prognosticates Survival for Patients with Stage 1 Bronchogenic Adenocarcinoma. Ann Surg Oncol. 2018 Dec;25(13):3812-3819. doi: 10.1245/s10434-018-6743-8.
Research question: UV12
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
Deng 2016 |
systematic review of Jeong 2018 more recent |
|
Marchevsky 2010 |
systematic review of Jeong 2018 more recent |
|
Dai 2013 |
included in syst review Jeong 2018 |
|
Dobashi 1997 |
included in syst review Jeong 2018 |
|
Digesu 2018 |
not relevant for PICO |
|
Lafuente-Sanchis 2018 |
no relevant outcome measures |
|
Nomori 2016 |
- |
|
Chanida 2014
|
not relevant for answering PICO (another intervention; not relevant outcomes) |
|
Hanagiri 2014
|
no comparison of survival between subgroups with or without micrometastases |
|
Moroga 2012 |
no relevant outcme measures for meta-analysis (survival) |
|
Nwogu 2013 |
no relevant outcome measures for meta-analysis (survival) |
|
Karamustafaoglu 2013 |
not relevant intervention |
|
Uribe-Etxebarria Lugariza-Aresti 2017 |
spanish |
|
Verhagen 2010 |
no relevant outcome measures |
|
Vodicka 2018 |
not relevant for PICO |
|
Wang 2012 |
not relevant population (Stage II-IV NSCLC); about development of method |
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-06-2020
Beoordeeld op geldigheid : 07-07-2020
Bij het opstellen van de modules heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodule komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten. De geldigheid is per module weergegeven.
|
Module |
Regiehouder(s) |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn |
Frequentie van beoordeling op actualiteit |
Wie houdt er toezicht op actualiteit |
Relevante factoren voor wijzigingen in aanbeveling |
|
micrometastasen |
NVVP |
2020 |
2025 |
5-jaarlijks |
NVVP |
- |
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financierder heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Werkgroep
- Dr. I. Bahce, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Drs. N.J.M Claessens, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Prof. dr. E.F.I. Comans, Nucleaire geneeskundige, Nederlandse Vereniging voor Nucleaire Geneeskunde
- Dr. W.A. Draaisma, chirurg, Nederlandse Vereniging voor Heelkunde (tot 1 december 2018)
- Dr. W.H. van Geffen, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Dr. K.J. Hartemink, chirurg, Nederlandse Vereniging voor Heelkunde (vanaf 1 december 2018)
- Dr. L.E.L. Hendriks, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Prof. dr. D. de Ruysscher, Radiotherapeut, Nederlandse Vereniging voor Radiotherapie en Oncologie
- Dr. C. Schaefer-Prokop, radioloog, Nederlandse Vereniging voor Radiologie
- Dr. J.H. Schouwink, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (voorzitter)
- Prof. dr. E.M.D. Schuuring, Klinisch Moleculair Bioloog in de Pathologie, Nederlandse Vereniging voor Pathologie
- Dr. E. Thunnissen, patholoog, Nederlandse Vereniging voor Pathologie
- Dr. J.H. von der Thüsen, patholoog, Nederlandse Vereniging voor Pathologie
- Prof. A.F.T.M. Verhagen, cardio-thoracaal chirurg Nederlandse Vereniging voor Thoraxchirurgie
- Dr. A.J. van der Wekken, longarts, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (vice-voorzitter)
Met ondersteuning van
- Dr. M. Moret-Hartman, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.N. Hofstede, senior adviseur, Kennisinstituut van de Federatie Medische Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in tabel met gemelde belangen in de bijlage. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Gezien een substantieel aantal van de werkgroepleden functies of werkzaamheden heeft die een mogelijke verstrengeling van belangen met zich meebrengen, zijn een aantal afspraken gemaakt over de werkwijze. Besproken is of het mogelijk was de deelname aan adviesraden voor de farmaceutische industrie stop te zetten gedurende de looptijd van het project. Dit werd echter onhaalbaar geacht, omdat de informatie uit de bijeenkomsten voor hen belangrijk werd geacht voor goede patiëntenzorg waarbij recente ontwikkelingen worden meegenomen. Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, bleek het onhaalbaar om tijdens het bespreken van aanbevelingen de werkgroepleden met mogelijke belangen te vragen de zaal te verlaten, omdat er dan slechts een klein aantal werkgroepleden zou overblijven. Daarom is besloten om overwegingen en aanbevelingen te formuleren tijdens een vergadering met de gehele werkgroep. De adviseurs hebben kritisch meegekeken bij de definitieve selectie van abstracts. Tot slot is een nieuwe voorzitter gezocht die geen bezwaar had tegen het opschorten van werkzaamheden voor de farmaceutische industrie gedurende de looptijd van het richtlijnproject. De oorspronkelijk beoogde voorzitter is als vice-voorzitter benoemd.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Bahce |
longarts |
geen |
Participeert incidenteel en op uitnodiging in adviesraden en nascholingen bij diverse farmaceutische bedrijven, te weten Boehringer Ingelheim, AstraZeneca, BMS, Roche.
voert als hoofdonderzoeker investigator-initiated onderzoek uit met sponsoring van Boehringer Ingeleheim (18F-Afatinib-PET) en AstraZeneca (89Zr-durvalumab-PET) |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Hendriks |
longarts |
t/m 31/10/18 postdoc lnstitut Gustave Roussy, Villejuif, Frankrijk |
bezig om een studie op te zetten die veranderingen neurocognitie na cerebrale bestraling concurrent met een tyrosine kinase inhibitor bij niet-kleincellig longkanker patiënten onderzoekt. We zijn bezig funding te zoeken, bedoeling is geld vanuit de industrie te krijgen: voor iedere TKI hebben we de betreffende firma benaderd (industrie heeft geen invloed op het studieprotocol of de analyse/publicatie van de resultaten)
subsidie bij de industrie aangevraagd om psychische belasting te onderzoeken bij patiënten die weten dat ze (asymptomatische) hersenmetastasen hebben. Roche heeft een grant toegezegd
funding gekregen van Roche om vermoeidheid na prophylactische schedelbestraling bij SCLC patiënten te onderzoeken (geen bemoeienis met protocol, analyse of publiceren van de resultaten)
neemt af en toe deel aan adviesraad van SMS (nivolumab) en Soehringer lngelheim (afatinib), betaald (instituut); van meerdere industrieen (Pfizer, Amgen, Soehringer lngelheim) in 2016 financhiele support gekregen voor drukken proefschrift (hersenmetastasen bij longkanker). Voor Astra Zeneca een stukje over mijn proefschrift voor hun website geschreven; voor SMS heb ik een voordracht gehouden. Van Roche, SMS, MSD en AstraZeneca financiele compensatie gekregen voor het houden van lezingen over longkanker |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Comans |
Nucleaire geneeskundige |
geen |
geen |
geen |
|
Draaisma |
chirurg |
geen |
geen |
geen |
|
Van Geffen |
longarts |
Editorial board Cochrane Airways: Onbetaald
Commisie Bronkhorst Nvalt: Onbetaald
|
Deelname aan een investigator initiated onderzoek naar COPD firma Novartis. Financiering is overgemaakt aan UMCG; Voor de bedrijven Chiesi, Boehringer en AstraZeneca deelname aan adviesraden. De hiervoor gebruikelijke CGR vergoeding wordt geweigerd. Reiskosten worden wel vergoed. |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Hartemink |
chirurg |
"Faculty NVALT cursus oncologie voor de longarts Bestuurslid tumorwerkgroep thoracale oncologie AvL commissielid "Kwaliteit" longchirurgijn Nederland Specialisten adviesraad longkanker Nederland Commissielid Wetenschap DLCA-S Bestuurslid PLCRG (research longkanker)" |
Diverse studies die de rol van neo adjuvante immunotherapie bij stadium I, II en III NSCLC onderzoeken |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Claessens |
longarts |
Lid sectie oncologie NVALT - onbetaald Incidenteel adviesraad Astra Zeneca - betaald Gelegenheidsredacteur iPulmonologist - betaald Bestuurslid Holland-Stellenbosch Medical Foundation - onbetaald |
Binnen ons ziekenhuis nemen wij deel en hebben wij deelgenomen aan verscheidende industrie-gedreven klinische trials, onder andere van Astra Zeneca, MSD, BMS, Eli-Lilly en regeneron. Hierbij bestond er onzerzijds geen persoonlijk financieel belang. |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
De Ruysscher |
radiotherapeut-oncoloog |
Hoogleraar Radiotherapie-Oncologie KU Leuven, België. Betaald. |
Onderzoek gefinancierd door Bristol-Myers-Squibb (principal investigator).
Advisory board van Bristol-Myers-Squibb, Roche/ Genentech, Merck/ Pfizer, Astra-Zeneca, Celgene. (betaald aan Maastro clinic) |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Schaefer-Prokop |
radioloog |
|
geen |
geen |
|
Schouwink |
longarts |
Voorzitter bestuur Emil starkenstein Stichting, onbezoldigd |
Hij heeft in het verleden (2015, 2016) tweemaal deelgenomen aan een adviesraad. |
Afgesproken om gedurende het project deelname aan adviesraden stop te zetten. |
|
Schuuring |
Klinisch Moleculair Bioloog in de Pathologie |
"Adviseur/KMBP voor Moleculaire Pathologie voor de Stichting Pathologie Friesland in Leeuwarden (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Martini Ziekenhuis te Groningen en Pathologie SSZOG/OZG in Winschoten (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Treant Zorggroep Bethesda ziekenhuis in Hoogeveen (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Pathologie van Isala in Zwolle (onbetaald)
Bestuurslid van de NVVP (Nederlandse Vereniging voor Pathologie) (onbetaald)
Bestuurslid/voorzitter van de NVVP-sectie Klinische Moleculaire Experimentele Pathologie (onbetaald)
Lid stuurgroep ZONMW-PATH: “Optimising Access to Personalised Cancer Therapy in the Netherlands; from Tissue to Therapy” (www.netwerk-path) (onbetaald)
Scientific Advisory Board. ESP-Quality Control committee (onbetaald)" |
Adviseur/consultant met betrekking tot (moleculaire) diagnostiek voor longkanker (en andere maligniteiten) voor de firma's AstraZeneca, Roche, Pfizer, Novartis, BMS, BioRad, Amgen, BioCartis (honoraria komen op een rekening op UMCG)
Adviseur/scientific expert voor organisatie van (inter)nationale ringstudies voor weefsel en plasma tbv diagnostiek van longkanker (External Quality Assessment) voor de European Society of Pathology (ESP) en overkoepelende IQNPATH
lezingen, onderwijs, nascholing op het gebied van de moleculaire pathologie van longkanker deels tegen vergoeding van firma zoals AstraZeneca, Roche, Pfizer, Novartis, BioRad, BioCartis (honoraria komen op een rekening op UMCG)
financiële ondersteuning voor onderzoek ontvangen van (als PI verantwoordelijk voor een workpackage (onderdeel) van het project) -Boehringer Ingelheim FGFR1 study / The NVALT-17 Study - Roche, Cobas / BMS (CA209-759) - |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Thunnissen |
patholoog |
histogenex, consultant long pathologie; training onder andere PD-L1. bezoldigd |
Investigator initiated research Pfizer naar ALK IHC+ m+ NSCLC (principal investigator)
advisory board bij farmaceutische industrie in verleden (MSD, Pfizer, Clovis, BMS, AstraZeneca, Amgen, Diaceutics, Abbvie,) bezoldigd tegen standaard tarief.
Adviseur UKNEQAS= organisation for external quality assurance in UK (onbezoldigd)" |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Von der Thüsen |
patholoog |
|
deelname advisory boards: AbbVie BMS MSD Roche" |
Aangezien een groot aantal werkgroepleden een potentiële verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Verhagen |
Cardio-thoracaal chirurg |
|
geen |
geen |
|
van der Wekken |
longarts |
|
Deelname aan eenmalige adviesraden voor: AstraZeneca, BMS, Roche, MSD, Pfizer, Boehringer-Ingelheim (geld gaat naar UMCG)
lectures voor AstraZeneca, Roche, BMS, Novartis, Pfizer, Boehringer-Ingelheim (geld gaat naar UMCG)
"Research grant voor investigator initiated study door AstraZeneca voor indicatie die niets met de huidige richtlijn ontwikkeling te maken heeft (geld gaat naar UMCG)
De afdeling longoncologie doet mee aan verschillende internationale onderzoeken, die betaald worden aan het UMCG door BMS, MSD, Roche, Novartis, AbbVie, Boehringer-Ingelheim, Pfizer, ARIAD (Takeda)." |
In verband met gemelde belangen is gezocht naar een nieuwe voorzitter zonder potentiële verstrengeling van belangen. Van de Wekken is vice-voorzitter die onder andere vergaderingen leidt. Schouwink zal onder andere zorgvuldigheid tijdens proces van formuleren van aanbevelingen bewaken. |
|
Moret-Hartman |
adviseur richtlijnontwikkeling |
- |
getrouwd met praktijkhoudend huisarts |
- |
|
Hofstede |
adviseur richtlijnontwikkeling |
- |
|
- |
Inbreng patiëntenperspectief
Er is een focusgroepbijeenkomst georganiseerd om knelpunten en aandachtspunten voor goede zorg te inventariseren bij patiënten met niet-kleincellig longcarcinoom. Een verslag hiervan (zie aanverwante producten) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de module. De conceptmodules zijn tevens voor commentaar voorgelegd aan de deelnemers van de focusgroep en de patiëntenvereniging Longkanker Nederland.
Methode ontwikkeling
Consensus based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de aanverwante producten. De werkgroep heeft geen interne kwaliteitsindicatoren ontwikkeld, omdat dit proces reeds is verankerd in de kwaliteitsregistratie longkanker (https://dica.nl/).
Werkwijze
AGREE
Deze module is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based module tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit de inventarisatie van de knelpunten door Sectie oncologie van de NVALT (SON) kwam naar voren dat er een noodzaak was voor de herziening van de richtlijn niet-kleincellig longarcinoom. Tijdens een invitational conference zijn er knelpunten aangedragen door Longkanker Nederland, de Inspectie Gezondheidszorg en Jeugd (IGJ), de Nederlandse Associatie Physician Assistants (NAPA), de Vereniging Innovatieve Geneesmiddelen (VIG) en de Nederlandse Vereniging van Ziekenhuisapothekers (NVZA). Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse is door de werkgroepleden en de adviseur een uitgangsvraag opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad ‘Zoekverantwoording’ voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration:
- AMSTAR - voor systematische reviews.
- Cochrane - voor gerandomiseerd gecontroleerd onderzoek.
- ACROBAT-NRS - voor observationeel onderzoek.
- QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij voldoende studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de module is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Kennislacunes
Tijdens de ontwikkeling van deze module is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de Kennislacunes. Deze zijn te vinden bij de aanverwante producten.
Commentaar- en autorisatiefase
De conceptmodules zijn aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren zijn de conceptmodules aangepast en definitief vastgesteld door de werkgroep. De definitieve modules zijn aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut via secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Zoekverantwoording
|
Uitgangsvraag: UV12 Welke lymfeklieronderzoeken zijn nodig voor adequate stadiering? |
|
|
Database(s): Medline, Embase |
Datum: 01-03-2019 |
|
Periode: > 2010 |
Talen: Engels |
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
2010 – maart 2019
|
1 (non-small cell lung and (carcinoma* or neoplasm* or cancer*)).ti. or exp *Carcinoma, Non-Small-Cell Lung/ or nsclc.ti. or (adenocarcinoma adj5 (lung or broncho*)).ti. (56990) 2 exp *Immunohistochemistry/ or exp *Sentinel Lymph Node Biopsy/ or exp *Reverse Transcriptase Polymerase Chain Reaction/ or exp *Neoplasm Micrometastasis/ or (sentinel or serial or immunohistochem* or rt-pcr or reverse transcription polymerase chain reaction or Reverse Transcriptase Polymerase Chain Reaction or micrometastas*).ti. (111340) 3 1 and 2 (808) 4 limit 3 to english language (727) 5 limit 4 to yr="2010 -Current" (422) 6 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (383735) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3130894) 8 5 and 6 (14) 9 5 and 7 (131) 10 9 not 8 (130) 11 8 or 10 (144)
= 144 |
347 |
|
Embase (Elsevier) |
('non small cell lung cancer'/exp/mj OR ('non-small cell lung':ti AND (carcinoma*:ti OR neoplasm*:ti OR cancer*:ti)) OR nsclc:ti OR ((adenocarcinoma NEAR/5 (lung OR broncho*)):ti)) AND ('immunohistochemistry'/exp/mj OR 'sentinel lymph node biopsy'/exp/mj OR 'reverse transcription polymerase chain reaction'/exp/mj OR 'micrometastasis'/exp/mj OR sentinel:ti OR serial:ti OR immunohistochem*:ti OR 'rt-pcr':ti OR 'reverse transcription polymerase chain reaction':ti OR 'reverse transcriptase polymerase chain reaction':ti OR micrometastas*:ti) AND (2010-2019)/py AND (english)/lim NOT 'conference abstract':it
Gebruikte filters: Systematische reviews: ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) = 19
Observationeel onderzoek: ‘major clinical study’/exp OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) = 280
= 299 |
