Behandeling van T1b niertumoren
Uitgangsvraag
Welke behandeling (partiële nefrectomie, totale nefrectomie, stereotactic ablative body radiotherapy (SABR), percutane ablatie) kan het beste worden toegepast bij patiënten met een niet-gemetastaseerd niercelcarcinoom tussen 4-7 cm (T1b)?
Aanbeveling
Overweeg bij cT1b niertumoren nefronsparende behandeling.
Gebruik RENAL nephrometry score bij bepalen van de behandelstrategie en registreer deze in het radiologie verslag en de conclusie van het multidisciplinair overleg.
Bepaal het behandeladvies in een multidisciplinair overleg en registreer de conclusie en overwegingen.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De werkgroep heeft een literatuurstudie verricht naar de (on)gunstige effecten van partiële nefrectomie, totale nefrectomie, SABR en percutane ablatie bij patiënten met een niet-gemetastaseerd niercelcarcinoom tussen 4-7 cm (T1b).
PICO 1a: partiële vs totale nefrectomie
Helaas blijken er maar een paar bruikbare publicaties te zijn om de vraag te beantwoorden of een partiële nefrectomie bij T1b tumoren te verkiezen is boven een radicale nefrectomie (Jiang, 2019). Veel studies zijn niet gerandomiseerd, gaan meer over technische verschillen in de partiële nefrectomie, en zijn niet vergelijkend met nefrectomie. Op basis van de resultaten van de literatuuranalyse lijken er geen verschillen te zijn tussen partiële nefrectomie en totale nefrectomie voor de cruciale uitkomstmaten overleving en ziektevrije overleving en de belangrijke uitkomstmaten complicaties en nierfunctie. De bewijskracht werd beoordeeld als zeer laag vanwege imprecisie, inconsistentie en risico op bias. De studie van Jiang laat een duidelijk voordeel in nierfunctiebehoud zien voor de partiële nefrectomie vergeleken met een nefrectomie, maar er zijn geen andere studies die hiernaar hebben gekeken: mogelijk omdat het zo evident is dat bij niersparend opereren er minder nierfunctieverlies is dan bij een nefrectomie. Opvallend is dat de kans op complicaties in de studie van Jiang niet verschilt voor partiële of radicale nefrectomie. Dit kan berusten op een selectiebias: keuze voor partiële nefrectomie vooral bij jongere, fittere patiënten. Er werd geen literatuur gevonden voor het verschil tussen partiële en totale nefrectomie voor de belangrijke uitkomstmaten tijd tot recidief en kwaliteit van leven.
Samenvattend kunnen op grond van de gevonden beperkte literatuur geen conclusies getrokken worden met een hogere gradering dan “zeer laag “ over de keuze tussen een partiële nefrectomie of een radicale nefrectomie bij T1b tumoren.
Naar de mening van de werkgroepleden is het verantwoord om een partiële nefrectomie bij T1b tumoren te overwegen mits dit technisch uitvoerbaar en oncologisch veilig is.
PICO 1b: (percutane) ablative techniques vs (partiële) nefrectomie
Helaas blijkt er maar 1 gedeeltelijk bruikbare publicatie te zijn die percutane ablatietechnieken vergelijkt met (partiele) nefrectomie voor de behandeling van cT1b tumoren. Op basis van de resultaten van de literatuuranalyse lijken er geen verschillen te zijn tussen (percutane) ablatieve therapieën en (partiële) nefrectomie voor de cruciale uitkomstmaten overleving en ziektevrije overleving en de belangrijke uitkomstmaten complicaties en nierfunctie. Hierbij dient te worden opgemerkt dat in deze review alle soorten percutane ablatie (MWA, RFA, Cryoablatie) door elkaar geanalyseerd werden. De bewijskracht werd beoordeeld als zeer laag vanwege risk of bias. Bij alle vergelijkende studies die percutane ablatie vergelijken met partiële nefrectomie of nefrectomie is sprake van een bias: patiënten die geopereerd worden zijn over het algemeen jonger en hebben minder comorbiditeit. Er werd geen literatuur gevonden dat percutane ablatieve therapieën met partiële nefrectomie voor de primaire uitkomstmaten tijd tot recidief en kwaliteit van leven vergelijkt. Er werd geen literatuur gevonden waarin SABR werd vergeleken met partiële nefrectomie.
Studies over recidiefkans en overleving van percutane ablatieve technieken bij T1b niercelcarcinoom zijn zeldzaam, en zijn niet-vergelijkend. De meeste technieken zijn ontwikkeld voor kleinere niertumoren en hebben een maximale grootte van een tumor waarvoor ze kunnen worden toegepast. Voor een aantal technieken in de praktijk tot 4-5 cm. Toepassing bij T1b tumoren tot 7 cm kan betekenen dat meerdere sessies nodig zijn om locale controle te verkrijgen. Voor de behandeling van T1b tumoren lijkt cryoablatie de aangewezen techniek aangezien daar door het gebruik van multipele naalden grotere ablatiezones te verkrijgen zijn dan met de op hitte gebaseerde ablatietechnieken. Verschillende retrospectieve studies laten zien dat cryoablatie een effectieve methode is voor de behandeling van T1b tumoren, met vergelijkbare lange termijnoverleving en met minder complicaties dan partiele nefrectomie maar wel met een hogere recidiefkans. (Aikawa, 2023; Caputo, 2017; Cazalas, 2023).
Er werden na de literatuursearch enkele niet-vergelijkende studies gevonden over SABR. Recent beschrijft Rich, 2022 in een overzichtsartikel de behandeling van T1a -T2 niertumoren met SABR. Het betreft meestal kleine series. De ervaringen die hierin worden beschreven, met korte follow-up, zijn gunstig, met goede lokale controle en beperkte toxiciteit. De resultaten van de recent gepubliceerde prospectieve fase II FASTRACK studie in 70 patienten bevestigen dit samen met een 5-jaarskanker specifieke overleving van 98% (Siva, 2024).
De fractionering van SABR (1-5 fracties) hangt af van tumorgrootte en nabijgelegen radiosensitieve organen. Routinematige biopten na SABR worden niet aanbevolen, omdat positieve resultaten niet voorspellend zijn voor tumorprogressie en de tumor door de behandeling veranderingen ondergaat, zoals verminderde cellulaire activiteit en verhoogde fibrose. Beeldvorming met CT wordt gebruikt om de respons te beoordelen, waarbij veranderingen in tumorgrootte en contrastversterking over een langere periode worden gevolgd. Hoewel contrastversterking na SABR langzaam kan afnemen, kan deze aanvankelijk ook toenemen door inflammatoire effecten op de bloedvaten. De RECIST-criteria worden momenteel gebruikt voor responsbeoordeling (Siva, 2024). Betrouwbare beoordeling van de radicaliteit van SABR of van het herkennen van vroege recidieven is hierdoor niet goed mogelijk (Siva, 2024).
Bij de behandeling van T1b tumoren is het belangrijk om, op basis van patientkarakteristieken zoals leeftijd, comorbiditeit en nierfunctie, in overleg met de patient de meest geschikte behandelingsmethode te kiezen. SABR en cryoablatie spelen vooral een rol bij oudere patienten met comorbiditeiten, voor wie een (partiele) nefrectomie niet haalbaar is.
Net als bij T1a tumoren lijkt het de werkgroep wenselijk om patiënten met cT1b niertumoren prospectief te registreren in een landelijke database waarbij tevens de RENAL score wordt vastgelegd zodat in de toekomst beter de voor- en nadelen van de behandelopties in de Nederlandse setting gewogen kunnen worden. Alhoewel er geen complexiteitsscore superieur is in vergelijking met de andere scores is de werkgroep van mening dat de RENAL score door de eenvoud en toepasbaarheid de voorkeur heeft. Dit vergt overeenstemming en inzet van de diverse betrokken disciplines.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Op grond van de beschikbare literatuur is het niet duidelijk of er verschil is tussen de diverse behandelingen voor de cruciale uitkomstmaten overleving en ziektevrije overleving en de belangrijke uitkomstmaten complicaties en nierfunctie.
Het postoperatieve herstel van patiënten na percutane technieken verloopt in het algemeen
vlotter dan na een partiële nefrectomie. De opnameduur voor een partiële nefrectomie is langer dan voor ablatieve technieken. Percutane ablatie dient daarom bij oudere patiënten met meer comorbiditeit als alternatief voor een partiële nefrectomie besproken te worden. Hetzelfde geldt voor patiënten waarbij een partiële nefrectomie op grond van eerdere chirurgie als veel gecompliceerder wordt ingeschat. In deze situatie kunnen cryoablatie en SABR als alternatief worden overwogen, waarbij SABR een niet-invasieve en poliklinische behandeling is.
Kosten (middelenbeslag)
De kosten effecten van percutane ablatieve technieken en partiële nefrectomie zijn niet goed onderzocht.
Aanvaardbaarheid, haalbaarheid en implementatie
Er zijn in Nederland ziekenhuizen waar ervaring is met het uitvoeren van partiele nefrectomie en alternatieve technieken (percutane ablatie / SABR). Ziekenhuizen die niet over deze ervaring of mogelijkheden beschikken dienen patienten met T1b niertumoren te bespreken met een expertisecentrum. Door patiënten te bespreken vindt er verspreiding van kennis plaats en wordt er meer naar eenduidig beleid gestreefd.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
De keuze tussen partiële nefrectomie , de verschillende percutane ablatieve technieken zoals RFA, MWA, cryoablatie en SABR of radicale nefrectomie dient te worden gemaakt op basis van tumor karakteristieken (zoals tumorgrootte, lokalisatie van de tumor), patiënt karakteristieken (zoals leeftijd, levensverwachting, comorbiditeit, eerdere chirurgie), en voorkeur van de patiënt (zekerheid over aard van de tumor, sneller herstel)
Onderbouwing
Gelokaliseerde niertumoren tussen 4-7 cm (T1b) worden regelmatig behandeld door middel van totale nefrectomie. De ontwikkelingen betreffende deze niertumoren laten zien dat partiële nefrectomie (niersparende operatie) ook mogelijk is. Tevens is de vraag of percutane ablatie of SABR ook mogelijke behandelingen zijn bij deze tumoren. In de huidige situatie is niersparende behandeling voor tumoren <4 cm (T1a) de richtlijn. Voor tumoren >4 cm moet niersparende behandeling overwogen worden. Met de toenemende centralisatie van behandeling van niertumoren is vaker niersparende behandeling uitvoerbaar. Wat is dan de beste techniek daarvoor?
Partial vs radical nephrectomy
|
Very low GRADE |
The evidence is very uncertain about the effect of partial nephrectomy on survival when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Sources: Jiang, 2019; Chong 2018; Venkatramani 2018 |
|
Very low GRADE |
The evidence is very uncertain about the effect of partial nephrectomy on disease-free survival when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Jiang, 2019 |
|
NO GRADE |
No evidence was found regarding the effect of partial nephrectomy on time to recurrence when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
|
|
Very low GRADE |
The evidence is very uncertain about the effect of partial nephrectomy on complications when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Jiang, 2019 |
|
NO GRADE |
No evidence was found regarding the effect of partial nephrectomy on quality of life when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
|
|
Very low GRADE |
The evidence is very uncertain about the effect of partial nephrectomy on renal function when compared with radical nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Jiang, 2019 |
Percutaneous ablative techniques vs (partial) nephrectomy
|
Very low GRADE |
The evidence is very uncertain about the effect of percutaneous ablative therapies on survival when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Chan, 2022 |
|
Very low GRADE |
The evidence is very uncertain about the effect of percutaneous ablative therapies on disease-free survival when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Chan, 2022 |
|
NO GRADE |
No evidence was found regarding the effect of percutaneous ablative therapies on time to recurrence when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma. |
|
Very low GRADE |
The evidence is very uncertain about the effect of percutaneous ablative therapies on complications when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Chan, 2022 |
|
NO GRADE |
No evidence was found regarding the effect of partial nephrectomy on quality of life when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
|
|
Very low GRADE |
The evidence is very uncertain about the effect of percutaneous ablative therapies on renal function when compared with partial nephrectomy in patients with a cT1b non-metastatic renal cell carcinoma.
Source: Chan, 2022 |
Partial vs radical nephrectomy
Description of studies
Jiang (2019) performed a systematic review and meta-analysis to compare long-term oncological outcomes in patients with 4 to 7 cm renal cell carcinoma treated with partial nephrectomy and radical nephrectomy. PUBMED, EMBASE and the Cochrane Central Register were searched for studies which were published in English dating from March 1998 to March 2018. Inclusion criteria were comparative partial nephrectomy or nephron-sparing-surgery and radical nephrectomy for the treatment of 4 to 7 cm renal tumors and evaluation of at least one oncological result such as recurrence-free survival, cancer-special survival, and overall survival. Case reports, reviews and articles without applicable data were excluded. Other exclusion criteria were studies that included both T1b and T2 or renal tumors larger than 7 cm and studies that were not comparative in nature. In total, 16 retrospective studies were included. Meta-analyses were presented for the 5- and 10-year overall survival, the 5- and 10-year cancer-special survival, the 5- and 10-year recurrence-free survival, tumor recurrence, postoperative complications and declined eGFR.
Chong (2018) compared overall survival and unplanned hospital readmissions within 30 days between partial nephrectomy and radical nephrectomy for clinically localized T1 renal tumors by analyzing the National Cancer Database between 2004 and 2013. Exclusion criteria were patients with clinical T2-4, N1, or M1 renal cell carcinoma, missing clinical stage data, renal tumors excised bilaterally or a horseshoe kidney, receiving additional treatment and concurrent or prior cancer diagnosis. Inverse probability of treatment weighting (IPTW) was performed, and therefore patients with missing data on baseline characteristics, survival, or readmission were excluded. In total, 12,656 patients underwent radical nephrectomy, and 4,419 patients underwent partial nephrectomy. The median follow-up was 44.5 months (IQR 25.7 to 68.1 months). Overall survival (months from diagnosis) was the primary outcome measure.
Venkatramani (2018) compared the overall survival and perioperative outcomes in patients with cT1b and cT2 renal cell carcinoma undergoing partial nephrectomy with those undergoing radical nephrectomy by analyzing the National Cancer Data Base (NCDB) registry data from 2004 to 2013. Patients diagnosed with renal cell carcinoma with clinical stage cT1b-T2N0M0 were included. Exclusion criteria were patients diagnosed at death or autopsy and those with missing or unknown data for clinical TNM stage. A 1:1 propensity score matching was performed for the likelihood of receiving partial nephrectomy resulting in a total of 5,534 patients with cT1b tumor that underwent partial nephrectomy and 5,534 patients receiving radical nephrectomy. The median follow-up was 35.6 months (22.2 to 54.1 months) for partial nephrectomy and 45.1 months (26.2 to 65.7 months) for radial nephrectomy. Overall survival was the primary outcome measure.
Results
Survival
Jiang (2019) reported the 5- and 10-year overall survival. At 5-years, no significant difference was found in overall survival between patients who underwent partial nephrectomy and radical nephrectomy (RR 1.02, 95% CI 1.00 to 1.05, p=0.05) (Figure 1.1). The overall survival at 10-years was also not significantly different between patients who underwent partial nephrectomy and radical nephrectomy (RR 1.17, 95% CI 0.95 to 1.44) (Figure 1.2).
Chong (2018) reported that partial nephrectomy is associated with improved overall survival as compared to radical nephrectomy (HR = 0.89, 95% CI 0.82 to 0.99, p=0.025), according to the IPTW-adjusted Cox proportional hazards regression. However, no significant difference was found when applying a more robust sandwich-type variance estimator (HR = 0.89, 95% CI 0.79 to 1.02, p =0.106). In addition, the 5-year IPTW-adjusted Kaplan-Meier (IPTW-KM) was 85.3% for partial nephrectomy and 84.3% for radical nephrectomy, while the 10-year IPTW-KM was 70.8% and 63.6%, respectively.
Venkatramani (2018) reported that partial nephrectomy is associated with a significantly better overall survival than radical nephrectomy (HR=0.81, 95% CI 0.73 to 0.90, p<0.001) on multivariate analyses.
Figure 1.1 5-year overall survival, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
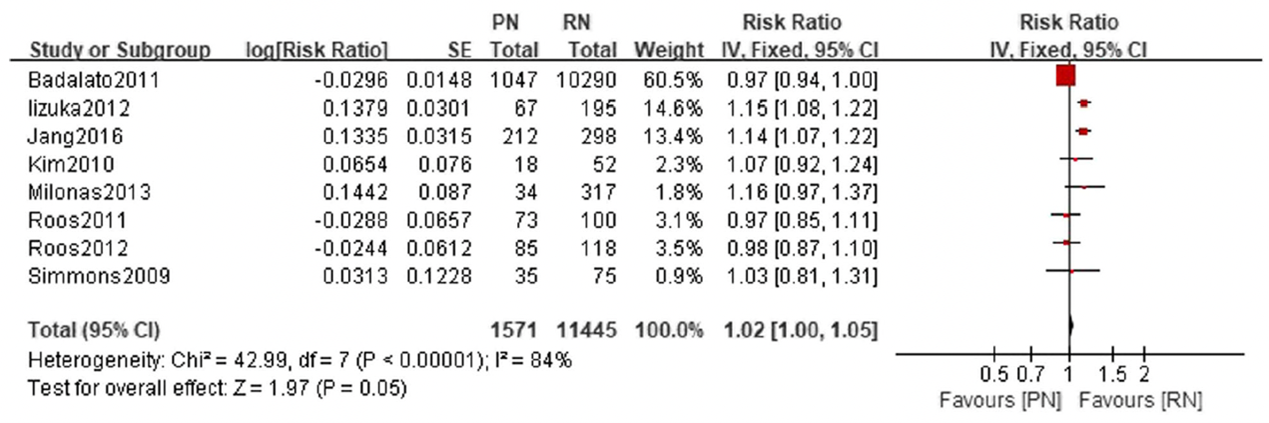
Adapted from Jiang 2019
Figure 1.2 10-year overall survival, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
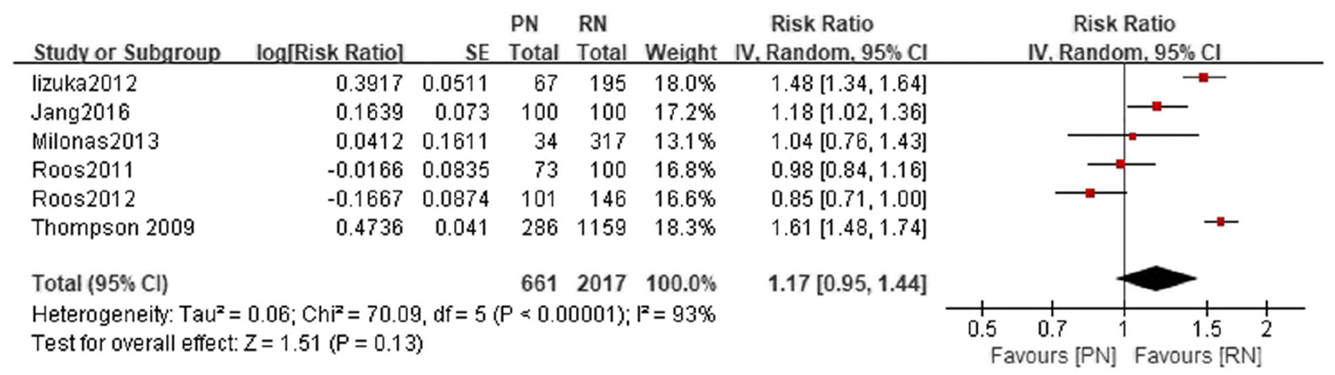
Adapted from Jiang 2019
Disease-free survival
Jiang (2019) reported the recurrence-free survival after 5- and 10-years. No significant difference in recurrence-free survival was found between patients undergoing partial nephrectomy and radical nephrectomy at 5-years (RR 0.99, 95% CI 0.98 to 1.01, p=0.20) (Figure 2.1). At 10-years, the recurrence-free survival was similar for patients who underwent partial nephrectomy and radical nephrectomy (RR 1.00, 95% CI 0.91 to 1.10) (Figure 2.2).
Figure 2.1 5-year recurrence-free survival, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
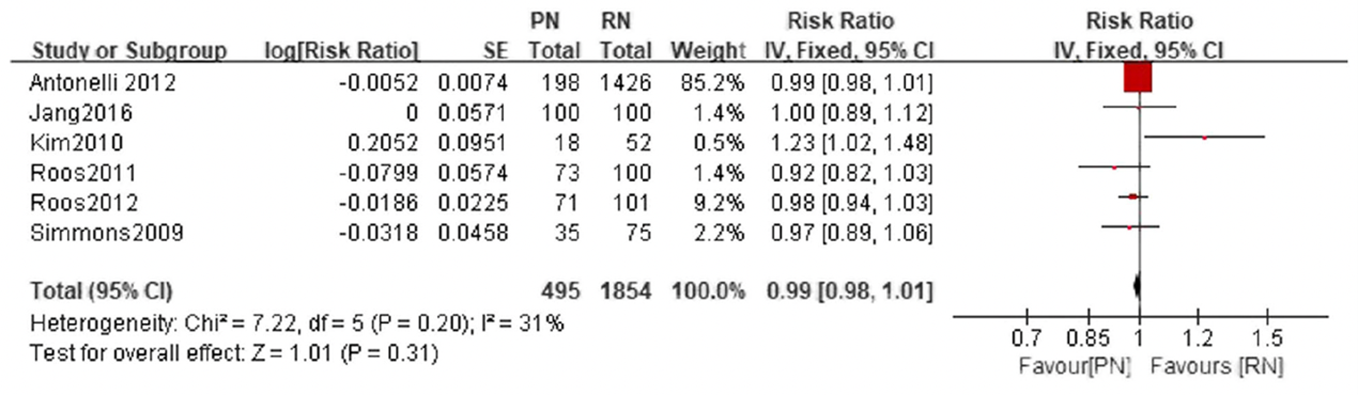
Adapted from Jiang 2019
Figure 2.2 10-year recurrence-free survival, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
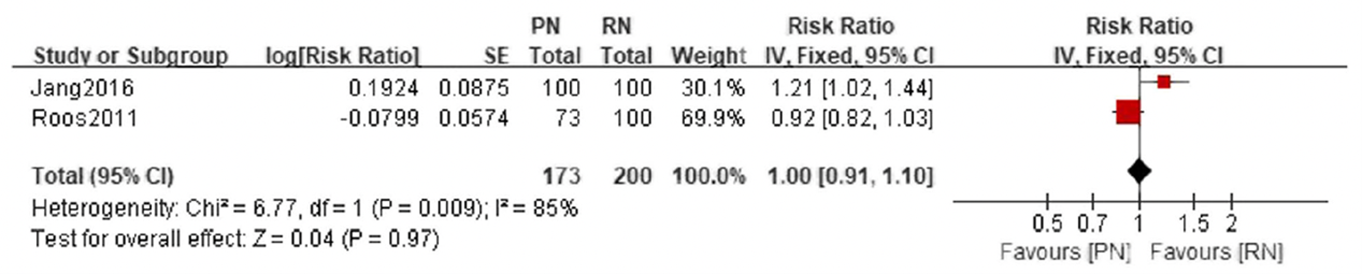
Adapted from Jiang 2019
Time to recurrence
Not reported.
Complications
Jiang (2019) reported post-operative complications. No difference in complications were found between patients who underwent partial nephrectomy and radical nephrectomy (OR 1.45, 95% CI 0.95 to 2.21) (Figure 3).
Figure 3 Postoperative complications, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
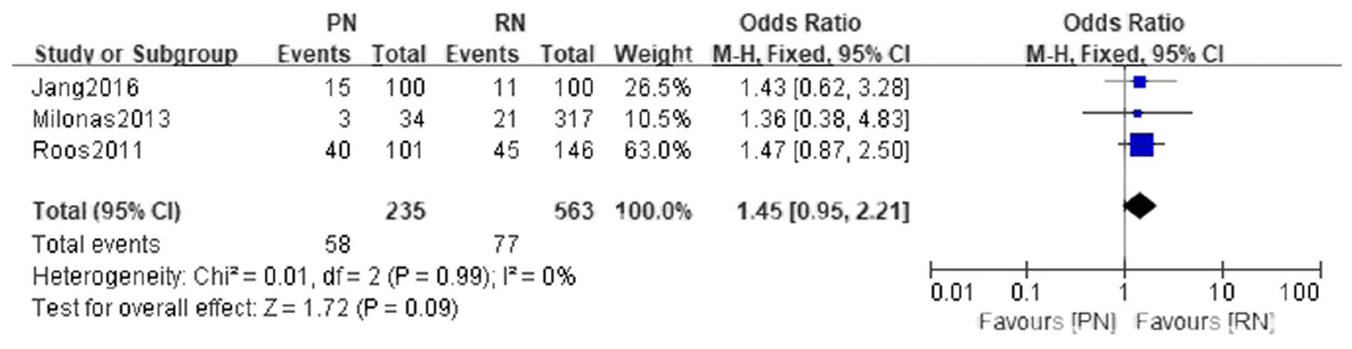
Adapted from Jiang 2019
Quality of life
Not reported.
Renal function
Jiang (2019) reported declined eGFR. A significant difference in declined eGFR was found between patients who underwent partial nephrectomy and radical nephrectomy (MD-11.21, 95% CI -10.30 to -7.99) (Figure 4).
Figure 4 Declined eGFR, comparison between partial nephrectomy (PN) and radical nephrectomy (RN)
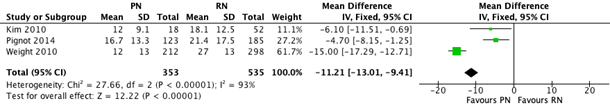
Level of evidence of the literature
According to GRADE, systematic reviews of observational studies and observational studies start at a low level of evidence.
The level of evidence regarding the outcome measure survival was downgraded to GRADE very low, one level for risk of bias and one level because of inconsistency.
The level of evidence regarding the outcome measure disease-free survival was downgraded to GRADE very low, one level because of risk of bias.
The level of evidence regarding the outcome measure time to recurrence could not be assessed with GRADE as this outcome measure was not studied in the included study.
The level of evidence regarding the outcome measure complications was downgraded to GRADE very low, one level for risk of bias and one level for imprecision.
The level of evidence regarding the outcome measure quality of life could not be assessed with GRADE as this outcome measure was not studied in the included study.
The level of evidence regarding the outcome measure renal function was downgraded to GRADE very low, one level for risk of bias, one level for inconsistency, and one level for imprecision.
Percutaneous ablative techniques vs (partial) nephrectomy
Description of studies
Chan (2022) performed a systematic review and meta-analysis to compare oncological outcomes in patients undergoing percutaneous ablative therapies (AT) or partial nephrectomy (PN) for T1a or T1b small renal masses. Medline, EMBASE, Cochrane CENTRAL and conference proceedings were search on 15th July 2020. No date limit was applied and only articles in English or those containing an English abstract were included. All randomized controlled trials or observational studies comparing the use of AT and PN in patients with T1a or T1b small renal masses that report the outcome of interest including survival outcomes and peri-operative outcomes were included. Exclusion criteria were studies only focusing on solitary kidneys, bilateral tumors, patients with inherited RCC syndromes or studies focusing on T1 solely without stratifying results into T1a and T1b. Besides, letters, editorials, single-arm studies, pediatric studies, and non-human studies were excluded. For T1b, eight retrospective cohort studies were included. Meta-analyses were presented for overall complications, minor complications, and major complications in T1b patients.
Results
Survival
In the study of Chan (2022), six studies reported the overall survival. Most studies found overall survival to be similar in both groups, but one found worse in ablative therapy patients.
Disease-free survival
In the study of Chan (2022), two studies reported contradicting results regarding the disease-free survival.
Time to recurrence
Not reported.
Complications
Chan (2022) reported overall, minor (Clavien Dindo Grade ≤2) and major (Clavien Dindo Grade ≥3) post-operative complications. Similar overall, minor, and major complication rates among ablative therapy and partial nephrectomy patients were found (RR =0.97, 95% CI 0.63 to 1.50, p = 0.91, Figure 5.1 and 5.2; RR = 0.96, 95% CI 0.57 to 1.61, p = 0.87, Figure 6.1 and 6.2; RR = 0.69, 95% CI 0.33 to 1.44, p = 0.28, Figure 7.1 and 7.2).
Figure 5.1 Overall complications in T1b patients by approach
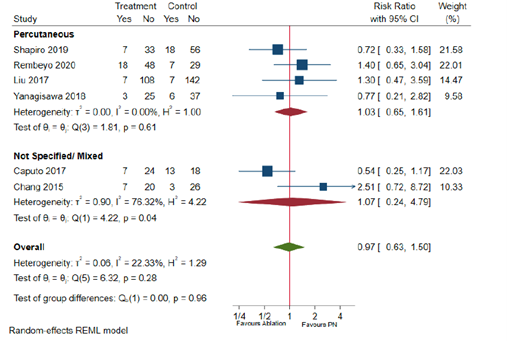
Adapted from Chan 2022
Figure 5.2 Overall complications in T1b patients by energy source
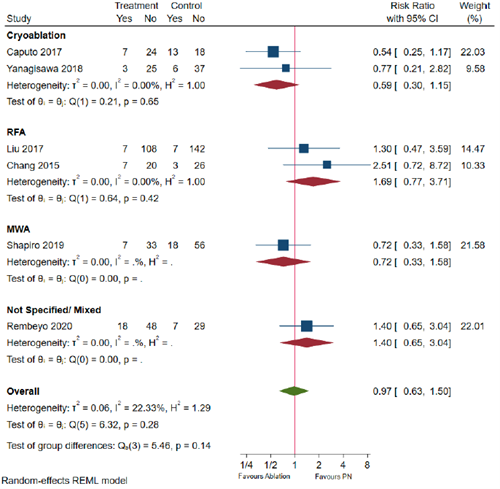
Adapted from Chan 2022, RFA=radiofrequency ablation; MWA= microwave ablation
Figure 6.1 Minor complications (Clavien Dindo Grade ≤2) in T1b patients by approach
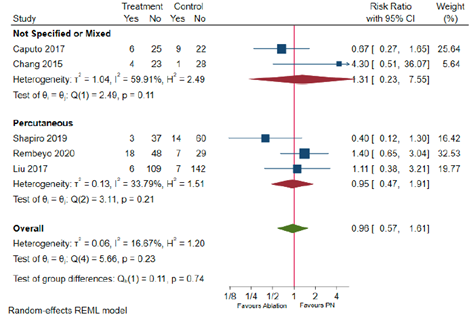
Adapted from Chan
Figure 6.2 Minor complications (Clavien Dindo Grade ≤2) in T1b patients by energy source
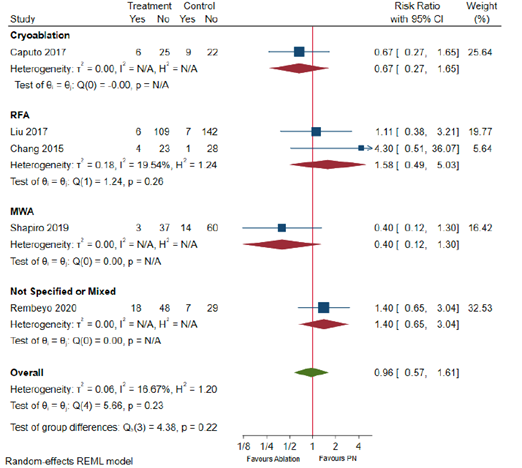
Adapted from Chan 2022, RFA=radiofrequency ablation; MWA= microwave ablation
Figure 7.1 Major complications (Clavien Dindo Grade ≥3) in T1b patients by approach
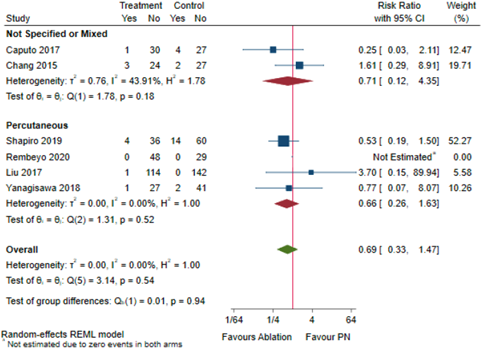
Adapted from Chan
Figure 7.2 Major complications (Clavien Dindo Grade ≥3) in T1b patients by energy source
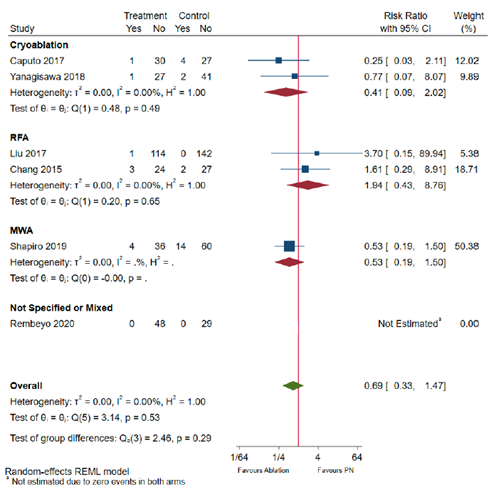
Adapted from Chan 2022, RFA=radiofrequency ablation; MWA= microwave ablation
Quality of life
Not reported.
Renal function
In the study of Chan (2022), four studies reported contradicting results about the change in renal function post-operatively.
Level of evidence of the literature
According to GRADE, systematic reviews of observational studies start at a low level of evidence.
The level of evidence regarding the outcome measure survival was downgraded to GRADE very low by one level for risk of bias.
The level of evidence regarding the outcome measure disease-free survival was downgraded to GRADE very low by one level for risk of bias.
The level of evidence regarding the outcome measure time to recurrence could not be assessed with GRADE as this outcome measure was not studied in the included study.
The level of evidence regarding the outcome measure complications was downgraded to GRADE very low by one level for risk of bias and two levels for imprecision.
The level of evidence regarding the outcome measure quality of life could not be assessed with GRADE as this outcome measure was not studied in the included study.
The level of evidence regarding the outcome measure renal function was downgraded to GRADE very low by one level for risk of bias.
A systematic review of the literature was performed to answer the following question:
What are the (un)favorable effects of partial nephrectomy, total nephrectomy, SABR, percutaneous ablation in patients with non-metastatic renal cell carcinoma between 4-7 cm (T1b)?
PICO 1a: partial vs radical nephrectomy
| P: |
Patients with a cT1b non-metastatic renal cell carcinoma |
| I: |
Partial nephrectomy |
| C: |
Radical nephrectomy |
| O: |
Survival, disease-free survival, time to recurrence, complications, quality of life, renal function |
PICO 1b: (Percutaneous) ablative techniques vs (partial) nephrectomy
| P: |
Patients with a cT1b non-metastatic renal cell carcinoma |
| I: |
Percutaneous treatment or SABR (stereotactic ablative body radiotherapy) |
| C: |
Partial or radical nephrectomy |
| O: |
Survival, disease-free survival, time to recurrence, complications, quality of life, renal function |
Relevant outcome measures
The guideline development group considered survival and disease-free survival as critical outcome measures for decision making; and time to recurrence, complications, quality of life and renal function as important outcome measures for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The GRADE-standard limit of 25% difference for dichotomous outcomes (RR < 0.8 or > 1.25) and 0.5 SD for continuous outcomes was taken as minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2000 until February, 10th 2022. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 106 hits. Studies were selected based on the following criteria:
- The study population had to meet the criteria as defined in the PICOs
- The intervention had to be as defined in the PICOs
- Research type: systematic review or randomized-controlled trial
- Articles written in English or Dutch
Twenty-nine studies were initially selected based on title and abstract screening. After reading the full text, 25 studies were excluded (see the table with reasons for exclusion under the tab Methods), and four studies were included (three studies for PICO 1a and one study for PICO 1b).
PICO 1a: partial vs radical nephrectomy
Results
One systematic review and two observational studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
PICO 1b: Percutaneous ablative techniques vs (partial) nephrectomy
Results
One systematic review was included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- 1 - Buse S, Hach CE, Klumpen P, Schmitz K, Mager R, Mottrie A, Haferkamp A. Cost‐effectiveness analysis of robot‐assisted vs. open partial nephrectomy. The International Journal of Medical Robotics and Computer Assisted Surgery. 2018 Aug;14(4):e1920.
- 2 - Chan VW, Abul A, Osman FH, Ng HH, Wang K, Yuan Y, Cartledge J, Wah TM. Ablative therapies versus partial nephrectomy for small renal masses - A systematic review and meta-analysis. Int J Surg. 2022 Jan;97:106194.
- 3 - Chong JT, Paulucci D, Lubin M, Beksac AT, Gin G, Sfakianos JP, Badani KK. Comparison of overall survival and unplanned hospital readmissions between partial and radical nephrectomy for cT1a and cT1b renal masses. Ther Adv Urol. 2018 Nov 9;10(12):383-391.
- 4 - Huang RS, Chow R, Benour A, Chen D, Boldt G, Wallis CJ, Swaminath A, Simone CB, Lock M, Raman S. Comparative efficacy and safety of ablative therapies in the management of primary localised renal cell carcinoma: a systematic review and meta-analysis. The Lancet Oncology. 2025 Feb 5.
- 5 - Jiang YL, Peng CX, Wang HZ, Qian LJ. Comparison of the long-term follow-up and perioperative outcomes of partial nephrectomy and radical nephrectomy for 4 cm to 7 cm renal cell carcinoma: a systematic review and meta-analysis. BMC Urol. 2019 Jun 7;19(1):48.
- 6 - Kumar A, Straka C, Courtney PT, Vitzthum L, Riviere P, Murphy JD. Cost-Effectiveness Analysis of Stereotactic Ablative Radiation Therapy in Patients With Oligometastatic Cancer. Int J Radiat Oncol Biol Phys. 2021 Apr 1;109(5):1185-1194. doi: 10.1016/j.ijrobp.2020.09.045. Epub 2020 Sep 28. PMID: 33002541.
- 7 - Rich BJ, Noy MA, Dal Pra A. Stereotactic body radiotherapy for localized kidney cancer. Current urology reports. 2022 Dec;23(12):371-81.
- 8 - Siva S, Correa RJM, Warner A, Staehler M, Ellis RJ, Ponsky L, Kaplan ID, Mahadevan A, Chu W, Gandhidasan S, Swaminath A, Onishi H, Teh BS, Lo SS, Muacevic A, Louie AV. Stereotactic Ablative Radiotherapy for ≥T1b Primary Renal Cell Carcinoma: A Report From the International Radiosurgery Oncology Consortium for Kidney (IROCK). Int J Radiat Oncol Biol Phys. 2020 Nov 15;108(4):941-949.
- 9 - Siva S, Ali M, Correa RJM, et al. 5-year outcomes after stereotactic ablative body radiotherapy for primary renal cell carcinoma: an individual patient data meta-analysis from IROCK (the International Radiosurgery Consortium of the Kidney). Lancet Oncol. 2022 Dec;23(12):1508-1516.
- 10 - Venkatramani V, Koru-Sengul T, Miao F, Nahar B, Prakash NS, Swain S, Punnen S, Ritch C, Gonzalgo M, Parekh D. A comparison of overall survival and perioperative outcomes between partial and radical nephrectomy for cT1b and cT2 renal cell carcinoma-Analysis of a national cancer registry. Urol Oncol. 2018 Mar;36(3):90.e9-90.e14.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: What are the (un)favorable effects of partial nephrectomy, total nephrectomy. SABR, percutaneous ablation in patients with non-metastatic renal cell carcinoma between 4-7cm?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Jiang, 2019 PICO1a
[individual study characteristics deduced from [Jiang, 2019]]
PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of retrospective cohort studies
Literature search up to March 2018
A: Kim, 2012 B: Badalato, 2011 C: Jang, 2016 D: Iizuka, 2012 E: Roos, 2011 F: Roos, 2012 G: Crepel, 2010 H: Milonas, 2013 I: Thompson, 2009 J: Pignot, 2014 K: Antonelli, 2012 L: Meskawi, 2013 M: Weight, 2010 N: Simmons, 2009 O: Robert, 2006 P: Patard, 2004
Study design: Retrospective cohort
Setting and Country: Not mentioned
Source of funding and conflicts of interest: Not mentioned for individual studies
|
Inclusion criteria SR: - comparative partial nephrectomy or nephron-sparing surgery and radical nephrectomy for the treatment of 4-7 cm renal tumors - evaluation of at least one oncological result such as recurrence-free survival, cancer-special survival, and overall survival
Exclusion criteria SR: - case reports, reviews, and articles without applicable data - studies that included both T1b and T2 or renal tumors larger than 7 cm - studies that were not comparative in nature
16 studies included
Important patient characteristics at baseline:
N, mean age A: 18 patients, 47.3 yrs vs 52 patients, 57.3 yrs B: 1047 patients, 58.4 yrs vs 10,209 patients, 60.7 yrs C: 100 patients, 55.3 yrs vs 100 patients, 55.7 yrs D: 67 patients, 57.6 yrs vs 195 patients, 58.1 yrs E: 73 patients, 60.4 yrs, 100 patients, 61.1 yrs F: 85 patients vs 118 patients (age unknown) G: 275 patients, 60.5 yrs vs 1100 patients, 60.5 yrs H: 34 patients, 62.2 yrs vs 317 patients, 63.4 yrs I: 286 patients vs 873 patients (age unknown) J: 123 patients, 57.6 yrs vs 185 patients, 61.6 yrs K: 198 patients, 58.2 yrs vs 1426 patients, 62.4 yrs L: 1526 patients, 60.3 yrs vs 6104 patients, 60.6 yrs M: 212 patients, 49 yrs vs 298 patients, 41 yrs N: 35 patients, 63.5 yrs vs 75 patients, 63.4 yrs O: 33 patients, 68.9 yrs vs 66 patients, 66.9 yrs P: 64 patients vs 576 patients (age unknown)
Sex: A: 72.2% male vs 69.2% male B: 35.4% male vs 59.2% male C: 71% male in both groups D: 76.1% male vs 61.0% male E: 90.4% male vs 38% male F: 65.9% male vs 73.7% male G: 63.6% male vs 60.6% male H: 44.1% male vs 51.7% male I: 68.5% male vs 61.6% male J: 65.0% male vs 68.7% male K: 67.7% male vs 63.3% male L: 67.7% male vs 67.8% male M: 65.6% male vs 59.1% male N: 74.3% male vs 52.0% male O: 78.8% male vs 66.7% male P: NA
Pathologic tumor size (cm): A: 5.0 vs 5.5 B: 4.86 vs 5.27 C: 4.9 vs 4.9 D: 4.9 vs 5.3 E: 5.0 vs 5.5 F: NA G: NA H: 4.67 vs 5.25 I: NA J: 5.2 vs 5.5 K: 5.0 vs 5.7 L: 5.14 vs 5.15 M: 4.8 vs 5.6 N: 4.6 vs 5.3 O: 5.2 vs 5.2 P: 5.3 vs 5.6
Unknown if groups were comparable at baseline
|
Describe intervention:
A: partial nephrectomy B: partial nephrectomy C: partial nephrectomy D: partial nephrectomy E: partial nephrectomy F: partial nephrectomy G: partial nephrectomy H: partial nephrectomy I: partial nephrectomy J: partial nephrectomy K: partial nephrectomy L: partial nephrectomy M: partial nephrectomy N: partial nephrectomy O: partial nephrectomy P: partial nephrectomy
|
Describe control:
A: radical nephrectomy B: radical nephrectomy C: radical nephrectomy D: radical nephrectomy E: radical nephrectomy F: radical nephrectomy G: radical nephrectomy H: radical nephrectomy I: radical nephrectomy J: radical nephrectomy K: radical nephrectomy L: radical nephrectomy M: radical nephrectomy N: radical nephrectomy O: radical nephrectomy P: radical nephrectomy
|
End-point of follow-up
A: 78.2 vs 66.5 months B: 120 months C: 48.1 vs 42.6 months D: 31.3 vs 93.0 months E: 55.2 vs 78 months F: 120 months G: 40.7 vs 46.7 months H: 168 months I: 57.6 months J: 39.5 vs 46.9 months K: 120 months L: 60 vs 120 months M: 49 vs 41 months N: NA O: 34.0 vs 48.5 months P: 120 months
For how many participants were no complete outcome data available? Not reported
|
Outcome measure-1: 5-year and 10-year overall survival
5-year overall survival Effect measure: RR (95% CI): A: 1.07 (0.92 to 1.24) B: 0.97 (0.94 to 1.00) C: 1.14 (1.07 to 1.22) D: 1.15 (1.08 to 1.22) E: 0.97 (0.85 to 1.11) F: 0.98 (0.87 to 1.10) H: 1.16 (0.97 to 1.37) N: 1.03 (0.81 to 1.31)
Pooled effect (fixed effects model): 1.02 [95% CI 1.00 to 1.05] favoring radical nephrectomy Heterogeneity (I2): 84%
10-year overall survival Effect measure: RR (95% CI): C: 1.18 (1.02 to 1.36) D: 1.48 (1.34 to 1.64) E: 0.98 (0.84 to 1.16) F: 0.85 (0.71 to 1.00) G: 1.61 (1.48 to 1.74) H: 1.04 (0.76 to 1.43)
Pooled effect (random effects model): 1.17 [95% CI 0.95 to 1.44] favoring radical nephrectomy Heterogeneity (I2): 93%
Outcome measure-2: 5-year and 10-year cancer-special survival 5-year overall cancer-special survival Effect measure: RR (95% CI): A: 1.00 (0.88 to 1.14) E: 0.97 (0.91 to 1.04) F: 0.98 (0.87 to 1.10) H: 1.20 (1.11 to 1.30) K: 0.97 (0.92 to 1.02) L: 1.02 (1.01 to 1.03) M: 1.04 (1.01 to 1.07) N: 1.07 (0.84 to 1.38) O: 0.98 (0.92 to 1.05)
Pooled effect (fixed effects model): 1.02 [95% CI 1.01 to 1.03] favoring radical nephrectomy Heterogeneity (I2): 68%
10-year overall cancer-special survival Effect measure: RR (95% CI): C: 1.02 (0.93 to 1.11) E: 0.95 (0.87 to 1.04) F: 0.95 (0.88 to 1.03) H: 1.04 (0.87 to 1.25) I: 1.12 (1.04 to 1.20) K: 1.03 (0.98 to 1.09) L: 1.05 (1.03 to 1.06)
Pooled effect (fixed effects model): 1.04 [95% CI 1.03 to 1.06] favoring radical nephrectomy Heterogeneity (I2): 57%
Outcome measure-3: 5-year and 10-year recurrence-free survival 5-year recurrence-free survival Effect measure: RR (95% CI): A: 1.23 (1.02 to 1.48) C: 1.00 (0.89 to 1.12) E: 0.92 (0.82 to 1.03) F: 0.98 (0.94 to 1.03) K: 0.99 (0.98 to 1.01) N: 0.97 (0.89 to 1.06)
Pooled effect (fixed effects model): 0.99 [95% CI 0.98 to 1.01] favoring partial nephrectomy Heterogeneity (I2): 31%
10-year recurrence-free survival Effect measure: RR (95% CI): C: 1.21 (1.02 to 1.44) E: 0.92 (0.82 to 1.03)
Pooled effect (fixed effects model): 1.00 [95% CI 0.91 to 1.10] (no effect) Heterogeneity (I2): 85%
Outcome measure-4: post-operative complications Effect measure: OR (95% CI): C: 1.43 (0.62 to 3.28) E: 1.47 (0.87 to 2.50) H: 1.36 (0.38 to 4.83)
Pooled effect (fixed effects model): 1.45 [95% CI 0.95 to 2.21] favoring radical nephrectomy Heterogeneity (I2): 0%
Outcome measure-5: declined eGFR Effect measure: mean difference (95% CI): A: -6.10 (-11.51 to -0.69) J: -4.70 (-8.15 to -1.25) M: -15.00 (-17.29 to -12.71)
Pooled effect (fixed effects model): -11.21 [95% CI -13.01 to -9.41] favoring partial nephrectomy Heterogeneity (I2): 93% |
Brief description of author’s conclusion - PN may provide comparable outcomes in terms of recurrence-free survival and overall survival, and better renal function preservation. cancer-special survival compared to PN. - PN had an equal incident of postoperative complications compared to RN.
Personal remarks on study quality, conclusions, and other issues (potentially) relevant to the research question - Only included non-RCTs - LnRR was used instead of LnHR for overall survival, cancer-special survival, and recurrence-free survival - Wrong study included in forest plot for declined eGFR - High levels of heterogeneity because of bias
Level of evidence: GRADE (per comparison and outcome measure) including reasons for down/upgrading Jiang 2019 used the GRADE approach for evidence grading. For all the outcomes, a moderate quality of evidence was found but no explanation was provided.
Sensitivity analyses: Jiang 2019 sequentially omitted a single study one by one to determine which studies contributed the most to the heterogeneity of the results.
Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroup analysis) The selection bias present in the included studies with regards to the tumor pathology (clear-cell carcinoma vs non-clear cell carcinoma) may account for the higher heterogeneity of the 10-year overall survival outcome.
After sensitivity analysis and meta-regression, no explicit causes of heterogeneity have been detected. |
|
Chan, 2022 PICO 1b
[individual study characteristics deduced from [Chang, 2022]]
PS., study characteristics and results are extracted from the SR (unless stated otherwise)
|
SR and meta-analysis of retrospective cohort studies
Literature search up to June 2020
Only studies about T1b described
A: Andrews, 2019 B: Caputo, 2017 C: Shapiro, 2019 D: Rembeyo 2020 E: Liu, 2017 F: Pecoraro, 2019 G: Yanagisawa, 2018 H: Chang, 2015
Study design: Retrospective cohort
Setting and Country: A: USA B: USA C: USA D: France E: China F: Canada G: Japan H: China
Source of funding and conflicts of interest: A: None declared B: 1 author received consultancy fees from a relevant company C: 5 authors are consultants, 1 author received prior grant funding. No external funding D: None declared E: Funding received from National Natural Science Foundation of China F: None declared G: Not reported H: Not reported
|
Inclusion criteria SR: - Studies comparing the use of ablative therapies and partial nephrectomy in patients with T1a or T1b small renal masses - All randomized controlled trials or observational studies - Only studies reporting the outcome of interest including survival outcomes and peri-operative outcomes
Exclusion criteria SR: - Studies solely focusing on solitary kidneys, bilateral tumors, or patients with inherited RCC syndromes - Studies focusing on T1 solely without stratifying results into T1a and T1b - Letters, editorials, single-arm studies, pediatric studies, and non-human studies
8 studies included
Important patient characteristics at baseline: Average age (years) A: Median [IQR] PN: 61 [52-70] CYRO: 77 [69.5-83] B: Median [IQR] Unmatched: CYRO: 68 (64-76) PN: 61 (52-68) Matched: CYRO: 68 (64-76) PN: 68 (64-76) C: Median [IQR] MWA: 69 [65-77] PN: 58 [51-65] D: Median [Range] CYRO: 72 [60.0-80.0] RFA: 84 [76.0-86.0] PN: 60 [54.8-66.0] E: Median [Range] Clear-cell (cc) RCC PRFA: 68 [35-85] PN: 58.5 [23-83] Non clear-cell (ncc) RCC PRFA: 65.5 [33-84] PN: 55 [24-84] F: Median CYRO: 71 PN: 61 G: NR (Patients in the CYRO group had significantly higher age) H: Mean [SD] RFA: 64.0 [8.4] PN: 56.9 [9.9]
Average tumour size (cm) A: Median [IQR] PN: 5.0 [4.5-5.5] CYRO: 4.8 [4.4-5.6] B: Median [IQR] Unmatched CYRO: 4.3 [4.2-4.7] PN: 5.0 [4.5-5.6] Matched CYRO: 4.3 (4.2-4.7) PN: 4.6 (4.3-4.9) C: Median [IQR] MWA: 4.4 [4.1-5] PN: 4.7 [4.1-5.3] D: Median [Range] CYRO: 4.6 (4.1-5.4) RFA: 4.2 (4.0-4.5) PN: 4.5 (4.0-5.45) E: Median [Range] ccRCC PRFA: 5.5 [4.3-7] PN: 5.8 [4.2-7] nccRCC PRFA: 5.5 [4.4-7] PN: 5.5 [4.2-7] F: Median CYRO: 4.69 PN: 5.10 G: Mean CYRO: 4.55 PN: 4.59 H: Mean [SD] RFA: 4.7 [0.5] PN: 5.2 [0.6]
Groups were not comparable at baseline.
|
Describe intervention:
A: Percutaneous cryoablation B: Laparoscopic or percutaneous cryoablation C: Percutaneous microwave partial nephrectomy D: Percutaneous cryoablation or radiofrequency ablation E: Percutaneous radiofrequency ablation F: Cryoablation G: Percutaneous cryoablation H: Radiofrequency ablation
|
Describe control:
A: Partial nephrectomy B: Robot-assisted partial nephrectomy C: Non-specified partial nephrectomy D: Robot-assisted partial nephrectomy E: Open or laparoscopic partial nephrectomy F: Partial nephrectomy G: Partial nephrectomy H: Partial nephrectomy |
End-point of follow-up
A: Median [IQR] PN: 8.7 [6.9-11.3] years CYRO: 6.0 [4.0-7.2] years B: Median [IQR] PN: 13.0 [3.19-19.2] months CYRO: 30.1 [13.2-64.0] months C: Median [IQR] MW: 33.9 [21.7-61.2] months PN: 35.1 [9.5-89] months D: Median [Range] CA: 19.9 (15.5-27.2) months RFA: 51.3 (31.1-56.5) months PN: 23.7 (15.5-32.2) months E: Median [Range] Full cohort: 78 [8-132] months F: Median: 38 months G: Median CRYO: 22 months PN: 17 months H: Mean [SD] RFA: 65.9 [17.9] PN: 70.2 [11.7]
For how many participants were no complete outcome data available? Not reported
|
Outcome measure-1: Overall complications Rates of overall complications in T1b patients by approach
Percutaneous Effect measure: RR (95% CI): C: 0.72 (0.33 to 1.58) D: 1.40 (0.65 to 3.04) E: 1.30 (0.47 to 3.59) G: 0.77 (0.21 to 2.82)
Not Specified/Mixed B: 0.54 (0.25 to 1.17) H: 2.51 (0.72 to 8.72)
Pooled effect (random effects model): 0.97 [95% CI 0.63 to 1.50] favoring ablation Heterogeneity (I2): 22.33%
Rates of overall complications in T1b patients by energy source
Cryoablation B: 0.54 (0.25 to 1.17) G: 0.77 (0.21 to 2.82)
RFA E: 1.30 (0.47 to 3.59) H: 2.51 (0.72 to 8.72)
MWA C: 0.72 (0.33 to 1.58)
Not Specified/Mixed D: 1.40 (0.65 to 3.04) Pooled effect (random effects model): 0.97 [95% CI 0.63 to 1.50] favoring ablation Heterogeneity (I2): 22.33%
Outcome measure-2: Minor complications Rates of minor complications in T1b patients by approach
Not specified or mixed B: 0.67 (0.27 to 1.65) H: 4.30 (0.51 to 36.07)
Percutaneous C: 0.40 (0.12 to 1.30) D: 1.40 (0.65 to 3.04) E: 1.11 (0.38 to 3.21)
Pooled effect (random effects model): 0.96 [95% CI 0.57 to 1.61] favoring ablation Heterogeneity (I2): 16.67%
Rates of minor complications in T1b patients by energy source
Cryoablation B: 0.67 (0.27 to 1.65)
RFA E: 1.11 (0.38 to 3.21) H: 4.30 (0.51 to 36.07)
MWA C: 0.40 (0.12 to 1.30) Not specified or mixed D: 1.40 (0.65 to 3.04)
Pooled effect (random effects model): 0.96 [95% CI 0.57 to 1.61] favoring ablation Heterogeneity (I2): 16.67%
Outcome measure-3: Rates of major complications in T1b patients by approach Not specified or mixed B: 0.25 (0.03 to 2.11) H: 1.61 (0.29 to 8.91)
Percutaneous C: 0.53 (0.19 to 1.50) D: Not estimated E: 3.70 (0.15 to 89.94) G: 0.77 (0.07 to 8.07)
Pooled effect (random effects model): 0.69 [95% CI 0.33 to 1.47] favoring ablation Heterogeneity (I2): 0%
Rates of major complications in T1b patients by energy source Cryoablation B: 0.25 (0.03 to 2.11) G: 0.77 (0.07 to 8.07)
RFA E: 3.70 (0.15 to 89.94) H: 1.61 (0.29 to 8.91)
MWA C: 0.53 (0.19 to 1.50)
Not specified or mixed D: Not estimated
Pooled effect (random effects model): 0.69 [95% CI 0.33 to 1.47] favoring ablation Heterogeneity (I2): 0%
Outcome measure-4: Oncological outcomes These single-centre studies display contradicting results, and it is important to note the potential for operator bias, leading to significant difference in oncological outcomes
Outcome measure-5: Change in eGFR post-operatively In T1b disease, four studies investigated change in eGFR pre- and post-operatively: two found the change to be similar while two found mixed approaches of RFA to have a significantly smaller drop in eGFR compared to PN |
Brief description of author’s conclusion AT have similar long-term oncological durability; lower rates of complications and superior kidney function preservation compared to PN. Given the low quality of evidence, AT is a reasonable alternative to PN in frail and co-morbid patients. Long-term high-quality studies are needed to confirm the potential benefits of AT, especially in T1b patients.
Personal remarks on study quality, conclusions, and other issues (potentially) relevant to the research question - Study of Chang 2015 included in forest plot, but not explained in characteristics table - High risk of bias and low confidence, especially confounding and selection bias of included patients. Tend to favor the control group
Level of evidence: GRADE (per comparison and outcome measure) including reasons for down/upgrading Certainty of evidence was assessed with GRADE. A very low GRADE was found for all outcomes: - Cancer-specific survival - Overall survival - Metastatic-Free survival - Disease-Free survival - Overall post-operative complications - Minor post-operative complications - Major post-operative complications - Change in renal function post-operatively
Sensitivity analyses: Planned sensitivity analyses were performed based on the RoB assessment, using studies with propensity-matched analyses or with a minimum follow-up time of 5-years. Sensitivity analyses were also performed on large population-based studies which may have a dominating effect on the outcome.
Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroup analysis) Planned subgroup analyses of different energy sources and approaches of AT were performed to identify potential sources of heterogeneity to inform clinical practice
|
Evidence table for intervention studies
Research question: What are the (un)favorable effects of partial nephrectomy, total nephrectomy. SABR, percutaneous ablation in patients with non-metastatic renal cell carcinoma between 4-7cm?
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Chong, 2018 |
Type of study: Retrospective cohort study
Setting and country: The American College of Surgeons’ National Cancer Database (NCDB) was applied from 2004 to 2013
Funding and conflicts of interest: This research received no specific grant from any funding agency in the public, commercial, or not-for-profit sectors. No conflicts of interest were reported.
|
Inclusion criteria: Patients with renal cancer who underwent partial nephrectomy or radical nephrectomy as definitive treatment from 2004 to 2013
Exclusion criteria: - Patients with clinical T2-4, N1, or M1 renal cell carcinoma - Patients with missing clinical stage data - Patients with renal tumors excised bilaterally or a horseshoe kidney - Patients receiving additional treatments - Patients with concurrent or prior cancer diagnosis
N total at baseline: Intervention: 12,656 Control: 4419
Important prognostic factors2: Age ± SD: I: 62.1 (11.3) C: 60.7 (10.6) p <0.001
Sex: I: 59.2% M C: 65.8% M p <0.001
Groups not comparable at baseline |
Describe control (treatment/procedure/test): Radical nephrectomy (RN) |
Describe intervention (treatment/procedure/test): Partial nephrectomy (PN)
|
Length of follow-up: Median follow up was 44.5 months (IQR 25.7 to 68.1 months)
Loss-to-follow-up: Not reported.
Incomplete outcome data: A complete case analysis was conducted and patients with missing data on baseline characteristics, survival, or readmission were excluded.
|
Outcome measures and effect size (include 95%CI and p-value if available):
Overall survival Unadjusted analysis:
IPTW-adjusted Cox proportional hazards regression: PN associated with improved overall survival (HR = 0.89, 95% CI 0.82 to 0.99, p=0.025)
Sandwich-type variance estimator: HR = 0.89, 95% CI 0.79 to 1.02, p =0.106
5-year IPTW-KM: 85.3% for PN 84.3% for RN
10-year IPTW-KM: 70.8% for PN 63.6% for RN |
Author’s conclusion PN compared with RN was associated with a modest survival benefit for patients with a cT1b renal mass. PN should be offered over RN when feasible despite a marginal increase in unplanned hospital readmissions for PN of cT1b tumors.
Remarks: Sensitivity analyses for pre-2012 and adjusting for all covariates |
|
Venkatramani, 2018 |
Type of study: Retrospective cohort study
Setting and country: National Cancer Data Base (NCDB) from US between 2004 and 2013
Funding and conflicts of interest: Not reported. |
Inclusion criteria: - Patients diagnosed with renal cell carcinoma - Clinical stage cT1b-T2N0M0
Exclusion criteria: - Patients diagnosed at death or autopsy - Missing or unknown data for clinical TNM stage
N total at baseline: 1:1 propensity score matching (for T1b) Intervention: 5,534 Control: 5,534
Important prognostic factors2: Not specified for T1b patients
Unknown if groups were comparable at baseline |
Describe intervention (treatment/procedure/test): Partial nephrectomy (PN)
|
Describe control (treatment/procedure/test): Radical nephrectomy (RN)
|
Length of follow-up: Median follow-up was 35.6 months for PN and 45.1 months for RN
Loss-to-follow-up: Not reported.
Incomplete outcome data: No missing data.
|
Outcome measures and effect size (include 95%CI and p-value if available):
Overall survival Multivariate Cox proportional hazard model: HR = 0.81 (0.73 to 0.90) favouring partial nephrectomy (p<0.001)
|
Author’s conclusion PN was associated with a significantly better overall survival than RN for cT1b.
Remarks: Numbers in text and tables do not match
|
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Jiang, 2019 PICO 1a |
No. Only a study aim was mentioned and inclusion criteria not much specified. |
Yes. Search period and search terms described and searched in PubMed, Embase and Cochrane Central Register. |
No. Exclusion reason are mentioned but not specified for each individual study. |
Yes. Age, sex, and pathologic tumor size were described per individual article. |
No. Only individual studies did a multivariate analysis or propensity score matching to eliminate any potential confounding factors.
|
Yes. Newcastle-Ottowa Scale for risk of bias assessment and GRADE for determining the quality of the evidence.
|
Unclear. Statistical heterogeneity is assessed (and was high for most outcomes) but clinical heterogeneity is not assessed. |
Yes. Funnel plots were made. |
No. Conflicts of interest not reported for individual studies. |
|
Chan, 2022 PICO 1b |
Yes. PICO described in PROSPERO registration and inclusion criteria were mentioned.
|
Yes. Search period and search strategy were described. Medline and Embase were searched. |
Yes. A list of excluded studies was provided with reasons for exclusion per individual study. |
Yes. Baseline characteristics were described for each individual study. |
No. No multivariate analysis was performed. |
Yes. Risks of biases of observational studies were assessed using the ROBINS-I tool. |
Unclear. Statistical heterogeneity is assessed and subgroup analyses to identify potential sources of heterogeneity to inform clinical practice, but clinical heterogeneity is not assessed.
|
Yes. Funnel plots were made, and Egger’s test was performed. |
Yes. Conflict of interest reported for systematic review and individual studies. |
Risk of bias table for interventions studies (cohort studies based on risk of bias tool by the CLARITY Group at McMaster University)
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population? |
Exposure
Can we be confident in the assessment of exposure? |
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study? |
Confounding-assessment
Can we be confident in the assessment of confounding factors? |
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome? |
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed? |
Co-interventions
Were co-interventions similar between groups? |
Overall Risk of bias |
|
Chong, 2018 |
Probably yes
Reason: Participants were selected from a registry
|
Probably yes
Reason: Received treatment derived from registry data |
Probably yes
Reason: Outcome of interest is overall survival which was derived from registry data
|
Probably yes
Reason: Demographic data presented for subgroup of T1b renal tumors |
Definitely yes
Reason: IPTW (inverse probability of treatment weighting) was employed to account for selection bias and confounding by demographic and clinical covariates |
Probably yes
Reason: Outcome data derived from registry data and no missing data
|
Probably yes
Reason: Follow-up for overall survival seems accurate and outcome data was complete |
No information
Reason: No data available on other interventions besides partial or radial nephrectomy |
Low |
|
Venkatramani, 2018 |
Probably yes
Reason: Participants were selected from a registry
|
Probably yes
Reason: Received treatment derived from registry data
|
Probably yes
Reason: Outcome of interest is overall survival which was derived from registry data
|
Probably no
Reason: Demographic and pathological characteristics described, but not separately for T1b |
Definitely yes
Reason: Authors performed a 1:1 propensity score matching
|
Probably yes
Reason: Outcome data derived from registry data and no missing data
|
Probably yes
Reason: Follow-up for overall survival seems accurate and outcome data was complete |
No information
Reason: No data available on other interventions besides partial or radial nephrectomy
|
Some concerns |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Deng, 2020 |
Robot-assisted partial nephrectomy vs. laparoscopic partial nephrectomy |
|
Mari, 2021 |
Open partial nephrectomy vs. laparoscopic PN vs. robot-assisted PN. Stage=t1a, t1b en t2 |
|
Propiglia, 2016
|
Open partial nephrectomy vs. laparoscopic PN vs. robot-assisted PN |
|
El-Ghazaly, 2014 |
SR with 32 case series about partial neprhectomy. No comparison |
|
Bedke, 2008 |
Reevaluation of the optimal tumor size cutoff point |
|
Bessede, 2015 |
Nephron-sparing surgery, no comparison. |
|
Best, 2017 |
Survey study about current opinions |
|
Eggener, 2015 |
PN with cold ischemia vs. PN with warm ischemia |
|
Ehsanullah, 2021 |
PN supra 12th rib miniflank incision with zero ischemia, no comparison. |
|
Gill, 2007 |
Wrong population. Laparoscopic partial nephrectomy vs. open partial nephrectomy. |
|
Gontero, 2021 |
PN with short life expectancy vs. PN with long life expectancy. |
|
Kumar, 2017 |
Videoabstract |
|
Lane, 2015 |
Potential candidates for PN, no comparison. |
|
Paulucci, 2018 |
Transperitoneal vs. retroperitoneal robotic partial nephrectomy. |
|
Ponsky, 2015 |
No comparison, dose-escalation study. |
|
Reynolds, 2017 |
ct1a vs. ct1b with robotic partial nephrectomy |
|
Salah, 2020 |
Prediciting outcome of PN with nephrometry score |
|
Schiavina, 2015 |
Wrong study design. Patients undergoing NSS, with results compared among different periods. |
|
Serni, 2015 |
Patients treated with simple enucleation, no comparison. |
|
Simone, 2016 |
Trends in the use of PN (European centers). |
|
Zargar, 2016 |
Partial nephrectomy, no comparison. |
|
Ljungberg, 2021 |
Wrong publication type |
|
Van Poppel, 2011 |
Narrative review |
|
Van Poppel, 2013 |
Narrative review |
|
Weight, 2013 |
Wrong publication type |
|
Furukawa, 2020 |
Robot-assisted partial nephrectomy, no comparison. |
|
Mehrazin, 2014 |
Active surveillance vs. delayed surgical intervention, wrong comparison. |
|
Schachter, 2007 |
Wrong outcome (histology). |
|
Takagi, 2015 |
PN with renorrhaphy vs PN without. |
|
Borghesi, 2013 |
Nonsystematic review (narrative) |
|
Zhang, 2021 |
Better SR of Jian 2019 with quality assessment |
|
Badalato, 2012 |
Included in SR of Jian 2019 |
|
Jang, 2016 |
Included in SR of Jian 2019 |
|
Weight, 2010 |
Included in SR of Jian 2019 |
|
Liu, 2017 |
Included in SR of Chan 2022 |
|
Shapiro, 2020 |
Included in SR of Chan 2022 |
|
Cazalas, 2021 |
Included studies with wrong comparisons |
Beoordelingsdatum en geldigheid
Publicatiedatum : 14-04-2026
Beoordeeld op geldigheid : 14-04-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met nierkanker en een vertegenwoordiger namens de patiëntenvereniging.
Werkgroep
- Dr. A. (Axel) Bex, uroloog, Antoni van Leeuwenhoek, Amsterdam, NVU (voorzitter)
- Dr. R.F.M. (Rob) Bevers, uroloog, Leids Universitair Medisch Centrum, Leiden, NVU
- Dr. J.F. (Hans) Langenhuijsen, uroloog, Radoudumc, Nijmegen, NVU
- Dr. A.P. (Paul) Hamberg, internist-oncoloog, Franciscus Gasthuis en Vlietland Ziekenhuis, Rotterdam, NIV/NVMO
- Dr. J.V. (Hans) van Thienen, internist-oncoloog, Antoni van Leeuwenhoek, Amsterdam, NIV/NVMO
- J. (Jolanda) Bloos-van der Hulst, verpleegkundig specialist, Antoni van Leeuwenhoek, Amsterdam, V&VN
- Dr. A.M.E. (Anna) Bruynzeel, radiotherapeut-oncoloog, Amsterdam Medisch Centrum, NVRO
- Dr. L. (Linda) Kerkmeijer, radiotherapeut-oncoloog, Radboudumc, Nijmegen, NVRO
- Drs. E. (Else) Wolak, belangenbehartiger Kwaliteit van zorg, Patiëntenvereniging Blaas- of Nierkanker
- Dr. M.A.J. (Mark) Meier, interventieradioloog, Isala Ziekenhuis, Zwolle, NVvR / NVIR
Met ondersteuning van
- Drs. D.A.M. (Danique) Middelhuis, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. M.H.D. (Majke) van Bommel, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. M. (Mohammadreza) Abdollahi, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J.H. (Hanneke) van der Lee, senior-adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. I.M. (Irina) Mostovaya, senior-adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Linda Niesink, medisch informatie specialist, Kennisinstituut van de Federatie Medisch Specialisten
- Esther van der Bijl, medisch informatie specialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Bex (voorzitter) |
Uroloog AVL Amsterdam. Afdelingshoofd in het Specialist Centre of Kidney Cancer, Royal Free London NHS Foundation Trust, Professor of Urology, UCL Division of Surgery and Investigational Science. |
Alle nevenfuncties zijn onbetaald: |
- Restricted educational grant van Pfizer tbv een neoadjuvante studie (sponsor is het NKI-AvL). - Steering committee op twee internationale adjuvante fase 3 studies van BMS en Roche. - Lid van medical steering committee van twee patientenorganisaties (Kidney Cancer Association en IKCC). - Financier BMS: randomised phase 3 trial of adjuvant nivolumab plus ipilimumab versus placebo in high risk RCC. - Financier Roche: randomised phase 3 trial of adjuvant atezolizumab versus placebo in high risk RCC. - Financier Pfizer: single-arm phase 2 trial of neoadjuvant avelumab plus axitinib in high risk RCC (funded by restricted educational grant) |
Geen restricties |
|
Bevers |
Uroloog LUMC Leiden |
Geen |
Geen |
Geen restricties |
|
Langenhuijsen |
Uroloog Radboudumc Nijmegen |
Invited speaker Update Urology (Astra Zeneca), vergoeding+reiskosten |
Financier: ZonMW Voorbereidende studie Doelmatigheidsonderzoek, Pentixafor PET vs veneuze sampling bij primair hyperaldosteronisme - Financier: PentixaPharm GmbH, CASTUS trial. |
Geen restricties |
|
Hamberg |
Oncoloog Franciscus Gasthuis en Vlietland Rotterdam |
voorzitter WIN-O nier (onbetaald) bestuurslid Pro RCC (onbetaald) |
- Adviesraden meerdere farmaceutische bedrijven actief binnen RCC zorg - lokale hoofonderzoeker van aantal adjuvante nierkanker studies (Farma sponsored). Tevens ook van studies (farma sponsored) naar medicamenteuze interventies bij gemetastaseerde ziekte (oa RCC) |
Geen restricties |
|
Van Thienen |
Internist-oncoloog NKI-AvL Amsterdam |
Alle nevenfuncties zjn onbetaald: - Inhoudelijk/vice voorzitter Medisch Inhoudelijke Standpunten (MIS) groep van DRCG - Lid wetenschappelijke adviesraad Stichting PRO-RCC |
Pfizer Neoadjuvant axitinib en avelumab bij niercelcarcinoom (projectleider); BMS Checkmate 914 Adjuvant immunotherapy in high-risk renal cancer (onderzoeker); Eisai CLEAR study: levantinib and everolimus or pembrolizumab vs sunitinib in mRCC (onderzoeker); Goethe University Frankfurt am Main Sunniforecast (nivolumab+ipilimumab vs sunitinib in non-clear cell mRCC)(onderzoeker); Roche Adjuvant atezolizumab in high risk renal cancer (onderzoeker) |
Geen restricties |
|
Bloos-van der Hulst |
Verpleegkundig specialist uro-oncologie AVL Amsterdam |
Geen |
Geen |
Geen restricties |
|
Kerkmeijer |
Radiotherapeut-oncoloog, Radboudumc Nijmegen. Plaatsvervangend keteneigenaar Urologische Oncologie Radboudumc Nijmegen |
Alle nevenfuncties zjn onbetaald: - DUOS bestuurslid - Raad van Advies Tie Ribbon - Associate Editor Frontiers in oncology - Radiotherapeut-oncoloog UMC Utrecht (gastaanstelling) |
KWF subsidie FLAME studie prostaatcarcinoom |
Geen restricties |
|
Wolak |
Belangenbehartiger kwaliteit van zorg Patiëntenvereniging blaas- of nierkanker (PBNK) |
Patiëntenvereniging blaas- of nierkanker |
Werkzaam bij patiëntenorganisatie Leven met blaas- of nierkanker, geen boegbeeldfunctie |
Geen restricties |
|
Meier |
Interventieradioloog Isala Zwolle Voorzitter RVE Medische Beeldvorming, Isala Zwolle |
|
Geen |
Geen restricties |
|
Bruynzeel |
Radiotherapeut-oncoloog, Amsterdam UMC |
Geen |
ViewRay Inc: Een onderzoek naar hoge en precieze bestraling (stereotactische ablatieve radiotherapie) bij patiënt |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van de Patiëntenvereniging blaas- of nierkanker (PBNK) voor de schriftelijke knelpunteninventarisatie en afvaardiging namens PBNK in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie per module ook “Waarden en voorkeuren van patiënten”). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenvereniging blaas- of nierkanker (PBNK) en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Module Behandeling van T1b niertumoren |
geen financiële gevolgen |
Uitkomst 1 |
De kwalitatieve raming volgt na de commentaarfase.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met nierkanker. Tevens zijn er knelpunten aangedragen door de NVU (Nederlandse Vereniging voor Urologie) en NVRO, NVVR en Patiëntenvereniging blaas- of nierkanker (PBNK) via een schriftelijke knelpuntenanalyse.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: Herziening Niercelcarcinoom |
|
|
Uitgangsvraag: Wat zijn de (on)gunstige effecten van partiële nefrectomie, totale nefrectomie, SABR, percutane ablatie patiënten met een niet-gemetastaseerd niercelcarcinoom tussen 4-7 cm? |
|
|
Database(s): Medline (OVID), Embase |
Datum: 10-02-2022 |
|
Periode: >2000 |
Talen: Engels, Nederlands |
|
Literatuurspecialist: Linda Niesink |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting:
→ Voor deze vraag is gezocht op de elementen cT1b (in het groen) niercelcarcinoom (in het blauw), en partiële nefrectomie (in het oranje).
→ De genoemde sleutelartikelen van Mir (2017) en Correa (2019) zitten in de zoekopbrengst. De artikelen van Caputo (2017), Rembeyo (2020), Antonelli (2008) en Yang (2019) vallen er buiten op studiedesign. Zonder beperking op SR en RCT’s zouden deze artikelen wel gevonden worden.
→ Resultaten staan in Rayyan. |
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (via embase.com) en Medline (via OVID) is op 10-02-2022 met relevante zoektermen gezocht naar systematische reviews en RCT’s over partiële nefrectomie bij patiënten met een cT1b niercelcarcinoom. De literatuurzoekactie leverde 106 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
26 |
19 |
27 |
|
RCTs |
79 |
13 |
79 |
|
Totaal |
105 |
32 |
106 |
Zoekstrategie
|
Database |
Zoektermen |
||||||||||||||||||||||||||||||
|
Embase
|
|
||||||||||||||||||||||||||||||
|
Medline (OVID)
|
1 exp Carcinoma, Renal Cell/ or exp Kidney Neoplasms/ or (('kidney' or 'renal' or nephroid or hypernephroid or 'collecting duct') adj3 (cancer* or carcinoma* or adenocarcinoma* or neoplasm* or tumor* or tumour* or mass*)).ti,ab,kf. or (grawitz* adj3 (tumor* or tumour*)).ti,ab,kf. or hypernephroma*.ti,ab,kf. or (RCC or MRCC or nccrcc or ncrcc).ti,ab,kf. (112726) 2 (t1b or ct1b or '7 cm').ti,ab,kf. (9072) 3 exp Radiosurgery/ or exp Radiofrequency Ablation/ or exp Cryosurgery/ or exp Microwaves/ or ((stereotactic or stereotaxic) adj3 (radiation or therap* or radiotherap*)).ti,ab,kf. or (partial adj3 (nephrectom* or 'kidney resection')).ti,ab,kf. or ('nephron sparing' or 'percutaneous treatment' or ablation or cryoablation or microwave* or 'micro wave*' or enucleation).ti,ab,kf. (211003) 4 1 and 2 and 3 (468) 5 limit 4 to ((english or dutch) and yr="2000 -Current") (409) 6 5 not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) (385) 7 (meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) (573135) 8 (exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf.) not (animals/ not humans/) (1351271) 9 6 and 7 (19) – SRs 10 (6 and 8) not 9 (13) - RCTs 11 9 or 10 (32) |
