Alternatieve entreetechniek bij MIC
Uitgangsvraag
Welke entreetechniek heeft de voorkeur bij volwassenen met een indicatie voor laparoscopie: een alternatieve entree techniek versus open of gesloten?
Aanbeveling
De onder-zicht-techniek lijkt een veilig alternatief voor de open of de gesloten entreetechniek, ook zonder pneumoperitoneum voorafgaand aan de insertie.
Kies hiervan de techniek welke de operateur geleerd heeft en waarmee hij/zij vertrouwd is, zodat door ervaring de risico’s beperkt worden.
Kijk voor speciale patiëntengroepen in de bijbehorende modules Speciale patiëntengroepen (obese patiënten (BMI>30), patiënten met een BMI<18, zwangere patiënten en patiënten die eerder een laparoscopie hebben ondergaan).
Overwegingen
De onderstaande overwegingen gelden in principe voor het overgrote deel van de patiëntenpopulatie waarop de uitgangsvraag betrekking heeft. Voor de subgroep “obese patiënten (BMI>30), patiënten met een BMI<18, zwangere patiënten en patiënten die eerder een laparoscopie hebben ondergaan” zijn aparte uitgangsvragen en aanbevelingen gevormd.
Rationale voor de aanbeveling
Op basis van de cruciale uitkomstmaten lijkt er geen verschil te zijn tussen de onder-zicht techniek en de open of gesloten (Veressnaald) entreetechniek. De onder-zicht techniek lijkt een veilig alternatief voor de open of de gesloten entreetechniek, ook wanneer voorafgaand aan de insertie van de trocar geen pneumoperitoneum is aangelegd. De bewijskracht van de literatuur is zeer laag.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor vasculair en visceraal letsel wordt geen klinisch relevant verschil gevonden tussen de onder-zicht techniek en de open of gesloten entreetechniek (Veressnaald). Het gebruik van de onder-zichttechniek, ook zonder voorafgaand pneumoperitoneum lijkt een veilig alternatief voor de open of de gesloten entreetechniek. Drie van de vier studies gebruikten deze techniek zonder voorafgaand pneumoperitoneum.
De bewijskracht voor de cruciale uitkomstmaten is zeer laag. De werkgroep is van mening dat op basis van de cruciale uitkomstmaten geen aanbeveling wordt gedaan ten aanzien van een voorkeurstechniek.
Er wordt geen verschil gezien tussen de onder-zicht techniek en de open of de gesloten techniek (Veressnaald) op grond van de belangrijke uitkomstmaten.
De werkgroep is van mening dat er geen reden is om een richting aan de besluitvorming te geven op basis van de belangrijke uitkomstmaten. Dit komt voornamelijk door de lage bewijskracht. De onder-zicht techniek lijkt een veilig alternatief voor de open of gesloten entreetechniek.
De werkgroep is wel van mening dat ervaring in een techniek de kans op complicaties verkleint en adviseert daarom ook de techniek te gebruiken die de operateur geleerd heeft en bekend mee is.
Overige overwegingen
Ten aanzien van de overige overwegingen: waarden en voorkeuren van de patiënt, kosten, aanvaarbaarheid voor de overige relevante stakeholders en haalbaarheid en implementatie zijn er geen noemenswaardige bezwaren vanuit het veld, die van invloed zijn op de besluitvorming.
Onderbouwing
De incidentie van complicaties bij laparoscopie is laag. Echter, inherent aan de toegepaste chirurgische techniek kunnen er complicaties optreden, zoals de entree-gerelateerde complicatie. Er zijn in hoofdlijnen drie verschillende entree technieken te onderscheiden: de open techniek, de gesloten techniek (directe trocar entree en Veressnaald insertie) en de steeds meer gebruikte hybride techniek. De gekozen techniek hangt af van de ervaring van de chirurg, de operatie-indicatie en eventuele voorgeschiedenis van de patiënt. De risico’s behorend bij elk van de technieken zijn onderzocht. In deze module worden de risico’s besproken en strategieën uiteengezet die kunnen worden gevolgd om entree-gerelateerde complicaties te voorkomen.
Wat is het effect van onder-zicht entreetechniek versus een gesloten entreetechniek op (ernstige) ongewenste voorvallen en complicaties?
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal vasculaire letsels tussen de onder-zicht techniek (directe optische trocar insertie) en de gesloten entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Tinelli, 2009; Tinelli, 2010) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal viscerale letsels tussen de onder-zicht techniek (directe optische trocar insertie) en de gesloten entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Tinell,i 2009; Tinelli, 2010) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal vasculaire letsels tussen de onder-zicht techniek (insertie optische trocar na pneumoperitoneum) en de gesloten entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Mohammadi, 2018; Tinell,i 2011) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal viscerale letsels tussen de onder-zicht techniek (insertie optische trocar na pneumoperitoneum) en de gesloten entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Tinelli, 2011) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal letsels van solide organen tussen de onder-zicht techniek (directe optische trocar insertie en insertie na pneumoperitoneum) en de open entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Minervini, 2008) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal falen van toegang tussen de onder-zicht techniek (directe optische trocar insertie) en de open entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Minervini, 2008) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het aantal bloedingen van de insteekopening tussen de onder-zicht techniek (directe optische trocar insertie) en de open entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Minervini, 2008) |
|
Zeer laag GRADE |
Er is wellicht geen verschil in het ontstaan van extraperitoneale insufflatie tussen de onder-zicht techniek (insertie optische trocar na pneumoperitoneum) en de open entreetechniek, maar het bewijs is zeer onzeker.
Bronnen: (Mohammadi, 2018) |
In totaal zijn vier afzonderlijke RCT’s opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
Beschrijving studies
Er zijn in totaal vier studies geïncludeerd in de analyses. De patiëntengroep bestond globaal uit volwassen patiënten, die een indicatie hadden voor laparoscopie. Twee studies excludeerden patiënten die eerder een open abdominale, of peri-umbilicale operatie hadden gehad (Tinelli, 2009; Tinelli, 2010). Indien de artikelen reeds door de Cochrane review (Ahmad, 2019) beoordeeld waren op risk-of-bias, is deze beoordeling overgenomen in de risk of bias tabellen.
Vier studies beschreven de onder-zicht techniek, waarbij drie studies een directe trocar insertie verrichten met de onderzicht-techniek (Minervini, 2008; Tinelli, 2009; Tinelli, 2010), terwijl één studie eerst een pneumoperitoneum creëerde door middel van een Veressnaald (Mohammadi, 2018). Er werden verschillende onder-zicht systemen gebruikt, zoals de bladeless Optiview system (Minervini, 2008), Visiport trocar system (Mohammadi, 2018) en Endopath trocars (Tinelli, 2009; Tinelli, 2010). Alle studies die de gesloten entreetechniek beschreven, gebruikten de Veressnaald techniek (Tinelli, 2009; Tinelli, 2010). Het punt van Palmer wordt gedefinieerd als het punt dat zich 3 cm distaal van de onderste rib miclaviculair bevindt.
Voor de artikelen die geïncludeerd zijn in de Cochrane review, werden de resultaten primair uit deze review gehaald. Deze werden aangepast indien er door ons andere of aanvullende resultaten in de originele artikelen werden gevonden. Deze aanpassingen zijn verantwoord in de evidencetabellen.
De studies bevatten veel beperkingen. Deze waren vooral op het gebied van imprecisie, gebaseerd op lage incidentie van de uitkomstmaat en suboptimale patiënten aantallen en op het gebied van beperkingen in de studieopzet en uitvoering (risico op bias). De studiemethoden werden slecht beschreven; vaak werd niet beschreven op welke manier patiënten werden gerandomiseerd, of er sprake was van blindering van patiënten en/of zorgverleners en of sprake was van geblindeerde toewijzing van patiënten aan de verschillende onderzoeksgroepen.
Resultaten
Mortaliteit
Geen van de geïncludeerde studies beschreven mortaliteit als uitkomstmaat.
Vasculair letsel
Er werden geen gevallen van vasculair letsel gerapporteerd in de vergelijking tussen de onder-zicht techniek en de gesloten entreetechniek (Veressnaald) (0/182 versus 0/198) (Tinelli 2009; Tinelli 2010).
Er werden geen gevallen van vasculair letsel gerapporteerd in de vergelijking tussen de onder-zicht techniek en de open entreetechniek (0/50 versus 0/50) (Tinelli, 2011).
Visceraal letsel
Er werden geen gevallen van visceraal letsel gerapporteerd in de vergelijking tussen de onder-zicht techniek en de gesloten entreetechniek (Veressnaald) (0/182 versus 0/198) (Tinelli 2009; Tinelli 2010).
Geen van de geïncludeerde studies beschreef visceraal letsel in de vergelijking tussen de onder-zicht techniek en de open entreetechniek.
Gasembolie
Geen van de geïncludeerde studies rapporteerde over de uitkomstmaat gasembolie.
Solide orgaanletsel
Geen van de geïncludeerde studies vergeleken de onder-zichttechniek met de gesloten entreetechniek voor de uitkomstmaat gasembolie.
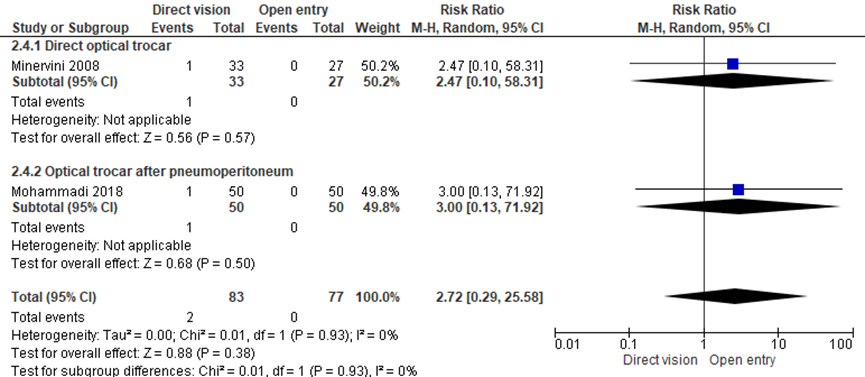
Studies lieten geen statistisch significant verschil zien voor solide orgaanletsel tussen de onder-zicht techniek (directe optische trocar insertie en optische trocar insertie na pneumoperitoneum) en de open entreetechniek (2/83 versus 0/77; RR 2.72 (0.29;25.58), I2 = 0%) (Minervini, 2008; Mohammadi, 2018). NNT: 42 patiënten behandelen met de open entreetechniek om bij één patiënt extra solide orgaanletsel te voorkomen, betrouwbaarheidsinterval loopt van 17 patiënten bij de open techniek tot 112 patiënten bij de onder-zicht techniek. De werkgroep beoordeelde deze schatting van het effect als niet klinisch relevant. De grenzen van het betrouwbaarheidsinterval omsluiten zowel een klinisch relevant voordeel als nadeel van de open entreetechniek.
Figuur 1 Forest plot voor de vergelijkingen onder-zichttechniek versus open entreetechniek. Uitkomstmaat: solide orgaanletsel
Falen van toegang
Geen van de geïncludeerde studies vergeleek de onder-zichttechniek met de gesloten entreetechniek (Veressnaald) voor deze uitkomstmaat.
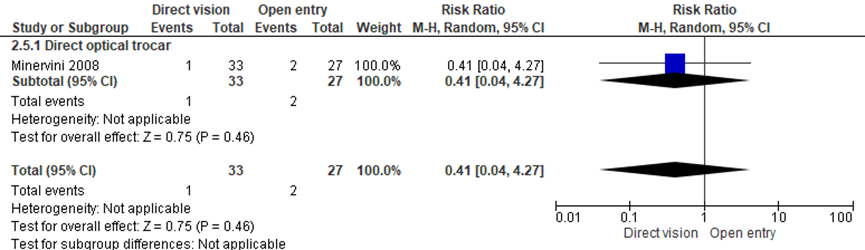
Men vond geen statistisch significant verschil voor het falen van toegang tussen de onder-zichttechniek (directe optische trocar insertie) en de open entreetechniek (1/33 versus 2/27; RR 0.41 (0.04;4.27)) (Minervini, 2008). NNT: 23 patiënten behandelen met de onder-zicht techniek, het betrouwbaarheid interval loopt van 6 patiënten met onder-zicht techniek behandelen tot 14 patiënten met de open entreetechniek. De werkgroep beoordeelde deze schatting van het effect als niet klinisch relevant. De grenzen van het betrouwbaarheidsinterval omsluiten zowel een klinisch relevant voordeel als nadeel van de onder-zicht techniek.
Figuur 2 Forest plot voor de vergelijking onder-zichttechniek versus open entreetechniek. Uitkomstmaat: falen van toegang
Bloeding insteekopening
Er werden geen bloedingen van de insteekopening gerapporteerd in de vergelijking tussen de onder-zicht techniek en de gesloten entreetechniek (Veressnaald) (0/93 versus 0/101) (Tinelli, 2010).
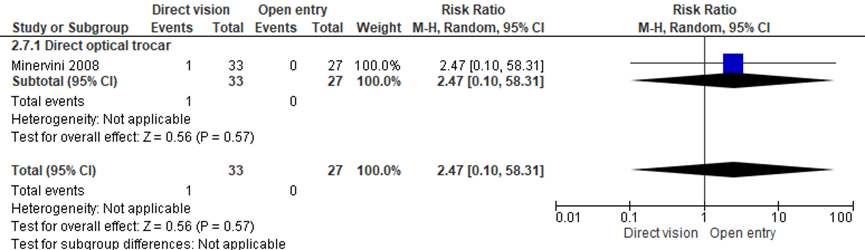
Men zag geen statistisch significant verschil tussen de onder-zicht techniek (directe optische trocar insertie) en de open entreetechniek (1/33 versus 0/27; RR 2.47 (0.10;58.31)) (Minervini, 2008). NNT: 33 patiënten behandelen met de open entreetechniek. Het betrouwbaarheidsinterval loopt van 11 patiënten behandelen met de open entreetechniek tot 35 patiënten behandelen met de onder-zicht techniek. De werkgroep beoordeelde deze schatting van het effect als niet klinisch relevant. De grenzen van het betrouwbaarheidsinterval omsluiten zowel een klinisch relevant voordeel als nadeel van de open entreetechniek.
Figuur 3 Forest plot voor de vergelijking onder-zichttechniek versus open entreetechniek. Uitkomstmaat: bloeding insteekopening
Extraperitoneale insufflatie
Geen van de geïncludeerde studies vergeleken de onder-zichttechniek met de gesloten entreetechniek (Veressnaald) voor deze uitkomstmaat.
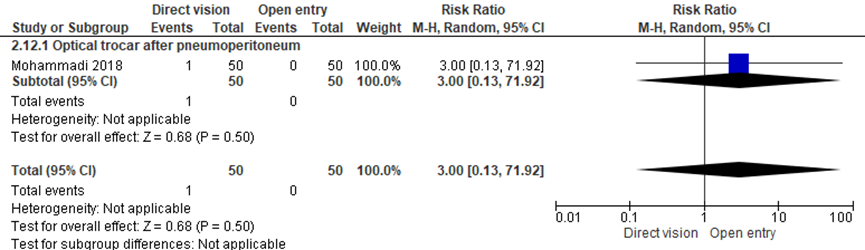
Er werd geen statistisch significant verschil gezien in extraperitoneale insufflatie (subcutaan emfyseem in deze studie) tussen de onder-zicht techniek (optische trocar insertie na pneumoperitoneum) en de open entreetechniek (1/50 versus 0/50; RR 3.00 (0.13;71.92)) (Mohammadi, 2018). NNT: 50 patiënten behandelen met de open entreetechniek, het betrouwbaarheidsinterval loopt van 17 patiënten behandelen met de open entreetechniek tot 53 patiënten behandelen met de onder-zicht techniek. De werkgroep beoordeelde deze schatting van het effect als niet klinisch relevant. De grenzen van het betrouwbaarheidsinterval omsluiten zowel een klinisch relevant voordeel als nadeel van de open entreetechniek.
Figuur 4 Forest plot voor de vergelijking onder-zichttechniek versus open entreetechniek. Uitkomstmaat: extraperitoneale insufflatie
Littekenbreuk
Geen van de geïncludeerde studies vergeleken de onder-zichttechniek met de Veressnaald of de open entreetechniek voor deze uitkomstmaat.
Relevante informatie uit niet-vergelijkende retrospectieve studies die de PICO beantwoorden
Twee studies uit de literatuurzoekactie voldeden niet aan de inclusiecriteria, omdat dit retrospectieve of niet-vergelijkende studies waren (Bianchi, 2016; Ternamian, 2010). Deze studies worden hier besproken, omdat deze wel relevante informatie over de technieken geven.
Ternamian (2010) beschreef in een prospectieve, niet-vergelijkende studie 4724 laparoscopieën, waarbij een optische trocarloze visuele canule met schroefdraad (EndoTip, Karl Storz) werd gebruikt (insertie na pneumoperitoneum). Men zag geen serieus intra-abdominaal vasculair letsel, geen vasculair buikwand letsel en één darmletsel. In een retrospectieve vragenlijststudie van Bianchi (2016) werd de open, gesloten en onder-zichttechniek (5/7 chirurgen gebruiken optische trocar insertie na pneumoperitoneum, 2/7 gebruiken de optische trocar zonder voorafgaand pneumoperitoneum, gebruikte trocar wordt niet benoemd) vergeleken, waarbij de onder-zichttechniek significant minder complicaties liet zien.
Bij de interpretatie van deze studies moet rekening gehouden worden met de beperkingen van deze studieopzet en daarmee de zeer lage bewijskracht.
Bewijskracht van de literatuur
Wat is het effect van onder-zicht entreetechniek versus een gesloten entreetechniek op (ernstige) ongewenste voorvallen en complicaties?
De bewijskracht voor de uitkomstmaat vasculair letsel is met drie niveaus verlaagd gezien risk of bias, en de kleine patiëntenpopulatie (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat visceraal letsel is met drie niveaus verlaagd gezien risk of bias, en de kleine patiëntenpopulatie (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat bloeding van de insteekopening is met drie niveaus verlaagd gezien risk of bias, en de kleine patiëntenpopulatie (imprecisie, twee niveaus).
Wat is het effect van onder-zicht entreetechniek versus een open entreetechniek op (ernstige) ongewenste voorvallen en complicaties?
De bewijskracht voor de uitkomstmaat vasculair letsel is met drie niveaus verlaagd gezien risk of bias, en het feit dat het maar één studie is (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat solide orgaan schade is met drie niveaus verlaagd gezien risk of bias, en het beiderzijds overlappen van de grens van klinische besluitvorming (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat falen van toegang is met drie niveaus verlaagd gezien risk of bias, en het beiderzijds overlappen van de grens van klinische besluitvorming en het feit dat maar één studie deze uitkomstmaat rapporteert (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat bloeding van de insteekopening is met drie niveaus verlaagd gezien risk of bias, en het beiderzijds overlappen van de grens van klinische besluitvorming en het feit dat maar één studie deze uitkomstmaat rapporteert (imprecisie, twee niveaus).
De bewijskracht voor de uitkomstmaat extraperitoneale insufflatie is met drie niveaus verlaagd gezien risk of bias, en het beiderzijds overlappen van de grens van klinische besluitvorming en het feit dat maar 1 studie deze uitkomstmaat rapporteert (imprecisie, twee niveaus).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
“Wat is het effect van alternatieve entreetechniek versus een open of gesloten entreetechniek op (ernstige) ongewenste voorvallen en complicaties?” en bijbehorende PICO:
P: volwassenen met een indicatie voor laparoscopie;
I: alternatieve entreetechniek;
C: open of gesloten entreetechniek;
O: mortaliteit, vasculair letsel, visceraal letsel (blaas- of darmletsel, solide organen), extraperitoneale insufflatie, CO2-lekkage, falen van toegang, lange termijn letsel/complicaties (zoals littekenbreuk, nerve entrapment syndrome, i.e. ACNES).
Relevante uitkomstmaten
De werkgroep achtte mortaliteit, visceraal letsel, vasculair letsel, gasembolie en bloeding van de insteekopening voor de besluitvorming cruciale uitkomstmaten. Falen van toegang, littekenbreuk en extraperitoneale insufflatie (insufflatie van CO2 buiten de peritoneaalholte, subcutaan emfyseem is hierin meegenomen, conform de Cochrane Review van Ahmad uit 2019) en solide orgaanschade (schade aan lever, milt) zijn voor de besluitvorming belangrijke uitkomstmaten.
Door de werkgroep is gekozen om, anders dan de Cochrane Review, Radially Expanding Trocar niet mee te nemen in deze uitgangsvraag, omdat deze in de praktijk nauwelijks gebruikt wordt. De radially expanding access technique of de radially expanding trocar is een huls voor gebruik om de trocar en Veressnaald, waarmee het weefsel langzaam opgerekt wordt.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
De werkgroep definieerde a priori geen klinisch (patiënt) relevante verschillen, maar gebruikte het “Number Needed to Treat” (NNT) of “Number Needed to Harm” (NNH) om de impact voor patiënten te beoordelen en te wegen.
Zoeken en selecteren (Methode)
In eerste instantie werd een Cochrane review uit 2019 geselecteerd (Ahmad, 2019), die reeds voor het beantwoorden van de uitgangsvraag “Welke entreetechniek heeft de voorkeur bij patiënten boven de 18 jaar met een indicatie voor laparoscopie: open of gesloten?” als basis is gebruikt. Deze Cochrane review beantwoordde exact de PICO. In de databases Medline, Embase, Emcare, Web of Science en Cochrane Library is op 19 april 2019 met relevante zoektermen gezocht naar complicaties bij alternatieve entreetechnieken. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 37 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: de studie betreft een randomized controlled trial (RCT), systematic review (SR), of een prospectieve cohort studie, de studiepopulatie bestaat uit volwassenen met een indicatie voor laparoscopie, de studie vergelijkt de hybride techniek met de open of gesloten entreetechniek en de studie beschrijft één of meer van de, voor deze richtlijn, relevante uitkomsten. Op basis van titel en abstract werden vervolgens uit de zoekactie in eerste instantie 21 artikelen voorgeselecteerd, met daarbij één extra artikel die werd gevonden via een andere uitgangsvraag. Na raadpleging van de volledige tekst, werden vervolgens 20 artikelen geëxcludeerd (zie exclusietabel), en één artikel definitief geselecteerd. De artikelen gebruikt in de Cochrane review (Ahmad, 2019), relevant voor deze uitgangsvraag, werden als individuele artikelen meegenomen. Twee artikelen uit de Cochrane review werden geëxcludeerd. Eén artikel ging namelijk specifiek over obese patiënten (Tinelli, 2013)en één artikel specifiek over patiënten die eerder een laparotomie of laparoscopie hadden ondergaan (Tinelli 2011), wat in een andere uitgangsvraag wordt beschreven. Vier artikelen uit de Cochrane review werden geëxcludeerd (Bhoyrul, 2000; Bisgaard, 2007; Feste, 2000; Mettler, 2009), omdat deze artikelen Radially Expending Trocars beschreven. Op deze manier zijn er in totaal vier artikelen geïncludeerd.
- Ahmad, G., Baker, J., Finnerty, J., Phillips, K., & Watson, A. (2019). Laparoscopic entry techniques. Cochrane Database Syst Rev, 1, Cd006583. doi:10.1002/14651858.CD006583.pub5.
- Bhoyrul, S., Payne, J., Steffes, B., Swanstrom, L., & Way, L. W. (2000). A randomized prospective study of radially expanding trocars in laparoscopic surgery. J Gastrointest Surg, 4(4), 392-397. doi:10.1016/s1091-255x(00)80018-9.
- Bianchi, G., Martorana, E., Ghaith, A., Pirola, G. M., Rani, M., Bove, P., . . . Micali, S. (2016). Laparoscopic access overview: Is there a safest entry method? Actas Urol Esp, 40(6), 386-392. doi:S0210-4806(16)00042-5 (pii);10.1016/j.acuro.2015.11.011 (doi).
- Bisgaard, T., Jakobsen, H. L., Jacobsen, B., Olsen, S. D., & Rosenberg, J. (2007). Randomized clinical trial comparing radially expanding trocars with conventional cutting trocars for the effects on pain after laparoscopic cholecystectomy. Surg Endosc, 21(11), 2012-2016. doi:10.1007/s00464-007-9517-0.
- Feste, J. R., Bojahr, B., & Turner, D. J. (2000). Randomized trial comparing a radially expandable needle system with cutting trocars. JSLS, 4(1), 11-15.
- Mettler, L., & Maher, P. (2009). Investigation of the Effectiveness of the Radially-Expanding Needle System, in Contrast to the Cutting Trocar in Enhancing Patient Recovery. Minimally Invasive Therapy & Allied Technologies, 9, 397-401. doi:10.3109/13645700009093715.
- Minervini, A., Davenport, K., Pefanis, G., Keeley, F. X., Jr., & Timoney, A. G. (2008). Prospective study comparing the bladeless optical access trocar versus Hasson open trocar for the establishment of pneumoperitoneum in laparoscopic renal procedures. Arch Ital Urol Androl, 80(3), 95-98.
- Mohammadi, M., Shakiba, B., & Shirani, M. (2018). Comparison of two methods of laparoscopic trocar insertion (Hasson and Visiport) in terms of speed and complication in urologic surgery. Biomedicine (Taipei), 8(4), 22. doi:10.1051/bmdcn/2018080422 (doi);bmdcn2018080422 (pii).
- Ternamian, A. M., Vilos, G. A., Vilos, A. G., Abu-Rafea, B., Tyrwhitt, J., & MacLeod, N. T. (2010). Laparoscopic peritoneal entry with the reusable threaded visual cannula. J Minim Invasive Gynecol, 17(4), 461-467. doi:S1553-4650(10)00113-5 (pii);10.1016/j.jmig.2010.03.001 (doi).
- Tinelli, A., Malvasi, A., Guido, M., Istre, O., Keckstein, J., & Mettler, L. (2009). Initial laparoscopic access in postmenopausal women: a preliminary prospective study. Obstetrical & gynecological survey, 65, 91â€92.
- Tinelli, A., Malvasi, A., Guido, M., Tsin, D. A., Hudelist, G., Stark, M., & Mettler, L. (2011). Laparoscopy entry in patients with previous abdominal and pelvic surgery. Surgical innovation, 18(3), 201-205. doi:https://dx.doi.org/10.1177/1553350610393989
- Tinelli, A., Malvasi, A., Istre, O., Keckstein, J., Stark, M., & Mettler, L. (2010). Abdominal access in gynaecological laparoscopy: a comparison between direct optical and blind closed access by Verres needle. Eur J Obstet Gynecol Reprod Biol, 148(2), 191-194. doi:S0301-2115(09)00641-1 (pii);10.1016/j.ejogrb.2009.10.025 (doi).
- Tinelli, A., Malvasi, A., Mynbaev, O. A., Tsin, D. A., Davila, F., Dominguez, G., . . . Nezhat, F. R. (2013). Bladeless direct optical trocar insertion in laparoscopic procedures on the obese patient. JSLS, 17(4), 521-528. doi:10.4293/108680813X13693422519398 (doi).
Evidence table for systematic reviews (SRs)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Ahmad 2019 (Cochrane)
Direct vision versus veress neelde |
SR and meta-analysis of RCTs
Literature search up to January 2018 A: Tinelli 2009 B: Tinelli 2010
Study design: RCT
Setting and Country: NVT
Source of funding and conflicts of interest: No
|
Inclusion criteria SR: RCT, that compared one entry technique with another. Men, women, children who were undergoing diagnostic, operative, or mixed laparoscopy, performed by gynaecologists or general surgeons. Type of intervention: open entry technique (direct trocar or veress needle), or closed entry technique
Exclusion criteria SR:
Important patient characteristics at baseline:
N, mean age A: 186 B: 194
Groups comparable at baseline? BMI was in both studies higher in the Veress needle group (+0.8 and +0.3) |
Describe intervention:
A: direct optical access Optical bladeless trocar (endopath trocars, ethicon, johnson & johnson)
B: direct optical access Optical bladeless trocar (endopath trocars, ethicon, johnson & johnson)
|
Describe control:
A: closed veress needle B: closed veress needle |
End-point of follow-up:
A: surgery B: surgery
For how many participants were no complete outcome data available? (intervention/control) A: 0/0 B: 0/0
|
Primary outcomes
Outcome measure-1 Vascular Injury
Effect measure: RR, RD, mean difference (95% CI): A: 0/89 versus 0/97, RR NE (Cochrane stated 1/89 versus 3/97, but the original article stated these injuries as “minor vascular injuries (jejunal small vessel or omental vessel, no interventions needed”. Major vascular injury was collected conform the methods section and not mentioned as event. Conform the statement in Cochrane “Vascular injury: Major vessels”, we excluded these minor vascular injuries from analysis. Also Cochrane did not count the same injuries as major injury for Tinelli 2010 and 2011)
B: 0/93 versus 0/101, RR NE (not mentioned in Cochrane, but original article states 2/93 versus 4/101 minor vascular injuries (jejunal small vessel or omental vessel, no intervention needed). Major vascular injury was collected conform the methods section and not mentioned as event. Conform the statement in Cochrane “Vascular injury: Major vessels”, we excluded these minor vascular injuries from analysis)
Outcome measure-2 Visceral Injury
Effect measure: RR, RD, mean difference (95% CI): A: 0/89 versus 0/97, RR NE B: 0/93 versus 0/101, RR NE (Cochrane stated 0/93 versus 2/101, but the original article stated these injuries as “minor bowel injuries, no intervention was needed (light ecchymosed bowel loops)”. we excluded these minor bowel injuries from analysis. Also Cochrane did not count these same injuries as bowel injuries in Tinelli 2011)
Secondary outcomes Outcome measure-3 Trocar site bleeding
Effect measure: RR, RD, mean difference (95% CI): A: NA B1: 0/93 versus 0/101, RR NE. (Cochrane stated 2/93 versus 4/101 , but the original article stated these injuries as “jejunal small vessels and omental vessels. We considered these injuries not relevant for the outcome measure trocar site bleeding and therefore excluded these injuries from analysis. Also Cochrane did not include these same injuries as trocar site bleeding for Tinelli 2009 and 2011) |
Facultative:
Differences in event rates between Cochrane review and original articles are mentioned with the relevant outcome measure.
Risk Ratio (RR) originates from our own analysis using RevMan. Mantel-Haenszel, with random effect was used, while Cochrane used Peto Odds Ratio. Pooled effect is therefore different and will not be stated in this evidence table |
|
Ahmad 2019 (Cochrane)
Direct vision versus open entry |
SR and meta-analysis of RCTs
Literature search up to January 2018 A: Minervini 2008
Study design: RCT
Setting and Country: NVT
Source of funding and conflicts of interest: No
|
Inclusion criteria SR: RCT, that compared one entry technique with another. Men, women, children who were undergoing diagnostic, operative, or mixed laparoscopy, performed by gynaecologists or general surgeons. Type of intervention: Direct entry versus veress needle
Exclusion criteria SR:
Important patient characteristics at baseline:
N, mean age A: 60 B: 168 C: 224
Groups comparable at baseline? Yes |
Describe intervention:
A: hasson open )
|
Describe control:
A: 12 mm bladeless trocar (ethicon endosurgery)
|
End-point of follow-up:
A: surgery
For how many participants were no complete outcome data available? (intervention/control) A: 0/0
|
Primary outcomes
Outcome measure-1 Vascular Injury
Effect measure: RR, RD, mean difference (95% CI): A: NA
Outcome measure-2 Visceral Injury
Effect measure: RR, RD, mean difference (95% CI): A: NA
Outcome measure 3- Solid organ injury Effect measure: RR, RD, mean difference (95% CI): A: 1/33 versus 0/27 RR 2.47 (0.10;58.31)
Outcome measure-4 Failed entry
Effect measure: RR, RD, mean difference (95% CI): A: 1/33 versus 2/27 0.41 (0.04;4.27)
Secondary outcomes Outcome measure-5 Trocar site bleeding
Effect measure: RR, RD, mean difference (95% CI): A: 1/33 versus 0/27 RR 2.47 (0.10;58.31) |
Tinelli 2013 included only obese patients and was therefore excluded from the evidence table
Tinelli 2011 included only patients with previous laparotomy of laparoscopy and was therefore excluded from the evidence table
Differences in event rates between Cochrane review and original articles are mentioned with the relevant outcome measure.
Risk Ratio (RR) originates from our own analysis using RevMan. Mantel-Haenszel, with random effect was used, while Cochrane used Peto Odds Ratio. Pooled effect is therefore different and will not be stated in this evidence table |
Evidence table for intervention studies (RCTs)
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Mohammadi 2018 |
Type of study: RCT
Setting and country: Iran, Ishafan University of medical sciences
Funding and conflicts of interest: No conflict |
Inclusion criteria: Over 18 years, candidates for urological laparoscopic surgery.
Exclusion criteria: Uncorrected coagulopathy, ileus, infection of the abdominal wall, history of open abdominal surgery, presence of malignant ascites and generalized peritonitis
N total at baseline: Intervention: 50 Control:50
Important prognostic factors2: For example age ± SD: I:41.4 C:41.6
Groups comparable at baseline?
|
Describe intervention (treatment/procedure/test):
Open laparoscopic treatment (hasson) |
Describe control (treatment/procedure/test):
Visiport trocar system |
Length of follow-up: Unknown
Loss-to-follow-up: Unknown
Incomplete outcome data: none
|
Outcome measures and effect size (include 95%CI and p-value if available):
Mean time to enter 95.4 (31.75) sec versus 37.7 (15.59) (Visiport) p=0.000
Complications Total Visiport 4/50 (8%) Hasson 0/50
Subcutaneous emphysema (included in extraperitoneal insufflation) visiport 1/50 (2%), hasson 0/50
Trocar site infection Visiport 1/50 (2%), hasson 0/50
Mild liver damage Visiport 1/50 (2%) Hasson 0/50
Small vessel damage (not included for vascular damage as Cochrane includes only major vessel damage) Visiport 0/5- (small vessel) Hasson 0/50
Visiport 1 (2%) (small vessel) Hasson 0/50 |
|
Risk of bias tabel

GRADEpro tabellen
Vraagstelling: Onder-zichttechniek versus Veress Naald voor Laparoscopie
|
Certainty assessment |
Aantal patiënten |
Effect |
Certainty |
Importantie |
||||||||
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
Onder-zichttechniek |
Veress Naald |
Relatief |
Absoluut |
||
|
Vascular Injury |
||||||||||||
|
2 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig b |
niet gevonden |
0/182 (0.0%) |
0/198 (0.0%) |
Niet te berekenen |
⨁◯◯◯ |
CRUCIAAL |
|
|
Visceral injury |
||||||||||||
|
2 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig b |
niet gevonden |
0/182 (0.0%) |
0/198 (0.0%) |
Niet te berekenen |
⨁◯◯◯ |
CRUCIAAL |
|
|
Trocar site bleeding |
||||||||||||
|
1 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig b,c |
niet gevonden |
0/93 (0.0%) |
0/101 (0.0%) |
Niet te berekenen |
⨁◯◯◯ |
BELANGRIJK |
|
CI: Confidence interval; RR: Risk ratio
Explanations
a. Serious risk of bias due to randomization, blinding and allocation concealment
b. Kleine patientenpopulatie
c. Eén studie
Vraagstelling: Onder-zichttechniek versus Open entreetechniek voor Laparoscopie
|
Certainty assessment |
Aantal patiënten |
Effect |
Certainty |
Importantie |
||||||||
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
Onder-zichttechniek |
Open entreetechniek |
Relatief |
Absoluut |
||
|
Vasculair letsel |
||||||||||||
|
1 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig b |
niet gevonden |
0/50 (0.0%) |
0/50 (0.0%) |
Niet te berekenen |
⨁◯◯◯ |
CRUCIAAL |
|
|
Solide orgaanletsel |
||||||||||||
|
2 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig c |
niet gevonden |
2/83 (2.4%) |
0/77 (0.0%) |
RR 2.72 |
0 minder per 1,000 |
⨁◯◯◯ |
BELANGRIJK |
|
Falen van toegang |
||||||||||||
|
1 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig c,d |
niet gevonden |
1/33 (3.0%) |
2/27 (7.4%) |
RR 0.41 |
44 minder per 1,000 |
⨁◯◯◯ |
BELANGRIJK |
|
Bloeding insteekopening |
||||||||||||
|
1 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig c,d |
niet gevonden |
1/33 (3.0%) |
0/27 (0.0%) |
RR 2.47 |
0 minder per 1,000 |
⨁◯◯◯ |
BELANGRIJK |
|
Extraperitoneal insufflation |
||||||||||||
|
1 |
gerandomiseerde trials |
ernstig a |
niet ernstig |
niet ernstig |
zeer ernstig c |
niet gevonden |
1/50 (2.0%) |
0/50 (0.0%) |
RR 3.00 |
0 minder per 1,000 |
⨁◯◯◯ |
BELANGRIJK |
CI: Confidence interval; RR: Risk ratio
Explanations
a. Serious risk of bias due to randomization, blinding and allocation concealment
b. Kleine patientenpopulatie
c. Betrouwbaarheidsinterval doorkruist de lijn van klinische relevantie tweemaal
d. Eén studie
Reden voor exclusie na het lezen van het volledige artikel.
|
Auteur en jaartal |
Redenen van exclusie |
|
Aust 2010 |
Geen vergelijkende studie, gebruikt tevens een alternatieve entreeplaats. Kleine populatie |
|
Bianchi 2016 |
Retrospectief vragenlijstonderzoek |
|
Bozkurt 2012 |
Turks artikel |
|
Carlson 2012 |
Geen gebruik van optische trocar, alleen speciale cannule |
|
Djokovic 2016 |
Richtlijn, gebruikt Cochrane Review data |
|
Kumar 2015 |
Directe trocar insertie, niet optisch. Geen vergelijkende studie |
|
Ott 2012 |
Niet systematische review |
|
Paul 2016 |
Retrospectieve observationele case-control studie, operatie in voorgeschiedenis |
|
Tinelli 2011 |
Inclusie specifiek patiënten die eerder een laparotomie of laparoscopie hebben ondergaan, deze patiëntengroep wordt in een andere uitgangsvraag besproken. |
|
Tinelli 2010 |
Zit in Cochrane Review, wordt via Cochrane Review wel meegenomen |
|
Vilos 2017 |
Richtlijn, gebruikt RCT die in Cochrane Review zit |
|
Zakherah 2010 |
Zit in Cochrane Review, wordt via Cochrane Review wel meegenomen |
|
Zaman 2016 |
Systematic Review, gebruikt geen andere data dan Cochrane Review. Besloten om Cochrane Review te includeren. |
|
Tanaka 2018 |
Uitkomstmaat entreetijd. Door werkgroep besloten deze uitkomstmaat niet mee te nemen |
|
Ternamian 2010 |
Geen vergelijkende studie |
|
Tinelli 2013 |
Inclusie specifiek obese patiënten, deze patiëntengroep wordt in een andere uitgangsvraag besproken. |
|
Sundbom 2016 |
Inclusie specifiek obese patiënten, deze patiëntengroep wordt in een andere uitgangsvraag besproken. |
|
Kosuta 2014 |
Inclusie specifiek obese patiënten, deze patiëntengroep wordt in een andere uitgangsvraag besproken. |
|
Kassir 2014 |
Artikel over uitleg van procedures, geen resultaten |
|
Tanaka 2018 |
Uitkomstmaat operatietijd. Door werkgroep besloten deze uitkomstmaat niet mee te nemen |
|
Bhoyrul 2000 |
Radially Expanding Trocar |
|
Bisgaar 2007 |
Radially Expanding Trocar |
|
Mettler 2000 |
Radially Expanding Trocar |
|
Feste 2000 |
Radially Expanding Trocar |
Beoordelingsdatum en geldigheid
Publicatiedatum : 16-08-2021
Beoordeeld op geldigheid : 16-08-2021
Frequentie van beoordeling op actualiteit: Eens per 5 jaar
Relevante factoren voor wijziging in aanbeveling: Geen factoren bekend
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). Patiënten participatie bij deze richtlijn werd medegefinancierd uit de Stichting Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ.
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten die een laparoscopie ondergaan.
Werkgroep
- Prof. dr. F.W. (Frank Willem) Jansen, gynaecoloog, Leids Universitair Medisch Centrum, Leiden, NVOG (voorzitter)
- Drs. F.H.M.P. (Fokkedien) Tummers, arts-onderzoeker gynaecologie, Leids Universitair Medisch Centrum, Leiden, NVOG
- Drs. T.A. (Tammo) Brouwer, anesthesioloog, Zorggroep Noorderbreedte, Leeuwarden, NVA
- Dr. S.F.P.J. (Sjors) Coppus, gynaecoloog, Máxima MC, Eindhoven, NVOG
- Dr. A. (Ahmet) Demirkiran, gastro-intestinaal & bariatrisch chirurg, Rode Kruis Ziekenhuis, Beverwijk, NVVH
- Dr. W.A. (Werner) Draaisma, chirurg, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch, NVEC
- Dr. B.W. (Brunolf) Lagerveld, uroloog, OLVG, Amsterdam, NVU
- Ir. E.S. (Esther) van Schrojenstein Lantman, klinisch fysicus, Albert Schweitzer ziekenhuis, Dordrecht, NVKF
- Drs. K. (Klaartje) Spijkers, senior adviseur patiëntenbelang, Patiëntenfederatie Nederland, Utrecht
Met ondersteuning van
- Dr. M. (Marleen) van Son, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf september 2020)
- Dr. L. (Laura) Viester, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf september 2020)
- Dr. J. (Julitta) Boschman, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf juli 2019 tot september 2020)
- Dr. R. (Roy) Elbers, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot juni 2019)
- Dr. E. (Elvira) den Breejen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot juni 2019)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Brouwer |
Anesthesioloog - werkzaam te Medisch Centrum Leeuwarden (MC) (#werkgever) |
- |
Geen |
Geen |
|
Coppus |
Gynaecoloog Maxima Medisch Centrum Eindhoven/Veldhoven |
Bestuurslid Werkgroep Gynaecologische Endoscopie (onbetaald) |
Geen |
Geen |
|
Demirkiran |
Gastro-intestinaal en bariatrisch chirurg. |
Geen |
Geen |
Geen |
|
Draaisma |
Chirurg Jeroen Bosch Ziekenhuis |
Geen |
Geen |
Geen |
|
Jansen |
Gynaecoloog LUMC Professor in Gynaecology and Minimally Invasive Surgery Leiden University |
Professor in Gynaecology and Minimally Invasive Surgery TU Delft |
Geen |
Geen |
|
Lagerveld |
Uroloog OLVG Amsterdam |
Geen |
Geen |
Geen |
|
Schrojenstein - Lantman |
Klinisch Fysicus in het Albert Schweitzer Ziekenhuis (ASZ) (0,9 fte) |
Geen |
Geen |
Geen |
|
Spijkers |
Senior adviseur patiëntenbelang |
Voorzitter Stichting Samen voor Duchenne |
Geen |
Geen |
|
Tummers |
ANIOS Gynaecologie & Verloskunde, Groene Hart Ziekenhuis Gouda |
Onderzoeker LUMC, afdeling Gynaecologie, betaald |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door participatie van een afgevaardigde van Patiëntenfederatie Nederland in de werkgroep. Deze afgevaardigde heeft de werkgroep van input voorzien bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep schriftelijk de knelpunten in de zorg voor patiënten met een indicatie voor een laparoscopie. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijn Minimaal Invasieve Chirurgie (NVOG, 2011) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door onder andere de Inspectie voor Gezondheidszorg en Jeugd, Lareb, het Nederlands Huisartsen Genootschap, de Nederlandse Vereniging voor Heelkunde, de Nederlandse Vereniging voor Klinische Fysica en de Nederlandse Vereniging voor Obstetrie en Gynaecologie. De ingebrachte knelpunten inclusief reactie van de werkgroep is opgenomen in de bijlagen.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij hanteerde de werkgroep een maximum van acht uitkomstmaten. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
19-4-2019: 38 referenties, afkomstig uit:
PubMed: 21 (RefID/Label 1-21)
MEDLINE (OVID): 20, waarvan 4 uniek (RefID/Label 22-25)
Embase: 24, waarvan 6 uniek (RefID/Label 26-31)
Emcare: 15, waarvan 0 uniek
Web of Science: 25, waarvan 6 uniek (RefID/Label 32-37)
COCHRANE Library: 8, waarvan 1 uniek (RefID/Label 42)
*ontbrekende RefID/Labels betreffen met de hand verwijderde dubbele referenties
PubMed - http://www.ncbi.nlm.nih.gov/pubmed?otool=leiden
(("Laparoscopy"(mesh:noexp) OR "Laparoscopy"(majr) OR "Minimally Invasive Surgical Procedures"(Mesh:noexp) OR laparoscop*(tw) OR minimal invasiv*(tw) OR minimally invasiv*(tw)) AND ("blunt tip"(tw) OR "endotip"(tw) OR endotip*(tw) OR "optiview"(tw) OR optiview*(tw) OR "visiport"(tw) OR visiport*(tw) OR "needle scope"(tw) OR "troc-doc"(tw) OR "trocdoc"(tw) OR "optical trocar"(tw) OR "alternative entry"(tw) OR "visual access"(tw) OR visual access*(tw) OR "optical access"(tw) OR optical access*(tw) OR ((alternativ*(ti) OR visual*(ti)) AND ("entry"(ti) OR "access"(ti))) OR (("visual"(tw) OR "alternative"(tw)) AND entry system*(tw))) AND ("open entry"(tw) OR open entr*(tw) OR "hasson"(tw) OR "hassen"(tw) OR "balloon trocar"(tw) OR "balloon trocars"(tw) OR "balloon trochar"(tw) OR "closed entry"(tw) OR closed entr*(tw) OR "direct trocar insertion"(tw) OR "direct trocar"(tw) OR "direct trocars"(tw) OR "endotip"(tw) OR endotip*(tw) OR "veress needle"(tw) OR "veress needles"(tw) OR "veress"(tw) OR "radially expanding"(tw) OR "radially expanding trocars"(tw) OR "step trocar"(tw) OR "step trocars"(tw) OR "direct entry"(tw) OR ("direct"(tw) AND ("entry"(tw) OR insert*(tw))) OR "point of entry"(tw) OR "place of entry"(tw) OR "palmer"(tw) OR palmer*(tw)) AND ("2010/01/01"(PDAT) : "3000/12/31"(PDAT)) NOT (("Child"(mesh) OR "Infant"(mesh) OR "Adolescent"(mesh) OR "Child"(ti) OR "children"(ti) OR "Infant"(ti) OR "Infants"(ti) OR Adolescen*(ti) OR pedatric*(ti) OR paediatric*(ti)) NOT ("Adult"(mesh) OR "adult"(tw) OR "adults"(tw))) AND english(la) NOT ("Animals"(mesh) NOT "Humans"(mesh))).
MEDLINE (OVID) - http://gateway.ovid.com/ovidweb.cgi?T=JS&MODE=ovid&NEWS=n&PAGE=main&D=prmz
(("Laparoscopy"/ OR exp *"Laparoscopy"/ OR "Minimally Invasive Surgical Procedures"/ OR laparoscop*.ti,ab,kf OR "minimal invasiv*".ti,ab,kf OR "minimally invasiv*".ti,ab,kf ) AND ("blunt tip".ti,ab,kf OR "endotip".ti,ab,kf OR endotip*.ti,ab,kf OR "optiview".ti,ab,kf OR optiview*.ti,ab,kf OR "visiport".ti,ab,kf OR visiport*.ti,ab,kf OR "needle scope".ti,ab,kf OR "troc-doc".ti,ab,kf OR "trocdoc".ti,ab,kf OR "optical trocar".ti,ab,kf OR "alternative entry".ti,ab,kf OR "visual access".ti,ab,kf OR "visual access*".ti,ab,kf OR "optical access".ti,ab,kf OR "optical access*".ti,ab,kf OR ((alternativ*.ti,ab,kf OR visual*.ti,ab,kf ) ADJ4 ("entry".ti,ab,kf OR "access".ti,ab,kf )) OR (("visual".ti,ab,kf OR "alternative".ti,ab,kf ) ADJ4 entry system*.ti,ab,kf )) AND ("open entry".ti,ab,kf OR "open entr*".ti,ab,kf OR "hasson".ti,ab,kf OR "hassen".ti,ab,kf OR "balloon trocar".ti,ab,kf OR "balloon trocars".ti,ab,kf OR "balloon trochar".ti,ab,kf OR "closed entry".ti,ab,kf OR "closed entr*".ti,ab,kf OR "direct trocar insertion".ti,ab,kf OR "direct trocar".ti,ab,kf OR "direct trocars".ti,ab,kf OR "endotip".ti,ab,kf OR endotip*.ti,ab,kf OR "veress needle".ti,ab,kf OR "veress needles".ti,ab,kf OR "veress".ti,ab,kf OR "radially expanding".ti,ab,kf OR "radially expanding trocars".ti,ab,kf OR "step trocar".ti,ab,kf OR "step trocars".ti,ab,kf OR "direct entry".ti,ab,kf OR ("direct".ti,ab,kf ADJ4 ("entry".ti,ab,kf OR insert*.ti,ab,kf )) OR "point of entry".ti,ab,kf OR "place of entry".ti,ab,kf OR "palmer".ti,ab,kf OR palmer*.ti,ab,kf ) AND (2010.yr OR 2011.yr OR 2012.yr OR 2013.yr OR 2014.yr OR 2015.yr OR 2016.yr OR 2017.yr OR 2018.yr OR 2019.yr) NOT ((exp "Child"/ OR exp "Infant"/ OR exp "Adolescent"/ OR "Child".ti OR "children".ti OR "Infant".ti OR "Infants".ti OR Adolescen*.ti OR pedatric*.ti OR paediatric*.ti) NOT (exp "Adult"/ OR "adult".ti,ab,kf OR "adults".ti,ab,kf)) AND english.la NOT (exp "Animals"/ NOT exp "Humans"/)).
Embase (OVID) - http://ovidsp.ovid.com/ovidweb.cgi?T=JS&PAGE=main&MODE=ovid&D=oemezd
((exp *"Laparoscopy"/ OR *"Minimally Invasive Surgery"/ OR laparoscop*.ti,ab OR "minimal invasiv*".ti,ab OR "minimally invasiv*".ti,ab ) AND ("blunt tip".ti,ab OR "endotip".ti,ab OR endotip*.ti,ab OR "optiview".ti,ab OR optiview*.ti,ab OR "visiport".ti,ab OR visiport*.ti,ab OR "needle scope".ti,ab OR "troc-doc".ti,ab OR "trocdoc".ti,ab OR "optical trocar".ti,ab OR "alternative entry".ti,ab OR "visual access".ti,ab OR "visual access*".ti,ab OR "optical access".ti,ab OR "optical access*".ti,ab OR ((alternativ*.ti,ab OR visual*.ti,ab ) ADJ4 ("entry".ti,ab OR "access".ti,ab )) OR (("visual".ti,ab OR "alternative".ti,ab ) ADJ4 entry system*.ti,ab )) AND ("open entry".ti,ab OR "open entr*".ti,ab OR "hasson".ti,ab OR "hassen".ti,ab OR "balloon trocar".ti,ab OR "balloon trocars".ti,ab OR "balloon trochar".ti,ab OR "closed entry".ti,ab OR "closed entr*".ti,ab OR "direct trocar insertion".ti,ab OR "direct trocar".ti,ab OR "direct trocars".ti,ab OR "endotip".ti,ab OR endotip*.ti,ab OR "veress needle".ti,ab OR "veress needles".ti,ab OR "veress".ti,ab OR "radially expanding".ti,ab OR "radially expanding trocars".ti,ab OR "step trocar".ti,ab OR "step trocars".ti,ab OR "direct entry".ti,ab OR ("direct".ti,ab ADJ4 ("entry".ti,ab OR insert*.ti,ab )) OR "point of entry".ti,ab OR "place of entry".ti,ab OR "palmer".ti,ab OR palmer*.ti,ab ) AND (2010.yr OR 2011.yr OR 2012.yr OR 2013.yr OR 2014.yr OR 2015.yr OR 2016.yr OR 2017.yr OR 2018.yr OR 2019.yr) NOT ((exp "Child"/ OR exp "Infant"/ OR exp "Adolescent"/ OR "Child".ti OR "children".ti OR "Infant".ti OR "Infants".ti OR Adolescen*.ti OR pedatric*.ti OR paediatric*.ti) NOT (exp "Adult"/ OR "adult".ti,ab OR "adults".ti,ab)) AND english.la NOT (exp "Animals"/ NOT exp "Humans"/) NOT (conference review or conference abstract).pt).
Emcare - http://ovidsp.ovid.com/ovidweb.cgi?T=JS&NEWS=n&CSC=Y&PAGE=main&D=emcr
((exp *"Laparoscopy"/ OR *"Minimally Invasive Surgery"/ OR laparoscop*.ti,ab OR "minimal invasiv*".ti,ab OR "minimally invasiv*".ti,ab ) AND ("blunt tip".ti,ab OR "endotip".ti,ab OR endotip*.ti,ab OR "optiview".ti,ab OR optiview*.ti,ab OR "visiport".ti,ab OR visiport*.ti,ab OR "needle scope".ti,ab OR "troc-doc".ti,ab OR "trocdoc".ti,ab OR "optical trocar".ti,ab OR "alternative entry".ti,ab OR "visual access".ti,ab OR "visual access*".ti,ab OR "optical access".ti,ab OR "optical access*".ti,ab OR ((alternativ*.ti,ab OR visual*.ti,ab ) ADJ4 ("entry".ti,ab OR "access".ti,ab )) OR (("visual".ti,ab OR "alternative".ti,ab ) ADJ4 entry system*.ti,ab )) AND ("open entry".ti,ab OR "open entr*".ti,ab OR "hasson".ti,ab OR "hassen".ti,ab OR "balloon trocar".ti,ab OR "balloon trocars".ti,ab OR "balloon trochar".ti,ab OR "closed entry".ti,ab OR "closed entr*".ti,ab OR "direct trocar insertion".ti,ab OR "direct trocar".ti,ab OR "direct trocars".ti,ab OR "endotip".ti,ab OR endotip*.ti,ab OR "veress needle".ti,ab OR "veress needles".ti,ab OR "veress".ti,ab OR "radially expanding".ti,ab OR "radially expanding trocars".ti,ab OR "step trocar".ti,ab OR "step trocars".ti,ab OR "direct entry".ti,ab OR ("direct".ti,ab ADJ4 ("entry".ti,ab OR insert*.ti,ab )) OR "point of entry".ti,ab OR "place of entry".ti,ab OR "palmer".ti,ab OR palmer*.ti,ab ) AND (2010.yr OR 2011.yr OR 2012.yr OR 2013.yr OR 2014.yr OR 2015.yr OR 2016.yr OR 2017.yr OR 2018.yr OR 2019.yr) NOT ((exp "Child"/ OR exp "Infant"/ OR exp "Adolescent"/ OR "Child".ti OR "children".ti OR "Infant".ti OR "Infants".ti OR Adolescen*.ti OR pedatric*.ti OR paediatric*.ti) NOT (exp "Adult"/ OR "adult".ti,ab OR "adults".ti,ab)) AND english.la NOT (exp "Animals"/ NOT exp "Humans"/) NOT (conference review or conference abstract).pt).
Web of Science - http://isiknowledge.com/wos
(ti=("Laparoscopy" OR "Minimally Invasive Surgery" OR laparoscop* OR "minimal invasiv*" OR "minimally invasiv*") AND ts=("blunt tip" OR "endotip" OR endotip* OR "optiview" OR optiview* OR "visiport" OR visiport* OR "needle scope" OR "troc-doc" OR "trocdoc" OR "optical trocar" OR "alternative entry" OR "visual access" OR "visual access*" OR "optical access" OR "optical access*" OR ((alternativ* OR visual*) NEAR/4 ("entry" OR "access")) OR (("visual" OR "alternative") NEAR/4 "entry system*")) AND ts=("open entry" OR "open entr*" OR "hasson" OR "hassen" OR "balloon trocar" OR "balloon trocars" OR "balloon trochar" OR "closed entry" OR "closed entr*" OR "direct trocar insertion" OR "direct trocar" OR "direct trocars" OR "endotip" OR endotip* OR "veress needle" OR "veress needles" OR "veress" OR "radially expanding" OR "radially expanding trocars" OR "step trocar" OR "step trocars" OR "direct entry" OR ("direct" NEAR/4 ("entry" OR insert*)) OR "point of entry" OR "place of entry" OR "palmer" OR palmer*) AND py=(2010 OR 2011 OR 2012 OR 2013 OR 2014 OR 2015 OR 2016 OR 2017 OR 2018 OR 2019) NOT ti=(("Child" OR "Infant" OR "Adolescent" OR "Child" OR "children" OR "Infant" OR "Infants" OR Adolescen* OR pedatric* OR paediatric*) NOT ("Adult" OR "adult" OR "adults")) AND la=english NOT ti=("veterinary" OR "rabbit" OR "rabbits" OR "animal" OR "animals" OR "mouse" OR "mice" OR "rodent" OR "rodents" OR "rat" OR "rats" OR "pig" OR "pigs" OR "porcine" OR "horse" OR "horses" OR "equine" OR "cow" OR "cows" OR "bovine" OR "goat" OR "goats" OR "sheep" OR "ovine" OR "canine" OR "dog" OR "dogs" OR "feline" OR "cat" OR "cats"))
NOT conference abstract.
Cochrane - http://www.cochranelibrary.com/
(("Laparoscopy" OR "Minimally Invasive Surgery" OR laparoscop* OR "minimal invasiv*" OR "minimally invasiv*") AND ("blunt tip" OR "endotip" OR endotip* OR "optiview" OR optiview* OR "visiport" OR visiport* OR "needle scope" OR "troc-doc" OR "trocdoc" OR "optical trocar" OR "alternative entry" OR "visual access" OR "visual access*" OR "optical access" OR "optical access*" OR ((alternativ* OR visual*) NEAR/4 ("entry" OR "access")) OR (("visual" OR "alternative") NEAR/4 "entry system*")) AND ("open entry" OR "open entr*" OR "hasson" OR "hassen" OR "balloon trocar" OR "balloon trocars" OR "balloon trochar" OR "closed entry" OR "closed entr*" OR "direct trocar insertion" OR "direct trocar" OR "direct trocars" OR "endotip" OR endotip* OR "veress needle" OR "veress needles" OR "veress" OR "radially expanding" OR "radially expanding trocars" OR "step trocar" OR "step trocars" OR "direct entry" OR ("direct" NEAR/4 ("entry" OR insert*)) OR "point of entry" OR "place of entry" OR "palmer" OR palmer*)):ti,ab,kw NOT (("Child" OR "Infant" OR "Adolescent" OR "Child" OR "children" OR "Infant" OR "Infants" OR Adolescen* OR pedatric* OR paediatric*) NOT ("Adult" OR "adult" OR "adults")):ti
py=(2010 OR 2011 OR 2012 OR 2013 OR 2014 OR 2015 OR 2016 OR 2017 OR 2018 OR 2019).
AND la=english.
NOT conference abstract.
