Optimale termijn bevalling monochoriale tweelingen
Uitgangsvraag
Wat is de optimale termijn om de bevalling na te streven bij een ongecompliceerde monochoriale diamniotische tweelingzwangerschap?
Aanbeveling
Streef bij een ongecompliceerde monochoriale diamniotische tweelingzwangerschap een bevalling tussen 36+0 en 37+0 weken zwangerschapsduur na, na counseling over kans op neonatale (respiratoire) morbiditeit en mortaliteit.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In de hierboven benoemde studies werd geen specifieke uitspraak gedaan over het inleiden van de bevalling bij monochoriale tweelingzwangerschappen. Er werd strikt genomen gekeken naar de zwangerschapsduur, hetgeen vervolgens werd gekoppeld aan de uitkomst. Het was onbekend hoeveel patiënten zijn ingeleid en hoeveel spontaan in partu zijn gekomen. Op basis van deze informatie is het dus niet goed mogelijk om een uitspraak te doen over “inductie van de baring“. Op basis van deze observationele data kan wel een uitspraak worden gedaan over het risico op overlijden per zwangerschapsduur, en dit afwegen tegen het risico op neonatale mortaliteit en morbiditeit.
Het risico op intra-uterien overlijden overschrijdt tussen 36 en 37 weken het risico op neonatale sterfte bij de ongecompliceerde monochoriale diamniotische tweelingzwangerschappen. Het risico op ernstige neonatale morbiditeit (mechanische ventilatie, IRDS, HIE, sepsis) is na deze termijn ook significant lager dan voor 36 weken.
Het bewijs is van ‘zeer laag niveau’ ten gevolge van de lage incidentie van monochoriale tweelingzwangerschappen en het ontbreken van RCT’s. Een dergelijke gerandomiseerde studie zal echter nooit tot uitvoer komen, gezien de enorme aantallen inclusies die nodig zijn om deze onderzoeksvraag te beantwoorden.
Derhalve is een afweging van het prospectieve risico op foetale sterfte versus de risico’s voor de neonaat bij geboorte per zwangerschapsweek de hoogst haalbare evidence; het intra-uteriene risico dient afgewogen te worden tegen het extra-uteriene risico in termen van zowel sterfte als neonatale morbiditeit. Individuele studies en verrichte meta-analyses laten hierin eenzelfde trend zien. Het electief inleiden van zwangeren met een ongecompliceerde monochoriale tweelingzwangerschap vanaf 36 weken zwangerschapsduur voorkomt weliswaar de kans op intra-uteriene sterfte (circa 4,5 op 1000 zwangerschappen na 37 weken amenorroe) en leidt niet tot toegenomen sterfte in de neonatale periode, maar geeft wel meer kans op neonatale morbiditeit voornamelijk in de vorm van respiratoire problematiek (risico op geassisteerde ventilatie tussen 36+0 en 36+6 32,4 op 1000 geboorten versus 16,9 per 1000 bij geboorte tussen 37+0 en 37+6; en risico op IRDS tussen 36+0 en 36+6 weken 29,1 op 1000 geboorten versus 11,1 per 1000 als geboren tussen 37+0 en 37+6 weken). Bij geboorte voor 37 weken is er ook een iets grotere kans op leer- en gedragsstoornissen in vergelijking met geboorte na 37 weken (OR 1,37 (BI 1,10-1,71)) (Murray, 2020). Daarom zou je kunnen overwegen om bij een ongecompliceerde MCDA tweeling pas in te leiden in de tweede helft van de 37e week (dus na 36 en halve week). Ouders dienen gecounseld te worden over het risico op laat-premature morbiditeit en de voor- en nadelen van een electieve inleiding versus een expectatief beleid dienen te worden afgewogen met de ouders. Daarbij dient met ouders ook besproken te worden dat er op basis van de literatuur weinig bekend is over verschillen in maternale uitkomsten of effect op de modus partus.
Waarden en voorkeuren van patiënten
In verband met het hogere risico op intra-uteriene sterfte na 37 weken geven de meeste ouders de voorkeur aan geboorte van de tweeling tussen 36 en 37 weken. Daarbij accepteren zij het feit dat nog een aanzienlijk gedeelte van deze kinderen moet worden opgenomen wegens neonatale morbiditeit.
Kosten (middelenbeslag)
Hoewel er geen aparte economische analyses beschreven zijn in de gesorteerde artikelen, leidt het inleiden van monochoriale tweelingen voor 37 weken tot meer randprematuriteit en daardoor tot een mogelijke stijging van kosten voor de gezondheidszorg; dit moet worden afgewogen tegen het risico op intra-uteriene sterfte.
Het voorgestelde beleid is al geïmplementeerd in Nederland en zal geen toename van kosten en middelenbeslag geven.
Aanvaardbaarheid, haalbaarheid en implementatie
Implementatie van de aanbeveling zal zonder problemen verlopen aangezien het inleiden van MCDA-tweelingzwangerschappen voor 37 weken al in de meeste klinieken wordt gedaan.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Hoewel de bewijskracht laag is, beveelt de werkgroep aan om ongecompliceerde monochoriale tweelingzwangerschappen tussen 36+0 en 37+0 weken zwangerschapsduur electief in te leiden aangezien het risicoverschil tussen intra-uteriene sterfte en neonatale sterfte keert tussen 36+0 en 37+0 weken ten gunste van het geboren laten worden van deze tweelingen. De kans op (respiratoire) neonatale morbiditeit dient in de counseling meegenomen te worden. Er kan worden overwogen in de tweede helft 37e week in te leiden om de kans op neonatale morbiditeit zoveel mogelijk te beperken.
Onderbouwing
Naar aanleiding van recente literatuur zijn er aanwijzingen om de geboorte van monochoriale diamniotische (MCDA) tweelingen na te streven voor 37 weken. Dit leidt mogelijk tot een verdere reductie in mortaliteit. Er zijn echter ook aanwijzingen dat de randprematuriteit (35+0 tot 36+6) leidt tot toename van de neonatale morbiditeit. In de huidige module zullen we deze uitgangsvraag proberen te beantwoorden.
Neonatal outcomes
|
Very low GRADE |
The evidence is very uncertain whether elective delivery before 37 weeks reduces the risk of intra-uterine mortality compared to the risk of neonatal mortality for uncomplicated monochorionic twin pregnancies.
Bronnen: (Cheong-See, 2016; Sung, 2016; Lee, 2016) |
|
Very low GRADE |
The evidence is very uncertain about the effect of timing of delivery before 37 weeks of gestation on neonatal infection in uncomplicated monochorionic twin pregnancies.
Bronnen: (Cheong-See, 2016) |
|
Very low GRADE |
The evidence is very uncertain about the effect of timing of delivery before 37 weeks of gestation on Apgar score of less than 7 at 5 minutes in uncomplicated monochorionic twin pregnancies.
Bronnen: (Cheong-See, 2016; Sung, 2016) |
|
Low GRADE |
Elective timing of delivery before 37 weeks of gestation may increase NICU admission in uncomplicated monochorionic twin pregnancies.
Bronnen: (Cheong-See, 2016; Sung, 2016; Lee, 2016) |
|
Very low GRADE |
The evidence is very uncertain about the effect of timing of delivery before 37 weeks of gestation on Respiratory Distress Syndrome in uncomplicated monochorionic twin pregnancies.
Bronnen: (Cheong-See, 2016; Sung, 2016) |
|
Low GRADE |
Timing of delivery before 37 weeks of gestation may result in a decreased birthweight in uncomplicated monochorionic twin pregnancies.
Bronnen: (Sung, 2016) |
|
- GRADE |
The effects of elective timing of delivery before 37 weeks of gestation on acute TTS and neonatal disability in uncomplicated monochorionic twin pregnancies are unclear. None of the included studies reported these outcomes. |
Maternal outcomes
|
Very low GRADE |
The evidence is very uncertain about the effect of timing of delivery before 37 weeks of gestation on mode of delivery in uncomplicated monochorionic twin pregnancies.
Bronnen: (Sung, 2016) |
|
- GRADE |
The effects of elective timing of delivery before 37 weeks of gestation on postpartum hemorrhage, analgesia, perineal trauma, breastfeeding at discharge, maternal satisfaction and psychological well-being/ anxiety in uncomplicated monochorionic twin pregnancies are unclear. None of the included studies reported these outcomes. |
Description of studies
Cheong-See (2016) performed a systematic review and meta-analysis to determine the risks of stillbirth and neonatal complications by gestational age in uncomplicated monochorionic and dichorionic twin pregnancies. Medline, Embase and Cochrane databases were searched from inception until December 2015 for observational cohort studies and cohorts nested in RCT’s reporting rates of stillbirth or neonatal outcomes in monochorionic and/or dichorionic twin pregnancies. Exclusion criteria were unclear chorionicity, monoamnionicity, inability to exclude twin to twin transfusion syndrome in fetuses, and outcomes not provided in weekly or two weekly gestational periods. Stillbirth was defined as a baby born without signs of life after the age of viability or any other definition. Neonatal mortality was defined as death up to 28 days after delivery. A total of 32 studies were included, reporting on 35171 women with twin gestation, from which 5486 monochorionic pregnancies in 25 studies.
Lee (2016) performed a retrospective cohort study with women with uncomplicated monochorionic and dichorionic pregnancies delivered at or beyond 35 weeks of gestation in a tertiary referral hospital in Seoul (Korea) from 1995 to 2013. The optimal gestational age for delivery was determined by comparing the neonatal composite morbidity rate between women who delivered and women who remained undelivered at each gestational week. A total of 697 twin pregnancies were included, from which 171 monochorionic twins. The mean age of the cohort was 32.8 (SD 4.7) years at 35 weeks of gestation.
Sung (2016) performed a retrospective cohort study of all consecutive twin pregnancies delivered at or beyond 34 weeks of gestation in a tertiary referral hospital in Seoul (Korea) from 1995 to 2014. This study seems to be the same study as reported by Lee (2016), but the numbers of deliveries differed for each gestational week and other outcomes were reported. A total of 1198 twin pregnancies were included, from which 302 monochorionic twins. The mean age of the cohort was 30.9 (SD 4.0) years at 34 weeks of gestation. Subjects were categorized into two groups. The late-preterm group (N=190) were twins born at a gestational age between 34 0/7 weeks and 36 6/7 weeks. The term group (N=112) were twins born at or beyond 37 0/7 weeks of gestation.
Results
1. Neonatal outcomes
1.1 Intra-uterine versus neonatal mortality
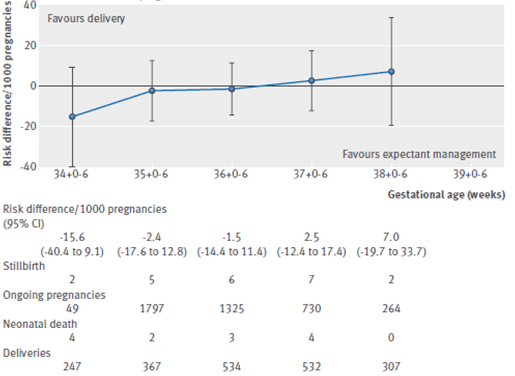
The outcome measure perinatal mortality was provided weekly after 34 weeks’ gestation in 13 of the included trials (Awwad, 2014; Barrett, 2012; Bhattachary, 2015; Breatnach, 2011; Burgess, 2014, Hack, 2008; Hack, 2011; Lewi, 2008; Liem, 2013; Lim, 2011; Nakayama, 2012; Norman, 2009; Rode, 2011). The prospective risk of perinatal mortality was calculated for each week from 34 weeks to 38 weeks of gestation. The prospective risk of stillbirth and neonatal death rates in monochorionic pregnancies were respectively 0.9 (95% CI 0.1 to 3.4) and 12.1 (95% CI 4.2 to 34.3) at 34 weeks, 2.8 (95% CI 0.9 to 6.5) and 8.1 (95% CI 3.4 to 19.3) at 35 weeks, 4.5 (95% CI 1.7 to 9.8) and 5.4 (95% CI 2.2 to 13.3) at 36 weeks, 9.6 (95% CI 3.9 to 19.7) and 3.6 (95% CI 1.2 to 11.1) at 37 weeks and 7.6 (95% CI 0.9 to 27.1) and 2.4 (95% CI 0.6 to 10.3) at 38 weeks (Table 1). The pooled risk differences per 1000 pregnancies were shown in figure 1. From 36,5 weeks, a trend was observed where the risk of stillbirth (9.6/1000) was higher than the risk of neonatal death (3.6/1000) with a risk difference of 2.5/1000 at 37 weeks.
Table 1 Prospective risk of stillbirth and risk of neonatal death in weekly intervals in uncomplicated monochorionic twin pregnancies from 34 weeks’ gestation (from Cheong-See, 2016)
|
Gestational age (weeks) |
No of stillbirths/No of ongoing pregnancies |
Crude risk of stillbirth (per 1000 pregnancies) (95% CI) |
No of neonatal deaths/No of women delivered |
Risk of neonatal death1 (per 1000 pregnancies) (95% CI) |
Pooled risk difference2 (per 1000 pregnancies) (95% CI) |
|
Monochorionic twin pregnancies (13 studies) |
|||||
|
34+0-6 |
2/2149 |
0.9 (0.1 to 3.4) |
4/247 |
12.1 (4.2 to 34.3) |
-15.6 (-40.4 to 9.1) |
|
35+0-6 |
5/1797 |
2.8 (0.9 to 6.5) |
2/367 |
8.1 (3.4 to 19.3) |
-2.4 (-17.6 to 12.8) |
|
36+0-6 |
6/1325 |
4.5 (1.7 to 9.8) |
3/534 |
5.4 (2.2 to 13.3) |
-1.5 (-14.4 to 11.4) |
|
37+0-6 |
7/730 |
9.6 (3.9 to 19.7) |
4/532 |
3.6 (1.2 to 11.1) |
2.5 (-12.4 to 17.4) |
|
38+0-6 |
2/264 |
7.6 (0.9 to 27.1) |
0/307 |
2.4 (0.6 to 10.3) |
7.0 (-19.7 to 33.7) |
1 Risk of neonatal death computed by multilevel logistic regression model.
2 Individual studies risk differences pooled by fixed effect model meta-analysis.
Figure 1 Prospective risks of stillbirths from expectant management compared with risks of neonatal mortality from delivery at weekly intervals from 34 weeks’ gestation (34+0-6; 35+0-6; 36+0-6; 37+0-6; 38+0-6; 39+0-6) in monochorionic twin pregnancies (Cheong-See, 2016)
Sung (2016) reported no difference in neonatal death between the term group (twins born ≥ 37 weeks of gestation) and the late-preterm group (twins born between 34 and 37 weeks of gestation). In the term group 1 out of 224 children died and in the late-preterm group 1 out of 372 children died (P=1.000). There was also no statistically significant difference in fetal death (stillbirth) between the groups, 0 out of 112 children in the term group born without signs of life and 4 out of 190 in the late-preterm group (P=0.301).
1.2 Neonatal infection
The outcome neonatal infection was reported as septicaemia in the systematic review of Cheong-See (2016). The outcome septicaemia was provided weekly after 34 weeks’ gestation in 11 of the included trials (Awwad, 2014; Barrett, 2012; Berezowsky, 2014; Breatnach, 2011; Burgess, 2014; Hack, 2008; Hack, 2011; Lewi, 2008; Lim, 2011; Norman, 2009; Rode, 2011). The prospective risk of septicaemia was calculated for each week from 34 weeks to 38 weeks of gestation. The risk of septicaemia per 1000 deliveries in monochorionic pregnancies was 54.3 (95% CI 23.9 to 118.8) at 34 weeks, 24.4 (95% CI 11.7 to 50.5) at 35 weeks, 10.8 (95% CI 4.6 to 24.9) at 36 weeks, 4.7 (95% CI 1.6 to 14.1) at 37 weeks and 2.1 (95% CI 0.5 to 8.5) at 38 weeks. The relative risk (RR) was calculated, comparing the group delivered before 37 weeks and the group delivered ≥ 37 weeks. The group delivered before 37 weeks had a statistically significant (P=0.01) higher risk on septicaemia compared to the group delivered ≥37 weeks (RR 4.85; 95% CI 1.47 to 16.59).
The studies of Lee (2016) and Sung (2016) did not report the outcome neonatal infection.
1.3 Apgar score of less than 7 at 5 minutes
The systematic review of Cheong-See (2016) did not report the outcome Apgar score of less than 7 at 5 minutes.
Sung (2016) reported no difference in the Apgar score of less than 7 at 5 minutes between the late-preterm group (twins born between 34 and 37 weeks of gestation) and the term group (twins born ≥ 37 weeks of gestation). The numbers with an Apgar score of less than 7 at 5 minutes were 4 out of 372 and 2 out of 224 (P=1.000) respectively, which was a RR of 1.20 (95% CI 0.22 to 6.51; P=0.83).
1.4 NICU/hospital admission
The outcome NICU admission was provided weekly after 34 weeks’ gestation in 9 of the included trials (Awwad, 2014; Barrett, 2012; Berezowsky, 2014; Burgess, 2014, Lewi, 2008; Liem, 2013; Lim, 2011; Norman, 2009; Rode, 2011). The prospective risk of NICU admission was calculated for each week from 34 weeks to 38 weeks of gestation. The risk of NICU admission per 1000 deliveries in monochorionic pregnancies was 501.6 (95% CI 306.1 to 696.6) at 34 weeks, 316.8 (95% CI 173.2 to 506.6) at 35 weeks, 176.1 (95% CI 88.0 to 321.4) at 36 weeks, 89.7 (95% CI 41.3 to 183.9) at 37 weeks, and 43.4 (95% CI 18.4 to 99.3) at 38 weeks. The relative risk (RR) was calculated, comparing the group delivered before 37 weeks and the group delivered ≥ 37 weeks. The group delivered before 37 weeks had a statistically significant (P<0.0001) higher risk on NICU admission compared to the group delivered ≥ 37 weeks (RR 3.10; 95% CI 2.23 to 4.31).
Sung (2016) reported a statistically significant difference in NICU admission between the late-preterm group (twins born between 34 and 37 weeks of gestation) and the term group (twins born ≥ 37 weeks of gestation). The numbers admitted to NICU were 129 out of 372 and 15 out of 224 (P<0.001) respectively, which was an RR of 5.31 (95% CI 3.19 to 8.82; P<0.0001).
1.5 Respiratory distress syndrome (RDS)
The outcome RDS was provided weekly after 34 weeks’ gestation in 13 of the included trials. The prospective risk of RDS was calculated for each week from 34 weeks to 38 weeks of gestation. The risk of RDS per 1000 deliveries in monochorionic pregnancies was 176.7 (95% CI 105.2 to 281.5) at 34 weeks, 74.2 (95% CI 43.6 to 123.7) at 35 weeks, 29.1 (95% CI 15.9 to 52.2) at 36 weeks, 11.1 (95% CI 5.3 to 22.8) at 37 weeks and 4.2 (95% CI 1.7 to 10.2) at 38 weeks. The relative risk (RR) was calculated, comparing the group delivered before 37 weeks and the group delivered ≥ 37 weeks. There was a statistically significant difference in RDS between the group delivered before 37 weeks and the group delivered ≥ 37 weeks (RR 6,55; 95% CI 3.30 to 12.98).
Sung (2016) reported a statistically significant difference in RDS between the late-preterm group (twins born between 34 and 37 weeks of gestation) and the term group (twins born ≥ 37 weeks of gestation). The numbers with RDS were 10 out of 372 and 0 out of 224 (P=0.016) respectively, which was an RR of 12.67 (95% CI 0.75 to 215.14; P=0.08).
1.6 Birthweight
The systematic review of Cheong-See (2016) did not report the outcome birthweight.
Sung (2016) reported a statistically significant difference in birthweight between the late-preterm group (twins born between 34 and 37 weeks of gestation, N=372) and the term group (twins born ≥ 37 weeks of gestation, N=224). The mean birthweights were 2.29 (SD 0.37) (P<0.001) and 2.53 (SD 0.35) respectively. This was a mean difference of 0.240 kg (SD 0.76), which was a minimal clinically important difference (SD 0.5).
1.7 Acute TTS
The systematic review of Cheong-See (2016) did not report the outcome acute TTS.
1.8 Disability (long term)
The systematic review of Cheong-See (2016) did not report the outcome disability.
2. Maternal outcomes
2.1 Mode of delivery
Sung (2016) reported no difference (P=0.409) in the delivery mode between the late-preterm group (women with twins born between 34 and 37 weeks of gestation) and the term group (women with twins born ≥ 37 weeks of gestation). The numbers with a vaginal-vaginal delivery, cesarean-cesarean and vaginal-cesarean delivery were 18 (9.5%), 172 (90.5%) and 0 (0%) in the late-preterm group and 14 (12.5%), 98 (87.5%) and 0 (0%) in the term group.
The systematic review of Cheong-See (2016) did not report the outcome mode of delivery.
2.2 Postpartum hemorrhage
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome postpartum hemorrhage.
2.3 Analgesia
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome analgesia.
2.4 Perineal trauma
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome perineal trauma.
2.5 Breastfeeding at discharge
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome breastfeeding at discharge.
2.6 Maternal satisfaction
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome maternal satisfaction.
2.7 Psychological well-being/ anxiety
The systematic review of Cheong-See (2016) and the studies of Lee (2016) and Sung (2016) did not report the outcome psychological well-being or anxiety.
Level of evidence of the literature
The level of evidence of all defined outcomes measures started low, because the evidence was based on observational cohort studies.
The level of evidence regarding the outcome measure intra-uterine and neonatal mortality was downgraded by 1 level because of imprecision (wide confidence interval and smaller sample size near term) (-1) to ‘very low’.
The level of evidence regarding the outcome measure neonatal infection was downgraded by 1 level because of imprecision (wide confidence interval and smaller sample size near term) (-1) to ‘very low’.
The level of evidence regarding the outcome measure Apgar score of less than 7 at 5 minutes was downgraded by 1 level because of imprecision (wide confidence interval) (-1) to ‘very low’.
The level of evidence regarding the outcome measure NICU/hospital admission remained ‘low’.
The level of evidence regarding the outcome RDS was downgraded by 1 level because of imprecision (wide confidence interval) (-1) to ‘very low’.
The level of evidence regarding the outcome measure birthweight remained ‘low’.
The level of evidence regarding the outcome measure mode of delivery of less than 7 at 5 minutes was downgraded by 1 level because of imprecision (small number of events) (-1) to very low’.
A systematic review of the literature was performed to answer the following question:
What are the effects of elective birth before 37 weeks of gestation with an uncomplicated monochorionic diamniotic twin pregnancy on maternal and neonatal outcomes compared to elective birth after 37 weeks?
P: pregnant women with an uncomplicated monochorionic diamniotic twin pregnancy;
I: elective timing of delivery before 37 weeks;
C: elective timing of delivery after 37 weeks;
O: neonatal outcomes: intra-uterine and neonatal mortality, infections, Apgar score < 7 at 5 minutes, hospital-/ (lenth of) Neonatale Intensive Care Unit (NICU) admission, respiratory distress syndrome (RDS), birth weight, acute Twin Transfusion Syndrome (TTS), disability (longterm).
Maternal outcomes: mode of delivery (spontaneous vaginal, instrumental or caesarean section, failure to progress, or fetal distress), maternal death, postpartum hemorrhage, analgesia, perineal trauma, breastfeeding at discharge, maternal satisfaction, psychological well-being/ anxiety.
Relevant outcome measures
The guideline development group considered intra-uterine and neonatal mortality as a critical outcome measure for decision making; and neonatal and maternal morbidity as important outcome measures for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
A priori, the working group did not define minimal clinically (patient) important differences for the outcome measures, as small changes in intra-uterine or neonatal death can have a huge impact on quality of care.
Search and select (Methods)
A combined search was performed for the questions about monochorionic twins and dichorionic twins. The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until December 12th, 2019. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 543 hits. Studies were selected based on the following criteria:
- The study population had to meet the criteria as defined in the PICO.
- Intervention as defined in the PICO.
- Original research or systematic review.
To answer the question about monochorionic twins, 28 studies were initially selected based on title and abstract screening. After reading the full text, 25 were excluded (see the table with reasons for exclusion under the tab Methods) and three were included.
Results
One systematic review and two additional studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Cheong-See, F., Schuit, E., Arroyo-Manzano, D., Khalil, A., Barrett, J., Joseph, K. S.,... & Liem, S. (2016). Prospective risk of stillbirth and neonatal complications in twin pregnancies: systematic review and meta-analysis. Bmj, 354, i4353.
- Lee, H. J., Kim, S. H., Chang, K. H. J., Sung, J. H., Choi, S. J., Oh, S. Y.,... & Kim, J. H. (2016). Gestational age at delivery and neonatal outcome in uncomplicated twin pregnancies: what is the optimal gestational age for delivery according to chorionicity?. Obstetrics & gynecology science, 59(1), 9-16.
- Murray S, MacKay D, Stock S, Pell J, Norman J. Association of Gestational Age at Birth With Risk of Perinatal Mortality and Special Educational Need Among Twins. JAMA Pediatr. 2020 May 1;174(5):437-445. doi: 10.1001/jamapediatrics.2019.6317. PMID: 32150231; PMCID: PMC7063542.
- Sung, J. H., Kim, S. H., Kim, Y. M., Kim, J. H., Kim, M. N., Lee, H. R.,... & Roh, C. R. (2016). Neonatal outcomes of twin pregnancies delivered at late-preterm versus term gestation based on chorionicity and indication for delivery. Journal of perinatal medicine, 44(8), 903-911.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Cheong-See, 2016
|
SR and meta-analysis of observational cohort studies and cohorts nested in RCTs
Literature search up to December 2015
Studies included: 32 trials, from which 25 studies about monochorionic twins
A: Awwad, 2014 B: Barigye, 2005 C: Barrett, 2012 D: Berezowsky, 2014 E: Bhattachary, 2015 F: Breatnach, 2011 G: Burgess, 2014 H: Dodd, 2012 I: Domingues, 2009 J: Farah, 2011 K: Hack, 2008 L: Hack, 2011 M: Lee, 2008 N: Lewi, 2008 O: Liem, 2013 P: Lim, 2011 Q: Mahony, 2011 R: McPherson, 2012 S: Nakayama, 2012 T: Norman, 2009 U: Rode, 2011 V: Rouse, 2007 W: Russo, 2013 X: Smith, 2010 Y: STORK, 2012
Study design: Retrospective cohort: B, E, G, I, J, K, L, M, Q, R, S, W, X, Y Prospective cohort: D, F, N, Prospective RCT: A, C, H, O, P, T, U, V
Setting and Country: A: Lebanon, single centre B: UK, single centre C: 25 countries, 106 centres D: Israel, single centre E: UK, single centre F: Ireland, multicentre G: USA, single centre H: Australia, New Zealand, 13 centres I: Portugal, single centre J: Ireland, single centre K: Netherlands, 2 centres L: Netherlands, 11 centres M: USA, single centre N: Belgium and Germany, 2 centres O: Netherlands, 40 centres P: Netherlands, 55 centres Q: Ireland, single centre R: USA, single centre S: Japan, single centre T: UK, 9 centres U: Denmark and Austria, 17 centres V: USA, 14 centres W: Italy, single centre X: USA, single centre Y: UK, 9 centres
Source of funding and conflicts of interest: Non-commercial funding, no conflicts of interests were reported.
|
Inclusion criteria SR: observational cohort studies and cohorts nested in randomised studies on rates of stillbirth or neonatal outcomes in monochorionic and/or dichorionic twin pregnancies
Exclusion criteria SR: Unclear chorionicity, monoamnionicity, inability to exclude twin to twin transfusion syndrome in fetuses, and outcomes not provided in weekly or two weekly gestational periods
Important patient characteristics at baseline: Number of patients; characteristics important to the research question
N, patients: A: N=39 B: N=151 C: N=660 D: N=332 E: N=422 F: N=185 G: N=167 H: N=40 I: N=111 J: N=144 K: N=119 L: N=466 M: N=130 N: N=149 O: N=173 P: N=109 Q: N=194 R: N=471 S: N=187 T: N=89 U: N=99 V: N=92 W: N=207 X: N=232 Y: N=527
Groups comparable at baseline? Not reported |
No intervention performed.
|
No control group.
|
End-point of follow-up:
A: 20 weeks until delivery and Discharge of babies from hospital B: 24 to >36 weeks C: 32 to >40 weeks D: 34 weeks until delivery E: 26 weeks until delivery F: 26 weeks until delivery G: 34 to ≥39 weeks H: 36+6 weeks to over 39+ weeks. I: 24 to 35+6 weeks J: 24 to 39+6 weeks K: 26 to >40 weeks L: 32 to >40 weeks M: 24 to >38 weeks N: 12 weeks until delivery O: 26 to 39+6 weeks P: 15-19 weeks until 6 weeks after delivery Q: 24 to >38 weeks R: 20 to >38 weeks S: 26 to >40 weeks T: 20 weeks until delivery U: 18 to 24 weeks until delivery (infants until 18 months post EDD) V: 16 weeks til delivery W: 26 to >40 weeks X: 26 to >40 weeks. Y: 26 to >40 weeks
For how many participants were no complete outcome data available? Not reported
|
Neonatal outcomes:
1. Perinatal death Defined as neonatal death: death up to 28 days after delivery
Effect measure: number of neonatal deaths/ number of women delivered 34+0-6: 4/247 35+0-6: 2/367 36+0-6: 3/534 37+0-6: 4/532 38+0-6: 0/307
Effect measure: risk of neonatal death per 1000 pregnancies (95% CI) 34+0-6: 12.1 (4.2 to 34.3) 35+0-6: 8.1 (3.4 to 19.3) 36+0-6: 5.4 (2.2 to 13.3) 37+0-6: 3.6 (1.2 to 11.1) 38+0-6: 2.4 (0.6 to 10.3)
Defined as risk of stillbirth: baby born without signs of life after the age of viability
Effect measure: crude risk of stillbirth per 1000 pregnancies (95% CI) 34+0-6: 0.9 (0.1 to 3.4) 35+0-6: 2.8 (0.9 to 6.5) 36+0-6: 4.5 (1.7 to 9.8) 37+0-6: 9.6 (3.9 to 19.7) 38+0-6: 7.6 (0.9 to 27.1)
Effect measure: pooled risk difference per 1000 pregnancies (95% CI) 34+0-6: −15.6 (−40.4 to 9.1) 35+0-6: −2.4 (−17.6 to 12.8) 36+0-6: −1.5 (−14.4 to 11.4) 37+0-6: 2.5 (−12.4 to 17.4) 38+0-6: 7.0 (−19.7 to 33.7)
2. Neonatal infection Defined as septicaemia
Effect measure: n/N (in 9 studies) 34+0-6: 9/196 35+0-6: 7/283 36+0-6: 3/406 37+0-6: 3/452 38+0-6: 0/237
Effect measure: risk/1000 deliveries (95% CI) 34+0-6: 54.3 (23.9 to 118.8) 35+0-6: 24.4 (11.7 to 50.5) 36+0-6: 10.8 (4.6 to 24.9) 37+0-6: 4.7 (1.6 to 14.1) 38+0-6: 2.1 (0.5 to 8.5)
3. Apgar score of less than 7 at 5 minutes Not reported
4. NICU/hospital admission Defined as NICU admission
Effect measure: n/N (in 9 studies) 34+0-6: 61/157 35+0-6: 61/229 36+0-6: 44/319 37+0-6: 34/345 38+0-6: 5/168
Effect measure: risk/1000 deliveries (95% CI) 34+0-6: 501.6 (306.1 to 696.6) 35+0-6: 316.8 (173.2 to 506.6) 36+0-6: 176.1 (88.0 to 321.4) 37+0-6: 89.7 (41.3 to 183.9) 38+0-6: 43.4 (18.4 to 99.3)
5. RDS Effect measure: n/N (in 10 studies) 34+0-6: 38/178 35+0-6: 22/261 36+0-6: 13/365 37+0-6: 9/424 38+0-6: 0/225
Effect measure: risk/1000 deliveries (95% CI) 34+0-6: 176.7 (105.2 to 281.5) 35+0-6: 74.2 (43.6 to 123.7) 36+0-6: 29.1 (15.9 to 52.2) 37+0-6: 11.1 (5.3 to 22.8) 38+0-6: 4.2 (1.7 to 10.2)
6. Birthweight Not reported
7. Acute TTS Not reported
8. Disability (long term) Not reported
Maternal outcomes: No maternal outcomes reported. |
Brief description of author’s conclusion: To minimise perinatal deaths, in uncomplicated monochorionic twin pregnancies delivery should be considered at 37 weeks’ gestation.
Level of evidence: The quality of the studies was adequately representative in 27/32 (84%) and inadequately or unclearly representative in 5/32 (16%). 20 studies (63%) had a low risk of misclassification bias for assessment of gestational age and 25/32 (78%) low risk for determination of chorionicity.
|
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy - otherwise the evidence table for studies of diagnostic test accuracy should be used.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3 |
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Lee, 2016 |
Type of study: retrospective cohort study
Setting: tertiary referral hospital
Country: Seoul, Korea
Source of funding: non-commercial (Ministry of Health and Welfare, Republic of Korea)
|
Inclusion criteria: All women with uncomplicated monochorionic and dichorionic twin pregnancies who delivered at the centre after 35 weeks of gestation
Exclusion criteria: Twin pregnancies complicated by twin-to-twin transfusion syndrome, monoamnionic twins, discordant twins, intrauterine fetal growth restriction, preterm labor, preterm premature rupture of membranes, placenta abruption, placenta previa, hypertension (gestational hypertension, preeclampsia, eclampsia, superimposed preeclampsia, and chronic hypertension), diabetes (gestational diabetes and overt diabetes), presence of other severe maternal medical diseases, fetal death before 35 weeks of gestation or chromosomal anomalies or major congenital malformation in one or more of twins
N total at baseline: Monochorionic: 171 Dichorionic: 526
Important prognostic factors2: Age ± SD: 32.8 ± 4.7 yrs
Groups comparable at baseline? NA
|
Not applicable (observational study)
|
Not applicable (observational study)
|
Length of follow-up: from 35 weeks till ≥39 weeks of gestation
Loss-to-follow-up: 0 Intervention:
|
Neonatal outcomes:
1. Perinatal death Defined as neonatal mortality (definition not reported)
Effect measure: number of neonatal deaths/ number of women delivered 35+0-6: 0/20 36+0-6: 1/61 37+0-6: 0/68 38+0-6: 0/16 39+: 1/6
Defined as fetal death in utero (stillbirth)
Effect measure: number of FDIU/ number of women delivered 35+0-6: 1/20 36+0-6: 0/61 37+0-6: 0/68 38+0-6: 0/16 39+: 0/6
2. Neonatal infection Not reported
3. Apgar score of less than 7 at 5 minutes
Effect measure: number with Apgar score<7 at 5 min/ number of women delivered 35+0-6: 0/20 36+0-6: 1/61 37+0-6: 1/68 38+0-6: 0/16 39+: 1/6
4. NICU/hospital admission Defined as NICU admission
Effect measure: number admitted at NICU/ number of women delivered 35+0-6: 7/20 36+0-6: 15/61 37+0-6: 9/68 38+0-6: 2/16 39+: 1/6
5. Birthweight Not reported
6. Acute TTS Not reported
7. Disability (long term) Not reported
Maternal outcomes: No maternal outcomes reported. |
|
|
Sung, 2016 |
Type of study: retrospective cohort study
Setting: tertiary referral hospital
Country: Seoul, Korea
Source of funding: non-commercial (Ministry of Health and Welfare, Republic of Korea)
|
Inclusion criteria: Twin pregnancies having both twin fetuses alive at 34 weeks of gestation and delivered at or beyond 34 weeks of gestation.
Exclusion criteria: Twin pregnancies complicated by twin-to-twin transfusion syndrome (TTTS), monoamniotic twins, fetal death before 34 weeks of gestation or chromosomal anomalies or major congenital malformation in one or both twins, and unknown chorionicity
N total at baseline: 302 Term: 112 Late-preterm: 190
Important prognostic factors2: Age ± SD: Term: 30.4 ± 3.1 yrs Late-preterm: 30.9 ± 4.0 yrs
Groups comparable at baseline?
|
Term group: twins born at or beyond 37 0/7 weeks of gestation
|
Late-preterm group: twins born at a gestational age between 34+ 0/7 weeks and 36+ 6/7 weeks |
Length of follow-up: from 35 weeks till ≥39 weeks of gestation
Loss-to-follow-up: 0 Intervention:
|
Neonatal outcomes:
1. Perinatal death Defined as neonatal death Term: 1/224 Late-preterm: 1/372 P=1.000
Defined as fetal death (stillbirth) Term: 0/112 Late-preterm: 4/190 P=0.301
2. Neonatal infection No quantitative data for each gestational week reported
3. Apgar score of less than 7 at 5 minutes Term: 2/224 Late-preterm: 4/372 P=1.000
4. NICU/hospital admission Defined as NICU admission Term: 15/224 Late-preterm: 129/372 P<0.001
5. Birthweight, mean±SD (kg) Term: 2.53±0.35 Late-preterm: 2.29±0.37 P<0.001
6. Acute TTS Not reported
7. Disability (long term) Not reported
Maternal outcomes: 1. Mode of delivery Defined as vaginal-vaginal Term: 14/112 Late-preterm: 18/190
Defined as caesarean-caesarean Term: 98/112 Late-preterm: 172/190 P=0.409
2. Postpartum hemorrhage Not reported
3. Analgesia Not reported
4. Perineal trauma Not reported
5. Breastfeeding at discharge Not reported
6. Maternal satisfaction Not reported
7. Psychological well-being/ anxiety Not reported |
Seems to be the same study as Lee (2016), but other numbers of deliveries were reported. |
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Cheong-See, 2016 |
Yes |
Yes |
No, excluded studies not described |
Yes |
Yes |
Yes |
Yes |
Yes |
No, not for the included studies |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Risk of bias table for intervention studies (observational: non-randomized clinical trials, cohort and case-control studies)
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Lee and Sung 2016 |
Unlikely |
Unclear, follow-up time not reported |
Unlikely |
Unlikely |
- Failure to develop and apply appropriate eligibility criteria: a) case-control study: under- or over-matching in case-control studies; b) cohort study: selection of exposed and unexposed from different populations.
- 2 Bias is likely if: the percentage of patients lost to follow-up is large; or differs between treatment groups; or the reasons for loss to follow-up differ between treatment groups; or length of follow-up differs between treatment groups or is too short. The risk of bias is unclear if: the number of patients lost to follow-up; or the reasons why, are not reported.
- Flawed measurement, or differences in measurement of outcome in treatment and control group; bias may also result from a lack of blinding of those assessing outcomes (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Failure to adequately measure all known prognostic factors and/or failure to adequately adjust for these factors in multivariate statistical analysis.
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
D'Antonio 2019 |
No studies >37 weeks of gestation included. Observational studies. |
|
MONOMONO Working Group 2019 |
Wrong comparison: inpatient versus outpatient management |
|
Murray 2019 |
Wrong study design: Chorionicity as covariate in model. No comparison <37 weeks and >37 weeks. |
|
Ko 2018 |
No distinction between mono and dicho |
|
Saccone 2016 |
No distinction between mono and dicho |
|
Berezowsky 2016 |
Included in Cheong-See 2016. Observational study |
|
Simoes 2016 |
37 weeks not included in analysis (only ≥36 weeks) |
|
Page 2015 |
No distinction between monochorionic and dichorionic |
|
Vilchez 2015 |
wrong comparison: 37 weeks not included in analysis. Twin pregnancy compared to singleton pregnancy. No distinction between monochorionic and dichorionic |
|
Burgess 2014 |
Included in Cheong-See 2016. |
|
Dias 2014 |
Non systematic review: overview article |
|
Dodd 2014 |
No distinction between monochorionic and dichorionic. Only 2 RCT's included (Dodd 2012, Suzuki, 2000) |
|
Ganchimeg 2014 |
Before search date (dec 2015) Cheong-See, 2016 |
|
Danon 2013 |
Wrong comparison: monochorionic versus dichorionic (32-33, 34-35 and 36-37 weeks) |
|
D'Antonio 2013 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Vergani 2013 |
Before search date (dec 2015) Cheong-See, 2018 |
|
Dodd 2012 |
Included in Cheong-See 2016. |
|
Doss, 2012 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Sela 2012 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Sullivan 2012 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Jha 2011 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Vayssiere 2011 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Zipori 2011 |
Before search date (dec 2015) Cheong-See, 2017 |
|
Dodd 2010 |
Protocol for RCT about the optimal time of birth for women with an uncomplicated multiple pregnancy at and beyond 37 weeks gestation |
|
Lopriore 2008 |
Before search date (dec 2015) Cheong-See, 2017 |
Beoordelingsdatum en geldigheid
Publicatiedatum : 25-07-2022
Beoordeeld op geldigheid : 25-07-2022
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Optimale termijn bevalling monochoriale tweelingen |
NVOG |
2022 |
2027 |
5 jaar |
NVOG |
Nieuwe literatuur |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De ontwikkeling van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
De richtlijn is ontwikkeld in samenwerking met:
- Nederlandse Vereniging voor Kindergeneeskunde
- Koninklijke Nederlandse Organisatie van Verloskundigen
- Nederlandse Vereniging voor Anesthesiologie
- Patiëntenfederatie Nederland
- Nederlandse Vereniging voor Ouders van Meerlingen
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2019 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor vrouwen zwanger van een meerling.
Werkgroep
- Dr. C.J. (Caroline) Bax, gynaecoloog-perinatoloog, werkzaam in het Amsterdam UMC te Amsterdam, NVOG (voorzitter)
- Dr. K.E.A. (Karien) Hack, gynaecoloog, werkzaam in Gelre Ziekenhuizen, locatie Apeldoorn, NVOG
- Dr. J.M. (Annemieke) Middeldorp, gynaecoloog-perinatoloog, werkzaam in het Leids Universitair Medisch Centrum te Leiden, NVOG
- Dr. M. (Marieke) Sueters, gynaecoloog, werkzaam in het Leids Universitair Medisch Centrum te Leiden, NVOG
- Dr. P.L.J. (Philip) DeKoninck, gynaecoloog-perinatoloog, werkzaam in het ErasmusMC Sophia te Rotterdam, NVOG
- Dr. J.B. (Jan) Derks, gynaecoloog-perinatoloog, werkzaam in het UMC Utrecht te Utrecht, NVOG
- Prof. dr. E. (Enrico) Lopriore, kinderarts-neonatoloog, werkzaam in het Leids Universitair Medisch Centrum te Leiden, NVK
- Drs. M.L. (Mark) van Zuylen, anesthesioloog, werkzaam in het Amsterdam UMC te Amsterdam, NVA
- Drs. I.C.M. (Ingrid) Beenakkers, anesthesioloog, werkzaam in het UMC Utrecht te Utrecht, NVA
- H. (Hanna) den Hartog-van Veen, zelfstandig verloskundige te Alphen aan den Rijn, KNOV
- J. (Jolein) Vernooij, klinisch verloskundige, werkzaam in het OLVG te Amsterdam, KNOV
- J.C. (Anne) Mooij, MSc, adviseur, Patientenfederatie Nederland
- Dr. S.V. (Steven) Koenen, gynaecoloog, werkzaam in het ETZ, locatie Elisabeth Ziekenhuis, NVOG, lid stuurgroep
- Dr. J.J. (Hans) Duvekot, gynaecoloog, werkzaam in het Erasmus MC, NVOG, lid stuurgroep
Meelezers
- J. (José) van Bijsterveld, Nederlandse Vereniging voor Ouders van Meerlingen
- J.D.M. (Jacobien) Wagemaker, MSc, Care4Neo
- Leden van de Otterlo-werkgroep (2020)
Met ondersteuning van
- Dr. J. (Janneke) Hoogervorst-Schilp, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. L. (Laura) Viester, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. M.A.C. (Marleen) van Son, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. W.J. (Wouter) Harmsen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Bax* |
Gynaecoloog-perinatoloog Amsterdam UMC |
Gastvrouw Hospice Xenia Leiden (onbetaald) |
Geen |
Geen actie |
|
Beenakkers |
Anesthesioloog UMCU/WKZ |
Geen |
Geen |
Geen actie |
|
DeKoninck |
Gynaecoloog, Erasmus MC |
Geen |
Geen |
Geen actie |
|
Derks |
Gynaecoloog/ perinatoloog |
Geen |
Geen |
Geen actie |
|
Duvekot |
Gynaecoloog, Erasmus MC |
Directeur 'Medisch Advies en Expertise Bureau Duvekot', Ridderkerk, ZZP'er |
Geen |
Geen actie |
|
Hack |
Gynaecoloog, Gelre Ziekenhuizen Apeldoorn |
Bestuurslid Werkgroep Klinische Verloskunde (NVOG) - onbetaald |
|
Geen actie |
|
Koenen |
Gynaecoloog, ETZ Tilburg |
Incidenteel juridische expertise (betaald) |
Geen |
Geen actie |
|
Lopriore |
Hoofd afdeling neonatologie LUMC sinds 2013 hoogleraar neonatologie, in het bijzonder foetale geneeskunde sinds 2016 |
Geen |
Geen |
Geen actie |
|
Middeldorp |
Leids Universitair Medisch Centrum |
Geen |
LUMC is nationaal verwijscentrum voor foetale behandeling, dus ook voor de behandeling van gecompliceerde monochoriale zwangerschappen. |
Geen actie |
|
Mooij |
Adviseur Patientenbelang, Patientenfederatie Nederland |
Geen |
Geen |
Geen actie |
|
Sueters |
Gynaecoloog, LUMC |
Geen |
Geen |
Geen actie |
|
Van Zuylen |
Anesthesioloog i.o. Amsterdam UMC- locatie AMC |
Geen |
Geen |
Geen actie |
|
Van Veen |
1e lijns verloskundige, zzp'er, waarneemster voor Vivre praktijk voor verloskunde en echoscopie in Alphen a/d Rijn |
Sensiplanconsulente: cursussen geven, vrijwilligersvergoeding. Toetsgroepbegeleider: voor 1e lijns verloskundigen, onbetaald |
Geen |
Geen actie |
|
Vernooij |
Klinisch verloskundige (1fte) - Physician Assistant in opleiding - klinisch verloskundige Werkgever: OLVG locatie Oost, Amsterdam |
Geen |
Geen |
Geen actie |
*Voorzitter werkgroep
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door vertegenwoordigers van de Patiëntenfederatie Nederland en de Nederlandse Vereniging voor Ouders van Meerlingen af te vaardigen in de clusterwerkgroep. De conceptrichtlijn werd tevens ter commentaar voorgelegd aan de betrokken patiëntenverenigingen.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens is er een knelpunteninventarisatie gedaan in november 2018 middels een Invitational conference met onder andere meerlingen als onderwerp.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodules worden aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren worden de conceptrichtlijnmodules aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodules worden aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas, T., Merglen, A., Heen, A. F., Kristiansen, A., Neumann, I., Brito, J. P.,... & Guyatt, G. H. (2017). UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ open, 7(11).
Alonso-Coello, P., Schünemann, H. J., Moberg, J., Brignardello-Petersen, R., Akl, E. A., Davoli, M.,... & Morelli, A. (2018). GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. Gaceta sanitaria, 32(2), 166-e1.
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G.,... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Cmaj, 182(18), E839-E842.
Hultcrantz, M., Rind, D., Akl, E. A., Treweek, S., Mustafa, R. A., Iorio, A.,... & Katikireddi, S. V. (2017). The GRADE Working Group clarifies the construct of certainty of evidence. Journal of clinical epidemiology, 87, 4-13.
Richtlijnen, A., & Kwaliteit, R. (2012). Medisch specialistische richtlijnen 2.0. Utrecht: Orde van Medisch Specialisten.
https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Neumann, I., Santesso, N., Akl, E. A., Rind, D. M., Vandvik, P. O., Alonso-Coello, P.,... & Guyatt, G. H. (2016). A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. Journal of clinical epidemiology, 72, 45-55.
Schünemann, H., Brożek, J., Guyatt, G., & Oxman, A. (2013). GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from guidelinedevelopment. org/handbook. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E.,... & Bossuyt, P. (2008). Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. Bmj, 336(7653), 1106-1110.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Uitgangsvraag: Wat is de optimale timing voor electieve inductie bij een ongecompliceerde monochoriale (UV3)/dichoriale (UV4) biamniotische gemelli zwangerschap ten opzichte van afwachtend beleid? |
|
|
Database(s): Medline, Embase |
Datum: 17 december 2019 |
|
Periode: 2008 - current |
Talen: Engels |
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
|
1 exp Pregnancy, Multiple/ or exp Multiple Birth Offspring/ or twin*.ti,ab,kf. or (multiple adj2 (pregnanc* or gestation*)).ti,ab,kf. (71517) 2 (exp Labor, Induced/ or labo*r.ti,ab,kf. or delivery.ti,ab,kf. or parturition.ti,ab,kf.) and (elective or planned or time or timing).ti,ab,kf. and (week*.ti,ab,kw. or term.ti,ab,kf.) (24764) 3 1 and 2 (1079) 4 limit 3 to (english language and yr="2008 -Current") (580) 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (424152) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1927809) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3323916) 8 4 and 5 (38) 9 (4 and 6) not 8 (91) 10 (4 and 7) not (8 or 9) (296) 11 8 or 9 or 10 (425)
38 SRs + 92 RCTs + 296 observationeel = 425 totaal (71 uniek) |
543 |
|
Embase
|
'multiple pregnancy'/exp OR 'multiple birth offspring'/exp OR 'dichorionic twin pregnancy'/exp OR 'monochorionic twin pregnancy'/exp OR twin*:ti,ab OR ((multiple NEAR/2 (pregnanc* OR gestation*)):ti,ab) AND ('labor induction'/exp OR labo*r:ti,ab OR delivery:ti,ab OR parturition:ti,ab) AND (elective:ti,ab OR planned:ti,ab OR time:ti,ab OR timing:ti,ab) AND (week*:ti,ab OR term:ti,ab) AND (english)/lim AND (2008-2019)/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
Gebruikte filters: Systematic reviews: 'meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de = 45
RCTs: 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti = 131
Observationele studies: 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) = 310
Totaal = 486 (472 uniek) |
