SGLT2-remmers bij zeerhoogrisicopatiënten met diabetes mellitus type 2 (DM2)
Uitgangsvraag
Wat is de optimale medicamenteuze behandeling van volwassen personen met DM2 en een zeer hoog risico op hart- en vaatziekten: toevoeging van een SGLT2-remmer?
What is the optimal pharmacotherapy of adults with diabetes mellitus type 2 and a very high risk of cardiovascular disease: supplementation of a SGLT-2 inhibitor?
Aanbeveling
Overweeg het gebruik van een SGLT2-remmer als monotherapie of toegevoegd aan metformine en/of elke andere combinatie van glucoseverlagende therapie (inclusief insulinetherapie) bij volwassenen met DM type 2 indien er sprake is van een zeer hoog risico op hart- en vaatziekten:
- eerder bewezen hart- en vaatziekten (inclusief hartfalen, ongeacht ejectiefractie) en/of
- chronische nierschade met: eGFR 20-44 ml/min/1,73 m2 zonder of met verhoogde albuminurie, eGFR 45-59 ml/min/1,73 m2 met matig verhoogde albuminurie (ACR > 3 mg/mmol/l) of eGFR ≥ 60 ml/min/1,73 m2 met ernstig verhoogde albuminurie (ACR > 30 mg/mmol)
Start een behandeling met SGLT2-remmers alleen bij een eGFR > 20 ml/min/1,73 m2. Indien de eGFR daalt tot < 20 ml/min/1,73 m2 tijdens gebruik van de SGLT2-remmer wordt geadviseerd om deze te continueren en pas te staken bij de start van dialyse.
Gebruik geen SGLT2-remmers indien er sprake is van recidiverende genitale (mycotische) infecties of indien er een verhoogd risico is op ketoacidose, zoals bij alcoholisme, ondervoeding, intermitterend vasten of een dieet met < 70 gram koolhydraten per dag. Staak het medicament als een voetulcus ontstaat.
Licht de patiënt in over het mogelijk optreden en herkennen van genitale bijwerkingen (met name mycotische infecties).
Bespreek met de patiënt de risicofactoren en symptomen van ketoacidose en informeer de patiënt over de noodzaak om inname van de SGLT2-remmer (tijdelijk) te staken bij elke situatie waarin de voedselinname fors verminderd is, bij koortsende ziekte, misselijkheid, braken, extreme dorst, diarree en bij een chirurgische ingreep, en om in deze gevallen contact op te nemen met de behandelend arts.
Bovenstaande aanbevelingen gelden ook voor kwetsbare ouderen.* Houdt hierbij wel rekening met de individuele patiëntkenmerken, de specifieke behandeldoel(en) en de hogere kans op bijwerkingen bij ouderen.
*Let op: dit beleid wijkt af van dat in de eerste lijn; informeer de huisarts hierover wanneer een patiënt wordt terugverwezen naar de eerste lijn.
Zie voor de positie van SGLT2-remmers in het medicamenteuze stappenplan van volwassenen met DM type 2 en een zeer hoog risico op hart- en vaatziekten de module ‘Stappenplan zeerhoogrisicopatiënten’.
Overwegingen
De literatuuranalyse is gebaseerd op de systematische review en netwerk meta-analyse van Palmer (2021). De systematische review van Palmer (2021) is uitgevoerd door een internationaal consortium en vormt de basis van de (MAGICapp) richtlijn 'Risk-based treatment with SGLT2 inhibitors or GLP-1 receptor agonists for adults with type 2 diabetes' (Li, 2021). In het kader van de bewuste richtlijn zijn 2 systematische reviews uitgevoerd naar de waarden en voorkeuren van personen met DM2 (González-González, 2021) en naar predictiemodellen voor cardiovasculaire en renale uitkomsten bij personen met DM2 (Buchan, 2021). Deze publicaties vormen de basis voor de huidige richtlijn en zijn aangevuld met argumenten en overwegingen van de richtlijnwerkgroep.
Note: in de 2026 update van deze module is enkel informatie over toegevoegd over de inzet van SGLT-remmers bij kwetsbare patiënten en/of ouderen. De systematische literatuuranalyse is niet geüpdatet.
Voor- en nadelen
Palmer (2021) onderscheidt een vijftal risicogroepen waarvan er 3 relevant zijn voor de huidige richtlijnmodule, die specifiek gericht is op personen met DM2 en een zeer hoog risico volgens de CVRM-richtlijn (NHG/NIV/NVvC, 2019). De absolute effecten van behandeling zijn berekend door de relatieve effecten uit de netwerk meta-analyse te combineren met het geschatte baseline risico in elke risicogroep. Palmer (2021) baseert zich bij de schatting van het baselinerisico met name op het predictiemodel RECODe (https://sanjaybasu.shinyapps.io/recode). Dit risicomodel is alleen gevalideerd voor de VS. Een schatting van de baselinerisico's voor cardiovasculaire en renale eindpunten in de Nederlandse situatie geeft echter aan dat de baselinerisico's die Palmer hanteert ook een goed uitgangspunt zijn voor de Nederlandse situatie (zie voor verdere toelichting de ‘Overwegingen’ in de module ‘Stappenplan zeerhoogrisicopatiënten’).
De resultaten (zie ‘Samenvatting literatuur’) kunnen als volgt worden samengevat:
Bij personen met DM2 en eerder bewezen hart- en vaatziekten leidt toevoeging van een SGLT2-remmer aan de standaardzorg gedurende 5 jaar tot een afname in totale sterfte (18 minder per 1000 personen), sterfte door hart- en vaatziekten (12 minder per 1000 personen), niet-fatale hartinfarcten (13 minder per 1000 personen), eindstadium nierfalen (6 minder per 1000 personen), en ziekenhuisopnames voor hartfalen (23 minder per 1000 personen), met weinig tot geen effect op het risico op een niet-fatale beroerte of diabetische ketoacidose. Behandeling met een SGLT2-remmer verhoogt het risico op (mycotische) genitale infecties (143 meer per 1000 personen) en verhoogt mogelijk het risico op amputaties (6 meer per 1000 personen; onzekere effectschatting).
Bij personen met DM2 en chronische nierschade (gedefinieerd als eGFR 45-75 ml/min/ 1,73 m2 met ACR > 30 mg/mmol of eGFR 15-45 ml/min/1,73 m2) leidt toevoeging van een SGLT2-remmer aan de standaardzorg tot een afname in totale sterfte (26 minder per 1000 personen), sterfte door hart- en vaatziekten (16 minder per 1000 personen), niet-fatale hartinfarcten (14 minder per 1000 personen), eindstadium nierfalen (25 minder per 1000 personen), en ziekenhuisopnames voor hartfalen (29 minder per 1000 personen), met weinig tot geen effect op het risico op een niet-fatale beroerte of diabetische ketoacidose. Behandeling met een SGLT2-remmer verhoogt het risico op (mycotische) genitale infecties (143 meer per 1000 personen) en verhoogt mogelijk het risico op amputaties (8 meer per 1000 personen; onzekere effectschatting).
Bij personen met DM2 en een combinatie van eerder bewezen hart- en vaatziekten en chronische nierschade (gedefinieerd als eGFR 45-75 ml/min/1,73 m2 met ACR > 30 mg/mmol of eGFR 15-45 ml/min/1,73 m2) leidt toevoeging van een SGLT2-remmer aan de standaardzorg tot een afname in totale sterfte (40 minder per 1000 personen), sterfte door hart- en vaatziekten (24 minder per 1000 personen), niet-fatale hartinfarcten (21 minder per 1000 personen), eindstadium nierfalen (38 minder per 1000 personen), en ziekenhuisopnames voor hartfalen (58 minder per 1000 personen), met weinig tot geen effect op het risico op een niet-fatale beroerte of diabetische ketoacidose. Behandeling met een SGLT2-remmer verhoogt het risico op (mycotische) genitale infecties (143 meer per 1000 personen) en verhoogt mogelijk het risico op amputaties (13 meer per 1000 personen; onzekere effectschatting).
De winst van behandeling is weergegeven voor de afzonderlijke uitkomstmaten. Omdat patiënten met een hoog tot zeer risico op (recidief) hart- en vaatziekten kans hebben op meerdere uitkomsten gedurende de follow-upperiode, is de algemene behandelwinst aanzienlijk groter: in totaal worden bij behandeling van 1000 personen gedurende 5 jaar 59 tot 155 cardiovasculaire en renale uitkomsten voorkomen (optelsom van totale sterfte, niet-fataal hartinfarct, niet-fatale beroerte, ziekenhuisopnames voor ernstig hartfalen en eindstadium nierfalen). Dit vertaalt zich in een NNT van 6 tot 17, afhankelijk van de risicogroep: 6 tot 17 patiënten moeten gedurende 5 jaar behandeld worden met SGLT2-remmers om 1 van die uitkomsten te voorkomen. Deze algemene NNT voldoet ruim aan de grens voor klinische besluitvorming die de werkgroep heeft vastgesteld (een maximale 5jaars-NNT van 30).
Aanvullende argumenten
Het primaire langetermijndoel van de behandeling van DM2 is het voorkomen van complicaties, zoals hart- en vaatziekten, nierfalen, blindheid, en amputaties met als resultaat een verbeterde kwaliteit van, en indien mogelijk, langer leven. De netwerk meta-analyse (Palmer, 2021) hanteert bij het definiëren van de patiëntenpopulatie een enigszins andere definitie voor chronische nierschade (eGFR 15-45 ml/min/1,73 m2 of eGFR 45-75 ml/min/1,73 m2 met ACR > 30 mg/mmol) dan de uitgangsvraag. De werkgroep is echter van mening dat dit niet leidt tot relevante problemen bij de interpretatie van de resultaten. Dit is daarom voor de werkgroep geen reden om de bewijskracht van de literatuurconclusie (verder) af te waarderen voor indirectheid. De definitie van de netwerk meta-analyse overlapt grotendeels met de definitie in de huidige richtlijn: eGFR < 30 ml/min/1,73 m2; eGFR 30-59 ml/min/1,73 m2 met ACR > 3 mg/mmol; of eGFR ≥ 60 ml/min/1,73 m2 met ACR > 30 mg/mmol. De discrepantie zit in de groep met een eGFR 45-59 ml/min/1,73 m2 en ACR 3-30 mg/mmol, die niet wordt beschreven in de netwerk meta-analyse en wel in de uitgangsvraag. Er zijn echter aanwijzingen dat bij mensen met DM2 de combinatie van een eGFR 45-59 ml/min/1,73 m2 en ACR 3-30 mg/mmol gepaard gaat met een zeer hoog risico op 10-jaarssterfte aan hart- en vaatziekten (sterfterisico > 10% conform de CVRM-richtlijn, NHG/NIV/NVVC, 2019; Ninomiya, 2009). Post-hoc analyses suggereren consistente effecten van SGLT2-remmers op alle relevante uitkomstmaten beoordeeld op basis van gegevens van personen met een gradatie in eGFR en ACR (Zelniker, 2019; Neuen, 2019). Omdat een eGFR van ≥ 30 ml/min/1,73 m² het inclusiecriterium was in alle cardiovasculaire veiligheidsstudies met SGLT2-remmers, met uitzondering van DECLARE-TIMI 58, waarbij een eGFR van ≥ 60 ml/min/1,73 m2 vereist was, kunnen de gerapporteerde effecten op de harde eindpunten niet direct worden geëxtrapoleerd naar eGFR < 30 ml/min/1,73 m². Inmiddels is de SPC (summary of product characteristics) voor empagliflozine en dapagliflozine o.b.v. studies aangepast; Starten van de behandeling bij een eGFR < 20 ml/min ontraden, wegens beperkte ervaring.
In de netwerk meta-analyse (Palmer, 2021) werden onder andere de volgende harde eindpunten gerapporteerd: totale mortaliteit, sterfte aan hart- en vaatziekten, niet-fataal hartinfarct, niet-fatale beroerte, ziekenhuisopnames voor hartfalen, en eindstadium nierfalen (eGFR < 15 ml/min/1,73 m2 of start nierfunctievervangende therapie). Palmer heeft expliciet gekozen voor de afzonderlijke uitkomstmaten en niet een samengestelde uitkomstmaat, zoals het frequent gerapporteerde MACE (sterfte aan hart- en vaatziekten, niet-fataal hartinfarct, niet-fatale beroerte) of een samengesteld renaal eindpunt bestaand uit 40% afname in eGFR, eindstadium van nierziekte of overlijden door nierziekte. In de huidige richtlijn volgen wij deze strategie en zullen er geen data over deze samengestelde eindpunten gerapporteerd worden. Het is echter goed te realiseren dat SGLT2-remmers tegelijkertijd meerdere afzonderlijke uitkomstmaten gunstig beïnvloeden. Verder hebben wij afgezien van een rapportage over het eindpunt acuut nierfalen, omdat de gebruikte definities voor dit eindpunt in de studies te heterogeen waren. Samengevat leidt toevoeging van een SGLT2-remmer aan andere glucoseverlagende therapie bij personen met DM2 en eerder bewezen hart- en vaatziekten en/of chronische nierschade (gedefinieerd als eGFR 15-45 ml/min/1,73 m2 of eGFR 45-75 ml/min/1,73 m2 met ACR > 30 mg/mmol; Palmer, 2021) tot een afname in totale mortaliteit, afname in sterfte aan hart- en vaatziekten, en een afname in nierfalen (bewijskracht volgens GRADE: redelijk tot hoog).
Bijwerkingen
In de netwerk meta-analyse (Palmer, 2021) werden de belangrijke bijwerkingen ketoacidose en (mycotische) genitale infecties gerapporteerd. Bij personen met DM2 leidt toevoeging van een SGLT2-remmer aan andere glucoseverlagende therapie tot een toename van (mycotische) genitale infecties, maar lijkt er geen belangrijk verschil te zijn in het risico op ketoacidose (bewijskracht volgens GRADE: hoog). Desondanks is de werkgroep van mening dat het (kleine) risico op ketoacidose en de risicofactoren en symptomen van ketoacidose met de patiënt besproken moeten worden. Informeer de patiënt over de noodzaak om inname van de SGLT2-remmer (tijdelijk) te staken bij misselijkheid, braken, diarree, extreme dorst en bij een chirurgische ingreep, en om in deze gevallen contact op te nemen met de behandelend arts. Wees terughoudend met het gebruik van SGLT2-remmers indien er een verhoogd risico is op ketoacidose, zoals bij alcoholisme, ondervoeding (gewichtsverlies van > 5% binnen 1 maand of > 10% binnen 6 maanden en/of een te laag lichaamsgewicht (18-65 jaar: BMI < 18,5 en > 65 jaar: BMI < 20 (Artsenwijzer Diëtiek)), intermitterend vasten of een sterk koolhydraatbeperkt dieet (< 70 gram koolhydraten per dag). Het gebruik van SGLT2-remmers is geassocieerd met een toename van genitale mycotische infecties. Een mycotische infectie is geen reden om SGLT2-remmers direct te staken en is over het algemeen goed te behandelen met een antimycotisch middel. Als de mycotische infectie ondanks een antimycotische behandeling recidiveert, heroverweeg dan de voortzetting van de SGLT2-remmer.
Er was weinig tot geen bewijs voor de effecten van SGLT2-remmers op amputatie, blindheid, oogaandoeningen die interventie behoeven, gangreen van Fournier en neuropathische pijn. Vanwege het amputatierisico in de CANVAS-trial zijn tijdens de DECLARE-TIMI-studie mensen met een amputatie in de voorgeschiedenis geëxcludeerd en werd het gebruik van dapagliflozine gestaakt bij symptomen van perifeer vaatlijden, zoals perifere ischemie of infectie. De netwerk meta-analyse (Palmer, 2021) geeft aan dat behandeling met SGLT2-remmers mogelijk resulteert in een toename van het aantal amputaties: afhankelijk van de risicogroep (eerder bewezen hart- en vaatziekten, chronische nierschade, of beide) 6-13 extra amputaties per 1000 mensen na 5 jaar behandeling. De effectschattingen zijn echter erg onnauwkeurig, de betrouwbaarheidsintervallen lopen van 2-4 minder amputaties tot 16-23 meer amputaties, en de bewijskracht volgens GRADE is laag. Men dient zich niettemin bewust te zijn van deze mogelijke bijwerking, ook al is er (nog) geen causaal verband aangetoond. Bij het ontstaan van een voetulcus dient de SGLT2-remmer te worden gestaakt (zie ook ‘Overwegingen’ in de module ‘Stappenplan’). Er zijn meldingen van gangreen van Fournier bij gebruik van SGLT2-remmers met de werkzame stof canagliflozine, dapagliflozine, empagliflozine of ertugliflozine. Gangreen van Fournier is een zeldzame, maar ernstige en levensbedreigende infectie. Het risico op gangreen van Fournier is ook opgenomen in de bijsluiter (CBG, 2020). In de netwerk meta-analyse (Palmer, 2021) is er mogelijk geen effect op gangreen van Fournier: 0 minder (1 minder tot 18 meer) per 1000 mensen na 5 jaar behandeling (bewijskracht volgens GRADE: laag). Men dient zich niettemin bewust te zijn van deze mogelijke bijwerking, ook al is er (nog) geen causaal verband aangetoond (Bersoff-Matcha, 2019). Behandelaars wordt geadviseerd om bij het vermoeden op gangreen van Fournier te stoppen met het gebruik van SGLT2-remmers en onmiddellijk te starten met een gerichte behandeling. Verder is er geen verhoogd risico op botfracturen (Cheng, 2019).
Ouderen en kwetsbaarheid
Veel ouderen hebben DM2, hartfalen en chronische nierinsufficiëntie, of meerdere van deze aandoeningen en komen daardoor in aanmerking voor een SGLT2-remmer. Binnen de populatie oudere patiënten kan onderscheid gemaakt worden tussen ‘fitte’ en kwetsbare ouderen. Een op de vijf ouderen behoort tot de populatie kwetsbare ouderen. Bij kwetsbare ouderen zijn artsen vaak terughoudend met het voorschrijven van nieuwe middelen vanwege twijfel over de balans tussen de potentieel gunstige effecten en de nadelen bij deze populatie. Kwetsbare ouderen zijn ondervertegenwoordigd in klinische onderzoeken. Het risico op geneesmiddelbijwerkingen is bij hen verhoogd (Van Marum, 2020). De presentatie van bijwerking bij ouderen kan bovendien anders. Onder andere volumedepletie is een relevant bijwerking bij oudere patiënten. Het expertisecentrum farmacotherapie bij ouderen (Ephor) levert uitgebreide informatie over het gebruik van SGLT-2 remmers bij ouderen.
In grote studies naar MACE en chronische nierfunctiestoornissen bij patiënten met DM2 zijn ouderen ≥75 jaar in het algemeen ondervertegenwoordigd, maar subgroep- en post-hocanalyses laten zien dat er geen leeftijd gerelateerde verschillen zijn (Karagiannis, 2021 en Perkovic, 2024), maar kwetsbaarheid is hierbij niet meegenomen. Voor verdere inleiding over kwetsbaarheid, zie Module Inleiding kwetsbaarheid van de richtlijn Cardiovasculair risicomanagement (CVRM) en Kim (2024).
Een Nederlands artikel (Van Bruggen DM, 2024) geeft een overzicht van de literatuur over de klinische effecten van SGLT2-remmers bij kwetsbare ouderen, vergeleken met niet-kwetsbare ouderen en de algemene volwassen populatie. Startpunt van deze review zijn de grote placebogecontroleerde onderzoeken naar cardiovasculaire eindpunten, met hierbij vooraf gedefinieerde analyses en post-hoc analyses naar leeftijd en kwetsbaarheid. Hoewel het onderzoek ook mensen zonder diabetes betreft zijn de conclusies van toepassing op patiënten met DM2 en een zeer hoog risico op hart- en vaatziekten. De bevindingen zijn daarom integraal overgenomen. De kernpunten uit het artikel zijn als volgt:
- Bij oudere patiënten die vooral kwetsbaar zijn vanwege een chronische cardiovasculaire aandoening verminderen SGLT2- remmers het aantal ziekenhuisopnames vanwege hartfalen, en verbeteren ze de symptoomlast.
- Op basis van de huidige literatuur zijn SGLT2-remmers even effectief bij jongere als oudere patiënten; wel hebben ouderen een hoger risico op bijwerkingen.
- Analyses van placebogecontroleerde onderzoeken naar kwetsbaarheid laten ook positieve effecten zien van SGLT2-remmers bij ouderen die kwetsbaar zijn op basis van cardiovasculaire ziekte.
- Patiënten met ernstige co-morbiditeit en algemene kwetsbaarheid (> 5 punten op de ‘clinical frailty scale’) namen geen deel aan de huidige trials naar SGLT2-remmers; voorzichtigheid met voorschrijven, rekening houdend met de individuele patiëntkenmerken (o.a. levensverwachting, voedingsstatus en gewichtsverloop), de specifieke behandeldoel(en) en potentiële bijwerking van het middel is hier op zijn plaats.
- ‘Sick day rules’ Om bijwerkingen te voorkomen, moeten patiënten worden geïnformeerd wanneer zij (tijdelijk) moeten stoppen met het gebruik van een SGLT2-remmer. Voor oudere patiënten gelden de sick day rules voor volwassen patiënten (zie ook module Stappenplan).
SGLT2-remmers worden in zowel nationale als internationale richtlijnen aanbevolen bij de behandeling van chronisch hartfalen, dit zowel bij patiënten met een verlaagde als behouden linkerventrikelfunctie (HFrEF, HFpEF en HFmrEF). Dit advies is gebaseerd op vier grote placebogecontroleerde studies (DAPA-HF, EMPEROR-Reduced, DELIVER en EMPEROR-preserved), die aantonen dat deze remmers het risico op cardiovasculaire sterfte en ziekenhuisopnames door hartfalen verlagen. Bij de leeftijdsanalyses blijkt dat minder dan een derde van de HFrEF-onderzoekspopulatie 75 jaar of ouder is, terwijl bij HFpEF dit percentage bijna de helft is.
HFpEF-studies zijn over het algemeen beter te extrapoleren naar kwetsbare ouderen omdat HFpEF vaker voorkomt bij ouderen en wordt beschouwd als een geriatrisch syndroom vanwege de sterke samenhang met leeftijd en comorbiditeiten zoals diabetes type 2 en atriumfibrilleren. Voor de kwetsbaarheidsanalyses is het relevant te vermelden dat in de onderzoeken steeds dezelfde ‘frailty index’ (FI), gebaseerd op de ‘cumulative deficit approach’ van Rockwood is gebruikt. Op basis hiervan werden patiënten verdeeld in drie groepen: niet kwetsbaar (FI-klasse 1), matig kwetsbaar (FI-klasse 2) en meest kwetsbaar (FI-klasse 3) (Butt, 2022-a en -b).
SGLT2-remmers verlagen het risico op cardiovasculaire sterfte (HR: 0,87; 95%-BI: 0,79-0,95) (Vaduganathan, 2022). Ook verlagen ze ziekenhuisopnames door hartfalen (HR: 0,72; 95%-BI: 0,67-0,78) (Vaduganathan, 2022) met een snelle ‘time-to-benefit’ van twee tot vier weken. Dit lagere risico op ziekenhuisopnames is extra belangrijk voor kwetsbare ouderen, die een groter risico lopen op functionele achteruitgang na een opname. In secundaire analyses is de risico-afname van cardiovasculaire uitkomstmaten consistent in alle onderzochte leeftijdscategorieën (< 65, 65-74, ≥ 75 jaar) en in alle drie de FI-klassen (Butt, 2022-a en -b en Martinez, 2020 en Böhm, 2022). De absolute risicoreductie was het grootst bij de meest kwetsbare patiënten (FI-klasse 3) (Butt, 2022-a).
De grote studies naar cardiovasculaire uitkomstmaten rapporteren ook uitkomstmaat symptoomlast tgv. hartfalen. In het algemeen wordt hiervoor een variant gebruikt van de ‘Summary Score’ van de Kansas City Cardiac Questionnaire (de KCCQ-CS- of KCCQ-OS-score) waarin een verbetering van 5 punten als klinisch relevant wordt beschouwd. Een meta-analyse liet een verbetering zien in de gemiddelde KCCQ-CS-score en KCCQ-OS-score ten opzichte van placebo (gemiddelde verschil KCCQ-CS-score: 5,17; 4,61- 5,73, gemiddelde verschil KCCQ-OS-score 4,00; 3,44- 4,56) (Guo, 2023). Post-hocanalyses toonden aan dat de verbetering in symptoomscore onafhankelijk is van leeftijd en kwetsbaarheid (Böhm, 2022). De verbetering is het grootst in de kwetsbaarste groep en trad relatief kort (circa vier maanden) na het begin van de behandeling op (Butt, 2022-b). Studies naar functionele verbetering lieten nog geen eenduidig resultaat zien, maar de trends zijn positief (Voorrips, 2022).
SGLT2-remmers laten renoprotectieve effecten zien – afname van het risico op eindstadium nierfalen en afname van de geleidelijke achteruitgang van de geschatte renale klaring – bij patiënten met een klaring tussen 25 en 75 ml/min per 1,73 m2 en matige tot ernstige albuminurie, zowel bij patiënten met als zonder diabetes mellitus (HR: 0,61; 95%-BI: 0,51-0,72) (Heerspink, 2020). Voor empagliflozine werden vergelijkbare resultaten gezien, ook bij patiënten met eGFR 20-45 ml/min/1,73 m2 zonder albuminurie (Herrington, 2023). In subgroep-analyses naar leeftijd (> 65 jaar voor dapagliflozine; > 70 jaar voor empagliflozine) werden consistent vergelijkbare effecten gevonden. Een post-hocanalyse liet zien dat kwetsbaarheidsstatus geen invloed heeft op de effectiviteit en veiligheid van behandeling met dapagliflozine (Vart, 2023).
1. SGLT2-remmers bij ouderen met diabetes mellitus type 2
Ouderen (≥ 75 jaar) zijn in het algemeen ondervertegenwoordigd in grote studies naar MACE bij patiënten met diabetes mellitus type 2, maar subgroep- en post-hocanalyses laten zien dat er geen leeftijd gerelateerde verschillen zijn (Scheen, 2023). Onderzoek naar kwetsbare ouderen komt met name van kwetsbaarheidsanalyses bij patiënten met hartfalen. In de kwetsbaarheidsanalyses bij hartfalen had een groot deel van de patiënten met FI-klasse 3 behalve hartfalen ook diabetes mellitus type 2 (> 70%) (Butt, 2022-a en -b).
2. Potentiële nadelen
De grote gerandomiseerde onderzoeken met SGLT2-remmers laten geen leeftijdsafhankelijke verschillen zien in de veiligheid van SGLT2-remmers bij patiënten jonger of ouder dan 65 jaar. Vergelijkingen tussen patiënten jonger of ouder dan 75 jaar zijn schaars (Scheen, 2023).
• Hypoglykemieën en ketoacidose
Hoewel SGLT2-remmers aanvankelijk zijn ontwikkeld als antidiabeticum, geven ze op zichzelf geen verhoogd risico op hypoglykemie. Dat is gunstig voor ouderen met diabetes mellitus, aangezien zij een verhoogd risico hebben op hypoglykemieën, moeilijker hiervan herstellen en sneller restschade oplopen (Sircar, 2016). Het risico op hypoglykemie is wél verhoogd wanneer SGLT2-remmers gelijktijdig worden gebruikt met een sulfonylureum(SU-)derivaat of insuline. Diabetische ketoacidose (DKA) of euglykemische diabetische ketoacidose is een zeldzame, maar potentieel ernstige bijwerking van SGLT2-remmers (absoluut risico: 0,6-2,2 gebeurtenissen per 1000 persoonsjaren) (Colacci, 2022). Het risico wordt bepaald door een aantal factoren. DKA treedt namelijk op door een relatief tekort aan insuline, bijvoorbeeld door een verminderde voedselinname, dehydratie, acute ziekte, gebruik van bepaalde geneesmiddelen, overmatig alcoholgebruik of rond een operatie. Bij opname in het ziekenhuis moet het middel daarom onderbroken worden bij een grote operatieve ingreep of ernstige acute ziekte. Patiënten moeten duidelijke instructies krijgen over wanneer ze contact moeten opnemen met een arts en tijdelijk moeten stoppen met het middel volgens de ‘sick day rules’ (Goldenberg, 2016). Bovendien moet er voldoende cognitieve reserve aanwezig zijn om deze inschatting te kunnen maken, of er moet adequate (mantel)zorg zijn om de veiligheid te waarborgen.
• Genitale en urineweginfecties
Urogenitale infecties zijn bekende bijwerkingen van SGLT2-remmers. Een recente meta-analyse van 10 RCT’s liet zien dat de ‘risk ratio’ (RR) voor genitale infecties 3,56 is (95%-BI: 2,84-4,46); voor urineweginfecties is die 1,06 (95%-BI: 1,00-1,12) (Lin, 2021). Hoewel dit over het algemeen goed behandelbare bijwerkingen zijn, kunnen ze voor kwetsbare ouderen toch belastend en potentieel gevaarlijk zijn. In de SOLD-studie werd de SGLT2-remmer bijna 2 keer zo vaak gestopt bij patiënten boven de 80 jaar, meestal vanwege urogenitale infecties of intolerantie (Lunati, 2022).
• Volumedepletie en orthostatische hypotensie
Gebruik van SGLT2-remmers kan door osmotische diurese leiden tot volumedepletie. In enkele studies werd aangetoond dat deze volumedepletie vaker voorkomt naarmate de leeftijd vordert en doorgaans ernstiger is bij ouderen, mogelijk als gevolg van gelijktijdig gebruik van een lisdiureticum (Scheen, 2023). In een kleine prospectieve studie werd gezien dat kwetsbare patiënten ruim twee keer zo vaak bijwerkingen hadden vergeleken met niet-kwetsbare controles, met name dehydratie en orthostatische hypotensie. Deze klachten waren echter dermate licht van aard, dat de medicatie niet gestopt hoefde te worden (Villarreal, 2023).
Voor aanvullende aanbevelingen omtrent de zorg voor kwetsbare ouderen met diabetes verwijst het cluster naar de Richtlijn Diabetes mellitus type 2 van Verenso.
Kwaliteit van bewijs
Het door de richtlijncommissie als cruciaal benoemde samengestelde cardiovasculaire eindpunt MACE ontbreekt in de systematische review van Palmer (2021), net als een eveneens als cruciaal bestempelde composiet renaal eindpunt. Deze uitkomstmaten worden echter voldoende gedekt door de cardiovasculaire en renale eindpunten die wel worden gerapporteerd. Daarnaast ontbreekt de cruciale uitkomstmaat acuut nierfalen. Daarmee is er, met uitzondering van de uitkomstmaten acuut nierfalen (geen bewijs) en niet-fatale beroerte (lage zekerheid van bewijs), een redelijke tot hoge zekerheid van het bewijs voor de cruciale uitkomstmaten.
Waarden en voorkeuren van patiënten
Uit de systematische review van waarden en voorkeuren bij personen met DM type 2 (González-González, 2021) kwam naar voren dat er een grote variatie is in de waarde die personen met DM type 2 hechten aan de voor- en nadelen van behandeling met SGLT2-remmers (en GLP1-receptoragonisten). Sommigen gaven aan geïnteresseerd te zijn in behandeling met een SGLT2-remmer of GLP1-receptoragonist als er sprake zou zijn van een klein voordeel van behandeling (een reductie in 5-jaars absoluut risico op cardiovasculair of renaal eindpunt van minder dan 5 op 1000 personen), terwijl anderen behandeling met SGLT2-remmers pas zouden overwegen als er sprake was van substantiële voordelen (een reductie in 5-jaars absoluut risico van meer dan 30 op 1000 personen). De deelnemers aan de patiëntenfocusgroep hechtten een vergelijkbare waarde aan het voorkomen van nierfalen en het voorkomen van sterfte, terwijl minder gewicht werd toegekend aan het voorkomen van een hartinfarct, beroerte of ernstig hartfalen (geoperationaliseerd als ziekenhuisopname vanwege hartfalen). Ten slotte gaf de focusgroep aan een sterke voorkeur te hebben voor orale medicatie in vergelijking met injecties.
Uiteraard moet er aandacht zijn voor de individuele wensen van de patiënt met diabetes, die goed besproken moeten worden en als uitgangspunt dienen voor elke nieuwe interventie. Het gaat dan om goede voorlichting (over het gebruik, effect, de risico’s en verplichtingen) en gezamenlijk beslissen, alsmede correcte begeleiding gedurende de behandeling. Bij de behandeling van DM type 2 heeft de gezamenlijke besluitvorming van de patiënt en arts een belangrijke plaats. Voor- en nadelen van SGLT2-remmers ten opzichte van alternatieve behandelopties dienen helder en open besproken te worden, zodat de patiënt goed geïnformeerd deelneemt aan de gezamenlijke besluitvorming en gemotiveerd de behandeling kan voortzetten.
Kosten (middelenbeslag)
Vanaf 1 augustus 2025 zijn er geen voorwaarden meer wat betreft vergoeding van SGLT2-remmers. Er is inmiddels een aantal kosteneffectiviteitsstudies uitgevoerd waarin behandeling van personen met DM type 2 met SGLT2-remmers wordt vergeleken met placebo of alternatieve behandelopties, zoals insuline, DPP4-remmer, GLP1-receptoragonist, sulfonylureumderivaat of acarbose. Een systematische review (Rahman, 2019), die de literatuur dekt tot juni 2018, includeert 37 studies (15 voor dapagliflozine, 10 voor canagliflozine en 12 voor empagliflozine). Deze studies verschillen van elkaar in de gebruikte analytische modellen, het gehanteerde perspectief en het land (gezondheidssysteem) waarop de studie betrekking heeft. De resultaten van recente cardiovasculaire trials (DECLARE-TIMI 58, CANVAS, EMPA-REG) zijn nog niet verwerkt in de geïncludeerde kosteneffectiviteitsmodellen. Ondanks deze verschillen en tekortkomingen blijken de SGLT2-remmers in alle gevallen kosteneffectief te zijn: de gezondheidswinst bij behandeling met SGLT2-remmers woog op tegen de meerkosten, algemeen geaccepteerde grenzen voor kosteneffectiviteit (kosten per gewonnen levensjaar) werden niet overschreden (Rahman, 2019). Op basis hiervan acht de werkgroep het waarschijnlijk dat ook de inzet van SGLT2-remmers, zeker bij zeerhoogrisicopatiënten met DM type 2 kosteneffectief zal zijn.
Aanvaardbaarheid
Er zijn naar inschatting van de werkgroep voor dit aspect geen noemenswaardige bezwaren vanuit het veld die van invloed zijn op de besluitvorming, haalbaarheid of implementatie.
Rationale: waarom deze aanbeveling?
De werkgroep heeft besloten tot een conditionele aanbeveling gericht op volwassen personen met een zeer hoog cardiovasculair risico, omdat de beslissing om een SGLT2-remmer in te zetten afhangt van de juiste balans tussen voor- en nadelen van de interventie en belasting voor de patiënt. Deze balans verschilt per individuele patiënt. Daarnaast komt uit een systematische review naar de waarden en voorkeuren van personen met DM type 2 naar voren dat de waarden en voorkeuren van individuele patiënten over de inzet van SGLT2-remmers aanzienlijk variëren. De beslissing om een SGLT2-remmer aan de behandeling toe te voegen moet samen met de patiënt worden genomen, met weging van de voor- en nadelen afgestemd op de individuele patiënt, en rekening houdend met de persoonlijke waarden en voorkeuren.
Aanbeveling (sterk of zwak/voor of tegen)
De werkgroep heeft besloten tot een zwakke oftewel conditionele aanbeveling gericht op volwassen personen met DM type 2 en een zeer hoog cardiovasculair risico.
Onderbouwing
Het primaire doel van de behandeling van DM2 is het voorkomen van complicaties, zoals hart- en vaatziekten, nierfalen, blindheid en amputaties, met als resultaat een verbeterde kwaliteit van, en indien mogelijk, langer leven. Recente cardiovasculaire veiligheidsstudies geven aan dat glucoseverlaging met SGLT2-remmers en GLP1 receptoragonisten mogelijk voordelen bieden in het voorkomen van deze complicaties bij mensen met DM2 en een zeer hoog risico volgens de CVRM-richtlijn (NHG/NIV/NVvC, 2019). De uitgangsvraag richt zich dan ook op de waarde van SGLT2-remmers in de medicamenteuze behandeling van zeerhoogrisicopatiënten met DM2 (tabel 1). In de 2025 update van deze module is enkel informatie over toegevoegd over de inzet van SGLT-remmers bij kwetsbare patiënten en/of ouderen.
Introduction (background)
The primary treatment goal for diabetes mellitus type 2 is prevention of complications such as cardiovascular disease, kidney failure, blindness and amputations, resulting in a better quality of life, and if possible, longer life. Recent cardiovascular safety studies have suggested that SGLT-2 inhibitors and GLP-1 receptor agonists may prevent complications in people with Diabetes mellitus type 2 having a high to very high risk of cardiovascular disease. The clinical question therefore focusses on the added value of SGLT-2 inhibitors in the pharmacotherapy of individuals with Diabetes mellitus type 2 who are at very high risk of cardiovascular disease (table 1). In the 2025 update of this module, information has been added on the use of SGLT-2 inhibitors in vulnerable or elderly patients.
See table 2-4 for summary of findings. Plain text conclusion are reproduced below.
Risk category: Adults with Diabetes mellitus type 2 and established CVD (but no CKD)
|
High GRADE |
SGLT2 inhibitors reduce the risk of death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of cardiovascular death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared with standard care. Sources: Palmer, 2021 |
|
High GRADE |
There is no important difference in risk of end-stage kidney disease between SGLT2 inhibitors and standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
There probably is no important difference in risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. Sources: Palmer, 2021 |
|
No GRADE |
We are uncertain of the effects of SGLT2 inhibitors on MACE, acute kidney failure (sudden loss of kidney function requiring hospitalization) and composite renal outcome (40% reduction in eGFR relative to baseline, endstage kidney failure or death as a result of kidney failure) compared with standard care. These endpoints were not reported. Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitor therapy may increase the risk of amputation compared with standard care. Sources: Palmer, 2021 |
Risk category: Adults with Diabetes mellitus type 2 and chronic kidney disease (but no CVD)
|
High GRADE |
SGLT2 inhibitors reduce the risk of death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of cardiovascular death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of end-stage kidney disease compared with standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
There probably is no important difference in risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. Sources: Palmer, 2021 |
|
No GRADE |
We are uncertain of the effects of SGLT2 inhibitors on MACE, acute kidney failure (sudden loss of kidney function requiring hospitalization) and composite renal outcome (40% reduction in eGFR relative to baseline, endstage kidney failure or death as a result of kidney failure) compared with standard care. These endpoints were not reported.
Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitor therapy may increase the risk of amputation compared with standard care. Sources: Palmer, 2021 |
Risk category: Adults with Diabetes mellitus type 2 and CVD and CKD
|
High GRADE |
SGLT2 inhibitors reduce the risk of death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of cardiovascular death compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared with standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors reduce the risk of end-stage kidney disease compared with standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. Sources: Palmer, 2021 |
|
Moderate GRADE |
There probably is no important difference in risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. Sources: Palmer, 2021 |
|
High GRADE |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. Sources: Palmer, 2021 |
|
No GRADE |
We are uncertain of the effects of SGLT2 inhibitors on MACE, acute kidney failure (sudden loss of kidney function requiring hospitalization) and composite renal outcome (40% reduction in eGFR relative to baseline, endstage kidney failure or death as a result of kidney failure) compared with standard care. These endpoints were not reported. Sources: Palmer, 2021 |
|
Low GRADE |
SGLT2 inhibitor therapy may increase the risk of amputation compared with standard care. Sources: Palmer, 2021 |
Description of studies
Palmer (2021) evaluated SGLT-2 inhibitors and GLP-1 receptor agonists in adult patients with Diabetes mellitus type 2 at varying cardiovascular and renal risk. The protocol for this systematic review was registered with PROSPERO (CRD42019153180). The literature search was conducted in Medline, Embase, and the Cochrane Central Register of Controlled Trials from March 2016 to 11 August 2020 (for search strategy, see Palmer, 2021). The search from a previous network meta-analysis (Palmer, 2016) provided records from database inception to March 2016. Thus, the systematic review covered the literature from database inception up to 11 August 2020. Studies were screened independently by two reviewers (for PRISMA flow diagram, see Palmer, 2021): 764 trials including 421 346 patients proved eligible. Three hundred and seven (40%) of 764 trials were at low risk of bias in random sequence generation and 529 (69%) were at low risk of bias in allocation concealment (see Palmer, 2021). Four hundred and sixty two trials (60%) reported blinding for participants and investigators, and 105 trials (14%) reported blinding for outcome assessment. Three hundred and twenty eight trials (43%) were at low risk of attrition bias and 355 trials (46.5%) were at low risk of bias from selective outcome reporting.
Parallel group randomised controlled trials were eligible if they compared SGLT-2 inhibitors or GLP-1 receptor agonists with one another or with other glucose lowering treatments, placebo, or standard care in adults with Diabetes mellitus type 2. Only studies reporting outcomes at 24 weeks or longer were included. Using definitions of outcomes specified in individual randomised controlled trials, the review examined all patient-important outcomes as defined by the guideline panel (see Palmer, 2021; Li, 2021), regardless of whether evidence was available in the eligible trials: all-cause mortality, cardiovascular mortality, non-fatal myocardial infarction, nonfatal stroke, kidney failure, admission to hospital for heart failure, severe hypoglycaemia, blindness, eye disease requiring intervention, health related quality of life, change in body weight, amputation, neuropathic pain, diabetic ketoacidosis, serious hyperglycaemia, genital infection, Fournier gangrene, severe gastrointestinal events, pancreatic cancer, and pancreatitis. HbA1c was also included in the review because it is prioritised by some decision makers. Thus, the systematic review (Palmer, 2021) covers all outcomes prioritised by the current guideline development group (see the section Search and select).
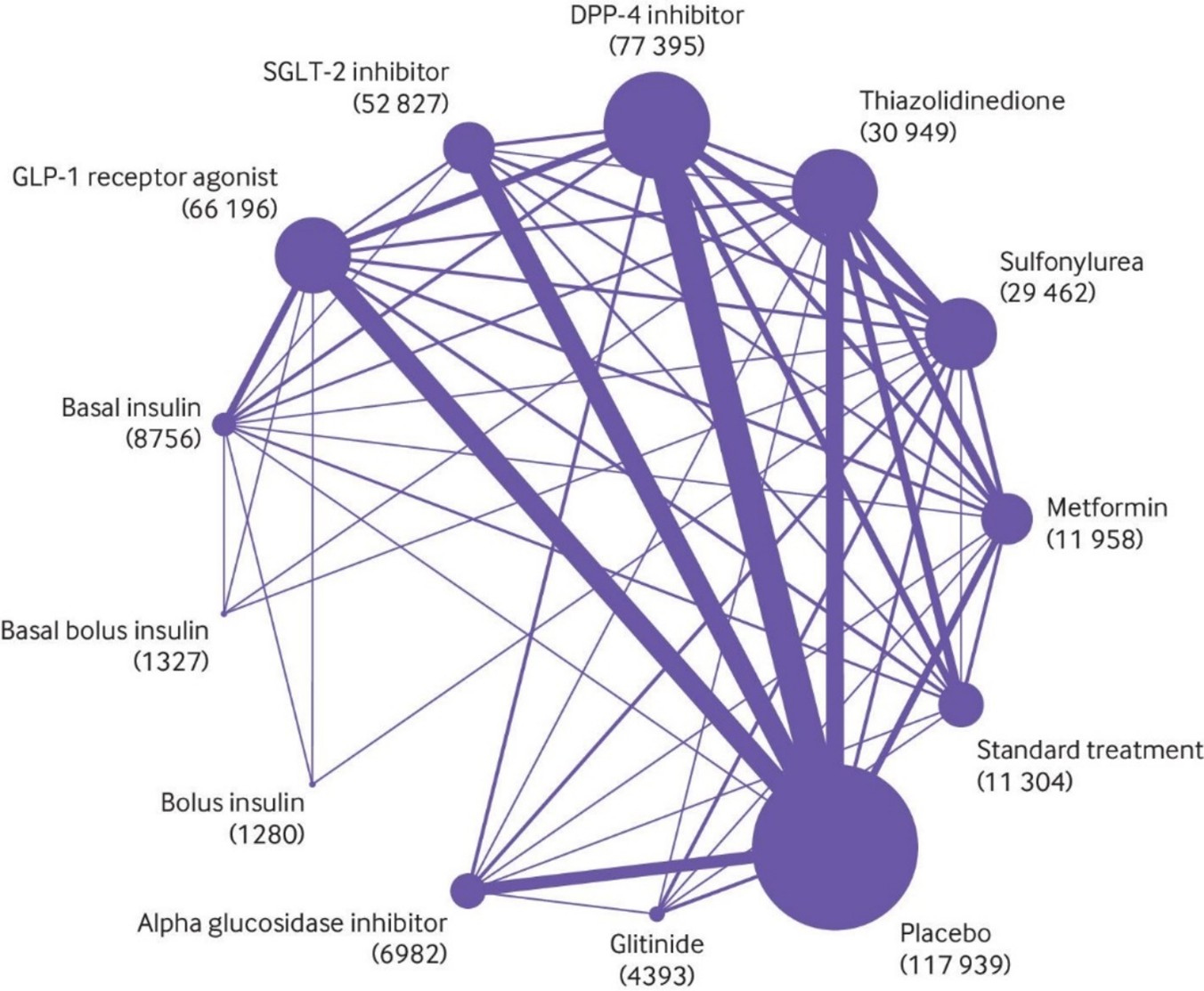
Palmer (2021) performed a frequentist random effects network meta-analysis and used GRADE to assess evidence certainty. The network compares 11 glucose lowering drugs, placebo, or standard care (for network plot see Fig. 1). The median trial mean age was 57.1 years, and the median proportion of men was 56%. At baseline, the median trial mean HbA1c was 8.1% (65 mmol/mol) and BMI was 30.1.
Figure. 1 Network plot of trials evaluating glucose lowering treatments for Diabetes mellitus type 2 (reproduced from Palmer, 2021). The size of each circle is proportional to the number of randomly assigned participants in the treatment comparisons (sample size shown in brackets). Line widths are proportional to the number of trials comparing the corresponding pair of treatments.
A network meta-analysis was performed for each relevant outcome. Subsequently, the estimates of relative effect (odds ratios) were combined with baseline risks representing the five risk categories to estimate absolute effects of treatment on cardiovascular and kidney outcomes in these categories of patients. These baseline risk estimates were based on several sources of evidence, including cohort studies, risk prediction equations, or the placebo arm in available trials. Most baseline risk estimates were based on the risk prediction model RECODe. Results included estimated absolute effects of treatment per 1000 patients treated for five years for patients at very low risk (no cardiovascular risk factors), low risk (three or more cardiovascular risk factors), moderate risk (cardiovascular disease), high risk (chronic kidney disease), and very high risk (cardiovascular disease and kidney disease). Chronic kidney disease was defined as an estimated glomerular filtration rate 45-75 mL/min/1.73 m2 with albuminuria > 300 mg/g (ACR 30 mg/mmol), or estimated glomerular filtration rate 15-45 mL/min/1.73 m2. Only the moderate, high and very high risk patients are relevant to the current guideline module, and therefore only results obtained for these three risk categories are summarized below. Moreover, only the results obtained for the outcomes prioritised by the guideline development group will be reported (for additional outcomes see Palmer, 2021).
Results (effects of interventions)
All results refer to the addition of SGLT-2 inhibitors to existing diabetes treatment. The authors developed evidence summaries and decision aids in MAGICapp, including an interactive decision support tool for multiple treatment choices (https://magicevidence.org/match-it/200820dist/#!/).
The summary of findings tables below provides an overview of the relative and absolute effect estimates per risk category, together with a GRADE assessment of the certainty of the evidence. Most GRADE assessments are taken from Palmer (2021), in some instances the certainty of the evidence was (further) downgraded if an effect estimate overlapped with the decision threshold defined by the guideline development group (see the section Relevant outcome measures, earlier in the text). Note that a five-year NNT 100 threshold (for potential benefits and mild side-effects) translates to a difference of 10 events per 1000 patients. A threshold at five year NNT 1000 (for serious harms) corresponds to a difference of 1 event per 1000 patients.
Table 2. Adults with Diabetes mellitus type 2 and established CVD (but no CKD)
Intervention: Sodium-Glucose Transport Protein 2 (SGLT-2) inhibitors
Comparator: Standard care
|
Outcome Timeframe 5 yrs
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence |
Plain text summary |
|
|
Standard care |
SGLT2 inhibitors |
||||
|
Potential benefits |
|||||
|
All-cause mortality |
Odds Ratio 0.85 (CI 95% 0.79 - 0.92) Based on data from 282,704 patients in 225 studies. |
120 per 1000 |
102 per 1000 |
High |
SGLT2 inhibitors reduce the risk of death compared with standard care. |
|
Difference: 18 fewer per 1000 (CI 95% 25 fewer - 10 fewer) |
|||||
|
Cardiovascular mortality |
Odds Ratio 0.84 (CI 95% 0.76 - 0.92) Based on data from 222,944 patients in 128 studies. |
79 per 1000 |
67 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of cardiovascular death compared with standard care. |
|
Difference: 12 fewer per 1000 (CI 95% 18 fewer - 6 fewer) |
|||||
|
Nonfatal myocardial infarction |
Odds Ratio 0.87 (CI 95% 0.79 - 0.97) Based on data from 262,168 patients in 199 studies. |
108 per 1000 |
95 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. |
|
Difference: 13 fewer per 1000 (CI 95% 21 fewer - 3 fewer) |
|||||
|
Nonfatal stroke |
Odds Ratio 1.01 (CI 95% 0.89 - 1.14) Based on data from 257,767 patients in 171 studies. |
108 per 1000 |
109 per 1000 |
Low Due to very serious imprecision |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared with standard care. |
|
Difference: 1 more per 1000 (CI 95% 11 fewer - 13 more) |
|||||
|
End-stage kidney disease |
Odds Ratio 0.71 (CI 95% 0.57 - 0.89) |
20 per 1000 |
14 per 1000 |
High |
There is no important difference in the risk of end-stage kidney disease between SGLT2 inhibitors and standard care.
|
|
Difference: 6 fewer per 1000 (CI 95% 9 fewer - 2 fewer) |
|||||
|
Hospital admission for heart failure |
Odds Ratio 0.7 (CI 95% 0.63 - 0.77) Based on data from 229,615 patients in 141 studies. |
80 per 1000 |
57 per 1000 |
High |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. |
|
Difference: 23 fewer per 1000 (CI 95% 28 fewer - 17 fewer) |
|||||
|
Potential harms |
|||||
|
Diabetic ketoacidosis |
Odds Ratio 1.04 (CI 95% 0.61 - 1.78) Based on data from 98,634 patients in 26 studies. |
2 per 1000 |
2 per 1000 |
Moderate Due to serious imprecision |
There probably is no important difference in the risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. |
|
Difference: 0 fewer per 1000 (CI 95% 1 fewer - 2 more) |
|||||
|
Genital infection |
Odds Ratio 3.5 (CI 95% 3.01 - 4.07) Based on data from 80,771 patients in 78 studies. |
73 per 1000 |
216 per 1000 |
High |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. |
|
Difference: 143 more per 1000 (CI 95% 119 more – 170 more) |
|||||
|
Amputation |
Odds Ration 1.14 (CI 95% 0.96, 1.35) |
45 per 1000 |
50 per 1000 |
Low Due to very serious imprecision |
SGLT2 inhibitor therapy may increase the risk of amputation compared with standard care. |
|
Difference: 6 more per 1000 (CI 95% 2 fewer to 16 more) |
|||||
Table 3. Adults with Diabetes mellitus type 2 and chronic kidney disease (but no CVD)
Intervention: Sodium-Glucose Transport Protein 2 (SGLT2) inhibitors
Comparator: Standard care
|
Outcome Timeframe 5 yrs
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence |
Plain text summary |
|
|
Standard care |
SGLT2 inhibitors |
||||
|
Potential benefits |
|||||
|
All-cause mortality |
Odds Ratio 0.85 (CI 95% 0.79 - 0.92) Based on data from 282,704 patients in 225 studies. |
170 per 1000 |
144 per 1000 |
High |
SGLT2 inhibitors reduce the risk of death compared with standard care. |
|
Difference: 26 fewer per 1000 (CI 95% 36 fewer - 14 fewer) |
|||||
|
Cardiovascular mortality |
Odds Ratio 0.84 (CI 95% 0.76 - 0.92) Based on data from 222,944 patients in 128 studies. |
112 per 1000 |
96 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of cardiovascular death compared with standard care. |
|
Difference: 16 fewer per 1000 (CI 95% 25 fewer - 8 fewer) |
|||||
|
Nonfatal myocardial infarction |
Odds Ratio 0.87 (CI 95% 0.79 - 0.97) Based on data from 262,168 patients in 199 studies. |
120 per 1000 |
106 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. |
|
Difference: 14 fewer per 1000 (CI 95% 23 fewer - 3 fewer) |
|||||
|
Nonfatal stroke |
Odds Ratio 1.01 (CI 95% 0.89 - 1.14) Based on data from 257,767 patients in 171 studies. |
120 per 1000 |
121 per 1000 |
Low Due to serious imprecision |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared to standard care. |
|
Difference: 1 more per 1000 (CI 95% 12 fewer - 15 more) |
|||||
|
End-stage kidney disease |
Odds Ratio 0.71 (CI 95% 0.57 - 0.89) Based on data from 79,896 patients in 31 studies. |
92 per 1000 |
67 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of end-stage kidney disease compared with standard care. |
|
Difference: 25 fewer per 1000 (CI 95% 37 fewer - 9 fewer) |
|||||
|
Hospital admission for heart failure |
Odds Ratio 0.7 (CI 95% 0.63 - 0.77) Based on data from 229,615 patients in 141 studies. |
105 per 1000 |
76 per 1000 |
High |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. |
|
Difference: 29 fewer per 1000 (CI 95% 36 fewer - 22 fewer) |
|||||
|
Potential harms |
|||||
|
Diabetic ketoacidosis |
Odds Ratio 1.04 (CI 95% 0.61 - 1.78) Based on data from 98,634 patients in 26 studies. |
2 per 1000 |
2 per 1000 |
Moderate Due to serious imprecision |
There probably is no important difference in the risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. |
|
Difference: 0 fewer per 1000 (CI 95% 1 fewer - 2 more) |
|||||
|
Genital infection |
Odds Ratio 3.5 (CI 95% 3.01 - 4.07) Based on data from 80,771 patients in 78 studies. |
73 per 1000 |
216 per 1000 |
High |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. |
|
Difference: 143 more per 1000 (CI 95% 119 more - 170 more) |
|||||
|
Amputation |
Odds Ration 1.14 (CI 95% 0.96, 1.35) |
55 per 1000 |
61 per 1000 |
Low Due to very serious imprecision |
SGLT2 inhibitor therapy may increase the risk of amputation compared to standard care. |
|
Difference: 8 more per 1000 (CI 95% 2 fewer to 19 more) |
|||||
Table 4. Adults with Diabetes mellitus type 2 and CVD and CKD
Intervention: Sodium-Glucose Transport Protein 2 (SGLT2) inhibitors
Comparator: Standard care
|
Outcome Timeframe 5 yrs
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence |
Plain text summary |
|
|
Standard care |
SGLT2 inhibitors |
||||
|
Potential benefits |
|||||
|
All-cause mortality |
Odds Ratio 0.85 (CI 95% 0.79 – 0.92) Based on data from 282,704 patients in 225 studies. |
265 per 1000 |
225 per 1000 |
High |
SGLT2 inhibitors reduce the risk of death compared with standard care. |
|
Difference: 40 fewer per 1000 (CI 95% 56 fewer - 21 fewer) |
|||||
|
Cardiovascular mortality |
Odds Ratio 0.84 (CI 95% 0.76 - 0.92) Based on data from 222,944 patients in 128 studies. |
175 per 1000 |
151 per 1000 |
High |
SGLT2 inhibitors reduce the risk of cardiovascular death compared with standard care. |
|
Difference: 24 fewer per 1000 (CI 95% 36 fewer - 12 fewer) |
|||||
|
Nonfatal myocardial infarction |
Odds Ratio 0.87 (CI 95% 0.79 - 0.97) Based on data from 262,168 patients in 199 studies. |
190 per 1000 |
169 per 1000 |
Moderate Due to serious imprecision |
SGLT2 inhibitors probably reduce the risk of nonfatal myocardial infarction compared with standard care. |
|
Difference: 21 fewer per 1000 (CI 95% 34 fewer - 5 fewer) |
|||||
|
Nonfatal stroke |
Odds Ratio 1.01 (CI 95% 0.89 - 1.14) Based on data from 257,767 patients in 171 studies. |
190 per 1000 |
192 per 1000 |
Low Due to very serious imprecision |
SGLT2 inhibitors may have little or no impact on the risk of nonfatal stroke compared with standard care. |
|
Difference: 2 more per 1000 (CI 95% 17 fewer - 21 more) |
|||||
|
End-stage kidney disease |
Odds Ratio 0.71 (CI 95% 0.57 - 0.89) Based on data from 79,896 patients in 31 studies. |
148 per 1000 |
110 per 1000 |
High |
SGLT2 inhibitors reduce the risk of end-stage kidney disease compared with standard care. |
|
Difference: 38 fewer per 1000 (CI 95% 58 fewer - 14 fewer) |
|||||
|
Hospital admission for heart failure |
Odds Ratio 0.7 (CI 95% 0.63 - 0.77) Based on data from 229,615 patients in 141 studies. |
235 per 1000 |
177 per 1000 |
High |
SGLT2 inhibitors reduce the risk of hospital admission for heart failure compared with standard care. |
|
Difference: 58 fewer per 1000 (CI 95% 73 fewer - 44 fewer) |
|||||
|
Potential harms |
|||||
|
Diabetic ketoacidosis |
Odds Ratio 1.04 (CI 95% 0.61 - 1.78) Based on data from 98,634 patients in 26 studies. |
2 per 1000 |
2 per 1000 |
Moderate Due to serious imprecision |
There probably is no important difference in the risk of diabetic ketoacidosis between SGLT2 inhibitors and standard care. |
|
Difference: 0 fewer per 1000 (CI 95% 1 fewer - 2 more) |
|||||
|
Genital infection |
Odds Ratio 3.5 (CI 95% 3.01 - 4.07) Based on data from 80,771 patients in 78 studies. |
73 per 1000 |
216 per 1000 |
High |
SGLT2 inhibitors increase the risk of genital infection compared with standard care. |
|
Difference: 143 more per 1000 (CI 95% 119 more - 170 more) |
|||||
|
Amputation |
Odds Ration 1.14 (CI 95% 0.96, 1.35) |
94 per 1000 |
104 per 1000 |
Low Due to very serious imprecision |
SGLT2 inhibitors may increase the risk of amputation compared to standard care. |
|
Difference: 13 more per 1000 (CI 95% 4 fewer to 23 more) |
|||||
Level of evidence of the literature
The level (certainty) of evidence of the literature was assessed per outcome, using the GRADE methodology (see Tables 2-4). The evidence came from RCTs and therefore started at HIGH certainty. The level of evidence was downgraded to MODERATE, LOW or VERY LOW certainty, in case of risk of bias, inconsistency, indirectness, imprecision, or publication bias. Most GRADE assessments were reproduced from Palmer (2021), in some instances the certainty of the evidence was (further) downgraded if an effect estimate overlapped with the decision threshold defined by the guideline development group.
A systematic review of the literature was performed to answer the following question: What is the optimal pharmacotherapy of adults with Diabetes mellitus type 2 and a very high risk of cardiovascular disease: supplementation of a SGLT-2 inhibitor?
Table 1. PICO
|
Patients |
Adult patients (18 years and older) with diabetes mellitus type 2 and very high cardiovascular risk according to the CVRM guideline (NHG/NIV/NVvC, 2019).* |
|
Intervention |
SGLT-2 inhibitor (canagliflozin, dapagliflozin, empagliflozin, ertugliflozin) monotherapy or added to metformin and/or any other combination of glucose-lowering medication. |
|
Control |
Standard of care (irrespective of background therapy) + placebo. |
|
Outcomes |
Crucial outcomes: total mortality, cardiovascular mortality, non-fatal MI, non-fatal stroke, hospitalization for heart failure (as a marker for serious heart failure), MACE, endstage kidney failure (eGFR < 15 ml/min/1,73 m2 or start or renal replacement therapy), acute kidney failure (sudden loss of kidney function requiring hospitalisation), composite renal outcome (and individual components: 40% reduction in eGFR relative to baseline, endstage kidney failure or death as a result of kidney failure). Important outcomes: side-effects of medication (bone fractures, urinary tract infections, genital infections, ketoacidosis, amputations, Fournier’s syndrome). |
* Individuals with diabetes mellitus type 2 and overt cardiovascular disease; i.e. acute coronary syndrome, angina pectoris, coronary revascularisation, TIA or stroke, aorto-iliofemoral atherosclerosis, aorto-aneurysm, claudicatio intermittens or peripheral revascularisation; also atherosclerotic stenosis or ischemia based on imaging. In addition, individuals with diabetes mellitus type 2 and organ damage, e.g. chronic kidney damage, or in combination with an important risk factor such as smoking (despite smoking cessation advice), or serious hypercholesterolemia (TC > 8 mmol/l despite maximally attainable therapy) or serious hypertension (≥ 180 mmHg despite maximally attainable therapy). Chronic kidney disease: eGFR < 30 ml/min/1,73 m2; eGFR 30-59 ml/min/1,73 m2 met ACR > 3 mg/mmol; or eGFR ≥ 60 ml/min/1,73 m2 with ACR > 30 mg/mmol. ACR: albumin/creatinine ratio. The definition of individuals with Diabetes mellitus type 2 and CKD considered at very high cardiovascular risk in which SGLT-2-inhibitors should be considered is slightly modified as compared to the definitions used in the CVRM guideline (NHG/NIV/NVvC, 2019) and Diabetic nephropathy guideline (NIV, 2020).
Relevant outcome measures
The guideline development group considered the following outcome measures as critical outcome measures for decision making: total mortality, cardiovascular mortality, non-fatal MI, non-fatal stroke, hospitalization for heart failure (as a marker for serious heart failure), MACE (Major Adverse Cardiovascular Events), endstage kidney failure (eGFR < 15 ml/min/1,73 m2 or start or renal replacement therapy), acute kidney failure (sudden loss of kidney function requiring hospitalisation), and a composite renal outcome (and individual components: 40% reduction in eGFR relative to baseline, endstage kidney failure or death as a result of kidney failure). Side-effects of medication (bone fractures, urinary tract infections, genital infections, ketoacidosis, amputations, Fournier’s syndrome) were considered important (but not critical) outcome measures for decision making.
A priori, the working group did not further define the outcome measures listed above but used the definitions used in the studies.
The guideline development group considered a time horizon of five years and a number needed to treat (NNT) of 30 as an adequate threshold for clinical decision making for a composite outcome of all cardiovascular and renal endpoints together, because patients at high or very high cardiovascular risk may suffer any of the cardiovascular and renal endpoints during follow-up. These numbers needed to treat correspond to the thresholds used for broadly accepted treatments such as treatments with antihypertensive or cholesterol-lowering drugs, or treatment with anticoagulants after a stroke. For judgements on individual outcomes (such as total mortality, MI, stroke, heart failure and endstage kidney failure) the guideline development group considered a five-year number needed to treat of 100 as an adequate threshold. This threshold was mainly used to judge the GRADE domain imprecision per outcome measure. Importantly, the NNT 100 threshold for individual outcomes was not used in the overall judgement to determine whether a SGLT2-inhibitor should be recommended or not. For serious side-effects and complications such as ketoacidosis and amputations a five-year NNT (number needed to treat for an additional harmful outcome) of 1000 was used as a threshold because these outcomes are potential harms, instead of potential benefits, of a treatment with SGLT-2 inhibitors. For judgements on less serious side-effects such as urinary tract infections and genital infections a five-year NNT of 100 was used.
Search and select (methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2015 until May 2020. The detailed search strategy is depicted in the Annex (Totstandkoming)/ (Verantwoording). In the early stages of searching and selecting literature, the guideline development group became aware of an elaborate network meta-analysis and guideline initiative addressing the exact same clinical question. The systematic review and network meta-analysis (Palmer, 2021) covers the research literature up to 11 August 2020.
Results (search)
One systematic review (Palmer, 2021) was included in the analysis of the literature. For patient and study characteristics and results, and risk of bias assessment of the individual studies included in the systematic review we refer to the aforementioned publication. Risk of bias was determined using the Cochrane tool for assessing risk of bias in randomised trials (Siemieniuk, 2016). The assessment of the risk of bias of the systematic review is summarized in the risk of bias table. The systematic review is of high quality (see risk of bias table in the Annex).
- Bersoff-Matcha SJ, Chamberlain C, Cao C, et al. Fournier gangrene associated with sodium-glucose cotransporter-2 inhibitors: a review of spontaneous postmarketing cases. Ann Intern Med 2019;170:764-9.
- Böhm M, Butler J, Filippatos G, et al; EMPEROR-Preserved Trial Committees and Investigators. Empagliflozin improves outcomes in patients with heart failure and preserved ejection fraction irrespective of age. J Am Coll Cardiol. 2022;80(1):1-18. doi:10.1016/j.jacc.2022.04.040. Medline
- Buchan TA, Malik A, Chan C, et al. Predictive models for cardiovascular and kidney outcomes in patients with type 2 diabetes: systematic review and meta-analyses. Heart 2021:DOI: 10.1136/heartjnl-2021-31924.
- Butt JH, Dewan P, Merkely B, et al. Efficacy and safety of dapagliflozin according to frailty in heart failure with reduced ejection fraction: a post hoc analysis of the DAPA-HF Trial. Ann Intern Med. 2022;175(6):820-830. doi:10.7326/M21-4776. Medline
- Butt JH, Jhund PS, Belohlávek J, et al. Efficacy and safety of dapagliflozin according to frailty in patients with heart failure: a prespecified analysis of the DELIVER Trial. Circulation. 2022;146(16):1210-1224. doi:10.1161/CIRCULATIONAHA.122.061754. Medline
- CBG (2020). College ter Beoordeling Geneesmiddelen. Geneesmiddeleninformatiebank. https://www.geneesmiddeleninformatiebank.nl/nl/ (geraadpleegd 9 april 2020).
- Chen K, Nie Z, Shi R, et al. Time to benefit of sodium-glucose cotransporter-2 inhibitors among patients with heart failure. JAMA Netw Open. 2023;6(8):e2330754. doi:10.1001/jamanetworkopen.2023.30754. Medline
- Cheng L, Li YY, Hu W, et al . Risk of bone fracture associated with sodium–glucose cotransporter-2 inhibitor treatment: a meta-analysis of randomized controlled trials. Diabetes Metabol 2019;45:436-45.
- Colacci M, Fralick J, Odutayo A, Fralick M. Sodium-glucose cotransporter-2 inhibitors and risk of diabetic ketoacidosis among adults with type 2 diabetes: a systematic review and meta-analysis. Can J Diabetes. 2022;46(1):10-15.e2. doi:10.1016/j.jcjd.2021.04.006. Medline
- Evans M, Morgan AR, Bain SC, et al. Defining the role of SGLT2 inhibitors in primary care: time to think differently. Diabetes Ther. 2022;13(5):889-911. doi:10.1007/s13300-022-01242-y. Medline
- FK (2021). Farmacotherapeutisch Kompas. https://www.farmacotherapeutischkompas.nl/ (geraadpleegd 9 april 2021).
- Goldenberg RM, Berard LD, Cheng AYY, et al. SGLT2 inhibitor-associated diabetic ketoacidosis: clinicalreview and recommendations for prevention and diagnosis. Clin Ther. 2016;38(12):2654-2664.e1. doi:10.1016/j.clinthera.2016.11.002. Medline
- González-González JG, González-Colmenero AD, Millán-Alanís JM, et al. Values, preferences and burden of treatment for the initiation of GLP-1 receptor agonists and SGLT-2 inhibitors in adult patients with type 2 diabetes: a systematic review. BMJ open 2021;11:e049130.Siemieniuk RA, Agoritsas T, Macdonald H, et al.. Introduction to BMJ rapid recommendations. BMJ 2016;354:i5191
- Guo ZM, Wang LJ, Yu J, Wang YQ, Yang ZQ, Zhou CH. The role of SGLT-2 inhibitors on health-related quality of life, exercise capacity, and volume depletion in patients with chronic heart failure: a meta-analysis ofrandomized controlled trials. Int J Clin PharmNet. 2023;45(3):800. doi:10.1007/s11096-023-01572-2. Medline
- Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al; DAPA-CKD Trial Committees and Investigators. Dapagliflozin in patients with chronic kidney disease. N Engl J Med. 2020;383(15):1436-1446. doi:10.1056/NEJMoa2024816. Medline
- Herrington WG, Staplin N, Wanner C, et al; The EMPA-KIDNEY Collaborative Group. Empagliflozin in patients with chronic kidney disease. N Engl J Med. 2023;388(2):117-127. doi:10.1056/NEJMoa2204233. Medline
- Karagiannis T, Tsapas A, Athanasiadou E, et al. GLP-1 receptor agonists and SGLT2 inhibitors for older people with type 2 diabetes: A systematic review and meta-analysis. Diabetes Res Clin Pract. 2021 Apr:174:108737. doi: 10.1016/j.diabres.2021.108737.
- Li S, Vandvik PO, Lytvyn L, et al. Risk-based treatment with SGLT-2 inhibitors or GLP -1 receptor agonists for adults with type 2 diabetes: a clinical practice guideline. BMJ 2021;373:n1091.DOI:10.1136/bmj.n109.
- Li S, Vandvik PO, Lytvyn L, et al (2021). MAGICApp. https://app.magicapp.org/#/guideline/4288.
- Lin DSH, Lee JK, Chen WJ. Clinical adverse events associated with sodium-glucose cotransporter 2 inhibitors: a meta-analysis involving 10 randomized clinical trials and 71 553 individuals. J Clin Endocrinol Metab. 2021;106(7):2133-2145. doi:10.1210/clinem/dgab274. Medline
- Lunati ME, Cimino V, Gandolfi A, et al. SGLT2-inhibitors are effective and safe in the elderly: The SOLD study. Pharmacol Res. 2022;183:106396. doi:10.1016/j.phrs.2022.106396. Medline
- Kim DH, Rockwood K. Frailty in Older Adults. N Engl J Med. 2024 Aug 8;391(6):538-548. doi: 10.1056/NEJMra2301292. PMID: 39115063; PMCID: PMC11634188.
- Van Marum RJ. Underrepresentation of the elderly in clinical trials, time for action. Br J Clin Pharmacol. 2020;86(10):2014-2016.doi:10.1111/bcp.14539. Medline
- Martinez FA, Serenelli M, Nicolau JC, et al. Efficacy and safety of dapagliflozin in heart failure with reduced ejection fraction according to age: insights from DAPA-HF. Circulation. 2020;141(2):100-111. doi:10.1161/CIRCULATIONAHA.119.044133. Medline
- Nassif ME, Windsor SL, Tang F, et al. Dapagliflozin effects on biomarkers, symptoms, and functional status in patients with heart failure with reduced ejection fraction: The DEFINE-HF Trial. Circulation. 2019;140(18):1463-1476. doi:10.1161/CIRCULATIONAHA.119.042929. Medline
- Neuen BL, Young T, Heerspink HJ, et al. SGLT2 inhibitors for the prevention of kidney failure in patients with type 2 diabetes: a systematic review and meta-analysis. Lancet Diabetes Endocrinol 2019;7:845-54.
- NHG/NIV/NVvC (2019). Cardiovasculair risicomanagement (CVRM). Richtlijnendatabase. https://richtlijnendatabase.nl/richtlijn/cardiovasculair_risicomanagement_cvrm/samenvatting_richtlijn_cvrm.html (geraadpleegd 16 maart 2021).
- Nierstichting en Nierpatiënten Vereniging Nederland (2016). Let op bij (dreigende) uitdroging: Soms moet u uw medicijnen even overslaan. https://www.nierstichting.nl/media/filer_public/2d/97/2d97bbc9-140e-436a-8601-61a903dcba5d/folder_soms_moet_u_uw_medicijnen_even_overslaan.pdf (geraadpleegd 9 april 2021).
- Ninomiya T, Perkovic V, De Galan BE, et al. Albuminuria and kidney function independently predict cardiovascular and renal outcomes in diabetes. J Am Soc Nephrol 2009;20:1813-21.
- NIV (2020). Richtlijn Diabetische nefropathie. Richtlijnendatabase. https://richtlijnendatabase.nl/richtlijn/diabetische_nefropathie (geraadpleegd 22 maart 2021).
- NVD. Artsenwijzer Diëtiek, Ondervoeding. http://www.artsenwijzer.info/site/?page=20&lg=nl (geraadpleegd op 23 juni 2021).
- Palmer SC, Mavridis D, Nicolucci A, et al. Comparison of clinical outcomes and adverse events associated with glucose-lowering drugs in patients with type 2 diabetes: a meta-analysis. JAMA 2016;316:313-24.
- Palmer SC, Tendal B, Mustafa RA, et al. Sodium-glucose cotransporter protein-2 (SGLT-2) inhibitors and glucagon-like peptide-1 (GLP-1) receptor agonists for type 2 diabetes: systematic review and network meta-analysis of randomised controlled trials. BMJ 2021;372:m4573. DOI:10.1136/bmj.m4573.
- Palmer SC, Tendal B, Mustafa RA, et al. Sodium-glucose cotransporter protein-2 (SGLT-2) inhibitors and glucagon-like peptide-1 (GLP-1)receptor agonists fortype 2 diabetes: systematic review and network meta-analysis ofrandomised controlled trials. BMJ. 2021 Jan 13;372:m4573. doi:10.1136/bmj.m4573. Medline
- Perkovic V, Tuttle KR, Rossing P, et al. Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes. N Engl J Med. 2024 Jul 11;391(2):109-121. doi: 10.1056/NEJMoa2403347.
- Rahman W, Solinsky PJ, Munir KM, Lamos EM. Pharmacoeconomic evaluation of sodium-glucose transporter-2 (SGLT2) inhibitors for the treatment of type 2 diabetes. Expert opinion on pharmacotherapy 2019;20:151-61.
- Scheen AJ, Bonnet F. Efficacy and safety profile of SGLT2 inhibitors in the elderly: how is the benefit/risk balance? Diabetes Metab. 2023;49(2):101419. doi:10.1016/j.diabet.2023.101419. Medline
- Sircar M, Bhatia A, Munshi M. Review of hypoglycemia in the older adult: clinical implications and management. Can J Diabetes. 2016;40(1):66-72. doi:10.1016/j.jcjd.2015.10.004. Medline
- Spertus JA, Jones PG, Sandhu AT, Arnold SV. Interpreting the Kansas City Cardiomyopathy Questionnaire in clinical trials and clinical care. J Am Coll Cardiol. 2020;76(20):2379-2390. doi:10.1016/j.jacc.2020KCC.09.542. Medline
- Tong D. SGLT2 inhibitors in patients with HFpEF: how old is too old? J Cardiovasc Aging. 2022;2:41. doi:10.20517/jca.2022.30. Medline
- Tromp J, Ouwerkerk W, van Veldhuisen DJ, et al. A Systematic review and network meta-analysis of pharmacological treatment of heart failure with reduced ejection fraction. JACC Heart Fail. 2022;10(2):73-84. doi:10.1016/j.jchf.2021.09.004. Medline
- Vart P, Butt JH, Jongs N, et al. Efficacy and safety of dapagliflozin in patients with chronic kidney disease across the spectrum of frailty. J Gerontol A Biol Sci Med Sci. 2023;glad181. doi:10.1093/gerona/glad181. Medline
- Vaduganathan M, Docherty KF, Claggett BL, et al. SGLT-2 inhibitors in patients with heart failure: a comprehensive meta-analysis of five randomised controlled trials. Lancet. 2022;400(10354):757-767. doi:10.1016/S0140-6736(22)01429-5. Medline
- Vaduganathan M, Claggett BL, Jhund PS, et al. Estimating lifetime benefits of comprehensive disease-modifying pharmacological therapies in patients with heart failure with reduced ejection fraction: a comparative analysis of three randomised controlled trials. Lancet. 2020;396(10244):121-128. doi:10.1016/S0140-6736(20)30748-0. Medline
- Villarreal D, Ramírez H, Sierra V, Amarís JS, Lopez-Salazar AM, González-Robledo G. Sodium-glucose cotransporter 2 inhibitors in frail patients with heart failure: clinical experience of a heart failure unit. Drugs Aging. 2023;40(3):293-299. doi:10.1007/s40266- 022-01004-2. Medline
- Voorrips SN, Saucedo-Orozco H, Sánchez-Aguilera PI, De Boer RA, Van der Meer P, Westenbrink BD. Could SGLT2 inhibitors improve Exercise intolerance in chronic heart failure? Int J Mol Sci. 2022;23(15):8631. doi:10.3390/ijms23158631. Medline
- Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet 2019;393:31-9.
Table of excluded studies (full text assessment)
See Palmer (2021), the systematic review on which the literature analysis was based.
Table of Patient and study characteristics and results
See Palmer (2021), the systematic review on which the literature analysis was based.
Table of Quality assessment (Risk of bias) of individual studies
See Palmer (2021), the systematic review on which the literature analysis was based.
Risk of bias table for systematic reviews
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
Research question: What is the optimal pharmacotherapy of adults with Diabetes mellitus type 2 and a very high risk of cardiovascular disease: supplementation of a SGLT-2-inhibitor?
|
Study
First author, year |
Appropriate and clearly focused question?
Yes/no/unclear |
Comprehensive and systematic literature search?
Yes/no/unclear |
Description of included and excluded studies?
Yes/no/unclear |
Description of relevant characteristics of included studies?
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?
Yes/no/unclear |
Potential risk of publication bias taken into account?
Yes/no/unclear |
Potential conflicts of interest reported?
Yes/no/unclear |
|
Palmer, 2021 |
Yes |
Yes |
Yes |
Yes |
not applicable |
Yes |
Yes |
Unclear1 |
Yes |
1 Risk of reporting bias was assessed, but potential risk of publication bias is not mentioned.
Beoordelingsdatum en geldigheid
Publicatiedatum : 02-05-2026
Beoordeeld op geldigheid : 02-05-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire cluster ingesteld. Het cluster Diabetes Mellitus bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden geven hun expertise in, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Dr. E.H. (Erik) Serné, internist in het AUMC te Amsterdam, NIV, voorzitter cluster
- Dr. L.P.F. (Luc) Janssens, kinderarts in het Isala te Zwolle, NVK
- Dr. W.J. (Wouter) de Waal, kinderarts in het Sint Antonius Ziekenhuis te Nieuwegein, NVK
- Dr. R.C. (Rebecca) Painter, gyneaocoloog in het AUMC te Amsterdam, NVOG
- Dr. B.E. (Bastiaan) de Galan, internist in het MUMC te Maastricht, NIV
- T.M. (Ties) Obers, patiëntvertegenwoordiger, Diabetesvereniging Nederland
Betrokken clusterexpertisegroepleden
- Dr. E.H. (Erik) Serné, internist in het AUMC te Amsterdam, NIV
- Drs. A.M. (Aisha) Salarbaks, klinisch geriater bij Ziekenhuisgroep Twente te Almelo, NVKG
- Dr. L. (Liselotte) van Bloemendaal, internist ouderengeneeskunde in het Zaans Medisch Centrum te Zaandam, NIV
Met ondersteuning van
- Dr. A.N. (Anh Nhi) Nguyen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Dr. L. (Leanne) Küpers, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Drs. J.M.H. (Harm-Jan) van der Hart, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Drs. F.A. (Fieke) Pepping, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Clusterstuurgroepleden
Tabel 3 Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Restrictie |
|
Dr. E.H. (Erik) Serné |
Internist-Vasculaire Geneeskunde binnen Amsterdam UMC, locatie VUmc |
Clustervertegenwoordiger (NIV, NVK, NHG) binnen bestuur Nederlandse Diabetes Federatie (betaald) Lid van Rondetafel Diabeteszorg (onbetaald) Hoofdredacteur Nederlands Tijdschrift voor Diabetologie (betaald) Redactielid platform Diabetesgeneeskunde.nl (betaald) Medisch directeur van Diabeter Centrum Amsterdam, een joint venture tussen Amsterdam UMC en Diabeter; aangesteld via een detacheringscontract vanuit Amsterdam UMC (betaald). Medtronic is deels eigenaar van Diabeter. |
Geen |
Doelmatigheidsproject ZonMw betreffende behandeling patiënten met 'hypoglycemia unawareness' met 'stepped care' bestaande uit cursus HypoBewust en vervolgens evetueel continueglucose monitoring (CGM) versus directe start CGM
Veelbelovende zorg ZonMw-project betreffende Bi-hormonale kunstalvleesklier bij volwassen patiënten met diabetes type 1 die hun behandeldoelen niet halen; Automated blood glucose control in type 1 diabetes: effectiveness of the artificial pancreas (DARE-study)
Doelmatigheidsproject ZonMw betreffende LOFIT: Lifestyle front Office For Integrating lifestyle medicine in the Treatment of patients: a novel care-model towards community-based options for lifestyle change |
Advisering binnen Ronde Tafel Diabeteszorg betreffende doelmatige inzet nieuwe behandelingen toont belangrijke parallellen met richtlijnvorming. Beide maken gebruik van 'evidence-based medicine' en GRADE om de beschikbare data te duiden. Hierbij is dus geen sprake van belangenverstrengeling, maar van synergie. |
Restrictie t.a.v. besluitvorming bij modules HCl bij zwangerschap met DM1 en Preventie hypoglykemie met sensor bij diabetes mellitus type 2 |
|
Dr. L.P.F. (Luc) Janssens |
Kinderarts Isala |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Dr. W.J. (Wouter) de Waal |
Kinderarts Diakonessenhuis Utrecht |
Kinderarts Diabetes Centraal |
Geen |
Geen |
Geen |
Geen |
|
Dr. R.C. (Rebecca) Painter |
Gynaecoloog-perinatoloog Amsterdam UMC, hoogleraar verloskunde Vrije Universiteit Per 1 sept: Gynaecoloog-perinatoloog Erasmus MC, Hoogleraar Erasmus Universiteit |
Wetenschappelijk Adviseur Stichting ZEHG (onbetaald) Voorzitter werkgroep NVOG Richtlijn "schildklier en zwangerschap" (vacatiegelden) Lid werkgroep NVOG Richtlijn "Hyperemesis gravidarum" (vacatiegelden) Lid Koepel Wetenschap NVOG, namense Pijler FMG (onbetaald) Vice voorzitter NVOG Pijler FMG Wetenschapscommissie (onbetaald) Voorzitter NVOG SIG Diabetes en Zwangerschap (onbetaald) Lid Stadscoaltie Amsterdam Kansrijke Start (onbetaald) Projectleider en lid kernteam Netwerk Geboortezorg Noordwest Nederland (onbetaald) Bestuurslid NRCG, Nederlandse Regionale Consortia Geboortezorg (onbetaald) Lid Bestuurd Verloskundig Samenwerkingsverband Amsterdam UMC (onbetaald) Projectleider en hoofdonderzoeker SugarDip, TANGO-DM, PI NL RCTs (onbetaald) |
Geen |
ZonMW: SugarDip, projectleider PI NL, projectleider Netwerk Geboortezorg Noordwest Nederland, projectleider VSV stimulering implementatie basiskader, projectleider Minder dieren, meer kennis: Metformine in diermodellen systematic review, project leider NRCG, nationale regionale geboorteconsortia, geen projectleider
Diabetes Fonds: Register Diabetes en Zwangerschap, geen projectleider
Leading the Change: Tango DM, projectleider
Toegevoegd tijdens vergadering: CRISTAL studie (HCL bij zwangeren met DM1). Deze studie is niet gefinancierd door een farmaceut maar Medtronic heeft wel middelen geleverd. |
Projectleider TANGO DM, onderzoekt de afkapwaarden die gebruikt worden voor de diagnose diabetes gravidarum.
Medeprojectleider van SugarDip, over de medicamenteuze behandeling van diabetes gravidarum (insuline vs orale therapie). |
Geen |
|
Dr. B.E. (Bastiaan) de Galan |
Internist, MUMC+, Maastricht (0,6 fte) Hoogleraar interne geneeskunde/diabetologie, UM, Maastricht (0,2 fte) Internist, Radboudumc, Nijmegen (0,2 fte) |
Docent/cursusleider DESG cursus voor aios interne geneeskunde en kindergeneeskunde (betaald; naar MUMC+) Associate editor Diabetologia (betaald; naar MUMC) Bestuurslid Nederlandse Vereniging voor Endocrinologie (NVE; onbetaald) Voozitter accreditatiecommissie NIV (vacatiegelden) Voorzitter Commissie van Uitvoering voor het Accreditatieoverleg (onbetaald) Organisatie nascholingsreeks Diabetes Overleg (betaald, naar MUMC) Organisatie nascholingsreeks Dutch Diabetes Academy (betaald, naar MUMC) Secretaris International Hypoglycaemia Study Group (onbetaald) |
Geen |
Horizon Europe Framework Programme: Hypo-RESOLVE (Hypoglycaemia - redefining solutions for better lives) 2018-2023 (afgerond). Novo Nordisk, Lilly, Medtronic en Abbott betrokken als research partners, projectleider: ja
MELISSA (mobile artificial intelligence solution for diabetes adaptive care) 2022-2026. Novo Nordisk levert insuline, projectleider: ja
REDDIE (Real-world evidence for decisions in diabetes) 2023-2027. Novo Nordisk betrokken als research partner, projectleider: nee
Novo Nordisk: ADREM study (investigator initiated trial naar aanpassing van degludec bij sport bij mensen met type 1 diabetes, unrestricted grant) 2021-2022 (afgerond). |
Geen |
Geen |
|
T.M. (Ties) Obers |
Beleidsadviseur Belangenbehartiging (0,6 FTE) Diabetesvereniging Nederland
Directeur (0,2 FTE) Stichting Knowledge for Children Nederland
Freelance Adviseur Non-Profit (0,2 FTE) Groei voor Goed |
Geen |
Geen |
Geen |
Bescherming van de reputatie/positie van Diabetesvereniging Nederland. Boegbeeldfunctie bij patiëntenorganisatie Diabetesvereniging Nederland. |
Geen |
Betrokken clusterexpertisegroepleden
Tabel 4 Gemelde (neven)functies en belangen betrokken clusterexpertisegroepleden
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Restrictie |
|
Dr. E.H. (Erik) Serné |
Zie tabel 1 |
|||||
|
Drs. A.M. (Aisha) Salarbaks |
Klinisch geriater in ZGT (sinds 2013) |
Geen |
Geen |
1. Dialogica studie 2. Hartfalen bij ouderen: fagiliteit, zelfzorg en kwaliteit van leven |
Geen |
Geen |
|
Dr. L. (Liselotte) van Bloemendaal |
Internist ouderengeneeskunde Zaans Medisch Centrum |
0-uren aanstelling voor wetenschap in Amsterdam umc. Onbetaald. |
Geen |
OMED2 studie. Optimalization of Medication in Elderly with Diabetes 1. ZonMW goed gebruik geneesmiddelen - Ontwikkeling van een deprescribing programma om deprescribing te bevorden van diabetes medicatie (projectleider NEE) |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door inbreng van de Diabetesvereniging Nederland.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
SGLT2-remmers |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze.
Zoekverantwoording
Zoekactie voor de vergelijking van SGLT2-remmers met standaardzorg. Uiteindelijk is besloten de literatuuranalyse niet te baseren op de resultaten van onderstaande zoekstrategie, maar gebruik te maken van een zeer recente systematische review en netwerk meta-analyse (Palmer, 2021), die de literatuur tot 11 augustus 2020 dekt.
|
Uitgangsvraag: Wat is de optimale behandeling van volwassen personen met DM type 2 en een zeer hoog risico op hart- en vaatzieken: toevoeging van een SGLT2-remmer? |
|
|
Database(s): Medline, Embase |
Datum: 22-1-2020, update op 18-5-2020 |
|
Periode: 2015-heden |
Talen: Engels |
|
Literatuurspecialist: Miriam van der Maten |
|
|
Toelichting en opmerkingen: In eerste instantie naar SR’s gezocht vanaf 2015 met als doel om geschikte SR’s vervolgens te updaten vanaf de zoekdatum gehanteerd in deze SR’s. De search is breed opgezet, omdat niet alle studies (voornamelijk SR’s) geïndexeerd zijn als DM2-specifiek. |
|
|
Database |
Zoektermen |
|
Medline (OVID)
|
1 exp Diabetes Mellitus/ or diabete*.ti,ab,kf. or diabetic*.ti,ab,kf. or dm2.ti,ab,kf. or d2m.ti,ab,kf. or niddm.ti,ab,kf. or 'dm 2'.ti,ab,kf. or t2d*.ti,ab,kf. or 'dm type 2'.ti,ab,kf. or 'dm type ii'.ti,ab,kf. or dm1.ti,ab,kf. or d1m.ti,ab,kf. or iddm.ti,ab,kf. or 'dm 1'.ti,ab,kf. or t1d*.ti,ab,kf. or 'dm type 1'.ti,ab,kf. or 'dm type i'.ti,ab,kf. or 'type* 1 diabet*'.ti,ab,kf. or 'type* i diabet*'.ti,ab,kf. or 'type* one diabet*'.ti,ab,kf. (676289) 2 exp Cardiovascular Diseases/ or angiocardio*.ti,ab,kf. or heart*.ti,ab,kf. or cardio*.ti,ab,kf. or cvd.ti,ab,kf. or 'cv risk*'.ti,ab,kf. 3 exp Sodium-Glucose Transporter 2 Inhibitors/ or ((sodium* adj3 glucose* adj3 (transporter* or cotransporter* or 'co-transporter*' or 'co transporter*' or receptor*) adj3 '2') and inhibit*).ti,ab,kf. or sglt*.ti,ab,kf. or canagliflozin*.ti,ab,kf. or dapagliflozin*.ti,ab,kf. or empagliflozin*.ti,ab,kf. or ertugliflozin*.ti,ab,kf. 4 1 and 2 and 3 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) 6 4 and 5 7 limit 6 to (english language and yr="2015 -Current") 8 exp Diabetes Mellitus, Type 2/ or ((diabete* or diabetic*) adj3 ('non insulin* depend*' or 'noninsulin depend*' or noninsulindepend* or 'non insulindepend*' or 'maturity onset*' or 'adult onset*' or 'slow onset*' or 'ketosis resistant*' or stable*)).ti,ab,kf. or dm2.ti,ab,kf. or d2m.ti,ab,kf. or niddm.ti,ab,kf. or 'dm 2'.ti,ab,kf. or t2d*.ti,ab,kf. or 'dm type 2'.ti,ab,kf. or 'type* 2 diabet*'.ti,ab,kf. or 'type* two diabet*'.ti,ab,kf. or 'type* ii diabet*'.ti,ab,kf. or 'dm type ii'.ti,ab,kf. ) 9 8 and 2 and 3 10 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) 11 (9 and 10) not 6 12 limit 11 to (english language and yr="2018 -Current") |
|
Embase
|
#10 #8 AND #9 NOT #6 #9 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti #8 #7 AND #2 AND #3 AND [english]/lim AND [2018-2020]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) #7 'non insulin dependent diabetes mellitus'/exp OR (((diabete* OR diabetic*) NEAR/3 ('non insulin* depend*' OR 'noninsulin depend*' OR noninsulindepend* OR 'non insulindepend*' OR 'maturity onset*' OR 'adult onset*' OR 'slow onset*' OR 'ketosis resistant*' OR stable*)):ti,ab,kw) OR dm2:ti,ab,kw OR d2m:ti,ab,kw OR niddm:ti,ab,kw OR 'dm 2':ti,ab,kw OR t2d*:ti,ab,kw OR 'dm type 2':ti,ab,kw OR 'type* 2 diabet*':ti,ab,kw OR 'type* two diabet*':ti,ab,kw OR 'type* ii diabet*':ti,ab,kw OR 'dm type ii':ti,ab,kw #6 #4 AND #5 #5 'meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de #4 #1 AND #2 AND #3 AND [english]/lim AND [2015-2020]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) #3 'sodium glucose cotransporter 2 inhibitor'/exp OR (((sodium* NEAR/3 glucose* NEAR/3 (transporter* OR cotransporter* OR 'co-transporter*' OR 'co transporter*' OR receptor*) NEAR/3 '2'):ti,ab,kw) AND inhibit*:ti,ab,kw) OR sglt*:ti,ab,kw OR canagliflozin*:ti,ab,kw OR dapagliflozin*:ti,ab,kw OR empagliflozin*:ti,ab,kw OR ertugliflozin*:ti,ab,kw #2 'cardiovascular disease'/exp OR 'cardiovascular risk'/exp OR angiocardio*:ti,ab,kw OR heart*:ti,ab,kw OR cardio*:ti,ab,kw OR cvd:ti,ab,kw #1 'diabetes mellitus'/exp OR diabete*:ti,ab,kw OR diabetic*:ti,ab,kw OR dm2:ti,ab,kw OR d2m:ti,ab,kw OR niddm:ti,ab,kw OR 'dm 2':ti,ab,kw OR t2d*:ti,ab,kw OR 'dm type 2':ti,ab,kw OR 'dm type ii':ti,ab,kw OR dm1:ti,ab,kw OR d1m:ti,ab,kw OR iddm:ti,ab,kw OR 'dm 1':ti,ab,kw OR t1d*:ti,ab,kw OR 'dm type 1':ti,ab,kw OR 'dm type i':ti,ab,kw OR 'type* 1 diabet*':ti,ab,kw OR 'type* i diabet*':ti,ab,kw OR 'type* one diabet*':ti,ab,kw |