Amnioninfusie bij MHVW
Uitgangsvraag
Welke waarde heeft amnioninfusie durante partu bij meconiumhoudend vruchtwater ter preventie van ernstige perinatale morbiditeit en/of mortaliteit?
Aanbeveling
Pas amnioninfusie niet routinematig toe bij meconiumhoudend vruchtwater vanwege gebrek aan bewezen effectiviteit om meconiumaspiratie en perinatale sterfte te voorkomen.
Overwegingen
De meta-analyse van Hofmeyr et al. uit 2014 is een redelijk opgezette studie. Helaas zijn de geïncludeerde trials niet allemaal van goede kwaliteit. Over het geheel gezien vinden zij veelbelovende resultaten voor het gebruik van routinematige amnioninfusie bij de aanwezigheid van meconiumhoudend vruchtwater. Echter, wanneer zij enkel die studies meenemen die in een situatie van optimale perinatale opvang zijn verricht, is het effect van amnioninfusie minder evident. Er is dan geen verschil in het optreden van MAS, perinatale sterfte en een lage Apgar-score. Het is niet duidelijk of het gebrek aan effect van amnioninfusie op perinatale sterfte en het optreden van MAS komt doordat het effect wordt gemaskeerd door co-interventies, of doordat amnioninfusie op zichzelf niet nuttig is.
Wel is er nog altijd een significante reductie in het aantal kinderen dat een NICU-opname nodig heeft en wordt een reductie gezien in het aantal sectio’s voor foetale nood, zonder een verhoogd risico op complicaties. Er wordt echter niet beschreven waarom neonaten worden opgenomen op de NICU en of dit eenzelfde soort NICU is als wij in Nederland kennen. Derhalve meent de werkgroep dat het verminderd aantal NICU-opnames geen reden is om amnioninfusie routinematig toe te passen. Het totaal aantal sectio’s wordt niet gereduceerd, dus ook hiervoor is de werkgroep van mening dat routinematige amnioninfusie niet moet worden toegepast.
In de meta-analyse van Hofmeyr et al. (2014) wordt niet gedefinieerd wat bedoeld wordt met ‘standaard’ foetale bewaking en ‘limited’ foetale bewaking. De studies die zijn uitgevoerd onder ‘limited fetal surveillance’ hebben geen continue CTG-bewaking en laten over het algemeen meer perinatale complicaties zien en een groter effect van amnioninfusie. In de Nederlandse situatie is er bij meconiumhoudend vruchtwater altijd een indicatie voor een partus in de 2e lijn met continue CTG-bewaking. Hierbij is er dus enkel een positief effect van routinematige amnioninfusie op het aantal NICU-opnames en het aantal sectio’s voor foetale nood, zonder daarbij het totaal aantal sectio’s te beïnvloeden.
In de meta-analyse van Hofmeyr et al. (2014) wordt geen verschil gezien in het optreden van endometritis, of ernstige maternale morbiditeit of mortaliteit. In de overige gerandomiseerde trials worden geen verhoogde risico’s op complicaties gezien bij het gebruik van amnioninfusie durante partu. Wel zijn er 8 case reports die maternale sterfte beschrijven ten gevolge van een vruchtwaterembolie bij het gebruik van amnioninfusie. Een causaal verband is echter niet aangetoond15. Tevens zijn er enkele case reports die ernstige foetale complicaties beschrijven door het gebruik van een intra-uteriene druklijn, die nodig is voor het geven van amnioninfusie16,17.
Gezien het mogelijke positieve effect op NICU-opnames en het relatief kleine risico op complicaties valt amnioninfusie te overwegen in individuele gevallen. Het is echter onduidelijk bij welke patiënten het geven van amnioninfusie voordelig is. De werkgroep raadt het gebruik van standaard amnioninfusie, in een setting van continue CTG-bewaking aangevuld met STAN-monitoring en/of MBO’s (micro bloedonderzoek), dan ook niet aan ter preventie van NICU-opnames of sectio caesarea.
Onderbouwing
Meconiumpassage in utero leidt tot meconiumhoudend vruchtwater. Meconiumhoudend vruchtwater is een klinisch belangrijke risicofactor voor perinatale morbiditeit en mortaliteit en heeft een incidentie van 5,6-24,6% in de à terme periode1. De incidentie neemt toe naarmate de zwangerschapsduur vordert. De aanwezigheid van meconium in het vruchtwater is geassocieerd met perinatale asfyxie en infecties en leidt bij ongeveer 5% van de kinderen geboren met meconiumhoudend vruchtwater tot een meconiumaspiratiesyndroom (MAS)1. MAS wordt gedefinieerd als ademhalingsproblemen bij een pasgeborene met meconiumhoudend vruchtwater, waarbij de ademhalingsproblemen niet anders verklaard kunnen worden1. Meconiumhoudend vruchtwater is, mede door het optreden van MAS, geassocieerd met perinatale sterfte. Tevens is meconiumhoudend vruchtwater geassocieerd met meer kunstverlossingen2.
Er zijn theorieën waarbij wordt gedacht dat door amnioninfusie de meconium verdund wordt waardoor er minder schade wordt toegebracht. Bij het toepassen van amnioninfusie wordt een intra-uteriene druklijn ingebracht. Via deze druklijn wordt vervolgens fysiologisch zout ingebracht, waardoor het meconium verdunt. In de NVOG-richtlijn uit 2011 werd het gebruik van amnioninfusie durante partu bij meconiumhoudend vruchtwater afgeraden vanwege gebrek aan bewezen effectiviteit3.
|
Laag GRADE |
Het gebruik van routinematige amnioninfusie op plekken met optimale perinatale zorg verlaagt de perinatale sterfte en het optreden van meconium-aspiratiesyndroom niet.
Bronnen: Hofmeyr 2014 |
|
Laag GRADE |
Het gebruik van routinematige amnioninfusie is geassocieerd met minder NICU-opnames en minder sectio’s voor foetale nood. Het gebruik van routinematige amnioninfusie is niet geassocieerd met het totaal aantal sectio’s.
Bronnen: Hofmeyr 2014 |
Bij de ‘evidence tabellen’ wordt ook een tabel gepresenteerd voor de studies die niet zijn meegenomen in de search van de meta-analyse van Hofmeyr. Deze studies zijn dus niet geïncludeerd, maar ook niet specifiek beargumenteerd geëxcludeerd. Voor de volledige lijst van de geëxcludeerde studies na onze search zie de zoekverantwoording. In de tabel worden de artikelen die wel zijn bekeken in de meta-analyse en de artikelen met een taalrestrictie niet beschreven. In de tabel staan onze argumenten om deze studies niet mee te nemen voor de uitwerking van de uitgangsvraag.
De studie van Hofmeyr et al. uit 2014 is een meta-analyse van gerandomiseerde en quasi-gerandomiseerde trials. Studies die in aanmerking kwamen voor inclusie waren studies die amnioninfusie vergeleken met een controle (geen amnioninfusie of een ‘sham infusion’). In totaal werden 14 studies geïncludeerd, met in totaal 4435 vrouwen.
De in- en exclusiecriteria zijn duidelijk beschreven. Ook is duidelijk beschreven waarom er 16 van de 30 gevonden studies werden geëxcludeerd. Na het bestuderen van de geëxcludeerde studies willen wij ook al deze individuele studies excluderen (zie evidence tabel voor de individuele redenen).
De studiekarakteristieken van de meta-analyse zijn helder beschreven. De Cochrane Handbook for Systematic Reviews of Interventions werd gebruikt om van de individuele studies de kwaliteit en “risk of bias” te bepalen. Dit proces is zeer duidelijk weergegeven voor alle individuele studies.
De interventie (amnioninfusie) is in alle studies vergelijkbaar, hoewel het op verschillende manieren wordt toegepast. In de meeste studies is een intra-uteriene druklijn ingebracht en is de amnioninfusie gegeven via een infuuspomp, maar er zijn ook studies waarbij de amnioninfusie via een uitzuigslang of maagsonde is toegediend. De gegeven hoeveelheid amnioninfusie verschilt tussen de studies.
Randomisatie is in de meeste studies goed uitgevoerd. In de meta-analyse wordt dit duidelijk beschreven. Blindering was niet mogelijk. Wel zijn enkele vrouwen geëxcludeerd, in meerdere studies vanwege bijvoorbeeld een snelle partus voor start amnioninfusie, abnormaal CTG of de noodzaak tot een spoedsectio. Dit maakt dat er incomplete data zijn bij veel studies. Hierdoor wordt de “risk of bias” groter.
Er werd voor alle uitkomstmaten een subgroep analyse uitgevoerd voor situaties met ‘standard fetal surveillance’ en ‘limited fetal surveillance’. Helaas hebben de auteurs niet beschreven wat zij hieronder verstaan. De 3 studies die onder ‘limited fetal surveillance’ worden geschaard beschrijven allen in hun studie-opzet dat zij geen continue foetale monitoring gebruiken, maar intermitterend de foetale harttonen ausculteren. Het is duidelijk beschreven welke studies zijn gerekend onder welke subgroep.
Resultaten
1. Vermindering meconium aspiratie syndroom (5-10% relatieve reductie)
Voor het analyseren van deze uitkomstmaat zijn in totaal 4518 vrouwen geïncludeerd. Hiervan zijn er 3374 patiënten met ‘standard fetal surveillance’ bevallen. Het relatief risico voor het optreden van MAS bij het gebruik van amnioninfusie is 0.52 [0.26-1.06], p=0.07. Hoewel er hier een trend gezien wordt richting vermindering van MAS is de risico-reductie niet statistisch significant in deze groep. Voor de groep met ‘limited fetal surveillance’ (N=1144), is het relatief risico op MAS bij het gebruik van amnioninfusie wel significant, namelijk 0.17 [0.05-0.52], p<0.05.
Voor de Nederlandse situatie, met continue CTG-bewaking (en dus uitgaand van standard ‘fetal surveillance’) geeft routinematige amnioninfusie bij meconiumhoudend vruchtwater, geen vermindering in het optreden van het meconium aspiratie syndroom.
2. Vermindering in perinatale sterfte met amnioninfusie voor foetussen met meconiumhoudend vruchtwater.
In de meta-analyse is slechts 1 artikel opgenomen dat deze uitkomstmaat beschrijft. Het gaat om 1975 vrouwen uit de studie van Fraser et al. met standaard fetal surveillance. Het RR voor perinatale sterfte of ernstige morbiditeit is 1.13 [0.88-1.47] bij het gebruik van amnioninfusie bij meconiumhoudend vruchtwater (p=0.33).
Routinematige amnioninfusie bij meconiumhoudend vruchtwater, geeft geen vermindering in het optreden van perinatale sterfte.
3. NICU-opname (5-10% relatieve reductie)
Er is sprake van een significante reductie in het aantal neonaten dat wordt opgenomen op de NICU en/of mechanische ventilatie nodig heeft bij het gebruik van amnioninfusie. Dit geldt zowel voor de gehele groep (RR0.51 [0.38-0.68], p<0.001), als voor de subgroep van ‘standaard’ perinatale zorg (RR 0.45 [0.23-0.90], p=0.023). Het absolute verschil in NICU-opnames voor de gehele studiegroep daalt van 16.6% in de controlegroep naar 14.9% in de amnioninfusiegroep.
Routinematige amnioninfusie bij meconiumhoudend vruchtwater, geeft een vermindering in het aantal opnames op de NICU.
4. Apgar-score <7 (5-10% relatieve reductie)
Voor deze uitkomstmaat zijn 4020 neonaten geanalyseerd. Er wordt significant minder vaak een Apgar-score <7 gevonden na 5 minuten (RR0.56 [0.39-0.79], p<0.001) bij het gebruik van amnioninfusie. Bij de 2873 kinderen die in een situatie van ‘standaard’ perinatale zorg geboren werden, was er echter geen significant verschil (RR0.80 [0.52-1.22], p=0.30) in Apgar-score <7 na 5 minuten bij het gebruik van amnioninfusie.
Voor de Nederlandse situatie, met standard ‘fetal surveillance’ en continue CTG-bewaking geeft routinematige amnioninfusie bij meconiumhoudend vruchtwater, geen vermindering in het optreden van een Apgar-score <7 na 5 minuten.
5. Sectio (absoluut verschil 1%)
In de meta-analyse van Hofmeyr et al. wordt er na amnioninfusie een significante reductie in het aantal sectio’s gezien voor foetale nood, zowel in de studies met ‘standard fetal surveillance’ (RR0.40 [0.19-0.86], p=0.018), als in de studies met ‘limited fetal surveillance’ (RR0.38 [0.27-0.54], p<0.001). Het absolute verschil in de ‘standard fetal surveillance’ groep is 1.56% (10.97% vs. 12.53%), en in de ‘limited fetal surveillance’ groep 12.92% (7.94% vs. 20.86%), wat dus klinisch relevante verschillen zijn.
Als er gekeken wordt naar het aantal sectio’s ongeacht de indicatie blijft de risico-reductie bij het gebruik van amnioninfusie in de ‘limited fetal surveillance’ groep aanwezig (RR 0.59 (0.41-0.85), p=0.0036). In de ‘standard fetal surveillance’ groep is er wel een trend naar minder overall sectio’s, maar geen significante reductie bij het gebruik van amnioninfusie (RR 0.78 (0.60-1.02), p=0.065).
Voor de Nederlandse situatie, met ‘standard fetal surveillance’ en continue CTG-bewaking geeft routinematige amnioninfusie bij meconiumhoudend vruchtwater, geen reductie in het totaal aantal sectio’s, maar wel een reductie in het aantal sectio’s voor foetale nood, met een absoluut verschil van 1.56% (p=0.018).
6. Complicaties amnioninfusie
In de meta-analyse van Hofmeyr et al. wordt er geen verschil gezien in het optreden van endometritis, of ernstige maternale morbiditeit of mortaliteit.
Bewijskracht van de literatuur
De bewijskracht (start hoog) voor alle uitkomstmaten is met 2 niveaus verlaagd gezien de meeste trials niet voldoende allocation concealment en een hoge loss to follow-up hebben. Daarnaast waren de meeste trials klein en zijn er geen betrouwbaarheidsintervallen geregistreerd.
Wel zijn er veelal dezelfde uitkomsten in verschillende studies gerapporteerd, zijn het vergelijkbare studies, zijn het allemaal Randomized Controlled Trials (RCT’s) en is erin vrijwel alle studies gekeken naar dezelfde uitkomstmaat.
Er zijn geen aanwijzingen voor publication bias.
Zie Table of quality assessment for systematic reviews, RCTs and observational studies.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de zoekvraag met behulp van de volgende PICO:
PICO
P (welke patiëntencategorie): foetus met meconiumhoudend vruchtwater
I (welke interventie): amnioninfusie durante partu
C (welke comparison): geen amnioninfusie
O (welke uitkomstmaten): perinatale sterfte, meconium-aspiratie syndroom, NICU-opname (Neonatale Intensive Care Unit), Apgar-score <7 na 5 min, Sectio Caesarea, complicaties amnioninfusie
Relevante uitkomstmaten
De werkgroep achtte perinatale sterfte en het optreden van meconium-aspiratie syndroom voor de besluitvorming kritieke uitkomstmaten. De werkgroep achtte het optreden van NICU-opname, Apgar-score <7 na 5 minuten, sectio Caesarea en complicaties van amnioninfusie voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde een klinisch relevant verschil als volgt:
- Vermindering meconium-aspiratie syndroom (5-10% relatieve reductie)
- Vermindering in perinatale sterfte (absoluut verschil 0.1%)
- NICU-opname (5-10% relatieve reductie)
- Apgar-score <7 (5-10% relatieve reductie)
- Sectio (absoluut verschil 1%)
- Complicaties amnioninfusie
Zoeken en selecteren (Methode)
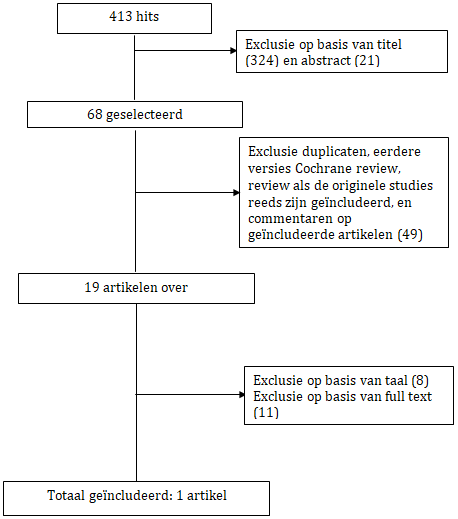
Er werd gezocht in Cochrane en Pubmed naar foetus met meconiumhoudend vruchtwater en amnioninfusie. Hiervoor werd de volgende zoekstrategie gebruikt: ((((((mecon* [tiab]) OR meconium [MeSH Terms]) AND amnioninfusie [tiab])) OR amnio-inf* [tiab]) OR amnioninf* [tiab]) OR amnioinf* [tiab]. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 413 treffers op. Studies werden geïncludeerd wanneer gerandomiseerd of quasi-gerandomiseerd het verschil onderzocht was tussen amnioninfusie of een controle (placebo (‘sham infusion’) of routine CTG-controle) bij meconiumhoudend vruchtwater. Er diende tenminste 1 neonatale uitkomst gerapporteerd te zijn (zoals meconiumaspiratiesyndroom, Apgar-score), of obstetrische interventies (zoals kunstverlossing) of complicaties van de amnioninfusie. Er was een taalrestrictie tot Engels of Nederlands. Artikelen over amnioninfusie voor een andere indicatie werden geëxcludeerd, evenals studies waarbij meerdere interventies tegelijk werden toegepast in de studiegroep.
Op basis van de titel en het abstract werden in eerste instantie 19 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 18 studies geëxcludeerd (zie exclusietabel onder het tabblad ‘verantwoording’), en slechts 1 meta-analyse definitief geselecteerd.
Uiteindelijk is er slechts 1 publicatie opgenomen in de literatuuranalyse. De overige studies zijn geëxcludeerd omdat de studie-opzet niet (quasi-)gerandomiseerd was, of van onvoldoende kwaliteit was. Het zijn veelal studies die zijn uitgevoerd in ontwikkelingslanden met een zeer hoge perinatale sterfte. De belangrijkste studiekarakteristieken en resultaten van zowel de geïncludeerde als de geëxcludeerde studies worden hieronder beschreven. De redenen voor de exclusie van de studies zijn opgenomen in de tabel (tabel: reden exclusie studies meta-analyse, p.9). De beoordeling van de individuele studieopzet is tevens hieronder beschreven.
- Cleary GM, Wiswell TE. Meconium-stained amniotic fluid and the meconium aspiration syndrome. An update. Pediatr Clin N Am 1998;45:511-29.
- Becker S, Solomayer E, Dogan C, Wallwiener D, Fehm T. Meconium-stained amniotic fluid - Perinatal outcome and obetstrical management in a low-risk suburban population. Eur J Obstet Gyn Repr Biol 2007;132:46-50.
- Richtlijn NVOG. Meconiumhoudend vruchtwater. Goedgekeurd op 23-03-2011.
- Dorairajan, G. and Soundararaghavan, S. (2005), CASE REPORT: Maternal death after intrapartum saline amnioinfusion—report of two cases. BJOG: An International Journal of Obstetrics & Gynaecology, 112: 1331–1333
- Wilmink FA, Wilms FF, Heydanus R, Mol BW, Papatsonis DN. Fetal complications after placement of an intrauterine pressure catheter: a report of two cases and review of the literature. J Maternal Fetal Neonatal Med. 2008 Dec; 21(12):880-3.
- Handwerker SM, Selick AM. Placental abruption after insertion of catheter tip intrauterine pressure transducers: a report of four cases. J reprod med. 1995 Dec;40(12):845-9.
- Hofmeyr GJ, Xu H, Eke AC, Amnioinfusion for meconium stained liquor in labor. Cochrane Database Syst Rev. 2014;(2):CD 000014.
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention |
Control |
Follow-up |
Outcome measures and effect size |
Comments |
|
Hofmeyr 2014 |
Type of study: meta-analysis Setting: inpatients, in labour
Country: various |
Inclusion criteria: women in labour with moderate to thick meconium
N at baseline: 4435 |
Amnioninfusion during labour with saline or Ringer’s. Given through intra-uterine pressure catheter or other method. |
No amnioninfusion or sham infusion |
Length of follow-up: until delivery
Incomplete data: described in detail in the study. Incomplete data in many of the included studies due to rapid delivery or need for emergency Caesarean section |
Outcome measure 1: Meconium aspiration syndrome Standard fetal surveillance. N=3374 RR [95% CI], 0.52 [0.26, 1.06], Limited fetal surveillance N=1144. RR 0.17 [0.05-0.52]. random effects model.
Outcome measure 2: Perinatal death. Limited fetal surveillance: not reported. Standard fetal surveillance N=1975. RR1.13 [0.88-1.47]. Fixed effects model.
Outcome measure 3: CS for fetal distress Standard fetal surveillance N=2765. RR0.40 [0.19-0.86]. Limited fetal surveillance N=1137. RR 0.38 [0.27-0.54]. Random effects model.
|
Conclusion study; routine amnioninfusion not recommend for settings with standard fetal surveillance. |
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
|
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Hofmeyer 2014 |
yes |
yes |
yes |
yes |
yes |
yes |
Not for all studies, random and fixed effect models are used. |
yes |
no |
|
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Bansal 2013 |
Artikel uit India, niet vergelijkbaar met Nederlandse situatie |
|
Bathia 2013 |
Artikel uit India, niet vergelijkbaar met Nederlandse situatie |
|
Engel 2008 |
Artikel in Pools |
|
Chabernaud 2007 |
Artikel in Frans |
|
Das 2007 |
Artikel uit India, niet vergelijkbaar met Nederlandse situatie. Geen CTG-bewaking toegepast. |
|
ACOG committee 2006 |
Richtlijntekst. Geen individuele studie |
|
Sood 2004 |
Artikel uit India, niet vergelijkbaar met Nederlandse situatie |
|
Gramellini 2000 |
Artikel in Italiaans |
|
Fraser 2000 |
Artikel in Frans |
|
Hourdequin 1999 |
Artikel in Frans |
|
De Meeus 1997 |
Artikel in Frans |
|
Folsom 1997 |
Review. Geen vergelijkende studie. |
|
Luton 1996 |
Artikel in Frans |
|
Rogers 1996 |
Case-controle studie, waarbij niet goed gematcht is. Geen goede vergelijkende studie-opzet. |
|
Ushing 1993 |
Retrospectieve studie. Co-interventies. |
|
Sivan 1992 |
Review. Geen vergelijkende studie. |
|
Wu 1991 |
Case-controle studie, geen goede vergelijkende opzet. |
|
Wu 1988 |
Artikel in Chinees |
Reden exclusie studies meta-analyse
|
Studie |
Interventie |
Outcome |
Risico MAS amnioninfusie |
Risico MAS controle |
RR / p-waarde |
GRADE |
Reden exclusie |
|
Gupta 2011 |
|
|
|
|
|
|
Alleen abstract beschikbaar. |
|
Regi 2009 |
|
|
|
|
|
|
Amnioninfusie voor andere indicatie (deceleraties), niet standaard bij meconiumhoudend vruchtwater. |
|
Engel 2008 |
|
|
|
|
|
|
Poolse studie, taalrestrictie. Geen gerandomiseerde studie. |
|
Das 2007 India (geen CTG) |
Amnioninfusie versus controle (N=50+100) Case-controle |
MAS |
4% |
18% |
0.22 (0.05-0.92) |
Very low |
Vergelijkende studie, weinig power. Setting niet vergelijkbaar met Nederlandse setting. |
|
Mukhopadhyay 2006 |
Amnioninfusie vs. Controle (N=93+95) |
Sectio Caesarea, Apgar-score |
9% 41% sectio foetale nood controle groep, 19.3% in studiegroep. |
3.3% |
N.S.
P<0.01 sectio
Apgar-score na 1 en 5min N.S. |
Very Low |
Geen gerandomiseerde trial, wel vergelijkend. Niet primair gekeken naar MAS. Geen CTG-controle. |
|
Ashfaq 2004 Setting: Pakistan |
Amnioninfusie versus controle (N=400) |
MAS |
24/200 (12%) |
70/200 (35%) |
p<0.001 |
Vey low |
Case-controle studie, weinig power, geen duidelijke randomisatie, setting niet vergelijkbaar met Nederlandse situatie |
|
Gonzales 2002 |
|
|
|
|
|
|
Beantwoordt uitgangsvraag niet. Vergelijkt verschillende vloeistoffen voor amnioninfusie, geen amnioninfusie versus controle |
|
Kirubamani 2000 |
|
|
|
|
|
|
Boekpublicatie, geen vergelijkend onderzoek. |
|
Lembet 1999 |
|
|
|
|
|
|
Geen data gepresenteerd. Transabdominale amnioninfusie niet vergelijkbaar met Nederlandse setting. |
|
Edwards 1998 |
Profylactisch cefazoline bij amnioninfusie |
|
|
|
|
|
Beantwoordt uitgangsvraag niet |
|
Gonzales 1998 |
|
|
|
|
|
|
Beantwoordt uitgangsvraag niet. Vergelijkt verschillende vloeistoffen voor amnioninfusie, geen amnioninfusie versus controle |
|
Khosla 1997 |
Amnioninfusie versus controle (N=50) |
Neonatale uitkomst |
|
|
Geen verschil |
Very low |
Niet gerandomiseerd. Kleine case-controle studie met slechts 25 patiënten per groep. |
|
Lo 1993 |
Amnioninfusie versus controle (keus patiënt), N=112 |
Neonatale uitkomsten, kunstverlossing |
|
|
Minder kunstverlossingen voor foetale nood, neonatale uitkomst verbetert. |
|
Niet gerandomiseerd. Kleine studie. Uitgevoerd in Hong Kong. Niet geheel vergelijkbaar met Nederlandse situatie. |
|
Ilagan 1992 |
|
|
|
|
|
|
Inadequate beschrijving studie. |
|
Nageotte 1991 |
|
|
|
|
|
|
Beantwoordt uitgangsvraag onvoldoende. Met name patiënten meegenomen met oligohydramnion in plaats van meconiumhoudend vruchtwater. |
|
Adam 1989 |
|
|
|
|
|
|
Resultaten gepresenteerd op congres, incomplete data. |
Karakteristieke studies niet opgenomen in meta-analyse Hofmeyr et. al 2014
|
Studie |
Interventie |
Outcome |
Risico MAS amnioninfusie |
Risico MAS controle |
RR / p-waarde |
GRADE |
Reden exclusie |
|
Bansal 2013 India |
Amnioninfusie versus controle (N=100) |
MAS |
3/50 (6%) |
5/50 (10%) |
0.0001 |
Very low |
Case-controle studie, lage power |
|
Bathia 2012 India |
Amnioninfusie versus controle (N=100) |
MAS |
3/50 (6%) |
10/50 (20%) |
0.037 |
Very low |
Case-controle studie, lage power |
|
Rogers 1996 Hong Kong |
Amnioninfusie versus controle N=298 in AI groep
|
MAS |
1.7% |
3.7% |
NS |
Very Low |
Case-controle studie, slechte matching, lage power |
|
Uhing 1993 USA |
Amnion-infusie versus controle. Routine uitzuigen. N=110+336 |
MAS |
1.8% |
5.5% |
|
Low |
Case-controle studie, lage power |
|
Wu 1991 China |
Amnioninfusie versus controle (N=73+104) Case-controle |
MAS |
|
|
<0.05 Verlaagd risico in amnioninfusie groep |
Very low |
Case-controle studie, lage power |
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-09-2019
Beoordeeld op geldigheid : 21-08-2019
© 2019 Nederlandse Vereniging voor Obstetrie en Gynaecologie (NVOG)
Momenteel is de werkgroep niet op de hoogte van grote trials die lopen naar dit onderwerp. Er zijn geen kennislacunes over de veiligheid van amnioninfusie. Wel is er een kennislacune over de effectiviteit van amnioninfusie voor de Nederlandse situatie.
De NVOG is als houder van deze module de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijnmodule deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijnmodule delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Samenstelling werkgroep
Voor het beoordelen van de actualiteit van deze richtlijnmodule is de Otterlo werkgroep (L. Monen (AIOS), M.M. Porath/Maxima MC en M.T.M. Franssen/UMCG) verantwoordelijk, die in stand zal blijven. Uiterlijk in 2022 bepaalt de Otterlo werkgroep van de NVOG of deze module nog actueel is. De geldigheid van deze module komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
Meelezers:
- Leden van de Otterlo- werkgroep
Met ondersteuning van:
- Dr. E.M.E. den Breejen, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen. (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Geen van de werkgroepleden heeft eventuele belangen.
Inbreng patiëntenperspectief
De conceptmodule is voor commentaar voorgelegd aan de Patiëntenfederatie Nederland (PFN) en de PFN onderschrijft deze module.
Methode ontwikkeling
Evidence based
Zoekverantwoording
Search details:
(((((mecon[tiab] OR mecon's[tiab] OR meconella[tiab] OR meconema[tiab] OR meconematinae[tiab] OR meconematini[tiab] OR meconemopsis[tiab] OR mecones[tiab] OR meconeum[tiab] OR meconh[tiab] OR meconh2[tiab] OR meconhch[tiab] OR meconia[tiab] OR meconial[tiab] OR meconian[tiab] OR meconic[tiab] OR meconidia[tiab] OR meconidium[tiab] OR meconin[tiab] OR meconine[tiab] OR meconiophages[tiab] OR meconiorrhexis[tiab] OR meconium[tiab] OR meconium'[tiab] OR meconium's[tiab] OR meconiumcrit[tiab] OR meconiumileus[tiab] OR meconiums[tiab] OR meconiumstained[tiab] OR meconiumstaining[tiab] OR meconiumthorax[tiab] OR meconiun[tiab] OR meconnabitre[tiab] OR meconnaissance[tiab] OR meconnt[tiab] OR meconnu[tiab] OR meconnue[tiab] OR meconnues[tiab] OR meconoh[tiab] OR meconoium[tiab] OR meconopsi[tiab] OR meconopsidis[tiab] OR meconopsis[tiab] OR meconopsishorridula[tiab] OR meconoquintupline[tiab] OR meconostigma[tiab] OR meconotherapy[tiab] OR meconuim[tiab]) OR "meconium"[MeSH Terms]) AND amnioninfusie[tiab]) OR amnio infusion[tiab]) OR (amnioninfection[tiab] OR amnioninfusion[tiab])) OR (amnioinfuion[tiab] OR amnioinfusate[tiab] OR amnioinfused[tiab] OR amnioinfusion[tiab] OR amnioinfusion'[tiab] OR amnioinfusions[tiab])