Wondbehandeling na littekenbreuk
Uitgangsvraag
Hoe dient de wond na een littekenbreuk behandeld te worden?
Aanbeveling
Overweeg negatieve-druktherapie (NDT) bij de behandeling van open buikwonden bij gesloten fascie na een littekenbreukoperatie.
Overweeg de gesloten incisie na een littekenbreukoperatie te behandelen met (profylactische) negatieve- druktherapie (NDT) bij hoogrisicopatiënten en gecontamineerde ingrepen.
Overwegingen
Alhoewel er geen studies gevonden zijn omtrent NDT versus andere wondbedekkingen bij open buikwonden na littekenbreukoperaties, zijn er wel verscheidene studies en reviews over NDT toegepast op wonden met een andere etiologie.
De Cochrane review van Dumville (2016) includeerde 2 studies van patiënten met chirurgische open wonden, die NDT vergeleken met alginaat en siliconengaas. In totaal werden 69 patiënten geïncludeerd. Tijd tot wondgenezing was in 1 studie korter met NDT dan met alginaat (gemiddeld 57 dagen bij NDT versus 104 dagen met alginaat). De andere studie (sin pil wonden) liet nauwelijks verschil in genezingstijd zien (NDT versus siliconenverband).
Vikatmaa (2008) is een systematische review naar de effectiviteit en veiligheid van NDT bij verschillende soorten ‘problematische’ wonden. Veertien RCT’s werden geïncludeerd (twee over decubituswonden, drie over posttraumatische wonden, vier over diabetische voetwonden en vijf over diverse chronische wonden). In alle onderzochte studies was NDT minstens even effectief en in sommige studies effectiever dan de controlebehandeling. Bij beenulcera’s en posttraumatische wonden werd het grootste voordeel voor NDT gevonden. Van de geïncludeerde studies waren er twee van goede kwaliteit, de rest had een lage interne validiteit.
De resultaten van deze studies kunnen niet zonder meer overgenomen worden voor buikwonden die kunnen ontstaan na een littekenbreuk operatie. Met name het a vu liggen van de mesh kan de wondgenezing bemoeilijken. De praktijk laat zien dat het granulatie weefsel moeizaam over/door de mesh groeit. NDT lijkt hier (practice-based) wel een meerwaarde te hebben.
Patiënten ervaren NDT wisselend. Een systematische review van Janssen (2016) naar de kwaliteit van leven van patiënten met NDT, laat zien dat de kwaliteit van leven aan het einde van de therapie verbetert, onafhankelijk van de therapie. In de eerste week NDT leidt NDT tot een lagere kwaliteit van leven, mogelijk door angst.
Er zijn meerdere studies naar de kosteneffectiviteit van NDT gedaan. De Leon (2009) vond dat NDT goedkoper is dan standaard wondzorg. Materialen van NDT zijn weliswaar duurder, maar dit wordt gecompenseerd door lagere zorgverlenerskosten (minder zorg momenten) en snellere wondheling. Het onderzoek van Driver (2016) ondersteunt deze bevindingen.
De keuze voor de therapie (NDT of anders) is patiëntafhankelijk. Er dient per patiënt bekeken te worden waar deze specifieke patiënt het best bij gebaat is. Afwegingen hierbij zijn het wel of niet a vu liggen van de mesh, de mate van angst bij de patiënt, de voorkeur van de patiënt voor de ene of de andere therapie (wenst de patiënt bijvoorbeeld dagelijks te douchen) et cetera.
NDT op gesloten incisies is een redelijk recente ontwikkeling. Er zijn nog weinig vergelijkende trials beschikbaar met betrekking tot littekenbreukwonden. Behalve de preventie van SSI’s, dient ook rekening gehouden te worden met kosteneffectiviteit. In dit kader dient NDT niet geplaatst te worden op alle gesloten incisies bij patiënten die een littekenbreukoperatie hebben ondergaan. Alleen de patiënten, die een hoger risico lopen op SSI komen in aanmerking voor NDT.
Naast de vier studies over NDT op gesloten incisies, heeft ook de WHO hier een uitspraak over gedaan. Zij stellen: “The panel suggests the use of prophylactic negative pressure wound therapy (pNPWT) in adult patients on primarily closed surgical incisions in high-risk wounds, for the purpose of the prevention of SSI, while taking resources into account. (Conditional recommendation, low quality of evidence).”
Recent is een retrospectieve vergelijkende studie gedaan bij patiënten met electieve, hoogcomplexe buikwandhersteloperaties (de Vries, 2017). In totaal werden 66 patiënten geincludeerd (32 pNPWT en 34 controlegroep). De studiegroep betrof in meer of mindere mate verontreinigde operaties door enterocutane fistels, enterostomieën of geïnfecteerde matten. De mediane duur van pNPWT was 5 dagen (IQR 5 tot 7). Totale percentage wondinfecties was 35%. pNPWT was geassocieerd met een significante afname van postoperatieve wondinfecties (24 versus 51%, p = 0,029, of 0,30 (95% CI 0,10
tot 0,90)). Wondinfecties van de incisies daalden van 48 tot 7% (p <0,01, of 0,08 (95% CI 0,16 tot 0,39). Het aantal subcutane abcessen was vergelijkbaar in beide groepen. Er waren minder interventies nodig in de pNPWT-groep (p<0,001). De Vries (2017) concludeerde dat gesloten incisie pNPWT een veelbelovende oplossing lijkt om de incidentie van wondinfecties bij complexe buikwandchirurgie te verminderen.
Onderbouwing
Na hersteloperaties van een littekenbreuk worden wonden soms opengelaten of ze gaan door verhoogde (abdominale) druk open. Soms ligt de mesh a vu, wat de granulatievorming en epithelialisatie bemoeilijkt, en derhalve de wondgenezing vertraagt.
Bij grote buikwonden kan vaak gekozen worden voor conventionele verbandmaterialen zoals natte gazen, ‘moderne’ wondverbanden die een vochtig wondmilieu bewerkstelligen of voor negatieve-druktherapie (NDT). De vraag bestaat of er een verschil is in genezingstijd en patiëntcomfort tussen de conservatieve wondbehandelingsmogelijkheden en behandeling met negatieve-druktherapie.
Daarnaast zien we de laatste jaren een opkomst van NDT op gesloten incisies, om SSI’s en overige complicaties (seroom, hematoom, wond dehiscentie, huidnecrose, fistelvorming) te voorkomen. De vraag bestaat of NDT op gesloten incisies bij littekenbreuken daadwerkelijk de kans op complicaties als SSI vermindert.
Er is geen literatuur gevonden over het effect van het gebruik van NDT versus andere wondbedekking bij open buikwonden na een littekenbreuk operatie. Er is wel literatuur gevonden over het effect van incisionele negatieve-druktherapie na een littekenbreuk operatie.
Wondbehandeling (wond dehiscentie)
|
Zeer laag GRADE |
Er is met zeer lage bewijskracht aangetoond dat incisionele negatieve druktherapienegatieve-druktherapie in vergelijking tot standaard wondbehandeling de kans op wonddehiscentie vermindert.
Bronnen (Swanson, 2016) |
Operatiewondinfecties (SSI)
|
Zeer laag GRADE |
Er is met zeer lage bewijskracht aangetoond dat incisionele negatieve- druktherapie in vergelijking tot standaard wondbehandeling de kans op operatiewondinfecties vermindert.
Bronnen (Swanson, 2016) |
Overige complicaties
|
Zeer laag GRADE |
Er is met zeer lage bewijskracht aangetoond dat incisionele negatieve- druktherapie in vergelijking tot standaard wondbehandeling de kans op overige complicaties (seroom, hematoom, necrotiserende huid en chirurgische complicaties) vermindert.
Bronnen (Swanson, 2016) |
De systematische review beschreef de resultaten van 5 studies: alle retrospectieve niet- gerandomiseerde studies, waarbij medische dossiers werden geraadpleegd van patiënten met een littekenbreuk (Gassman, 2015; Condé-Green, 2013; Olona, 2014; Pauli, 2013; Soares, 2014). De studie van Soares (2015) bevatte 115 patiënten in de interventiegroep en 84 in de controlegroep, de studie van Pauli bevatte 49 patiënten in de interventiegroep en 70 in de controlegroep, de studie van Gassmann (2015) bevatte 29 patiënten in de interventiegroep en 32 in de controlegroep, de studie van Olona beschreef 5 patiënten in de interventie- en 37 in de controlegroep, en de studie van Condé-Green (2013) bevatte 23 patiënten in de interventiegroep en 33 in de controlegroep.
Verschillende vormen van negatieve-druktherapie (NDT) werden vergeleken met de standaard wondbedekking op gesloten incisies na buikwandreconstructies. In de studie van Soares (2015) werd een hybride NDT vergeleken met droge gazen. De bedekking in de hybride NDT-groep bestond uit kleine blokjes polyurethaan white foam met daaromheen de open cell polyurethaanfoam gelegd en het geheel werd bedekt met folie. Continue druk van 125 mmHg werd toegepast en het verband werd na 3 dagen verwijderd. Indien de white foam blokjes verzadigd waren, werden ze verplaatst en werd opnieuw 48 uur NDT toegepast. In 2 andere studies werd de wond primair gesloten en werden droge gazen vergeleken met NDT. In de NDT-groep werd de wond bedekt met niet-verklevend gaas met daarover polyurethaan foam (zwart), en werd gedurende maximaal 7 dagen continu 125 mmHg druk toegepast (Pauli, 2013; Gassman, 2014). Ook in de studie van Condé-Green (2013) werd de wond primair gesloten en werden gazen vergeleken met NDT. In de NDT-groep werd de wond bedekt met niet-verklevend gaas en bedekt met zwart polyurethaan foam. Er werd een continue negatieve druk van 125mm Hg toegepast tot op de 5de postoperatieve dag (Condé-Green, 2013).
Patiënten werden niet gerandomiseerd maar ondergingen de type wondbehandeling, gebaseerd op chirurg voorkeur (Gassman, 2014) of door volgorde in de tijd. Patiënten die later werden geincludeerd ontvingen vaker NDT dan de standaard wondbedekking (Soares, 2015; Pauli, 2013; Condé-Green, 2013).
De volgende uitkomsten werden beschreven: operatiewondinfecties en overige complicaties (seroom, hematoom, wonddehiscentie, huidnecrose, Dindo–Clavien- classificatie voor chirurgische complicaties en operatiewondvoorvallen (optelsom van operatiewondinfecties, seroma, wonddehiscentie en enterocutaneous fistel)). In alle studies lag de gemiddelde leeftijd van patiënten tussen de 54 en 56 jaar in beide groepen. Het gemiddelde percentage mannen in de interventiegroep was 44±25 en in de controlegroep 36±21, maar de verdeling per groep in de studie van Condé-Green (2013) werd niet gerapporteerd (n=56, waarvan 33 vrouw en 23 man).
De volgende uitkomsten werden niet in de literatuur beschreven: wondgenezing, tijd tot herstel, gereed voor split-skin graft, huidtransplantatie, pijn, patiëntvoorkeuren, patiënt comfort, kwaliteit van leven en mortaliteit.
Resultaten
Wondbehandeling
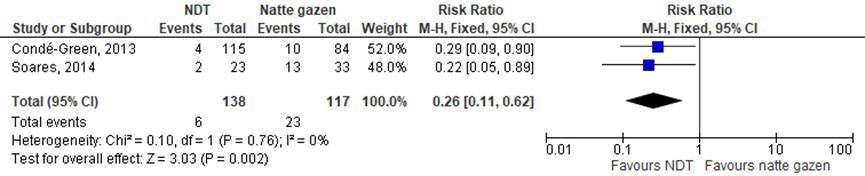
Uit 2 studies bleek dat de behandeling met negatieve-druktherapie (NDT) het risico op het openblijven van de wond statisch significant verkleint. In de NDT-groep bleven 6/138 wonden open. In de controlegroep waren dat er 23/117. Het relatieve risico op het openblijven van de wond in de NDT-groep ten opzichte van de controlegroep was 0,25 (95% CI 0,11 tot 0,62; I2=0%).
Figuur 1 Meta-analyse waarin het verschil in effect tussen NDT en natte gazen op de uitkomstmaat wonddehiscentie wordt getoond
Complicaties wondbehandeling
Operatiewond infecties (SSI)
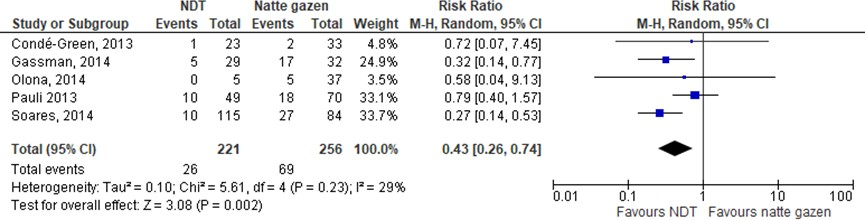
Alle studies onderzochten het effect van NDT bij littekenbreuken op operatiewondinfecties (Surgical Site Infections; SSI). Het meetmoment (tussen 30 en 90 dagen) was heterogeen, maar in het algemeen valt op in een meta-analyse van de studies dat gemiddeld het risico op een SSI in de NDT-groep statisch significant kleiner is (relatief risico= 0,43; 95% CI 0,26 tot 0,74; I2=29%). In de studies werd niet gecorrigeerd voor mogelijke confounders.
Er waren ook significant minder operatiewondvoorvallen in de NDT-groep ten opzichte van standaard wondbedekking (17% NDT versus 42% standaard wondbehandeling; OR 0,21, 95% CI 0,09 tot 0,52; P<0,001). Condé-Green (2013) bekeek ook een samengestelde maat, en beschreef huiddehiscentie, huid/vet-necrose en infectie gezamenlijk als algehele wondcomplicaties. Er waren significant minder algehele wondcomplicaties in de NDT- groep (22% NDT versus 63,6% standaard wondbehandeling; p=0,02; OR 6,3, 95% CI 1,37
tot 34,14).
Bewijskracht van de literatuur
Observationele studies beginnen ‘laag’ in bewijskracht volgens de GRADE-methodiek. De bewijskracht voor de uitkomstmaat operatiewondinfecties is verder verlaagd gezien beperkingen in de onderzoeksopzet (uitkomstmaten zijn niet gecorrigeerd voor belangrijke confounders) en het geringe aantal events (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Figuur 2 Meta-analyse waarin het verschil in effect tussen NDT en natte gazen op de uitkomstmaat SSI wordt getoond
Bewijskracht van de literatuur
Observationele studies beginnen ‘laag’ in bewijskracht volgens de GRADE-methodiek. De bewijskracht voor de uitkomstmaat operatiewondinfecties is verder verlaagd gezien beperkingen in de onderzoeksopzet (uitkomstmaten zijn niet gecorrigeerd voor belangrijke confounders) en het geringe aantal events (n=95) (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Seroom
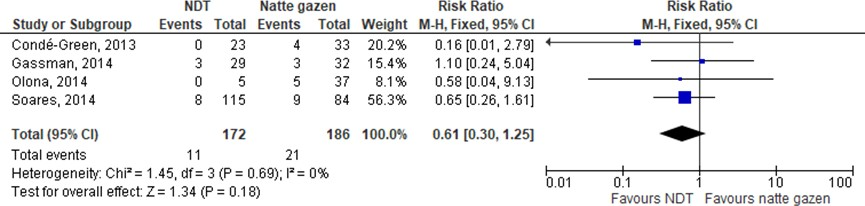
4 studies beschreven uitkomsten op seroom. Een meta-analyse van deze resultaten laat een niet-significant relatief risico zien van 0,61 (95% CI 0,30 tot 1,25). Het is op basis van deze gegevens daarom niet te voorspellen welke interventie beter is.
Figuur 3 Meta-analyse waarin het verschil in effect tussen NDT en natte gazen op de uitkomstmaat seroom wordt getoond
Bewijskracht van de literatuur
Observationele studies beginnen ‘laag’ in bewijskracht volgens de GRADE-methodiek. De bewijskracht voor de uitkomstmaat operatiewond infecties is verder verlaagd gezien beperkingen in de onderzoeksopzet (uitkomstmaten zijn niet gecorrigeerd voor belangrijke confounders) en het zeer geringe aantal events (n=32) (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Recidiverende littekenbreuk
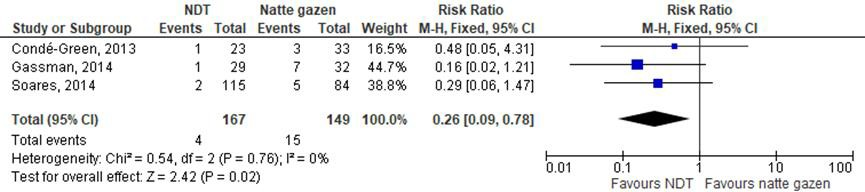
In 3 studies werd onderzocht hoe vaak de littekenbreuk na behandeling weer terugkwam (recidief). Een meta-analyse van deze resultaten laat een statistisch significant voordeel zien voor de behandeling met NDT ten opzichte van natte gazen (controlebehandeling). RR= 0,26 (95% CI 0,09 tot 0,78; I2=0%). De resultaten zijn gebaseerd op een zeer klein aantal events (n=19).
Figuur 4 Meta-analyse waarin het verschil in effect tussen NDT en natte gazen op de uitkomstmaat recidief wordt getoond
Bewijskracht van de literatuur
Observationele studies beginnen ‘laag’ in bewijskracht volgens de GRADE-methodiek. De bewijskracht voor de uitkomstmaat recidief is verder verlaagd gezien beperkingen in de onderzoeksopzet (uitkomstmaten zijn niet gecorrigeerd voor belangrijke confounders) en het zeer geringe aantal events (n=19) (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Overige complicaties
Overige complicaties (hematoom, en necrotiserende huid) hadden allen een lage incidentie tussen de 0 tot 12% per groep, waarbij alleen in de studie van Condé-Green de incidentie van necrotiserend huid- én vetweefsel (gezamenlijk) 18% in de controlegroep was. Gassman (2015) en Condé-Green (2013) vonden geen significant verschil voor hematoom en necrotiserende huid (waarbij Condé-Green (2013) necrotiserende huid en necrotiserend vet combineerde in één uitkomstmaat). Soares (2015) beschreef 2 samengestelde maten voor complicaties, de Dindo–Clavien Bewijskracht van de literatuur Observationele studies beginnen ‘laag’ in bewijskracht volgens de GRADE-methodiek. De bewijskracht voor de uitkomstmaat recidief is verder verlaagd gezien beperkingen in de onderzoeksopzet (uitkomstmaten zijn niet gecorrigeerd voor belangrijke confounders) en het zeer geringe aantal events (n=19) (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.-classificatie voor chirurgische complicaties en operatiewond voorvallen (optelsom van operatiewondinfecties, seroma, dehiscentie en enterocutaneous fistel). Er waren significant minder chirurgische complicaties volgens de Dindo–Clavien-classificatie in de NDT-groep ten opzichte van standaard wondbedekking (19% NDT versus 31% standaard wondbehandeling; OR 0,41, 95% CI 0,17 tot 0,96; p=0,04).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvragen:
Wat zijn de (on)gunstige effecten van negatieve-druktherapie ten opzichte van andere wondbehandelingen ter behandeling van de open wond na een littekenbreuk?
P: patiënten met een littekenbreuk; I: negatieve-druktherapie;
C: tijdelijke wondbedekking, natte gazen of andere wondbedekkingen;
O: wondgenezing, tijd tot genezing, gereed voor split-skin graft, huidtransplantatie, pijn, patiëntvoorkeuren, patiëntcomfort, kwaliteit van leven, complicaties en mortaliteit.
Relevante uitkomstmaten
De werkgroep achtte snellere wondgenezing een kritieke uitkomstmaat voor de besluitvorming; en pijn, patiëntencomfort en patiëntenvoorkeuren belangrijke uitkomstmaten voor de besluitvorming.
Wat zijn de (on)gunstige effecten van (incisie)negatieve-druktherapie ten opzichte van andere wondbedekkingen ter behandeling van de gesloten wond na een littekenbreuk?
P: patiënten met een littekenbreuk; I: (incisie) negatieve-druktherapie; C: andere wondbedekkingen;
O: SSI en overige complicaties (seroom, hematoom, wond dehiscentie, huidnecrose, fistelvorming).
Relevante uitkomstmaten
De werkgroep achtte minder SSI’s en minder overige complicaties (seroom, hematoom, wond dehiscentie, huidnecrose, fistelvorming) belangrijke uitkomstmaten voor de besluitvorming.
Zoeken en selecteren (Methode)
In de database Medline (via OVID), Embase (via Embase.com) is met relevante zoektermen gezocht naar systematische reviews, RCT’s, CCT’s en observationeel onderzoek gericht op de behandeling van littekenbreuken die gepubliceerd zijn vanaf 2006. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 3041 treffers op. Een adviseur van het Kennisinstituut van de Federatie Medisch Specialisten maakte een voorselectie van studies waar twee of meer behandelingen gericht op littekenbreuken met elkaar waren vergeleken. Na de voorselectie zijn er 243 studies overgebleven waarvan 172 vergelijkende studies en 71 systematische reviews. Voor het beantwoorden van de uitgangsvraag werden studies geselecteerd op grond van de volgende selectiecriteria: systematische reviews, RCT’s of vergelijkend observationeel onderzoek en patiënten met een littekenbreuk.
Op basis van titel en abstract werd in eerste instantie één systematische literatuurreview (Swanson, 2016) voorgeselecteerd en één vergelijkende cohortstudie (Condé-Green, 2013). Na raadpleging van de volledige tekst werden de systematische literatuurreview en de cohortstudie geïncludeerd. De cohortstudie van Condé-Green was opgenomen in de review van Swanson en is zodoende niet apart uitgewerkt (zie exclusietabel onder het tabblad Verantwoording).
Betreffende de eerste uitgangsvraag over negatieve-druktherapie bij open wonden na littekenbreukoperaties is geen studie gevonden die NDT vergeleek met andere wondbedekkingen op open buikwonden na een littekenbreukoperatie.
De systematische review beschreef vijf studies. De review is opgenomen in de literatuuranalyse voor wat betreft de tweede uitgangsvraag. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias- tabellen.
- Condé-Green A, Chung TL, Holton LH 3rd, et al. Incisional negative-pressure wound therapy versus conventional dressings following abdominal wall reconstruction: a comparative study. Ann Plast Surg. 2013;71(4):394-7. doi: 10.1097/SAP.0b013e31824c9073. PubMed PMID:22868327.
- Driver VR, Eckert KA, Carter MJ, et al. Cost-effectiveness of negative pressure wound therapy in patients with many comorbidities and severe wounds of various etiology. Wound Repair Regen. 2016;24(6):1041-1058. PMID: 27669667.
- Dumville JC, Gray TA, Walter CJ, et al. Dressings for the prevention of surgical site infection. Cochrane Database Syst Rev. 2016;12:CD003091. PMID: 27996083.
- Gassman A, Mehta A, Bucholdz E, et al. Positive outcomes with negative pressure therapy over primarily closed large abdominal wall reconstruction reduces surgical site infection rates. Hernia. 2015;19(2):273-8. doi: 10.1007/s10029-014-1312-y. PubMed PMID:25337870.
- Janssen AH, Mommers EH, Notter J, et al. Negative pressure wound therapy versus standard wound care on quality of life: a systematic review. J Wound Care. 2016;25(3):154, 156-9. PMID: 26947696.
- Leon de JM, Barnes S, Nagel M, et al. Cost-effectiveness of negative pressure wound therapy for postsurgical patients in long-term acute care. Adv Skin Wound Care. 2009;22(3):122-7 PMID: 19247013.
- Pauli EM, Krpata DM, Novitsky YW, et al. Negative pressure therapy for high-risk abdominal wall reconstruction incisions. Surg Infect (Larchmt). 2013;14(3):270-4. doi: 10.1089/sur.2012.059. PubMed PMID: 23590852.
- Soares KC, Baltodano PA, Hicks CW, et al. Novel wound management system reduction of surgical site morbidity after ventral hernia repairs: a critical analysis. Am J Surg. 2015;209(2):324-32. PubMed PMID: 25194761.
- Vikatmaa P, Juutilainen V, Kuukasjärvi P, et al. Negative pressure wound therapy: a systematic review on effectiveness and safety. Eur J Vasc Endovasc Surg. 2008;36(4):438-48. PubMed PMID: 18675559.
- Vries de FEE, Atema JJ, Lapid O, et al. Closed incision prophylactic negative pressure wound therapy in patients undergoing major complex abdominal wall repair. Hernia. 2017;21(4):583-589. PMID: 28534258; PubMed.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3 |
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Soares, 2014 |
Type of study: Retrospective non- randomized study (review of medical records)
Setting: Single institution, single surgeon at The Johns Hopkins University School of Medicine |
Inclusion criteria: Outpatient referrals of all consecutive patients who underwent ventral hernia repairs (VHR) by a single experienced surgeon
Exclusion criteria: - |
A modified negative-pressure wound therapy system management system (Hybrid Vacuum Assisted Closure or HVAC) after ventral hernia repairs (VHRs)
Rectangular strips, or wicks, of reticulated open-cell polyurethane white foam were inserted through the dermal layer into the subcutaneous space Exposed areas of skin between the wicks were covered with silver-impregnated nonadherent dressing. A piece of reticulated open-cell polyurethane black foam was secured with adhesive dressing. Negative-pressure VAC therapy was applied at a continuous pressure of 2125 mm Hg.
HVAC dressing was removed on postoperative day 3. Replacement wicks were made shorter and narrower with each dressing change and were removed once they were qualitatively dry. The skin VAC |
Standard wound dressings (SWD). The skin was closed with staples and dry gauze was placed over the closed incision. The dressing was removed on postoperative day 2 and the incision was left open to air. |
Length of follow-up: Mean follow- up: 8.7 ± 9.9 months Intervention: 6.6 ± 6 months Control: 11.9 ± 13 months
Loss-to-follow- up: Not applicable; retrospective study design
Incomplete outcome data: Not applicable; retrospective study design |
90-day SSI (surgical site infections): 9% HVAC versus 32% SWD OR. 10, 95% CI. 03-.30; P<.001
Severe SSI: 2% HVAC versus 10% SWD OR. 22, 95% CI. 03-1.69; P=.14
SSO rate (surgical site occurrences=SSI+seroma +wound dehiscense+EC fistula): 17% HVAC versus 42% SWD OR. 21, 95% CI. 09-.52; P<.001
Seroma: 7% HVAC versus 11% SWD OR. 81, 95% CI. 21-3.13; P=.76
Wound dehiscence: 4% HVAC versus 12% SWD OR. 60, 95% CI. 13–2.78; P=.52
Dindo–Clavien Classification for surgical complications rate ≥3: 19% HVAC versus 31% SWD OR. 41, 95% CI. 17–.96; P=.04 |
|
|
|
Country: USA |
N total at baseline: Intervention: 115 Control: 84 |
|
||||
|
|
Source of funding: Investigator-initiated trial grant from KCI grant number 115258 |
Important prognostic factors2: Age ± SD: I: 56 ± 14 C: 56 ± 15 |
|
||||
|
|
|
Sex: I: 44% M C: 36% M |
|
||||
|
|
|
BMI: ± SD: I: 33.5 ± 9.9 C: 32.3 ± 7.3 |
|
|
|
|
Groups were comparable at baseline |
was then reapplied for 48 hours. At that point, the VAC was removed and the wound was approximated with steri-strips and covered with a dry dressing. The closed suction drains remained in place until drainage was 20 mL/day or less for 2 consecutive days. |
|
|
No mortality in both groups
All outcomes adjusted for age BMI, ASA classification, hernia grade, anesthesia type, total operative time, length of stay, wound classification, and mesh location. |
|
|
Pauli, 2013 |
Type of study: Retrospective non- randomized study (review of medical records)
Setting: A single academic institution, two surgeons at Department of Surgery, Case Comprehensive Hernia Center, University Hospitals Case Medical Center, Cleveland, Ohio
Country: USA |
Inclusion criteria: Patients were selected with potentially contaminated or contaminated ventral hernias undergoing repair with and without negative- pressure therapy (NPT).
Exclusion criteria: enterocutaneous or colo-cutaneous fistulae, pannicul- ectomy done simultaneously with hernia repair, and anterior components separation |
The dressings for NPT were also applied under sterile conditions in the OR. These consisted of knitted cellulose impregnated with a petrolatum emulsion and applied over the patient’s surgical incision to protect the skin from a strip of reticulated open-cell polyurethane black foam that was secured with adhesive dressings. Negative- pressure therapy was applied at a continuous pressure of -75mm Hg for seven days or until the day of the patient’s discharge from the hospital. Dressings for NPT that had a high rate of leakage were reinforced or replaced at the bedside. |
The SWD was a dry gauze adhesive dressing applied under sterile conditions in the OR. The SWDs were removed on postoperative day 2. |
Length of follow-up: 30 day follow- up for primary outcome in medical records
Loss-to-follow- up: Not applicable; retrospective study design
Incomplete outcome data: Not applicable; retrospective study design |
30-day SSI (surgical site infections): 20.4% NPT versus 25.8% SWD; p=0.50 |
Remark: Only univariate analyses |
|
|
Source of funding: Not reported |
N total at baseline: Intervention: 49 Control: 70 |
|
|
|
|
|
|
|
|
Important prognostic factors2: Age ± SD: |
|
|
|
|
|
|
|
|
I: 55.4 ± 13.8 |
|
|
|
|
|
|
C: 56.3 ± 11.8 |
|||||||
|
Sex: |
|||||||
|
I: 48.6% M |
|||||||
|
C: 53.1% M |
|||||||
|
BMI: ± SD: |
|||||||
|
I: 34.8 ± 9.8 |
|||||||
|
C: 33.5 ± 8.8 |
|||||||
|
ASA classification: |
|||||||
|
I: 3.0 ± 0.5 |
|||||||
|
C: 2.8 ± 0.44 |
|||||||
|
The NPT group had a |
|||||||
|
significantly higher |
|||||||
|
mean ASA |
|||||||
|
Classification (p<0.01) |
|||||||
|
and significantly more |
|||||||
|
component |
|||||||
|
separations than did |
|||||||
|
the SWD group |
|||||||
|
(p<0.01) |
|||||||
|
Gassman, 2015 |
Type of study: Retrospective non- randomized study (review of medical records)
Setting: Two large university teaching hospitals
Country: USA |
Inclusion criteria: Patients who underwent complex abdominal wall reconstruction (AWR) requiring the use of biologic mesh >200 cm2
Exclusion criteria: -
N total at baseline: |
The PVC (primary vacuum closure) patients received the same, stapled, primary skin closure with topical NPT as an overlay adjunct. These patients had a KCI commercial vacuum- assisted closure (VAC) device applied in a linear strip along the length of their closed incision. Care was taken to protect the underlying skin with either a layer of Adaptic non-adhering dressing or perforated silastic |
Primary closure PC wounds were otherwise followed in the same fashion as in the PVC group. |
Length of follow-up: Intervention: 240 days Control: 334 days
Loss-to-follow- up: Not applicable; retrospective study design |
Surgical site infection (SSI): 5/29 (17%) PVC versus 17/32 (53%) PC; P=0.01
Hematoma: 0/29 (0%) PVC versus 2/32(6%) PC; P=0.49
Seroma: 3/29(10%) PVC versus 3/32 (9%) PC; P=1.00
Skin flap necrosis: |
Remarks: -Only univariate analysis |
|
|
Source of funding: Not reported |
Intervention: 29 Control: 32
Important prognostic factors2: Age: Mean age 54 (not reported per arm, and no SD) |
sheets. The black polyurethane foam was cut as the same width as the protective skin dressing. Once complete adhesion and seal were certain, the wounds then received 7 days of continuous 125 mmHg NPT with the VAC device. At 7 days, the NPT was removed. |
|
Incomplete outcome data: Not applicable; retrospective study design |
3/29(10%) PVC versus 2/32 (6%) PC; P=0.67 |
|
|
|
Sex: I: 27.6% M C: 46.9% M |
|
|
|
|||
|
|
Obesity (≥BMI 30: I: 72% C: 31% P=0.002 |
|
|
|
|||
|
|
The PVC closure group had a higher percentage of prior intra-abdominal infections and a higher portion of patients that had a BMI >30. |
|
|
|
|||
|
Condé- Green, 2013 |
Type of study: Retrospective non- randomized study (review of medical records)
Setting: Single institution, single surgeon at the University of |
Inclusion criteria: Primary closure of abdominal incision at the end of operation, postoperative wound management by NPWT or conventional dressings, age ≥21
Exclusion criteria: |
Immediately postoperatively the incisions were covered with non- adherent dressing. Polyurethane foam (black) was cut and placed along the entire length of the incision. Drape was placed over the foam and 3-5 cm of surrounding skin. Tubing and a TRAC-pad were placed on the inferior aspect of the dressing. |
Conventional dressings consisting of dry gauze |
Length of follow-up: Mean follow- up: 15 months (range: 4 months – 3 years) Intervention: not reported |
Overall wound complications I: 22% C: 63.6% Sign. difference (p=0.02) OR 6.3 (95%CI: 1.37 to 34.14)
Skin dehiscence I: 9% C: 39% Sign difference (p=0.014) |
Only univariate analyses |
|
|
Maryland Medical Center in Baltimore
Country: USA
Source of funding: No source reported, no conflicts of interest declared. |
None reported.
N total at baseline: Intervention: 23 Control: 33
Important prognostic factors2: All patients presented with large ventral hernias and underwent primary fascial closure.
Age (range): I: 54 (21-72) C: 55 (23-81)
Sex (M/F): Total:23/33 I: not reported C: not reported
BMI: ± SD: I: 36.4 C: 36.1
Prior abdominal surgery (mean): I: 2 C: 2.3
Groups were comparable at baseline for BMI and prior surgery, however the |
Adhesion and airtight seal were ensured before negative pressure was initiated. A negative pressure of -125mm Hg was applied continuously and the device was removed on the fifth day postoperatively. |
|
Control: not reported
Loss-to-follow- up: Not applicable; retrospective study design
Incomplete outcome data: Not applicable; retrospective study design |
OR 6.83 (95%CI: 1.37-34.14)
Skin and fat necrosis I: 9% C: 18% No sign. difference
Hernia recurrence I: 4% C: 9% No sign. difference
Seroma I: 0% C: 12% No sign. difference
Infection I: 4% C: 6% No sign. difference
hematoma I: 0% C: 0% No sign. difference |
|
|
|
|
distribution of sex among groups is unclear. |
|
|
|
|
|
Risk of bias table
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Soares, 2014 |
likely |
likely |
unlikely |
unlikely |
|
Pauli, 2013 |
likely |
unlikely |
unlikely |
likely |
|
Gassman, 2015 |
likely |
unclear |
unclear |
likely |
Beoordelingsdatum en geldigheid
Publicatiedatum : 07-11-2018
Beoordeeld op geldigheid : 23-11-2018
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep wel/niet in stand gehouden. Uiterlijk in 2023 bepaalt het bestuur van de Nederlandse Vereniging voor Heelkunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse vereniging Voor Heelkunde is regiehouder van deze richtlijn Littekenbreuken en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn Littekenbreuken. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Autorisatie en commentaarfase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (http://www.kennisinstituut.nl) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel van het project is het ontwikkelen van een multidisciplinaire evidencebased richtlijn voor de diagnostiek en behandeling van patiënten met complexe littekenbreuken. Met behulp van deze richtlijn kan de praktijkvariatie worden teruggedrongen en kan de zorg aan deze patiëntengroep worden verbeterd. Een evidencebased richtlijn zal bijdragen aan meer uniformiteit in de behandeling en zal waardevol zijn om toegewijde chirurgen en andere gerelateerde zorgverleners te ondersteunen bij een effectieve en veilige behandeling.
Doelgroep
Deze richtlijn geldt voor alle volwassen patiënten met één of meerdere littekenbreuken in de buikwand tussen de laterale zijde van de musculus abdominis recti.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2016 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met Littekenbreuken te maken hebben.
Werkgroep
- Dr. S.W. (Simon) Nienhuijs, chirurg, werkzaam in het Catharina ziekenhuis, Eindhoven, NVvH (voorzitter)
- Dr. T.J. (Theo) Aufenacker, chirurg, werkzaam in het Rijnstate, Arnhem, NVvH
- E. (Elske) Berkvens, MSc, fysiotherapeut, werkzaam in het Elkerliek ziekenhuis, Helmond, KNGF
- Prof. dr. M.A. (Marja) Boermeester, chirurg, werkzaam in het AMC, Amsterdam, NVvH
- S. (Sandra) Janssen MSc, verpleegkundig specialist, werkzaam in het Elkerliek ziekenhuis, Helmond, V&VN
- Dr. R.K.J. (Rogier) Simmermacher, chirurg, werkzaam in het UMC, Utrecht, NVvH
- Dr. T.S. (Tammo) de Vries Reilingh, chirurg, werkzaam in het Elkerliek ziekenhuis, Helmond, NVvH
- P. (Pieter) Zwanenburg MSc., arts onderzoeker, werkzaam in het AMC, Amsterdam
Met ondersteuning van:
- Dr. W.A. van Enst, senior-adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- H. Kooijmans, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- D.P. Gutierrez, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Aufenacker |
Chirurg |
Penningmeester DHS/ werkgroep buikwand chirurgie van NVGIC. Lid Steering committee Herniasurge: International guidelines for groin hernia management |
- |
Geen |
|
Berkvens |
Fysiotherapeut |
Extern beoordelaar scripties bij Fontys Hogeschool opleiding Fysiotherapie |
- |
Geen |
|
Boermeester |
GE Chirurg |
Advisory board member and/of speaker for Acelity/KCI, Bard, Johnson&Johnson Vice-president van |
Grants en pending grants voor investigator-initiated onderzoek (geen contract onderzoek) van Baxter, Ipsen, Bard, Acelity/KCI, Mylan, Johnson&Johnson, LifeCell/Allergan |
Geen |
|
|
|
Surgical Infection Society Europe |
|
|
|
Enst, van |
Senior-adviseur |
Lid van GRADE working group / Dutch GRADE Network |
- |
Geen |
|
Janssen |
Verpleegkundig Specialist wondzorg |
Docent opleiding wondverpleegkundige Zorgacademie Radboud UMC en Zorgacademie Erasmus MC Docent opleiding wondconsulent Zorgacademie Radboud UMC Bestuurslid V&VN Lid Wondplatform Nederland |
- |
Geen |
|
Nienhuijs |
Chirurg |
DHS/ voorzitter werkgroep buikwand chirurgie van NVGIC |
Deelname hernia umbilcalis/epigastrica studie zowel Medtronic als bij Johnson & Johnson. |
Geen |
|
Simmermacher |
Chirurg en Hoofd afdeling Heelkunde |
- |
- |
Geen |
|
Vries, de Reilingh |
Gastro- Intestinaal chirurg en Chirurg Oncoloog |
- |
Multicenter studies geinitieerd elders: Phasix trial, Sanics II trial, Close-up trial |
Geen |
|
Zwanenburg |
Promovendus / onderzoeker |
- |
Promotie traject gefinancierd vanuit een grant voor het AMC als "center of expertise" van Acelity/KCI |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een focusgroep. Een verslag hiervan (zie aanverwante producten) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Tijdens de oriënterende zoekactie werd gezocht op literatuur naar patiëntenperspectief (zie Strategie voor zoeken en selecteren van literatuur).
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft geen interne kwaliteitsindicatoren ontwikkeld maar doet suggesties wat geregisteerd kan worden.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidencebased richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door Nederlandse vereniging voor Heelkunde, Koninklijk Nederlands Genootschap Fysiotherapie, Verpleegkundigen & Verzorgende Nederland, Kenniscentrum Wondzorg, Kenniscentrum Wondzorg, Zorgverzekeraars Nederland via een Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen Nice en Sign richtlijnen, systematische reviews via Medline (OVID). Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE- methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE- methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Randvoorwaarden.
Indicatorontwikkeling
Er werden geen interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum. 2004.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) – juli 2016 |
6 2 and 3 (196) 7 2 and 4 (442) 8 2 and 5 (1450) 9 6 or 7 or 8 (1662)
= 1662 (1615 uniek) |
243 (na voorselectie) |
|
Embase (Elsevier) |
'incisional hernia'/exp OR 'incisional hernia':ab,ti OR 'ventral hernia':ab,ti OR 'complex hernia':ab,ti AND (english)/lim AND (2006-2016)/py AND (embase)/lim NOT 'conference abstract':it
Gebruikte filters: Systematische reviews: 'meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de
RCTs: 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti NOT 'conference abstract':it
Observationeel: 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR (cohort NEAR/1 (study OR studies)):ab,ti OR (case:ab,ti AND (control NEAR/1 (study OR studies)):ab,ti) OR (follow:ab,ti AND (up NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)):ab,ti OR (epidemiologic NEAR/1 (study OR studies)):ab,ti OR ('cross sectional' NEAR/1 (study OR studies)):ab,ti
= 1289 (1272 uniek) |
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Geen |
- |
