Behandeling bij kinderen met een liesbreuk
Uitgangsvraag
Hoe wordt een liesbreuk bij kinderen behandeld?
Deze uitgangsvraag omvat de volgende deelvragen:
- Hoe dient een liesbreuk behandeld te worden bij kinderen met een primaire liesbreuk? (open operatieve behandeling/ breukzakresectie inguinaal versus laparoscopische correctie)?
- Hoe dient een liesbreuk behandeld te worden bij kinderen met een recidief liesbreuk? (open operatieve behandeling/ breukzakresectie inguinaal versus laparoscopische correctie)
- Hoe dient een liesbreuk behandeld te worden bij kinderen met een unilaterale liesbreuk? (unilaterale operatieve correctie versus unilaterale operatieve correctie en tevens contralaterale exploratie)
- Hoe dient een liesbreuk behandeld te worden bij kinderen met een beklemde liesbreuk? (poging tot repositie en afwachtend secundair operatief behandelen versus acute exploratie)
- Hoe dient een liesbreuk behandeld te worden bij jongens met tevens niet-scrotale testis?
Aanbeveling
Behandel een kind met een primaire liesbreuk via een open benadering waarbij breukzakresectie wordt verricht.
Behandel kinderen met een recidief liesbreuk via een open of een laparoscopische benadering afhankelijk van de ervaring van de chirurg.
Exploreer bij kinderen ouder dan zes maanden met een unilaterale liesbreuk niet de contralaterale zijde. Bespreek met ouders van kinderen jonger dan zes maanden de voor- en nadelen van contralaterale exploratie om een Metachrone Contralaterale Inguinale Hernia (MCIH) te voorkomen.
Probeer een beklemde liesbreuk te reponeren. Indien de liesbreuk niet reponibel is, opereer dan met spoed (operatieve urgentie categorie 2 conform de richtlijn beleid rondom spoedoperaties, zie ook module Timing). Indien de liesbreuk wel reponibel is, opereer dan binnen 2 tot 7 dagen.
Verricht bij jongens met een liesbreuk en een ipsilaterale niet-scrotale testis tevens een orchidopexie, tegelijk met de breukzakresectie.
Overwegingen
Kwaliteit van het bewijs
De mate van (on)zekerheid over effecten en veiligheid is groot. Met lage bewijskracht werd geen verschil in complicaties gevonden bij de vergelijking tussen een open en laparoscopische benadering. Voor andere vragen werd geen vergelijkend onderzoek gevonden.
Professioneel perspectief
De behandeling van een liesbreuk bij kinderen bestaat uit een breukzakresectie. Liesbreukingrepen tussen de 16 en 18 jaar komen zeer weinig voor en er is geen onderzoek naar de ideale behandeling voor patiënten van deze leeftijd. De werkgroep pleit voor een behandeling zonder mat bij patiënten tot 18 jaar.
De werkgroep is van mening dat er geen plek is voor afwachtend beleid, omdat de kans op beklemming groot is. Dit komt doordat een kinderliesbreuk altijd een laterale breuk is, waarbij de breukpoort relatief klein is en ook niet meer vanzelf zal sluiten. De timing van operatie na presentatie van een kind met een liesbreuk is nooit goed bestudeerd; de werkgroepleden adviseren chirurgische correctie van een liesbreuk bij een kind op korte termijn na presentatie van de liesbreuk te verrichten. Hierbij geldt: hoe jonger het kind, des te sneller opereren in verband met het hogere risico op beklemming. In de module ‘Timing’ komt dit aan bod. Speciale aandacht vragen we voor de meisjes met een ovarium als inhoud van de breukzak: wegens de grote kans op ischemie van het ovarium dient operatieve correctie binnen twee weken te gebeuren.
De meeste kinderchirurgen en chirurgen bij kinderen verrichten een open breukzakresectie: het is de meest verrichte operatie door kinderchirurgen en chirurgen bij kinderen en er is veel ervaring mee. Er zijn steeds meer publicaties over laparoscopische technieken om een kinderliesbreuk te herstellen. Het is nog niet duidelijk of laparoscopisch herstel een voordeel oplevert. Het is ook nog niet duidelijk welke laparoscopische techniek het best toegepast kan worden en hoe de leercurve er uitziet voor laparoscopische herstel van een liesbreuk. Een voordeel van de open benadering via de lies is dat deze ook kan plaatsvinden onder regionale anesthesie, bijvoorbeeld spinaal anesthesie. Een voordeel van laparoscopisch liesbreukherstel bij kinderen met een unilaterale liesbreuk is de mogelijkheid om direct de contralaterale lies te evalueren en eventueel te behandelen. Bij kinderen met een recidief liesbreuk is laparoscopisch herstel de moeite waard, omdat in maagdelijk gebied geopereerd kan worden en de gehele inguinale en femorale regio overzichtelijk a vue komt.
De werkgroepleden adviseren open breukzakresectie bij een kind met een primaire liesbreuk. Echter, chirurgen met ervaring in laparoscopisch herstel van een liesbreuk bij kinderen kunnen laparoscopische correctie overwegen.
Tachtig procent van de kinderen presenteert zich met een unilaterale liesbreuk. 7 tot 15% van deze kinderen ontwikkelt een tweede liesbreuk aan de contralaterale kant, hetgeen we Metachrone Contralaterale Inguinale Hernia (MCIH) noemen. Contralaterale exploratie met eventueel sluiten van een open processus vaginalis kan MCIH met tweede narcose op korte termijn voorkomen. Contralaterale exploratie brengt echter ook het risico op complicaties met zich mee en is in veel kinderen onnodig. Recente systematische reviews (Nataraja, 2011; Wenk, 2015) laten zien dat routinematig contralaterale exploratie in alle kinderen met een unilaterale liesbreuk zinloos is, omdat 17 tot 18 patiënten contralateraal geëxploreerd moeten worden om één MCIH te voorkomen (NNT is dus 17 tot 18). Bij kinderen jonger dan zes maanden tijdens presentatie met een unilaterale liesbreuk moeten negen kinderen geëxploreerd worden om een MCIH te voorkomen (Nataraja, 2011). Bij deze patiënten kan met de ouders worden gesproken over het eventuele nut van contralaterale exploratie. Recente publicaties en de waarschuwing van de US Food and Drug Administration (FDA) over de mogelijk schadelijke effecten van herhaalde algehele anesthesie bij kinderen jonger dan drie jaar op neurocognitieve ontwikkeling moeten leiden tot voorzichtigheid met betrekking tot een tweede narcose bij kinderen op jonge leeftijd en discussie met ouders over contralaterale exploratie (Andropulos, 2017; Flick, 2011; Wang, 2014; DiMaggio, 2009; Wilder, 2009):
Beklemde liesbreuken dienen zo spoedig mogelijk gereponeerd te worden. Pijnstilling, ervaring en geduld zijn hierbij behulpzaam. Na een geslaagde repositie is het naar de mening van de werkgroep raadzaam om enkele dagen te wachten alvorens de breukzakcorrectie plaatsvindt, omdat de voorheen oedemateuze breukzak dan makkelijker behandeld kan worden. Als een beklemming langer dan zes uur bestaat, adviseert de werkgroep om het kind op te nemen ter observatie na succesvolle repositie en te beoordelen of er tekenen van darmnecrose optreden. Als een beklemde liesbreuk niet gereponeerd kan worden, dient met spoed chirurgische behandeling plaats te vinden (volgens categorie 2 van de classificatie van de NVVH: binnen enkele uren, maximaal 8 uur). Daarbij adviseert de werkgroep ook de darm, en bij meisjes het ovarium, te inspecteren via de breukzak ofwel laparoscopie. Een ischemisch ovarium kan in situ blijven (Dasgupta, 2018).
Als een kind zich presenteert met een liesbreuk en gelijktijdige niet-scrotale testis, dan is een orchidopexie in dezelfde sessie als de breukzakresectie aan te bevelen. Een tweede operatie in al geopereerd gebied kan daarmee voorkomen worden.
Kosten
Een laparoscopische benadering is duurder dan een open benadering. Daarbij kost het ook meer tijd. Het is uit de literatuur niet duidelijk wat het verschil is in effectiviteit, daardoor is de kosteneffectiviteit ook niet te bepalen van beide behandelmogelijkheden.
Wat vinden patiënten: patiëntenvoorkeur
Patiëntenvoorkeur is niet bekend bij de werkgroep.
Haalbaarheid
De behandeling van een liesbreuk bij kinderen is afhankelijk van de beschikbaarheid van de chirurg bij kinderen, kinderchirurg en kinder-anesthesist. In de richtlijn Anesthesie bij kinderen wordt beschreven welke kinderen in welk soort centrum behandeld dienen te worden en of de behandeling in dagopname of klinische opname kan plaatsvinden.
Onderbouwing
Het is onduidelijk wat bij verschillende patiëntgroepen de beste behandeling is van liesbreuk:
- Bij kinderen met een primaire liesbreuk of recidief is het onduidelijk of de laparoscopische operatietechniek even goed is als de, op dit moment meest gangbare, open operatietechniek.
- Bij kinderen met een unilaterale liesbreuk is het onduidelijk of de contralaterale exploratie de voorkeur verdient boven alleen de unilaterale correctie (op dit moment het meest gangbaar).
- Bij kinderen met een beklemde liesbreuk is het onduidelijk of acute exploratie de voorkeur verdient boven een poging tot repositie en vervolgens afwachtend en secundair operatief behandelen (op dit moment het meest gangbaar).
|
Laag GRADE |
Postoperatieve complicaties (hydrocele, scrotaal hematoom, roodheid van de wond, testis atrofie, ascensus testis, recidief hernia, pijn en ongemak) lijken gelijk bij de laparoscopische operatietechniek voor liesbreuk bij kinderen en de open operatietechniek.
Bronnen: (Feng, 2015; Gause, 2017) |
|
- GRADE |
We kunnen geen conclusies formuleren ten aanzien van de effecten van een open operatieve behandeling een versus laparoscopische correctie bij kinderen met een recidief liesbreuk
Bronnen: (Davies, 2017) |
|
- GRADE |
We kunnen geen conclusies formuleren ten aanzien van de effecten van een unilaterale operatieve correctie of een unilaterale operatieve correctie en tevens contralaterale exploratie.
Bronnen: (Davies, 2017; Wenk, 2015) |
|
- GRADE |
We kunnen geen conclusies formuleren ten aanzien van de effecten van een poging tot repositie en afwachtend secundair operatief behandelen versus acute exploratie bij kinderen met een beklemde liesbreuk. |
|
- GRADE |
We kunnen geen conclusies formuleren ten aanzien van de voor- en nadelen van liesbreukcorrectie met of zonder orchidopexie bij niet-scrotale testis. |
Deelvraag 1: Wat is de beste behandeling bij kinderen met een primaire liesbreuk?
Beschrijving studies
Feng (2015) includeerde vijf studies (Chan, 2005; Koivusalo; 2009, Celebi, 2014, Shalaby, 2012 en Saranga, 2008) met in totaal 553 patiënten (278 in de open operatie-groep en 275 in de laparoscopische operatie-groep). De duur van de follow-up varieerde van 3,5 maand (Saranga, 2008) tot 24 maanden (Koivusalo; 2009, Celebi, 2014, Shalaby, 2012).
In drie studies (Chan, 2005; Koivusalo, 2009, Celebi, 2014) gebruikte men een intraperitoneale benadering en in twee studies (Shalaby, 2012 en Saranga, 2008) een extraperitoneale benadering. Patiënt- en studiekarakteristieken zijn in onderstaande tabel (Tabel 1) weergegeven. Verschillen in de patiëntpopulatie, benaderingswijze en instrumentarium (trocars) liggen mogelijk ten grondslag aan verklaarbare, klinische heterogeniteit in de resultaten.
Tabel 1 Patiënt- en studiekarakteristieken van de studies
|
Studie |
n (laparoscopisch, open) |
Leeftijd |
Follow-up (maanden) |
|
Celebi, 2014 |
30, 32 |
>6 jaar |
3-24 |
|
Chan, 2005 |
41, 42 |
≥3 maanden |
11,8 |
|
Gause, 2017 |
26, 15 |
≤3 jaar |
3-12 |
|
Koivusalo, 2009 |
47, 42 |
4 maanden - 16 jaar |
3-24 |
|
Saranga, 2008 |
35, 34 |
<14 jaar |
3,5 |
|
Shalaby, 2012 |
125, 125 |
<24 maanden |
24 |
Feng (2015) koos ervoor om odds ratio’s (OR’s) te berekenen. Aangezien alle geïncludeerde studies RCT’s betrof, kozen wij ervoor om relatieve risico’s (RR’s) te berekenen en zo te voorkomen dat een OR onterecht als RR zou worden geïnterpreteerd. Verder koos Feng (2015) ervoor om een fixed-effects model te gebruiken voor hun meta-analyse op basis van de mate van statistische heterogeniteit. Wij kozen voor een random-effects model, gebaseerd op de klinische heterogeniteit tussen de studies (zie tabel 1). De aanname dat het effect van de operatietechnieken gelijk zou moeten zijn in alle studies leek ons niet gerechtvaardigd, vanwege verschillen in de laparoscopische operatietechnieken en grote diversiteit in de leeftijd van de patiënten tussen de studies.
Resultaten
Kritieke uitkomstmaat: postoperatieve complicaties
In alle zes studies werden postoperatieve complicaties gerapporteerd: hydrocele, scrotaal hematoom, roodheid van de wond, wondinfectie, testis atrofie, ascensus testis en recidief. Het totaalaantal postoperatieve complicaties was niet statistisch significant verschillend tussen beide groepen (RR: 0,66, 95% BI 0,28 tot 1,52) (Figuur 1).
Figuur 1 Meta-analyse voor de uitkomstmaat postoperatieve complicaties (totaal); laparoscopische operatietechniek versus open operatietechniek
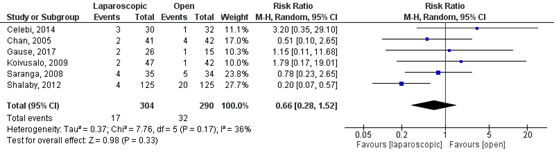
In twee studies (Saranga, 2008; Shalaby, 2012) rapporteerde men het optreden van ernstige complicaties bij jongens (scrotaal hematoom, testis atrofie, ascensus testis). In de (relatief grotere) studie van Shalaby (2012) traden ernstige complicaties op bij drie patiënten in de laparoscopisch geopereerde groep tegenover twaalf in de open geopereerde groep. In de kleinere studie van Saranga (2008) zag men in totaal drie patiënten met ernstige complicaties: één in de laparoscopisch geopereerde groep en twee in de groep die middels de open techniek was geopereerd (Figuur 2). De schatting van het gepoolde effect bedroeg RR 0,31 (95% BI: 0,10 tot 0,91). (NNT is 1269; gemiddeld zullen 1269 jongens laparoscopisch in plaats van open geopereerd moeten worden voor één extra mannelijke patiënt zonder ernstige complicaties).
Figuur 2 Meta-analyse voor de uitkomstmaat postoperatieve complicaties bij jongens; laparoscopische operatietechniek versus open operatietechniek
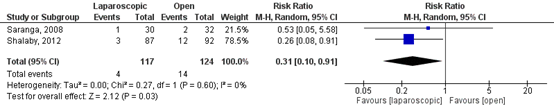
In drie studies (Gause, 2017, Koivusalo, 2009; Shalaby, 2012) rapporteerde men het optreden van recidieven. In totaal hadden vier patiënten in de laparoscopisch geopereerde groep een recidief liesbreuk tegenover eveneens vier patiënten in de open-operatiegroep (Figuur 3).
Figuur 3 Meta-analyse voor de uitkomstmaat recidief; laparoscopische operatietechniek versus open operatietechniek
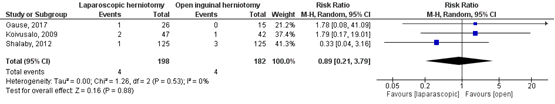
Pijn, ongemak (belangrijke uitkomstmaat)
Celebi (2014) randomiseerde 62 jongens die een bilaterale operatie ondergingen (32 middels de open techniek en 30 middels de laparoscopische techniek). De postoperatieve pijnscores (geëvalueerd door een visuele analoge schaal, VAS) bleken alleen hoger te zijn in de open geopereerde groep één uur na de operatie (p = 0,05), maar niet op enig tijdstip daarna tot en met 24 uur na de operatie.
Zowel Chan (2005) als Gause (2017) evalueerden postoperatieve pijn door het vergelijken van de totale aantal acetaminophen doses. Chan (2005) vergeleek 83 patiënten die ofwel de laparoscopische herniaoperatie ondergingen (n=41) of een open operatie (n=42). De patiënten die een open operatie ondergingen hadden meer doses nodig dan de patiënten die de laparoscopische operatie ondergingen (1,05 versus 0,84 doses per patiënt, p = 0,03). Gause (2017) vergeleek 15 patiënten die een open operatie ondergingen met 26 patiënten die een laparoscopische operatie ondergingen, maar vond geen statistisch significant verschil in het totale aantal doses (unilaterale open versus laparascopische liesbreukoperaties: 9 (SD 9,7) versus 5,3 (SD 2,9); bilaterale open versus laparascopische operaties 4,8 (SD 1,7) versus 9,6 (SD 7,3).
Bewijskracht van de literatuur
De bewijskracht is afkomstig uit RCT’s en startte derhalve op ‘Hoog’. De bewijskracht voor de uitkomstmaat postoperatieve complicaties (totaal) is met twee niveaus verlaagd tot ‘Laag’ vanwege ernstige (klinische) heterogeniteit en imprecisie (aantal events zeer laag en de studiepopulatie <2000). Alhoewel er sprake was van enige methodologische beperkingen in de studies (zoals het ontbreken van blindering van patiënten en/of artsen), is hiervoor niet afgewaardeerd omdat beïnvloeding van de resultaten door deze beperkingen hoogstwaarschijnlijk niet ernstig is.
De bewijskracht voor de uitkomstmaat pijn, ongemak is met drie niveaus verlaagd tot ‘Zeer laag’ gezien ernstige (klinische) heterogeniteit en zeer kleine populatiegroottes (imprecisie).
Deelvraag 2: Wat is de beste behandeling bij kinderen met een recidief liesbreuk?
Shalaby (2012) randomiseerde 150 kinderen: 27 daarvan hadden een recidief liesbreuk. Shalaby (2012) rapporteerde geen resultaten voor deze groep apart. Conclusies ten aanzien van de beste behandeling bij kinderen met een recidief liesbreuk kunnen derhalve niet worden getrokken.
Deelvraag 3: Wat is de beste behandeling bij kinderen met een unilaterale liesbreuk: alleen unilaterale operatieve correctie of een unilaterale operatieve correctie en tevens contralaterale exploratie?
Er zijn geen gerandomiseerde studies waarbij kinderen werden toegewezen aan een groep die alleen een unilaterale operatieve correctie onderging of aan een groep waarbij een unilaterale operatieve correctie en tevens contralaterale exploratie werd uitgevoerd (Davies, 2017). Op basis van de beschikbare gegevens uit verschillende typen onderzoek, schat Davies (2017) dat 20 tot 30% van de patiënten met een unilaterale liesbreuk ook een zichtbare contralaterale patent processus vaginalis (PPV) heeft. Het lijkt erop dat een kwart hiervan zich uiteindelijk ontwikkelt tot een metachrone liesbreuk.
Wenk (2015) onderzocht systematisch de incidentie van een contralaterale liesbreuk bij kinderen met een eenzijdige liesbreuk om op basis daarvan een uitspraak te kunnen doen over routinematige exploratie van het contralaterale lieskanaal. Wenk (2015) voerde een systematische zoekactie in medisch-wetenschappelijke databases uit tot augustus 2014 en selecteerde alleen prospectieve studies. Andere inclusiecriteria waren: minimale follow-up van één jaar, studiepopulatie van 0 tot 19 jaar, en zonder contralaterale exploratie of laparoscopische correctie.
Wenk (2015) includeerde zes studies met in totaal 1669 kinderen (1405 (84%) jongens en 264 (16%) meisjes). In totaal 945 (57%) kinderen hadden een rechtszijdige liesbreuk en 545 (33%) hadden een liesbreuk aan de linkerzijde. Van 179 (11%) was niet gerapporteerd aan welke zijde de liesbreuk was. Wenk (2015) vond voor metachrone liesbreuken een gepoolde overall incidentie van 6% (95%BI 4% tot 8%). De NNT was 17, wat betekent dat er 17 contralaterale exploraties nodig zijn om één metachrone liesbreuk te voorkomen. Bij meisjes was de incidentie hoger dan bij jongens (8% versus 4%, respectievelijk; odds ratio (OR) 1,8 (95%BI 0,99 tot 3,30).
Drie studies gevonden door Wenk (2015) rapporteerde aparte incidentiecijfers voor verschillende leeftijdsgroepen. De OR voor kinderen jonger dan een jaar ten opzichte van oudere kinderen was 1,87 (95%BI 0,97 tot 3,62). De incidentie in de leeftijdsgroep tot een jaar bedroeg 7% (95% BI 4% tot 11%) versus 4,5% (95%BI 3% tot 6%) in de leeftijdsgroep ouder dan een jaar.
Deelvraag 4: Wat is de beste behandeling bij kinderen met een beklemde liesbreuk?
Er zijn geen gerandomiseerde studies gevonden waar alleen kinderen met een beklemde liesbreuk werden geïncludeerd of publicaties van RCT’s waarin resultaten apart voor deze groep werden gerapporteerd.
Deelvraag 5: Wat zijn de voor- en nadelen van liesbreukcorrectie met of zonder orchidopexie bij niet-scrotale testis?
Radmayr (1999) rapporteerde de resultaten van kinderen (gemiddelde leeftijd 2,7 jaar) die exploratie en herstel van cryptorchisme, liesbreuk en/of hydrocele ondergingen. Van de 61 jongens ondergingen er 6 tegelijkertijd orchidopexie en een laparoscopische liesbreukcorrectie. Dertien jongens ondergingen tijdens één ingreep orchidopexie en correctie van een open processus vaginalis. In geen van de patiënten was er sprake van perioperatieve complicaties of recidief (na een follow-up van zes jaar).
Riquelme (2007) rapporteerde over 31 patiënten met cryptorchisme: 23 van hen hadden ook een liesbreuk en deze werden laparoscopisch hersteld. Deze 23 patiënten werden gemiddeld gedurende bijna 22 maanden gevolgd. In deze periode was er geen recidief. Wel trad er bij één patiënten vaatletsel op dat resulteerde in testiculaire atrofie.
In de studies werd een operatieduur voor de liesbreukcorrectie met orchidopexie variërend van gemiddeld 50 minuten (Riquelme, 2007) tot 60 minuten (Radmayr, 1999) gerapporteerd.
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht naar de volgende zoekvragen:
- Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een primaire liesbreuk?
- Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een recidief liesbreuk?
- Wat zijn de voor- en nadelen van een unilaterale operatieve correctie versus unilaterale operatieve correctie en tevens contralaterale exploratie?
- Wat zijn de voor- en nadelen van een poging tot repositie en afwachtend secundair operatief behandelen versus acute exploratie bij kinderen met een beklemde liesbreuk?
- Wat zijn de voor- en nadelen van liesbreukcorrectie met of zonder orchidopexie bij niet-scrotale testis?
Relevante uitkomstmaten
De werkgroep achtte postoperatieve complicaties (zoals ileus, scrotaal hematoom, recidief/ residu liesbreuk) en late complicaties (zoals testis atrofie, ascensus testis, contralaterale metachrone hernia, ischemisch ovarium, darmischemie, recidief liesbreuk) voor de besluitvorming kritieke uitkomstmaten; en pijn/ ongemak een voor de besluitvorming belangrijke uitkomstmaat.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
De informatiespecialist van Cochrane Nederland doorzocht Medline en Embase (op 11 april 2017) en het Cochrane Register (op 12 april 2017) naar artikelen over de diagnostiek of behandeling van kinderen met liesbreuk zonder beperkingen op de publicatiedatum. De zoekgegevens worden weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 1381 treffers op. Literatuurexperts excludeerden de studies die duidelijk niet relevant waren voor het beantwoorden van vragen over liesbreuken bij kinderen. In totaal bleven er 963 publicaties over die door de werkgroep werden beoordeeld. Studies werden door hen geselecteerd op grond van de volgende selectiecriteria: de studie betreft kinderen jonger dan 18 jaar, het betreft behandeling van liesbreuk(en), de uitkomstmaten betreffen postoperatieve complicaties, late complicaties of pijn, het onderzoeksdesign is prospectief en vergelijkend.
De werkgroepleden selecteerden op basis van titel en abstract 290 studies die mogelijk voldeden aan één van de PICO’s. Na raadpleging van de volledige tekst, werden vervolgens 287 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording). Drie studie werd definitief geselecteerd.
Drie studies zijn opgenomen in de literatuuranalyse (Davies, 2017; Feng, 2015; Shalaby, 2012). De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
Studies voor deelvraag 1 werden geselecteerd op grond van de volgende selectiecriteria:
- de studiepopulatie bestaat uit kinderen jonger dan 18 jaar met een primaire liesbreuk;
- betreft richtlijn, systematische review of primair (origineel) onderzoek;
- er is sprake van een vergelijking tussen de laparoscopische operatietechniek en de open operatietechniek;
- uitkomstmaten komen overeen met gekozen uitkomstmaten.
In eerste instantie werd één systematische review voorgeselecteerd (Feng, 2015, op basis van Davies, 2017) die in totaal vijf RCT’s includeerde. Er werd één recentere RCT (Gause, 2017) aan toegevoegd. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabel.
Studies voor deelvraag 2 werden geselecteerd op grond van de volgende selectiecriteria:
- de studiepopulatie bestaat uit kinderen jonger dan 18 jaar met een recidief liesbreuk;
- betreft richtlijn, systematische review of primair (origineel) onderzoek;
- er is sprake van een vergelijking tussen de laparoscopische operatietechniek en de open operatietechniek;
- Uitkomstmaten komen overeen met gekozen uitkomstmaten.
In eerste instantie werd één systematische review voorgeselecteerd (Feng, 2015, op basis van Davies, 2017) die één relevante RCT includeerde. Op basis van titel en abstract werden daarnaast twee recentere studies geselecteerd. Na raadpleging van de volledige tekst, werden deze studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording).
Één onderzoek is opgenomen in de literatuuranalyse (Shalaby, 2012). De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
Studies voor deelvraag 3 werden geselecteerd op grond van de volgende selectiecriteria:
- de studiepopulatie bestaat uit kinderen jonger dan 18 jaar met een unilaterale liesbreuk;
- betreft richtlijn, systematische review of primair (origineel) onderzoek;
- er is sprake van een vergelijking tussen unilaterale operatieve correctie versus unilaterale operatieve correctie en tevens contralaterale exploratie;
- uitkomstmaten komen overeen met gekozen uitkomstmaten.
In eerste instantie werden twee SR’s voorgeselecteerd (Wenk, 2015; Kokorowski, 2014), maar deze voldeden beide niet aan de PICO en werden geëxcludeerd. De SR met de meest recente zoekdatum (Wenk, 2015) is alsnog opgenomen in de literatuursamenvatting. Er werden geen evidence-tabellen opgesteld en de studies werden niet beoordeeld aan de hand van GRADE. De studie werd beschreven onder het kopje Samenvatting literatuur.
Studies voor deelvraag 4 werden geselecteerd op grond van de volgende selectiecriteria:
- de studiepopulatie bestaat uit kinderen jonger dan 18 jaar met een beklemde liesbreuk;
- betreft richtlijn, systematische review of primair (origineel) onderzoek;
- er is sprake van een vergelijking tussen een poging tot repositie en afwachtend secondair operatief behandelen versus acute exploratie;
- uitkomstmaten komen overeen met gekozen uitkomstmaten.
Op basis van titel en abstract werden in eerste instantie 28 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens alle studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en geen studies definitief geselecteerd.
Studies voor deelvraag 5 werden geselecteerd op grond van de volgende selectiecriteria:
- de studiepopulatie bestaat uit kinderen jonger dan 18 jaar met een liesbreuk en niet-scrotale testi;
- betreft richtlijn, systematische review of primair (origineel) onderzoek;
- er is sprake van een vergelijking tussen liesbreukcorrectie met of zonder orchidopexie;
- uitkomstmaten komen overeen met gekozen uitkomstmaten.
Op basis van titel en abstract werden in eerste instantie twee studies voorgeselecteerd (Riquelme, 2007; Radmayr, 1999). Na raadpleging van de volledige tekst, werden vervolgens deze twee studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en geen studies definitief geselecteerd.
De twee onderzoeken zijn alsnog opgenomen in de literatuursamenvatting. Er werden geen evidence-tabellen opgesteld en de studies werden niet beoordeeld aan de hand van GRADE. De twee studies worden beschreven onder het kopje Samenvatting literatuur.
Data-extractie en -analyse
We extraheerden de belangrijkste studiekarakteristieken en resultaten uit de systematische reviews of raadpleegden de originele studies (bijvoorbeeld bij ontbrekende informatie in de review of het ontbreken van de studie in de review). We verwerkten de informatie in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
Indien mogelijk en zinvol berekenden we relevante gepoolde en eventueel gestandaardiseerde effectmaten met Review Manager 5.3 (Cochrane Collaboration, Oxford, United Kingdom). Wanneer samenvatten niet mogelijk bleek, beschreven we de uitkomsten en resultaten van de statistische toetsing gerapporteerd door de auteurs van de betreffende publicatie.
De werkgroep definieerde voor geen van de uitkomstmaten klinische (patiënt) relevante verschillen. We hanteerden daarom, indien van toepassing, de onderstaande grenzen voor klinische relevantie voor continue uitkomstmaten en vergeleken de resultaten met deze grenzen: Risk ratio (RR) <0,75 of >1,25) (GRADE recommendation) of Standardized mean difference (SMD=0,2 (klein); SMD=0,5 (matig); SMD=0,8 (groot). De interpretatie van dichotome uitkomstmaten is sterk context gebonden en hiervoor werden a priori geen grenzen voor klinische relevante benoemd. Voor dichotome uitkomstmaten werd het absolute effect berekend (Number Needed to Treat; NNT).
- Andropoulos DB & Green MF. Anesthesia and developing brains Implications of the FDA warning. N Eng J Med 2017;376:905-907.
- Celebi S, Uysal AI, Inal FY, et al. A single-blinded, randomized comparison of laparoscopic versus open bilateral hernia repair in boys. J Laparoendosc Adv Surg Techn. 2014;24:117121.
- Chan KL, Hui WC, Tam PKH. Prospective, randomized, singlecentre, single blind comparison of laparoscopic versus open repair of pediatric inguinal hernia. Surg Endosc. 2005;19:927932.
- Dasgupta R, Renaud E, Goldin AB, et al. Ovarian torsion in pediatric and adolescent patients: A systematic review. J Pediatr Surg. 2018;53(7):1387-1391.
- DiMaggio C, Sun LS, Kakavouli A, et al. A retrospective cohort study of the association of anesthesia and hernia repiar surgery with behavioural and developmental disorders in young children. J Neurosurg Anesthesiol. 2009;21:286-91.
- Feng S, Zhao L, Liao Z, et al. Open versus laparoscopic inguinal herniotomy in children: A systematic review and meta-analysis focusing on postoperative complications. Surg Laparosc Endosc Percutan Tech. 2015;25: 275280.
- Flick RP et al. Cognitive and behavioural outcomes after early exposure to anesthesia and surgery. Pediatrics 2011;128:e1053-61.
- Koivusalo AI, Korpela R, Wirtavuori K, et al. A single-blinded, randomized comparison of laparoscopic versus open hernia repair in children. Pediatrics. 2009;123:332337.
- Nataraja RM, Mahomed AA. Systematic review for paediatric metachronous contralateral inguinal hernia: a decreasing concern. Pediatr Surg Int. 2011;27(9):953-61. doi: 10.1007/s00383-011-2919-z. Epub 2011 May 21.
- Radmayr C, Corvin S, Studen M, et al. Cryptorchidism, open processus vaginalis, and associated hernia: laparoscopic approach to the internal inguinal ring. Eur Urol. 1999;36(6):631-4.
- Riquelme M, Aranda A, Rodriguez C, et al. Incidence and management of the inguinal hernia during laparoscopic orchiopexy in palpable cryptoorchidism: preliminary report. Pediatr Surg Int. 2007;23(4):301-4. Epub 2007 Feb 8.
- Saranga Bharathi R, Arora M, Baskaran V. Pediatric inguinal hernia: laparoscopic versus open surgery. JSLS. 2008;2:277281.
- Shalaby R, Ibrahem R, Shahin M, et al. Laparoscopic hernia repair versus open herniotomy in children: a controlled randomized study. Minim Invas Surg. 2012;id:484135.
- Wang X, Xu Z, Miao CH. Current clinical evidence on the effect of general anesthesia on neurodevelopment in children: an updated systematic review with mega-regression. PLoS One 2014;9:e85760.
- Wenk K, Sick B, Sasse T, et al. Incidence of metachronous contralateral inguinal hernias in children following unilateral repair - A meta-analysis of prospective studies. J Pediatr Surg. 2015;50(12):2147-54. doi: 10.1016/j.jpedsurg.2015.08.056. Epub 2015 Sep 10.
- Wilder RT et al. Early exposure to anestheia and larning disabilities in a population-based birth cohort. Anesthesiology 2009;110:796-804.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een primaire liesbreuk?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison/ control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Davies, 2017
(individual study characteristics deduced from Feng, 2015)
|
SR and meta-analysis of RCTs
Dec 31 2015
Study design: RCT
Setting and Country: Hospital, Canada
Source of funding: The International Pediatric Endosurgery Group (IPEG) Evidence-Based Review Committee. |
Inclusion criteria SR: evidence examining minimally invasive approaches to inguinal hernia repair (IHR)
Exclusion criteria SR: not reported
5 RCTs included
Important patient characteristics at baseline:
N, mean age N total: 553 I: 278 C: 275
Children younger than 18 years |
Describe intervention:
Laparoscopic herniorrhaphy.
Intraperitoneal approaches in 3 studies, extraperitoneal approaches in 2 studies |
Describe control:
Open herniorrhaphy |
End-point of follow-up:
3-24 months
For how many participants were no complete outcome data available? (intervention/control)
not reported
|
Outcome measure-1 Discomfort, pain Not reported
Outcome measure-2 Total complications Pooled effect, odds ratio, fixed effects model: OR: 0.45 (0.24-0.86) favoring laparoscopic herniotomy Heterogeneity (I2): 47%
Pooled effect, risk ratio, random effects model. RR: 0.64 (0.25-1.65) Heterogeneity (I2): 45%
The common postoperative complications of patients who underwent LH or OH included hydrocele, scrotal edema, erythema, testicular atrophy, iatrogenic ascent of the testis, recurrence
Outcome measure-3 Major postoperative complications for male patients (scrotal edema, iatrogenic ascent of the testis, and testicular atrophy) Pooled effect, odds ratio, fixed effects model: OR: 0.28 (0.09-0.87) favoring laparoscopic herniotomy Heterogeneity (I2): 0%
Pooled effect, risk ratio, random effects model. RR: 0.31 (0.10-0.91) Heterogeneity (I2): 0%
Recurrence rate Pooled effect, odds ratio, fixed effects model: OR: 0.71 (0.15-3.24) favoring laparoscopic herniotomy Heterogeneity (I2): 2%
Pooled effect, risk ratio, random effects model. RR: 0.74 (0.14-3.84) Heterogeneity (I2): 2%
Other outcomes: Operative time I: N=119 C: N=123 Mean difference: -1.79 (-9.08 to 5.50) I2 = 94% |
Facultative:
Brief description of author’s conclusion
Personal remarks on study quality, conclusions, and other issues (potentially) relevant to the research question
Level of evidence: GRADE (per comparison and outcome measure) including reasons for down/upgrading
Sensitivity analyses (excluding small studies; excluding studies with short follow-up; excluding low quality studies; relevant subgroup-analyses); mention only analyses which are of potential importance to the research question
Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroupanalysis) |
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
Research question: Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een primaire liesbreuk?
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Gause, 2017 |
Type of study: RCT
Setting: Clinical
Country: USA
Source of funding: Not reported |
Inclusion criteria: <3 years of age at the time of scheduled surgery; - reducible unilateral or bilateral inguinal hernias
Exclusion criteria: - Need for a concomitant intraabdominal procedure; - history of prior inguinal hernia repair - liver disease or contraindication to acetaminophen, midazolam, fentanyl or bupivacaine use - expected prolonged hospitalization due to active concurrent illness.
N total at baseline: 41 Intervention: n=26 (n = 23 unilateral; n = 3 bilateral) Control: n=15 (n = 14 unilateral, n = 1 bilateral)
Important prognostic factors2: Age (days) ± SD: I: unilateral: 376 (225) bilateral: 289 (336) C: unilateral: 200 (140) bilateral: 93 (67) Sex: I: unilateral: n=13 M; n=4 F bilateral: n=6 M; n=3 F C: unilateral: n=9 M; n=1F bilateral: n=3 M; n=2 F
Age among groups not comparable at baseline. (Patients in control group younger) |
Describe intervention (treatment/procedure/test):
Open herniorrhaphy (OH)
|
Describe control (treatment/procedure/test):
Laparoscopic herniorrhaphy (LH) LH was performed via subcutaneous endoscopically assisted ligation of the internal ring (SEAL technique)
|
Length of follow-up: Minimum of 3 and 12 months
Loss-to-follow-up: Intervention: 0
Control: 0
Incomplete outcome data: Complete pain medication datasets for 31/41 patients (75.6%) Intervention: N (%) Reasons (describe)
Control: N (%) Reasons (describe)
|
Outcome measures and effect size (include 95%CI and p-value if available):
Postoperative complications: Unilateral OH: 0% LH: 5.88% (p>0.99) Bilateral OH: 20% LH: 11.11% (p>0.99)
Pain Doses acetaminophen, mean SD) Unilateral OH: 9 (9.68) LH: 5.3 (2.93) (p=0.23) Bilateral OH: 4.75 (1.71) LH: 9.63 (7.3) (P=0.23)
|
|
Research question: Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een recidief liesbreuk?
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Shalaby, 2012 |
Type of study: RCT
Setting: Pediatric Surgery Unit
Country: Egypt
Source of funding: Not reported |
Inclusion criteria: bilateral inguinal hernia, recurrent hernia, hernia in obese child, inguinal hernia with umbilical hernia and hernia on ipsilateral with questionable contralateral side.
Exclusion criteria: unilateral inguinal hernia in nonobese child and hernia with undescended testicles.
N total at baseline: 250 Intervention: n=125 Recurrent inguinal hernia: n=12 (9.6%)
Control: n=125 Recurrent inguinal hernia: n=15 (12%)
Important prognostic factors2: Age (months) ± SD: 61.6 ± 28.3 (range 5-96)
Sex: I: 179 (72%) C: 79 (28%) |
Describe intervention (treatment/procedure/test):
Laparoscopic assisted inguinal hernia repair
|
Describe control (treatment/procedure/test):
Open herniotomy (OH) |
Length of follow-up: 7 days, 2 weeks, 6 months, 1 year, and 2 years.
Loss-to-follow-up: Intervention: not reported
Control: not reported
Incomplete outcome data: Intervention: not reported N (%) Reasons (describe)
Control: not reported N (%) Reasons (describe)
|
Outcome measures and effect size (include 95%CI and p-value if available):
Postoperative complications: Postoperative hydrocele: I: n=3 C: n=5
Late complicaties Iatrogenic ascent of the testis: I: 0 C: 4.35% (n=4)
Recurrence 24 months: I: 0.8% (1/125) C: 2.4% (3/125
Significant diminution of testicular perfusion and size, indicating atrophy. I: 0 C: 3.3% (n=3)
|
NO SEPARATE DATA REPORTED FOR PATIENTS WITH RECURRENT INGUINAL HERNIA
|
Table of quality assessment for systematic reviews of RCTs and observational studies
Research question: Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een primaire liesbreuk?
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Feng, 2015 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
No |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Risk of bias table for intervention studies (randomized controlled trials)
Research question: Wat zijn de voor- en nadelen van een open operatieve behandeling/breukzakresectie inguinaal versus laparoscopische correctie bij kinderen met een primaire liesbreuk?
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Gause, 2017 |
Unlikely
A block stratified randomization (BSR) computer program was used to randomize patients to obtain balanced comparison groups of similar size. The computer program created block stratified assignments with a user selected block size. The pseudorandom number generator is a linear congruential algorithm of Park and Miller with Bays-Durham shuffling and has a period of over 2 billion. The total number of open and laparoscopic repair assignments was equally distributed in both unilateral and bilateral groups prior to randomization. |
Unlikely
After anesthesia induction the patient’s assigned envelope was opened, |
Unlikely
Families and staff caring for patients were not informed of which procedure was performed. Operative wound dressings were applied at both open and laparoscopic sites regardless of procedure performed and remained in place throughout the hospital stay to ensure integrity of the blinding process. |
Unlikely
Staff caring for patients were not informed of which procedure was performed. |
Unclear |
Unlikely |
Unlikely |
Unclear
|
Beoordelingsdatum en geldigheid
Publicatiedatum : 19-03-2019
Beoordeeld op geldigheid : 05-03-2019
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep in stand gehouden. Uiterlijk in 2024 bepaalt het bestuur van de NVvH of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVvH is regiehouder van deze richtlijn(modules) en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn(modules). De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Behandeling liesbreuk kind |
NVvH |
2019 |
2024 |
eens per 5 jaar |
NVvH |
- |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). Patiëntenparticipatie bij deze richtlijn werd medegefinancierd uit de Stichting Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ.
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het hoofddoel van de richtlijn is de patiëntresultaten te verbeteren en de perioperatieve zorg rondom liesbreukoperaties van kinderen te optimaliseren.
Doelgroep
De richtlijn wordt geschreven voor de medisch specialisten die betrokken zijn bij de zorg voor patiënten met liesbreuk.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2017 een werkgroep ingesteld, bestaande uit vertegenwoordigers van de Nederlandse Vereniging voor Heelkunde. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. J.H. Allema, kinder- & traumachirurg, Haga Ziekenhuis, locatie Juliana Kinderziekenhuis te Den Haag, NVvH, voorzitter
- Dr. J.P.M. Derikx, kinderchirurg, Emma Kinderziekenhuis AMC en VUmc te Amsterdam, NVvH
- Dr. H.R. Langeveld, kinderchirurg, Erasmus MC-Sophia te Rotterdam, NVvH
Met ondersteuning van:
- Dr. W.A. van Enst, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J.S. Boschman, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- D.P. Gutierrez, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Allema |
kinder- & traumachirurg |
- |
geen (14/06/2017, update 4/6/2018) |
niet van toepassing. |
|
Derikx |
kinderchirurg |
- |
geen (28/05/2017)_ Update 4/6/2018: Principal investigator van intern gefinancierd onderzoek (HERNIIA-trial) en extern gefinancierd onderzoek (LIKE-trial, subsidie Innovatiefonds Zorgverzekeraars) |
geen |
|
Langeveld-Benders |
kinderchirurg |
- |
Deelname extern gefinancierd onderzoek (HIP-trial, externe financiering vanuit V.S. (20/06/2017, update 4/6/2018) |
geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door inbreng van: 1) patiëntenvereniging Stichting Kind en Ziekenhuis (mevrouw Eva Schmidt – Cnossen MSc) tijdens de invitational conference en 2) een aantal ouders/verzorgers van een kind met liesbreuk via een door Stichting Kind en Ziekenhuis uitgezette enquête. Tijdens de invitational conference kwam naar voren dat het kiezen voor wel of niet opereren een erg belangrijk keuzemoment is en dat de verschillende opties moeten worden uitgelegd. Verder werd genoemd dat individualisering ook relevant is bij kinderen.
De reacties naar aanleiding van deze invitational (zie het volledige verslag van de invitational conference Liesbreuk bij de aanverwante producten) en enquête (zie aanverwante producten) zijn besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Kind en Ziekenhuis.
De werkgroep streeft ernaar om in een later stadium geschikte informatie voor ouders/verzorgers van kinderen met een liesbreuk en kinderen zelf te ontwikkelen. Op dit moment bestaat er weinig peroperatief voorbereidingsmateriaal voor kinderen. Ten tijde van het richtlijnontwikkelingstraject (2018) wordt (met steun van Stichting Kind en Ziekenhuis) onderzoek gedaan naar de meeste geschikte informatiemodaliteit voor kinderen (film, cartoon, app, website, et cetera). De waarde van dergelijk informatiemateriaal is naar verwachting medio 2019 bekend.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Patiëntenvereniging Stichting Kind en Ziekenhuis bevestigden deze knelpunten via de Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal, belangrijk (maar niet cruciaal) en onbelangrijk. Tevens poogde de werkgroep tenminste voor de cruciale uitkomstmaten te definiëren welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
De informatiespecialist van Cochrane Nederland doorzocht Medline en Embase (op 11 april 2017) en het Cochrane Register (op 12 april 2017) naar artikelen over de diagnostiek of behandeling van kinderen met liesbreuk zonder beperkingen op de publicatiedatum. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria en in instantie de studies met de hoogste bewijskracht. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Indicatorontwikkeling
Er werden geen interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://www.demedischspecialist.nl/onderwerp/raad-kwaliteit. 2012.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html. 2013.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Zoekverantwoording
De zoekstrategie is intellectueel eigendom van Cochrane Netherlands en is beschikbaar voor inzage op aanvraag bij het Kennisinstituut van de Federatie Medisch Specialisten.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Burcharth, 2016 |
Retrospectieve database studie |
|
Hamid, 2017 |
Controle komt niet overeen met PICO |
|
Galvan, 2017 |
Geen vergelijkend onderzoek |
|
Ahmen, 2016 |
Geen vergelijkend onderzoek |
|
Eginel, 2016 |
Geen vergelijkend onderzoek |
|
Baradaran, 2016 |
Geen vergelijkend onderzoek |
|
Pogorelic, 2017 |
Geen vergelijkend onderzoek |
|
Raveenthiran, 2017 |
Scoping review |
|
Obata, 2016 |
Beantwoord niet de zoekvraag |
|
Zhu, 2017 |
Retrospectieve cohort studie |
|
Emura, 2016 |
Beantwoord niet de zoekvraag |
|
Chen, 2017 |
Beantwoord niet de zoekvraag |
|
Esposito, 2016 |
Scoping review |
|
Lee, 2017 |
Beantwoord niet de zoekvraag |
|
Esposito, 2017 |
Geen vergelijkend onderzoek |
|
Le Roux, 2016 |
Geen vergelijkend onderzoek |
|
Esposito, 2016 |
Geen vergelijkend onderzoek |
|
Ordorica-Flores, 2016 |
Beantwoord niet de zoekvraag |
|
Saha, 2016 |
Beantwoord niet de zoekvraag |
|
Yan, 2016 |
Beantwoord niet de zoekvraag |
|
Miyake, 2016 |
Retrospectieve studie |
|
Thomas, 2016 |
Beantwoord niet de zoekvraag |
|
Burcharth, 2016 |
Beantwoord niet de zoekvraag |
|
Le Roux, 2016 |
Geen vergelijkend onderzoek |
|
Kokorowski, 2014 |
Recentere review beschikbaar |
|
Lee, 2016 |
Retrospectieve studie |
|
Baradaran, 2017 |
Beantwoord niet de zoekvraag |
|
Zaidi, 2017 |
Controle komt niet overeen met PICO |
|
Chan, 2011 |
Geen vergelijkend onderzoek |
|
Li, 2013 |
Geen vergelijkend onderzoek |
|
Blackburn, 2012 |
Geen vergelijkend onderzoek |
|
Ikeda, 1993 |
Beantwoord niet de zoekvraag |
|
Gahukamble, 1996 |
Geen vergelijkend onderzoek, wel relevant |
|
Esposito, 2013 |
Retrospectief |
|
Ameh, 1999 |
Retrospectief |
|
Grosfeld,1991 |
Geen vergelijkend onderzoek |
|
Balquet, 1990 |
Franstalig |
|
Koivusalo, 2007 |
Retrospectief |
|
Shalaby, 2007 |
Geen vergelijkend onderzoek |
|
Youngson, 1991 |
Reactie op Davies, 1990 |
|
Lin, 2002 |
Geen vergelijkend onderzoek |
|
Stylianos, 1993 |
Geen vergelijkend onderzoek |
|
Murase, 2016 |
Beantwoord niet de zoekvraag |
|
Ram, 2011 |
Beantwoord niet de zoekvraag |
|
Onuora, 1993 |
Beantwoord niet de zoekvraag |
|
Pillay, 2015 |
Beantwoord niet de zoekvraag |
|
Houben, 2015 |
Beantwoord niet de zoekvraag |
|
Davies, 1990 |
Geen vergelijkend onderzoek |
|
Fraser, 1993 |
Geen vergelijkend onderzoek |
|
Kaya, 2006 |
Geen vergelijkend onderzoek |
|
Kamaledeen, 1997 |
Geen vergelijkend onderzoek |
|
Lau, 2007 |
Geen vergelijkend onderzoek |
|
Akkersdijk, 2011 |
Reactie op Ram, 2011 |
|
Jones, 1994 |
Fulltext niet beschikbaar |
|
Yin, 2016 |
Beantwoord niet de zoekvraag |
|
Thapa, 2012 |
Geen vergelijkend onderzoek, wel relevant |
|
Riquelme, 2007 |
Geen vergelijkend onderzoek |
|
Radmayr, 1999 |
Geen vergelijkend onderzoek |

