Effect van zwangerschap op bloedingsneiging
Uitgangsvraag
Wat is het effect van zwangerschap op de uitslag van bloedstollingstesten?
Aanbeveling
Zwangerschap heeft duidelijke effecten op de meeste stollingsparameters (pro-coagulante status). Zowel de aanvragend arts als de laboratoriumspecialist klinische chemie dient zich bewust te zijn van deze verandering. Met name bij analyse (congenitale of onbegrepen) bloedingsneiging kan zwangerschap, afwijkingen in de hemostase maskeren. Deze bevinding kan gebruikt worden om laboratoriumonderzoek naar bloedingsneiging bij patiënten met hoge verdenking uit te voeren, bij voorkeur >2 maanden na de bevalling.
Overwegingen
De referentie intervallen zoals beschreven in het artikel van Szecsi et al. (2010) kunnen als leidraad dienen wanneer men stollingstesten aanvraagt gedurende de zwangerschap. Daarnaast moet men er ook op bedacht zijn dat de effecten van de zwangerschap kunnen aanhouden tot 2 maanden na de bevalling. Bij de behandeling van (massale) bloedingen rondom de partus (fluxus) kan overwogen worden om andere streefwaarden (bv. fibrinogeen) voor behandeling te hanteren.
Onderbouwing
Conclusies / Summary of Findings
|
Patiëntenvoorbereiding Zwangerschap |
Conclusies (gradatie, aantal studies) |
|
PT |
Stabiel of verkort. (3B, n=9) |
|
aPTT |
Stabiel of verkort. (3B, n=9) |
|
D-dimeren |
Verhoogd. (3B, n=9) |
|
Fibrinogeen |
Verhoogd. (3B, n=9) |
|
Stollingsfactoren |
Gedurende de zwangerschap blijven de volgende stollingsfactoren stabiel; FII, FV, FX en FXI. De overige stollingsfactoren zijn verhoogd gedurende de zwangerschap; FVII, FVIII, FIX en FXII. (3B, n=17) |
|
vWF |
Sterk verhoogd. (3B, n=17) |
|
Trombinetijd |
Stabiel. (3B, n=9) |
|
ROTEM |
Gedurende de zwangerschap zijn de uitslagen van verschillende ROTEM/TEG parameters gewijzigd; alfa angle verhoogd, korte stollingstijd, verhoogde stolselsterkte. (3B, n=4) |
|
TEG |
|
|
LTA |
Verhoogde activiteit [ADP, col]. (3B, n=3) |
|
PFA |
Gedurende de zwangerschap kan de PFA verkort zijn in aanwezigheid van ADP en EPI. (3B, n=3) |
Samenvatting literatuur
In de literatuur wordt beschreven dat gedurende een normale zwangerschap de hemostatische balans tussen bloedstolling en fibrinolyse is verstoord. Gedurende een normale zwangerschap vindt er een verschuiving plaats naar een protrombotisch e status waarbij verschillende stollingsfactoren verhoogd kunnen zijn (Brenner, 2004; Holmes en Wallace, 2005; Hellgren, 2003; Ataullakhanov et al., 2016). Een recent review door Ataullakhanov et al. (2016) geeft een mooi overzicht van de bevindingen die gedaan zijn op het gebied van hemostase gedurende een normale zwangerschap.
PT, aPTT, fibrinogeen en D-dimeren
Cerneca et al. (1997) onderzocht in 117 zwangere vrouwen de hemostatische verandering gedurende de zwangerschap door verschillen bloedstollingstesten te volgen. De auteurs observeerden een verkorte PT midden in het tweede trimester, welke significant verkort bleef gedurende de gehele zwangerschap tot zelfs enkele dagen na de bevalling. De aPTT bleef onveranderd gedurende de zwangerschap. Verder, vond men dat fibrinogeen verhoogd was aan het einde van het eerste trimester en deze significant steeg gedurende de zwangerschap tot enkele dagen na de zwangerschap. Szecsi et al. (2010) onderzocht dezelfde hemostatische parameters gedurende de zwangerschap in 391 zwangere vrouwen. In lijn met de bevindingen van Cerneca et al. (1997) bleef de aPTT onveranderd gedurende de zwangerschap. De auteurs observeerden wel een variatie in aPTT testuitslagen tussen de verschillende gebruikte reagentia in de studie. Er werden geen verschillen aangetoond voor de PT. Vanaf de laatste week van het tweede trimester observeerden de auteurs een sterke toename in fibrinogeenconcentratie, welke ongeveer twee keer zo hoog werd dan die in niet zwangere vrouwen. Deze hoge waardes hielden aan tot enkele dagen na de bevalling. Vergelijkbare resultaten werden gevonden voor D-dimeren. De PT en aPTT bleven stabiel in de eerste weken van het eerste trimester van de zwangerschap in een prospectieve longitudinale studie van Hui et al. (2012). Wel observeerden de auteurs een significante verlaging van de PT en aPTT gedurende de zwangerschap in vergelijking met niet zwangere vrouwen en met vrouwen in het eerste trimester van de zwangerschap. Ook in deze studie observeerden de auteurs een toename van de fibrinogeenconcentratie gedurende de zwangerschap in vergelijking met niet zwangere vrouwen. Dezelfde veranderingen in D-dimeren werden gevonden gedurende de zwangerschap. Ercan et al. (2015) vond vergelijkbare resultaten in 416 zwangere vrouwen waar D-dimeren- en fibrinogeenconcentraties gedurende de zwangerschap waren verhoogd. Hierbij werden de hoogste concentraties gemeten in het derde trimester van de zwangerschap. Gedurende de zwangerschap observeerden de auteurs een verkorte aPTT ten opzichte van die in niet zwangeren. De PT bleef stabiel gedurende de zwangerschap (Ercan et al., 2015). Choi en Pai (2002) laat vergelijkbare resultaten zien op het gebied van PT, aPTT, fibrinogeen en Ddimeren. Men kan hieruit concluderen dat PT en aPTT redelijk stabiel blijven gedurende de zwangerschap. Daarnaast ziet men dat gedurende de zwangerschap D-dimeren- en fibrinogeenconcentraties verhoogd zijn.
vWF en stollingsfactoren
In het onderzoek van Szecsi et al. (2010) is ook gekeken naar de veranderingen van verschillende stollingsfactoren gedurende de zwangerschap. Gedurende de zwangerschap werden er geen significante verschillen gezien in FII, FV, FX en FXI. Met uitzondering van FV (verhoogd), bleven de overige stollingsfactoren ook stabiel tot twee dagen na de bevalling. In het derde trimester van de zwangerschap vonden de auteurs een verhoogd FVII ten opzichte van de concentratie in niet zwangeren. FVII bleef verhoogd tot enkele dagen na de bevalling. Zowel FVIII als FIX zijn verhoogd in zwangere vrouwen en stijgen gedurende de verschillende trimesters, waarbij de hoeveelheid FVIII het sterkste toeneemt. Daarnaast observeerden de auteurs een lichte stijging in FXII, welke stabiel bleef gedurende de zwangerschap. Een vergelijkbare stijging in FVIII is geobserveerd in 40 zwangere vrouwen in een studie van Mahieu et al. (2007) waarbij er een stabiele stijging plaats vond van ongeveer 24% per trimester. Zes weken na de bevalling was FVIII weer met 50% gereduceerd ten opzichte van de waarde in het derde trimester. vWF was ook verhoogd gedurende de zwangerschap en hierbij vond men ook een 50% reductie van vWF zes weken na de bevalling ten opzichte van die in het derde trimester. Choi en Pai (2002) observeerden geen veranderingen in trombocytenconcentratie en FXI gedurende en na zwangerschap. Men observeerde wel toename in stollingsactiviteit van de volgende stollingsfactoren gedurende de zwangerschap: VII, VIII, IX en XII. Deze stollingsactiviteit daalde binnen de eerste vier weken na de bevalling en bereikte de normale waarde tussen de vijf á acht weken na de bevalling. In contrast met deze bevindingen vond Clark et al. (1998) in een eerdere studie dat de FV-activiteit steeg in het derde trimester van de zwangerschap en dat deze drie dagen na de bevalling nog verhoogd was. Wel vond men een vergelijkbare stijging in FVIII-activiteit gedurende de zwangerschap, welke drie dagen na de bevalling nog zichtbaar was. Een kleine stijging werd geobserveerd in FIX aan het einde van het tweede trimester maar deze daalde daarna gedurende de zwangerschap met een kleine stijging na de bevalling. FX en FXII lieten vanaf het tweede trimester een stijging zien in activiteit gedurende de zwangerschap en daarna. vWF toonde veel variatie gedurende de zwangerschap maar was het hoogst aan het einde van de zwangerschap en de dagen na de bevalling. Echter, Sattar et al. (1999) en Drury-Stewart et al. (2014) observeerden een gelijkmatige stijging in vWF gedurende de zwangerschap met een piek in het derde trimester van de zwangerschap. Men zag waardes die twee keer zo hoog waren dan die in niet-zwangere vrouwen. Drury-Stewart et al. (2014) observeerde ook een stijging in FVIII gedurende de zwangerschap. Daarnaast concludeerden de auteurs dat hoogmoleculair gewicht vWF-multimeren verloren gaan gedurende de zwangerschap. Deze hemostatische veranderingen in stollingsfactoren werden ook gevonden in andere studies (Ercan et al., 2015; Stirling et al., 1984; Condie, 1976; Hellgren en Blombäck, 1981; Sharief et al., 2014; Bremme et al., 1992). De reeds besproken studies laten een goed beeld zien over de effecten gedurende de zwangerschap. Met betrekking tot routine stollingstesten en het testen van stollingsactiviteit, observeerde Saha et al. (2009) dat deze toename in hypercoagulabiliteit kan aanhouden tot 3 weken na de bevalling.
In het algemeen kan men concluderen dat zowel routine als speciale stollingstesten kunnen afwijken gedurende de zwangerschap. In een ideale situatie zou het bepalen van specifieke referentiewaarden per trimester voor bepaalde stollingstesten een uitkomst zijn voor klinische interpretatie en ondersteunen bij het daarnaar handelen. Enkele studies die in deze module besproken zijn, hebben referentiewaardes gedurende de zwangerschap bepaald, maar beter is als deze per methode gevalideerd te worden (Szecsi et al., 2010; Ercan et al., 2015). Daarnaast adviseert Blombäck et al. (2007) dat voor de diagnose van vWF-ziekte en FVIII-deficiëntie bloedafname moet plaatsvinden gedurende een normale menstruatieperiode en het liefst voor of minimaal 2 maanden na zwangerschap. Met betrekking tot de effecten op trombocytenfunctietesten gedurende zwangerschap, onderzocht Antony et al. (2015) de veranderingen op TEG en PFA-100 en vergeleek deze met referentiewaarden van niet zwangeren. Auteurs observeerden bij TEG-analyses in zwangeren een verkorte stollingstijd (R).
Daarnaast was de “angle” (α) vergroot in vergelijking met die van niet-zwangeren. Ook werd een verkorte CT-waarde van PFA-100 in aanwezigheid van ADP en EPI gezien bij analyses in zwangere vrouwen. Vergelijkbare observaties werden gedaan door Polak et al. (2011) waarbij ook een verkorte
R en verhoogd α gevonden werden. Ook Huissoud et al. (2009), van Rheenen-Flach et al. (2013) en de Lange et al. (2014) onderzochten de hemostatische verandering gedurende de zwangerschap of rondom de partus in ROTEM/TEG-analyses en vonden vergelijkbare resultaten.
Zoeken en selecteren
De zoekverantwoording is weergegeven onder het tabblad Verantwoording. Zie de zoekverantwoording voor de uitgebreide zoekstrategieën per module.
Referenties
- Ahuja KD, Thomas GA, Adams MJ, Ball MJ. Postprandial platelet aggregation: effects of different meals and glycemic index. Eur J Clin Nutr. 2012;66(6):722-6.
- Ambrus JL, Mink IB. Effect of cigarette smoking on blood coagulation. Clin Pharmacol Ther. 1964 JulAug;5:428-31.
- Ammaturo V, Perricone C, Canazio A, Ripaldi M, Ruggiano A, Zuccarelli B, Monti M. Caffeine stimulates in vivo platelet reactivity. Acta Med Scand. 1988;224(3):245-7.
- Andrew M, Carter C, O'Brodovich H, Heigenhauser G. Increases in factor VIII complex and fibrinolytic activity are dependent on exercise intensity. J Appl Physiol (1985). 1986 Jun;60(6):1917-22.
- Antony KM, Mansouri R, Arndt M, Rocky Hui SK, Jariwala P, McMullen VM, Teruya J, Aagaard K. Establishing thromboelastography with platelet-function analyzer reference ranges and other measures in healthy term pregnant women. Am J Perinatol. 2015;32(6):545-54.
- Arai M, Yorifuji H, Ikematsu S, Nagasawa H, Fujimaki M, Fukutake K, Katsumura T, Ishii T, Iwane H. Influences of strenuous exercise (triathlon) on blood coagulation and fibrinolytic system. Thromb Res. 1990;57(3):465-71.
- Ataullakhanov FI, Koltsova EM, Balandina AN, Serebriyskiy, II, Vuimo TA, Panteleev MA. Classic and global hemostasis testing in pregnancy and during pregnancy complications. Semin Thromb Hemost. 2016;42(7):696716.
- Austin AW, Patterson SM, von Känel R. Hemoconcentration and hemostasis during acute stress: interacting and independent effects. Ann Behav Med. 2011;42(2):153-73.
- Austin AW, Wirtz PH, Patterson SM, Stutz M, von Känel R. Stress-induced alterations in coagulation: assessment of a new hemoconcentration correction technique. Psychosom Med. 2012;74(3):288-95.
- Austin AW, Wissmann T, von Känel R. Stress and hemostasis: an update. Semin Thromb Hemost. 2013;39(8):902-12.
- Bak AA, van Vliet HH, Grobbee DE. Coffee, caffeine and hemostasis: results from two randomized studies. Atherosclerosis. 1990;83(2-3):249-55.
- Bartsch P, Haeberli A, Straub PW. Blood coagulation after long distance running: antithrombin III prevents fibrin formation. Thromb Haemost. 1990;63(3):430-4.
- Bazzano LA, He J, Muntner P, Vupputuri S, Whelton PK. RElationship between cigarette smoking and novel risk factors for cardiovascular disease in the united states. Ann Intern Med. 2003 Jun 3;138(11):891-7.
- Blombäck M, Konkle BA, Manco-Johnson MJ, Bremme K, Hellgren M, Kaaja R. Preanalytical conditions that affect coagulation testing, including hormonal status and therapy. J Thromb Haemost. 2007;5(4):855-8.
- Bremme K, Ostlund E, Almqvist I, Heinonen K, Blombäck M. Enhanced thrombin generation and fibrinolytic activity in normal pregnancy and the puerperium. Obstet Gynecol. 1992;80(1):132-7.
- Brenner B. Haemostatic changes in pregnancy. Thromb Res. 2004;114(5-6):409-14.
- Bridges AB, McLaren M, Saniabadi A, Fisher TC, Belch JJ. Circadian variation of endothelial cell function, red blood cell deformability and dehydro-thromboxane B2 in healthy volunteers. Blood Coagul Fibrinolysis. 1991 Jun;2(3):447-52.
- Bridges AB, McLaren M, Scott NA, Pringle TH, McNeill GP, Belch JJ. Circadian variation of tissue plasminogen activator and its inhibitor, von Willebrand factor antigen, and prostacyclin stimulating factor in men with ischaemic heart disease. Br Heart J. 1993;69(2):121-4.
- Bydlowski SP, Yunker RL, Rymaszewski Z, Subbiah MT. Coffee extracts inhibit platelet aggregation in vivo and in vitro. Int J Vitam Nutr Res. 1987;57(2):217-23.
- Cattaneo M, Cerletti C, Harrison P, Hayward CP, Kenny D, Nugent D, Nurden P, Rao AK, Schmaier AH, Watson SP, Lussana F, Pugliano MT, Michelson AD. Recommendations for the standardization of light transmission aggregometry: a consensus of the working party from the Platelet Physiology Subcommittee of SSC/ISTH. J Thromb Haemost. 2013 Apr 10.
- Cerneca F, Ricci G, Simeone R, Malisano M, Alberico S, Guaschino S. Coagulation and fibrinolysis changes in normal pregnancy. Increased levels of procoagulants and reduced levels of inhibitors during pregnancy induce a hypercoagulable state, combined with a reactive fibrinolysis. Eur J Obstet Gynecol Reprod Biol. 1997 May;73(1):31-6.
- Choi JW, Pai SH. Tissue plasminogen activator levels change with plasma fibrinogen concentrations during pregnancy. Ann Hematol. 2002 Nov;81(11):611-5.
- Clark P, Brennand J, Conkie JA, McCall F, Greer IA, Walker ID. Activated protein C sensitivity, protein C, protein S and coagulation in normal pregnancy. Thromb Haemost. 1998;79(6):1166-70.
- CLSI. Platelet function testing by aggregometry; approved guideline. CLSI Document H58-A. Wayne, PA: Clinical and Laboratory Standards Institue; 2008.
- Condie RG. A serial study of coagulation factors XII, XI and X in plasma in normal pregnancy and in pregnancy complicated by pre-eclampsia. Br J Obstet Gynaecol. 1976;83(8):636-9.
- Dalby MC, Davidson SJ, Burman JF, Davies SW. Diurnal variation in platelet aggregation iwth the PFA-100 platelet function analyser. Platelets. 2000;11(6):320-4.
- de Lange NM, van Rheenen-Flach LE, Lancé MD, Mooyman L, Woiski M, van Pampus EC, Porath M, Bolte AC, Smits L, Henskens YM, Scheepers HC. Peri-partum reference ranges for ROTEM(R) thromboelastometry. Br J Anaesth. 2014 May;112(5):852-9.
- DeSouza CA, Jones PP, Seals DR. Physical activity status and adverse age-related differences in coagulation and fibrinolytic factors in women. Arterioscler Thromb Vasc Biol. 1998;18(3):362-8.
- Drury-Stewart DN, Lannert KW, Chung DW, Teramura GT, Zimring JC, Konkle BA, Gammill HS, Johnsen JM. Complex changes in von Willebrand factor-associated parameters are acquired during uncomplicated pregnancy. PLoS One. 2014;9(11):e112935.
- Eliasson M, Asplund K, Evrin PE, Lundblad D. Relationship of cigarette smoking and snuff dipping to plasma fibrinogen, fibrinolytic variables and serum insulin. The Northern Sweden MONICA Study. Atherosclerosis. 1995;113(1):41-53.
- El-Sayed MS, Lin X, Rattu AJ. Blood coagulation and fibrinolysis at rest and in response to maximal exercise before and after a physical conditioning programme. Blood Coagul Fibrinolysis 1995;6(8):747-52.
- Engelberg H, Futterman M. Cigarette smoking and thrombotic coagulation of human blood. Further in vitro studies. Arch Environ Health. 1967 Feb;14(2):266-70.
- Engelberg H. Cigarette smoking and the in vitro thrombosis of human blood. JAMA 1965;193:1033-5.
- Ercan S, Ozkan S, Yucel N, Orcun A. Establishing reference intervals for D-dimer to trimesters. J Matern Fetal Neonatal Med. 2015;28(8):983-7.
- Ferguson EW, Guest MM. Exercise, physical conditioning, blood coagulation and fibrinolysis. Thromb Diath Haemorrh. 1974;31(1):63-71.
- Feuring M, Wehling M, Ruf A, Schultz A. Circadian variation of platelet function measured with the PFA-100. Platelets. 2009 Nov;20(7):466-70.
- Finkel A, Cumming GR. Effects of exercise in the cold on blood clotting and platelets. J Appl Physiol. 1965;20(3):423-4.
- Freese R, Mutanen M. Postprandial changes in platelet function and coagulation factors after high-fat meals with different fatty acid compositions. Eur J Clin Nutr. 1995;49(9):658-64.
- Grignani G, Pacchiarini L, Zucchella M, Tacconi F, Canevari A, Soffiantino F, Tavazzi L. Effect of mental stress on platelet function in normal subjects and in patients with coronary artery disease. Haemostasis. 1992;22(3):138-46.
- Harrison P, Mackie I, Mumford A, Briggs C, Liesner R, Winter M, Machin S; British Committee for Standards in Haematology. Guidelines for the laboratory investigation of heritable disorders of platelet function. Br J Haematol. 2011;155(1):30-44.
- Haus E, Cusulos M, Sackett-Lundeen L, Swoyer J. Circadian variations in blood coagulation parameters, alphaantitrypsin antigen and platelet aggregation and retention in clinically healthy subjects. Chronobiol Int. 1990;7(3):203-16.
- Hegde SS, Goldfarb AH, Hegde S. Clotting and fibrinolytic activity change during the 1 h after a submaximal run. Med Sci Sports Exerc. 2001;33(6):887-92.
- Hellgren M, Blombäck M. Studies on blood coagulation and fibrinolysis in pregnancy, during delivery and in the puerperium. I. Normal condition. Gynecol Obstet Invest. 1981;12(3):141-54.
- Hellgren M. Hemostasis during normal pregnancy and puerperium. Semin Thromb Hemost. 2003;29(2):125-30.
- Hilberg T, Prasa D, Sturzebecher J, Glaser D, Schneider K, Gabriel HH. Blood coagulation and fibrinolysis after extreme short-term exercise. Thromb Res. 2003;109(5-6):271-7.
- Holmes VA, Wallace JM. Haemostasis in normal pregnancy: a balancing act? Biochem Soc Trans. 2005;33(Pt 2):428-32.
- Hui C, Lili M, Libin C, Rui Z, Fang G, Ling G, Jianping Z. Changes in coagulation and hemodynamics during pregnancy: a prospective longitudinal study of 58 cases. Arch Gynecol Obstet. 2012;285(5):1231-6.
- Huissoud C, Carrabin N, Benchaib M, Fontaine O, Levrat A, Massignon D, Touzet S, Rudigoz RC, Berland M. Coagulation assessment by rotation thrombelastometry in normal pregnancy. Thromb Haemost. 2009;101(4):755-61.
- Iatridis SG, Ferguson JH. Effect of physical exercise on blood clotting and fibrinolysis. J Appl Physiol. 1963;18:337-44.
- Iversen PO, Groot PD, Hjeltnes N, Andersen TO, Mowinckel MC, Sandset PM. Impaired circadian variations of haemostatic and fibrinolytic parameters in tetraplegia. Br J Haematol. 2002;119(4):1011-6.
- Jern C, Eriksson E, Tengborn L, Risberg B, Wadenvik H, Jern S. Changes of plasma coagulation and fibrinolysis in response to mental stress. Thromb Haemost. 1989 Sep 29;62(2):767-71.
- Kapiotis S, Jilma B, Quehenberger P, Ruzicka K, Handler S, Speiser W. Morning hypercoagulability and hypofibrinolysis. Diurnal variations in circulating activated factor VII, prothrombin fragment F1+2, and plasminplasmin inhibitor complex. Circulation. 1997;96(1):19-21.
- Knudsen JB, Brodthagen U, Gormsen J, Jordal R, Norregaard-Hansen K, Paulev PE. Platelet function and fibrinolytic activity following distance running. Scand J Haematol. 1982;29(5):425-30.
- Krekels JPM, Verhezen PWM, Henskens YMC. Platelet aggregation in healthy participants is not affected by smoking, drinking coffee, consuming a high-fat meal, or performing physical exercise. Clin Appl Thromb Hemost. 2019 Jan-Dec;25:1076029618782445.
- Lee KW, Lip GY. Effects of lifestyle on hemostasis, fibrinolysis, and platelet reactivity: a systematic review. Arch Intern Med. 2003;163(19):2368-92.
- Lima-Oliveira G, Salvagno GL, Lippi G, Danese E, Gelati M, Montagnana M, Picheth G, Guidi GC. Could light meal jeopardize laboratory coagulation tests? Biochem Med (Zagreb). 2014;24(3):343-9.
- Lippi G, Maffulli N. Biological influence of physical exercise on hemostasis. Semin Thromb Hemost. 2009;35(3):269-76.
- Lippi G, Salvagno GL, Montagnana M, Lima-Oliveira G, Guidi GC, Favaloro EJ. Quality standards for sample collection in coagulation testing. Semin Thromb Hemost. 2012;38(6):565-75.
- Lippi G1, Lima-Oliveira G, Salvagno GL, Montagnana M, Gelati M, Picheth G, Duarte AJ, Franchini M, Guidi GC. Influence of a light meal on routine haematological tests. Blood Transfus. 2010;8(2):94-9.
- Mahieu B, Jacobs N, Mahieu S, Naelaerts K, Vertessen F, Weyler J, Jacquemyn Y, Van der Planken M. Haemostatic changes and acquired activated protein C resistance in normal pregnancy. Blood Coagul Fibrinolysis. 2007 Oct;18(7):685-8.
- Mandalaki T, Dessypris A, Louizou C, Panayotopoulou C, Dimitriadou C. Marathon Run III: effects on coagulation, fibrinolysis, platelet aggregation and serum cortisol levels. A 3-year study. Thromb Haemost 1980;43(1):49-52.
- Montagnana M, Salvagno GL, Lippi G. Circadian variation within hemostasis: an underrecognized link between biology and disease? Semin Thromb Hemost. 2009;35(1):23-33.
- Naesh O, Hindberg I, Trap-Jensen J, Lund JO. Post-exercise platelet activation--aggregation and release in relation to dynamic exercise. Clin Physiol. 1990;10(3):221-30.
- Naismith DJ, Akinyanju PA, Szanto S, Yudkin J. The effect, in volunteers, of coffee and decaffeinated coffee on blood glucose, insulin, plasma lipids and some factors involved in blood clotting. Nutr Metab. 1970;12(3):14451.
- Natella F, Nardini M, Belelli F, Pignatelli P, Di Santo S, Ghiselli A, Violi F, Scaccini C. Effect of coffee drinking on platelets: inhibition of aggregation and phenols incorporation. Br J Nutr. 2008;100(6):1276-82.
- Pamukcu B, Oflaz H, Onur I, Cimen A, Nisanci Y. Effect of cigarette smoking on platelet aggregation. Clin Appl Thromb Hemost. 2011 Nov-Dec;17(6):E175-80.
- Pieters M, de Maat MP. Diet and haemostasis - a comprehensive overview. Blood Rev. 2015 Jul;29(4):231-41.
- Polagruto JA, Schramm DD, Wang-Polagruto JF, Lee L, Keen CL. Effects of flavonoid-rich beverages on prostacyclin synthesis in humans and human aortic endothelial cells: association with ex vivo platelet function. J Med Food. 2003;6(4):301-8.
- Polak F, Kolnikova I, Lips M, Parizek A, Blaha J, Stritesky M. New recommendations for thromboelastography reference ranges for pregnant women. Thromb Res. 2011;128(4):e14-7.
- Ribeiro J, Almeida-Dias A, Ascensão A, Magalhães J, Oliveira AR, Carlson J, Mota J, Appell HJ, Duarte J. Hemostatic response to acute physical exercise in healthy adolescents. J Sci Med Sport. 2007;10(3):164-9.
- Rock G, Tittley P, Pipe A. Coagulation factor changes following endurance exercise. Clin J Sport Med. 1997;7(2):94-9.
- Rocker L, Drygas WK, Heyduck B. Blood platelet activation and increase in thrombin activity following a marathon race. Eur J Appl Physiol Occup Physiol. 1986;55(4):374-80.
- Rudnicka AR, Rumley A, Lowe GD, Strachan DP. Diurnal, seasonal, and blood-processing patterns in levels of circulating fibrinogen, fibrin D-dimer, C-reactive protein, tissue plasminogen activator, and von Willebrand factor in a 45-year-old population. Circulation. 2007;115(8):996-1003.
- Saha P, Stott D, Atalla R. Haemostatic changes in the puerperium '6 weeks postpartum' (HIP Study) - implication for maternal thromboembolism. BJOG. 2009;116(12):1602-12.
- Sattar N, Greer IA, Rumley A, Stewart G, Shepherd J, Packard CJ, Lowe GD. A longitudinal study of the relationships between haemostatic, lipid, and oestradiol changes during normal human pregnancy. Thromb Haemost. 1999;81(1):71-5.
- Sharief LT, Lawrie AS, Mackie IJ, Smith C, Peyvandi F, Kadir RA. Changes in factor XIII level during pregnancy. Haemophilia. 2014;20(2):e144-8.
- Smith JE. Effects of strenuous exercise on haemostasis. Br J Sports Med 2003;37(5):433-5.
- Snieder H, Huizink AC, Boomsma DI, Van Doornen LJP. Influence of mental stress on fibrinogen, von Willebrand factor and tissue-type plasmonigen activator antigen. Fibrinolysis 1996; 10(supp 2): 137-139.
- Steptoe A, Kunz-Ebrecht S, Rumley A, Lowe GD. Prolonged elevations in haemostatic and rheological responses following psychological stress in low socioeconomic status men and women. Thromb Haemost. 2003;89(1):83-90.
- Stirling Y, Woolf L, North WR, Seghatchian MJ, Meade TW. Haemostasis in normal pregnancy. Thromb Haemost. 1984;52(2):176-82.
- Sucker C, Zotz RB, Senft B, Scharf RE, Kröger K, Erbel R, Möhlenkamp S. Exercise-induced hemostatic alterations are detectable by rotation thrombelastography (ROTEM): A marathon study. Clin Appl Thromb Hemost. 2010;16(5):543-8.
- Szecsi PB, Jorgensen M, Klajnbard A, Andersen MR, Colov NP, Stender S. Haemostatic reference intervals in pregnancy. Thromb Haemost. 2010;103(4):718-27.
- Thrall G, Lane D, Carroll D, Lip GY. A systematic review of the effects of acute psychological stress and physical activity on haemorheology, coagulation, fibrinolysis and platelet reactivity: Implications for the pathogenesis of acute coronary syndromes. Thromb Res. 2007;120(6):819-47.
- van den Burg PJ, Hospers JE, van Vliet M, Mosterd WL, Bouma BN, Huisveld IA. Changes in haemostatic factors and activation products after exercise in healthy subjects with different ages. Thromb Haemost 1995;74(6):1457-64.
- van Rheenen-Flach LE, Zweegman S, Boersma F, Lenglet JE, Twisk JW, Bolte AC. A prospective longitudinal study on rotation thromboelastometry in women with uncomplicated pregnancies and postpartum. Aust N Z J Obstet Gynaecol. 2013 Feb;53(1):32-6.
- von Känel R, Mills PJ, Fainman C, Dimsdale JE. Effects of psychological stress and psychiatric disorders on blood coagulation and fibrinolysis: a biobehavioral pathway to coronary artery disease? Psychosom Med. 2001;63(4):531-44.
- von Känel R, Preckel D, Zgraggen L, Mischler K, Kudielka BM, Haeberli A, Fischer JE. The effect of natural habituation on coagulation responses to acute mental stress and recovery in men. Thromb Haemost. 2004 Dec;92(6):1327-35.
- Wallen NH, Held C, Rehnqvist N, Hjemdahl P. Effects of mental and physical stress on platelet function in patients with stable angina pectoris and healthy controls. Eur Heart J. 1997;18(5):807-15.
- Weiss C, Seitel G, Bartsch P. Coagulation and fibrinolysis after moderate and very heavy exercise in healthy male subjects. Med Sci Sports Exerc. 1998;30(2):246-51.
- Yarnell JW, Sweetnam PM, Rumley A, Lowe GD. Lifestyle and hemostatic risk factors for ischemic heart disease : the Caerphilly Study. Arterioscler Thromb Vasc Biol. 2000;20(1):271-9.
- Zgraggen L, Fischer JE, Mischler K, Preckel D, Kudielka BM, von Känel R. Relationship between hemoconcentration and blood coagulation responses to acute mental stress. Thromb Res. 2005;115(3):175-83.
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 05-11-2020
Voor het beoordelen van de actualiteit van deze richtlijn wordt (een deel van) de werkgroep in stand gehouden. Op modulair niveau is een onderhoudsplan beschreven. Bij het afronden van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten. De NVKC is regiehouder van deze richtlijn(module) en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn(module).
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
- Het opstellen van laboratorium technische adviezen, voor zover mogelijk Evidence-Based met betrekking tot de pre-analyse van minimaal 10 testen die veel gebruikt worden in Nederland en die noodzakelijk zijn voor de analyse, diagnose en behandeling van patiënten met bloedingsneiging.
- Een bijdrage leveren aan de standaardisatie van hemostase testen en de grotere uitwisselbaarheid van uitslagen en hemostase laboratoriumdiagnostiek tussen ziekenhuislaboratoria.
- Een handreiking geven van de bekende literatuur op het gebied van de pre-analytische fase op het gebied van hemostase (t/m juli 2018).
Doelgroep
Deze richtlijn is een handreiking voor alle laboratoriumspecialisten klinische chemie (NVKC/VHL) die nauw in contact staan met de medisch specialist, waarbij de klinisch chemicus op het gebied van analyse bloedingsneigingen consultaties geeft en (eind)verantwoordelijk is voor de bloedafname, analyse en rapportage van stollingstesten. Indirecte gebruikers van deze voorschriften kunnen artsen en verpleegkundigen zijn, die de diagnose stellen en/of bloed afnemen ten behoeve van stollingsonderzoek. Hierbij kan onderscheid gemaakt worden tussen de huisartsen die basale testen aanvragen en aanvragers van het uitgebreide stollingspakket zoals internisten, internist-hematologen, gynaecologen, anesthesisten, kinderartsen, radiologen, tandartsen, en (kaak)chirurgen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2017 een werkgroep ingesteld. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr.ir. Y.M.C. (Yvonne) Henskens, laboratoriumspecialist klinische chemie, Maastricht UMC+, Maastricht (voorzitter), namens NVKC/VHL
- Dr. Dr. M.L.J (Mike) Jeurissen, onderzoeker, Maastricht UMC+, Maastricht, namens NVKC
- Dr. A.K. (An) Stroobants, laboratoriumspecialist klinische chemie, Amsterdam UMC, locatie AMC, Amsterdam, namens NVKC/VHL
- Dr. M.P.M. (Moniek) de Maat, biochemicus, Erasmus MC, Rotterdam, namens VHL
- C.A.M. (Caroline) Klopper, vakanalist, Amsterdam UMC, locatie AMC, namens NVTH werkgroep Hemostase
- P.W.M. (Paul) Verhezen, vakanalist, Maastricht UMC+, Maastricht, namens NVTH werkgroep Hemostase
- Dr. K.M.T. (Kim) de Bruyn, laboratoriumspecialist klinische chemie, Tergooi, Hilversum, Blaricum, namens NVKC/VHL
- Dr. R.W.L.M. (René) Niessen, laboratoriumspecialist klinische chemie, OLVG, Amsterdam, namens NVKC/SKML
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben. Een overzicht van de belangen van werkgroepleden is in onderstaande tabel weergegeven; er zijn geen restricties m.b.t. deelname aan de werkgroep.
|
Naam |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Y. Henskens |
Klinisch chemicus |
Lid LGR Sanquin Voorzitter gebruikersraad Sanquin ZON/Limburg Voorzitter concilium NVKC (opleiding) Lid Kennisplatform Transfusiegeneeskunde ZO Bestuurslid VHL Lid werkgroep Hemostase VHL (allen onbetaald) Richtlijn commissie Antitrombotisch beleid FMS/NIV namens NVKC Richtlijn werkgroep FMS Bloedtransfusie (massaal bloedverlies) (vacatiegeld) |
Voor alle studies in het kader van MUMC+ onderzoekslijn “laboratory predictors of bleeding” worden IVD gebruikt die geheel of gedeeltelijk worden gesponsord door IVD firma’s |
Geen: het betreft geen IVD in het kader van preanalyse |
|
M. Jeurissen |
Onderzoeker |
Geen |
Geen |
Geen |
|
A. Stroobants |
Klinisch chemicus |
Bestuurslid VHL Voorzitter werkgroep Hemostase VHL Richtlijn commissie Antitrombotisch beleid FMS/NIV namens NVKC |
Geen |
Geen |
|
M. de Maat |
Biochemicus |
Lid RvT ECAT (vacatievergoeding) Lid Council International Fibrinogen Research (onbetaald) |
Geen |
Geen |
|
C. Klopper |
Vakanalist |
Lid WHD: Werkgroep Hemostase Diagnostiek NVTH (onbetaald) |
Geen |
Geen |
|
P. Verhezen |
Vakanalist |
Lid WHD: Werkgroep Hemostase Diagnostiek NVTH (onbetaald) |
Geen |
Geen |
|
K. de Bruyn |
Klinisch chemicus |
ISO 15189 auditor (betaald) |
Geen |
Geen |
|
R. Niessen |
Klinisch chemicus |
Bestuurslid: SKML sectie Hematologie Sectie SKS-SKML FNT (allen onbetaald) |
Geen |
Geen |
Inbreng patiëntenperspectief
De richtlijn richt zich voornamelijk op de bloedstollingstesten die ingezet kunnen worden bij patiënten die verdacht worden van een congenitale (stollingsfactoren, trombopathie) of verworven (anticoagulantia, massaal bloedverlies) bloedingsneiging. In samenspraak met de Nederlandse Vereniging van Hemofilie Patiënten (NVHP) is uitleg opgesteld voor patiënten waarbij bloed wordt afgenomen voor stollingsonderzoek. De uitleg is op B1 niveau geformuleerd, met kernbegrippen waarop een patiënt zelf verder kan zoeken, indien gewenst.
Methode ontwikkeling
Evidence based
Implementatie
Tijdens de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is opgenomen bij de aanverwante producten.
Werkwijze
Knelpuntenanalyse
Tijdens de voorbereidende fase werden de knelpunten geïnventariseerd en een lange lijst van uitgangsvragen opgesteld. Tijdens een bijeenkomst werd door alle werkgroepleden een prioritering ingevuld van de verzamelde uitgangsvragen. De vragen met de hoogste prioriteit werden vervolgens gebruikt voor deze richtlijn.
Uitgangsvragen
De werkgroep heeft de volgende uitgangsvragen geprioriteerd:
- Welke patiënten kenmerken (biologische status) kunnen de uitkomsten van bloedstollingstesten beïnvloeden?
- Welke factoren kunnen invloed hebben op de (kwaliteit van de) bloedafname en hebben daardoor invloed op de uitkomsten van bloedstollingstesten?
- Welke factoren kunnen invloed hebben op het transport van patiëntmateriaal waardoor ze hebben de uitkomst van bloedstollingstesten kunnen beïnvloeden?
- Welke factoren kunnen invloed hebben op de verwerking van patiëntmateriaal tot plasma of plaatjes-rijk plasma waardoor ze de uitkomst van bloedstollingstesten kunnen beïnvloeden?
- Hoe lang kan volbloed en plasma bewaard worden, zonder de uitkomst van bloedstollingstesten te beïnvloeden?
Strategie voor zoeken en selecteren van literatuur
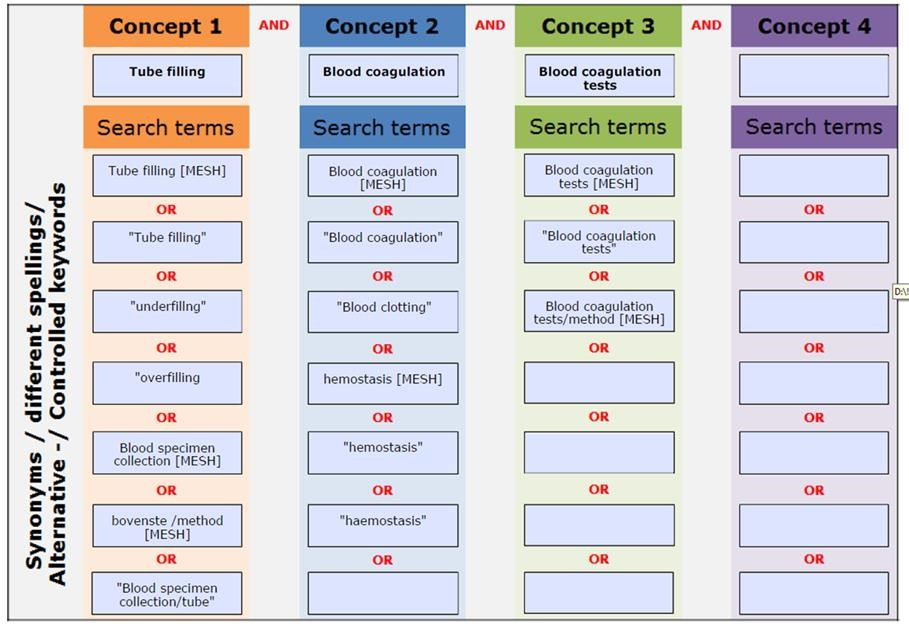
De zoekstrategieën die zijn verricht in het kader van de uitgangsvragen zijn systematisch uitgevoerd. De zoekstrategieën hebben plaats gevonden in het database Pubmed en/of Medline. Enkele zoektermen die veelvoudig zijn gebruikt zijn: blood coagulation, blood coagulation tests, blood clotting, hemostasis, blood collection, blood specimen. Deze zoektermen werden in combinatie gebruikt met specifiekere zoektermen gericht op het onderwerp. Zie de zoekverantwoording voor de uitgebreide zoek strategieën per module.
Samenvatten van de literatuur
De belangrijkste bevindingen uit de wetenschappelijke literatuur zijn beschreven in de samenvatting van de literatuur.
De intentie voor het graderen van literatuur voor deze richtlijn was om gebruik te maken van GRADE. De beschikbare stollingstesten om de primaire en secondaire hemostase te analyseren zijn sterk afhankelijk van pre-analytische variabelen, die de uitslagen van deze testen sterk kunnen beïnvloeden. De literatuur biedt geen consensus in de optimale pre-analytische omstandigheden waarbij bloedstolling testen uitgevoerd kunnen worden. Om kwaliteit en de sterkte van aanbevelingen te kwantificeren werd eerst onderzocht of het GRADE-systeem implementeerbaar is in deze richtlijn. De vraag die wij ons hierbij eerst gesteld hebben is: is GRADE toepasbaar in een pre-analytische setting van de laboratoriumdiagnostiek? Bij GRADE wordt de kwaliteit van de studie per uitkomstmaat bepaald, geformuleerd via het PICO-principe. Vijf factoren bepalen de kwaliteit per uitkomstmaat: publicatiebias, beperking in studieopzet, imprecisie, indirectheid en inconsistentie (Guyatt et al., 2011, Boluyt et al., 2012). Om te kijken of GRADE toepasbaar is hebben we een kleine zoekopdracht uitgevoerd, waarbij gekeken is naar de interferentie van hemolyse op bloedstollingstesten om knelpunten van GRADE te identificeren. Knelpunten werden gevonden in de formulering van de PICO; keuze van populatie (patiënt en gezond), aangezien pre-analytische variaties in elke populatie kan voorkomen en daarbij de keuze van de juiste uitkomstmaat. De zoekopdracht resulteerde in drie studies die de juiste uitkomstmaat gebruikte uit een selectie van ±600 hits. Daarbij toonde de gekozen studies grote verschillen in apparatuur, reagentia, en methode van inductie en definitie van hemolyse. Op basis van de criteria volgens GRADE zou deze uitkomstmaten een zeer lage of geen gradatie krijgen. Onze conclusie was dat de PICO’s binnen GRADE zeer klinisch en patiëntgericht zijn waarbij voornamelijk gekeken wordt naar interventies; daardoor is GRADE niet toepasbaar binnen een preanalytische setting.
Op basis hiervan werd de literatuur gegradeerd m.b.v. het gradatiesysteem dat gebruikt is in de aanverwante richtlijn “Diagnostiek en behandeling van hemofilie en aanverwante hemostasestoornissen 2009”. Het gradatiesysteem dat in deze richtlijn wordt beschreven is gebaseerd op de US Agency for Health Care Policy and Research”. Zie voorbeeld in de onderstaande tabellen.
Tabel 1: Indeling van de literatuur naar mate van bewijskracht
|
Bewijskracht |
Soort bewijs |
|
Graad 1 |
Bewijs verkregen van meta-analyse van gerandomiseerd gecontroleerde onderzoeken (1a) of ten minste één geblindeerd gerandomiseerd gecontroleerd onderzoek (1b) |
|
Graad 2 |
Bewijs verkregen uit ten minste een goed gedefinieerd gecontroleerd onderzoek, zonder randomisatie (2a) of een cohort- of patiëntcontrole-onderzoek van goede kwaliteit (2b) of een systematisch review zonder meta-analyse |
|
Graad 3 |
Bewijs verkregen uit goed gedefinieerde, niet experimentele beschrijvende onderzoeken, zoals vergelijkende onderzoeken, correlatieonderzoeken of patiëntcontroleonderzoeken van slechte kwaliteit |
|
Graad 4 |
Bewijs verkregen van expertpanels of opinies van deskundigen |
Tabel 2: Niveau van aanbeveling
|
Niveau |
Soort bewijs |
|
A |
Een onderzoek van graad 1a of 1b |
|
B |
Ten minste twee onderzoeken van graad 2a, 2b of graad 3 |
|
C |
Berustend op bewijs van graad 4 |
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald. De werkgroepleden maakten de balans op van elke interventie (conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt gewogen. De bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje ‘Overwegingen’.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast wetenschappelijke publicaties ook andere aspecten belangrijk om te worden meegewogen, zoals de expertise van de werkgroepleden, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld onder het kopje ‘Overwegingen’.
Kennislacunes
Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van de aanbevelingen voor nader/vervolgonderzoek is opgenomen onder het kopje ‘Kennislacunes’ (bij Aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de leden van de NVKC, VHL, SKML subcommissie stolling, NIV en aan Patiëntenfederatie Nederland voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De autorisatieversie van de richtlijn is ter stemming gebracht tijdens de algemene ledenvergadering van de NVKC, en voorgelegd aan Patiëntenfederatie Nederland ter autorisatie c.q. instemming.
Literatuur
Boluyt N, Rottier BL, Langendam MW. [Guidelines are made more transparent with the GRADE method: considerations for recommendations are explicit in the new method]. Ned Tijdschr Geneeskd. 2012; 156: A4379.
Guyatt G, Oxman AD, Akl EA, Kunz R, Vist G, Brozek J, Norris S, Falck-Ytter Y, Glasziou P, DeBeer H, Jaeschke R, Rind D, Meerpohl J, Dahm P, Schünemann HJ. GRADE guidelines: 1. Introduction-GRADE evidence profiles and summary of findings tables. J Clin Epidemiol. 2011; 64: 383-394.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
