Behandeling van diabetes bij patiënten met CF
Uitgangsvraag
(Hoe) moet een vastgestelde stoornis in de glucosehuishouding worden behandeld bij patiënten met CF?
Aanbeveling
Start behandeling van stoornissen in het glucose metabolisme bij patiënten met CF na adequate classificatie van de stoornis:
- Start behandeling bij CFRD.
- Overweeg glucose verlagende behandeling bij CF-IGT.
- Schakel een gespecialiseerde diëtist in voor de gezamenlijke afweging van therapiekeuze: (eerst) dieetaanpassing en/of medicamenteus.
Bij CFRD is behandeling met insuline de eerste keus.
Overwegingen
Kwaliteit van het bewijs en balans tussen voor- en nadelen.
De kwaliteit van het bewijs is laag. Er zijn uit de studies geen criteria af te leiden die starten van een behandeling kunnen sturen. Keuze tussen verschillende preparaten insuline kan op basis van geraadpleegde studies niet worden gemaakt.
Bij CFRD heeft insulinebehandeling aantoonbaar positief effect op klinische CF parameters. Bij patiënten met CF-IGT is dit positieve effect niet goed onderzocht. Het ligt echter voor de hand dat bij patiënten met CF-IGT, waarvan beschreven is dat dit tot verslechtering leidt van klinische CF parameters, insuline behandeling ook tot klinische verbetering zal leiden. Bij patiënten met IGT en klinische exacerbaties kan tijdelijke intensivering van insuline behandeling nodig zijn. De voordelen van insulinebehandeling zijn de beschreven positieve effecten, nadelen zijn de invasieve route en de belasting die het voor patiënten is om zowel insuline te spuiten als de daarbij behorende bloedglucosemetingen te verrichten. Voordeel van de orale medicamenten is de eenvoudiger toedieningsroute.
Wat vinden patiënten: patiëntenvoorkeur
Het is uit de literatuur niet bekend wat patiënten vinden van glucose behandeling en hoe ze dat zouden willen vormgeven. De praktijk laat zien dat het veeleer de patiënten zwaar valt dát ze iets moeten gaan doen met suikermetabolisme en minder wát gedaan moet worden. Het ligt voor de hand te veronderstellen dat patiënten orale behandeling prefereren boven injecties. Aan de andere kant kan orale behandeling met meerdaags tabletten soms ook weer extra belastend zijn. Afspraken over de soort behandeling dienen dus samen met de patiënt te worden gemaakt waarbij diens voorkeuren worden betrokken.
Wat vinden artsen: professioneel perspectief
In de literatuur werd geen overtuigend bewijs gevonden dat een bepaald type insuline, of insuline in het algemeen of orale behandeling superieur is boven een andere behandelmodaliteit. De meeste ervaring is opgedaan met insuline, en de meeste clinical guidelines adviseren insuline als eerste behandeloptie. Met hulp van CGM kan de insuline goed getarget en geïndivualiseerd worden. Aandachtspunt bij een eventuele orale behandeling is het bijwerkingen profiel dat bij patiënten met CF kritisch beoordeeld dient te worden. De internationale ECSF-consensus raadt gebruik van repaglinide, ondanks dat er aanwijzingen zijn dat dit vergelijkbare effecten heeft op klinische CF-uitkomsten, niet aan. De werkgroep concludeert dat insuline behandeling van keuze is, en dat voor het gebruik van additionele middelen nog onvoldoende evidence en ervaring is om in deze kwaliteitsstandaard op te nemen.
Tevens is een relevant perspectief te bestuderen wat de impact is van CFTR-modulatoren op glucosehuishouding bij CF.
Kosten
Kosten voor behandeling met insuline of repaglinide zijn niet duidelijk, maar zullen niet tot grote zorgkosten leiden. De opbrengst die wordt beoogd, namelijk mitigatie van verslechtering van de klinische situatie met betrekking tot groei/ontwikkeling/longfunctie is lastig te substantiëren.
Haalbaarheid
Zowel insulinebehandeling als behandeling met orale preparaten zijn haalbaar. Wel dient hiervoor goede samenwerking te bestaan tussen gespecialiseerde diabetes-behandelaren en gespecialiseerde CF zorg.
Onderbouwing
Problemen met de glucose stofwisseling hebben invloed op het klinisch beloop van CF. Tijdige onderkenning en behandeling is daarom essentieel. Goede criteria voor starten van insulinebehandeling (timing en type) zijn niet voorhanden en dus is er grote praktijkvariatie. Integratie van goede diabeteszorg in de behandeling van CF heeft ook organisatorische implicaties voor behandelcentra.
I. Insuline versus geen medicatie
|
Zeer laag GRADE |
Het is onzeker of er een verschil in effect is op verandering in glykemische controle (HbA1c) bij patiënten met CFRD van een insulinebehandeling vergeleken met geen medicatie na 12 maanden.
Bronnen: (Onady 2016; Moran, 2009) |
I. Insuline versus geen medicatie
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op de verandering in longfunctie (FEV1% en FVC) bij patiënten met CFRD van een insulinebehandeling vergeleken met geen medicatie na 12 maanden.
Bronnen: (Onady 2016; Moran, 2009) |
I. Insuline versus geen medicatie
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in BMI bij patiënten met CFRD van een insulinebehandeling vergeleken met geen medicatie na 12 maanden.
Bronnen: (Onady 2016; Moran, 2009) |
I. Insuline versus geen medicatie
|
Laag GRADE |
Er lijkt niet of nauwelijks verschil in effect te zijn op het aantal hypoglykemieën bij patiënten met CFRD van een insulinebehandeling vergeleken met geen medicatie in de eerste 2 tot 3 maanden.
Bronnen: (Onady 2016; Moran, 2009; Moran, 2001) |
I. Insuline versus geen medicatie
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het effect op kwaliteit van leven bij patiënten met CFRD van een insulinebehandeling vergeleken met geen medicatie over tijd.
Bronnen: (Onady, 2016; Moran, 2009; Moran, 2001) |
I. Orale repaglinide versus placebo
|
Zeer laag GRADE |
Het is onzeker of er een verschil in effect is op verandering in Glykemische controle (HbA1c) bij patiënten met CFRD van een repaglinide behandeling vergeleken met een placebobehandeling na 12 maanden.
Bronnen: (Onady, 2016; Moran, 2009) |
II. Orale repaglinide versus placebo
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in longfunctie (FEV1% en FVC) bij patiënten met CFRD van een repaglinide behandeling vergeleken met een placebobehandeling na 12 maanden.
Bronnen: (Onady, 2016; Moran, 2009) |
II. Orale repaglinide versus placebo
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in BMI tussen bij patiënten met CFRD van een repaglinide behandeling vergeleken met een placebobehandeling na 12 maanden.
Bronnen: (Onady, 2016; Moran, 2009) |
II. Orale repaglinide versus placebo
|
Laag GRADE |
Er lijkt niet of nauwelijks een verschil in effect te zijn op het aantal hypoglykemieën bij patiënten met CFRD van een repaglinide behandeling vergeleken met een placebobehandeling in de eerste 3 maanden.
Bronnen: (Onady, 2016; Moran, 2009) |
II. Orale repaglinide versus placebo
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het effect op kwaliteit van leven bij patiënten met CFRD van een repaglinide behandeling vergeleken met een placebobehandeling.
Bronnen: (Onady, 2016; Moran, 2009) |
III. Insuline versus orale repaglinide
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in Glykemische controle (HbA1c) bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling na 12 en 24 maanden.
Bronnen: (Onady, 2016; Ballman, 2014; Moran, 2009) |
III. Insuline versus orale repaglinide
|
Zeer laag GRADE |
Het is onzeker of er een verschil in effect is op verandering in Glykemische controle (post-prandiale glucose levels) bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling twee en vijf uur na de maaltijd.
Bronnen: (Moran, 2009; Moran, 2001) |
III. Insuline versus orale repaglinide
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in longfunctie (FEV1%) bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling na 12 en 24 maanden.
Er lijkt geen effect te zijn op verandering in longfunctie (FVC) bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling na 12 maanden.
Bronnen: (Onady, 2016; Ballman, 2014; Moran, 2009) |
III. Insuline versus orale repaglinide
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op verandering in BMI tussen bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling na 12 maanden.
Er lijkt een klein positief verschil in effect te zijn op verandering in BMI z-scores tussen bij patiënten met CFRD op insuline vergeleken met een repaglinide behandeling na 12 maanden. Dit effect is verdwenen na 24 maanden.
Bronnen: (Onady, 2016; Ballman, 2014; Moran, 2009) |
III. Insuline versus orale repaglinide
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op het aantal hypoglykemieën bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling in de eerste 3 maanden.
Bronnen: (Onady, 2016; Moran, 2009) |
III. Insuline versus orale repaglinide
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het effect op kwaliteit van leven bij patiënten met CFRD van insuline vergeleken met een repaglinide behandeling.
Bronnen: (Onady, 2016; Moran, 2009) |
IV. NPH-Insuline versus glargine
|
Laag GRADE |
Er lijkt niet of nauwelijks een verschil in effect te zijn op verandering in glykemische controle (glucose levels nuchter en twee uur post-prandiaal) patiënten met CFRD van glargine vergeleken met NPH-insuline na 3 maanden.
Bronnen: (Onady, 2016; Grover, 2008) |
IV. NPH-Insuline versus glargine
|
Laag GRADE |
Er lijkt geen verschil effect te zijn op verandering in gewicht (in kg) bij patiënten met CFRD van glargine vergeleken met NPH-insuline na 3 maanden.
Bronnen: (Onady, 2016; Grover, 2008) |
IV. NPH-Insuline versus glargine
|
Laag GRADE |
Er lijkt geen verschil in effect te zijn op het aantal hypoglykemische events per patiënt bij patiënten met CFRD van glargine vergeleken met NPH-insuline na 3 maanden.
Bronnen: (Onady, 2016; Grover, 2008) |
IV. NPH-Insuline versus glargine
|
Zeer laag GRADE |
Het is onzeker of er een verschil is in het effect op kwaliteit van leven bij patiënten met CFRD van glargine vergeleken met NPH-insuline.
Bronnen: (Onady, 2016; Grover, 2008) |
Beschrijving studies
De systematische Cochrane literatuurreview van Onady (2016) onderzocht de effectiviteit van insuline en orale preparaten als behandeling voor CFRD. Er is tot april 2016 gezocht naar randomized controlled trial (RCT) studies die verschillende typen behandelingen voor CFRD met elkaar vergeleken. Er waren vier RCT’s in de systematische review geïncludeerd (Ballman, 2014; Grover, 2008; Moran, 2009 en Moran, 2001).
In de open-label RCT van Ballman (2014) werden 73 patiënten geïncludeerd met een gemiddelde leeftijd van 22,2 ± 8,8 jaar. Alle patiënten hadden CFRD vastgesteld door een OGTT-test volgens WHO standaarden. Eén groep ontving insuline (start 0,05 eenheid insuline/kg injecties 3 dd) en dit werd wekelijks opgebouwd tot een optimale dosis en vergeleken met een groep die orale repaglinide (start 0,5 mg orale rapaglinide 3 dd) ontving met een opbouwend wekelijks schema tot maximaal 12 mg per dag, maximaal 3dd 4mg. Patiënten werden gevolgd voor 24 maanden (Ballman, 2014).
De cross-over RCT van Grover, 2008, includeerde 20 patiënten, met een gemiddelde leeftijd van 34±8 jaar. Alle patiënten hadden CFRD met nuchtere hyperglykemie. Patiënten werden niet geblindeerd voor de volgorde van behandeling. De resultaten uit het cross-over design konden niet worden meegenomen, en zijn uiteindelijk geanalyseerd als een parallel RCT. Deze benadering geeft conservatieve resultaten en de groepen zijn niet onafhankelijk van elkaar omdat dezelfde patiënten in de interventie en controle groep deelnemen. Een groep met een behandeling met neutral protamine Hagedorn (NPH) insuline werd vergeleken met een groep die glargine insuline ontving. Doseringen werden individueel bepaald op basis van een insuline: koolhydraat ratio en een correctieschaal. Patiënten werden gevolgd voor 12 weken (Grover, 2008).
Moran (2009) voerde een RCT uit met drie interventiearmen met in totaal 100 patiënten met een gemiddelde leeftijd van 28 ± 9 jaar. 81 patiënten voltooiden de studie waarvan 61 met CFRD en 20 met glucose intolerantie, allen zonder nuchtere hyperglykemie. Patiënten werden geblindeerd voor de orale toedieningen, niet voor de insuline toediening. Insuline (0,5 eenheid insuline aspart/15 gram koolhydraat) (n=38), 2,0 mg orale repaglinide (n=32) en een orale placebo (n=30) werden met elkaar vergeleken. De dosering voor repaglinide werd voor vier patiënten verlaagd, ten opzichte van twee patiënten in de insulinegroep. Patiënten werden gevolgd voor 12 maanden (Moran, 2009).
In een cross-over RCT met drie interventiearmen van Moran (2001) werden 7 patiënten geïncludeerd met een gemiddelde leeftijd van 24 ± 5 jaar. Patiënten met CFRD zonder nuchtere hyperglykemie werden geïncludeerd Patiënten werden niet geblindeerd voor de volgorde van behandeling. Insuline (0,1 unit/kg), 1,0 mg orale repaglinide en geen medicatie werden met elkaar vergeleken. Patiënten werden gevolgd voor 1 tot 2 maanden (Moran, 2001).
Resultaten
Vier verschillende vergelijkingen (I, II, III, IV) zijn gerapporteerd in de systematische literatuurreview van Onady (2016) voor de uitkomstmaten; glykemische controle, longfunctie, voedingsstatus, hypoglykemie en kwaliteit van leven.
I. Insuline versus no medication
Glykemische controle (HbA1c)
Er waren geen significante verschillen in HbA1C levels tussen beide groepen na 12 maanden. De precieze data is niet gerapporteerd (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat HbA1C is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Longfunctie (FEV1% en FVC)
Er waren geen significante verschillen in de verandering in FEV1% en FVC na twaalf maanden tussen de insulinebehandeling en de placebobehandeling. Het gemiddeld verschil was voor FEV1% 1,20 (95% Betrouwbaarheidsinterval (BI) -5,63 tot 8,03) en voor FVC 0,60 (95% BI -5,67 tot 6,87) in het voordeel van de insulinebehandeling (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat longfunctie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Voedingsstatus (BMI)
Er was geen significant verschil in de verandering in BMI na twaalf maanden tussen de insulinebehandeling en de placebobehandeling. Het gemiddeld verschil was 0,41 (95% BI -0,23 tot 1,05) in het voordeel van de insulinebehandeling (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat voedingsstatus is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Hypoglykemie
Er was geen significant verschil in het voorkomen van hypoglykemie na 2 of 3 maanden tussen de insulinebehandeling en de placebobehandeling. Moran (2001) rapporteerde in 2/7 patiënten een milde hypoglykemie na insulinebehandeling en geen hypoglykemie na de placebobehandeling na twee maanden. Moran (2009) rapporteerde in 5/30 van de patiënten in de insulinegroep in de eerste drie maanden een hypoglykemie vergeleken met 0/25 in de placebogroep. Na drie maanden was er geen verschil tussen de groepen.
Relatieve risico’s (RR) werden gerapporteerd van RR 9,23 (95% BI 0,5 tot 159,1) (Moran, 2009) en RR 2,00 (95% BI 0,2 tot 17,3) (Moran, 2001), met een niet significante hogere kans op hypoglykemie in de insulinegroep, maar een zeer breed betrouwbaarheidsinterval. Moran (2009) geeft niet aan of de hypoglykemie voorvallen bij patiënten voorkwamen met CFRD of glucose intolerantie (Moran, 2001; Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypoglykemie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Kwaliteit van leven
Er waren geen verschillen in gezondheid gerelateerde kwaliteit van leven (HRQoL) tussen beide groepen over tijd (Moran, 2009; Moran, 2001). De precieze data is niet gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
II. Orale repaglinide versus Placebo
Glykemische controle (HbA1c)
Er waren geen significante verschillen in HbA1C levels tussen beide groepen na 12 maanden. De precieze data is niet gerapporteerd (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat HbA1C is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Longfunctie (FEV1% en FVC)
Er waren geen significante verschillen in de verandering in FEV1% en FVC na twaalf maanden tussen de repaglinide behandeling en de placebobehandeling. Het gemiddeld verschil was voor FEV1% 1,7 (95% BI -5,1 tot 8,5) in het voordeel van de repaglinide behandeling en voor FVC -1,0 in het voordeel van de placebobehandelng (95% BI -7,4 tot 5,4) (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat longfunctie (FEV1% en FVC) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; exclusie van patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Voedingsstatus (BMI)
Er was geen significant verschil in de verandering in BMI na twaalf maanden tussen de repaglinide behandeling en de placebobehandeling. Het gemiddeld verschil was 0,17 (95% BI -0,47 tot 0,81), in het voordeel van de repaglinide behandeling (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat voedingsstatus (BMI) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; exclusie van diabetische patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Hypoglykemie
Moran (2009) rapporteerde in 6/26 patiënten in de insulinegroep in de eerste drie maanden een milde hypoglykemie vergeleken met 0/25 in de placebogroep. Na drie maanden was er geen verschil tussen de groepen.
Een relatief risico van 12,52 (95% BI 0,74 tot 211,20) werd berekend met een niet significante hogere kans op hypoglykemie in de repaglinide groep, maar een zeer breed betrouwbaarheidsinterval. Moran (2009) geeft niet aan of de hypoglykemie voorvallen bij patiënten voorkwamen met CFRD of glucose intolerantie (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypoglykemie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; exclusie van patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Kwaliteit van leven
Er waren geen verschillen in gezondheid gerelateerde kwaliteit van leven (HRQoL) tussen beide groepen over tijd (Moran, 2009). De precieze data is niet gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; exclusie van diabetische patiënten met een nuchtere hyperglykemie, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
III. Insuline versus orale repaglinide
Glykemische controle (HbA1c)
Er waren geen significante verschillen in de verandering in HbA1c na 12 en 24 maanden. Het gemiddeld verschil tussen de insuline en orale repaglinide behandeling was respectievelijk -0,09 (95% BI -0,53 tot 0.35) in het voordeel van de insuline behandeling en 0,40 (95% BI -0,08 tot 0,88) in het voordeel van de repaglinide behandeling (Ballman, 2014). Moran (2009) gaf ook aan dat er geen significant verschil was in de verandering van HbA1c na 12 maanden, er werden geen effect of spreidingsmaten gerapporteerd (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat glykemische controle (HbA1c) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie en verschil in optimale dosering tussen groepen) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Longfunctie (FEV1% en FVC)
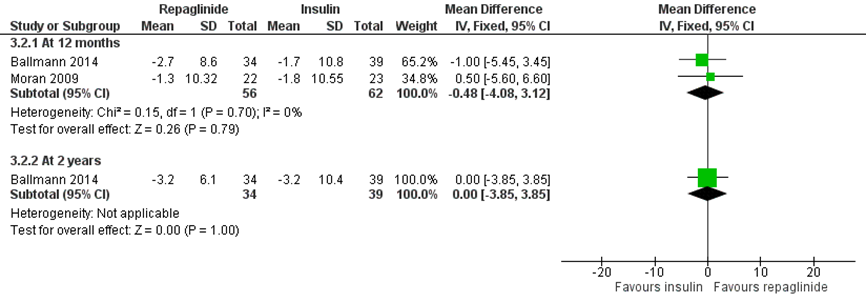
Er was geen significant verschil in de verandering in FEV1% na twaalf maanden tussen de insuline en repaglinide behandeling. Het gepoolde gemiddeld verschil was -0,48 (95% CI -4,08 tot 3,12) in het voordeel van de insulinebehandeling, p=0,79, fixed model, I2=0% (zie figuur 1) (Ballman, 2014; Moran, 2009). In de studie van Ballman (2014) werd er een langere follow-up periode van 24 maanden aangehouden, hier werd ook geen significante verandering gevonden in FEV1%, het gemiddeld verschil was 0,00 (95% BI -3,85 tot 3,85).
Moran (2009) vond ook geen significant verschil tussen de groepen in verandering in FVC, met een gemiddeld verschil van -1,60 (95% CI -7,28 tot 4,08) in het voordeel van de insuline behandeling na 12 maanden.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat longfunctie (FEV1% en FVC) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie en verschil in optimale dosering tussen groepen) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Figuur 1 Forestplot voor longfunctie gemeten middels verandering in FEV1 (% voorspeld) na twaalf maanden, vergelijking tussen insuline en orale repaglinide verandering
Voedingsstatus (BMI en BMI z-scores)
Er was geen significant verschil in de verandering in BMI na twaalf maanden tussen de insuline en repaglinide behandeling. Het gemiddeld verschil was 0,24 (95% BI -0,34 tot 0,82) (Moran, 2009). Ballman (2014) vond na 12 maanden een significant verschil in verandering in de BMI z-scores tussen de groepen met een gemiddeld verschil in BMI verandering van -0,27 (95% CI -0,45 tot -0,09) in het voordeel van de insuline behandeling, dit verschil was niet meer significant na 24 maanden, -0.21 (95% CI -0,45 tot -0,03).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat voedingsstatus (BMI en BMI z-scores) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie en verschil in optimale dosering tussen groepen) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Hypoglykemie
Moran (2009) rapporteerde in 6/26 patiënten in de insulinegroep in de eerste drie maanden een milde hypoglykemie vergeleken met 5/25 in de placebogroep.
Een relatief risico van 1,38 (95% BI 0,48 tot 4,01) werd berekend met een niet significante hogere kans op hypoglykemie in de repaglinide groep. Moran geeft niet aan of de hypoglykemie voorvallen bij patiënten voorkwamen met CFRD of glucose intolerantie (Moran, 2009).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat hypoglykemie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Kwaliteit van leven
Er waren geen verschillen in gezondheid gerelateerde kwaliteit van leven (HRQoL) tussen beide groepen over tijd (Moran, 2009). De precieze data is niet gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van diabetische patiënten met een nuchtere hyperglykemie, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
IV. NPH Insuline versus glargine
Glykemische controle (Glucose levels nuchter en twee uur post-prandiaal)
Grover (2008) berekende het gemiddelde verschil in glucose levels (mg/dl) nuchter en twee uur post-prandiaal na een follow-up periode van drie maanden. Er waren geen significante verschillen in de veranderingen van de glucoselevels voor beide momenten. Het gemiddeld verschil in nuchtere glucoselevels tussen de NPH insuline en glargine behandeling na drie maanden was respectievelijk 10,00 (-12,86 tot 32,86) in het voordeel van de glargine behandeling. Het gemiddeld verschil in 2 uur postprandiale glucoselevels tussen de NPH insuline en glargine behandeling was respectievelijk 8,00 (-10,07 tot 26,07) in het voordeel van de glargine behandeling (Grover, 2008).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat glykemische controle (glucose levels nuchter en twee uur post-prandiaal) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van patiënten met diabetische bloedsuikerwaardes en cross-over trial kon alleen als parallel trial worden geanalyseerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Voedingsstatus (gewicht)
Er was geen significant verschil in de verandering in gewicht in kilogrammen na drie maanden tussen de NPH insuline en glargine behandeling. Het gemiddeld verschil was -1,00 (95% BI -2,39 tot 0,39) in het voordeel van de glargine behandeling (Grover, 2008).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat voedingsstatus (verschil in gewicht) is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van patiënten met diabetische bloedsuikerwaardes en cross-over trial kon alleen als parallel trial worden geanalyseerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘laag’.
Hypoglykemie
Grover (2008) rapporteerde gemiddeld 5 ± 4.36 milde hypoglykemische events per patiënt in de NPH insulinegroep in de eerste drie maanden en 6 ± 4.36 in de glargine groep.
Een gemiddeld verschil van -1,00 (95% BI -3,77 tot 1,77) in het voordeel van NPH-insuline, dit verschil is niet significant.
Kwaliteit van leven
Er waren geen significante verschillen in gezondheid gerelateerde kwaliteit van leven (HRQoL) tussen beide groepen over tijd (Grover, 2008). De precieze data is niet gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; blindering, exclusie van patiënten met diabetische bloedsuikerwaardes en cross-over trial kon alleen als parallel trial worden geanalyseerd, geen data gepresenteerd) en het geringe aantal patiënten (imprecisie). Het niveau van de bewijskracht komt uit op GRADE ‘zeer laag’.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat zijn de (on)gunstige effecten van een behandeling met insuline of orale antidiabetische medicatie, vergeleken met een andere behandeling, bij een afwijkende screening van glucose metabolisme in patiënten met CF?
P (Patiënten): patiënten met CF en afwijkende screening van glucose metabolisme;
I (Interventie): behandeling met insuline of orale anti-diabetische medicatie;
C (Comparison): placebo, geen of andere behandeling;
O (Outcomes): growth; target height; lung function; HbA1c; weight; weight for height, BMI; glucose variability; microvascular complications; lung infection; deterioration lung function; lung function improvement; quality of life; anabolism; body composition; antibiotic need/use.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 27 juli 2017 met relevante zoektermen gezocht naar Engelstalige systematische reviews, gerandomiseerde gecontroleerde studies (RCT’s), gecontroleerde klinische studie (CCT’s) en vergelijkend observationeel onderzoek gepubliceerd vanaf 1987 gericht op de (on)gunstige effecten van een behandeling met insuline bij een afwijkende glucose metabolisme in patiënten met. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 315 treffers op. Vergelijkend onderzoek over de (on)gunstige effecten van insuline vergeleken met een ander type behandeling in CF-patiënten werd geïncludeerd. Op basis van titel en abstract werden in eerste instantie 31 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 30 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en 1 studie definitief geselecteerd.
Eén systematische literatuurreview is opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Onady GM, Stolfi A. Insulin and oral agents for managing cystic fibrosis-related diabetes. Cochrane Database Syst Rev. 2016 Apr 18;4:CD004730.doi: 10.1002/14651858.CD004730.pub4.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Onady, 2016 |
Yes |
Yes |
Yes |
Yes |
NA |
Yes |
NA, most outcomes could not be pooled |
No |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Yi (2016) |
Vergelijkende groep bestaat uit patiënten zonder CF |
|
Pu (2016) |
Beschrijvende niet vergelijkende studie |
|
Coriati (2016) |
Studie naar de associatie tussen bloed glucose waarden en verschillende klinische uitkomsten. |
|
Wooldridge (2015) |
Studie naar de insuline secretie in patiënten met cystic fibrosis |
|
Merjaneh (2015) |
Vergelijkend onderzoek waarbij niet-CF patiënten als controlegroep worden gebruikt. |
|
Hameed (2015) |
Beschrijvende review |
|
Wickens-Mitchell (2014) |
Vergelijkend onderzoek naar de verschillen in protocollen tussen ziekenhuizen. |
|
Scheuing (2014) |
Vergelijkend onderzoek naar de variabiliteit van de glucosewaarden in patiënten met Cystic Fibrosis. |
|
Rayas (2014) |
Vergelijkend onderzoek naar het effect van algoritmen op de compliance aan CF-richtlijnen. |
|
Middleton (2014) |
Richtlijn |
|
Leclerq (2014) |
Vergelijkend onderzoek naar CGM profiel in patiënten met normale OGTT screening. |
|
Ballmann (2014) |
Onderdeel van systematische review Onady (2016) |
|
Bellin (2013) |
Beschrijvende niet vergelijkende studie |
|
Minicucci (2012) |
Letter to the editor |
|
Hameed (2015) |
Beschrijvende review |
|
Rana (2011) |
Vergelijkend onderzoek naar het verschil in incidentie en de bijbehorende demografische en klinische kenmerken tijdens diagnose. |
|
Raman (2011) |
Studie naar de risicofactoren gerelateerd aan hyperglycemia en diabetes mellitus. |
|
Sterescu (2010) |
Onderzoek naar de glucose homeostase in CF-patiënten |
|
Moran (2010) |
Richtlijn |
|
Hameed (2010) |
Vergelijkend onderzoek naar de associatie tussen bloedglucose waarden en gezondheidsuitkomsten |
|
Frohnert (2010) |
Studie naar de associatie tussen bloed glucose waarden en klinische status |
|
Moran (2009) |
Onderdeel van systematische review Onady (2016) |
|
Hardin (2009) |
Vergelijking data baseline en follow-up |
|
Grover (2008) |
Onderdeel van systematische review Onady (2016) |
|
Elder (2007) |
Studie naar de prevalentie van abnormaliteiten in glucose metabolisme onder CF-patiënten |
|
Onady (2006) |
Case studie |
|
Mueller (2005) |
Beschrijvende niet vergelijkende studie |
|
Rosenecker (2001) |
Studie naar de klinische paramaters van diabetes |
|
Moran (2001) |
Onderdeel van systematische review Onady (2016) |
|
Finkelstein (1988) |
Vergelijkende groep zijn patiënten zonder CF |
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-07-2020
Beoordeeld op geldigheid : 28-10-2019
Voor het beoordelen van de actualiteit van deze kwaliteitsstandaard is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepalen de besturen van de NVALT, NVK en NCFS of de modules van deze kwaliteitsstandaard nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de kwaliteitsstandaard heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de kwaliteitsstandaard komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVALT, NVK en NCFS zijn regiehouders van deze Kwaliteitsstandaard en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de modules. De andere aan deze kwaliteitsstandaard deelnemende wetenschappelijke verenigingen of gebruikers van de kwaliteitsstandaard delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module |
Regiehouder(s) |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn |
Frequentie van beoordeling op actualiteit |
Wie houdt er toezicht op actualiteit |
Relevante factoren voor wijzigingen in aanbeveling |
|
Behandeling CFRD |
NVK en NVALT |
2020 |
2025 |
Eens in de vijf jaar |
NVK en NVALT |
Beschikbaarheid nieuwe middelen en literatuur |
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Landelijke Vereniging Medische Psychologie
- Nederlands Instituut van Psychologen
- Nederlandse Vereniging van Diëtisten
De ontwikkeling van de medisch inhoudelijke modules binnen deze Kwaliteitsstandaard werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De module over psychosociale zorg en de organisatie van zorg modules werden ondersteund vanuit de Samenwerkende Ouder- en Patiëntenorganisaties (VSOP) en gefinancierd vanuit ZonMW. De financierders hebben geen enkele invloed gehad op de inhoud van de kwaliteitsstandaard.
Doel en doelgroep
Doel
Het tot stand brengen van een evidence-based kwaliteitsstandaard Cystic Fibrosis, een combinatie van een zorgstandaard en een medisch specialistische richtlijn om patiënten met Cystic Fibrosis optimale afgestemde zorg te bieden.
Doelgroep
De doelgroep zijn alle patiënten met Cystic Fibrosis. De kwaliteitsstandaard behelst de gebieden van diagnostiek, behandeling en follow-up conform de diverse stadia van de aandoening en de verschillende leeftijdscategorieën.
Samenstelling werkgroep
Voor het ontwikkelen van de kwaliteitsstandaard is in 2016 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met CF en vertegenwoordigers van de NCFS.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze kwaliteitsstandaard.
Werkgroep
- Drs. G.D. (George) Nossent, longarts, UMCG te Groningen, NVALT (voorzitter)
- Dr. O.W. (Onno) Akkerman, longarts, UMCG te Groningen, NVALT
- S. (Sigrid) Amstelveen-Bökkerink, diëtist, Radboud UMC te Nijmegen, NVD
- Dr. H.G.M. (Bert) Arets, kinderlongarts, Wilhelmina Kinderziekenhuis en UMC Utrecht te Utrecht, NVK
- Dr. M. (Marleen) Bakker, longarts, Erasmus MC te Rotterdam, NVALT
- Drs. J.M.W. (Annemarie) van den Berg, longarts, Hagaziekenhuis te Den Haag, NVALT
- Dr. M.C. (Maaike) Berkhout, KNO arts, OLVG te Amsterdam, NVKNO
- Dr. F.A.J.A. (Frank) Bodewes, kinderarts-MDL, UMCG te Groningen, NVK
- A. (Annet) Bongen, maatschappelijk werker, UMC Utrecht te Utrecht, BPSW
- J. (Jacqueline) Boekhoff, maatschappelijk werker, Amsterdam UMC, locatie VUMC te Amsterdam, BPSW
- Drs. L.H. (Hassan) el Bouzzaoui, longarts, Hagaziekenhuis te Den Haag, NVALT
- D. (Dagmar) Brocke, maatschappelijker werker, UMC Utrecht te Utrecht, BPSW
- Drs. E.J. Brokaar, poliklinisch apotheker, Hagaziekenhuis te Den Haag, NVZA
- Dr. I. (Inez) Bronsveld, longarts, UMC Utrecht te Utrecht, NVALT
- Drs. A. (Agnes) Clement-de Boer, kinderarts (endocrinologie), Hagaziekenhuis te Den Haag, NVK
- W. (Wytze) Doeleman, fysiotherapeut, UMC Utrecht te Utrecht, KNFG
- Dr. M.M. (Menno) van der Eerden, longarts, Erasmus MC te Rotterdam, NVALT
- Prof. Dr. C.K. (Kors) van der Ent, Kinderlongarts, Wilhelmina Kinderziekenhuis en UMC Utrecht te Utrecht, NVK
- Dr. B.C.T. (Boudien) Flapper, kinderarts-sociale pediatrie, UMCG te Groningen, NVK
- Dr. L. (Lianne) van der Giessen, kinderfysiotherapeut, Erasmus MC Sophia Kinderziekenhuis te Rotterdam, KNGF
- Drs. N. (Nanko) de Graaf, kinderradioloog, Erasmus MC te Rotterdam, NVvR
- Dr. V. (Vincent) Gulmans, Hoofd Onderzoek en Kwaliteit van zorg NCFS te Baarn, NCFS
- Prof. dr. H.G.M. (Harry) Heijerman, longarts, UMC Utrecht te Utrecht, NVALT
- Drs. D.M. (Danielle) Hendriks, kinderarts (MDL), Juliana Kinderziekenhuis te Den Haag, NVK
- Dr. J.J.E. Hendriks, kinderlongarts, Zuyderland Medisch Centrum te Heerlen, NVK
- Prof. dr. B. (Bart) van Hoek, MDL-arts, UMC te Leiden, NVMDL
- Drs. R.A.S. (Rogier) Hoek, longarts, Erasmus MC te Rotterdam, NVALT
- Dr. A. (Ageeth) Hofsteenge, kinderdiëtist, Amsterdam UMC, locatie VUMC en AMC, te Amsterdam, NVD
- Drs. C. (Chantal) Hoge, MDL arts, Maastricht UMC+ te Maastricht, NVMDL
- F.M. (Francis) Hollander, diëtist, UMC Utrecht, Utrecht, NVD
- Prof. dr. R.H.J. (Roderick) Houwen, kinderarts MDL, Wilhelmina Kinderziekenhuis en UMC Utrecht te Utrecht, NVK
- Dr. J. (Jakko) van Ingen, arts microbioloog, Radboud UMC te Nijmegen, NVMM
- Dr. H.M. (Hettie) Janssens, (kinder)longarts, Erasmus MC Sophia Kinderziekenhuis te Rotterdam, NVK
- Drs. A.J. (Arjan) Jansz, arts microbioloog, Stichting PAMM te Eindhoven, NVMM
- H.J. (Hetty) van der Kamp, kinderarts-endocrinoloog, HMC Bronovo te Den Haag en Wilhelmina Kinderziekenhuis UMC Utrecht te Utrecht, NVK
- C. (Cora) de Kiviet, verpleegkundig specialist, Wilhelmina Kinderziekenhuis en UMC Utrecht te Utrecht, V&VN
- A. (Annelies) Kok, verpleegkundig consulent, Erasmus MC te Rotterdam, CF Netwerk verpleegkundigen Nederland
- Dr. B.G.P. (Bart) Koot, kinderarts (MDL), Amsterdam UMC, locatie AMC te Amsterdam, NVK
- M.A. (Marian) Kruijswijk, verpleegkundig specialist, UMC Utrecht te Utrecht, V&VN
- Dr. C.J. (Christof) Majoor, longarts, Amsterdam UMC, locatie AMC te Amsterdam, NVALT
- R. (Renske) van der Meer, longarts, Hagaziekenhuis te Den Haag, NVALT
- Dr. P.J.F.M. (Peter) Merkus, kinderlongarts, Radboud MC te Nijmegen, NVK
- Dr. D. (Dick) Mul, kinderarts (endocrinologie), Diabeter te Rotterdam, NVK
- Drs. A.F. (Ad) Nagelkerke, kinderlongarts, Amsterdam UMC, locatie VUmc te Amsterdam, NVK
- drs. J. (Jacquelien) Noordhoek, directeur patiëntenorganisatie NCFS te Baarn, NCFS
- Marit van Oirschot-van de Ven, verpleegkundig specialist, UMC Utrecht te Utrecht, V&VN
- Dr. M (Marianne) Nuijssink, kinderlongarts, Haga ziekenhuis te Den Haag, NVK
- Dr. M.H.E. (Monique) Reijers, longarts, Radboudumc te Nijmegen, NVALT
- Dr. S. (Sietze) Reitsma, KNO-arts, Amsterdam UMC, locatie AMC te Amsterdam, NVKNO
- Prof. dr. Y.B. (Yolanda) de Rijke, afdelingshoofd Klinische Chemie, Erasmus MC te Rotterdam, NVKC
- Dr. B.L. (Bart) Rottier, kinderlongarts, UMCG te Groningen, NVK
- R.A. (Revka) Schrijver, verpleegkundig consulent, Hagaziekenhuis te Den Haag, CF Netwerk verpleegkundigen Nederland
- Drs. L. (Luciënne) Speleman, KNO arts, Wilhelmina Kinderziekenhuis en UMC Utrecht, te Utrecht, NVKNO
- Dr. S.W.J. (Suzanne) Terheggen-Lagro, kinderlongarts, Amsterdam UMC, locatie AMC te Amsterdam, NVK
- Prof. dr. H.A.W.M (Harm) Tiddens, (kinder)longarts, Erasmus MC Sophia Kinderziekenhuis te Rotterdam, NVK
- H. (Hilda) Vale-Eeman, kinderverpleegkundige, Amsterdam UMC, locatie AMC te, Amsterdam, V&VN
- Dr. H. (Hester) van der Vaart, longarts UMCG te Groningen, NVALT
- Dr. H.W. (Harold) de Valk, internist-endocrinoloog UMCU te Utrecht, NIV
- Dr. M. (Marieke) Verkleij, GZ-psycholoog/cognitief gedragstherapeut, Amsterdam UMC, locatie VUMC te Amsterdam, VGCT
- Dr. E.J.M. (Els) Weersink, longarts, Amsterdam UMC, locatie AMC te Amsterdam, NVALT
- M. (Marion) Wessels, Verpleegkundige, UMC Utrecht te Utrecht, V&VN
- Dr. B.J. (Barbara) Wijnberg-Williams, klinisch psycholoog, UMCG te Groningen en Isala Ziekenhuis te Zwolle, NIP
- Dr. K.M. (Karin) de Winter- de Groot, kinderlongarts, Wilhelmina Kinderziekenhuis en UMC Utrecht te Utrecht, NVK
- Dr. P.J.G. (Petra) Zwijnenburg, klinisch geneticus, Amsterdam UMC, locatie VUMC te Amsterdam, VKGN
Met ondersteuning van
- Dr. F. (Floor) Willeboordse, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Ir. T. (Teus) van Barneveld, directeur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. A. (Anne) Speijer, coördinator kwaliteit van zorg, VSOP
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Drs. G.D. (George) Nossent (voorzitter) |
Longarts UMCG |
Bestuurslid NVALT |
Geen |
Geen actie |
|
O. Akkerman |
Longarts, fulltime, UMCG |
Lid nascholingscommissie VvAwT; onbetaald Lid visitatieteam TBC screening LRCB; onbetaald |
Geen |
Geen actie |
|
S. Amstelveen-Bokkerink |
Diëtist Radboudumc Dekkerswald |
Geen |
Geen |
Geen actie |
|
B. Arets |
Kinderlongarts, UMC Utrecht |
Academisch kinder(long)arts, deels Associate Professor Medisch Onderwijs Universiteit.
|
|
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is. |
|
M. Bakker |
Longarts, Erasmus MC Rotterdam |
Geen |
Deelname aan diverse studies Vertex (chloortransportmodulatoren) |
Geen trekker van module CFTR modulatoren (wel meelezer).
Toelichting op onderzoek gesponsord door Vertex: Betrokken bij inclusie van patiënten en dataverzameling. Niet betrokken bij data-analyse, wel principal investigator, geen auteur. |
|
T. van Barneveld |
Directeur Kennisinstituut Federatie Medisch Specialisten |
|
Geen |
Geen actie |
|
A. van den Berg |
Longarts Hagaziekenhuis Den Haag |
Geen |
Geen |
Geen actie |
|
M. Berkhout |
KNO-arts in opleiding in het Academisch Medisch Centrum Amsterdam. Opleider: Prof. dr. F.G. Dikkers |
Geen |
Geen |
Geen actie |
|
F. Bodewes |
Kinderarts-MDL UMC Groningen |
Geen |
Geen |
Geen actie |
|
J. Boekhoff |
medisch maatschappelijk werker Amsterdam UMC, locatie VUmc |
Geen |
Geen |
Geen actie |
|
A. Bongen |
Medisch maatschappelijk werker UMC Utrecht |
Geen |
Geen |
Geen actie |
|
H. Bouazzaoui |
Longarts Hagaziekenhuis Den Haag |
Geen |
Geen |
Geen actie |
|
D. Brocke |
Medisch maatschappelijk werk UMC Utrecht Divisie Hart en Longen |
Geen |
Geen |
Geen actie |
|
E. Brokaar |
Poliklinisch apotheker in de Haga Apotheek, HagaZiekenhuis |
Geen |
Gedeeltelijke vergoeding voor internationaal CF congres door Novartis (2012 en 2014) |
Geen actie |
|
I. Bronsveld |
Pulmonoloog UMC Utrecht |
Geen |
Geen |
Geen actie |
|
A. Clement - Boers, de |
Kinderarts, diabetes HAGA/Julianaziekenhuis Den Haag |
Voorzitter Stichting D-Support (ondersteuning voor gezinnen met diabetes) onbetaald |
Geen |
Geen actie |
|
W. Doeleman |
Fysiotherapeut UMC-Utrecht |
Geen |
Geen |
Geen actie |
|
H. Eeman |
Kinderverpleegkundig consulent CF Werkgever: Academisch Medisch Centrum Amsterdam |
Geen |
Geen |
Geen actie |
|
M. Eerden |
Longarts Erasmus MC |
Geen |
Geen |
Geen actie |
|
K. van der Ent |
Kinderarts, hoogleraar kinderlongziekten UMC Utrecht |
|
Onderzoeksubsidies afgelopen vijf jaar:
Instituut heeft betalingen ontvangen voor klinische studies en adviesraad bijeenkomsten van Gilead, Vertex, GSK, Nutrica, TEVA, ProQR, Galapagos en Proteastasis.
|
Gemelde belangen en nevenfuncties zijn besproken met initiatief nemende verenigingen NVALT en NVK.
Deelname in werkgroep als meelezer bij alle modules op basis van expertise over CF.
Geen trekker van modules over CFTR modulatoren waarvoor er financiële belangen zijn. |
|
B. Flapper |
Kinderarts, sociale pediatrie |
Geen |
Geen |
Geen actie |
|
L. van der Giessen |
0,8 Kinderfysiotherapeut Erasmus MC Sophia 0,1 Coordinator onderwijs Erasmus MC 0,1 docentbegeleiding Erasmus MC |
B. Gastdocent Hogeschool Rotterdam Post HBO kinderfysio B. Cursusleider NPI B. Gastdocent Maas en Meer (B=betaald) |
Geen |
Geen actie |
|
V. Gulmans |
Hoofd onderzoek en kwaliteit van zorg bij Nederlandse Cystic Fibrosis Stichting |
Geen |
Geen persoonlijke vergoedingen. De NCFS heeft corporate sponsorovereenkomsten met meerdere bedrijven (farmaceuten en hulpmiddelen). De overeenkomsten zijn aangemeld bij het transparantieregister. De totale sponsorinkomsten bedragen niet meer dan 10 % van de totale NCFS-begroting. De sponsors hebben geen invloed op de inhoud van NCFS-uitingen. |
Geen actie |
|
H. Heijerman |
Longarts, hoofd afdeling longziekten UMC Utrecht. |
|
|
Gemelde belangen en nevenfuncties zijn besproken met initiatief nemende verenigingen NVALT en NVK.
Deelname in werkgroep als meelezer bij alle modules op basis van expertise over CF.
Geen trekker van modules over CFTR modulatoren waarvoor advies is gegeven. |
|
D. Hendriks |
kinderarts-maagdarmleverziekten Juliana Kinderziekenhuis/Hagaziekenhuis Den Haag |
Geen |
Geen |
Geen actie |
|
H. Hendriks |
kinderarts-longarts in Zuyderland MC en 0,1 fte gedetachteerd naar MUMC + voor CF zorg. |
Geen |
Geen |
Geen actie |
|
B. Hoek |
gastroenteroloog en hepatoloog, LUMC Hoogleraar |
Geen |
Geen gesponsord onderzoek op het gebied van CF. Bij genoemde studies mogelijk auteur en: Novartis: PI, inclusie patiënten Zambon: PI, design studies, data analyse Chiesi: design studie, patiënt inclusie, data analyse Abbvie, Norgine, Astellas: patiënt inclusie CLIF: patiënt inclusie Perspectum: patiënt inclusie, design deel van studie Organ Assist: PI, patiënt inclusie Novartis - deelname aan internationale medicijnstudie bij auto-immuun hepatitis Zambon-unrestricted grant voor onderzoek naar auto-immuun hepatitis en overlap syndromen Chiesi - investigator-initiated studie naar farmacoklnetiek van Envarsus (tacrolimus) na levertransplantatie Abbvie - studie naar langetermijn effect op leverfibrose na DAA behandeling van hepatitis C Norgine - deelname aan rifaximin bij hepatische encefalopathie studie CLIF consortium - deelname aan internationale studies naar accuut - op chronisch leverfalen Perspectum - studies naar nieuew NRI technieken bij leverziekte en na levertransplantatie Astellas - deelname aan immuunsuppressie studie na levertransplantatie OrganAssist - deelname aan studie met machineperfusie voor levertransplantatie |
Geen actie |
|
R. Hoek |
Longarts Erasmus MC Centrum voor Longtransplantatie Centrum voor Cystic Fibrosis en Recidiverende Luchtweginfecties |
Nederlands Transplantatievereniging
allen onbezoldigd |
Geen |
Geen actie |
|
A. Hofsteenge |
Dietist: CF-team (kindergeneeskunde) (Vumc en AMC) Kindergeneeskunde (polikliniek) (VUmc) |
Geen |
Geen |
Geen actie |
|
C. van Hoge |
Maag- darm- leverarts MUMC+ |
Geen |
Geen |
Geen actie |
|
F. Hollander-Kraaijeveld |
Diëtist UMC Utrecht |
Geen |
Geen |
Geen actie |
|
R. Houwen |
Hoofd afdeling kinder-MDL UMCU/WKZ |
De (poli)klinische zorg voor patienten met MDL problematiek, het geven van onderwijs alsmede het vooruitbrengen van de zorg en kennis op dit gebied, onder meer door (meewerken aan) publicaties. Tevens aansturen van de subafdeling kinder-MDL. Deze taken worden verricht in een 100% dienstverband. |
|
Geen actie |
|
J. van Ingen |
Arts-microbioloog, Radboudumc, Nijmegen |
Geen |
Mede-auteur van de internationale richtlijn voor diagnostiek en behandeling van niet-tuberculeuze mycobacterieën bij pantiënten met CF (Floto, 2016). |
Geen actie |
|
H. Janssens |
Kinderlongarts, Erasmus MC/Sophia Kinderziekenhuis |
Voorzitter CF-team Sophia |
Co-promotor bij meerdere studies gefinancierd door unrestricted grant van Chiesi en Gilead. |
Geen actie, meelezer bij module over behandeling P.Aeruginosa (Gilead, Chiesi), geen trekker.
Toelichting gesponsorde onderzoeken. -Studies van Chiesi en Gilead waren met een unrestricted grant, financieen gerund door Sophia BV. De aard van de studies kon door het onderzoeksteam vrij ingevuld worden en gepubliceerd. -Deelname centrum aan sponsor initiated studies van Vertex, en Gilead. Geen mede-auteur. Als voorzitter van CF-team verantwoordelijk voor uitvoer van de studie, en beoordeling adverse events en lab uitslagen van deelnemende patiënten. |
|
A. Jansz |
arts-microbioloog, St PAMM, streeklaboratorium voor de volksgezondheid Veldhoven |
Coördinerend arts-microbioloog, RIVM/IDS, Bilthoven, een detachering van 20% auditor voor de RvA |
Geen |
Geen actie |
|
H. van der Kamp |
kinderarts-endocrinoloog (0,7 fte) werkzaam in het WKZ Utrecht en in het Bronovo ziekenhuis in Den Haag (0,15 fte). |
Lid bestuur NVE (onbetaald) Lid adviesgroep groeihormoon (onbetaald) Lid adviesgroep neonatale screening AGS & CHT (onbetaald) |
Geen |
Geen actie |
|
C. de Kiviet |
Verpleegkundig Specialist Bij CF-centrum UMC Utrecht, locatie WKZ |
Lid van Accreditatiecommissie Van de RSV (Register Verpleegkundig Specialismen) >Vacatievergoeding per bijeenkomst -Beoordelaar scholing voor herregistratie Verpleegkundig Specialisten > Vergoeding per beoordeelde scholing |
Geen |
Geen actie |
|
A. Kok |
verpleegkundig consulent CF Erasmus MC-Sophia Rotterdam |
Geen |
Geen |
Geen actie |
|
B. Koot |
kinderarts AMC Amsterdam |
Bestuur sectie kinder MDL, NVK, onbetaald |
Geen |
Geen actie |
|
M. Kruiswijk |
verpleegkundig specialist afdeling Cystic Fibrosis |
Geen |
Geen |
Geen actie |
|
C. Majoor |
Longarts, Amsterdam UMC, locatie AMC |
|
Inclusie patiënten aan fase IIa, IIb, III en IV studies van Vertex en Galapagos |
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is. |
|
R. van der Meer |
Longarts, aandachtsgebied Cystic Fibrose. Werkzaam in Hagaziekenhuis. Den Haag. |
Geen |
Geen |
Geen actie |
|
P. Merkus |
Kinderarts-pulmonoloog, Radboudumc Amalia Kinderziekenhuis |
|
Deelname Studies bij CF door farmaceutische bedrijven: Vertex, PTC (PI, betrokken bij inclusie, betrokken bij data-analyse) |
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is. |
|
D. Mul |
Kinderarts-endocrinoloog bij Diabeter |
|
Geen |
Geen actie, trekker module diabetes (screening en behandeling)
Toelichting op deelname adviesraad medisch Novo Nordisk: conflicteert niet met trekkersrol van diabetes modules. |
|
A. Nagelkerke |
Kinderlongarts VU medisch centrum |
Geen |
|
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is.
|
|
J. Noordhoek |
Directeur Nederlandse Cystic Fibrosis Stichting |
|
|
Geen actie |
|
M. Nuijsink |
Kinderarts Juliana Kinderziekenhuis/ HAGA ziekenhuis |
Geen |
|
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is. |
|
M. van Oirschot-van de Ven |
Kinderverpleegkundig consulent CF, Academisch Medisch Centrum Amsterdam |
Geen |
Geen |
Geen actie |
|
M. Reijers |
Longarts, Radboud UMC, Nijmegen |
|
|
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is.
|
|
S. Reitsma |
KNO-arts AMC Amsterdam |
Geen |
Geen |
Geen actie |
|
Y de Rijke |
Afdelingshoofd Klinische Chemie Erasmus MC te Rotterdam |
Geen |
Geen |
Geen actie |
|
B. Rottier |
UMC Groningen, kinderlongarts |
Geen |
Geen |
Geen actie |
|
R. Schrijver |
Verpleegkundig consulent CF Hagaziekenhuis |
Geen |
Geen |
Geen actie |
|
A. Speijer |
Coördinator kwaliteit van zorg |
Lid advies - en expertcommissie AQUA van Zorginstituut Nederland.
|
Geen |
Geen actie |
|
L. Speleman |
paediatrische KNO, UMC Utrecht Wilhelminakinderziekenhuis |
|
Geen |
Geen actie |
|
S. Terheggen-Lagro |
Kinderlongarts AMC |
|
Geen |
Geen actie |
|
H. Tiddens |
Kinderlongarts, Erasmus MC, Sofia kinderziekenhuis
|
|
|
Geen actie, meelezer bij module over behandeling P.Aeruginosa geen trekker.
Toelichting gesponsorde onderzoeken. iABC: Co-investigator, CT aquisitie, analyse van CTs, geen betrokkenheid bij inclusie van patiënten ALPINE II: betrokken bij inclusie van patiënten |
|
H. van der Vaart |
Longarts UMCG |
Geen |
Geen |
Geen actie |
|
H. de Valk |
Internist-endocrinoloog, UMC Utrecht |
|
Geen |
Geen actie |
|
H. Verkade |
Kinderarts MDL, UMCG Groningen |
|
Geen |
Geen actie |
|
M. Verkleij |
GZ-psycholoog/cognitief gedragstherapeut, Amsterdam UMC locatie VUmc |
Geen |
Geen |
Geen actie |
|
E. Weersink |
longarts, AMC Amsterdam |
Geen |
|
Geen actie
Toelichting: Niet direct betrokken bij module waarop de potentiële belangenverstrengeling van toepassing is. |
|
M. Wessels-Bakker |
Verpleegkundig Specialist Longtransplantatie, onderzoeker |
Geen |
Geen |
Geen actie |
|
B. Wijnberg-Williams |
Klinisch psycholoog/medisch psycholoog, richting kinderen en jeugdigen, UMCG (0,4 fte) en Isala ziekenhuis (0,7fte) |
Lid van Accreditatiecommissie Federatie van Gezondheidszorgpsychologen en Psychotherapeuten (FGzPt) (vacatiegelden) |
Geen |
Geen actie |
|
F. Willeboordse |
Adviseur Kennisinstituut Federatie Medisch Specialisten |
Geen |
Via werk partner aandelen bij moederbedrijf Johnson & Johnson. Partner is werkzaam bij Janssen Vaccines BV. |
Geen actie |
|
K. Winter-de Groot |
kinderarts-pulmonoloog WKZ/UMC Utrecht |
|
Geen |
Geen actie |
|
P. Zwijnenburg |
kinderarts-klinisch geneticus VUMC afd. klinische genetica |
Geen |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname aan de werkgroep van de patiëntenorganisatie NCFS en de VSOP voor zeldzame en genetische aandoeningen. De uitgangsvragen zijn getoetst via een online peiling onder patiënten en ouders. Voor sommige onderwerpen is het patiënten-panel van de NCFS geraadpleegd om input te verkrijgen over patiëntenvoorkeuren over een behandeling of screeningsmethode.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de kwaliteitsstandaarden de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de kwaliteitsstandaard in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
Deze medisch inhoudelijke modules in deze kwaliteitsstandaard is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Voor de modules over psychosociale zorg en de modules over organisatie van zorg is er volgens de AQUA methode gewerkt: GRADE. De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie https://www.gradeworkinggroup.org/docs/Criteria_for_using_GRADE_2016-04-05.pdf).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de stuurgroep en de adviseur de knelpunten. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten. Tevens zijn er knelpunten aangedragen door VSOP, NCFS, NVK, NVALT, Patiëntenfederatie, Lareb, NVMDL, ZiN, ZN, NIP, NVKNO, VKGN, Vereniging innovatieve geneesmiddelen, NVKC, V&VN, NVMM, KNGF, NIV, NVvR, NVD, NVAB, NVZA via een invitational conference.
De concept uitgangsvragen zijn door de NCFS online voorgelegd aan mensen met CF en ouders van kinderen met CF. Vrijwel alle uitgangsvragen werden door tenminste 85% van de 68 respondenten als zinvol tot zeer zinvol ervaren. Bij twee vragen was dit percentage lager (56% respectievelijk 72%), veroorzaakt door het feit dat 25% van de respondenten bij deze vragen geen mening had.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de stuurgroep en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er is voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Voor deze kwaliteitsstandaard was de Europese Best Practice richtlijn van de ECFS (Castellani, 2018) een belangrijk uitgangspunt voor bijna alle modules.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de kwaliteitsstandaard is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Indicatorontwikkeling
De werkgroep heeft besloten geen indicatoren te ontwikkelen bij de huidige richtlijn omdat er geen substantiële barrières konden worden geïdentificeerd die implementatie van de aanbeveling zouden kunnen bemoeilijken.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G., ... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Castellani C, Duff AJA, Bell SC, Heijerman HGM, Munck A, Ratjen F, Sermet-Gaudelus I, Southern KW, Barben J, Flume PA, Hodková P, Kashirskaya N, Kirszenbaum MN, Madge S, Oxley H, Plant B, Schwarzenberg SJ, Smyth AR, Taccetti G, Wagner TOF, Wolfe SP, Drevinek P. ECFS best practice guidelines: the 2018.
revision. J Cyst Fibros. 2018 Mar;17(2):153-178. doi: 10.1016/j.jcf.2018.02.006. Epub 2018 Mar 3. Review.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E., ... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1987-juli 2017
Engels |
Cystic Fibrosis/ or (cystic adj3 fibros*).ti,ab,kf. or (pancreatic adj3 fibros*).ti,ab,kf. or mucoviscidos*.ti,ab,kf. or CFTR*.ti,ab,kf. (47113) 6 exp "Diabetes Mellitus"/ or exp hyperglycemia/ or exp "Glucose Intolerance"/ or exp "Insulin Resistance"/ or exp "Glucose Metabolism Disorders"/ or (hyperglyc* or CFRD or IGT or "glucose def*" or diabet* or "impaired glucose tolerance" or "cystic fibrosis related diabetes").ti,ab,kf. (676846) 7 1 and 6 (1740) 9 limit 7 to (english language and yr="1987-Current") (1416) 10 exp proinsulin/ or insulin, regular, human/ or insulin*.ti,ab,kf. or (insulin adj3 therap*).ti,ab,kf. or "insulin antagonists"/ or (oral adj3 agents).ti,ab,kf. or (oral adj3 antidiabetic).ti,ab,kf. or exp "Hypoglycemic Agents"/ or (hypoglycemic adj3 agent*).ti,ab,kf. or exp "Sulfonylurea Compounds"/ or sulfonyl*.ti,ab,kf. or SU.ti,ab,kf. or (care adj10 diabetes).ti,ab,kf. or exp "nutrition therapy"/ or exp Diet/ or (diet* adj3 intervention).ti,ab,kf. or (diet* adj3 treatment).ti,ab,kf. or diet*.ti,ab,kf. or (carbohydrat* adj3 reduction).ti,ab,kf. (1021719) 11 9 and 10 (530) 13 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (335944) 14 11 and 13 (19) 15 ((clinical adj3 pathway) or (clinical adj3 pathways) or (practice adj3 parameter) or (practice adj3 parameters)).ti,ab,kw. or algorithms/ or care pathway.ti,ab,kw. or care pathways.ti,ab,kw. or clinical protocols/ or Consensus/ or Consensus Development Conference.pt. or Consensus Development Conference, NIH.pt. or Consensus Development Conferences as Topic/ or Consensus Development Conferences, NIH as Topic/ or critical pathway/ or guidance.ti,ab. or guideline*.ti. or guidelines as topic/ or practice guidelines as topic/ or Health Planning Guidelines/ or practice guideline/ (529445) 16 11 and 15 (23) 17 14 or 16 (38) 18 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1749564) 19 11 and 18 (60) 20 (Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ or 11) and ("research support, american recovery and reinvestment act" or research support, nih, extramural or research support, nih, intramural or research support, non us gov't or research support, us gov't, non phs or research support, us gov't, phs).pt. [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (1012663) 21 11 and 20 (199) 22 19 or 21 (228) 23 22 not 17 (210) 24 17 or 23 (248) – 233 uniek |
315 |
|
EMBASE |
((('cystic fibrosis'/exp/mj OR ((cystic NEAR/3 fibros*):ti,ab) OR ((pancreatic NEAR/3 fibros*):ti,ab) OR mucoviscidos*:ti,ab)
AND ('diabetes mellitus'/exp/mj OR 'hyperglycemia'/exp/mj OR 'glucose intolerance'/exp/mj OR 'insulin resistance'/exp/mj OR 'disorders of carbohydrate metabolism'/exp OR hyperglyc*:ti,ab OR cfrd:ti,ab OR igt:ti,ab OR 'glucose def*':ti,ab OR diabet*:ti,ab OR 'impaired glucose tolerance':ti,ab OR 'cystic fibrosis related diabetes':ti,ab)
AND ('proinsulin'/exp/mj OR 'human insulin'/exp/mj OR 'antidiabetic agent'/exp/mj OR 'sulfonylurea derivative'/exp/mj OR 'diet therapy'/exp/mj OR 'diet'/exp/mj OR insulin*:ti,ab OR ((insulin NEAR/3 therap*):ti,ab) OR ((oral NEAR/3 agents):ti,ab) OR ((oral NEAR/3 antidiabetic):ti,ab) OR ((hypoglycemic NEAR/3 agent*):ti,ab) OR sulfonyl*:ti,ab OR su:ti,ab OR ((care NEAR/10 diabetes):ti,ab) OR ((diet* NEAR/3 intervention):ti,ab) OR ((diet* NEAR/3 treatment):ti,ab) OR diet*:ti,ab OR ((carbohydrat* NEAR/3 reduction):ti,ab))
AND [english]/lim AND [embase]/lim AND [1987-2017]/py NOT 'conference abstract':it)
AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)))
OR (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it))
OR 'major clinical study')
OR (('practice guideline'/exp OR 'algorithm'/exp OR 'clinical pathway'/exp OR 'clinical protocol'/exp OR 'consensus development'/exp) OR (((clinical NEAR/3 pathway):ti,ab) OR ((clinical NEAR/3 pathways):ti,ab) OR ((practice NEAR/3 parameter):ti,ab) OR ((practice NEAR/3 parameters):ti,ab) OR 'care pathway*':ti,ab OR guidance:ti,ab OR guideline*.ti.))) (186) 82 uniek |
|
