Psychosociale zorg bij IBD
Uitgangsvraag
Welke psychosociale interventies worden er ingezet om psychosociale problemen bij kinderen en adolescenten met IBD te verminderen? En wat is de effectiviteit?
Aanbeveling
Wees als behandelaar voor jongeren met IBD alert op signalen voor psychologische problemen (zoals somberheid, angst en schoolproblemen) en bevraag jongeren hier actief op.
Screen elke jongere op de IBD-polikliniek minstens één keer per jaar op angst en depressieklachten met een valide meetinstrument dat ten minste angst en depressie meet, zoals bijvoorbeeld de Strengths & Difficulties Questionnaire (SDQ, zie bijlage 5). Verwijs bij een verhoogde score voor aanvullende psychologische diagnostiek en behandeling. Screen de eerste keer minstens een half jaar na diagnose.
Zorg dat (vanuit het IBD-behandelteam) psychologische diagnostiek en behandeling laagdrempelig beschikbaar is. Verwijs in overleg met de jongere wanneer dat nodig blijkt naar psychologen die ervaringen hebben met het begeleiden van somatisch zieke jongeren voor cognitieve gedragstherapie of ondersteunende non-directive therapie.
Overwegingen
De literatuur besproken in bijlage 4 toont evident dat IBD impact kan hebben op zowel de psychologische gezondheid van de adolescent, de psychosociale ontwikkeling, en het school- en gezinsfunctioneren. Naar angst en depressieklachten is veruit het meeste onderzoek gedaan, waarbij de meerderheid van de studies toont dat dit voorkomt bij ongeveer 25% van de adolescenten met IBD. Een systematische review met meta-analyse over de prevalentie van angst en depressie bij adolescenten met IBD is helaas (nog) niet beschikbaar. De studies naar angst bij jongeren met IBD zijn van de laatste jaren (Reigada,2015; Reigada,2016) en er zijn nog geen kwalitatief goede studies beschikbaar die interventies bij angstklachten bij adolescenten met IBD onderzoeken. Daarnaast zijn er weinig studies beschikbaar over de andere psychosociale problemen, de studies die zijn gepubliceerd, zijn klein en van lage kwaliteit.
In de internationale richtlijnen voor jongeren met IBD wordt geen antwoord gegeven op de vraag of alle jongeren met IBD gescreend zouden moeten worden op psychosociale problemen, of specifiek angst en depressie, en op welke manier dit het beste kan gebeuren. Ook is onduidelijk hoe screening het best geïmplementeerd kan worden in de Nederlandse situatie, welke kosten aan screening verbonden zijn, en waar patiënten die positief uit de screening komen het best naar verwezen kunnen worden voor psychologische diagnostiek en behandeling.
Er zijn grofweg twee manieren van screening denkbaar. De één is screenen door middel van (digitale) vragenlijsten op de polikliniek (in de wachtkamer of thuis), de ander is screening door de arts in de spreekkamer.
Een recente studie van Iturralde (2017) is één van de eerste studies die de eerste vorm heeft onderzocht. Op 3 subspecialistische kinderpoliklinieken in Amerika (IBD, Cystic Fibrosis, en diabetes) werden patiënten in de wachtkamer op de polikliniek gescreend op depressie en globale gezondheid met twee digitale vragenlijsten. De studie toont dat standaard screening haalbaar en effectief is, geaccepteerd wordt door zowel patiënt als behandelteam, de doorstroom op de polikliniek niet verstoort en ervoor zorgt dat patiënten die het nodig hebben psychologische hulp krijgen (Iturralde, 2017). De keuze voor een screeningsinstrument hangt af van het doel: wil men breed screenen op de sociaal emotionele gezondheid of specifieker, bijvoorbeeld alleen gericht op bijvoorbeeld angst/depressieve klachten. Een geschikt instrument om breed te screenen is bijvoorbeeld de SDQ: Strengths and Difficulties Questionnaire, welke in 25 vragen de sociaal emotionele gezondheid van kinderen en jongeren het afgelopen half jaar in kaart brengt (Muris, 2003). De vragen zijn gericht op vijf subschalen: emotionele problemen (angst/depressie), gedragsproblemen, hyperactiviteit/aandachtstekort, problemen met leeftijdsgenoten, prosociaal gedrag. Bij een verhoogde score op een van de subschalen wordt geadviseerd te verwijzen naar een psycholoog voor verdere diagnostiek en/of behandeling. Voordeel van de SDQ is dat het breder kijkt dan alleen emotionele problemen en dat het een relatief korte vragenlijst is die weinig tijd vergt.
Er zijn verschillende gevalideerde vragenlijsten in het Nederlands beschikbaar voor specifieke screening op angst en depressie bij adolescenten, zoals bijvoorbeeld de CDI, SCARED, MASC, RCMAS (https://www.nji.nl/). Nadeel van deze vragenlijsten is dat ze allemaal lang zijn en veel tijd vergen. De kortere vragenlijsten zoals de Patient Health Questionnaire (PHQ-9 voor depressie) en de Generalized Anxiety Disorder (GAD-7) zijn vooral gevalideerd in volwassen patiënten in de eerste lijn en nog onvoldoende in adolescenten in de tweede of derde lijn.
Optie twee, screenen door de arts in de spreekkamer, is een goed alternatief, en biedt gelegenheid om in de spreekkamer het gesprek over emotionele problemen te starten. Het moet uiteraard gebeuren met een aantal zeer korte vragen zodat het niet te veel tijd in beslag neemt. Als gekeken wordt welke instrumenten beschikbaar zouden zijn, zijn er helaas maar een beperkt aantal korte screeningsinstrumenten in het Nederlands beschikbaar. Voor depressie bestaat er een verkorte versie van de Patient Health Questionnaire (PHQ-9), de PHQ-2 (Kroenke, 2003), waar de 2 belangrijkste depressieve symptomen worden uitgevraagd. Voor angst is er een verkorte versie van de SCARED (de SCARED-5) en de Generalized Anxiety Disorder (GAD-7), de GAD-2. Voor deze verkorte instrumenten is weinig onderzoek beschikbaar die de betrouwbaarheid in adolescenten in de tweede of derdelijns zorg beschrijft (Holly, 2012; Richardson, 2010; Sudhanthar, 2015).
Wanneer gekeken wordt naar internationale richtlijnen over psychologische screening bij adolescenten met andere chronische ziekten zoals diabetes en cystische fibrosis, wordt geadviseerd jaarlijks te screenen op ten minste angst en depressieve klachten (Monaghan, 2010; Silverstein, 2005; Quittner, 2016). Vanwege het feit dat iedere adolescent een periode nodig heeft om zich aan te passen aan het hebben van een chronische ziekte, wordt geadviseerd na diagnose 6 maanden te wachten alvorens te screenen.
De werkgroep is van mening dat er voldoende studies zijn die tonen dat er een hoge prevalentie bestaat van angst en depressieklachten bij adolescenten met IBD, en dat dit ertoe zou moeten leiden dat er meer aandacht komt voor psychologische gezondheid in de zorg voor deze patiëntengroep. Dit wordt onderschreven door de patiëntengroep zelf.
De werkgroep is van mening dat, ondanks het feit dat er weinig studies zijn waarmee dit wetenschappelijk onderbouwd kan worden, het belangrijk is om jongeren met IBD jaarlijks te screenen op ten minste angst en depressieve klachten en indien daar aanwijzingen voor zijn te verwijzen voor aanvullende diagnostiek en psychologische behandeling. Daarnaast constateert de werkgroep dat het wenselijk zou zijn als er een betrouwbaar en kort screeninginstrument beschikbaar zou zijn waarmee de arts in de spreekkamer kan screenen. Op basis van de beschikbare literatuur is het echter niet mogelijk daarvoor een specifiek instrument aan te bevelen. Er zijn wel betrouwbare vragenlijsten beschikbaar om breed dan wel gericht te screenen met langere (digitale) vragenlijsten op de polikliniek.
Voor het beantwoorden de uitgangsvraag bleven alleen studies over die een interventie bestudeerden bij adolescenten met IBD en depressieklachten. Twee van de drie geïncludeerde studies betrof een kleine RCT (n=41), waarbij de korte termijn (3 maanden; Szigethy, 2007) en lange termijn (tot 15 maanden; Thompson, 2012) resultaten werden gerapporteerd. De grotere derde RCT (Szigethy, 2014), eveneens van dezelfde onderzoeksgroep, beschreef dat twee onderzochte psychotherapieën (CGT versus SNDT) beide verbetering gaven van de ernst van de depressie, kwaliteit van leven en ziekteactiviteit op korte termijn. Of deze verbeteringen ook allemaal klinisch relevant waren was niet uit de gerapporteerde resultaten op te maken, en kon niet achteraf berekend worden met de beschikbare data (Wise, 2004). Over de verbetering in ziekteactiviteitscore valt te vermelden dat dit lager is dan de criteria geadviseerd voor farmacologische interventiestudies (Turner, 2007; Hyams, 2005). Uitkomstmaten met betrekking tot het gezin- of schoolfunctioneren waren in deze studies niet meegenomen.
Bij volwassen patiënten met IBD is meer onderzoek gedaan, en zijn er meerdere systematische reviews gepubliceerd over het effect van psychologische interventies.
Een Cochrane review in 2011 includeerde 21 studies ((quasi) gerandomiseerd, en niet gerandomiseerd) waarbij verschillende psychotherapieën werden onderzocht in zowel gescreende als ongescreende patiënten. Samenvattend werd geen effect van psychotherapie gevonden op kwaliteit van leven en depressieklachten bij volwassenen. Eveneens was het deel van patiënten waarvan de ziekte niet in remissie was niet verschillend na psychotherapie. De 2 studies bij adolescenten die waren geïncludeerd (waaronder Szigethy, 2007) toonden een effect op depressieve symptomen, ziekte specifieke kwaliteit van leven en coping (Timmer, 2011).
McCombie (2013) publiceerde in 2013 een review en een update van het Cochrane review, waarbij 18 studies met een psychologische interventie en een controlegroep werden geïncludeerd, er werd geen meta-analyse verricht. Vier studies waren verricht bij kinderen en drie studies hadden patiënten geïncludeerd met psychologische klachten bij baseline. Dit review ondersteunt de conclusie van het Cochrane review dat er onvoldoende bewijs is dat psychotherapie angst, depressie, kwaliteit van leven en het ziektebeloop verbetert. Maar ziet wel aanwijzingen voor een mogelijk effect op pijn, moeheid en therapietrouw (McCombie, 2013).
Dit jaar verscheen een systematic review met meta-analyse in The Lancet Gastroenterology Hepatology. Hierin waren 14 RCT’s geïncludeerd die verschillende psychologische interventies onderzochten in een ongeselecteerde (ongescreende) populatie. De meta-analyse toont dat psychologische therapie bij volwassen patiënten mogelijk verbetering geeft op korte termijn van depressieve symptomen en kwaliteit van leven in IBD-patiënten in remissie. Er waren helaas maar 2 studies beschikbaar bij patiënten met actieve ziekte. Daarnaast werd er geen effect gevonden op angstsymptomen, ziekteactiviteit en waargenomen stress. Een subanalyse van 5 RCT’s (511 patiënten) met cognitieve gedragstherapie als interventie, toonde een significante verbetering in kwaliteit van leven aan het einde van de psychologische interventie (8 tot 12 weken) (Gracie, 2017). De verschillende soorten therapieën onderzocht in de reviews, met een verschillend aantal sessies, en verschillende therapie vormen (telefonisch, face to face, digitaal) compliceren het doen van specifieke aanbevelingen.
Vanuit de CCUVN is in 2017 een enquête verstuurd naar alle jongeren met IBD tussen 16 tot 23 jaar waarin onder andere naar hun behoefte aan en ervaringen met psychologische hulp werd gevraagd. 71 jongeren hadden de vragenlijst ingevuld, de helft had ooit psychologische hulp vanwege IBD gehad, de meeste waren tussen de 14 tot 18 jaar toen ze hulp kregen. De hulp was in de meeste gevallen geadviseerd door de kinderarts of op verzoek van ouders. Hoewel niet alle ervaringen positief waren, vinden alle jongeren dat psychologische zorg aangeboden moet worden.
De jongeren geven aan dat het starten van de hulp op verzoek van de jongere moet gebeuren, en in samenspraak met de arts (en ouders). Ook komt uit de enquête dat psychologische hulp vooral niet opgedrongen moet worden (https://www.crohn-colitis.nl/onderzoek/cc-panel/resultaten-onderzoek-cc-panel/).
De werkgroep is van mening dat het onderzoek naar de behandeling van psychosociale problemen bij jongeren beperkt en eenzijdig is: er zijn maar 2 kwalitatief goede studies beschikbaar die 2 soorten psychotherapieën onderzoeken als behandeling voor depressieve klachten bij jongeren met IBD. Bij voorkeur worden aanbevelingen uiteraard niet enkel gebaseerd op maar 2 studies, welke ook nog eens van dezelfde onderzoeksgroep zijn. Totaal zijn twee soorten psychotherapieën onderzocht (CGT en SNDT), er is geen overtuigend bewijs dat één het meest effectief is (Szigethy, 2014). Daarnaast is nog onvoldoende onderzocht welke intensiteit (duur en frequentie) de psychotherapie zou moeten hebben om effectief te zijn. Een studie door de onderzoeksgroep van Levy, 2016 toont dat 3 sessies cognitieve gedragstherapie bij jongeren met IBD (zonder psychologische problemen bij baseline) genoeg is om kwaliteit van leven te verbeteren en schoolverzuim te verminderen. Uitkomstmaten in de beschreven studies waren verbetering van depressieklachten, globaal functioneren, ziekte specifieke kwaliteit van leven en ziekteactiviteit, maar is niet gekeken naar andere mogelijk relevante uitkomstmaten zoals moeheid, schoolverzuim en zorgconsumptie. Wanneer onderzoeken verbetering van psychologische symptomen vermelden is het ook belangrijk en wenselijk dat gerapporteerd wordt of deze verbetering naast statistisch significant ook klinisch relevant is. Er zijn diverse methodes om dit te beschrijven, maar deze zijn helaas niet gebruikt in de beschreven studies.
Tot slot is het belangrijk om het beloop van (milde) psychische klachten zonder interventie te onderzoeken, om te beoordelen of ingrijpen überhaupt nodig is, of dat het natuurlijk beloop van de klachten gunstig is.
Concluderend bestaat er nog een groot aantal vragen over psychologische interventies bij jongeren met IBD en psychische klachten, waar op basis van de huidige literatuur geen antwoord op te formuleren is.
Onderbouwing
Achtergrond
Psychosociale problemen komen frequent voor bij kinderen en adolescenten met IBD. Patiënten kunnen een lager gevoel van eigenwaarde en sociaal functioneren hebben, en er kunnen problemen ontstaan in het gezinsfunctioneren (Mackner, 2013). Daarnaast ervaren jongeren moeite op school doordat ze veel afwezig zijn ten gevolge van bijvoorbeeld een actieve darmontsteking, moeheidsklachten en frequent ziekenhuisbezoek (Assa, 2015). In de gespecialiseerde kinder-IBD centra wordt dan ook vaak de onderwijsconsulent voor kinderen met een chronische ziekte ingeschakeld om school te adviseren en tussen de patiënt en school te bemiddelen. De problemen die het meest voorkomen en het meest onderzocht zijn, zijn angst en depressieklachten, met een gemiddelde prevalentie van 20 tot 30%. Voor een uitgebreid overzicht over de soorten psychosociale problemen, hun voorkomen, bekende risicofactoren en de onderzochte psychologisch behandelingen, verwijzen we u naar bijlage 4. Al deze problemen kunnen (in)direct ook invloed hebben op de ernst van de darmontsteking: patiënten zijn vaak minder therapietrouw, maar er zijn ook aanwijzingen dat er een direct effect is van psychologische problemen op het beloop van de darmontsteking (en vice versa) (via de brain gut axis, zie bijlage 4).
In de huidige klinische praktijk is er weinig bekend over welk soort problemen er kunnen spelen en worden deze problemen vanwege de complexiteit en de beperkte tijd per patiënt vaak niet herkend. De beschikbare literatuur rapporteert uiteenlopende prevalenties over het voorkomen van psychosociale problemen. Er zijn duidelijke aanwijzingen dat de prevalentie van angst en/of depressie onder adolescenten met IBD hoger is dan bij gezonde adolescenten of adolescenten met andere chronische ziekten. In de internationale richtlijnen voor jongeren met IBD wordt geen antwoord gegeven op de vraag of alle jongeren met IBD gescreend zouden moeten worden op psychosociale problemen. Ook zijn er nauwelijks studies die onderzoeken of standaard screenen van IBD-patiënten op angst en depressie nodig, helpend of effectief is. Een eenduidig antwoord op deze vraag is ook lastig gezien het feit dat onderzoek naar psychosociale problemen bij jongeren met IBD nog jong is en er relatief weinig kwalitatief goed onderzoek beschikbaar is. Ook is de setting en methode van de verschillende onderzoeken in ieder land en centrum verschillend, dit zorgt ervoor dat studies lastig met elkaar te vergelijken zijn en compliceert het formuleren van eenduidige conclusies. Daarnaast is de beschikbaarheid, organisatie en vergoeding van psychologische zorg in ieder land en ieder ziekenhuis anders en is niet in elk ziekenhuis of IBD-centrum een psycholoog laagdrempelig beschikbaar in het IBD-behandelteam. Sommige centra laten elke nieuwe jongere met IBD kennismaken met de psycholoog, anderen doen dit alleen als er een indicatie is. Als psychologische begeleiding nodig is worden patiënten soms verwezen naar een kinderpsycholoog vanuit de medische psychologie in het eigen ziekenhuis, maar ook naar de Geestelijke Gezondheidzorg (GGZ), of naar de huisarts met het verzoek de verwijzing te regelen.
Als er daadwerkelijke psychologische problemen geconstateerd worden, is onbekend welke psychologische behandeling het beste is voor deze patiëntengroep en door wie die gegeven zou moeten worden (eerstelijns psycholoog of een medisch psycholoog?). Het type behandeling is onderwerp van de huidige uitgangsvraag. De literatuur toont dat voor depressieklachten enkel kwalitatief goed onderzoek is verricht naar cognitieve gedragstherapie (CGT) en ondersteunende non-directieve therapie bij jongeren met IBD. Studies over CGT zullen in de literatuurbespreking aan bod komen.
Conclusies / Summary of Findings
|
Laag GRADE |
Cognitieve gedragstherapie kan op korte en lange termijn depressieve symptomen verminderen bij adolescenten met IBD vergeleken met een controlegroep zonder psychologische behandeling.
Bronnen (Szigethy, 2007; Thompson 2012) |
|
Redelijk GRADE |
Cognitieve gedragstherapie en ondersteunende non-directieve therapie zijn op korte termijn even effectief in het verminderen van de ernst van depressieklachten, IBD-ziekteactiviteit en het verbeteren van ziekte specifieke kwaliteit van leven.
Bronnen (Szigethy, 2014) |
|
Redelijk GRADE |
Cognitieve gedragstherapie en ondersteunende non-directieve therapie kunnen op korte en middellange termijn het globaal (psychosociaal) functioneren verbeteren.
Bronnen (Szigethy, 2007; Thompson, 2012; Szigethy, 2014) |
Samenvatting literatuur
Beschrijving studies
Er werden drie gerandomiseerde studies geïncludeerd (Szigethy, 2007; Szigethy, 2014; Thompson, 2012), waarbij Szigethy (2007) en Thompson (2012) respectievelijk de korte (3 maanden) en lange (15 maanden) termijn resultaten zijn van dezelfde studie. Szigethy (2007) en Thompson (2012) vergelijken het effect van een IBD-specifieke cognitieve gedragstherapie met een controlegroep zonder psychologische interventie (treatment as usual) bij 41 voorgescreende adolescenten met IBD en een subklinische depressieve stoornis (gediagnosticeerd met een psychiatrisch interview). De primaire uitkomstmaat was ‘depressieve symptomen’, gemeten als de somscore van de ouder en kind gerapporteerde depressieve symptomen op de Child Depression Inventory (CDI)-vragenlijst. Secundaire uitkomstmaten betroffen een zelfrapportage vragenlijst over cognitieve verwerking (waargenomen controle) en een score over globaal functioneren door de clinicus ingevuld.
Szigethy (2014) vergelijkt dezelfde IBD-specifieke cognitieve gedragstherapie met een ondersteunende non-directieve therapie (supportive non-directive therapy (SNDT)) bij 217 adolescenten met IBD en een depressieve stoornis (klinisch (major) en subklinisch (minor), gediagnosticeerd met een psychiatrisch interview). Het artikel beschrijft de korte termijn resultaten op 3 maanden. Primaire uitkomstmaat betrof de ernst van de depressie gemeten met de Children's Depression Rating Scale – Revised (CDRS-R) score, een veelgebruikte score waarmee de ernst van een depressie gescoord kan worden. Secundaire uitkomstmaten betroffen psychosociaal functioneren, ziekte specifieke kwaliteit van leven en ziekteactiviteit.
Resultaten
De belangrijkste kenmerken en resultaten van de geïncludeerde studies worden beschreven in de Evidencetabellen.
Depressieve symptomen (ouder en kind vragenlijst en aantal symptomen op het psychiatrisch interview)
Szigethy (2007) toont dat na 3 maanden de gecombineerde ouder en kind CDI-score in de CGT-groep significant lager is dan in de controlegroep, met een grote effect grootte (1.01, t=3.18, p=0.003). Daarnaast is gekeken naar het aantal depressieve symptomen, gescoord tijdens het psychiatrisch interview door een geblindeerde beoordelaar. In de twee artikelen wordt deze uitkomst verschillend gerapporteerd. In Szigethy (2007) worden deze gerapporteerd als niet significant verschillend tussen de CGT en de controlegroep (effect grootte 0.63, t=1.98, p=0.55). In de studie van Thompson (2012) zijn deze alleen na 3 maanden significant lager in de CGT-groep dan in de controlegroep (effect size 0.99 (0.02 tot 1.76), p=0.013). Op 9 en 15 maanden is er geen significant verschil. Wel had de CGT-groep een grotere afname in depressieve symptomen op de vragenlijst van baseline naar 15 maanden dan de controlegroep (p=0.002).
Cognitive processing (ervaren controle over levensgebeurtenissen)
Szigethy (2007) toont dat er op 3 maanden meer waargenomen controle is over levensgebeurtenissen in de CGT-groep dan in de controlegroep (effect grootte 0.71, t=2.13, p=0.042). Deze uitkomstmaat wordt niet meer beschreven op de andere tijdsmomenten.
Ernst depressie
In de trial van Szigethy (2014) wordt beschreven dat er verbetering is van de ernst van depressie in zowel de CGT als de SNDT-groep (β=2.55 (0.96-6.06), z=1.42, p=0.16) met een grote voor-na effect grootte voor beide therapieën (voor CGT=1.31; voor SNDT: 1.30). De behandelrespons (gedefinieerd als het verlagen van de CDRS-score naar ≤28) is niet significant verschillend tussen de 2 groepen (CGT: 53.5 versus 47.1 % SNDT (OR 1.29 (0.71 tot 2.36), p>0.05). Eveneens was er geen significant verschil in het aantal patiënten dat complete remissie had van de depressie (CGT: 67.7 versus 63.2 % SNDT (OR 1.29 (0.66 tot 2.28), p>0.05))
Globaal/psychosociaal functioneren (Children's Global Assessment Scale (CGAS))
Szigethy (2007) en Thomson (2012) tonen dat er na 3 maanden (Szigethy, 2007; effect grootte 0.86, t=2.72, p=0.01/ Thomson, 2012; p=0.012 of effect grootte -1.37 (-2.43 tot -0.32), p=0.012) en na 9 maanden (effect grootte, -1.12 (-2.06- -0.17), p=0.022) een verbetering is in het globaal functioneren in de CGT-groep vergeleken met de controlegroep.
Szigethy (2014) toont verbetering van het globaal functioneren in zowel de CGT als de SNDT-groep (β -1.46 (-2.96 tot 0.04), z=1.90, p=0.06). Deze verbetering was niet significant verschillend tussen de twee behandelingen.
Health related quality of Life
Szigethy (2014) toont verbetering in ziekte specifieke kwaliteit van leven in zowel de CGT als de SNDT-groep (β -6.42 (-13.28 tot 0.45), z=1.83, p=0.07).
Ziekteactiviteit
Szigethy (2014) toont verbetering van de ziekteactiviteit score in zowel de CGT als de SNDT-groep, met een grotere verbetering in de CGT-groep (β 0.31 (0.008 tot 0.62), z=2.01, p=0.04). Als gekeken wordt naar de verbetering in ruwe ziekteactiviteit score dan daalt de PCDAI-score voor Crohn patiënten in de CGT-groep van 21 (SD 16.2) naar 9.49 (SD 2.48) en van 25.9 (SD 3.8) naar 15.3 (SD 12.11) in de SDNT-groep. Voor colitis ulcerosa patiënten daalt de PUCAI-score in de CGT-groep van 23.3 (SD 24.9) naar 11.39 (SD 12.7) en in de SDNT-groep 22.4 (SD 16.9) naar 11.47 (SD 16.5).
Bewijskracht van de literatuur
Depressieve symptomen
De bewijskracht voor de uitkomstmaat depressieve symptomen is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; -1) en het geringe aantal patiënten (imprecisie; -1).
Ernst depressie, Health related quality of Life, ziekteactiviteit
De bewijskracht voor de uitkomstmaat ernst depressie, Health related quality of Life, en ziekteactiviteit is met 1 niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: -1).
Globaal/psychosociaal functioneren
De bewijskracht voor de uitkomstmaat globaal functioneren is met 1 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias; -1).
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht:
Welke psychosociale interventies worden er ingezet om psychosociale problemen bij kinderen en adolescenten met IBD te verminderen? En wat is de effectiviteit?
P: kind/adolescent met IBD met een psychosociaal probleem;
I: (Cognitieve) gedragstherapie, psychotherapie, counseling, gezinstherapie, psychoeducatie;
C: geen psychologische behandeling of een andere psychologische behandeling;
O: verbetering psychologische klachten, kwaliteit van leven, schoolprestaties, gezinsfunctioneren.
Relevante uitkomstmaten
De werkgroep achtte verbetering van psychologische klachten (een) voor de besluitvorming kritieke uitkomstmaat; Kwaliteit van leven, schoolprestaties, gezinsfunctioneren werden beschouwd als voor de besluitvorming belangrijke uitkomstmaten.
Zoeken en selecteren (Methode)
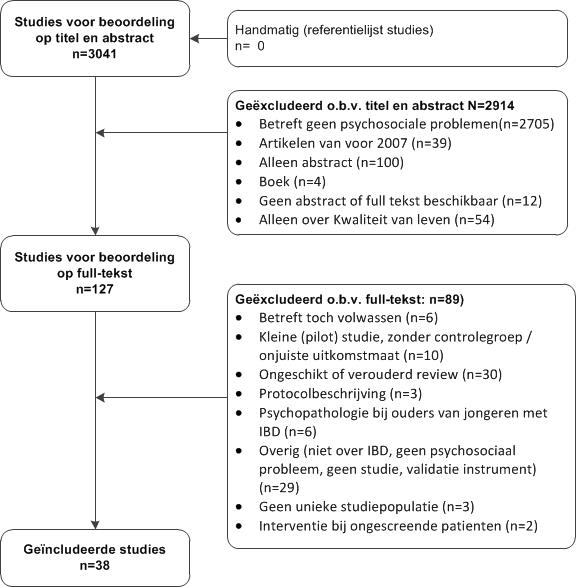
In de databases Medline (via OVID), Embase (via Embase.com), web of science, psychinfo ovid, Cochrane Library en google scholar is op 1 juni 2017 met relevante zoektermen gezocht. Alle studietypen werden vanwege de achtergrondvraag meegenomen. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 3041 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: onderzoek van na 2007 (gezien de huidige richtlijnupdate een vervolg is op de richtlijn van 2007) bij kinderen en adolescenten met IBD waarin psychosociale problemen beschreven of onderzocht waren. Op basis van titel en abstract werden in eerste instantie 127 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 89 studies geëxcludeerd (zie exclusietabel onder het tabblad verantwoording), en 38 studies opgenomen in de literatuuranalyse. Hiervan konden 35 studies gebruikt worden voor het overzicht van de psychosociale problemen bij jongeren met IBD (bijlage 4), en werden 3 studies, betreffende 2 unieke gerandomiseerde studies geselecteerd voor uitgangsvraag 1. Zie de aanverwante producten voor een flowchart met overzicht van het selectieproces. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen
Referenties
- Assa A, Ish-Tov A, Rinawi F, et al. School Attendance in Children With Functional Abdominal Pain and Inflammatory Bowel Diseases. J Pediatr Gastroenterol Nutr. 2015;61(5):553-7. PMID: 25950089.
- Birmaher B, Brent DA, Chiappetta Let al. Psychometric properties of the Screen for Child Anxiety Related Emotional Disorders (SCARED): a replication study. J Am Acad Child Adolesc Psychiatry. 1999;38(10):1230-6. PubMed PMID: 10517055.
- Gracie DJ, Irvine AJ, Sood R, et al. Effect of psychological therapy on disease activity, psychological comorbidity, and quality of life in inflammatory bowel disease: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol. 2017;2(3):189-199. doi:10.1016/S2468-1253(16)30206-0. Epub 2017 Jan 18. PubMed PMID: 28404134.
- Hyams J, Markowitz J, Otley A, et al. Pediatric Inflammatory Bowel Disease Collaborative Research Group. Evaluation of the pediatric crohn disease activity index: a prospective multicenter experience. J Pediatr Gastroenterol Nutr. 2005;41(4):416-21. PubMed PMID: 16205508.
- Iturralde E, Adams RN, Barley RC, et al. Implementation of Depression Screening and Global Health Assessment in Pediatric Subspecialty Clinics. J Adolesc Health. 2017;61(5):591-598. doi: 10.1016/j.jadohealth.2017.05.030. Epub 2017 Aug 19. PubMed PMID: 28830798.
- Kroenke K, Spitzer RL, Williams JB. The Patient Health Questionnaire-2: validity of a two-item depression screener. Med Care. 2003;41(11):1284-92. PubMed PMID: 14583691.
- Kroenke K, Spitzer RL, Williams JB, et al. Anxiety disorders in primary care: prevalence, impairment, comorbidity, and detection. Ann Intern Med.2007;146(5):317-25. PubMed PMID: 17339617.
- Levy RL, Van Tilburg MA, Langer SL, et al. Effects of a cognitive behavioral therapy intervention trial to improve disease outcomes in children with inflammatory bowel disease. Inflammatory bowel diseases. 2016;22(9), 2134-2148.
- Mackner LM, Greenley RN, Szigethy E, et al. Psychosocial issues in pediatric inflammatory bowel disease: report of the North American Society for Pediatric Gastroenterology, Hepatology, and Nutrition. J Pediatr Gastroenterol Nutr. 2013;56(4):449-58. PubMed PMID: 23287808.
- Monaghan M, Singh C, Streisand R, et al. Screening and identification of children and adolescents at risk for depression during a diabetes clinic visit. Diabetes spectrum 2010;23(1):25-31.
- McCombie AM, Mulder RT, Gearry RB. How IBD patients cope with IBD: a systematic review. J Crohns Colitis. 2013;7(2):89-106. doi: 10.1016/j.crohns.2012.05.021. Epub 2012 Jun 18. Review. PubMed PMID: 22718016.
- Mossman SA, Luft MJ, Schroeder HK, et al. The Generalized Anxiety Disorder 7-item scale in adolescents with generalized anxiety disorder: Signal detection and validation. Ann Clin Psychiatry. 2017;29(4):227-234A. PubMed PMID: 29069107.
- Muris P, Meesters C, van den Berg F. The Strengths and Difficulties Questionnaire (SDQ)--further evidence for its reliability and validity in a community sample of Dutch children and adolescents. Eur Child Adolesc Psychiatry. 2003;12(1):1-8. PubMed PMID: 12601558.
- Quittner AL, Abbott J, Georgiopoulos AM, et al. Cystic Fibrosis Foundation and European Cystic Fibrosis Society consensus statements for screening and treating depression and anxiety. Thorax. 2016;71(1):26-34. PubMedPMID: 26452630;
- Ramsawh HJ, Chavira DA, Kanegaye JT, et al. Screening for adolescent anxiety disorders in a pediatric emergency department. Pediatr Emerg Care. 2012;28(10):1041-7. PubMed PMID: 23023473.
- Reigada LC, Hoogendoorn CJ, Walsh LC, et al. Anxiety symptoms and disease severity in children and adolescents with Crohn disease. J Pediatr Gastroenterol Nutr. 2015;60(1):30-5. doi: 10.1097/MPG.0000000000000552. PubMed PMID: 25187105.
- Reigada LC, Satpute A, Hoogendoorn CJ, et al. Patient-reported Anxiety: A Possible Predictor of Pediatric Inflammatory Bowel Disease Health Care Use. Inflamm Bowel Dis. 2016;22(9):2127-33. doi: 10.1097/MIB.0000000000000864. PubMed PMID: 27482980.
- Richardson LP, Rockhill C, Russo JE, et al. Evaluation of the PHQ-2 as a brief screen for detecting major depression among adolescents. Pediatrics. 2010;125(5):e1097-103. PubMed PMID: 20368315.
- Silverstein J, Klingensmith G, Copeland Ket al. Care of children and adolescents with type 1 diabetes: a statement of the American Diabetes Association. Diabetes Care. 2005;28(1):186-212. PubMed PMID: 15616254.
- Sudhanthar S, Thakur K, Sigal Y, et al. Improving validated depression screen among adolescent population in primary care practice using electronic health records (EHR). BMJ Qual Improv Rep. 2015;4(1). pii: u209517.w3913. PubMed PMID: 26734415.
- Szigethy E, Kenney E, Carpenter J, et al. Cognitive-behavioral therapy for adolescents with inflammatory bowel disease and subsyndromal depression. J Am Acad Child Adolesc Psychiatry. 2007;46(10):1290-8. PMID: 17885570.
- Timmer A, Preiss JC, Motschall E, et al. Psychological interventions for treatment of inflammatory bowel disease. Cochrane Database Syst Rev. 2011;(2):CD006913. doi: 10.1002/14651858.CD006913.pub2. Review. PubMed PMID: 21328288.
- Turner D, Otley AR, Mack D, et al. Development, validation, and evaluation of a pediatric ulcerative colitis activity index: a prospective multicenter study. Gastroenterology. 2007;133(2):423-32. PMID: 17681163.
- Wise EA. Methods for analyzing psychotherapy outcomes: a review of clinical significance, reliable change, and recommendations for future directions. J Pers Assess. 2004;82(1):50-9. PMID: 14979834.
Evidence tabellen
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Szigethy, 2014 |
Type of study: randomised parallel group trial
Setting: outpatients from two tertiary hospitals
Country: United States of America
Source of funding: National institute of Mental Health |
Inclusion criteria screening for depression:
Inclusion criteria randomisation:
Exclusion criteria:
N total at baseline:
Intervention: 110 Control: 107
Important prognostic factors2: Crohn’s disease: I: 79% C:74%
Sex: I: 49.1% Male C: 44.9% Male
Depression severity: I: 45.1 (SD 12.1) C: 48.9 (SD 12.8)
Disease duration (months) I: 22.8 (SD 30.4) C: 23.7 (SD 28.5)
Group differences at baseline: - white race (CBT 94.6%, SNDT 84.1%), - surgical resection rate (CBT 5.6%, SNDT 14.2%) - baseline depressive severity: CDRS-R score CBT 45.1 vs SNDT 48.9/, |
Describe intervention (treatment/procedure/test):
Cognitive behavioural therapy (CBT)
PASCET-PI CBT protocol
|
Describe control (treatment/procedure/test):
Cognitive behavioural therapy (CBT) (n=110)
Supportive non-directive therapy (SNDT) protocol: (n=107)
|
Length of follow-up: 3 months
Loss-to-follow-up: Intervention:28 ( 25%) Reasons not reported
Control:36 (33.6%) N (%) Reasons not reported
*N=1 unspecified
Incomplete outcome data: see loss to follow up
|
Outcome measures and effect size (include 95%CI and p-value if available):
Depression severity CDRS-R score (clinician rated) Improvement CBT and SDNT group (no group difference, β 2.55 (0.96-6.06), z=1.42, p=0.16)
Raw means CDRS-R score: CBT baseline 45.1 (SD 12.1)à 3 months 29.11 SDNT 48.9 (SD 12.8)à 3 months 29.11
Prepost effect size (cohens D) - CBT=1.31 - SNDT: 1.30
Treatment respons (CDRS ≤28): CBT: 53.5 vs 47.1 % SNDT (OR 1.29 (0.71-2.36), p>0.05)
Remission depression: CBT: 67.7 vs 63.2 % SNDT (OR 1.22 (0.66-2.28), p>0.05)
Psychosocial functioning (CGAS) Improvement CBT and SDNT group (no group difference, β -1.46 (-2.96-0.04), z=1.90, p=0.06)
Health Related Quality of Life. Improvement CBT and SDNT group (no group difference, β -6.42 (-13.28-0.45), z=1.83, p=0.07)
Disease activity Improvement in CBT and SDNT group (group difference favouring CBT, β 0.31 (-0.009-0.62), z=2.01, p=0.04)
Raw means:
Baseline PCDAI CBT: 21 (SD 16.2), à 3 months 9.49 (SD 2.48)
Baseline PCDAI SNDT: 25.9 (3.8) à 15.30 (12.11)
Baseline PUCAI CBT: 23.3 (SD 24.9) à 3 months SNDT 11.39 (SD 12.7)
Baseline PUCAI SNDT 22.4 (16.9) à 3 months 11.47 (SD 16.56) |
|
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-04-2019
Beoordeeld op geldigheid : 17-12-2018
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2023 bepaalt het bestuur van de Nederlandse Vereniging voor Kindergeneeskunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Kindergeneeskunde is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het doel van de richtlijn is om een effectieve en efficiënte diagnostiek en behandeling te realiseren bij kinderen met een inflammatoire darmziekte (de ziekte van Crohn of colitis ulcerosa (IBD, Inflammatory Bowel Disease).
Doelgroep
Deze richtlijn is bedoeld voor kinderartsen, kinderartsen-MDL, MDL-artsen, IBD-verpleegkundig specialisten, IBD-physician assistants en IBD-verpleegkundigen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2016 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor kinderen en adolescenten met inflammatoire darmziekten.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Prof. Dr. J.C. Escher, kinderarts maag-darm-leverziekten, werkzaam in het Erasmus Medisch Centrum-Sophia Kinderziekenhuis te Rotterdam, NVK, voorzitter
- Drs. M.A. Aardoom MSc, arts-onderzoeker, werkzaam in het Erasmus Medisch Centrum-Sophia Kinderziekenhuis te Rotterdam, NVK
- Drs. G. van den Brink MSc, arts-onderzoeker, werkzaam in het Erasmus Medisch Centrum-Sophia Kinderziekenhuis te Rotterdam, NVK
- Dr. K. Diederen, MSc, onderzoeker binnen de kindergeneeskunde, werkzaam in het Academisch Medisch Centrum-Emma Kinderziekenhuis te Amsterdam, NVK
- M.A.C. van Gaalen, verpleegkundig specialist kinder-MDL, werkzaam in het Erasmus Medisch Centrum-Sophia Kinderziekenhuis te Rotterdam, V&VN
- Drs. S. Haisma MSc, arts-onderzoeker, werkzaam in het Universitair Medisch Centrum-Beatrix Kinderkliniek te Groningen, NVK
- Dr. A. Kindermann, kinderarts maag-darm-leverziekten, werkzaam in het Emma Kinderziekenhuis-Emma Kinderziekenhuis te Amsterdam en in het Academisch Medisch Centrum te Amsterdam, NVK
- Drs. M. Oldenziel, klinisch psycholoog, werkzaam in het Gelre ziekenhuis te Apeldoorn, NIP
- Dr. P.F. van Rheenen, kinderarts maag-darm-leverziekten, werkzaam in het Universitair Medisch Centrum-Beatrix Kinderkliniek te Groningen, NVK
- Dr. L. de Ridder, kinderarts maag-darm-leverziekten, werkzaam in het Erasmus Medisch Centrum-Sophia Kinderziekenhuis te Rotterdam, NVK
- Prof. Dr. C.J. van der Woude, maag-darm-leverarts, werkzaam in het Erasmus Medisch Centrum te Rotterdam, NVMDL
Klankbordgroep
De klankbordgroepleden hebben gedurende de ontwikkeling van de richtlijn meegelezen met de conceptteksten en deze becommentarieerd.
- Dr. J. Curvers, klinisch chemicus, werkzaam in het Catharina ziekenhuis te Eindhoven, NVKC
- Dr. W. van Gemert, chirurg, werkzaam in het Universitair Medisch Centrum te Maastricht, NVvH
- Dr. L. Hanff, ziekenhuisapotheker, werkzaam in het Prinses Máxima Centrum te Utrecht, , NVZA
- T. Markus, directeur, werkzaam bij de Crohn en Colitis Ulcerosa Vereniging Nederland te Woerden
- H. Rippen, directeur, werkzaam bij Stichting Kind en Ziekenhuis te Utrecht
- H. van der Wielen, verpleegkundig specialist kinder-MDL, werkzaam in het Jeroen Bosch Ziekenhuis te Den Bosch, V&VN
Met ondersteuning van:
- Dr. I.M. Mostavaya, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.M.M. Vaes, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Escher |
kinderarts maagdarmleverziekten |
-adviserend arts voor cyberpoli IBD, (onbetaald) -editor voor diverse vaktijdschriften, (onbetaald) -Bestuurslid NVGE (onbetaald) -Voorzitter kinder-IBD-werkgroep (KICC; sectie kinder-MDL, NVK) (onbetaald)
|
-Deelname aan en advisory board member register studie DEVELOP (sponsor is Janssen) -Deelname aan en advisory board member register studie CAPE (sponsor is Abbvie) -Deelname aan TISKIDS studie (ZONMW, co-sponsor is Pfizer) -Biomarkers studie (co-sponsor is MSD) |
Geen actie |
|
Aardoom |
Arts-onderzoeker in Erasmus MC Sophia op gebied van IBD bij kinderen |
Bestuurslid (secretaris) van Young-ICC (onbetaald)
|
- |
Geen actie |
|
Van den Brink |
Arts-onderzoeker in Erasmus MC-Sophia op het onderzoek HAPPY-IBD (angst/depressieklachten bij jongeren met IBD) |
|
- |
Geen actie |
|
Diederen |
Onderzoeker |
Onderzoeker in het Academisch Medisch Centrum-Emma op gebied van IBD bij kinderen |
- |
Geen actie |
|
Van Gaalen |
Verpleegkundig specialist kinder-MDL |
- |
- |
Geen actie |
|
Haisma |
Arts-onderzoeker |
Arts-onderzoeker in UMC Groningen op gebied van IBD bij kinderen |
- |
Geen actie |
|
Kindermann |
kinderarts maagdarmleverziekten |
-Lid commissie voeding NVK (onbetaald) -Lid commissie ondervoeding NVK (onbetaald) -Penningmeester kinder-IBD werkgroep (KICC; sectie kinder-MDL, NVK)(onbetaald)
|
-Deelname DEVELOP register studie (sponsor is Janssen) -Deelname CAPE register studie (sponsor is Abbvie) |
Geen actie |
|
Oldenziel |
Klinisch Psycholoog Hoofd vakgroep psychologie kind & jeugd Opleider |
-Docent aan de opleiding tot Gezondheidszorgpsycholoog, betaald -Docent/trainer, agressietraining, betaald -Deelnemer werkgroep NOLK, onbetaald |
- |
Geen actie |
|
Van Rheenen |
kinderarts maagdarmleverziekten |
-Associate Professor International Child Health (onbetaald) -Coordinator Tropical Medicine Master Education (onbetaald) -Secretaris kinder-IBD werkgroep (KICC; sectie kinder-MDL, NVK) (onbetaald) -Voorzitter P-ECCO (Paediatricians of European Crohn's and Colitis Organisation) (onbetaald) |
-SELFIE-studie, gefinancierd door Buhlmann Laboratories AG -GRINCH-studie, gefinancierd door CisBo BioAssays -CACATU-studie, gefinancierd door CisBo BioAssays |
Geen actie |
|
De Ridder |
kinderarts maagdarmleverziekten |
Lid kinder-IBD werkgroep (KICC; sectie kinder-MDL, NVK) (onbetaald) Secretaris ESPGHAN IBD Porto werkgroep (onbetaald) Penningmeester PIBDnet (onbetaald) Bestuurslid P-ECCO (Paediatricians of European Crohn's and Colitis Organisation) (onbetaald)
|
-Deelname DEVELOP register studie (sponsor is Janssen) -Deelname CAPE register studie (sponsor is Abbvie) -PI van TISKIDS studie (ZONMW, co-sponsor is Pfizer) -PI van REDUCE RISK (Horizon 2020) studie voor Nederland |
Geen actie |
|
Van Der Woude |
Maag-darm-leverarts |
-Lid educatie commissie UEG (onbetaald) -Lid scientific commissie ECCO (onbetaald) -Secretaris NVGE (onbetaald) |
- ZonMw - Pfizer - Danone - Tramedico |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een enquête onder leden van de CCUVN, welke door de CCUVN is geïnitieerd, en waaraan een aantal werkgroepleden inhoudelijk heeft meegewerkt. Het verslag hiervan is besproken in de werkgroep en de belangrijkste overwegingen zijn verwerkt in de richtlijn. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de CCUVN, Stichting Kind en Ziekenhuis en de Patiëntenfederatie Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn(module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (Nederlandse Vereniging voor Kindergeneeskunde, 2008) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door belanghebbende partijen tijdens de Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: 1) klinische relevantie; 2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit; 3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html. 2012.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Zoekverantwoording
|
Embase.com |
2005 |
1971 |
|
Medline Ovid |
1292 |
380 |
|
Web of science |
957 |
381 |
|
Cochrane central |
40 |
0 |
|
psycinfo ovid |
361 |
213 |
|
Google scholar |
200 |
105 |
|
Total |
4855 |
3050 |
Embase.com
('inflammatory bowel disease'/exp OR ((inflamma* NEAR/3 bowel* NEAR/3 disease*) OR ibd OR crohn* OR (ulcer* NEAR/3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/3 Ileitis)):ab,ti) AND ('anxiety'/de OR 'anxiety disorder'/exp OR 'fear'/de OR 'depression'/exp OR 'antidepressant agent'/de OR 'cognitive therapy'/de OR 'emotion'/de OR 'school stress'/de OR 'academic achievement'/exp OR 'school reentry'/de OR 'absenteeism'/de OR 'self esteem'/de OR 'self concept'/de OR 'body image'/de OR 'social interaction'/exp OR 'family life'/de OR 'family relation'/exp OR 'family coping'/de OR 'family functioning'/de OR 'family interaction'/de OR 'psychiatric treatment'/de OR psychotherapy/exp OR 'counseling'/de OR 'family counseling'/de OR 'parent counseling'/de OR 'patient counseling'/de OR 'e-counseling'/de OR 'psychoeducation'/de OR 'psychosocial disorder'/de OR 'psychological wellbeing assessment'/exp OR 'psychological well being'/de OR 'mental health'/de OR 'conduct disorder'/de OR stress/exp OR 'stress management'/de OR (anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/3 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/3 achieve*) OR (self NEXT/1 (esteem OR image)) OR body-imag* OR (social* NEAR/3 (interact* OR function* OR relation*)) OR (famil* NEAR/3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/3 (relation*))):ab,ti) AND (child/exp OR adolescent/exp OR 'young adult'/de OR adolescence/exp OR 'child behavior'/de OR 'child parent relation'/de OR pediatrics/exp OR childhood/exp OR 'child development'/de OR 'child growth'/de OR 'child health'/de OR 'child health care'/exp OR 'child care'/exp OR 'childhood disease'/exp OR 'child psychiatry'/de OR 'child psychology'/de OR 'pediatric ward'/de OR 'pediatric hospital'/de OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEXT/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/3 (adult* OR women OR men OR woman OR man))):ab,ti)
Medline Ovid
(exp "Inflammatory Bowel Diseases"/ OR ((inflamma* ADJ3 bowel* ADJ3 disease*) OR ibd OR crohn* OR (ulcer* ADJ3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* ADJ3 Ileitis)).ab,ti.) AND (exp "anxiety"/ OR exp "Anxiety Disorders"/ OR "fear"/ OR "depression"/ OR "Depressive Disorder"/ OR "Depressive Disorder, Major"/ OR "Antidepressive Agents"/ OR "Cognitive Therapy"/ OR "emotions"/ OR "Absenteeism"/ OR "Self Concept"/ OR "body image"/ OR "Interpersonal Relations"/ OR exp "Family Relations"/ OR Psychotherapy/ OR "counseling"/ OR "mental health"/ OR "Mind-Body Therapies"/ OR "Conduct Disorder"/ OR "Stress, Psychological"/ OR (anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) ADJ3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school ADJ3 (problem* OR attend* OR reentry OR absen*)) OR (academic ADJ3 achieve*) OR (self ADJ (esteem OR image)) OR body-imag* OR (social* ADJ3 (interact* OR function* OR relation*)) OR (famil* ADJ3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) ADJ3 (relation*))).ab,ti.) AND (exp Child/ OR exp Infant/ OR exp Adolescent/ OR exp "Child Behavior"/ OR exp "Parent Child Relations"/ OR exp "Pediatrics"/ OR exp "Child Welfare"/ OR "Child Development"/ OR exp "Child Health Services"/ OR exp "Child Care"/ OR "Child Psychiatry"/ OR "Psychology, Child"/ OR "Hospitals, Pediatric"/ OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under ADJ age*) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) ADJ3 (adult* OR women OR men OR woman OR man))).ab,ti.)
psycinfo ovid
(((inflamma* ADJ3 bowel* ADJ3 disease*) OR ibd OR crohn* OR (ulcer* ADJ3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* ADJ3 Ileitis)).ab,ti.) AND (100.ag. OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under ADJ age*) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) ADJ3 (adult* OR women OR men OR woman OR man))).ab,ti.)
Cochrane central
(((inflamma* NEAR/3 bowel* NEAR/3 disease*) OR ibd OR crohn* OR (ulcer* NEAR/3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/3 Ileitis)):ab,ti) AND ((anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/3 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/3 achieve*) OR (self NEXT/1 (esteem OR image)) OR body-imag* OR (social* NEAR/3 (interact* OR function* OR relation*)) OR (famil* NEAR/3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/3 (relation*))):ab,ti) AND ((adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEXT/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/3 (adult* OR women OR men OR woman OR man))):ab,ti)
Web of science
TS=((((inflamma* NEAR/2 bowel* NEAR/2 disease*) OR ibd OR crohn* OR (ulcer* NEAR/2 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/2 Ileitis))) AND ((anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/2 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/2 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/2 achieve*) OR (self NEAR/1 (esteem OR image)) OR body-imag* OR (social* NEAR/2 (interact* OR function* OR relation*)) OR (famil* NEAR/2 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/2 (relation*)))) AND ((adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEAR/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/2 (adult* OR women OR men OR woman OR man)))) )
Google scholar
"inflammatory bowel disease"|crohn|"ulcerative colitis" anxiety|fear|depression|depressive|emotion|"cognitive|behavior therapy"|psychotherapy|stress|"school problems"|"self esteem"| "social|family life|interaction" adolescents|adolescence|infants|children
Selectie artikelen
Flowchart selectie literatuur
|
Database |
Zoektermen |
Totaal |
|
Embase |
Embase.com ('inflammatory bowel disease'/exp OR ((inflamma* NEAR/3 bowel* NEAR/3 disease*) OR ibd OR crohn* OR (ulcer* NEAR/3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/3 Ileitis)):ab,ti) AND ('anxiety'/de OR 'anxiety disorder'/exp OR 'fear'/de OR 'depression'/exp OR 'antidepressant agent'/de OR 'cognitive therapy'/de OR 'emotion'/de OR 'school stress'/de OR 'academic achievement'/exp OR 'school reentry'/de OR 'absenteeism'/de OR 'self esteem'/de OR 'self concept'/de OR 'body image'/de OR 'social interaction'/exp OR 'family life'/de OR 'family relation'/exp OR 'family coping'/de OR 'family functioning'/de OR 'family interaction'/de OR 'psychiatric treatment'/de OR psychotherapy/exp OR 'counseling'/de OR 'family counseling'/de OR 'parent counseling'/de OR 'patient counseling'/de OR 'e-counseling'/de OR 'psychoeducation'/de OR 'psychosocial disorder'/de OR 'psychological wellbeing assessment'/exp OR 'psychological well being'/de OR 'mental health'/de OR 'conduct disorder'/de OR stress/exp OR 'stress management'/de OR (anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/3 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/3 achieve*) OR (self NEXT/1 (esteem OR image)) OR body-imag* OR (social* NEAR/3 (interact* OR function* OR relation*)) OR (famil* NEAR/3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/3 (relation*))):ab,ti) AND (child/exp OR adolescent/exp OR 'young adult'/de OR adolescence/exp OR 'child behavior'/de OR 'child parent relation'/de OR pediatrics/exp OR childhood/exp OR 'child development'/de OR 'child growth'/de OR 'child health'/de OR 'child health care'/exp OR 'child care'/exp OR 'childhood disease'/exp OR 'child psychiatry'/de OR 'child psychology'/de OR 'pediatric ward'/de OR 'pediatric hospital'/de OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEXT/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/3 (adult* OR women OR men OR woman OR man))):ab,ti) |
1971 |
|
Medline Ovid |
(exp "Inflammatory Bowel Diseases"/ OR ((inflamma* ADJ3 bowel* ADJ3 disease*) OR ibd OR crohn* OR (ulcer* ADJ3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* ADJ3 Ileitis)).ab,ti.) AND (exp "anxiety"/ OR exp "Anxiety Disorders"/ OR "fear"/ OR "depression"/ OR "Depressive Disorder"/ OR "Depressive Disorder, Major"/ OR "Antidepressive Agents"/ OR "Cognitive Therapy"/ OR "emotions"/ OR "Absenteeism"/ OR "Self Concept"/ OR "body image"/ OR "Interpersonal Relations"/ OR exp "Family Relations"/ OR Psychotherapy/ OR "counseling"/ OR "mental health"/ OR "Mind-Body Therapies"/ OR "Conduct Disorder"/ OR "Stress, Psychological"/ OR (anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) ADJ3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school ADJ3 (problem* OR attend* OR reentry OR absen*)) OR (academic ADJ3 achieve*) OR (self ADJ (esteem OR image)) OR body-imag* OR (social* ADJ3 (interact* OR function* OR relation*)) OR (famil* ADJ3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) ADJ3 (relation*))).ab,ti.) AND (exp Child/ OR exp Infant/ OR exp Adolescent/ OR exp "Child Behavior"/ OR exp "Parent Child Relations"/ OR exp "Pediatrics"/ OR exp "Child Welfare"/ OR "Child Development"/ OR exp "Child Health Services"/ OR exp "Child Care"/ OR "Child Psychiatry"/ OR "Psychology, Child"/ OR "Hospitals, Pediatric"/ OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under ADJ age*) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) ADJ3 (adult* OR 381women OR men OR woman OR man))).ab,ti.) |
380 |
|
Psychinfo Ovid |
(((inflamma* ADJ3 bowel* ADJ3 disease*) OR ibd OR crohn* OR (ulcer* ADJ3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* ADJ3 Ileitis)).ab,ti.) AND (100.ag. OR (adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under ADJ age*) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) ADJ3 (adult* OR women OR men OR woman OR man))).ab,ti.) |
213 |
|
Cochrane |
(((inflamma* NEAR/3 bowel* NEAR/3 disease*) OR ibd OR crohn* OR (ulcer* NEAR/3 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/3 Ileitis)):ab,ti) AND ((anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/3 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/3 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/3 achieve*) OR (self NEXT/1 (esteem OR image)) OR body-imag* OR (social* NEAR/3 (interact* OR function* OR relation*)) OR (famil* NEAR/3 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/3 (relation*))):ab,ti) AND ((adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEXT/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/3 (adult* OR women OR men OR woman OR man))):ab,ti) |
0 |
|
Web of Science |
TS=((((inflamma* NEAR/2 bowel* NEAR/2 disease*) OR ibd OR crohn* OR (ulcer* NEAR/2 (colit* OR colorectit*)) OR Ileocolit* OR (Terminal* NEAR/2 Ileitis))) AND ((anxi* OR fear* OR depressi* OR panic* OR ((cogniti* OR psychiatr* OR psycho* OR behav* OR family) NEAR/2 (therap* OR treat* OR intervent* OR screen* OR prevent* OR monitor*)) OR psychotherap* OR psychoeducation* OR emotion* OR antidepress* OR stress* OR distress* OR (school NEAR/2 (problem* OR attend* OR reentry OR absen*)) OR (academic NEAR/2 achieve*) OR (self NEAR/1 (esteem OR image)) OR body-imag* OR (social* NEAR/2 (interact* OR function* OR relation*)) OR (famil* NEAR/2 (coping OR life OR function* OR interact*)) OR counseling OR counselling OR psychosocial* OR conduct-disorder* OR Mind-Body OR relaxation OR mental* OR ((family OR mother* OR father* OR sibling* OR parent*) NEAR/2 (relation*)))) AND ((adolescen* OR infan* OR child* OR kid OR kids OR teen* OR boy* OR girl* OR minors OR underag* OR (under NEAR/1 (age* OR aging)) OR juvenil* OR youth* OR kindergar* OR puber* OR pubescen* OR prepubescen* OR prepubert* OR pediatric* OR paediatric* OR school* OR preschool* OR highschool* OR ((young OR early*) NEAR/2 (adult* OR women OR men OR woman OR man) |
381 |
|
Google Scholar |
"inflammatory bowel disease"|crohn|"ulcerative colitis" anxiety|fear|depression|depressive|emotion|"cognitive|behavior therapy"|psychotherapy|stress|"school problems"|"self esteem"| "social|family life|interaction" adolescents|adolescence|infants|children |
105 |
|
|
|
3050* |
Tabel Exclusie na het lezen van het volledige artikel
