Klinische relevantie negatieve directe antiglobulinetest
Uitgangsvraag
Is vervolgonderzoek geïndiceerd bij een negatieve directe antiglobulinetest (DAT) bij een pasgeborene met klinisch relevante hyperbilirubinemie (TSB > behandelgrens)?
Aanbeveling
Verricht diagnostiek naar (ir)regulaire erytrocytenantistoffen bij de diagnostiek naar de oorzaak van hyperbilirubinemie, omdat dit direct beleidsconsequenties heeft. Hanteer een lagere behandelgrens bij een antistof-gemedieerde afbraak van erytrocyten.
Voor AB0-incompatibele en AB0 compatibele moeder - kind paren geldt:
Behandel het kind met hyperbilirubinemie en een positieve DAT volgens een lagere behandelgrens, tenzij de positieve DAT door bijvoorbeeld anti-D toediening is veroorzaakt (de DAT is dan meestal slechts zwak positief en er is vrij anti-D in plasma of serum van het kind). Verricht vervolgdiagnostiek zoals een eluaat en antistoftiter bepaling tijdens kantooruren.
Voor AB0-incompatibele moeder - kind paren geldt:
Behandel het kind met hyperbilirubinemie en een negatieve DAT volgens een lagere behandelgrens alsof er toch sprake is van hemolyse is door erytrocyten antistoffen in afwachting van aanvullende diagnostiek. Bepaal daarom met spoed vrije antistoffen in het plasma of een eluaat bij een negatieve DAT bij een AB0 incompatibiliteit.
Streef ernaar, indien de voorgestelde diagnostiek niet mogelijk is in het eigen centrum, om < 24 uur de betreffende uitslagen te hebben. Hanteer een normale behandelgrens als er geen antistoffen in het plasma of eluaat kunnen worden aangetoond.
Voor AB0- compatibele moeder - kind paren geldt:
Bij een negatieve DAT bij het kind en een AB0 compatibele moeder en kind is de kans op een antagonisme als oorzaak van de hyperbilirubinemie erg klein. Hanteer de normale behandelgrens (tenzij er andere risicofactoren zijn). Verricht vervolgdiagnostiek zoals een eluaat en antistoftiter bepaling tijdens kantooruren.
Overwegingen
Er bestaan zeer vele artikelen over de (in)directe antiglobulinetest en het eluaat. We verwijzen naar twee ervan (Overbeeke, 2011; Hamer, 2018). In onderstaande tekst staat zeer beknopt enige informatie over de achtergrond van de (in)directe antiglobulinetest en het eluaat. En wordt er antwoord gegeven op de vragen: Kan de DAT fout-negatief of fout-positief zijn, wat zijn hiervan de oorzaken en wat is de rol van de eluaat test?
Achtergrond van de directe en indirecte antiglobulinetest
De directe en indirecte antiglobulinetest (DAT en IAT) zijn testen waarmee de aanwezigheid van antilichamen of complement op respectievelijk de rode bloedcel (RBC) of in het serum kan worden aangetoond (zie Figuur 4.1). De eerste stap in de diagnostiek van een kind met een ernstige hyperbilirubinemie is een bloedgroeptypering en een DAT. Bij een DAT wordt anti-humaanglobuline (anti-IgG) soms in combinatie met anti-complement (anti-C3d) toegevoegd aan de RBCs van de patiënt. Indien agglutinatie ontstaat is de DAT positief en is dit een indicatie voor belading van de erytrocyten met IgG en/of complement. Testen met anti-complement is in het algemeen bij neonaten niet nodig, omdat neonaten vrijwel nooit complement belading op de erytrocyten hebben. Hemolyse wordt veroorzaakt door IgG gemedieerde afbraak.
Kan de DAT fout-negatief zijn en wat zijn hiervan de oorzaken?
Er zijn verschillende oorzaken die kunnen leiden tot een negatieve DAT terwijl er wel antistoffen in het bloed van het kind aanwezig die hemolyse kunnen veroorzaken (fout-negatieve test).
Het komt er eigenlijk allemaal op neer dat er een te lage belading met antistoffen is van de circulerende erytrocyten. Of dit nu komt doordat veel erytrocyten laag gesensibiliseerd zijn door lage expressie, of weinig erytrocyten met hoge belading maar te laag voor detectie in de DAT of hoog gesensibiliseerde erytrocyten die al uit de circulatie verdwenen zijn en laag gesensibiliseerde die over zijn of een combinatie van dit alles, is niet goed vast te stellen. Ergo: Bij een fout-negatieve test zijn er te weinig antistoffen gebonden om in de DAT aan te kunnen tonen. Hieronder staat dat nog eens uitgebreider beschreven:
1. Bij een hyperbilirubinemie veroorzaakt door anti-A en/of anti-B antistoffen kan een negatieve DAT gevonden worden bij het pasgeboren kind terwijl er wel degelijk sprake kan zijn van antistof gemedieerde hemolyse. Dit in tegenstelling tot hyperbilirubinemie die wordt veroorzaakt door irregulaire antistoffen zoals bijvoorbeeld anti-D of anti-E of anti-K of anti-c waarbij de DAT positief zal zijn. De negatieve DAT houdt verband met de relatief zwakke belading van de antistoffen aan de erytrocyten door een relatief lage expressie van de A/B antigenen bij de pasgeborene.
2. Daarnaast komen de A en B antigenen ook op andere weefsels voor in tegenstelling tot bijvoorbeeld de Rh antigenen die alleen tot expressie komen op erytrocyten. Hierdoor kunnen de antistoffen ook op ander plaatsen binden dan aan de erytrocyt. De anti-A of anti-B antistoffen worden als het ware verdund.
3. Bij enorme hemolyse kan de expressie van de A en/of B antigenen op de (nog niet gehemolyseerde) jonge erytrocyten van het kind zo laag zijn, dat er te weinig gebonden antistoffen zijn om gedetecteerd te worden met een DAT. Met een zogenaamd eluaat is het mogelijk de gebonden antistoffen van de cellen te isoleren en te concentreren waarna de aanwezigheid aangetoond kan worden in een IAT (zie figuur 4.1).
Figuur 4.1 DAT, IAT en eluaat (1,2)
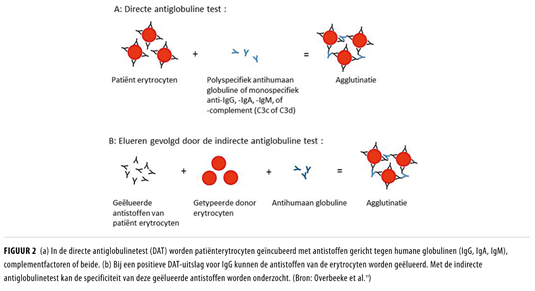
Voor het maken van een eluaat kunnen verschillende methodes gebruikt worden waarbij een vrieseluaat het gevoeligst is voor het opsporen van anti-A of -B antistoffen en een zuur eluaat voor andere antagonismes. Indien in het eluaat specifieke antistoffen worden aangetoond, kan onderzocht worden of de antistoffen ook aanwezig zijn in het serum van het kind en kan een titer van de antistoffen bepaald worden. De antistoftiter kan ook zonder eluaat bepaald worden, maar dit gebeurt niet in elk laboratorium. Ook het maken van een eluaat is voor veel laboratoria geen routinebepaling. Het is zeer arbeidsintensief en vereist speciale kennis en vaardigheden. Als deze diagnostiek naar erytrocytenimmunisatie uitbesteed wordt (bijvoorbeeld aan Sanquin of aan een laboratorium gelieerd aan een universitair ziekenhuis), dan laat de uitslag van het eluaat soms even op zich wachten.
Wat betekent een positieve DAT?
Een positieve DAT betekent niet per se dat er hemolyse is. Vooral zwak positieve reacties kunnen veroorzaakt worden door aspecifieke binding van plasma-eiwitten aan de RBC van het kind. Ook kan anti-D, afkomstig van eerder toegediende immunoprofylaxe aan moeder, resulteren in een positieve DAT bij het kind. Vervolgonderzoek zal moeten plaatsvinden om de specificiteit van de antistoffen vast te stellen en daarmee een inschatting van het klinisch belang. Het bepalen van de specificiteit van antistoffen kan met een eluaat.
Welk vervolgonderzoek is geïndiceerd bij een negatieve DAT?
De DAT is niet 100% sensitief en specifiek. Bij het interpreteren van de DAT is het belangrijk informatie te hebben over de mogelijkheid van een AB0 (in)compatibiliteit tussen moeder en kind. Een negatieve DAT bij een AB0 incompatibiliteit is niet informatief; er kan wel degelijk een hemolyse op basis van erytrocytenantistoffen aan de hyperbilirubinemie ten grondslag liggen. Een negatieve DAT bij een moeder die AB0 compatibel is met haar kind maakt de kans op een antagonisme als oorzaak van de hyperbilirubinemie heel erg klein.
Indien er sterke verdenking is op hemolyse t.g.v. erytrocytenantistoffen is nader onderzoek met een eluaat en titer bepaling van vrije antistoffen in plasma of serum van het kind aangewezen. Omdat hemolyse op basis van erytrocytenantistoffen een risicofactor is voor bilirubine geassocieerde hersenschade, wordt de TSB behandelgrens lager.
Indien de voorgestelde diagnostiek niet mogelijk is in het eigen centrum, is het streven om < 24 uur de betreffende uitslagen te hebben.
In afwachting hiervan, is het advies de behandelgrens te verlagen (alsof er sprake is van hemolyse is door erytrocyten antistoffen) indien er sprake is van hyperbilirubinemie in combinatie met AB0 incompabiliteit tussen moeder en kind.
Voor de interpretatie van de DAT en het in te zetten serologisch vervolgonderzoek is het belangrijk twee typen antagonismes te onderscheiden (zie Tabel 4.2):
- Een bloedgroepantagonisme ten gevolge van een AB0 incompatibiliteit tussen moeder en kind.
- Een bloedgroepantagonisme ten gevolge van irregulaire antistoffen zoals anti-D, c, E, K, et cetera.
In beide gevallen is er dus sprake van erytrocytenantistoffen, alleen bij irregulaire antistoffen is er sprake van erytrocytenimmunisatie (de zwangere heeft IgG antistoffen geproduceerd als reactie op foetale antigenen).
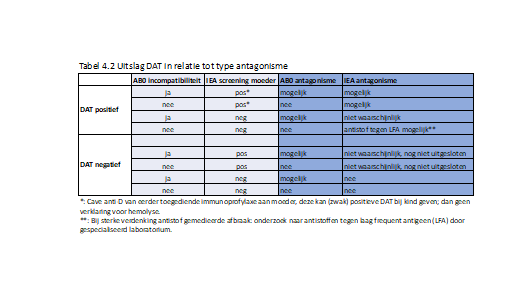
- Bij een bloedgroepantagonisme ten gevolge van een AB0 incompatibiliteit tussen moeder en kind kan de DAT van de erytrocyten van het kind zowel positief als negatief zijn. Dit houdt verband met de lage expressie van de AB0 bloedgroep bij pasgeborenen. Hoewel een eluaat sensitiever is dan een DAT, omdat de antistoffen geconcentreerd worden, kunnen zowel de DAT als het eluaat negatief zijn terwijl er wel antistoffen circuleren bij het kind. Bij de persisterende verdenking op een AB0 antagonisme is het daarom van belang onderzoek te verrichten naar circulerende antistoffen in het serum. Indien anti-A en/of B aantoonbaar zijn, zal actief A0 of B0 antagonisme de oorzaak zijn van de hyperbilirubinemie.
- Bij een bloedgroepantagonisme ten gevolge van irregulaire antistoffen zal de DAT vrijwel altijd positief zijn. Vervolgonderzoek moet ingezet worden om de specificiteit vast te stellen en te bewijzen dat de gevonden antistoffen de oorzaak zijn voor de hemolyse en uit te sluiten dat het geen fout-positieve reactie betreft. Indien de antistoffen bij moeder bekend zijn, kan gericht een eluaat van de erytrocyten van het kind in de IAT getest worden. Met de titerbepaling van deze irregulaire antistoffen in het serum/plasma van het kind kan een inschatting gemaakt worden hoe lang de afbraak mogelijk nog kan aanhouden.
Cave 1: Bij aanwezigheid van een (zwak reactieve) anti-D moet rekening gehouden worden met de mogelijkheid van passief toegediende immuunprofylaxe aan moeder die een zwak positieve DAT bij het kind kan veroorzaken. Deze antistoffen zijn niet verantwoordelijk voor hemolyse bij het kind.
Cave 2: Bij een positieve DAT bij het kind en een negatieve antistofscreening bij moeder en een sterke verdenking op immuungemedieerde hemolyse kan vervolgonderzoek geïndiceerd zijn naar de aanwezigheid van een antistof tegen een laagfrequent antigeen. Dit onderzoek zal tijdens kantoortijden (dus niet acuut) in een gespecialiseerd laboratorium moeten plaats vinden.
Indien de DAT negatief is en er is geen AB0 incompatibiliteit tussen moeder en kind is, is de aanwezigheid van een antistofgemedieerde afbraak onwaarschijnlijk. Eventueel kan de gevoeligheid van het serologisch onderzoek verbeterd worden door een eluaat van de erytrocyten van het kind te testen in de IAT met een screeningspanel. Dit onderzoek zal tijdens kantooruren (dus niet acuut) in een gespecialiseerd laboratorium moeten plaats vinden.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Vanuit epidemiologisch onderzoek naar de lange termijn uitkomsten van kinderen met een ernstige hyperbilirubinemie is bekend (maar onbegrepen) dat kinderen met hemolyse op basis van erytrocytenantistoffen een slechtere neurologische uitkomst hebben. In voorkomende gevallen zal bij het kind een lagere behandelgrens gehanteerd worden. Een behandeling of intensivering ervan zal dus eerder geïndiceerd zijn bij een hyperbilirubinemie op basis van erytrocytenantistoffen.
Bij elk kind met een ernstige hyperbilirubinemie wordt regelmatig bloed afgenomen. Hierbij hoort ook bloed voor de typering van de bloedgroep van het kind en de screening op antistoffen. De titerbepaling van antistoffen is een belangrijke parameter met betrekking tot het voorspellen van het beloop van de hyperbilirubinemie. Een eluaat ten behoeve van de typering van de antistoffen kan in hetzelfde bloedsample worden gemeten.
Indien aanvullende diagnostiek (eluaat, antistof bepaling) niet direct verricht kan worden bij een incompatibele bloedgroep van moeder en kind en een negatieve DAT, is het advies de behandelgrens te verlagen (alsof er sprake is van hemolyse is door erytrocyten antistoffen). Zeer waarschijnlijk zal met spoed de aanbevolen diagnostiek kunnen worden ingezet en door intensieve fototherapie zal de kans op een slechtere neurologische uitkomst bij het kind met hemolyse op basis van erytrocytenantistoffen kleiner worden. De keerzijde is dat in dergelijke casus de wisseltherapiegrens ook eerder gepasseerd kan worden. Echter de kans dat dit onder intensieve fototherapie nodig is, wordt zeer klein geacht.
Kosten (middelenbeslag)
De kosten van een DAT, IAT, vrije antistoftiterbepaling (< € 50,-) en een eluaat (circa € 150,-) moeten worden afgewogen tegen de kosten van een intensievere behandeling of zelfs wisseltransfusie als het kind volgens een lagere behandelgrens wordt behandeld (als men deze uitslagen niet weet en het kind toch maar in een hogere risicogroep met een lagere behandelgrenzen indeelt).
Aanvaardbaarheid voor de overige relevante stakeholders
De bloedafname kan enig ongemak veroorzaken, maar is sowieso noodzakelijk voor een adequate diagnose, risico inschatting en behandeling.
Het verrichten van een eluaat is arbeidsintensief, maar de relevantie is duidelijk.
Haalbaarheid en implementatie
De DAT en IAT kunnen in elk ziekenhuis verricht worden. Een eluaat en titers van vrij anti-A of anti-B antistoffen kunnen niet in elk ziekenhuis op elk moment van de dag verricht worden in verband met noodzaak tot specifieke analytische kennis en kunde, benodigde apparatuur en de benodigde tijd. Er zijn specifieke indicaties voor het bepalen van een eluaat bij een kind met een klinisch relevante hyperbilirubinemie.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Wat is de geadviseerde laboratoriumdiagnostiek bij een kind met een klinisch relevante hyperbilirubinemie en verdenking op erytrocyten antistoffen?
Stroomschema diagnostiek verdenking hemolyse door erytrocytantistoffen
Voor de diagnostische stappen verwijzen we naar de stroomschema’s. Het stroomschema begint bij de mogelijkheid van een AB0 incompatibiliteit. Als dit mogelijk is, zal een eluaat (en IAT) en het bepalen van de vrije antistoftiter altijd een logische vervolgstap zijn, die cito verricht dient te worden als de DAT negatief is. Als dat niet kan, dan < 24 uur. Als de DAT positief is, kan het aanvullend onderzoek tijdens kantooruren verricht worden. Een kind met een hyperbilirubinemie en een positieve DAT heeft altijd een lagere behandelgrens. Maar ook bij een fout-negatieve DAT is er een indicatie voor een lagere behandelgrens. Of de DAT fout-negatief is, zal uit het cito aanvullend onderzoek blijken. Als de DAT terecht negatief is, kan de behandelgrens weer veranderd worden.
Als er geen AB0 incompatibiliteit is, bestaat er afhankelijk van de DAT uitslag en de aanwezigheid van maternale irregulaire antistoffen een mogelijk IEA antagonisme. Ook hiervoor geldt: een kind met een hyperbilirubinemie en een positieve DAT heeft een lagere behandelgrens. Een eluaat met screeningspanel, inclusief het antigeen waartegen maternale antistoffen gericht zijn, is geïndiceerd. De DAT zal slechts zeer zelden fout-negatief zijn als er geen AB0 incompatibiliteit is. Het is onwaarschijnlijk dat er een indicatie is voor een lagere behandelgrens; het aanvullend onderzoek hoeft niet met spoed aangevraagd te worden en kan tijdens kantooruren verricht worden.
NB. Bij hyperbilirubinemie is het dus van belang om na te gaan of moeder bekend is met irregulaire erytrocytenantistoffen. Dit kan aangetoond zijn in de reguliere prenatale screening (zie https://www.nvog.nl/wp-content/uploads/2018/03/Erytrocytenimmunisatie-Figuur-1-Beslisschema-diagnostiekcorrmvp-juli-2011.pdf) of door postnataal onderzoek (aangewezen bij een negatieve screening).
Naast serologisch onderzoek om vast te stellen of bij een vrouw erytrocytenantistoffen aanwezig zijn moet door het typerend laboratorium de landelijke database TRIX “transfusieregister irregulaire antistoffen en kruisproefproblemen” geraadpleegd worden. Alle ziekenhuis/transfusielaboratoria in Nederland zijn aangesloten op TRIX en kunnen deze database raadplegen. Laboratoria waar ooit antistoffen zijn vastgesteld voeren deze gegevens in, tenzij de betreffende persoon hiertegen bezwaar heeft gemaakt.
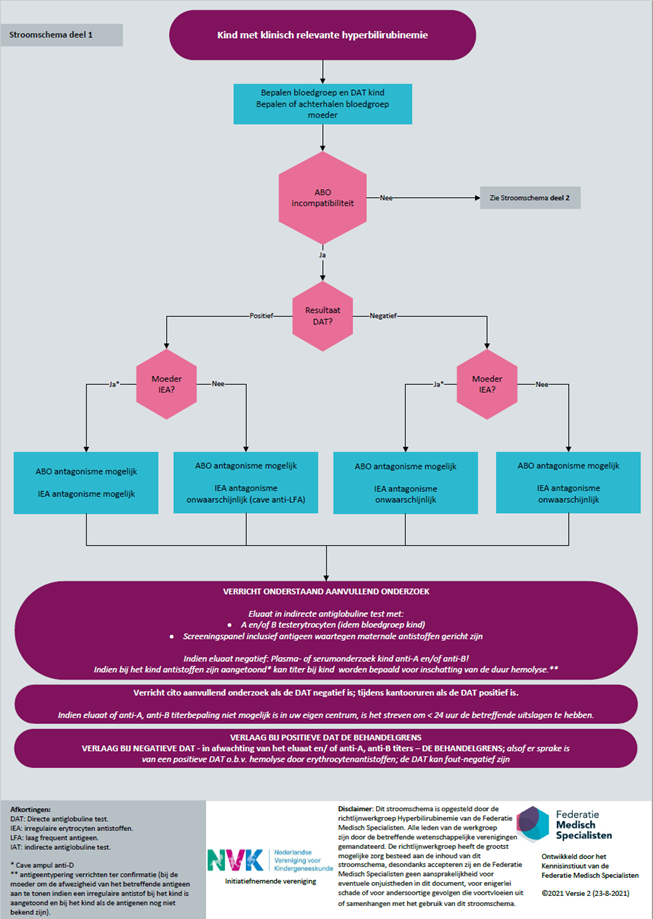
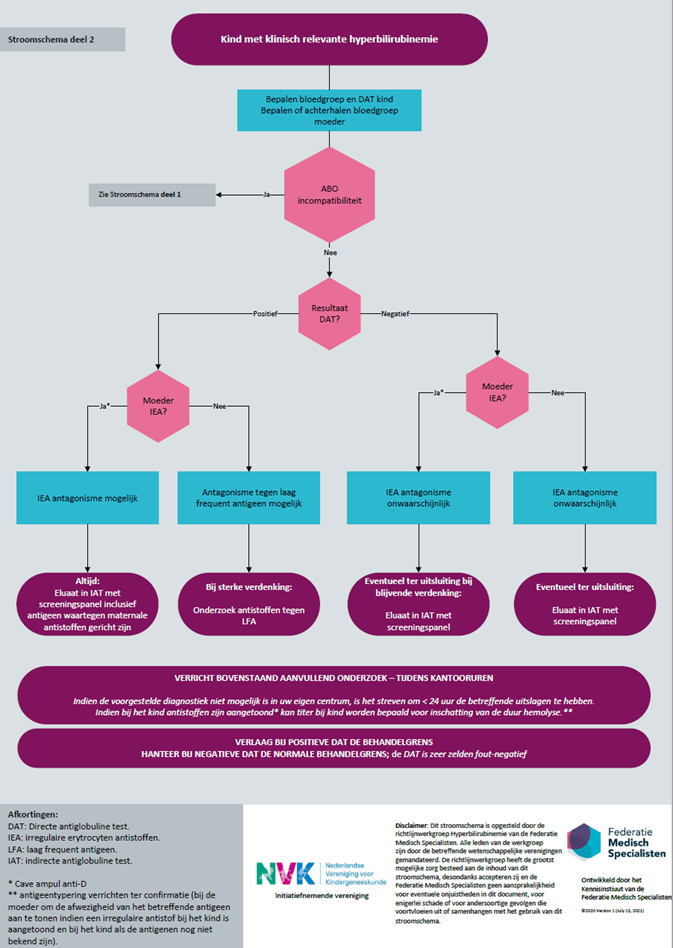
Onderbouwing
Hemolyse bij de foetus en/of pasgeborene kan optreden wanneer maternaal IgG geproduceerd wordt gericht tegen foetale erytrocyt antigenen. Door passage via de placenta kunnen deze de antigenen op de rode bloedcel (RBC) van het kind binden, waarna hemolyse op kan treden. De meest relevante zijn de Rh antigenen (voornamelijk D, c en E) en Kell antigenen. Meest frequent voorkomend is tegenwoordig - na de invoering van toediening van anti-D aan Rhesus negatieve zwangeren - hemolyse ten gevolge van AB0 incompatibiliteit. AB0 incompatibiliteit tussen moeder en kind treedt op in 15 tot 25% van de zwangerschappen. Hemolyse ten gevolge van AB0 incompatibiliteit is veel minder frequent, verloopt meestal milder en is pas klinisch relevant na de partus. Dit in tegenstelling tot bijvoorbeeld de Rh en Kell antagonismes die al in utero hemolytische ziekte van de foetus kunnen veroorzaken door erytrocytenimmunisatie. Hiervoor bestaan diverse oorzaken. De anti-A en anti-B antistoffen in het bloed van de moeder zijn grotendeels van de IgM klasse en passeren de placenta niet. Het gevaar voor hemolyse ontstaat door de IgG anti-A en anti-B, die de placenta wel gepasseerd zijn. Echter, de expressie van AB0 antigenen op de RBC van het kind bij de geboorte is nog laag, waardoor minder kans op het binden van IgG anti-A en/of anti-B op de RBC. Daarnaast zijn ongebonden A en B antigenen in het plasma aanwezig bij veel non-0 kinderen (de zogeheten “secretors”). Deze vrije antigenen zullen eventuele IgG anti-A en anti-B antistoffen wegvangen (waardoor ze niet ook nog aan een RBC kunnen binden).
Als kinderen in de eerste levensweek opgenomen worden in verband met geelzien en een te hoge totaal serumbilirubine (TSB) concentratie, zal ook onderzoek worden ingezet naar hemolyse door erytrocytenantistoffen. Enerzijds om een verklaring voor de hyperbilirubinemie te krijgen. Anderzijds omdat hemolyse ten gevolge van erytrocytenantistoffen (ook wel ‘actief bloedgroepantagonisme’ genoemd) een risicofactor is voor bilirubine neurotoxiciteit door een nog onverklaard mechanisme (Kaplan, 2014). Kinderen met een hyperbilirubinemie waarbij er sprake is van hemolyse op basis van erytrocytenantistoffen (ten gevolge van IgG anti-A, anti-B, of irregulaire antistoffen) worden dus eerder behandeld; ze hebben een lagere behandelgrens. Diagnostiek naar hemolyse op basis van erytrocytenantistoffen dient daarom vlot verricht te worden. Dit gebeurt onder andere door het bepalen van de bloedgroep, erytrocytenantistoffen en de zogenaamde directe antiglobuline test (DAT of Coombs’ test) bij het kind.
In de veldraadpleging voorafgaand aan de formulering van de uitgangsvragen ten behoeve van de revisie van deze richtlijn, werd gediscussieerd over de onduidelijkheid die er is als de DAT negatief is. Kan er dan toch sprake zijn van hemolyse door erytrocyten antistoffen en moet dus een lagere behandelgrens gehanteerd worden?
In onderstaande tekst wordt antwoord gegeven op de vraag of en welk vervolgonderzoek geïndiceerd is bij een negatieve DAT.
|
Zeer laag GRADE |
Het is onduidelijk wat de sensitiviteit en negatief voorspellende waarde van de DAT is voor bloedgroepantagonisme bij à terme neonaten met hyperbilirubinemie.
Bronnen: (Van Rossum, 2015) |
Beschrijving studies
In de paper van Van Rossum (2015) wordt een onderzoek beschreven waarin onder andere de DAT en de eluaat test werden onderzocht bij 282 neonaten; 33 neonaten hadden 4 tot 6 dagen na de geboorte een geelzien score ≥ 4 (de mogelijke scores varieerden van 0 tot 8). Hemolytische ziekte van de foetus of pasgeborene (HZFP) door actief bloedgroepantagonisme werd gedefinieerd als de combinatie van een geelzien score ≥ 4 en serologische aanwijzingen voor erytrocytenimmunisatie door een positieve DAT of positieve eluaat test, in afwezigheid van andere oorzaken voor neonatale geelzucht. Vier van de 33 kinderen hadden deze diagnose; van hen hadden 2 een positieve DAT; bij alle 4 was het eluaat positief.
Resultaten
Van alle 282 kinderen hadden er 21 een positieve DAT test. Bij 4 kinderen was er sprake van HZFP. De sensitiviteit van de DAT was 50% en de specificiteit 93%. De PPV was laag: 10% en de NPV hoog: 99%. Van de DAT bij de kinderen met een geelzien score ≥ 4 was de sensitiviteit 50%, de specificiteit 100%, de PPV 100% en de NPV 94%. De cruciale uitkomst fout-neg. DAT: (1-sens) =50%; (1-NPV) =6%.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat fout-negatieve DAT is met 3 niveaus verlaagd gezien de risk of bias (-1) en imprecisie (zeer gering aantal patiënten) (-2).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat is de voorspellende waarde van een negatieve direct antiglobulinetest (DAT) voor de aanwezigheid van hemolyse ten gevolge van erytrocytenantistoffen (= ‘actief bloedgroepantagonisme’) bij een pasgeborene met klinisch relevante hyperbilirubinemie (TSB > behandelgrens)
P: Pasgeborenen ≥ 35wk AD bij geboorte met klinisch relevante hyperbilirubinemie;
I: DA(G)T/directe Coombs;
C: Uitgebreid onderzoek (inclusief indirecte AT);
O: Bloedgroepantagonisme.
Relevante uitkomstmaten
De werkgroep achtte het percentage fout-negatieve DAT (uitgedrukt als (1-sens) en (1-NPV)) een voor de besluitvorming cruciale uitkomstmaat.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 4 april 2019 met relevante zoektermen gezocht naar systematic reviews, RCTs en observationeel onderzoek gepubliceerd sinds 2008. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 162 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: neonaten met geelzucht werden geïncludeerd bij wie de diagnostische accuratesse van de directe antiglobulinetest werd onderzocht met als referentiestandaard uitgebreider onderzoek naar bloedgroepantagonisme. Op basis van titel en abstract werden in eerste instantie 20 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 19 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en werd één studie definitief geselecteerd.
Resultaten
Eén onderzoek is opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabel. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabel.
- van Rossum, H. H., de Kraa, N., Thomas, M., Holleboom, C. A., Castel, A., & van Rossum, A. P. (2015). Comparison of the direct antiglobulin test and the eluate technique for diagnosing haemolytic disease of the newborn. Practical laboratory medicine, 3, 17-22.
- De Haas M. Uitleg bijzonder laboratoriumonderzoek Immuun-gemedieerde anemie, zoals Auto Immuun Hemolytische Anemie en Hemolytische Ziekte van de Foetus en Pasgeborene. https://hematologienederland.nl/wp-content/uploads/2020/02/Diagnostiek-AIHA-en-HZFP220102012.pdf.
- Erytrocytenimmunisatie en zwangerschap (versie 2.1) https://www.nvog.nl/wp-content/uploads/2018/03/Erytrocytenimmunisatie-en-zwangerschap_.pdf.
- Draaiboek Prenatale Screening Infectieziekten en Erytrocytenimmunisatie (versie 6.0 april 2018). https://www.pns.nl/sites/default/files/2019-12/111815_010453_PSIE_TG.pdf.
- Overbeeke MAMV, Vreeswijk NJ, Ligthart PC, Meulenbroek AJ. Erytrocytenserologie. Amsterdam: Sanquin; 2011.
- Hamer HM, Beckers EA, Henskens YM. Hemolyse: rol van directe antiglobulinetest en eluaat. Ned Tijdschr Geneeskd. 2018;162:D1290.
- Kaplan, M., Bromiker, R., & Hammerman, C. (2014). Hyperbilirubinemia, hemolysis, and increased bilirubin neurotoxicity. In Seminars in perinatology (Vol. 38, No. 7, pp. 429-437). WB Saunders.
- Newman, T. B., Liljestrand, P., Jeremy, R. J., Ferriero, D. M., Wu, Y. W., Hudes, E. S., & Escobar, G. J. (2006). Outcomes among newborns with total serum bilirubin levels of 25 mg per deciliter or more. New England Journal of Medicine, 354(18), 1889-1900.
|
Study reference |
Study characteristics |
Patient characteristics
|
Index test (test of interest) |
Reference test
|
Follow-up |
Outcome measures and effect size |
Comments |
|
van Rossum, 2015 |
Type of study[1]: consecutive neonates
Setting and country: hospital, Netherlands
Funding and conflicts of interest: no funding, no CoI |
Inclusion criteria: Neonates Exclusion criteria: none N=282; jaundice score ≥4 : 33 Prevalence: 4/33
Age: 4-6 days
Sex: not reported
Other important characteristics: |
Describe index test: Direct antiglobulin test
Cut-off point(s): not reported
Comparator test[2]: eluate test
Cut-off point(s): not reported
|
Describe reference test[3]: a jaundice score of ≥4 as well as serological evidence for erythrocyte immunization by DAT or elution techniques, in the absence of other causes of abnormal post-partum jaundice
Cut-off point(s): not reported
|
Time between the index test and reference test: 4-6 days
For how many participants were no complete outcome data available? 0 (0%)
Reasons for incomplete outcome data described? |
Outcome measures and effect size (include 95%CI and p-value if available)4: DAT: sens 50% spec 100% PPV 100% NPV 94%
eluate: sens 100% spec 97% PPV 80% NPV 100% |
Only results of neonates with jaundice score ≥4 presented here.
Reference test contains index and comparison tests |
[1] In geval van een case-control design moeten de patiëntkarakteristieken per groep (cases en controls) worden uitgewerkt. NB; case control studies zullen de accuratesse overschatten (Lijmer et al., 1999)
[2] Comparator test is vergelijkbaar met de C uit de PICO van een interventievraag. Er kunnen ook meerdere tests worden vergeleken. Voeg die toe als comparator test 2 etc. Let op: de comparator test kan nooit de referentiestandaard zijn.
[3] De referentiestandaard is de test waarmee definitief wordt aangetoond of iemand al dan niet ziek is. Idealiter is de referentiestandaard de Gouden standaard (100% sensitief en 100% specifiek). Let op! dit is niet de “comparison test/index 2”.
[4] Beschrijf de statistische parameters voor de vergelijking van de indextest(en) met de referentietest, en voor de vergelijking tussen de indextesten onderling (als er twee of meer indextesten worden vergeleken).
|
Study reference |
Patient selection
|
Index test |
Reference standard |
Flow and timing |
Comments with respect to applicability |
|
van Rossum, 2015 |
Was a consecutive or random sample of patients enrolled? Yes
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Yes
|
Were the index test results interpreted without knowledge of the results of the reference standard? Yes
If a threshold was used, was it pre-specified? No threshold reported
|
Is the reference standard likely to correctly classify the target condition? Unclear
Were the reference standard results interpreted without knowledge of the results of the index test? No
|
Was there an appropriate interval between index test(s) and reference standard? Unclear
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Unclear
Were all patients included in the analysis? Yes |
Are there concerns that the included patients do not match the review question? No
Are there concerns that the index test, its conduct, or interpretation differ from the review question? Unclear
Are there concerns that the target condition as defined by the reference standard does not match the review question? No |
|
CONCLUSION: Could the selection of patients have introduced bias?
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias?
RISK: LOW |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias?
RISK: HIGH |
CONCLUSION Could the patient flow have introduced bias?
RISK: UNCLEAR |
|
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Zonneveld, 2017 |
Populatie voldoet niet aan de PICO |
|
Hemmati, 2016 |
Populatie voldoet niet aan de PICO |
|
Bhat 2012 |
Geen referentietest (C) |
|
Khurana, 2019 |
Geen referentietest (C) |
|
Matteocci, 2018 |
Populatie voldoet niet aan de PICO |
|
Khan, 2018 |
Geen referentietest (C) |
|
Jones, 2017 |
Populatie voldoet niet aan de PICO |
|
Peeters, 2016 |
Populatie voldoet niet aan de PICO |
|
Valsami, 2015 |
Geen referentietest (C) |
|
Özgönenel, 2015 |
Geen referentietest (C) |
|
Oztekin, 2014 |
Geen referentietest (C) |
|
Kaplan, 2014 |
Uitkomst voldoet niet aan de PICO |
|
Shahid, 2012 |
Populatie voldoet niet aan de PICO |
|
Weng, 2011 |
Uitkomst voldoet niet aan de PICO |
|
Karatas, 2011 |
Geen full text |
|
Dillon, 2011 |
Uitkomst voldoet niet aan de PICO |
|
Schutzman, 2010 |
Populatie voldoet niet aan de PICO |
|
Kaplan, 2010 |
Uitkomst voldoet niet aan de PICO |
|
Besser, 2010 |
Populatie voldoet niet aan de PICO |
Conclusie
|
Zeer laag GRADE |
Het is onduidelijk wat de sensitiviteit en negatief voorspellende waarde van de DAT is voor bloedgroepantagonisme bij à terme neonaten met hyperbilirubinemie.
Bronnen: (Van Rossum, 2015) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-06-2022
Beoordeeld op geldigheid : 29-06-2022
De Nederlandse Vereniging voor Kindergeneekunde (NVK) is regiehouder van deze richtlijn en eindverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijnmodules. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied. De geldigheid van richtlijnmodules zal bij herbeoordeling komen te vervallen wanneer nieuwe ontwikkelingen aanleiding geven om een herzieningstraject te starten.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Klinische relevantie van een negatieve directe antiglobulinetest |
NVK |
2022 |
2027 |
5 jaar |
NVK |
|
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor pasgeborenen ≥ 35 weken zwangerschap met hyperbilirubinemie.
Werkgroep
- Dr. C.V. Hulzebos, Kinderarts-neonatoloog, NVK (voorzitter)
- H. Burggraaff, Huisarts, NHG
- Ir. A.J. Dam-Vervloet, Klinisch fysicus, NVKF
- Dr. P.H. Dijk, Neonatoloog, NVK
- G. Fokkens (†2021), Zorgdeskundige, Kraamzorg Het Groene Kruis, B. de Vries beleidsmedewerker KCKZ
- M.C. Hootsen MSc, Verloskundige, KNOV
- Dr. A.R. Hulsmann, Neonatoloog, NVK
- Dr. F.C.J.M Klumper, Gynaecoloog-perinatoloog, NVOG
- Drs. E.A. van der Linden, Arts Maatschappij en Gezondheid, AJN Jeugdartsen Nederland
- R. Mevius, Verpleegkundige, V&VN Vrouw & Kind
- Dr. C.H.H. Schoenmakers, Laboratoriumspecialist klinische chemie/ medisch manager, NVKC
- Dr. T.W. de Vries, Kinderarts, NVK
Meelezers
- Ir. M.S. Toll, Klinisch fysicus audioloog, NVKF
- Stichting Kind en Ziekenhuis
Met ondersteuning van
- Dr. L. Viester, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J.H. van der Lee, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Actie |
|
Mevius |
O&G/OHC verpleegkundige UMCG |
Bestuurslid/penningmeester beroepsvereniging V&VN VOG |
Geen persoonlijke en/of financiële belangen |
Nee |
Nee |
Geen intellectuele belangen |
Nee |
27-8-2018 |
Geen actie |
|
Van der Linden |
Jeugdarts, fulltime verband, Jeugdgezondheidszorg Zuid-Holland West |
Taskforce Rookvrije start Alliantie Nederland Rookvrij deelnemer namens AJN onbetaald, beide |
Geen |
Geen, normaal professioneel niet persoonlijk |
Nee |
Geen |
Nee |
10-10-2018 |
Geen actie |
|
Schoenmakers |
klinisch chemicus Elkerliek |
Stafvoorzitter Elkerliek betaald |
Geen |
Geen |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
24-9-2018 |
Geen actie |
|
Burggraaff |
Praktijkhouder verloskundige huisartspraktijk De Stethoscoop te Weesp |
Huisartsopleider Vumc 0.10 |
Geen |
Geen |
Geen |
Geen |
Geen |
6-11-2018 |
Geen actie |
|
Klumper |
LUMC: gynaecoloog-perinatoloog (100 %) |
Stichting Perined: bestuurslid (onbetaald) |
Geen (financieel) belang bij te formuleren advies, anders dan betere patiëntenzorg. |
Geen |
Geen |
Vanuit betrokkenheid bij foetale therapie, specifiek foetale problematiek tgv erytrocyten-immunisaties (met mogelijk gevolg neonatale bilirubinemie) heeft de afdeling Obstetrie en Foetale Therapie bijzondere expertise opgebouwd. Van directe belangenverstrengeling of van bescherming reputatie/erkenning lijkt me geen sprake. |
Geen |
1-11-2018 |
Geen actie |
|
Hootsen |
1e lijns verloskundige, werkzaam als zelfstandig verloskundig waarneemster bij twee verloskundige praktijken in regio Utrecht en Gelderland. |
Lid van communicatie werkgroep binnen VSV (verloskundig samenwerkingsverband), onbetaald |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
28-11-2018 |
Geen actie |
|
de Vries (TW) |
Kinderarts, Medisch Centrum Leeuwarden. |
onbetaald: redactielid Praktische Pediatrie; lid Wetenschappelijke Advies Raad Geneesmiddelenbulletin, bestuurslid NKFK. |
Geen |
Geen |
Op dit moment participeer ik in onderzoek, een wordt gefinancierd door Zon Mw, de ander door het Longfonds. Beide onderzoeken richten zich niet op het onderwerp |
Geen |
Geen |
24-11-2018 |
Geen actie |
|
Hulzebos* |
Kinderarts-neonatoloog UMC Groningen |
NLS en NALS instructeur (onbetaald) |
Geen |
Neen |
Geen deelname aan voor dit onderwerp relevante onderzoeken. |
Neonatale icterus heeft al enkele jaren mijn aandacht, zoals ook blijkt uit een aantal publicaties in de afgelopen jaren. Ik werk voor het "bilirubine onderzoek" samen met diverse (inter)nationale collega's. Het is mogelijk dat deze publicaties meer aandacht krijgen door het werk van de commissie. |
Neen |
4-12-2018 |
Geen actie |
|
Fokkens |
Zorgdeskundige 24 uur per week Praktijkopleider 8 uur per week Werkgever is Kraamzorg Het Groene Kruis B.V. |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
6-12-2018 |
Geen actie |
|
De Vries (B) |
Beleidsmedewerker 24 uur per week bij KCKZ |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
6-9-2021 |
Geen actie |
|
Dijk |
Kinderarts-neonatoloog, Beatrix Kinderziekenhuis, UMCGroningen. 0.9 FTE, betaald. |
Neonatologie Netwerk Nederland (N3): lid Nederlands Neonatologie Research Netwerk (NNRN) en lid werkgroep benchmarking namens UMC Groningen en lid Raad van Advies N3. onbetaald. Voor aantal multicenterstudies van het NNRN principle investigator in UMCG. onbetaald. Lid Zonmw Cie programma Zwangerschap en Geboorte waarvoor vacatiegelden en reiskostenvergoeding. Lid werkgroep Netwerk Algemene Kindergeneeskunde (Nederlandse Vereniging voor Kindergeneeskunde). onbetaald. Lid Nederlands Kennisnet Farmacotherapie voor kinderen (NKFK) en Kinderformulatium. onbetaald. Lid PEDMED-NL- netwerk voor geneesmiddelen onderzoek met kinderen in Nederland. onbetaald. |
Geen dienstverbanden met bedrijven. Geen betaald adviseurschap. Geen directe financiële belangen. Geen eigendom van patent of product |
Er zijn geen mensen in mijn directe omgeving die baat kunnen hebben bij mijn deelname aan deze richtlijn werkgroep. |
Geen deelname aan onderzoek dat gefinancierd wordt door overheid, fondsen of industrie waarbij de financier belang kan hebben mij de uitkomsten van deze richtlijn ontwikkeling. In 2007-2011 Zonmw doelmatigheidssubsidie en VIMP voor multicenter studie naar de Bilirubine-Albumine Ratio in prematuren (BARTrial) nr: 94507407. |
Als voorzitter van de werkgroep huidige CBO Richtlijn Hyperbilirubinemie heb ik wel een duidelijke relatie met de huidige richtlijn, na het implementatieproces, op praktische wijze weergegeven wordt. De website wordt door mij beheerd en betaald, en kan gezien worden als intellectueel eigendom. ik wordt landelijk en internationaal gezien als expert op gebied van de inhoud van die richtlijn. |
Wij doen in het UMCGroningen, als lever-transplantatie-centrum, uitgebreid onderzoek naar verschillende aspecten van hyperbilirubinemie en leverfalen, zowel bij pasgeborenen, kinderen en volwassenen. Bij pasgeborenen ben ik betrokken bij onderzoek naar hyperbilirunemie zowel qua diagnostiek als behandeling. Via de perinatale audit Nederland hebben wij het thema 'ernstige hyperbilirubinemie' ingebracht, met als doel de oorzaken van ernstige hyperbilirubinemie en de suboptimale zorgaspecten te vinden. Ik maak ook deel uit van de werkgroep. |
16-1-2019 |
Geen actie |
|
Hulsmann |
Kinderarts-neonatoloog , Amphia Ziekenhuis te Breda |
Geen |
Ik verricht wetenschappelijk onderzoek naar fotometrtische bepaling (huidskleur) bij hyperbilirubinemie. Er is een externa partij betrokken maar ik ontvang hievoor geen vergoeding. De methode/techniek zal mogelijk op enig moment (jaren) tot de ontwikkeling van het commercieel verkrijgbaar instrumentarium (transcutane bepaling bilirubinegehalte) leiden. Mijns inziens geen invloed op de richtlijn en geen financieel voordeel voor mij te verwachten. |
Neen |
zie boven |
De literatuursearch en de bijeenkomsten van de commissie helpen mij bij mijn onderzoek: “Skin colour measurements of jaundiced neonates over 30 weeks as an indication of development of hyperbilirubinemia”; een onderzoek naar fotometrische bepaling van hyperbilirubinemia bij zuigelingen”. |
Neen |
23-1-2019 |
Geen actie |
|
Dam-Vervloet |
klinisch fysicus Isala (Zwolle) |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
11-7-2019 |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van patiëntorganisaties voor de Invitational conference. Het verslag hiervan (zie aanverwante producten) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en Stichting Kind en Ziekenhuis en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten in de zorg voor pasgeborenen met hyperbilirubinemie. Tevens zijn er knelpunten aangedragen via een Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De module 1 van de richtlijn hyperbilirubinemie is niet officieel gautoriseerd door de KNOV.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Database |
Zoektermen |
|
Medline (OVID)
2008 – april 2019
|
1 exp Hyperbilirubinemia, Neonatal/ or exp Kernicterus/ or exp Jaundice, Neonatal/ or (neonat* or newborn or infant*).ti,ab,kw. or ((bilirubin* or hyperbilirubin*) adj3 encephalopath*).ti,ab,kw. or (kernicterus or jaundice).ti,ab,kw. (666549) 2 exp Coombs Test/ or coomb*.ti,ab,kw. or (direct adj2 antiglobulin*).ti,ab,kw. or dat.ti,kw. or dagt.ti,kw. (7306) 3 1 and 2 (899) 4 limit 3 to (english language and yr="2008 -Current") (236) 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (387783) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1843241) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3153030) 8 4 and 5 (9) 9 4 and 6 (18) 10 4 and 7 (85) 11 8 or 9 or 10 (101)
= 101 |
|
Embase (Elsevier) |
('neonatal hyperbilirubinemia'/exp OR 'kernicterus'/exp OR 'newborn jaundice'/exp OR neonat*:ab,ti OR newborn:ab,ti OR infant*:ab,ti OR (((bilirubin* OR hyperbilirubin*) NEAR/3 encephalopath*):ab,ti) OR kernicterus:ab,ti OR jaundice:ab,ti)
AND ('coombs test'/exp OR coomb*:ab,ti OR ((direct NEAR/2 antiglobulin*):ab,ti) OR dat:ti OR dagt:ti)
AND (english)/lim AND (2008-2019)/py NOT 'conference abstract':it
Gebruikte filters:
Systematische reviews: ('meta-analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
RCTs: ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it
Observationeel onderzoek: ‘major clinical study’/exp OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
= 141 |
