Instellen van hoortoestellen met de NAL- of DSL-rekenregel bij licht blijvend gehoorverlies
Uitgangsvraag
Welke rekenregel (NAL of DSL) heeft de voorkeur bij de instelling van de versterking van de hoortoestellen bij kinderen van 4 tot 18 jaar met een licht blijvend gehoorverlies in het beste oor?
Aanbeveling
Neem de DSL-v5 rekenregel als uitgangspunt voor het instellen van hoortoestellen bij kinderen van 4 tot 18 jaar met licht blijvend gehoorverlies.
Verifieer of de beoogde versterking ook daadwerkelijk behaald wordt via Real-ear meting (REM).
Ga bij controlebezoeken na of het versterkte geluid niet als te hard ervaren wordt (zie de module 'Diagnostiek voor controle van het auditief functioneren'. Maak in geval van discomfort bij harde geluiden extra gebruik van geluidsbewerkingstechnieken in het hoortoestel, of stap over op een lagere doelversterking zoals NAL.
Overwegingen
Rekenregels DSL en NAL
DSL en NAL onderscheiden zich op een aantal belangrijke punten omdat ze vanuit verschillende uitgangspunten ontwikkeld zijn. DSL is oorspronkelijk ontwikkeld voor kinderen en legt het accent op optimale hoorbaarheid van geluid en dus ook spraak. NAL is gericht op het optimaliseren van het spraakverstaan bij een comfortabele luidheid en houdt zodoende meer rekening met de eigenschappen van spraak. In het algemeen schrijft DSL een hogere versterking voor dan NAL. Dit geldt vooral in het gebied onder 1 kHz en boven 2 kHz. Deze verschillen zijn het duidelijkst in de eerdere versies, DSL i/o en NAL-NL1. De nieuwste versies NAL-NL2 en DSL-v5 zijn meer vergelijkbaar. Zo wordt er bij NAL-NL2 nu ook extra versterking voorgeschreven voor kinderen. Toch zijn er nog steeds duidelijke verschillen in versterking bij kinderen, zoals te zien is in het artikel van Ching (2018).
Wetenschappelijk bewijs voor keuze tussen DSL en NAL
Er is geen bewijs gevonden dat het spraakverstaan in ruis, de spraak- en taalontwikkeling of de subjectieve geluidsbeleving verschilt tussen toepassing van de DSL- of NAL-rekenregel in slechthorende kinderen tussen 4 en 18 jaar. Echter, toepassing van DSL leidt ten opzichte van NAL wel tot het beter kunnen verstaan van zachte spraak in stilte. Ondanks de lage bewijskracht, met name op basis van aantallen en studieopzet, gaat het om een consistent waargenomen verschil. Dit verschil is te verklaren uit de hogere versterking die DSL geeft voor lage geluidsniveaus, resulterend in een betere hoorbaarheid van zachte spraakklanken. Het is bekend dat incidenteel leren een belangrijke rol speelt bij de spraak- en taalontwikkeling van een jong kind. Hiervoor is het verstaan van zachtere spraak op afstand een cruciale voorwaarde. Ook in latere leeftijdsfases zijn er veel dagelijkse situaties, zoals tijdens het volgen van onderwijs, waarin het essentieel is om zachte delen van de spraak goed te kunnen verstaan. Gegeven het bovenstaande krijgt toepassing van DSL in het algemeen de voorkeur boven NAL.
Versterking volgens DSL zorgt in sommige gevallen voor een relatief hoge luidheid van het versterkte geluid. Dit kan tot discomfort leiden, en mogelijk zelfs tot verminderd functioneren in situaties met harde bijgeluiden. Er dient tijdens de hoorrevalidatie daarom structurele monitoring plaats te vinden of het geluid niet als te hard ervaren wordt (zie module Diagnostiek voor controle van het auditief functioneren). Zo nodig kan een rustige opbouw van de versterking worden toegepast, bijvoorbeeld bij een eerste aanpassing, een plots toegenomen gehoorverlies of overgang van NAL op DSL. Als er sprake is van discomfort, dient allereerst overwogen te worden gebruik te maken van de regelbare geluidsbewerkingstechnieken in het hoortoestel. Denk hierbij aan het verhogen van de amplitudecompressie (terugbrengen van de versterking voor hoge intensiteitsniveaus) en/of verlagen van de maximale output (MPO) en aan het (extra) activeren van ruisonderdrukking al of niet voor specifieke luistersituaties/ programma’s (zie module Inzet van de technische mogelijkheden van hoortoestellen). Indien de klachten blijven, is het raadzaam over te gaan op een rekenregel die minder versterking voorschrijft, zoals NAL. Het is belangrijk om vervolgens te evalueren of het verstaan van zachtere spraak niet te veel achteruitgaat na toepassing van deze veranderingen.
Duiding voor de groep met een licht blijvend gehoorverlies
De meeste vergelijkende studies zijn uitgevoerd met kinderen met grotere gehoorverliezen. Voor lichtere gehoorverliezen zullen de verschillen in hoorbaarheid tussen DSL en NAL in het algemeen kleiner zijn en minder impact hebben op het verstaan van spraak. Het risico dat het geluid als te luid ervaren wordt met DSL speelt echter ook voor de lichtere gehoorverliezen een rol. Ching (2010) geeft aan dat er voor lichtere gehoorverliezen vaker een voorkeur is voor de NAL rekenregel, terwijl DSL voor de grotere gehoorverliezen vaker geprefereerd wordt. Dit betekent dat voor kinderen met een licht gehoorverlies eventuele discomfort met DSL extra goed gemonitord moet worden en tijdig overwogen dient te worden om over te stappen naar NAL.
Verificatie
Een essentieel onderdeel van het hoorrevalidatietraject is verificatie. Verificatie is noodzakelijk om zeker te zijn of de rekenregel goed toegepast wordt, dat wil zeggen of de beoogde doelversterking inderdaad behaald wordt. Bij verificatie zijn twee aspecten belangrijk: de methode waarop de output van het hoortoestel gemeten wordt en de gebruikte stimuli (frequentie eigenschappen, temporele eigenschappen en intensiteiten). Deze worden hieronder toegelicht.
De weergave van het geluid bij het trommelvlies wordt bepaald door de versterking/ geluidsbewerking in het hoortoestel, de koppeling naar het oor (toonbocht, hoorslang en oorstukje) en de akoestiek van de gehoorgang. Het is dan ook belangrijk om al deze effecten mee te nemen in de verificatie. Dit vraagt om real-ear-measurement (REM), dat wil zeggen het meten van het geluidsniveau in de gehoorgang. REM kan uitgevoerd worden door het geluidsniveau nabij het trommelvlies te meten met het hoortoestel in-situ (Real-ear aided response (REAR)), eventueel vertaald naar een verschil ten opzichte van het input niveau (Real-ear aided gain (REAG)). Bij jongere of beweeglijke kinderen is de Real-ear to Coupler Difference (RECD) methode een praktisch alternatief. Hierbij worden de effecten van oorslang, oorstukje en gehoorgang apart gemeten om vervolgens de Real-ear aided respons (REAR) in een testbox te kunnen simuleren ten behoeve van de verificatie. Het nadeel van de RECD-methode is dat deze geen inzicht geeft in de directe instroom van geluid via een eventuele venting in het oorstukje.
Om de werking van het hoortoestel in verschillende luistersituaties te verifiëren aan de doelversterking is het belangrijk om een voor het dagelijks leven realistisch stimulussignaal te gebruiken en bij verschillende geluidsniveaus te meten. Meer specifiek dient het stimulussignaal de eigenschappen van spraak te hebben en moet het aangeboden worden op 3 verschillende intensiteitsniveaus die representatief zijn voor zachte spraak/spraak op afstand (55 dB SPL), spraak op een normaal spraakniveau (65 dB SPL) en luide spraak (75 dB SPL). Voor elk niveau dient de output-curve gemeten te worden gemiddeld over een periode van minstens een tiental seconden om rekening te houden met eventuele inregeltijden van de geluidsbewerking in het hoortoestel. De gemeten of gesimuleerde REAR of REAG grafieken kunnen vervolgens vergeleken worden met de berekende doelcurves, op basis van de ingestelde rekenregel, het gehoorverlies en (eventueel) de leeftijd van het kind. Bij afwijking van de doelcurve dient de versterking te worden aangepast. Als vuistregel kan een marge tussen de versterking en de doelcurve van 5 dB worden gehanteerd, een voor slechthorende kinderen veel gebruikte grenswaarde in de literatuur als afwijking van de target (McCreery, 2013). Eventueel kan ook een aanpassing aan het oorstukje overwogen worden.
Naast verificatie van de versterking voor spraaksignalen op realistische geluidsniveaus, is het in situaties van (vermoeden van) discomfort bij hardere geluiden te overwegen om te verifiëren hoe het hoortoestel reageert op zeer hoge geluidsniveaus (MPO waarden). De DSL biedt ook hier doelwaarden voor die hierbij gebruikt kunnen worden. Een optie is om deze verificatie niet door middel van in-situ metingen wordt uit te voeren omwille van comfort en veiligheid, maar via de RECD methode (in de testbox).
Overwegingen in de praktijk
Het doel van het toepassen van de juiste versterking van het hoortoestel is het bereiken van een optimaal profijt van de hoortoestellen bij kinderen. Hierbij staat het hoorbaar maken van spraakklanken, zowel stille situatie als in situaties met achtergrondgeluiden, voorop. Dit is nodig voor een goede communicatie met de omgeving, met daarbij het specifieke belang van goede ontwikkeling van gesproken taal bij de jongste kinderen en het volgen van onderwijs voor de oudere kinderen.
Een bijkomend aspect van het adequaat toepassen van hoortoestelversterking is dat omgevingsgeluiden van verschillende niveaus op een veilige en natuurlijke manier worden doorgegeven. Harde geluiden mogen niet als onaangenaam ervaren worden. Dit kan verstorend werken op het dagelijks gebruik van de hoortoestellen en mogelijk zelfs tot schade leiden. Verder moeten niveauverschillen tussen harde en zachte geluiden en ruimtelijke aspecten van geluid ook voor een slechthorend kind zo goed mogelijk te onderscheiden zijn om een goede inschatting te kunnen maken van wat er in de omgeving gebeurt, zoals in verkeerssituaties.
Het is belangrijk bovenstaande aspecten ten alle tijden in het licht te plaatsen van het individuele kind. Specifieke kindfactoren kunnen de aanpasser doen besluiten om af te wijken van een eerder gekozen rekenregel. In geval van bijkomende problematiek, zoals een verstandelijke beperking, kan het kind bijvoorbeeld gebaat zijn bij een lagere versterking dan de rekenregels voorschrijven, omdat het optimaal kunnen spraakverstaan minder zwaar meeweegt. Kindspecifieke afwegingen kunnen gevoed en (periodiek) geëvalueerd worden door enerzijds het auditief functioneren van het kind met de hoortoestellen te controleren (zie module Diagnostiek voor controle van het auditief functioneren) en anderzijds informatie te verkrijgen van het kind en zijn/haar omgeving. Op deze manier is de instelling van de versterking in het hoortoestel (en de keuze voor DSL of NAL) onderdeel van de steeds terugkerende verbetercyclus (cyclus (‘plan-do-check-act’) voor het bieden van hoorzorg op maat (zie module Algemene inleiding).
Als laatste wordt ook geadviseerd aanvullende otogenetische diagnostiek, voor zover aanwezig, mee te wegen bij de in te stellen versterking van het hoortoestel. Bij bepaalde afwijkingen in het binnenoor is er namelijk meer dan gemiddeld versterking nodig. Het bekendste voorbeeld hiervan is het TECTA-gen, dat bij DFNA8/12 en DFNB21 een belangrijke rol speelt. Ondanks de cochleaire aard van dit type gehoorverlies, gedraagt het zich meer als een conductief gehoorverlies. Dit betekent dat er meer versterking en minder dynamiekcompressie nodig is dan berekend op basis van DSL of NAL. Dit kan gerealiseerd worden door een conductieve component op te nemen in het uitgangstoonaudiogram op basis waarvan de versterking berekend wordt. Een alternatief is om de versterking boven de doelcurve uit te laten komen. Er is echter nog meer wetenschappelijk onderzoek nodig om tot gerichte adviezen te komen voor de in te stellen versterking op basis van de gevonden genetische afwijking.
Onderbouwing
Achtergrond
De meest gangbare interventie bij kinderen met gehoorverlies is het aanpassen van hoortoestellen. Een hoortoestelaanpassing heeft als primair doel om voldoende hoorbaarheid van met name spraakklanken te garanderen in verschillende luistersituaties en met maximaal behoud van de geluidskwaliteit. De basis hiervoor is de instelling van de versterking die het hoortoestel biedt. Voor de versterking van geluid kan gekozen worden uit verschillende rekenregels waarbij op basis van het gehoorverlies berekend wordt wat de benodigde versterking is voor verschillende geluidsfrequenties en geluidsniveaus. De twee meest gangbare rekenregels voor kinderen zijn NAL en DSL. Het is onduidelijk welke rekenregel de voorkeur heeft bij het instellen van hoortoestellen van kinderen van 4 tot 18 jaar.
Conclusies / Summary of Findings
|
Laag GRADE |
Spraakverstaan in stilte Het is mogelijk dat het instellen van hoortoestellen, bij kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies, met behulp van de DSL-rekenregel leidt tot een beter spraakverstaan in stilte dan wanneer hoortoestellen ingesteld worden met behulp van de NAL-rekenregel.
Bronnen: (Marriage, 2018; Quar, 2013; Scollie, 2010) |
|
Laag GRADE |
Spraakverstaan in ruis Het is mogelijk dat het instellen van hoortoestellen, bij kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies, met behulp van de NAL- of DSL-rekenregel leidt tot een vergelijkbaar spraakverstaan in ruis.
Bronnen: (Quar, 2013; Scollie, 2010; Ching, 2018) |
|
Laag GRADE |
Spraak- en taalontwikkeling Het is mogelijk dat het instellen van hoortoestellen, bij kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies, met behulp van de NAL- of DSL-rekenregel leidt tot een vergelijkbare spraak- en taalontwikkeling.
Bronnen: (Ching, 2018) |
|
Zeer laag GRADE |
Subjectieve Beleving Het is onduidelijk of het instellen van hoortoestellen, bij kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies, met behulp van de NAL-of DSL-rekenregel leidt tot verschillende effecten op de subjectieve beleving.
Bronnen: (Ching, 2010; Ching, 2018; Quar, 2013) |
Samenvatting literatuur
Beschrijving studies
De studie van Marriage (2018) onderzoekt of er significante verschillen zijn in spraakscores bij kinderen met een bilateraal gehoorverlies, waarvan hun hoortoestel is ingesteld door middel van de DSL i/o, DSL V of NAL-NL1 rekenregel.
De studiepopulatie bestond uit 44 kinderen met een matig of ernstig bilateraal perceptief gehoorverlies. Gehoorverlies werd hierbij vastgesteld op basis van de audiometrische drempels voor het betere oor, gemiddeld over de frequenties 0,5, 1, 2 en 4 kHz. De kinderen hadden een leeftijd tussen 3 tot 9 jaar en werden in drie groepen verdeeld: groep 1 (2 tot 3 jaar): n = 8 (4 matig, 4 ernstig), groep 2 (4 tot 5 jaar): n = 15 (8 matig, 7 ernstig), groep 3 (6 tot 9 jaar): n = 21 (16 matig, 5 ernstig). Verschillende hoortoestellen en hulpmiddelen werden gebruikt (onder andere de hoortoestellen Phonak Savia Art, Eterna en Naida, en Oticon Safran en Spirit P).
Alle kinderen werden in eerste instantie getest met hun eigen hoortoestellen, ingesteld door de eigen audioloog (voornamelijk ingesteld met DSL). De resultaten hiervan zijn niet gepubliceerd. Vervolgens werd de spraak getoetst nadat de hoortoestellen ingesteld werden met behulp van DSL- en NAL-rekenregel. De kinderen konden 2 tot 4 weken acclimatiseren aan de instelling van hun hoortoestel alvorens de testen werden afgenomen.
De studie van Quar (2013) beschrijft een cross-over studie met 4 perioden waarin de prestaties van 16 schoolgaande kinderen met matig-ernstig tot zeer ernstig perceptief gehoorverlies worden onderzocht. Alle deelnemende kinderen kregen een Phonak Naida V SP-hoortoestel welke werd ingesteld door middel van NAL-NL1 en DSL v5 rekenregel. De kinderen waren tussen 7 en 17 jaar oud (gemiddeld 12,7 jaar), 2 meisjes en 14 jongens. Twee kinderen hadden geen ervaring met hoortoestellen voorafgaand aan het onderzoek. Elf kinderen volgden regulier onderwijs, drie kinderen speciaal onderwijs en 5 kinderen volgden een speciaal programma voor dove kinderen.
In de eerste periode van 6 weken droegen de kinderen het hoortoestel ingesteld met NAL-NL1 (of DSL v5) regel. In de tweede periode van 6 weken werd het hoortoestel ingesteld met de DSL v5 (en vice versa met NAL-NL1). De derde periode duurde drie weken. Tijdens deze periode konden de kinderen zelf de instelling kiezen. Tevens konden ze zelf tussen de instellingen wisselen. Ook tijdens de vierde periode, van eveneens 3 weken, konden de kinderen zelf de instelling kiezen. Echter was de keuze programmering omgedraaid ten opzichte van de derde periode.
De studies van Ching (2010) en Scollie (2010), beschrijven de resultaten van een dubbel geblindeerde, 4-perioden-studie onder 48 kinderen met een mild tot matig-ernstig bilateraal perceptief gehoorverlies. De studiepopulatie betreft 24 kinderen uit Australië en 24 kinderen uit Canada. De gemiddelde leeftijd bij deelname was 11,6 jaar (6,6 tot 19,8 jaar), 29 jongens en 18 meisjes. Het gemiddelde gehoorverlies was 46,1 dB HL (SD = 12,9 (21,7 tot 71,7) voor kinderen in Australië en 48,3 dB HL (SD = 17,1 (15,0 tot 71,7) voor kinderen in Canada.
Tijdens de eerste periode van 8 weken werden de hoortoestellen van de kinderen ingesteld met de NAL- of DSL-rekenregel. De keuze hiervan was random. Tijdens de tweede periode van 8 weken werd het hoortoestel ingesteld met de alternatieve rekenregel. Tijdens de derde en vierde periode, elk van 4 weken, hadden de kinderen toegang tot beide rekenregels welke ze zelf op elk gewenst moment via hun hoortoestel konden instellen. Aan het einde van iedere periode werden testen afgenomen.
De studie van Ching (2018) beschrijft effecten van het gebruik van de NAL- en DSL-rekenregel op het auditief functioneren en de ontwikkeling van kinderen op 5-jarige leeftijd. In dit onderzoek werd het auditief functioneren op 5-jarige leeftijd onderzocht in een groep van 232 kinderen met gehoorverlies met een hoortoestel, ingesteld met NAL (NAL-NL1 of NAL-NL2) of DSL (DSL-v4 of DSL-v5) rekenregel. In deze groep waren 138 (59,5%) jongens. De kinderen droegen hoortoestellen vanaf gemiddeld 10,5 maanden leeftijd. 57 kinderen (24,6%) hadden een mild gehoorverlies (≤ 40 dB), 127 kinderen (54,7%) hadden een matig gehoorverlies (21 tot 40 dB) en 48 kinderen hadden een ernstig gehoorverlies (61 tot 80 dB). De mate van gehoorverlies werd bepaald op basis van de audiometrisch gemeten gehoordrempels gemiddeld over de frequenties 0,5 , 1, 2, en 4 kHz.
Om de effecten op de ontwikkeling te onderzoeken werd een gerandomiseerde trial gedaan bij een groep van 163 kinderen. Het hoortoestel van deze kinderen werd na diagnose van het gehoorverlies random ingesteld met behulp van de NAL of DSL rekenregel. Initieel was dit NAL-NL1 en DSL-v4, echter gedurende het onderzoek werden de kinderen indien gewenst omgezet naar een nieuwere versie van de rekenregel (NAL-NL2 of DSL-v5). In de NAL groep waren 57 jongens (64%) en in de DSL-groep 40 (54.1%). De kinderen in de NAL-groep droegen hoortoestellen vanaf een gemiddelde leeftijd van 11,2 maanden, die van de DSL groep vanaf 10 maanden.
In de NAL-groep waren 20 (22,5%) kinderen met een mild gehoorverlies (≤ 40 dB HL), 51 (57,3%) met een matig gehoorverlies (41 tot 60 dB HL) en 18 (20,2%) met een ernstig gehoorverlies (61 tot 80 dB HL). In de DSL groep waren dit respectievelijk 23 mild (31,1%), 36 matig (48,6%) en 15 ernstig (20,3%).
Resultaten
De beschikbare studies tonen methodologische verschillen in de gebruikte instrumenten voor de effectmetingen. Om deze reden worden de resultaten voor spraakverstaan in ruis, spraakverstaan in stilte en spraak- en taalontwikkeling per studie besproken. Voor de subjectieve beleving wordt wel een overkoepelende effectschatting gegeven.
Spraakverstaan in stilte
Marriage (2018) rapporteert spraakverstaan in stilte gemeten met de CAWL 50 dB (Cambridge Auditory Word Lists) en CphT (Common Phrases-test). Bij de CAWL werden woorden aangeboden op een laag stimulatieniveau (50 dB), die nagezegd moesten worden. De scores werden afgeleid van het aantal fonemen dat correct was voor elk van de doelwoorden. De CphT test werd gebruikt om de spraakreceptiedrempel (SRT) in stilte te schatten, gerapporteerd in dB(A). Dit is het spraakniveau waarop 50% van de klanken nog goed worden verstaan.
De spraakscore op de CAWL bij 50 dB was significant beter met DSL i/o en DSL V dan met NAL-NL1 (F(2,62) = 10.30, p < 0.001, n = 32 - CAWL 50 dB Score: DSL i/o: 23.2 (0.6), DSL-V: 22.8 (0.9), NAL-NL: 19.7 (0.8)). Kinderen met een matig gehoorverlies hadden hogere scores dan kinderen met een ernstig gehoorverlies. Dit verschil was niet significant.
De SRT geschat met behulp van de CPhT-test was significant hoger (slechter) voor NAL-NL1 dan voor DSL (i/o) of DSL-v5. Het verschil was significant (F (2,68) = 7,1, p <0,002; η2 = 0,02). Vergelijkingen per paar toonden aan dat DSL i/o en DSL-v5 significant betere scores gaven dan NAL-NL1, maar scores voor DSL i/o en DSL-v5 waren niet significant verschillend van elkaar.
Quar (2013), beschrijft spraakverstaan in stilte (65 dB) adaptief gemeten met Malay hearing in noise test (HINT) waarbij de spraak zonder achtergrondruis wordt aangeboden. Hierbij wordt de SRT weergegeven. De resultaten worden weergegeven over de gehele trial periode. Hierbij liggen gemiddelde SRT-waarden voor DSL-v5 voor alle trial perioden lager dan die van NAL-NL1 (p=<0,01), hetgeen betekent dat met DSL een gunstiger resultaat wordt behaald. Er wordt een significant effect van trial periode gerapporteerd waarbij de SRT-waarden (voor zowel DSL-v5 als NAL-NL) afnemen over de tijd. Dit wijst op een leereffect en maakt de interpretatie van de individuele trial periode lastiger.
Scollie (2010) rapporteert medeklinkerherkenning in stilte gemeten met de University of Western Ontario Distinctive Features Difference test (UWO-DFD) voor de Canadese populatie en door middel van het aanbieden van opnames van een mannelijke spreker die 21 Engelse medeklinkers uitsprak (dezelfde fonemen als in Canada) in een klinker-medeklinker-klinker context (VCV). De spraak werd aangeboden bij 55, 70 en 80 dB SPL. Voor geen van de testcondities werden significante verschillen in testscores gevonden (p=0.7) tussen kinderen waarvan hun hoortoestel ingesteld was met NAL-NL1 en DSL-i/o.
Spraakverstaan in ruis
Quar (2013), beschrijft spraakverstaan in ruis gemeten met Malay hearing in noise test (HINT). Hierbij werd de SRT weergegeven. De resultaten worden weergegeven over de gehele trial periode. Er werd geen verschil gevonden in SRT tussen DSL-v5 en NAL-NL1. Net als bij de SRT in stilte werd ook voor SRT in ruis een significant effect waargenomen van trial. De gemiddelde SRT scores namen af over de tijd, wat een leereffect suggereert.
Scollie (2010), rapporteert spraakverstaan in ruis gemeten met de HINT-C test voor de Canadese populatie en gemeten met de NAL opname van Bamford-Kowal-Bench (BKB-A) voor de kinderen uit Australië. De testen werden aangeboden bij 70dB SPL.
Er werden geen verschillen gevonden in SRT scores (p=0,63).
Ching (2018) evalueert spraakverstaan in ruis (SRT) voor woorden of zinnen) onder twee testomstandigheden. In een situatie waarbij spraak gepresenteerd werd vanuit een luidspreker die op 0 ° azimut was geplaatst en waarbij als ruis spraak van 8 verschillende sprekers werd gepresenteerd uit dezelfde richting (S0N0). En in een tweede situatie waarbij ongecorreleerde spraak van 4 sprekers gepresenteerd werd vanuit twee luidsprekers geplaatst aan linker- en rechterkant van de luisteraar op 0 ° azimut (S0N ± 90). Voor beide situaties werden geen verschillen aangetoond voor kinderen waarvan hun hoortoestel ingesteld was met de NAL of DSL rekenregel.
Spraak- en taalontwikkeling
Alleen Ching (2018) rapporteert de spraak-taal ontwikkeling voor kinderen van 4 tot 18 jaar. De testen bestonden uit de Preschool Language Scale versie 4 (PLS-4; Zimmerman, 2002) voor het testen van expressieve en receptieve taal; De Peabody Picture Vocabulary test versie 4 (PPVT-4; Dunn & Dunn, 2007) om receptief vocabulaire te testen; en de articulatie- en fonologiesubtest van de Diagnostic Evaluation of Articulation and Phonology test (DEAP; Dodd, 2002) om spraakproductie te testen. Voor geen van de subtests werden significante verschillen in de spraak- en taalontwikkeling waargenomen bij kinderen waarvan de hoortoestellen ingesteld werden met de NAL- of DSL-rekenregel.
Subjectieve beleving
De studies genoemd in figuur 1 tot 3 rapporteerden de subjectieve beleving gemeten met de PEACH vragenlijst. De resultaten uit de studie van Ching (2010)1 zijn apart weergegeven voor de groep kinderen uit Australië en Canada. De waarden voor de gemiddelden en standaard deviaties uit de studies van Ching (2010) en Quar (2013) zijn geschatte waarden op basis van de figuren 2 en 2a respectievelijk uit de desbetreffende publicaties.
De vragenlijst bevat items met betrekking tot situaties in stilte en in ruis. De overall resultaten en de items met betrekking op stilte en ruis zijn apart weergegeven.
De gemiddelde PEACH-scores (zowel overall, in stilte als in ruis) verschillen niet tussen de groepen.
Figuur 1 forest plot van subjectieve beleving gemeten met PEACH vragenlijst (totaal)
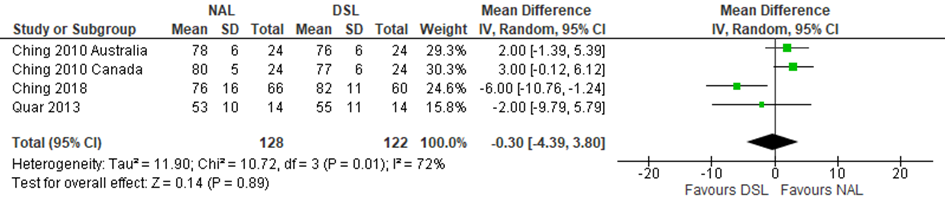
Figuur 2 forest plot van subjectieve beleving gemeten met PEACH vragenlijst (in stilte)
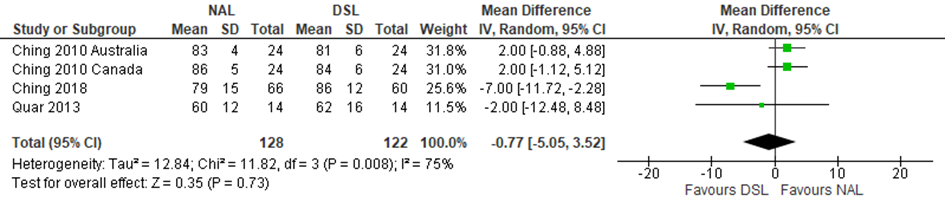
Figuur 3 forest plot van subjectieve beleving gemeten met PEACH vragenlijst (in ruis)
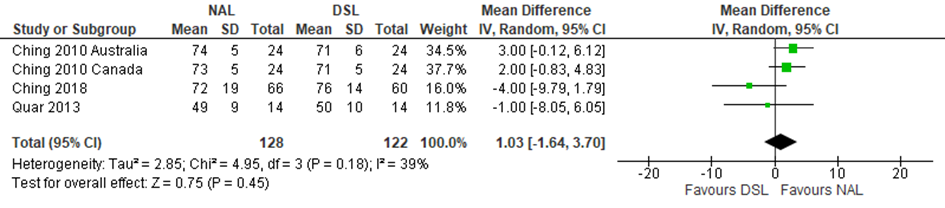
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat spraakverstaan in stilte is gebaseerd op drie gerandomiseerde trials en start zodoende ‘hoog’. De bewijskracht is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: onduidelijke randomisatie) en het geringe aantal patiënten (imprecisie). De bewijskracht komt daarmee uit op ‘laag’.
De bewijskracht voor de uitkomstmaat spraakverstaan in ruis is gebaseerd drie gerandomiseerde trials en start zodoende ‘hoog’. De bewijskracht is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: onduidelijke randomisatie) en het geringe aantal patiënten (imprecisie). De bewijskracht komt daarmee uit op ‘laag’.
De bewijskracht voor de uitkomstmaat spraak-taal ontwikkeling is gebaseerd op één gerandomiseerde trial (n=78) en start zodoende op ‘hoog’. De bewijskracht is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: onduidelijke randomisatie) en omdat er slechts één studie met een gering aantal patiënten (imprecisie) was. De bewijskracht komt daarmee uit op ‘laag’.
De bewijskracht voor de uitkomstmaat subjectieve beleving is gebaseerd op drie gerandomiseerde trials en start zodoende ‘hoog’. De bewijskracht is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: onduidelijke randomisatie), tegenstrijdige resultaten (inconsistentie) en het geringe aantal patiënten (imprecisie). De bewijskracht komt daarmee uit op ‘zeer laag’.
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Welke rekenregel (NAL of DSL) heeft de voorkeur bij de instelling van de versterking van de hoortoestellen bij kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies?[1]
P: kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies met luchtgeleidingsdrempels gelijk of ongunstiger dan 20 dB HL (al of niet beperkt tot de hoge tonen of één oor);
I: hoortoestel(len) waarvan de versterking is ingesteld volgens rekenregel NAL;
C: hoortoestel(len) waarvan de versterking is ingesteld volgens rekenregel DSL;
O: auditief functioneren (met hoortoestel) en (effect op) de spraak- en taal ontwikkeling.
Relevante uitkomstmaten
De werkgroep achtte spraakverstaan in stilte, spraakverstaan in ruis en spraak- en taal ontwikkeling voor de besluitvorming cruciale uitkomstmaten; en subjectieve beleving een voor de besluitvorming belangrijke uitkomstmaat.
De werkgroep definieerde de uitkomstmaten als volgt:
- Spraakverstaan in stilte: gemeten met spraakscores op klank- of woordniveau voor zachte en gemiddelde spraakniveaus of 50% correct drempel voor het verstaan van zinnen (de spraakreceptiedrempel ofwel SRT).
- Spraakverstaan in ruis: gemeten met spraakscores in ruis op klank of woordniveau op een vaste signaalruisverhouding, of de SRT met zinnen in ruis.
- Gesproken spraak- en taalontwikkeling: Maten voor receptieve woordenschat en taalbegrip, productieve woordenschat, articulatie en fonologie.
- Subjectieve beleving gemeten met vragenlijsten.
Zoeken en selecteren (Methode)
In de databases Pubmed en Embase (via Embase.com) is op 8 oktober 2019 met relevante zoektermen gezocht naar artikelen over de kinderen van 4 tot 18 jaar met een blijvend gehoorverlies, waarbij hun hoortoestel is ingesteld met behulp van de NAL- of DSL-rekenregel. Hierbij zijn verschillende versies van de rekenregels meegenomen (alle versies van DSL en voor NAL de versies NL1 en NL2).
De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 19 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- primair vergelijkend onderzoek;
- artikel full tekst beschikbaar in Nederlands of Engels;
- patiënten tussen de 4tot 18 jaar oud met een langdurig of blijvend gehoorverlies en een hoortoestel;
- vergelijking tussen de NAL en DSL rekenregel voor de instelling van de versterking van het hoortoestel;
- beschrijving van tenminste één uitkomstmaat.
Op basis van titel en abstract werden in eerste instantie 12 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 7 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 5 studies definitief geselecteerd.
Resultaten
Er zijn 5 onderzoeken opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
[1] Het literatuuronderzoek en de analyse van de gevonden literatuur is voor alle categorieën van gehoorverlies gezamenlijk uitgevoerd.
Referenties
- Ching, T., Zhang, V., et al., (2018). Hearing aid fitting and developmental outcomes of children fit according to either the NAL or DSL prescription: fit-to-target, audibility, speech and language abilities. Int J Audiol. 2018 May ; 57(SUP2): S41–S54. doi:10.1080/14992027.2017.1380851.
- Ching, T., Scollie, S., et al., (2010). Evaluation of the NAL-NL1 and the DSL v.4.1 prescriptions for children: Paired-comparison intelligibility judgments and functional performance ratings. International Journal of Audiology 2010; 49:S35–S48.
- Quar, T., Ching, T., et al., (2013). Evaluation of real-world preferences and performance of hearing aids fitted according to the NAL-NL1 and DSL v5 procedures in children with moderately severe to profound hearing loss. International Journal of Audiology, 52:5, 322-332, DOI: 10.3109/14992027.2012.755740.
- Scollie, S., Ching, T., et al., (2010). Children's speech perception and loudness ratings when fitted with hearing aids using the DSL v.4.1 and the NAL-NL1 prescriptions. International Journal of Audiology, 49:sup1, S26-s34, DOI: 10.3109/14992020903121159.
- Marriage, J., Vickers, D., et al., (2018). Comparison of Different Hearing Aid Prescriptions for Children. Ear & Hearing, vol. 39, no. 1, 20–31.
Evidence tabellen
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Marriage, 2018 |
Type of study: RCT, balanced double-blind design.
Setting and country: United Kingdom
Funding and conflicts of interest: Study funded by Deafness Research UK (now part of Action on Hearing Loss). Phonak and Oticon provide the study hearing aids, PC Werth and Audioscan the Verifit system.
The authors have no conflicts of interest to disclose |
Inclusion criteria: Children with moderate or severe bilateral hearing loss
Exclusion criteria: Non clearly described
N total at baseline: N=44
Important prognostic factors2: age (range): 3-9 years - 2 to 3 years: n = 8 4 to 5 years: n = 15 6 to 9 years: n = 21
Sex: I: % M - NA C: % M - NA
Hearing losses of the children were classified as moderate or severe based on the average audiometric thresholds for the better ear over the frequencies 500, 1000, 2000, and 4000 Hz: N=28 moderate, n=16 severe. |
Describe intervention (treatment/procedure/test):
All children were initially tested on all of the tests using their own hearing aids, as fitted by their own audiologist. Most of the children had been fitted using DSL i/o targets.
A program was coded as C1, C2, and C3, with a random assignment of fitting method to program number (NAL-NL1, DSL i/o, DSL V). The order of activation and testing with the different prescriptions was randomized across children to control for order effects. The time allowed for each child to become familiar with the amplification characteristics for a specific prescription was selected bearing in mind the time available for the study and the changing listening skills of the child with increasing age. Children wore the study hearing aids with each prescription in turn, typically for between 2 and 4 weeks for each prescription. At the end of this familiarization/acclimatization period, they were assessed using the speech test battery and the next prescription was programmed in. |
Describe control (treatment/procedure/test):
See intervention |
Length of follow-up: 2-4 weeks for each prescription
Loss-to-follow-up: - Fifty-four children were initially enrolled into the study and 44 children completed speech testing for each prescription condition for their age group. Of the 10 children who dropped out of the study, only 1 dropped out due to an inability to complete the speech testing. This child had more global communication difficulties. The main reason for dropping out of the study was family difficulties in attending the required five appointments.
Incomplete outcome data: -
|
Outcome measures and effect size (include 95%CI and p-value if available):
CAWL for the level of 50 dBA, there was a significant effect of prescription (F(2,62) = 10.30, p < 0.001) (DSL better than NAL) and a significant effect of severity of hearing loss (F(1,30) = 5.2, p = 0.03). |
Several hearing aid types were used for the study. The hearing aids used were: Savia Art, Eterna and Naida aids manufactured by Phonak and Safran and Spirit P aids manufactured by Oticon. |
|
Quar, 2013 |
Type of study: crossover, four period trial of prescriptions – single blinded
Setting and country: Audiology and Speech Sciences Clinic, School of Rehabilitation Sciences of UKM in Kuala Lumpur.
Funding and conflicts of interest: The authors report no conflicts of interest.
Phonak Switzerland provided the hearing aids for this research.
|
Inclusion criteria: School-aged children with moderately severe to profound hearing losses
Exclusion criteria: Not clearly specified
N total at baseline: N=16
Important prognostic factors:
age ± SD: 12.7 years; SD 2.8 (range 7-17).
Sex: - %M: 88%
Hearing losses ranged from moderately severe to profound (four frequency average (4FA) at 0.5, 1, 2 and 4 kHz 81.9 dB HL; SD 17.7; range 51.9 to 115 dB HL).
All children had bilateral sensorineural hearing loss except for one child who had a mixed hearing loss in one ear and an unaidable hearing loss in the other ear. |
Describe intervention (treatment/procedure/test): This trial takes 4 periods.During the first two periods, each lasting six weeks, children had access to one prescription only. During the third and fourth trial period, each lasting three weeks, children had access to both the prescriptions via their hearing aid remote controls.
At the start of the study - half of the children were randomly assigned to receive the NAL-NL1 prescription while the other half were fitted according to the DSL v5 prescriptive procedure. After the fitting, the children underwent a six week home trial with the hearing aids. At the end of the first home trial, children’s hearing aids which had been fitted according to NAL-NL1 prescription in the previous trial, were switched to the DSL v5 prescription and vice versa. This was followed by another six weeks of home trial with the hearing aids. During trail period 3 both the NAL-NL1 and DSL v5 prescriptions were activated in the hearing aids so the children could access both prescriptions via the tactronics push-button on the hearing aids. Children were required to fill in a short diary which allowed them to compare the performance of the two programs in different listening situations. Also, by the end of the three weeks trial, the children returned to the clinic to complete a paired comparison judgments test as well as a speech perception test. To avoid bias among children towards the prescription set as the default memory program during the third trial, the default program was counterbalanced in the fourth trial session. This means the relative positions of the two programs in trial 3 were reversed. The paired-comparison tests and speech perception tests were repeated at the end of the trial session. |
Describe control (treatment/procedure/test):
See intervention |
Length of follow-up: Measurements took place directly after each trial period.
Loss-to-follow-up: Not specified
Incomplete outcome data:
Consonant discrimination test: results were obtained from only 15/16 children, as one child had difficulty completing the evaluation test.
The sentence reception threshold (SRT) of the Malay HINT was measured from 7/16 children. Other children were not able to complete this task due to high linguistic demands.
Paired-comparison judgments of speech intelligibility tests were completed by 15/16 children at the end of each of the four trials*. 14/16 parents completed for PEACH, 15/16 teachers for TEACH*. Children’s prescription ratings and preferences were assessed using a diary in trials 3 and 4. Results were obtained from 15/16 children*.
*reason for missing data not specified. |
SRTs in quiet for DSL v5 procedure were slightly lower/better than the NAL-NL1 procedure. The general linear model repeated measure analysis revealed a significant main effect of prescription (F (1,6) = 17.130, p= 0.01) and trial (F 3, 18)= 6.765, p=0.01).
In noise, a significant main effect of trial was found (F (3, 18) = 6.285, p= 0 .01). Unlike the SRT in quiet, there was no significant difference between the NAL-NL1 and DSL v5 procedure for SRT in noise (p =0.81).
PEACH: the DSL v5 had higher scores than NAL-NL1 for all the subscales and scales evaluated. The general linear model repeated measures analysis was used to analyse the data with scale as dependent variable and prescription (NAL-NL1 and DSL v5) and listening condition (quiet and noise) as independent variables. The results showed a significant main effect of prescription for PEACH (F (1, 13) = 6.869, p= 0.02). |
Except for two children, all were experienced hearing-aid users. Eleven children were in mainstream schools, with three of them receiving special support in classroom (inclusive program). The other five children were in a unit for deaf children or special program.
All children were fitted with new Phonak Naida V SP Standard hearing aids.
|
|
Ching, 20101 |
Type of study: four-period, two-treatment crossover design – double blinded
Setting and country: Australia and Canada
Funding and conflicts of interest: Support for this collaborative research was provided by the Oticon Foundation. The authors report no conflicts of interest. |
Inclusion criteria: Children with bilateral sensorineural hearing loss with the following audiometric criterion were included: the difference in target gains between prescriptions for an average speech input of 70 dB not less than 5 dB or greater than 15 dB at two or more audiometric frequencies between 0.25 and 4 kHz. Children with tympanometry within normal limits (0.7 mL < equivalent volume < 1.5 mL) were included. The air-bone gap was restricted to ≤ 15 dB at each audiometric frequency or ≤ 10 dB at two or more consecutive audiometric frequencies.
Exclusion criteria: Children who had a history of fluctuating hearing loss, evidence of middle ear or retro-cochlear pathology, known auditory processing deficit, known language impairment, abnormalities of the external ear canal, or who had disabilities in addition to hearing impairment, were excluded.
N total at baseline: N= 48 (n=24 Australia, n=24 Canada)
Important prognostic factors: age (range): Australia: 11.6 years (6.6 - 19.8) Canada: 11,2 years ( 6.7 - 17.3)
Sex: Australie: 50% M Canada: 71% M
Their hearing threshold levels were measured by using ER3A insert earphones coupled to the children’s personal earmolds. In Australia, 22 children were bilaterally aided; two wore hearing aids in one ear only. In Canada, all children were aided bilaterally. |
Describe intervention (treatment/procedure/test):
At each of the two test sites, half of the participants received the NAL-NL1 and the other half the DSL v.4.1 prescription for fitting at the first trial period. After experiencing one prescription for eight weeks, each participant received the other prescription for the second trial period of another eight weeks. During the third and fourth trial periods, the two prescriptions were put into separate programs in hearing aids for access via a remote control by the participants at all times. Each of the third and fourth trial periods lasted for four weeks. The allocation of prescription to programs was counterbalanced across participants and trial periods. At the end of each trial period, a battery of assessments was administered. A double-blind protocol was implemented so that neither the audiologist who administered the tests nor the child participants (including their parents and teachers) knew which prescription was used in each hearing aid program during each trial.
|
Describe control (treatment/procedure/test):
See intervention |
Length of follow-up: Measurements took place directly after each trial period.
Loss-to-follow-up: Intervention: Not specified
Incomplete outcome data: Intervention: Not specified
|
Outcome measures and effect size (include 95%CI and p-value if available):
PEACH: The main effect of subscale (F(1,46) = 106.5, p < 0.001) was significant, suggesting that performance in quiet (mean: 85.0%) was better than in noisy situations (mean: 71.9%). Neither the effect of prescription (p = 0.2) nor the effect of site was significant (p = 0.3). There were no significant interactions (p > 0.05). A univariate test of significance for planned comparisons indicated no significant difference between prescriptions for either the Quiet subscale (p = 0.3) or the Noise subscale (p = 0.5), on average, in either site. |
In Australia, prior to enrolment in the study, all children wore hearing aids , fitted according to the NAL-RP prescription. In Canada, prior to study enrolment, hearing aids were fitted with some approximation to the DSL v.4.1 prescription.
During the study, All 24 children in Australia and 14 of the 24 children in Canada received the Bernafon Smile 110 hearing aids. The remaining 10 children in Canada were fitted with Siemens Prisma hearing aids to ensure compatibility with their personal FM systems.
Reported results based on trial period 1 and 2 only.
|
|
Scollie, 2010 |
Type of study: See Ching, 20101
Setting and country: See Ching, 20101
Funding and conflicts of interest: See Ching, 20101
|
Inclusion criteria: See Ching, 20101 Exclusion criteria: See Ching, 20101
N total at baseline: See Ching, 20101
Important prognostic factors: See Ching, 20101 |
Describe intervention (treatment/procedure/test):
See Ching, 20101 |
Describe control (treatment/procedure/test):
See Ching, 20101 |
Length of follow-up: See Ching, 20101
Loss-to-follow-up: Intervention: See Ching, 20101
Incomplete outcome data: Intervention: See Ching, 20101
|
Outcome measures and effect size (include 95%CI and p-value if available): Consonant recognition in quiet: There was a significant main effect of site (p < 0.001), time (p < 0.04), and level (p < 0.001). The main effect of prescription was not significant (p = 0.7)
Sentence recognition in noise: The sentence recognition thresholds in noise were submitted to a repeated measures analysis of variance, with time and prescription as within-participants variables and test site as a grouping variable. On average, the main effects of site and of time were significant (p < 0.0001 and p = 0.003 respectively), but the effect of prescription was not significant (p = 0.63). |
See Ching, 20101
|
|
Ching, 2018 |
Type of study: Cohort and RCT
Setting and country: Australia
Funding and conflicts of interest: This work was partly supported by the National Institute on Deafness and Other communication Disorders (Award Number R01DC008080). The project was also partly supported by the Commonwealth of Australia through the Office of Hearing Services. Also financial supported by the HEARing CRC, by New South Wales Department of Health, Australia; Phonak Ltd; and the Oticon Foundation.
Authors one and two are employees of the National Acoustics Laboratories. The third author has a part-time Audiology practice, Johnson Hearing Technology and Communication, PLLC. |
Inclusion criteria: Children who were diagnosed with bilateral hearing loss and first received HAs before 3 years of age.
Exclusion criteria: Not specified
N total at baseline: N=232 (Cohort) N=163 (RCT)
Important prognostic factors Cohort: Sex % M: 138 (59.5%)
Degree of Hearing Loss (4FA HL in better ear): Mild (≤ 40 dB) n=57 (24.6%), Moderate (41–60 dB) n=127 (54.7%), Severe (61–80 dB) n=48 (20.7%).
Fitted with NAL (NAL-NL1 or NAL-NL2) prescription n=158 (68.1%). fitted with DSL (DSL v.4 or DSL v.5) prescription n=74 (31.9%).
Important prognostic factors RCT:
NAL group (N) n=89 – (43 NAL-NL1, 46 NAL-NL2) DSL group (D) n=74 - (70 DSLv.5, 4 DSLv.4)
Sex % M – N/D: n=57 (64.0%) / n=40 (54.1%)
Degree of Hearing Loss (4FA HL in better ear) – N/D: Mild (≤ 40 dB) n=20 (22.5%) / n=23 (31.1%) Moderate (41–60 dB) n=51 (57.3%)/ n=36 (48.6%) Severe (61–80 dB) n=18 (20.2%) / n=15 (20.3%) |
Describe intervention (treatment/procedure/test):
Cohort: HA fitting outcomes of children whose HAs were fit according to either the NAL or the DSL prescription were compared at age of ~5 year. All children were fit by a clinical audiologist of a single government-funded national hearing service provider, Australian Hearing (AH). They controlled for variability due to service provision and technology. For each prescription group the deviation from targets and the rms error of fitting was examined. Aided audibility in terms of standard SII as well as a modified version of SII that incorporated hearing loss desensitization was computed.
RCT: a randomised controlled trial of prescription in the LOCHI study to compare 5- year developmental outcomes of children who were randomly assigned to fitting with either the NAL or the DSL prescription after diagnosis of PCHL.
At initial fitting, the NAL prescription used was NAL-NL1 and the DSL prescription used was DSL v.4. As part of the routine clinical service, the children’s HAs would be updated according to individual needs, with changes in HA fittings according to changes in hearing levels and/or new versions of the respective prescriptions (either NAL-NL2 or DSL v.5.
Developmental outcomes were evaluated at ~5 years of age.
|
Describe control (treatment/procedure/test):
Cohort: see intervention
RCT: see intervention |
Length of follow-up: Evaluation at 5 years of age.
Loss-to-follow-up: Not specified
Incomplete outcome data: RCT: Data for all 8 measures (PLS-receptive language, PLS-expressive language, PPVT-receptive vocabulary, PEACH-quiet score, PEACH-noise score, DEAP-consonant score, DEAP-vowel score, speech perception in collocated noise – SRT, speech perception in spatially separated noise – SRT) were available for 90/163 (55%) children (44 NAL, 46 DSL).
Reasons (describe): Not specified.
|
Outcome measures and effect size (include 95%CI and p-value if available): There were no significant differences in SRTs for listening to speech in babble: Speech reception threshold in signal-to-noise ratio for the S0N0 condition: n, mean (SD) NAL: n=59, 4.1 (3.2) DSL: n=60, 3.6 (3.3), p= 0.35 Speech reception threshold in signal-to-noise ratio for the S0N±90 condition: NAL: n= 91.2 (3.3) DSL: n=60, 1.2 (3.8), p=0.98 DEAP-PVC: n, mean (SD) – NAL: n=78, 4,1 (2,1) DSL: n=70, 4.0 (1,6), p=0,95 DEAP-PVC: n, mean (SD) – NAL: n=78, 5,0 (2,6) DSL:n=70, 5,0 (2,6), p=0,81 PEACH (n, mean (SD)) - PEACH-quiet: NAL: n=66, 79.4 (15.3) DSL: n= 60, 86.3 (11.5)- p=0.01 PEACH-noise: NAL: n=66, 71.7 (18.5) DSL: n= 60, 75.8 (13.8)- p= 0.16 PEACH_Total: NAL: n=66,75.9 (15.5) DSL: n=60, 81.5 (11.0)- p=0.02 |
Cohort: to address the question: Do HA fitting outcomes vary in proximity to targets and aided audibility, depending on which prescription was used for fitting? RCT to address: Do developmental outcomes at 5 years of age vary according to the prescription used in fitting HAs?
Participants of the LOCHI study were born with hearing loss between 2002 and 2007 in New South Wales, Victoria and Queensland in Australia. (Ching et al.., 2013).
|
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Risk of bias table
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Marriage, 2018 |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
|
Quar, 2013 |
Unclear - Not clearly described |
Unclear – as randomisation is not clearly described |
unlikely |
Likely – testers were not blinded |
unlikely |
unlikely |
unlikely |
unlikely |
|
Ching, 20101 |
Unclear - Not clearly described |
Unclear - Not clearly described |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
|
Scollie, 2010 |
Unclear - Not clearly described |
Unclear - Not clearly described |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
unlikely |
|
Ching, 2018 |
Unclear - Not clearly described |
Unclear - Not clearly described |
unlikely |
unlikely |
unlikely |
unlikely |
Likely - lots of incomplete outcome data (90/163 (55%) complete) without reporting of reason. |
likely |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules.
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear.
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Ching T, 1997 |
Oude studie met zeer kleine populatie, recentere vergelijkbare studies van zelfde auteur geïncludeerd. |
|
Ching T, 2010 |
Paper is overzicht/samenvatting van de geïncludeerde artikelen van Ching 2010 en Scollie 2010 – beschrijving design en overview of findings |
|
Ching T, 2013 |
Onjuiste patiëntpopulatie |
|
Ching T, 2015 |
Onjuiste/niet geselecteerde uitkomst |
|
Johnson E, 2013 |
Onjuiste patiëntpopulatie |
|
Dilon H, 2010 |
Geen origineel onderzoek, betreft letter van de Director, National Acoustic Laboratories |
|
Scollie S, 2010 |
Onjuiste/niet geselecteerde uitkomst |
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 01-05-2021
Eerstvolgende beoordeling actualiteit 1 mei 2026, Bij het opstellen van de modules heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden. De geldigheid van de richtlijnmodules komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Doel en doelgroep
Doel
Het doel is de kwaliteit van zorg verder te verbeteren door de richtlijn te herzien, aan te vullen en op te stellen voor en met medisch specialisten en andere relevante zorgverleners. De richtlijn verschaft duidelijkheid over de te leveren zorg voor kinderen in de leeftijd van 4 tot 18 jaar met een hulpvraag op het gebied van het gehoor om zo bij te dragen aan de kwaliteit van zorg. Bovendien is deze herziene richtlijn multidisciplinair opgesteld, waarbij de hoorzorg breder gedefinieerd is dan enkel de audiologisch technische hoorzorg in de voorgaande versie van de richtlijn.
Door gehoorproblemen bij slechthorende kinderen zo goed mogelijk te reduceren of te compenseren kunnen achterstanden in de spraak- en taalontwikkeling en/of didactische ontwikkeling voorkomen dan wel geminimaliseerd worden, en kan de sociaal-emotionele ontwikkeling en het welbevinden worden bevorderd. Het uiteindelijke doel is hierbij een optimale participatie in de maatschappij.
Doelgroep
Deze richtlijn is primair bestemd voor zorgverleners binnen de Audiologische Centra die betrokken zijn bij de zorg voor kinderen van 4 tot 18 jaar met een langdurig of blijvend gehoorverlies in één of beide oren. Voor overige hulpverleners die betrokken zijn bij deze doelgroep, zoals KNO-artsen, kinderartsen, jeugdartsen en huisartsen, geldt deze richtlijn ter informatie en als naslagwerk. De leeftijdsaanduiding van 4 tot 18 jaar moet hierbij niet star worden geïnterpreteerd, maar eerder als een ontwikkelingsleeftijd.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2017 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor kinderen met slechthorendheid in de leeftijd van 4 tot 18 jaar.
Werkgroep
- Dr. ir. F.L. Theelen-Van den Hoek, Klinisch fysicus - audioloog, Amsterdam Universitair Medisch Centrum, (voorzitter), NVKF
- Dr. ir. P. Brienesse, Klinisch fysicus - audioloog, Amsterdam Universitair Medisch Centrum, NVKF
- Dr. ir. A. Goedegebure, Klinisch fysicus - audioloog, Erasmus Medisch Centrum, Rotterdam, NVKF
- Dr. Y.J.W. Simis, Klinisch fysicus - Klinisch fysicus - audioloog , Amsterdam Universitair Medisch Centrum, NVKF
- Drs. E.A. Doorduin, Klinisch linguiïst, Audiologisch centrum Auris, VKL
- W. Harkema, Maatschappelijk werk, Audiologisch Centrum Holland Noord, LWMA
- M. van Eijk, Gedragswetenschapper, Pento Audiologisch Centrum, FENAC (tot november 2019)
- Drs. E. van Roosendaal, Psycholoog, Audiologisch centrum Auris, NIP (vanaf januari 2020)
Klankbordgroep
- Dr. L.J.C. Rotteveel, KNO-arts, Leiden Universitair Medisch Centrum, Leiden, NVKNO
- I.J.G. Podt, Logopedist, Kentalis, Enschede, NVLF
- Drs. J.E. Hoogeveen, orthopedagoog, FODOK/FOSS
Met ondersteuning van
- I. van Dusseldorp, senior informatiespecialist, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. E. Paap, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. H. Graveland, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. ir. F.L. Theelen-Van den Hoek |
Klinisch fysicus – audioloog, Amsterdam UMC, locatie AMC |
Lid commissie kwaliteit NVKF, onbetaald. Lid taakgroep kwaliteit FENAC (brancheorganisatie audiologische centra), onbetaald. |
geen |
geen actie vereist |
|
Dr. ir. P. Brienesse |
Klinisch fysicus – audioloog, Amsterdam UMC, locatie AMC |
Penningmeester Nederlandse Vereniging Audiologie (NVA), onbetaald Lid concilium stichting Opleiding Klinische Fysica (OKF), onbetaald |
geen |
geen actie vereist |
|
Dr. ir. A. Goedegebure |
Klinisch-fysicus audioloog, Erasmus MC |
Bestuurslid FENAC (brancheorganisatie audiologische centra), onbetaald |
geen |
geen actie vereist |
|
Dr. Y.J.W. Simis |
Klinisch Fysicus-audioloog, Amsterdam UMC, locatie Vumc |
Lid taakgroep kwaliteit FENAC (brancheorganisatie audiologische centra), onbetaald. |
geen |
geen actie vereist |
|
Drs. E.A. Doorduin |
Klinisch linguïst, Audiologisch Centrum Auris |
Geen |
geen |
geen actie vereist |
|
W. Harkema |
Maatschappelijk werk, Audiologisch Centrum Holland Noord |
Geen |
geen |
geen actie vereist |
|
Drs. E. van Roosendaal |
Psycholoog, Audiologisch Centrum Auris |
Geen |
geen |
geen actie vereist |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigde patiëntenvereniging in de klankbordgroep. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de volledige klankbordgroep en de commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden in de bijlagen.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitkomstvragen
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten.
De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVKF) op noodzaak tot revisie. De werkgroep stelde vervolgens een lijst met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Er is systematisch gezocht naar literatuur om de uitgangsvragen te kunnen beantwoorden. Hiervoor is specifiek gezocht naar de vooraf gedefinieerde PICO: P=patiënt, I=interventie, C=comparison, O=outcome. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
Definitie |
|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
- Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R,Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
- Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
- Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
- Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
- Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. https://richtlijnendatabase.nl/over_deze_site.html
- Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
- Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
- Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
- Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
