Transport van een patiënt met high flow
Uitgangsvraag
Wanneer en op welke wijze dient een patiënt die behandeld wordt met high flow te worden vervoerd?
De uitgangsvraag omvat de volgende deelvragen:
- Wanneer moet een patiënt die high flow krijgt in een algemeen ziekenhuis worden getransporteerd naar een ziekenhuis met een kinder intensive care?
- Hoe moet een patiënt die high flow krijgt in een algemeen ziekenhuis worden getransporteerd naar een ziekenhuis met een kinder intensive care?
Aanbeveling
Deelvraag 1
Volg het stroomdiagram in figuur 1.
Transporteer de patiënt naar een ziekenhuis met kinder intensive care indien de patiënt na de start met high flow niet opknapt of verslechtert in overeenstemming met de module ‘Monitoring’).
Deelvraag 2
Volg het stroomdiagram in figuur 1.
Figuur 1 Stroomdiagram transport patiënt aan high flow
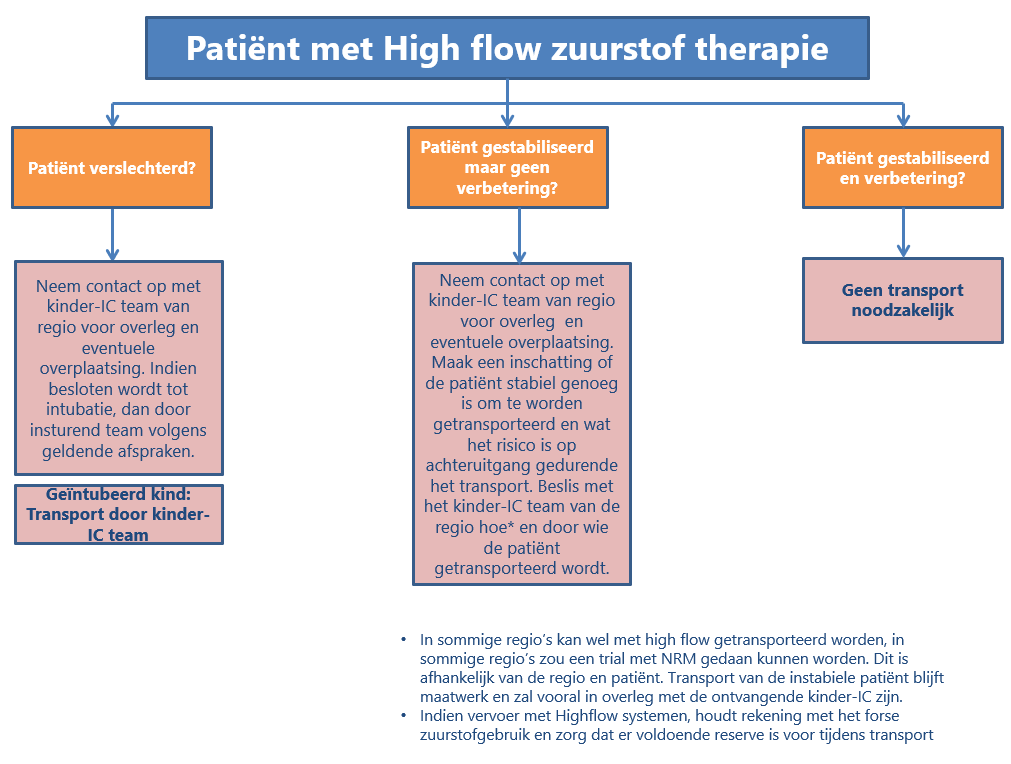
Afkortingen: NRM non-rebreathing masker
Overwegingen
De onderstaande overwegingen gelden in principe voor de gehele patiëntenpopulatie zoals geformuleerd in de uitgangsvragen.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is geen systematische zoekactie verricht.
Het doel van overplaatsing van een kritisch zieke patiënt naar een centrum met een kinder intensive care is om de klinische uitkomst van de patiënt te verbeteren en om de mortaliteit te verlagen. Het transport van een kritisch zieke patiënt blijft een uitdaging omdat het een hoogrisicohandeling is met beperkte middelen en minder mogelijkheid om de patiënt adequaat te monitoren. Daarnaast wordt eventuele achteruitgang van een patiënt beïnvloed door transportgerelateerde factoren zoals transporttijd, stabilisatietijd, onderliggend lijden, manier van transporteren en de ervaring van het transporterend team. Daarom is het identificeren van risicofactoren (zoals geïdentificeerd in de module ‘Monitoring’) die geassocieerd zijn met potentiële achteruitgang tijdens transport van essentieel belang. Afhankelijk van de risicofactoren wordt besloten op welke wijze een patiënt veilig kan worden overgeplaatst.
Waarden en voorkeuren van patiënten
Tijdens transport staat de veiligheid van de patiënt voorop. In overleg met transporterend team en indien de veiligheid het toelaat, kan een ouder mee gaan ter comfort en rust van de patiënt.
Kosten (middelenbeslag)
De werkgroep verwacht geen stijging van de kosten door de aanbeveling in deze module. De aanbeveling sluit aan bij de dagelijkse praktijk.
Aanvaardbaarheid voor de overige relevante stakeholders
Er zijn ambulancediensten die de mogelijkheid hebben om high flow toe te dienen in de ambulance. Het kan voorkomen dat de ambulance wel is uitgerust om een patiënt aan high flow te transporteren maar dat de koppelstukken niet overeen komen of dat het transporterende team niet geschoold is in het gebruik hiervan. De werkgroep adviseert dan om de patiënt met een non-rebreathing masker te transporteren.
Haalbaarheid en implementatie
De werkgroep is van mening dat belangrijke afwegingen in het besluiten tot het overgaan tot transport van een patiënt met high flow moeten worden gemaakt in een algemeen ziekenhuis.
- De patiënt moet stabiel genoeg zijn voor een transport.
- Indien de patiënt niet door een kinder-IC team wordt getransporteerd moet het risico op achteruitgaan van een patiënt tijdens een transport zo goed mogelijk worden ingeschat.
De werkgroep is van mening dat bij het overgaan tot transport er eerst een adequate inschatting moet worden gemaakt hoe de patiënt het veiligst kan worden getransporteerd.
- In overleg met de regionale kinder intensive care wordt besloten of een patiënt moet worden overgeplaatst naar een (ziekenhuis met) kinder intensive care.
- In overleg met de regionale kinder intensive care wordt besloten of een patiënt moet worden geïntubeerd en getransporteerd door het kinder-IC team. Indien een patiënt niet wordt geïntubeerd, wordt de patiënt getransporteerd door het insturend team.
- Slechts enkele ambulance regio’s hebben de mogelijkheid voor high flow ondersteuning gedurende het transport. Als transport met high flow mogelijk is, is het nog steeds afhankelijk van het transporterend team of dit team ook voldoende geschoold is om te transporteren aan high flow. Derhalve is transporteren met een non-rebreathing masker in de meeste gevallen noodzakelijk. Bedenk dat high flow systemen geen accu hebben en dan een transport naar de ambulance toe altijd met NRM zal moeten.
Het is van belang dat, ook indien de geschatte duur van het transport wel high flow kan worden toegediend, de patiënt stabiel kan blijven gedurende het transport met een non-rebreathing masker. Bij een technisch mankement van de high flow of in het geval van een niet geschoold transportteam zal de patiënt vervoerd worden aan de non-rebreathing masker.
Rationale/ balans tussen voor- en nadelen van de interventie
Op basis van literatuur is niet aan te geven in welke gevallen de patiënt moet worden getransporteerd en op welke wijze dat dient te gebeuren. Onderstaande aanbevelingen zijn gebaseerd op de mening van de werkgroep en het patiëntenperspectief.
Onderbouwing
Achtergrond
Respiratoire insufficiëntie is een belangrijke reden voor overplaatsing van patiënten naar (een ziekenhuis met) een kinder intensive care. Er bestaat geen duidelijke protocol voor een optimaal transport van een ernstig benauwde patiënt naar een ander ziekenhuis. Een dergelijk transport is risicovol gezien de kans op complicaties en achteruitgang door onder andere minder adequate monitoring en beperkte mogelijkheid om de respiratoire ondersteuning te op te schalen naar bijvoorbeeld invasieve beademing. Daarom wordt een patiënt die respiratoir insufficiënt is in een algemeen ziekenhuis waar geen kinder intensive care is, ter plaatse door het perifere insturende team geïntubeerd en getransporteerd naar een kinder intensive care door een kinder-IC transportteam.
Het kan voorkomen dat een patiënt die high flow zuurstoftherapie (verder: high flow) krijgt ligt opgenomen in een algemeen ziekenhuis, maar dat het wenselijk is om de patiënt over te plaatsen naar een ziekenhuis met kinder intensive care danwel intern moet worden overgeplaatst. Op dat moment moet er door het insturende team (in overleg met de kinder intensive care) een inschatting worden gemaakt hoe en door wie dit transport dient plaats te vinden. Deze module beschrijft de werkwijze van het transport van een patiënt met high flow die opgenomen ligt in een algemeen ziekenhuis en die getransporteerd moet worden naar een ziekenhuis met beschikking over een kinder intensive care.
Samenvatting literatuur
Er bestaat geen vergelijkende literatuur over de vraagstelling. Hiernaast betreft het ook specifiek een vraag voor de Nederlandse situatie. De werkgroep heeft daarom geen systematische literatuur search gedaan, maar op basis van expert opinion aanbevelingen geformuleerd.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-07-2020
Beoordeeld op geldigheid : 26-06-2020
Uiterlijk in 2024 bepaalt het bestuur van de Nederlandse Vereniging voor Kindergeneeskunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Kindergeneeskunde is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module |
Regiehouder(s) |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn |
Frequentie van beoordeling op actualiteit |
Wie houdt er toezicht op actualiteit |
Relevante factoren voor wijzigingen in aanbeveling |
|
NVK |
NVK |
2020 |
2025 |
Eens per 5 jaar |
SICK |
Nieuwe Veldnorm IC. Eventuele beschikbaarheid high flow in Ambulance |
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van relevante specialismen die betrokken zijn bij de zorg van kinderen met toegenomen zuurstofbehoefte en/of ademarbeid. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname en de werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn. De wetenschappelijke verenigingen van de spoedeisende hulpartsen en de ambulanceverpleegkundigen zijn ook gevraagd om te participeren in de werkgroep, maar dit bleek helaas niet mogelijk.
Werkgroep
- Dr. B. Kapitein, kinderarts-intensivist, werzaam in het Amsterdam Universitair Medisch Centrum te Amsterdam, NVK, voorzitter
- Dr. W. Balemans, kinderarts-pulmonoloog, werkzaam in het Antonius Ziekenhuis te Nieuwegein, NVK
- Drs. G. Brinkhorst, kinderarts-pulmonoloog, werkzaam bij Noordwest Ziekenhuisgroep Alkmaar-Den Helder, NVK
- Drs. R. Klein-Blommert, intensive care kinderverpleegkundige, werkzaam in het VU medisch Centrum te Amsterdam, V&VN
- Drs. I. Morsing, kinder-intensivist, werkzaam in het Utrecht Medisch Centrum te Utrecht, NVK
- E. Schmidt-Cnossen, MSc, senior projectmedewerker, werkzaam bij Stichting Kind en Ziekenhuis - tot april 2019
- J. Pingen, MSc, junior project- en beleidsmedewerker, werkzaam bij Stichting Kind en Ziekenhuis - vanaf mei 2019
- Dr. S. Terheggen-Lagro, kinderarts-pulmonoloog, werkzaam bij het Amsterdam Universitair Medisch Centrum te Amsterdam, NVK
Met ondersteuning van
- Dr. J. Buddeke, adviseur, Kennisintituut van de Federatie Medisch Specialisten
- Dr. E. Breejen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Kapitein |
Kinderarts-intensivist, Amsterdam UMC, locatie AMC |
Human factor en crew resource management trainer (onbetaald) |
Geen |
Geen |
|
Balemans |
Kinderarts-pulmonoloog |
gastdocent TNO (astma bij kinderen voor jeugdartsen) Lid van MEC-U (medische ethische toetsingscommissie; samenwerking tussen het St. Antonius Ziekenhuis te Utrecht/Nieuwegein, het Catharina Ziekenhuis te Eindhoven, het Diakonessenhuis te Utrecht /Zeist /Doorn, het Maasstad Ziekenhuis te Rotterdam, het Meander Medisch Centrum te Amersfoort /Baarn en het OLVG te Amsterdam Visiteur voor de Registratiecommissie Geneeskundig Specialisten (RGS) -instellingsvisitaties |
Geen |
Geen |
|
Brinkhorst |
Kinderarts-pulmonoloog |
Lid Centraal Medisch Tuchtcollege (onkostenvergoeding) Instructeur SSHK (reiskostenvergoeding) |
Geen |
Geen |
|
Morsing |
Kinder-intensivist, UMC Utrecht |
Human factor en crew resource management trainer in healthcare |
Geen |
Geen |
|
Klein -Blommert |
Intensive care kinderverpleegkundige |
Docent aan de opleiding voor intensive care kinderen bij de Amstel Academie |
Geen |
Geen |
|
Schmidt – tot april 2019 |
Projectmanager - stichting kind en ziekenhuid 32 u p/w |
Psycholoog - laat ons ouders zijn (8/16 u p/w) Vrijwilliger ouderraad Sophia vrijwilliger VOC en vrijwilliger stichting Hiva |
Geen |
Geen |
|
Pingen – vanaf mei 2019 |
Junior project- en beleidsmedewerker |
Verzorgende niveau 3 |
Geen |
Geen |
|
Terheggen-Lagro |
Subafdelingshoofd kinderlongziekten, Amsterdam AMC, locatie AMC |
Betrokken bij ontwikkeling kwaliteitsstandaard CF (onbetaald) |
Geen |
Geen |
Inbreng patiëntenperspectief
Tijdens alle stappen van het ontwikkelproces is rekening gehouden met het patiëntperspectief. Een medewerker van stichting Kind en Ziekenhuis had zitting in de werkgroep. Tijdens de knelpuntenanalyse heeft stichting Kind en Ziekenhuis een knelpuntenanalyse uitgevoerd onder haar achterban. Tevens is de conceptrichtlijn voor commentaar aan stichting Kind en Ziekenhuis voorgelegd.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten van elke module. De werkgroep heeft besloten geen indicatoren te ontwikkelen bij de huidige richtlijn, omdat er geen substantiële barrières konden worden geïdentificeerd die de implementatie van de aanbeveling zouden kunnen bemoeilijken.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de ervaren knelpunten rondom de zorg van high flow onder relevante partijen. Middels een schriftelijke knelpuntenanalyse is er input gevraagd op het conceptraamwerk aan de Nederlandse Vereniging voor Kindergeneeskunde, Verpleegkundige en Verzorgende Nederland, Nederlandse Vereniging voor Spoedeisende Hulp Artsen, Ambulancezorg, Nederlands Huisartsen Genootschap, stichting Kind en Ziekenhuis, Longfonds, Patientenfederatie, Inspectie voor de Gezondheidszorg en Jeugd, Nederlandse Federatie van Universitair Medische Centra, Nederlandse Vereniging van Ziekenhuizen, Samenwerkende Topklinische opleidingsZiekenhuizen, Zorginstituut Nederland, Zelfstandige Klinieken Nederland, Zorgverzekeraars Nederland, DBC-onderhoud, ZonMW en de Nederlandse Zorgautoriteit. Een beknopte samenvatting van de schriftelijke knelpuntenanalyse is opgenomen in de is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal, belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: Cochrane – voor gerandomiseerd gecontroleerd onderzoek en PROBAST – voor prognostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Indicatorontwikkeling
De werkgroep heeft besloten geen indicatoren te ontwikkelen bij de huidige richtlijn, omdat er geen substantiële barrières konden worden geïdentificeerd die implementatie van de aanbeveling zouden kunnen bemoeilijken.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
