Vergroot ovarium in de zwangerschap
Uitgangsvraag
- Is het beter een benigne ovariumcyste/-tumor chirurgisch te verwijderen dan het in situ te laten in de zwangerschap?
- Welke benadering is beter voor de behandeling van een benigne vergroot ovarium tijdens de zwangerschap: laparoscopisch of laparotomisch?
Aanbeveling
Indien een ovariumcyste in de zwangerschap geen klachten geeft en er geen verdenking is op maligniteit is er plaats voor een expectatief beleid tot na de zwangerschap, ongeacht de grootte van de cyste.
In het eerste trimester van de zwangerschap is terughoudendheid geboden inzake chirurgische behandeling van een ovariumcyste gezien de kans dat de cyste spontaan verdwijnt en er mogelijk sprake is van een functionele cyste, tenzij er aanwijzingen zijn voor torsie van het ovarium of ovariumcarcinoom.
Indien in het eerste trimester sprake is van een torsie van het ovarium, dan is detorsie geïndiceerd en dient in principe geen cystectomie plaats te vinden.
Indien besloten wordt tot chirurgische behandeling van een ovariumcyste in de zwangerschap heeft het de voorkeur dit te plannen in het 2e trimester.
Indien sprake is van een ovariumcyste moet het risico op ovariumcarcinoom worden overwogen aangezien de zwangerschap niet mag leiden tot uitstel van behandeling van het ovariumcarcinoom.
Een laparoscopische benadering voor behandeling van een vergroot ovarium lijkt de voorkeur te hebben boven een laparotomische benadering omdat net zoals buiten de zwangerschap er minder bloedverlies peroperatief is en postoperatief minder pijn en een sneller herstel bij vergelijkbare neonatale uitkomsten.
Een laparoscopie in de zwangerschap dient te worden uitgevoerd door een ervaren laparoscopist.
Indien de uterus reikt tot boven de navel dient tijdens de zwangerschap een laparotomie sterk te worden overwogen.
De wijze waarop een laparoscopie uitgevoerd moet worden in de zwangerschap valt buiten het bestek van deze richtlijn. Hiervoor wordt verwezen naar de multidisciplinaire richtlijn 'Minimaal invasief'.
Overwegingen
Uitgangsvraag 1:
Gezien de kans dat een vergroot adnex veroorzaakt wordt door een (progesteron producerende) corpus luteumcyste is terughoudendheid geboden inzake chirurgie in het eerste trimester van de zwangerschap. Indien in het eerste trimester sprake is van een torsie van het ovarium is detorsie geïndiceerd en dient in principe geen cystectomie plaats te vinden.
Ook de grote kans dat een cyste spontaan verdwijnt is een argument om met chirurgische behandeling te wachten tot het 2e trimester van de zwangerschap.
Daarnaast is het risico op teratogeniciteit door anesthetica en het risico op een miskraam kleiner bij operatie in het 2e trimester (van de Velde, 2007).
In het 3e trimester van de zwangerschap wordt de zwangere uterus de beperkende factor voor veilig chirurgisch handelen.
Indien het vermoeden bestaat op ovariumcarcinoom is de zwangerschap geen contraindicatie voor chirurgische behandeling van een adnexcyste.
Uitgangsvraag 2:
Door het ontbreken van gerandomiseerde onderzoeken is er geen evident bewijs dat een laparoscopische benadering voorkeur heeft boven een laparotomische benadering in geval van een adnexcyste in de zwangerschap. Er is een beperkt aantal artikelen beschikbaar die de vergelijking maken tussen het laparoscopisch en laparotomisch verwijderen van een vergroot adnex in de zwangerschap. Vaak vergelijkt men een ‘oudere’ groep laparotomische ingrepen met een meer recente groep laparoscopische ingrepen.
Peroperatieve complicaties
De uitkomstmaat peroperatieve complicaties (spill/ruptuur/darm-ureter- of uterusletsel) wordt niet beschreven; de hoeveelheid bloedverlies lijkt bij een laparoscopische benadering lager te zijn dan bij een laparotomische benadering. Zoals bij elke scopie moet bij de counseling van een patiënte met een adnexcyste in de zwangerschap een kans op conversie naar laparotomie besproken worden (4-8%).
Postoperatieve complicaties
Net als bij een operatie buiten de zwangerschap zijn er aanwijzingen dat een laparoscopische benadering postoperatief sneller herstel, minder pijn en minder ileus geeft in vergelijking met een laparotomische benadering.
Om deze redenen zou een laparoscopische benadering de voorkeur hebben boven een laparotomische benadering van een vergroot adnex.
Negatieve neonatale uitkomsten
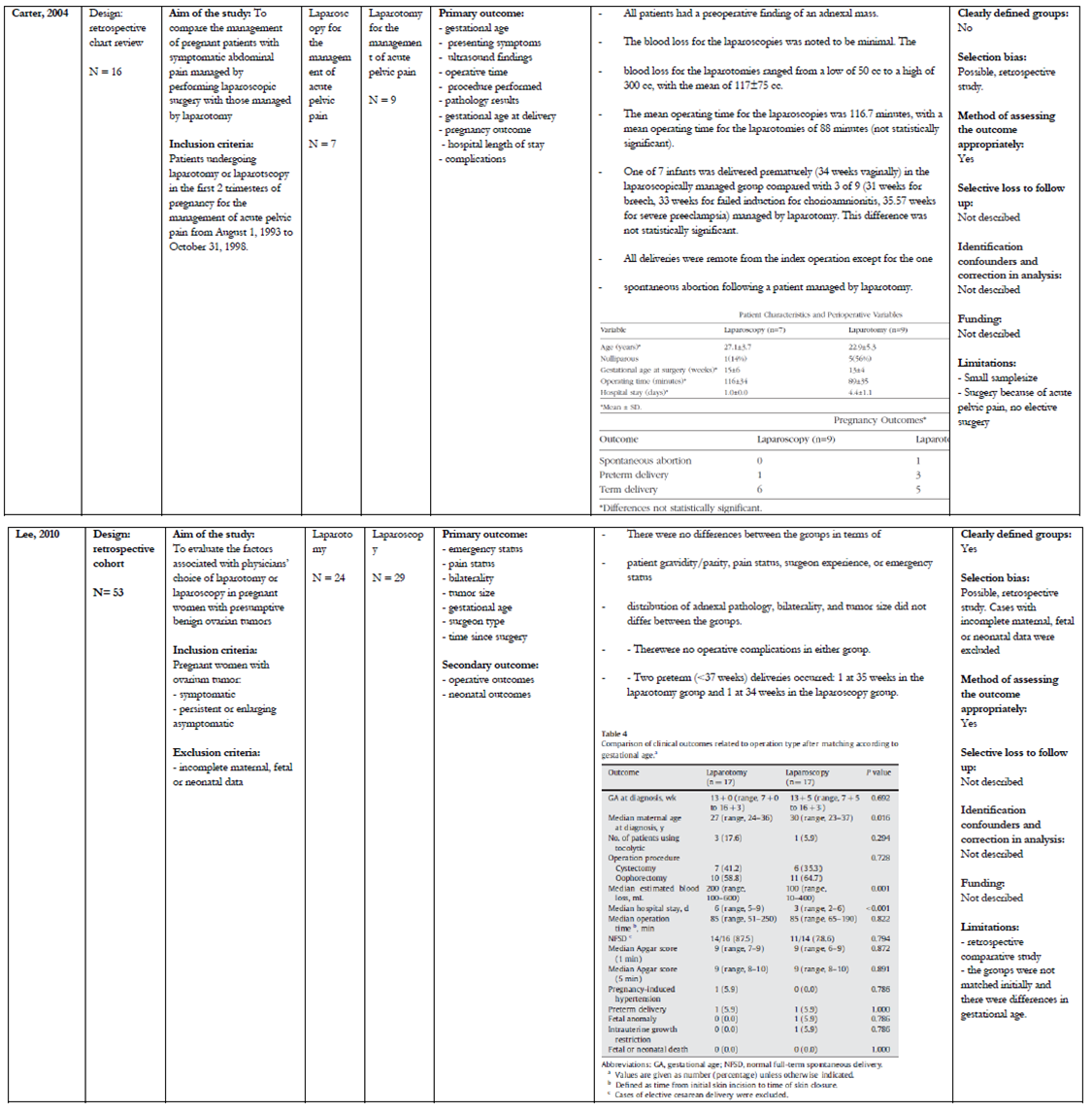
Het risico op vroeggeboorte in de algemene populatie is afhankelijk van de gebruikte definitie 4-8%. De onderzoekspopulaties zijn relatief klein en er is geen verschil in neonatale uitkomst gevonden. Het opereren van een vergroot adnex tijdens de zwangerschap wordt geassocieerd met een kans op miskraam en vroeggeboorte (Balthazar, 2011). Vroeggeboortes worden beschreven in beide groepen en zijn niet significant verschillend (Balthazar, 2011; Carter, 2004; Ribic, 2007; Soriano, 1999). Er kan bovendien niet in alle gevallen een relatie worden gelegd tussen vroeggeboorte en de ingreep. Ook miskramen worden gevonden in beide groepen.
Op basis van de gevonden literatuur kan geen uitspraak worden gedaan over de voorkeur voor laparotomische of laparoscopische benadering voor wat betreft neonatale effecten. Indien een patiënte geopereerd wordt aan een vergroot adnex in de zwangerschap dient zij geïnformeerd te worden over de kans op vroeggeboorte ongeacht de manier van opereren. Een laparoscopie is een minimaal invasieve ingreep met minder perioperatieve complicaties en sneller postoperatief herstel. Het risico op vroeggeboorte is in beide groepen niet significant verschillend. Om deze redenen zou een laparoscopische benadering van een vergroot adnex in de zwangerschap dus de voorkeur hebben. Een laparoscopische procedure in een verder gevorderde zwangerschap waarbij de uterus tot aan de navel reikt kan echter lastig zijn door gebrek aan ruimte voor manipulatie aan het vergrote ovarium waardoor in theorie meer kans is op conversie en complicaties. Indien geen ervaren laparoscopist beschikbaar is dient een laparotomie overwogen te worden om een langdurige ingreep en/of complicaties te voorkomen.
Onderbouwing
Door echoscopisch onderzoek vroeg in de zwangerschap worden er frequent ovariële cysten gediagnosticeerd in de zwangerschap. Dit zijn veelal luteale/functionele cysten die spontaan verdwijnen. Echter een ovariumcyste in de zwangerschap kan ook persisteren en leiden tot complicaties als torsie, ruptuur, bloeding of inklemming. Een reden om van chirurgie af te zien zijn risico’s op chirurgische en obstetrische complicaties. In dit hoofdstuk wordt beschreven hoe groot de risico’s zijn van een expectatief beleid ten opzichte van de risico’s van chirurgisch ingrijpen. Verder wordt beschreven of er voorkeur is voor een laparoscopische benadering dan wel laparotomische benadering in de zwangerschap.
|
Uitgangsvraag 1 |
|
|
Kwaliteit van bewijs: ZEER LAAG |
Over het spontane verloop van ovariële cysten in zwagerschap wordt wisselend gerapporteerd. Mediaan verdwijnen spontaan 61% van de ovariële cysten (spreiding 26-74%).
Bernhard 2009, Condous 2004, Thorton 1987, Zanetta 2003 |
|
Kwaliteit van bewijs: ZEER LAAG |
Op basis van de gevonden literatuur kan geen uitspraak worden gedaan over het risico op groei van een ovariële cyste in de zwangerschap.
Caspi 2000 |
|
Kwaliteit van bewijs: ZEER LAAG |
Inklemming, ruptuur en bloeding van een ovariële cyste in de zwangerschap worden wel beschreven in de literatuur maar lijken een sporadisch voorkomend probleem te zijn.
Bernhard 2009, Caspi 2000, Katz 2010 |
|
Kwaliteit van bewijs: ZEER LAAG |
Het mediane risico op torsie van een ovariële cyste in de zwagerschap is 3.2% (spreiding 0-10%).
Bernhard 2009, Caspi 2000, Condous 2004, Katz 2010, Schmeler 2005, Zanneta 2003 |
|
Kwaliteit van bewijs: ZEER LAAG |
De kans op torsie van een ovariële cyste in de zwangerschap lijkt het grootst bij diameter tussen 6-10 cm.
Yen 2009 |
|
Kwaliteit van bewijs: ZEER LAAG |
Het risico op ovariumcarcinoom bij ovariële cyste in de zwangerschap lijkt zeer laag (<1%)
Balci 2008, Bernhard2009, Condous 2004, George 1997, Ko 2009, Koo-1 2011, Kumai 2006, Platek 1995, Schmeler 2005, Thorton 1987, Turkcouglu 2009, Usui 2000, Yen 2009, Zanetta 2003 |
|
Kwaliteit van bewijs: ZEER LAAG |
Obstetrische complicaties als (dreigende) vroeggeboorte en IUVD bij chirurgie aan een ovariële cyste in de zwangerschap worden beschreven in de literatuur. De hoogte van het risico op obstetrische complicaties is onbekend omdat het vaak lastig is om een causaal verband te leggen.
Ko 2009, Koo-2 2011, Mathevet 2003, Moore 1999, Nahar 2008, Ramli 2009, Turkcouglu 2009, Usui 2000, Zanetta 2003 |
|
Uitgangsvraag 2 |
|
|
Kwaliteit van bewijs: ZEER LAAG |
Bij laparoscopische benadering lijken er minder peri- en postoperatieve complicaties op te treden dan bij laparotomische benadering.
Akira 1999, Balthazar 2011, Carter 2004, Lee 2010, Ribic 2007, Soriano 1999 |
|
Kwaliteit van bewijs: ZEER LAAG |
Er is geen verschil in neonatale uitkomsten tussen laparoscopische en laparotomicshe benadering van een vergroot ovarium.
Akira 1999, Balthazar 2011, Carter 2004, Lee 2010, Ribic 2007, Soriano 1999 |
Uitgangsvraag 1: Is het beter een benigne ovariumcyste/-tumor chirurgisch te verwijderen dan het in situ te laten in de zwangerschap?
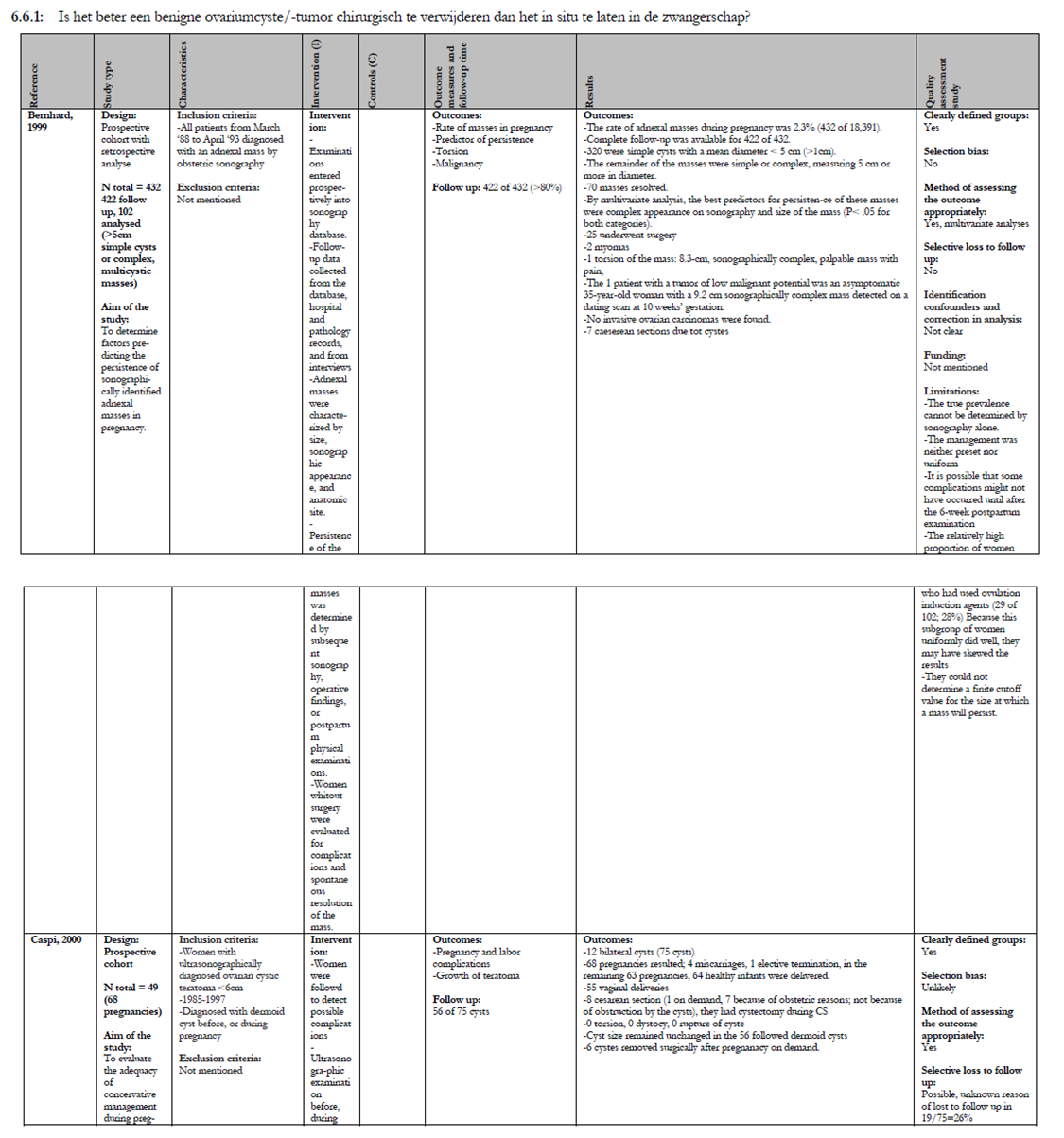
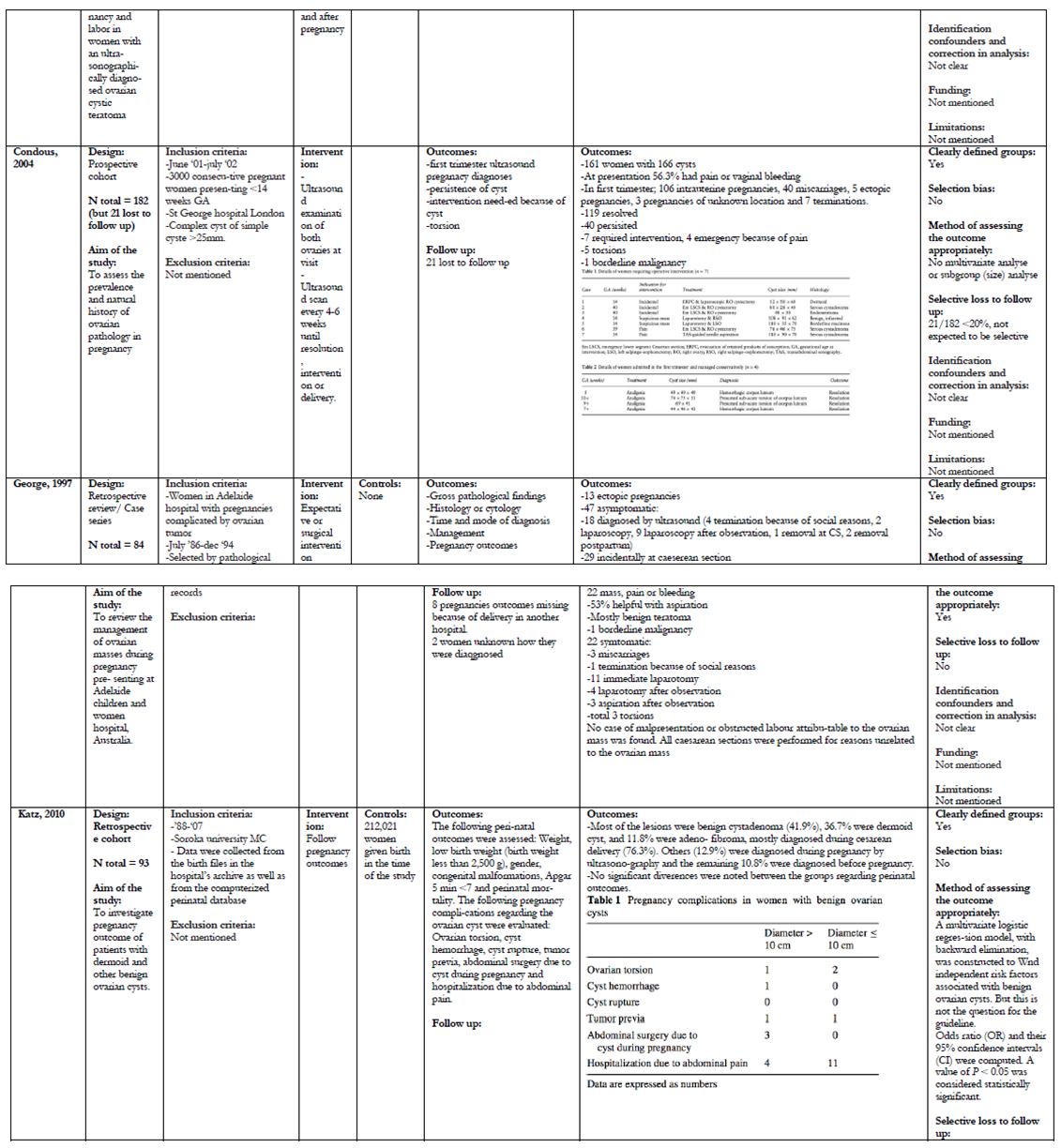
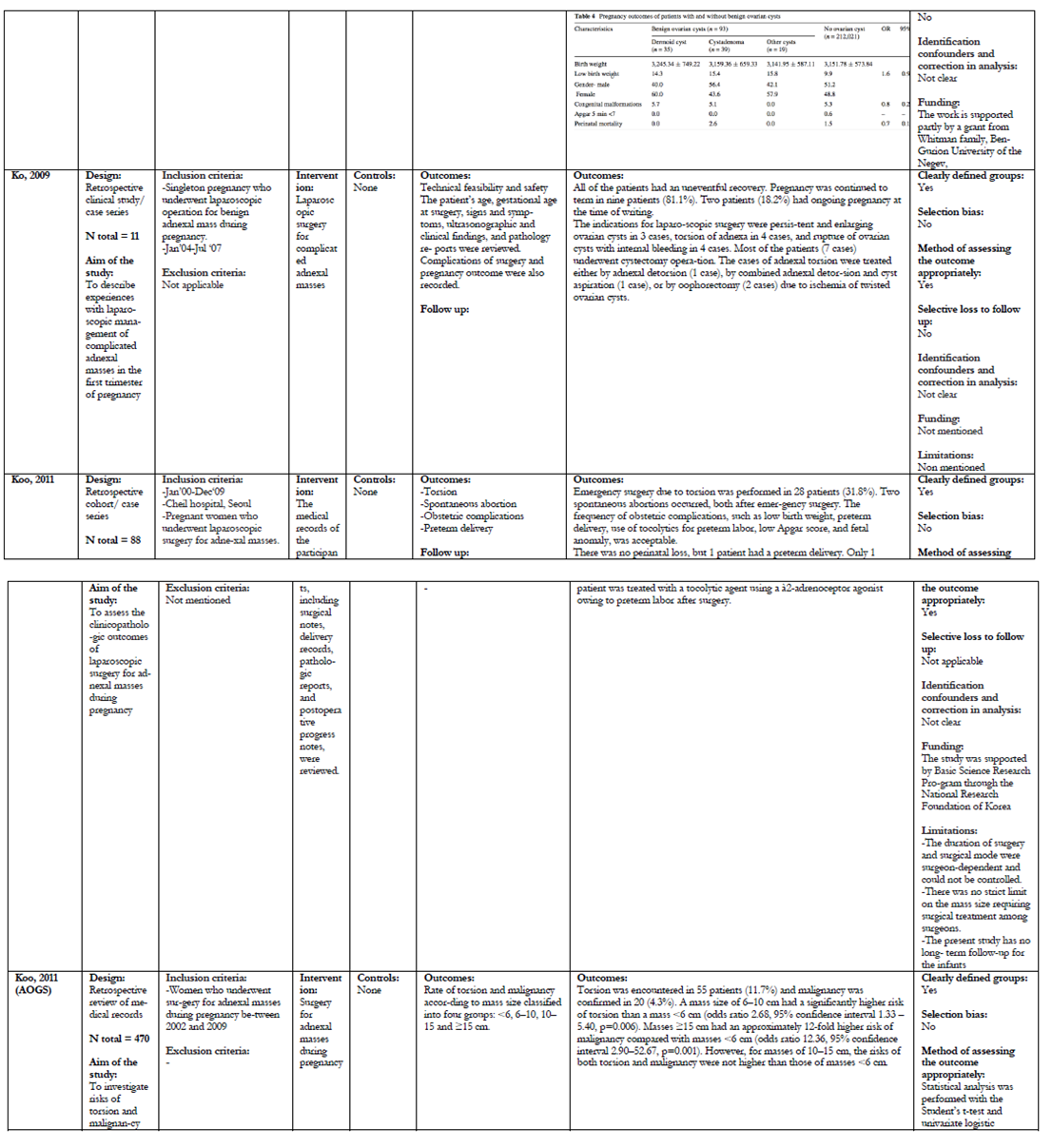
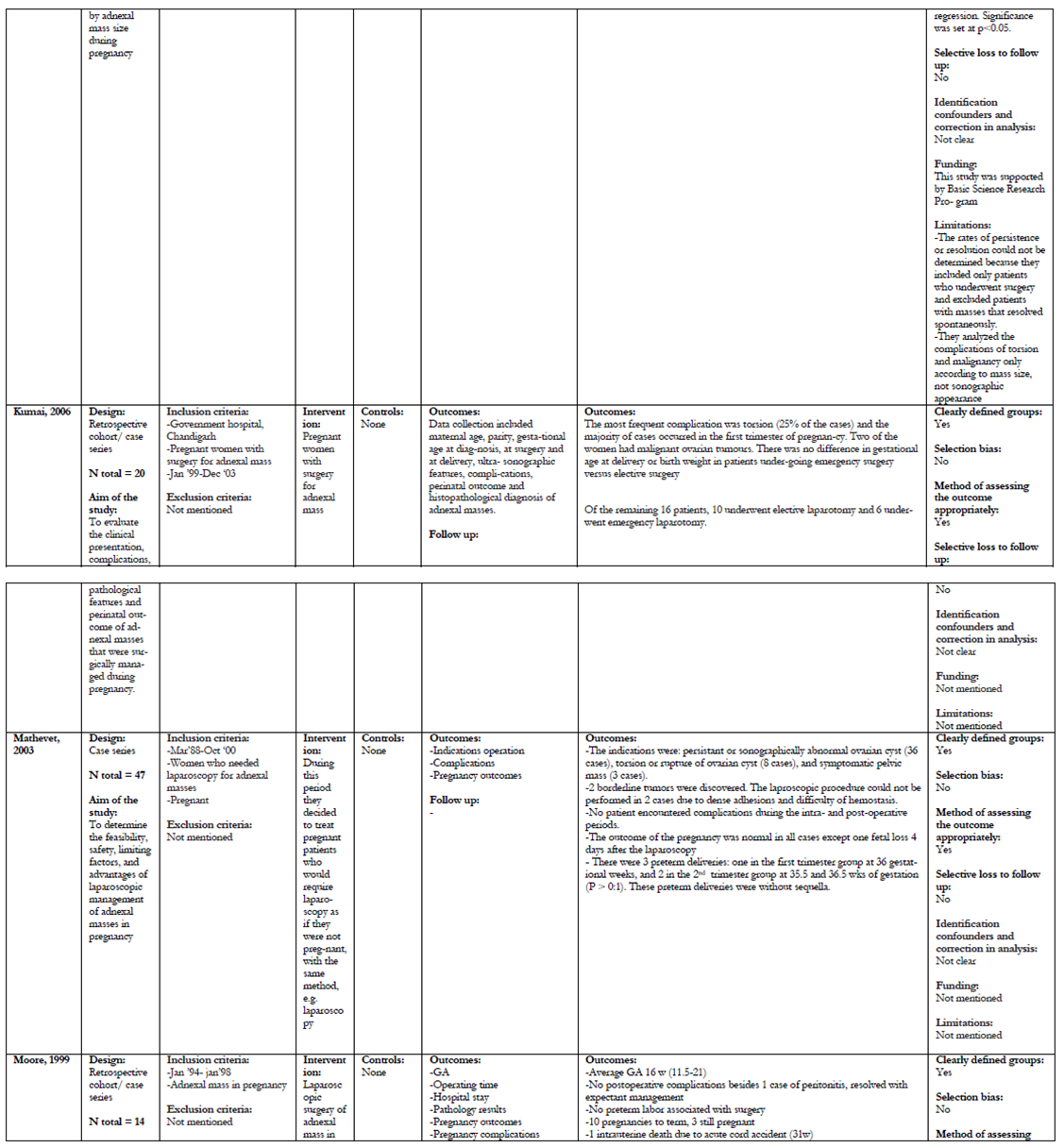
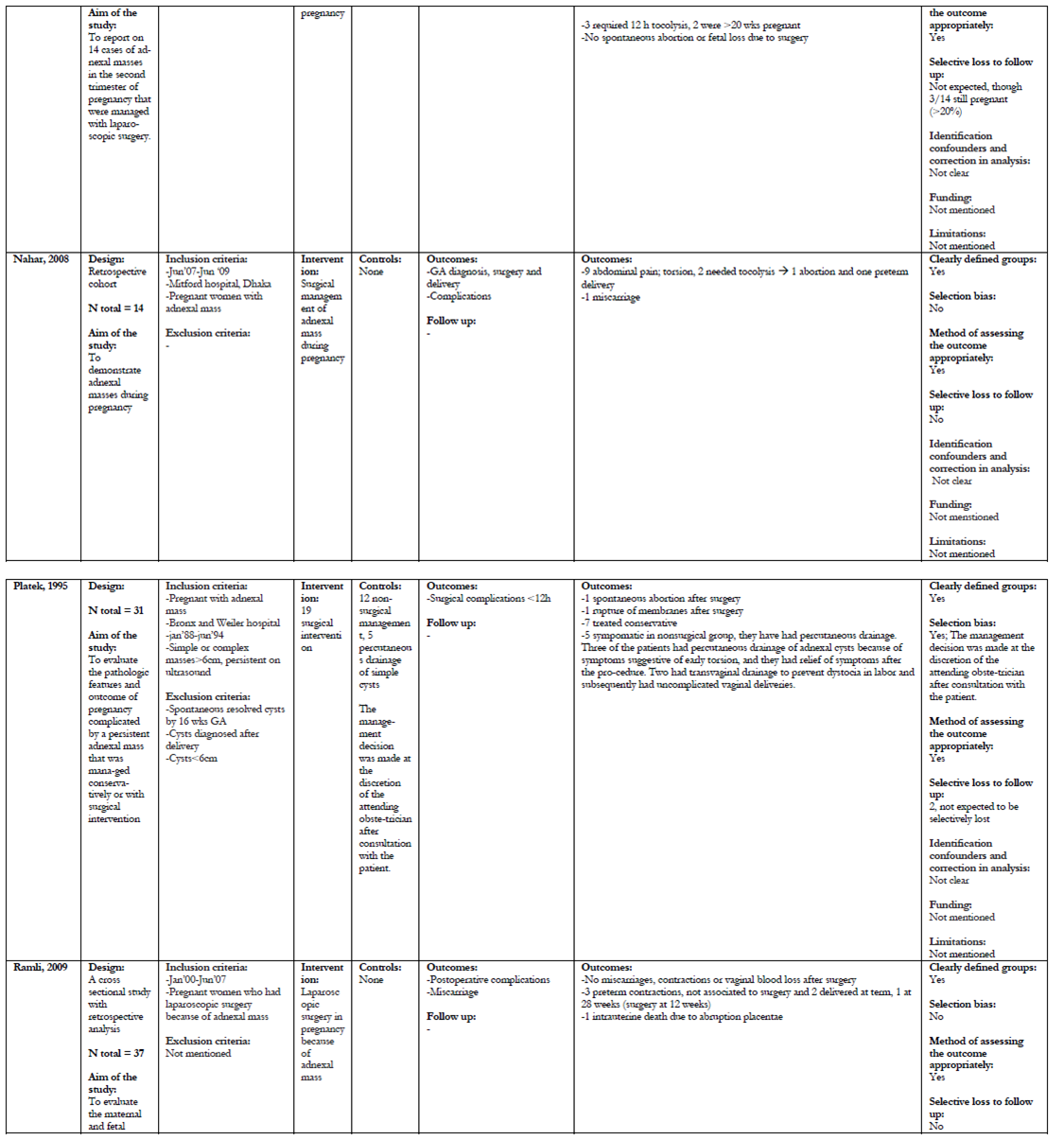
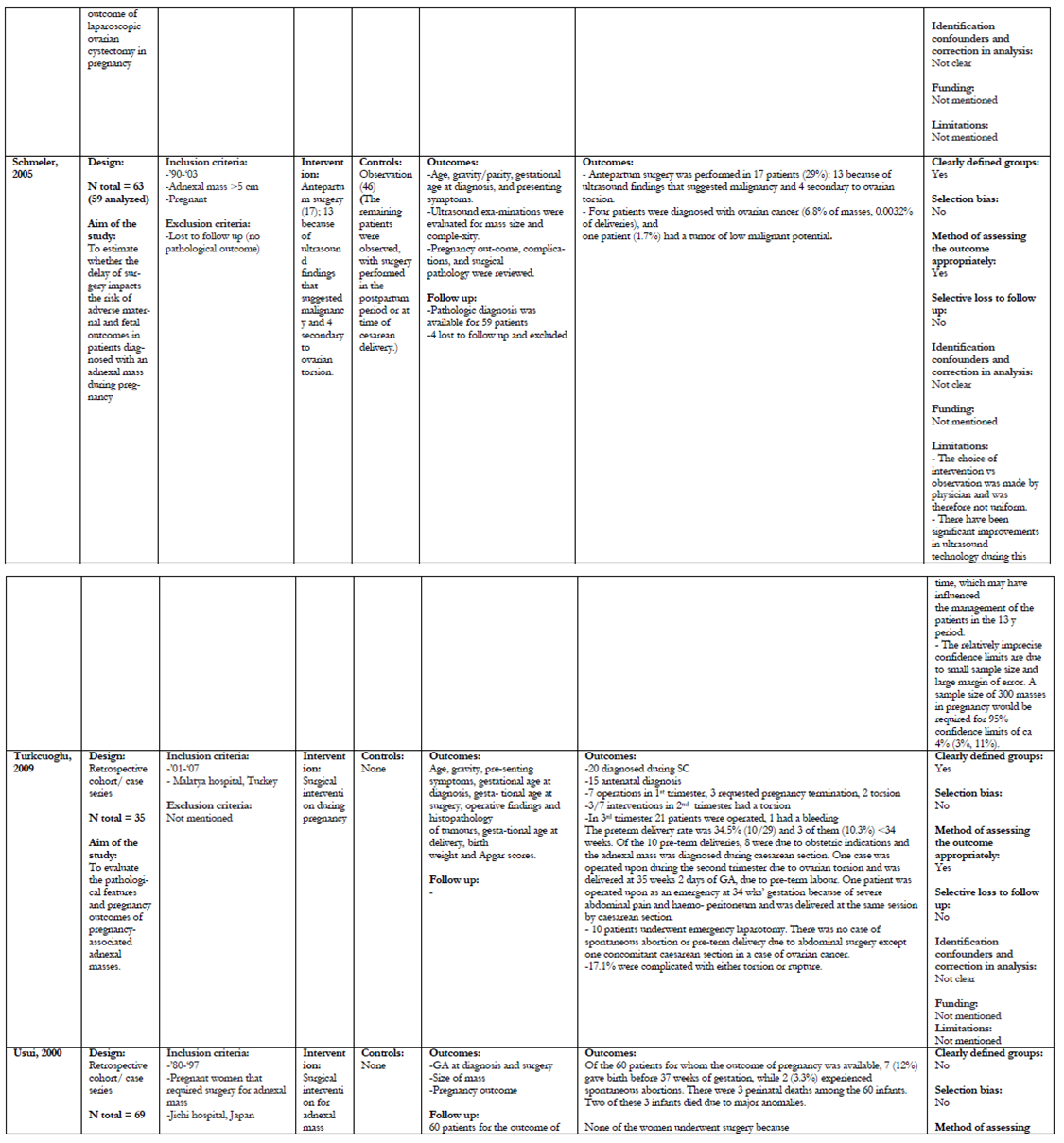
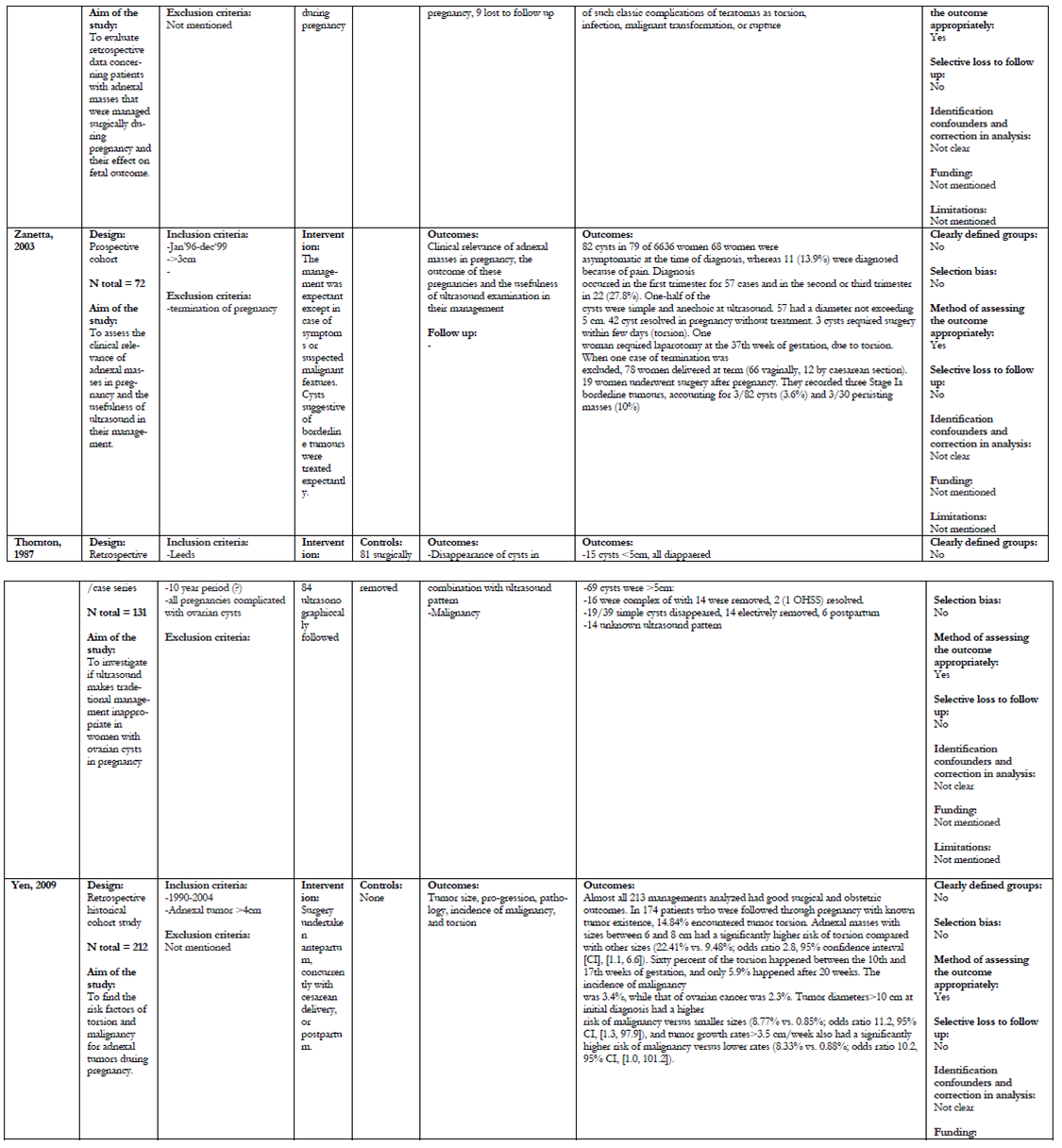
Er zijn 21 onderzoeken geselecteerd voor het beantwoorden van deze uitgangsvraag (Balci, 2008; Bernhard, 2009; Caspi, 2000; Condous, 2004; George, 1997; Katz, 2010; Ko, 2009; Koo-1, 2011; Koo-2, 2011; Kumai, 2006; Mathevet, 2003; Moore, 1999; Nahar, 2008; Platek, 1995; Ramli, 2009; Schmeler, 2005; Thornton, 1987; Turkcouglu, 2009; Usui, 2000; Yen, 2009; Zanetta, 2003).
De uitkomsten van deze retrospectieve cohortstudies/caseseries met een matige tot lage kwaliteit staan samengevat in bijlage 3 (tabel A en B); de grade tabellen staan in deze tekst.
Er zijn geen RCT’s die expectatief beleid met chirurgische interventies bij vergrote ovaria in de zwangerschap vergelijken. Bij de 21 geïncludeerde onderzoeken is onderscheid gemaakt in onderzoeken waarbij alle patiënten met (verdenking op) een vergroot ovarium in de zwangerschap werden geopereerd (Balci, 2008; George, 1997; Ko, 2009; Koo-1, 2011; Koo- 2, 2011; Kumai, 2006; Mathevet, 2003; Moore, 1999; Nahar, 2008; Ramli, 2009; Turkcouglu, 2009; Usui, 2000; Yen, 2009) en onderzoeken waarbij in principe een expectatief beleid werd gevoerd, tenzij er complicaties optraden of als er op basis van echografische bevindingen een verdenking op maligniteit was (Bernhard, 2009; Caspi, 2000; Condous, 2004; Katz, 2010; Platek, 1995; Schmeler, 2005; Thornton, 1987; Zanetta, 2003). Voor de foetale uitkomstmaten (IUVD, tocolyse en vroeggeboorte) en risico maligniteit zijn alle onderzoeken geïncludeerd. Voor de uitkomstmaten spontane regressie, groei, ruptuur, torsie, bloeding en inklemming zijn de onderzoeken gebruikt waarbij een expectatief beleid werd gevoerd.
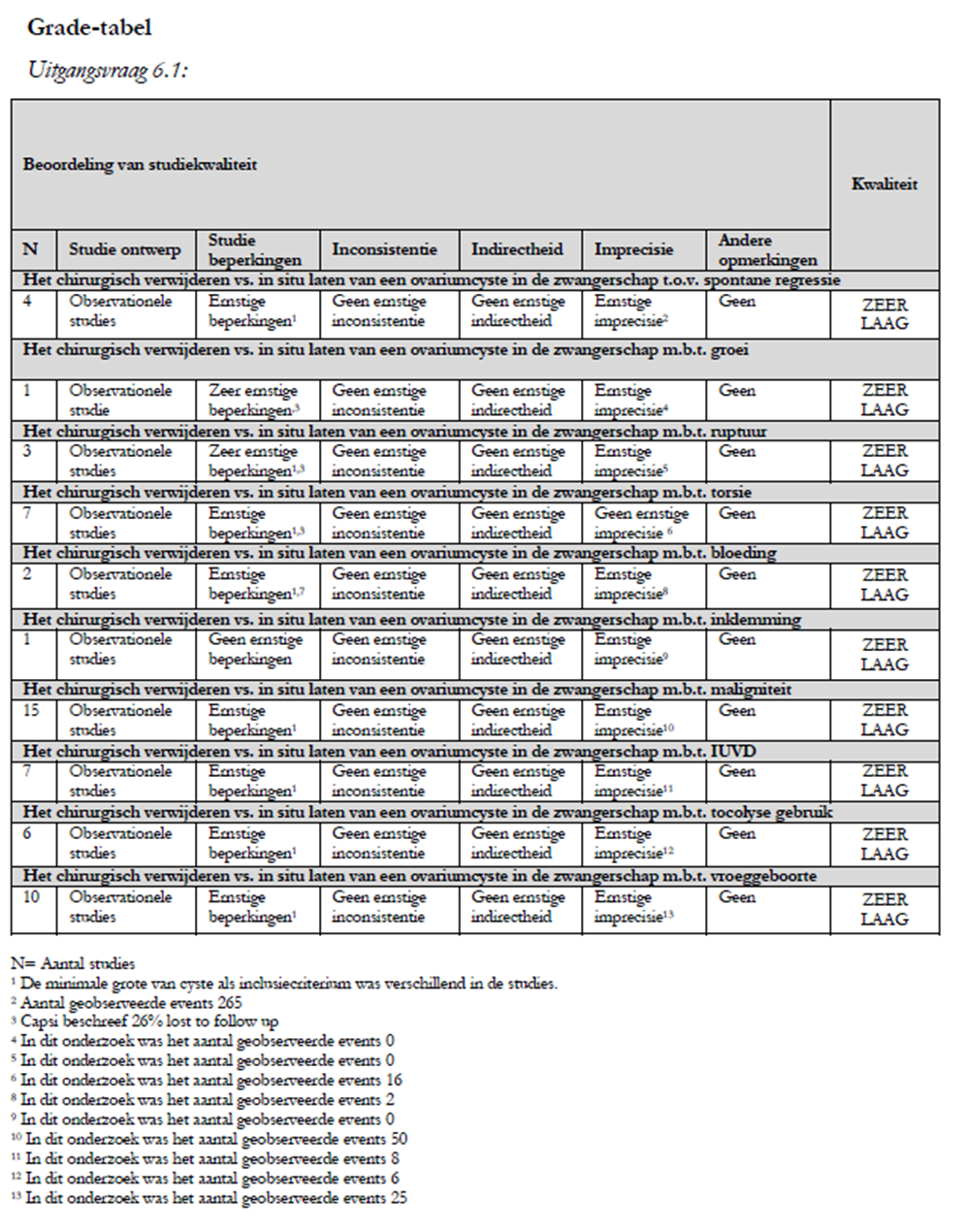
Spontane regressie van de ovariële cyste
Vier onderzoeken beschrijven spontane regressie van de cyste tijdens de zwangerschap (Bernhard, 2009; Condous, 2004; Thornton, 1987; Zanetta, 2003). Mediaan verdwijnen 61% van de cysten die tijdens de zwangerschap worden gevonden (min 26%- max 74%). Bernhard analyseert complexe, multicysteuze adnexa en ovariële cysten groter dan 5 cm. Bij 70/102 (69%) verdwijnt de cyste. Condous beschrijft de grootste groep cysten (n=161), waarvan er 119 spontaan verdwijnen (74%). Thornton beschrijft een spontane regressie van 26%, echter heeft slechts 84 van de 131 vrouwen met cysten in de zwangerschap echografisch vervolgd. Er werden 15 cysten <5 cm gezien, welke allemaal weg waren bij volgend onderzoek. Van 39 uniloculaire cysten groter dan 5 cm verdwenen er 19 (49%). Zanetta beschrijft het verdwijnen of het afnemen van de massa voor >50% bij 42/79 cysten (53.2%). Dit was bij 27/39 (69%) uniloculaire cysten van max 15 cm (22 waren kleiner dan vijf cm).
Groei van de ovariële cyste/massa
Groei van de cyste wordt slechts in één onderzoek gemeld (Caspi, 2000). Caspi heeft complete follow-up van 56/63 zwangerschappen. Hierbij werd geen significante toename van de grootte van de cysten gezien.
Ruptuur van de massa
Drie onderzoeken beschrijven het wel of niet voorkomen van een ruptuur van een ovariële cyste (Bernhard, 2009; Caspi, 2000; Katz, 2010). Hierbij werd bij de totaal geïncludeerde 541 vrouwen geen ruptuur van de ovariële cyste gezien.
Torsie van het ovarium
Zes onderzoeken beschrijven het voorkomen van een torsie van het ovarium (Bernhard, 2009; Caspi, 2000; Condous, 2004; Katz, 2010; Schmeler, 2005; Zanetta, 2003); mediane incidentie is 3.2% (range 0%-10%).
Bernhard heeft 320 vrouwen gediagnosticeerd met een uniloculaire cyste <5 cm en 102 vrouwen met een complexe/multicysteuze/>5 cm massa. Geen van de vrouwen met een uniloculaire cyste hebben een torsie gehad. Van de resterende 102 vrouwen tordeerde één ovarium met een complexe cyste van 8.3 cm.
Caspi heeft vrouwen met een cysteus teratoom van het ovarium in de zwangerschap gevolgd. Bij de 68 geïncludeerde vrouwen was geen enkele torsie van het ovarium.
Condous omschrijft een torsie bij vijf van de 166 vrouwen (3%). Drie in het eerste trimester, waarvan twee conservatief werden behandeld en één een transabdominale aspiratie van de cyste (9 cm) kreeg bij 14 weken zwangerschap. Eén vrouw werd bij 14 weken zwangerschap geopereerd wegens echografische verdenking op maligniteit (8.7 cm) bij de torsie, wat benigne bleek. De laatste vrouw had een torsie bij 39 weken zwangerschap en heeft tegelijkertijd met de cystectomie (6.6 cm) een sectio gekregen.
Katz beschrijft bij drie van de 93 benigne cysten in de zwangerschap een torsie, waarbij één cyste groter was dan 10 cm (3%).
In Schmeler’s onderzoek werd bij drie vrouwen met verdenking op een torsie percutane drainage toegepast. De klachten verdwenen hierop direct, waarop Schmeler de verdenking torsie aannemelijk vindt. De cysten waren respectievelijk 10, 15 en 23 cm.
Zanetta rapporteert vier torsies in zijn onderzoek (n=82) (4.9%). Twee vrouwen met een zwangerschapsduur van zeven weken en een cyste van 4-5 cm hadden een laparoscopie 1-3 dagen na diagnose van de cyste wegens een torsie. Eén vrouw, acht weken zwanger, kreeg een laparotomische detorsie van de corpus luteum cyste. De laatste torsie vond plaats in de 37e zwangerschapsweek; de cystectomie werd gecombineerd met een sectio.
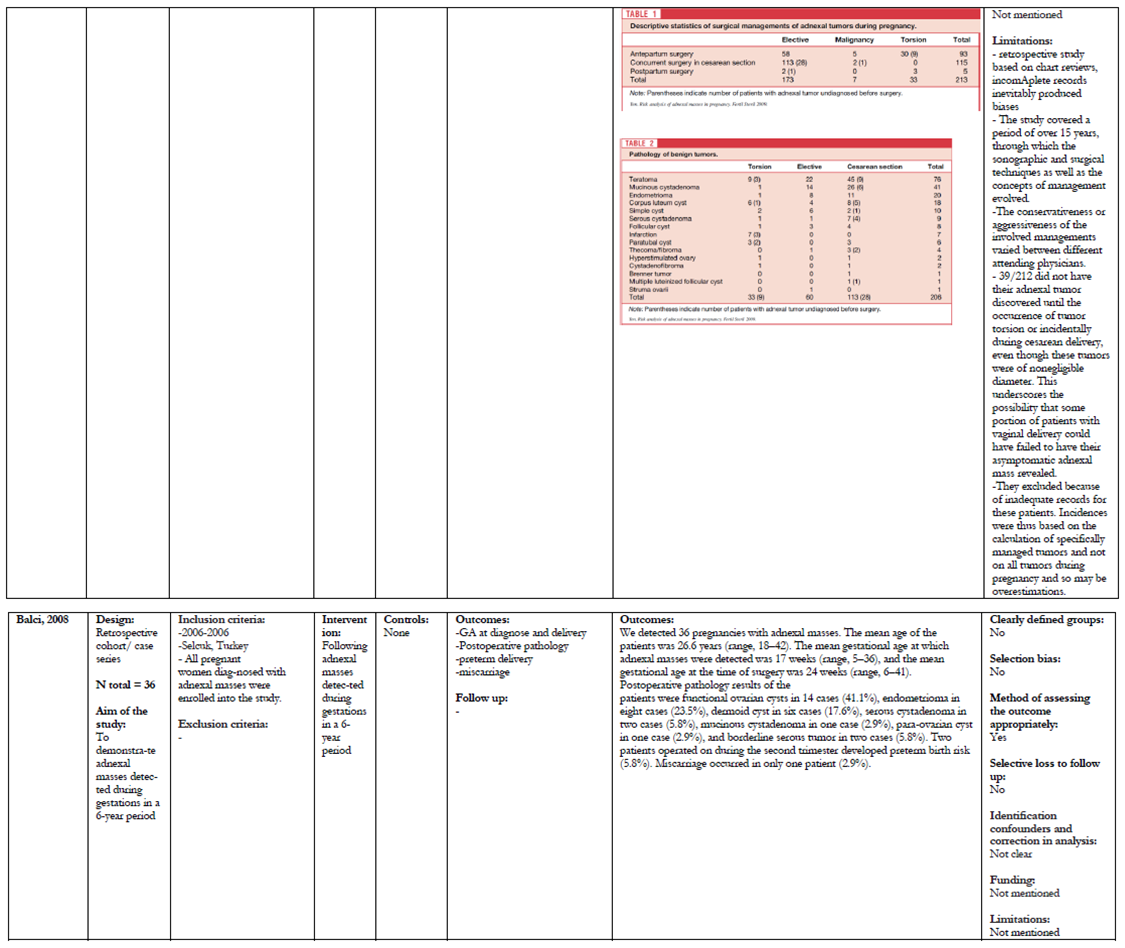
In het onderzoek van Yen worden vrouwen geïncludeerd die direct werden geopereerd. Voor de incidentiecijfers wordt dit onderzoek niet meegenomen, echter hierbij wordt wel het risico van torderen beschreven bij verschillende grootten van de cyste. Yen beschrijft bij 212 geïncludeerden 33 torsies, waarvan er drie postpartum optraden. Bij 24 van de 174 vrouwen met een bekende cyste werd een torsie geobserveerd, hierbij kwam een torsie significant vaker voor bij een cyste van 6-8 cm (22% vs. 9%, p<0.05). De kans op torsie bij een ovarium van die grootte is driemaal zo hoog, OR 2.8 (95% CI 1.1-6.6).
Bloeding van de cyste
Twee onderzoeken beschrijven het al dan niet voorkomen van een bloeding van de massa van het ovarium (Bernhard, 2009; Katz, 2010).
Een bloeding komt voor bij 1% van de adnexcysten (mediaan, spreiding 1.0-1.1%). In het onderzoek van Bernhard (n=422) werd bij de 102 vrouwen met een complexe, multicysteuze of grote (>5 cm) cyste eenmalig een bloeding gezien. Bij de 31 geopereerde cystes bleek één een hemorragisch corpus luteum. Katz (n—93) heeft bij één van de benigne ovariumcysten een bloeding beschreven.
Inklemming
Eén onderzoek noemt de mogelijkheid van inklemming van het ovarium (Bernhard, 2009). In dit onderzoek is het niet voorgekomen.
Risico op maligniteit
Vijftien onderzoeken beschrijven het risico op maligniteit bij een vergroot adnex (Balci, 2008; Bernhard, 2009; Condous, 2004; George, 1997; Ko, 2009; Koo-1, 2011; Koo-2, 2011; Kumai, 2006; Platek, 1995; Schmeler, 2005; Thornton, 1987; Turkcouglu, 2009; Usui, 2000; Yen, 2009; Zanetta, 2003).
De onderzoeken van Condous, Platek en Thornton lijken het meest betrouwbaar voor inschatting van het risico op maligniteit, omdat deze onderzoeken een echte expectatieve groep hebben. Bij de andere onderzoeken is groot risico op selectiebias, omdat alle geïncludeerde patiënten een adnexoperatie ondergaan. Het inclusiecriterium is bij deze onderzoeken dus niet een zwangere met een echoscopisch vergoot adnex, maar een zwangere die een operatie heeft ondergaan in verband met een vergroot adnex (tijdens zwangerschap en tijdens sectio). In het onderzoek van Thornton is ook een echte expectatieve tak, echter gezien de huidige echoscopische technieken is dit onderzoek niet (meer) representatief.
Condous heeft 7/161 vrouwen geopereerd, twee in verband met een op maligniteit verdachte massa. Bij één van deze vrouwen was sprake van een borderline mucineus tumor van 11 cm, deze werd bij een zwangerschapsduur van 14 weken verwijderd. De andere patiënte met verdenking maligniteit werd bij 14 weken zwangerschap geopereerd aan een benigne geïnfarceerde cyste.
Platek beschrijft in zijn onderzoek van 31 vrouwen geen maligniteit, echter één patiënte waarbij expectatief beleid werd gevolgd was bij het schrijven van het artikel nog niet bevallen en twee vrouwen waren lost to follow-up, waardoor geen pathologieuitslag kon worden weergegeven.
Thornton heeft geen maligniteit in zijn onderzoek (n=131), echter wel zes borderline casussen. Alle massa’s waren groter dan 5 cm (6, 8, 10, 12, 12 en 28cm).
Intra uteriene vruchtdood (IUVD).
Zeven onderzoeken maken melding van het al dan niet optreden van een intrauterine vruchtdood in combinatie met een vergroot adnex (Ko, 2009; Koo-2, 2011; Mathevet, 2003; Moore, 1999; Ramli, 2009; Usui, 2000; Zanetta, 2003).
Zanetta, Ko, Ramli en Koo-2 melden dat er geen IUVD’s zijn opgetreden (totale onderzoekspopulatie n= 208).
Bij zes van de zeven onderzoeken werd de samenhang met de ovariële cyste verworpen, echter de overgebleven inclusie met mogelijke samenhang wordt niet nader omschreven. Mathevet heeft één IUVD in zijn onderzoek (n=47). Bij deze patiënte overleed de foetus vier dagen na laparoscopische cystectomie bij 17 weken zwangerschap. Er werden geen abnormale parameters van de anesthesie en de operatie achterhaald.
Moore (n=14) heeft één IUVD. Bij autopsie bleek het te gaan om een di-amniotische, monochoriale gemelli met meerdere vasculaire anastomosen tussen een gedeeltelijke mola placenta, die leidde tot een vasculair event. De correlatie met de ovariële massa werd verworpen.
Usui heeft één IUVD in zijn groep van 60 vrouwen. De patiënt had een teratoom van 10 cm, die bij een zwangerschap van 13 weken werd verwijderd. Bij 41 weken zwangerschap beviel zij van een overleden normaal gevormd kind van 3784 gram. Bij autopsie is de doodsoorzaak niet vastgesteld maar de placenta liet tekenen van chorioamnionitis zien.
Tocolyse en vroeggeboorte
Zes onderzoeken beschrijven de uitkomsten van vroeggeboorte en het gebruik van tocolyse bij een vergroot adnex (Balci, 2008; Ko, 2009; Koo-2, 2011; Moore, 1999; Nahar, 2008; Platek, 1995). Vier onderzoeken beschrijven alleen vroeggeboorte (Kumai, 2006; Ramli, 2009; Turkcouglu, 2009; Usui, 2000).
Balci heeft 34/36 geïncludeerde patiënten geopereerd; hierbij was bij twee vrouwen sprake van een vroeggeboorte. Zij werden in het derde trimester geopereerd, waarna zij tekenen van een dreigende vroeggeboorte ontwikkelden. Ze werden opgenomen en er werd gestart met tocolyse. Bij een zwangerschapstermijn van 32 respectievelijk 33 weken kregen zij een sectio en kwamen twee gezonde kinderen ter wereld die geen NICU opname behoefden.
Platek beschrijft een patiënt met spontaan gebroken vliezen tijdens een bilaterale cystectomie bij 20 weken zwangerschap. Er was geen tocolyse nodig, patiënte beviel a terme van een gezond kind.
In het onderzoek van Ko werden alle foetussen (n=11) a terme geboren, net als in het onderzoek van Moore (n=14). Echter in het laatste onderzoek kregen drie vrouwen tocolytica postoperatief. Twee patiënten waren langer dan 20 weken zwanger en één 16 weken. Zij konden na 2 dagen het ziekenhuis gezond verlaten en zijn bevallen van a terme kinderen.
Koo-2 (n=88) beschrijft één vroeggeboorte (<37 w) na operatief ingrijpen, waarbij het gebruik van ritodrine geen soelaas gaf. Er zijn geen gegevens over de operatie, zwangerschap of uitkomst bekend.
Preterme bevalling (niet nader omschreven) komt in het onderzoek van Kumai (n=20) twee maal voor, één na een spoedingreep en één na een electieve laparotomie.
Alle negen vrouwen met een torsie in het tweede trimester werden geopereerd in het onderzoek van Nahar (n=14); hiervan ontwikkelden twee vrouwen ondanks tocolytica blijvende uterusactiviteit, waarvan één resulteerde in een spontane abortus en één in een vroeggeboorte waarbij een sectio wegens foetale nood werd uitgevoerd.
Ramli (n=37) beschrijft drie casussen dreigende vroeggeboorte bij 28 weken, waarvan één patiënte daadwerkelijk bij die termijn beviel. Zij had een ongecompliceerde cystectomie gehad bij 12 weken zwangerschap.
Van de 35 geïncludeerde vrouwen in het onderzoek van Turkcouglu werden 20 tijdens de sectio gediagnosticeerd met een cyste. In de gehele groep waren tien premature geboortes, echter de verdeling over symptomatische cyste, antenatale diagnose en diagnose bij sectio is onbekend.
In het onderzoek van Usui eindigde 7/60 zwangerschappen in een geboorte voor 37 weken. Verdere details zijn niet bekend.
Uitgangsvraag 2: Welke benadering is beter voor de behandeling van een benigne vergroot ovarium tijdens de zwangerschap: laparoscopisch of laparotomisch?
Er waren in totaal zes artikelen bruikbaar voor het beantwoorden van onze vraagstelling (zie bijlage 5.6.2 voor de zoekverantwoording en bijlage 6.6.2 voor de evidencetabel).
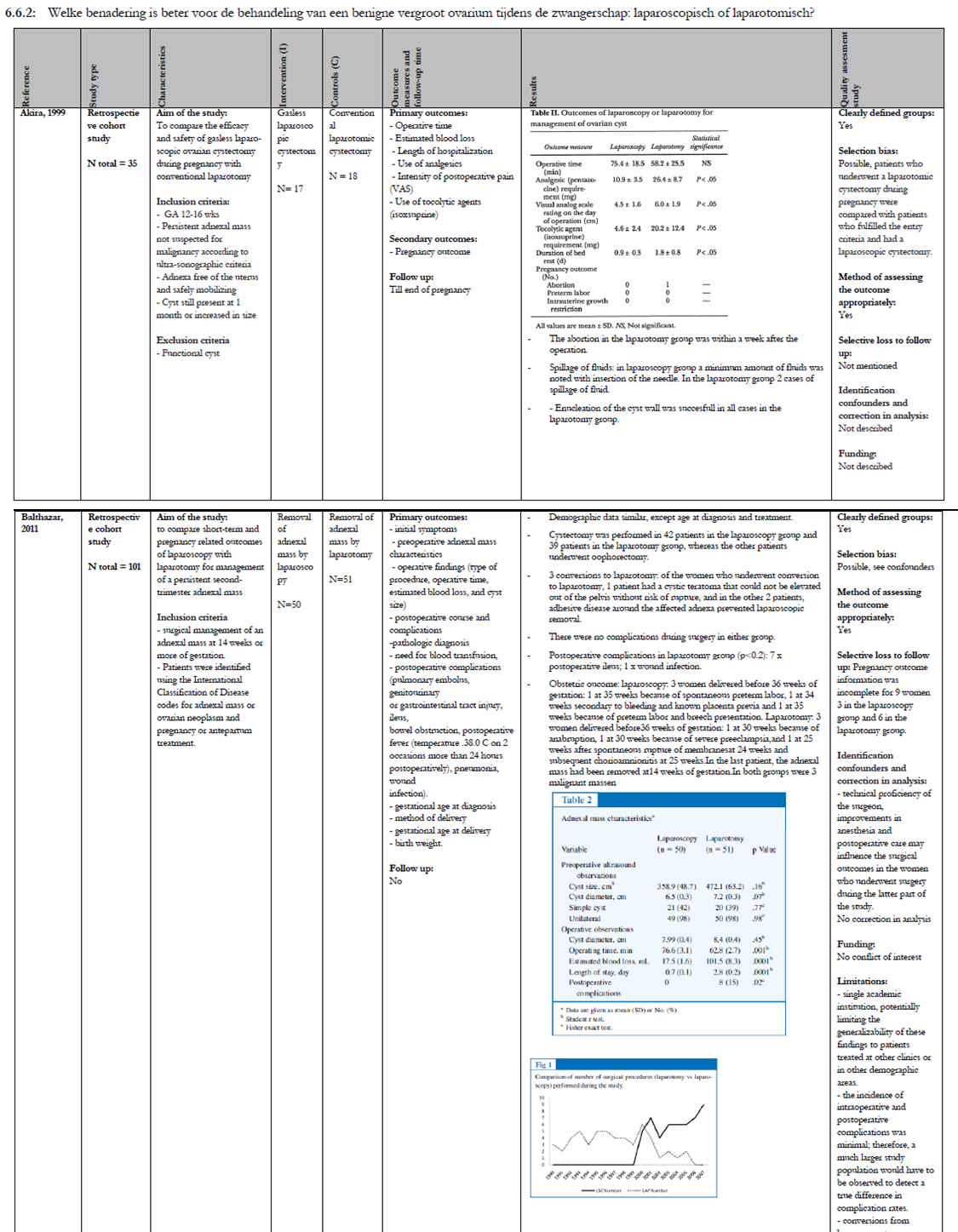
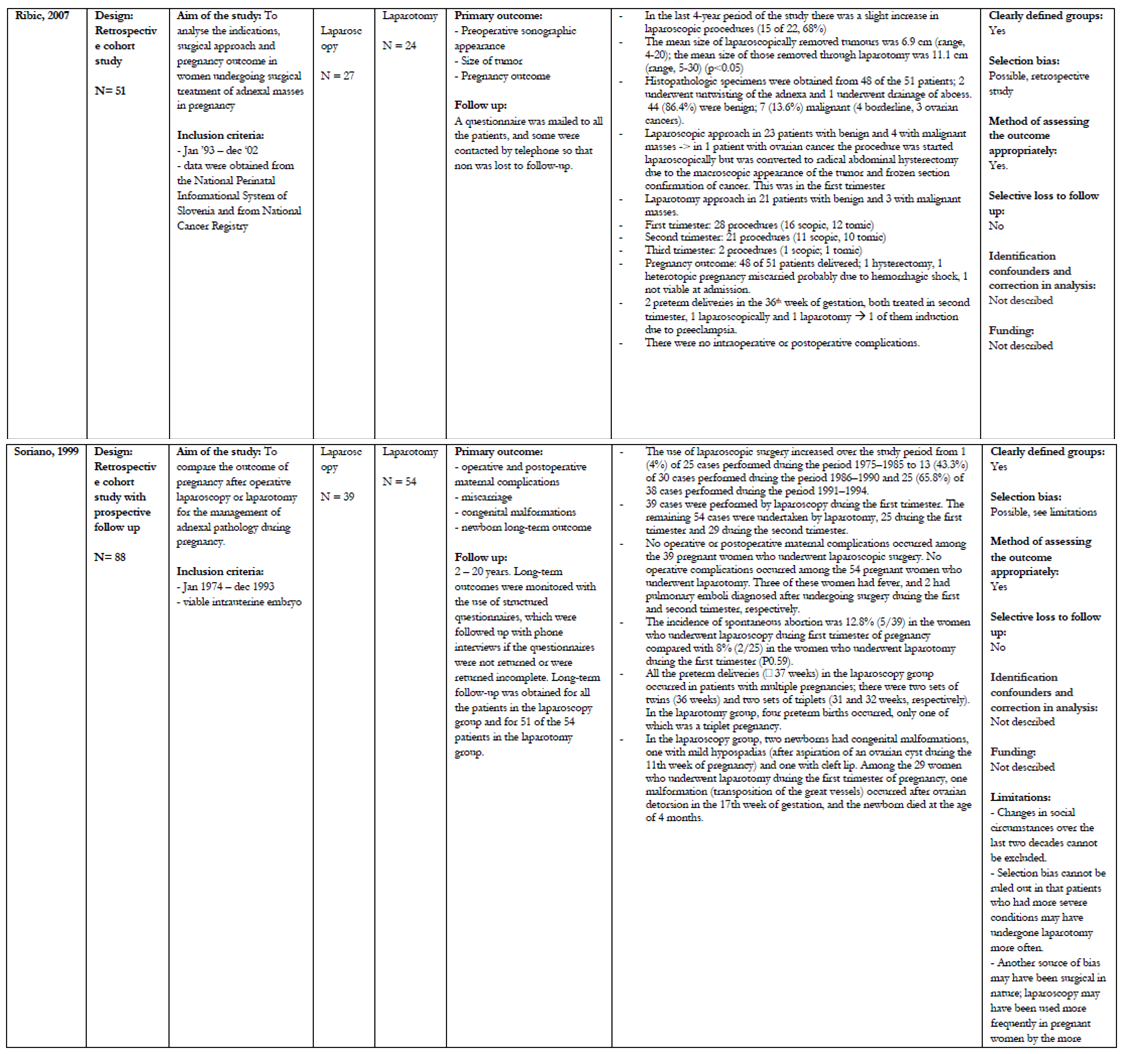
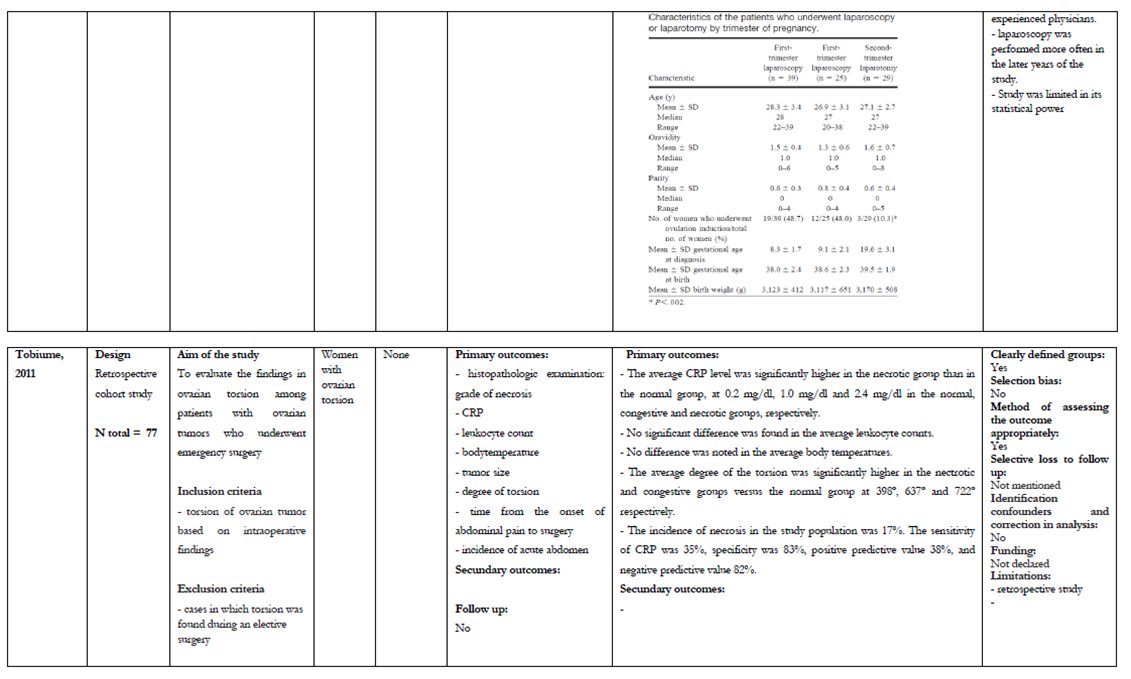
In zes retrospectieve onderzoeken (Akira, 1999; Balthazar, 2011; Carter, 2004; Lee, 2010; Ribic, 2007; Soriano, 1999) heeft men laparoscopie vergeleken met laparotomie bij een vergroot adnex in de zwangerschap. Hierbij moet wel opgemerkt worden dat in de meeste onderzoeken het percentage laparoscopieën sterk toenam aan het einde van het onderzoek.
Er zijn geen RCT’s die laparoscopie en laparotomie met elkaar vergelijken bij de behandeling van een vergroot adnex in de zwangerschap. De zes geselecteerde onderzoeken zijn retrospectieve cohortstudies/caseseries met een matige tot lage kwaliteit. Er is een Cochrane review (Bunyavejchevin, 2006) verschenen, maar hierbij zijn geen analyses gedaan aangezien er geen RCT’s zijn gepubliceerd over dit onderwerp.
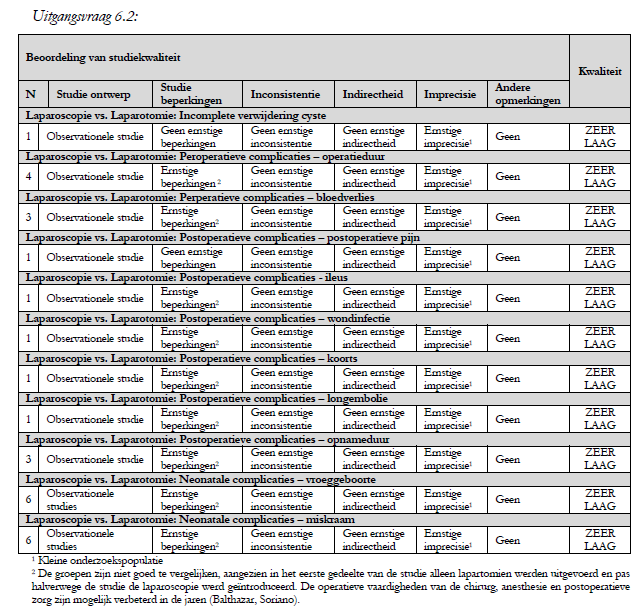
Incomplete verwijdering van de cyste
In Akira’s retrospectieve cohort zijn alle cysten in de laparoscopie groep (n=17) compleet verwijderd. Hiervan wordt geen melding gemaakt in de laparotomie groep. Er zijn verder geen onderzoeken gevonden die incomplete verwijdering van een adnexcyste als uitkomstmaat hebben meegenomen in de vergelijking laparoscopie en laparotomie.
Peroperatieve complicaties
In de vergelijkende onderzoeken laparoscopie en laparotomie in verband met adnexcyste in de zwangerschap worden peroperatieve spill, cysteruptuur, darm- en ureterletsels niet meegenomen als uitkomstmaten.
Er zijn drie onderzoeken die kijken naar de hoeveelheid bloedverlies (Balathazar, 2011; Carter, 2004; Lee, 2010) en vier naar de operatieduur (Akira, 1999; Balathazar, 2011; Carter, 2004; Lee, 2010), zie tabel 6.1.
Tabel 6.1: peri- en postoperatieve complicaties bij laparoscopie en laparotomie in verband met een adnexcyste in de zwangerschap
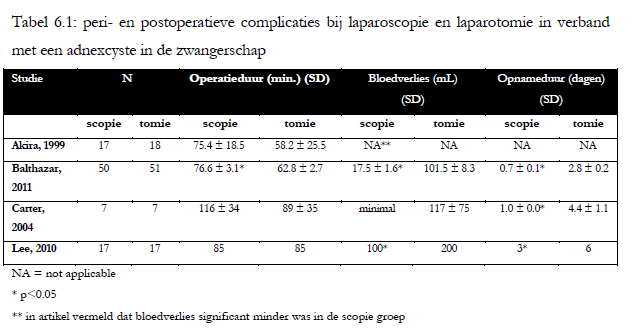
Conversie
Conversie van laparoscopie naar laparotomie werd in meerdere onderzoeken genoemd. In het cohort van Balthazar gebeurde dit in drie van de 50 laparoscopieën bij een zwangerschapsduur van 17 weken. Bij Ribic was er van 27 laparoscopieën één conversie naar een laparotomie, waarbij in verband met een maligniteit ook een hysterectomie is verricht. In de andere onderzoeken was geen sprake van peroperatieve complicaties.
Postoperatieve complicaties
Uit het onderzoek van Akira (n=35) bleek dat de intensiteit van postoperatieve pijn, gemeten met VAS-score, significant lager was in de laparoscopie groep.
In het cohort van Balthazar (n=101) zijn acht postoperatieve complicaties gemeld, alle in de laparotomie groep (p<0.02). Er was zeven keer sprake van een ileus en eenmaal van een wondinfectie.
Van de 54 vrouwen die in het cohort van Soriano een laparotomie ondergingen, kregen er drie postoperatief koorts en twee een longembolie, tegenover geen complicaties in de laparoscopie groep. In de andere onderzoeken was geen sprake van postoperatieve complicaties.
Wat betreft opnameduur zijn er drie onderzoeken die dit vermelden (Balthazar, 2001; Carter, 2004; Lee, 2010).
Neonatale complicaties
De incidentie van miskramen en vroeggeboorten wordt in alle zes de onderzoeken genoemd. In het onderzoek van Akira waarin 35 vrouwen zijn geïncludeerd vonden alle ingrepen tussen een amenorroeduur van 12 en 16 weken plaats. Er was sprake van 1 miskraam in de laparotomie groep (N=18); deze werd vastgesteld binnen één week na de ingreep. Er waren geen neonatale complicaties in de laparoscopie groep.
In het onderzoek van Lee (vergelijking 24 tomische adnexoperaties met 29 scopische adnexoperaties bij een gemiddelde zwangerschapsduur van 13 weken) komt in beide groepen één vroeggeboorte voor, verder waren er geen neonatale complicaties.
In het (retrospectieve) cohortonderzoek van Balthazar werden 101 vrouwen met een vergroot adnex geïncludeerd. Zij ondergingen een laparoscopie (n=50) danwel laparotomie (n=51) tussen de 14 en 24 weken amenorroeduur. In beide groepen zijn drie vrouwen voor de 36 weken bevallen, deze bevallingen konden niet direct in verband worden gebracht met de ingreep.
In het (retrospectieve) cohortonderzoek van Carter (n=16) ondergingen zeven vrouwen een laparoscopie en negen een laparotomie in de eerste twee trimesters van de zwangerschap. In dit onderzoek wordt melding gemaakt van één miskraam in de laparotomie groep, deze vond kort na de ingreep plaats. In de laparoscopie groep was één vroeggeboorte bij een zwangerschapsduur van 34 weken. In de laparotomie groep lag dit aantal op drie, bij een zwangerschapsduur van respectievelijk 31, 33 en 35 weken.
In een (retrospectief) cohort van Ribic van 51 vrouwen met een vergroot adnex zijn 27 laparoscopisch en 24 laparotomisch geopereerd. Er vonden 28 procedures in het 1e trimster plaats, 21 in het 2e trimster en twee in het 3e trimester. Laparoscopie en -tomie waren gelijk verdeeld over de trimesters. Van deze 51 vrouwen zijn er uiteindelijk 48 bevallen. Eén patiënt onderging een hysterectomie vanwege maligniteit en er was twee maal sprake van een miskraam, waarvan één waarschijnlijk ten gevolg van een hemorragische shock en één missed abortion vastgesteld bij opname. In welke groep de miskramen plaatsvonden, staat niet vermeld in het artikel. In beide groepen was één vroeggeboorte in de 36e week, ingrepen vonden plaats in het 2e trimster.
Tot slot zijn in het retrospectieve cohortonderzoek van Soriano 88 vrouwen geïncludeerd. Er zijn 39 laparoscopieën en 54 laparotomieën verricht. Alle laparoscopieën en 25 laparotomieën vonden plaats in het eerste trimester en 29 laparotomieën in het tweede. De incidentie van miskramen in het 1e trimster lag in de laparoscopie groep op 12.8 % (5/39), terwijl dit in de laparotomie groep 8% (2/25) was. De zeven miskramen vonden plaats in de groep van 50 vrouwen met een torsie bij een gehyperstimuleerd ovarium. Alle vier de vroeggeboortes in de laparoscopie groep waren het gevolg van een meerlingzwangerschap. Ook waren er vier vroeggeboortes in de laparotomie groep; hierbij was sprake van één meerlingzwangerschap. Geen van de vroeggeboortes werd in verband gebracht met de ingreep.
- Akira S., Yamanaka A., Ishihara T., Takeshita T., Araki T. Gasless laparoscopic ovarian cystectomy during pregnancy: comparison with laparotomy. American Journal of Obstetrics & Gynecology 1999; Mar;180(3:Pt 1):t-7.
- Balci O., Gezginc K., Karatayli R., Acar A., Celik C., Colakoglu M.C. Management and outcomes of adnexal masses during pregnancy: a 6-year experience. Journal of Obstetrics & Gynaecology Research 2008; Aug;34(4):524-8.
- Balthazar U., Steiner A.Z., Boggess J.F., Gehrig P.A. Management of a persistent adnexal mass in pregnancy: what is the ideal surgical approach? J Minimally Invasive Gynecol 2011; Nov;18(6):720-5.
- Bernhard L.M., Klebba P.K., Gray D.L., Mutch D.G. Predictors of persistence of adnexal masses in pregnancy. Obstetrics & Gynecology 1999; Apr;93(4):585-9.
- Bunyavejchevin S., Phupong V. Laparoscopic surgery for presumed benign ovarian tumor during pregnancy. [Review] [26 refs]. Cochrane Database Syst Rev 2006;(4):CD005459.
- Carter J.F., Soper D.E. Operative laparoscopy in pregnancy. Journal of the Society of laparoendoscopic Surgeons 2004;8(1):57-60.
- Caspi B., Levi R., Appelman Z., Rabinerson D., Goldman G., Hagay Z. Conservative management of ovarian cystic teratoma during pregnancy and labor. American Journal of Obstetrics & Gynecology 2000; Mar;182(3):503-5.
- Condous G., Khalid A., Okaro E., Bourne T. Should we be examining the ovaries in pregnancy? Prevalence and natural history of adnexal pathology detected at first-trimester sonography. Ultrasound in Obstetrics & Gynecology 2004; Jul;24(1):62-6.
- George K., Khong T.Y. Peripartum ovarian masses. Journal of Obstetrics & Gynaecology 1997; Nov;17(6):531-4.
- Katz L., Levy A., Wiznitzer A., Sheiner E. Pregnancy outcome of patients with teratoom and other benign ovarian cysts. Archives of Gynecology & Obstetrics 2010; May;281(5):811-5.
- Ko M.L., Lai T.H., Chen S.C. Laparoscopic management of complicated adnexal masses in the first trimester of pregnancy. Fertility & Sterility 2009; Jul;92(1):283-7.
- Koo Y.J., Kim T.J., Lee J.E., Kwon Y.S., Kim H.J., Lee I.H., et al. Risk of torsion and malignancy by adnexal mass size in pregnant women. Acta Obstet Gynecol Scand 2011; Apr;90(4):358-61.
- Koo Y.J., Lee .JE., Lim K.T., Shim J.U., Mok J.E., Kim T.J. A 10-year experience of laparoscopic surgery for adnexal masses during pregnancy. International Journal of Gynaecology & Obstetrics 2011; Apr;113(1):36-9.
- Kumai I., Kaur S., Mohan H., Huria A. Adnexal masses in pregnancy: A 5-year review. Aust New Zealand J Obstet Gynaecol 2006;46(1):52-4.
- Lee Y.Y., Kim T.J., Choi C.H., Lee J.W., Kim B.G., Bae D.S. Factors influencing the choice of laparoscopy or laparotomy in pregnant women with presumptive benign ovarian tumors. International Journal of Gynecology and Obstetrics 108 (2010;) 1215
- Mathevet P., Nessah K., Dargent D., Mellier G. Laparoscopic management of adnexal masses in pregnancy: a case series. European Journal of Obstetrics, Gynecology, & Reproductive Biology 2003; Jun 10;108(2):217-22.
- Moore R.D., Smith W.G. Laparoscopic management of adnexal masses in pregnant women. Journal of Reproductive Medicine 1999; Feb;44(2):97-100.
- Nahar S., Begum T., Naher L., Siddique T., Rani C., Raihan-Ul-Kabir M. Surgical management and outcome of adnexal masses during pregnancy: A 2 year retrospective study. Bangladesh J Obstet Gynecol 2008;23(2):51-5.
- Platek D.N., Henderson C.E., Goldberg G.L. The management of a persistent adnexal mass in pregnancy. American Journal of Obstetrics & Gynecology 1995; Oct;173(4):1236-40.
- Ramli R., Ghazali H.W., Omar M.J., Zainudin A.M. Laparoscopic cystectomy in pregnancy: An 8 year series. Int Med J 2009;16(4):279-82.
- Ribic-Pucelj M., Kobal B., Peternelj-Marinsek S. Surgical treatment of adnexal masses in pregnancy: indications, surgical approach and pregnancy outcome. Journal of Reproductive Medicine 2007; Apr;52(4):273-9.
- Schmeler K.M., Mayo-Smith W.W., Peipert J.F., Weitzen S., Manuel M.D., Gordinier M.E. Adnexal masses in pregnancy: surgery compared with observation. Obstetrics & Gynecology 2005; May;105(5:Pt 1):t-103.
- Soriano D., Yefet Y., Seidman D.S., Goldenberg M., Mashiach S., Oelsner G. Laparoscopy versus laparotomy in the management of adnexal masses during pregnancy. Fertility & Sterility 1999; May;71(5):955-60.
- Thornton J.G., Wells M. Ovarian cysts in pregnancy: does ultrasound make traditional management inappropriate? Obstetrics & Gynecology 1987; May;69(5):717-21.
- Turkcuoglu I., Meydanli M.M., Engin-Ustun Y., Ustun Y., Kafkasli A. Evaluation of histopathological features and pregnancy outcomes of pregnancy associated adnexal masses. Journal of Obstetrics & Gynaecology 2009; Feb;29(2):107-9.
- Usui R., Minakami H., Kosuge S., Iwasaki R., Ohwada M., Sato I. A retrospective survey of clinical, pathologic, and prognostic features of adnexal masses operated on during pregnancy. Journal of Obstetrics & Gynaecology Research 2000; Apr;26(2):89-93.
- Van De Velde M., De Buck F. Anesthesia for non-obstetric surgery in the pregnant patient. Minerva Anestesiol. 2007; Apr;73(4):235-40.
- Yen C.H., Lin S.K., Murk W., Wang C.J., Lee C.L., Soong Y.K., Phil M., Arici A. Risk analysis of torsion and malignancy for adnexal masses during pregnancy. Fertility and Sterility 2009; May;91(5):1895-1902
- Zanetta G., Mariani E., Lissoni A., Ceruti P., Trio D., Strobelt N., Mariani S. A prospective study of the role of ultrasound in the management of adnexal masses in pregnancy. BJOG 2003; June;110:578-583.
Beoordelingsdatum en geldigheid
Publicatiedatum : 11-03-2021
Beoordeeld op geldigheid : 11-03-2021
Bij het opstellen van de module heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodule komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
De richtlijnmodule is goedgekeurd door:
- Stichting Bekkenbodem4All
Doel en doelgroep
Doel
Het doel is om gynaecologen te voorzien van een landelijk gedragen richtlijn voor het voorkomen en het behandelen van vrouwen met een (benigne) vergroot ovarium en die voldoet aan de eisen van een AGREE-instrument volgens de EBRO-methode. De te ontwikkelen richtlijn voorziet in de meest recente 'evidence based' informatie over het onderwerp (benigne) vergroot ovarium.
Met het opstellen van een dergelijke richtlijn wordt beoogd de onduidelijkheid en onzekerheid over het diagnosticeren en behandelen van een (benigne) ovariumcyste weg te nemen.
Doelgroep
Patiëntencategorie
De richtlijn geldt voor alle pre- en postmenopauzale vrouwen met een vergroot ovarium (vanaf de menarche), bij wie niet eerder een maligniteit (mamma, ovarium, GE) werd vastgesteld.
Richtlijngebruikers
Deze richtlijn is geschreven voor alle leden van de beroepsgroep van gynaecologen. Daarnaast kan deze richtlijn ingezien en gebruikt worden door alle zorgverleners die te maken krijgen met vrouwen met een vergroot ovarium.
Samenstelling werkgroep
Samenstelling werkgroep update 2018
- Dr. P.M.A.J. Geomini, gynaecoloog, werkzaam in het Máxima Medisch Centrum te Eindhoven, NVOG, voorzitter richtlijncommissie
- Dr. D. van den Broek, klinisch chemicus, werkzaam bij het NKI te Amsterdam, NVKC
- Dr. J. Kaijser, gynaecoloog, werkzaam bij het Ikazia ziekenhuis te Rotterdam, NVOG
- Dr. A.J. Krüse, gynaecoloog, werkzaam bij Isala te Zwolle, NVOG
- Dr. C.A.R. Lok, gynaecoloog, werkzaam bij het NKI te Amsterdam, NVOG
- Dr. A. Stiekema, AIOS gynaecologie, werkzaam bij het Academisch Medisch Centrum te Amsterdam, NVOG
- M. Bosch, belangenbehartiging en PR Stichting Bekkenbodem4All, Stichting Bekkenbodem4All
Met ondersteuning van
- dr. E.J.M. den Breejen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. A. Bijlsma-Rutte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. W.J. Harmsen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
Oude samenstelling werkgroep
- Mw. dr. P.M.A.J. Geomini, gynaecoloog, Maxima Medisch Centrum, Veldhoven (voorzitter)
- Dhr. prof. dr. H.A.M. Brölmann, gynaecoloog, VU Medisch Centrum, Amsterdam
- Dhr. dr. F.P.H.L.J. Dijkhuizen, gynaecoloog, ziekenhuis Rijnstate, Arnhem
- Dhr. dr. T. Van Gorp, gynaecologisch oncoloog, Maastricht Universitair Medisch Centrum, Maastricht
- Mw. dr. C.A.R. Lok, gynaecologisch oncoloog, Centrum Gynaecologische Oncologie, Amsterdam
- Mw. drs. B.M. Pijlman, gynaecoloog, Jeroen Bosch Ziekenhuis, Den Bosch
- Mw. Dr. F. Vernooij, AIOS Obstetrie & Gynaecologie, epidemioloog, Meander Medisch Centrum, Amersfoort
- Mw. dr. Y.M. de Mooij, AIOS, VU Medisch Centrum, Amsterdam
- Ir. T.A. van Barneveld, klinisch epidemioloog, Orde van Medisch Specialisten, Utrecht
- Dhr. drs. K.Y. Heida, richtlijnondersteuner Nederlandse Vereniging voor Obstetrie en Gynaecologie, Utrecht
- Mw. drs. M.E.P.F. Rückert, richtlijnondersteuner Nederlandse Vereniging voor Obstetrie en Gynaecologie, Utrecht
- Mw. drs. C.A.L. van Rijn, richtlijnondersteuner Nederlandse Vereniging voor Obstetrie en Gynaecologie, Utrecht
Extern advies
- Mw. drs. M. Wessels, informatiespecialist, Orde van Medisch Specialisten, Utrecht
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Belangenverklaringen werkgroep update 2018
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Geomini* |
Gynaecoloog |
Geen |
mede organisator van Nederlandse IOTA cursus (gericht op implementeren IOTA regels voor echo beschrijving bij vergroot adnex) 1e auteur review: Geomini et al. The accuracy of risk scores in predicting ovarian malignancy: a systematic review. Obstet Gynecol. 2009 Feb;113:384-94. |
Geen |
|
Kruse |
Gynaecoloog-oncoloog, Isala, Zwolle |
Geen |
Geen |
Geen |
|
Kaijser |
gynaecoloog Ikazia Ziekenhuis Rotterdam |
Cursusinstructeur: echografie van het vergrote ovarium: Nederlandse IOTA cursus. Specialistische echocursus voor afwijkingen in de adnexiele regio. Jaarlijkse eendaags cursus voor gynaecologen en AIOS mede georganiseerd door Biomedic-Samsung, Nederland. Locatie Almere. Medio Juni 2019 zal dit voor de 4e maal plaatsvinden. Sprekersvergoeding à 500 euro. |
Klinisch werkzaam met Samsun WS80 echotoestel met geïntegreerd IOTA ADNEX model voor differentiatie van adnextumoren. Toestel wordt door Ikazia Ziekenhuis via officieel huurcontract afgenomen bij Biomedic Samsung, Nederland |
Geen trekker (1e auteur) bij module over diagnostische modellen (UV4) |
|
Lok |
Gynaecologisch-oncoloog Antoni van Leeuwenhoek - Nederlands Kanker Instituut |
Geen betaalde nevenfuncties Begeleiding van promovendi |
2 jaar geleden (kleine) subsidie (4x5000 euro) van Fujirebio gehad om een onderzoeker parttime HE4 te laten onderzoeken. Geen voorwaarden aan subsidie verbonden. Ging louter om het gebruiken van hun apparatuur voor analyse van samples. Huidig onderzoek wordt niet gefinancierd door Fujirebio.
Heeft eerder ook subsidies ontvangen voor onderzoek, waarbij de subsidies altijd aan het instituut werden uitbetaald om een onderzoeker van de betalen. Geen persoonlijk financieel gewin. Ging louter om het gebruik van technologieën van de betreffende industrie, geen voorwaarden verbonden aan de publicaties. Heeft zowel positieve als negatieve bevindingen over gepubliceerd.
Huidig onderzoek dat raakvlakken met de richtlijn heeft: onderzoek naar RMI en IOTA en het meten van markers, waarmee de selectie van patiënten zou kunnen worden verbeterd. Geen sponsoring van de industrie voor deze studie.
Heb wel over HE4 gepubliceerd, maar ook over CA-125 en RMI. Betreft louter wetenschappelijke publicaties van trial resultaten etc. Geen opiniestukken. Deze publicaties werden niet gesponsord door de industrie. Hier hangt m.i. geen intellectueel belang aan vast omdat zowel de voor- als nadelen van bv HE4 gewoon zijn gepubliceerd. |
Geen trekker (1e auteur) bij module over tumormarkers (UV3). |
|
Broek |
Klinisch chemicus/afdelingshoofd Algemeen klinisch laboratorium (fulltime) Antoni van Leeuwenhoek, Amsterdam |
Vakdeskundige Raad van Accreditatie ten behoeve van IS015189 (Detachering vanuit AVL, betaald) Lid commissie slimme en snelle diagnostiek (onbetaald) Lid flexpool ZonMW call vroege opsporing (vergoeding aan AVL, nu geen deelname aan ronde) Lid METC (onbetaald) Voorzitter instituut review board (onbetaald) Lid commissie moleculaire biologische diagnostiek NVKC (onbetaald) Voor alle werkzaamheden waar een vergoeding tegenover staat komt deze ten goede aan de werkgever. |
Geen Ik ben betrokken bij onderzoek dat wordt gefinancierd door fondsen en/of industrie, echter de onderwerpen van deze studies richten zich op moleculaire analyses in bloed of andere lichaamsvloeistoffen. Er zijn geen projecten die aan het onderwerp van deze richtlijn raken. |
Geen |
|
Bosch |
Vice Voorzitter en PR Stichting Bekkenbodem4All |
Geen |
Wij behartigen belangen van patiënten en geven voorlichting en ondersteuning aan mannen, vrouwen en kinderen met bekkenbodemproblemen in de breedste zin van het woord, zonder eigen belang of financieel belang. |
Geen |
|
Stiekema |
AIOS Gynaecologie, Amsterdam UMC locatie AMC Meibergdreef |
Geen |
Afgerond promotieonderzoek februari 2016 naar de rol van biomarker van HE4 bij onder andere het vergrote ovarium. Financiering voor dit onderzoek voor een heel klein deel (kits om laboratorium bepalingen uit te voeren) via Fujirebio. Deze contacten zijn na 2016 beëindigd. |
Geen trekker (1e auteur) bij module over tumormarkers (UV3). |
*voorzitter richtlijncommissie
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de patiëntenvereniging Stichting Bekkenbodem4All in de werkgroep deel te laten nemen. De modules worden tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en aan de Stichting Bekkenbodem4All.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden in de bijlagen. Er werden geen indicatoren ontwikkeld bij deze modules.
Werkwijze
AGREE
Deze module is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based module tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit de inventarisatie van de knelpunten door werkgroep bleek dat er een noodzaak was voor revisie en updaten van verschillende richtlijnmodules uit de richtlijn het Vergrote Ovarium (2013). Tijdens deze inventarisatie zijn er knelpunten aangedragen door relevante partijen via een schriftelijke Invitational conference. Een verslag hiervan is opgenomen in de bijlagen.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroepleden en de adviseur uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet kritiek) en onbelangrijk. Indien mogelijk definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad ‘Zoekverantwoording’ voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration:
- AMSTAR - voor systematische reviews.
- Cochrane - voor gerandomiseerd gecontroleerd onderzoek.
- ACROBAT-NRS - voor observationeel onderzoek.
- QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de module is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld bij deze modules.
Kennislacunes
Tijdens de ontwikkeling van deze module is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de bijlage Kennislacunes.
Commentaar- en autorisatiefase
De module worden aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve module werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Hultcrantz M, Rind D, Akl EA, et al. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Onderwerp: |
Database |
Zoekstrategie |
Aantal |
|
5.6.1 Is het beter een benigne ovariumcyste/-tumor chirurgisch te verwijderen dan om het in situ te laten in de zwangerschap ?
|
Medline (OVID), 1980-april 2012 Engels,
Nederlands Embase (Elsevier) Cochrane (Wiley) |
Zoekstrategie zie vraag 5.1 AND zoektermen voor zwangerschap Medline: 13 exp Pregnancy/ (659260) 14 pregnan*.ti,ab. (328026) 15 13 or 14 (724538) 1278 referenties (1276 uniek) Embase: ('pregnancy'/exp/mj OR pregnan*:ab,ti) 703 referenties (493 uniek) Cochrane: #11 MeSH descriptor Pregnancy explode all trees #12 (pregnan*):ti,ab,kw 182 referenties, 154 uniek |
1923
|
|
5.6.2 Welke benadering is beter voor de behandeling van een benigne vergroot ovarium tijdens de zwangerschap, laparoscopisch of laparotomisch?
|
Medline (OVID), 1980-april 2012 Engels, Nederlands
Embase (Elsevier)
Cochrane (Wiley)
|
Zoekstrategie zie vraag 5.3 AND zoektermen voor zwangerschap
Medline: 13 exp Pregnancy/ (659260) 14 pregnan*.ti,ab. (328026) 15 13 or 14 (724538) 371 uniek Embase: ('pregnancy'/exp/mj OR pregnan*:ab,ti) 201 uniek Cochrane: #11 MeSH descriptor Pregnancy explode all trees #12 (pregnan*):ti,ab,kw 34 uniek |
606
|

