Risicogedrag
Uitgangsvraag
Beïnvloeden van het risicogedrag in het revalidatieprogramma
Aanbeveling
De commissie is van mening dat alle patiënten en hun eventuele partnersvoorlichting dienen te krijgen over gewenste voedingsgewoonten en leefstijlaspecten (niveau C; klasse IIb).
De commissie adviseert om patiënten die hun voedingsgewoonten en leef-stijl daadwerkelijk willen veranderen te ondersteunen. Bijvoorbeeld door het aanbieden van of verwijzen naar groepsprogramma’s gericht op gedragsverandering (niveau C; klasse IIb).
Overwegingen
Er zijn bij deze uitgangsvraag geen overwegingen geformuleerd.
Onderbouwing
Conclusies
|
Beïnvloeden van risicogedrag |
• Het is aangetoond dat een roker met een coronaire hartziekte zijn kans op een (nieuwe) cardiale gebeurtenis kan verminderen door alsnog met roken te stoppen. (Niveau A; klasse I).
• Het is aangetoond dat coronaire hartpatiënten die deelnemen aan een fysiek trainingsprogramma en daarna een lichamelijk actieve leefstijl onderhouden, hun overlijdensrisico verlagen. (Niveau A; klasse I)
• Het is aannemelijk dat matig alcoholgebruik bij patiënten met coronair vaatlijden de kans op nieuwe vasculaire gebeurtenissen en op overlijden verlaagt. (Niveau B; klasse IIa)
• Het is aangetoond dat voedingsinterventies verschillende risicofactoren voor hart- en vaatziekten gunstig kunnen beïnvloeden en het risico van ziekte en sterfte voor coronaire hartpatiënten kunnen beperken. (Niveau A; klasse I) |
Samenvatting literatuur
De doelen gericht op risicoreductie door het aanleren van een gezonde leefstijl zijn: bekendheid met de aard van de ziekte en de risicofactoren (11), stoppen met roken (12), ontwikkelen en onderhouden van een lichamelijk actieve leefstijl (13), ontwikkelen van een gezond voedingspatroon (14) en ontwikkelen van therapietrouw aan medicatie (15) (zie voor de genoemde doelen tabel D in Inleiding Revalidatie). Leefstijlfactoren zoals lichamelijke inactiviteit, ongezonde voedingsgewoonten en rookgedrag behoren tot de risicofactoren waarop invloed kan worden uitgeoefend door het aanpassen van de leefstijl. Daarnaast zijn er risicofactoren waarop geen invloed kan worden uitgeoefend, zoals leeftijd, geslacht en voorgeschiedenis. Zie voor een overzicht tabel E hieronder.
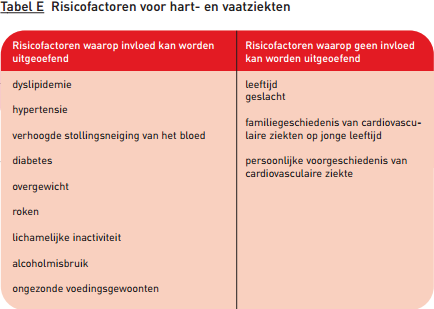
Om doelgericht de individuele kans op (nieuwe) cardiovasculaire gebeurtenissen te verlagen, moeten de risicofactoren waarop invloed kan worden uitgeoefend per patiënt in kaart worden gebracht. Patiënten met manifeste vaatziekten hebben bij dezelfde waarde van de risicofactoren een veel hogere kans op een nieuwe cardiovasculaire gebeurtenis dan mensen die geen symptomen van vaatziekten hebben. Hun risico om binnen 10 jaar een nieuw cardiovasculair incident mee te maken varieert – afhankelijk van de bijkomende risicofactoren – van circa 25% (Goldberg 1998, LIPID Study Group 1998) tot 60% of hoger (Haffner1999). De impact van risicoreductie is in deze patiëntengroep daarom veel groter dan in de algemene populatie.
Risicoreductie kan bereikt worden door het veranderen van de leefstijl en door medicatie om het lipidenprofiel te verbeteren, de bloeddruk te verlagen, de diabetes te reguleren en/of de trombogene factoren profylactisch te beïnvloeden. Op het gebied van risicoreductie valt er in Nederland nog een aanzienlijke gezondheidswinst te behalen: een half jaar na de behandeling voor een hartziekte rookt 28% van de patiënten nog steeds, heeft 79% overgewicht (Body Mass Index (BMI) >25 kg/m2), is 28% obees (BMI >30 kg/m2), heeft 54% een bloeddruk boven de 140/90 mm Hg en 44% een serumcholesterolspiegel hoger dan 5 mmol/l (EuroaspireII 2001). Zie voor de medicamenteuze risicoreductie en profylaxe de nationale richtlijnen (CBO-consensus cholesterol en hypertensie) en de richtlijnen op internationaal niveau (Wood 1998, National Cholesterol Education Program 2001). Internationaal bestaat er consensus over de volgende leefstijlaanbevelingen voor de preventie van hart- en vaatziekten (Wood 1998, Kromhout 2002):
- Rook niet
- Zorg voor voldoende lichaamsbeweging
- Als je alcohol gebruikt, doe het met mate
- Zorg voor een gezond gewicht
- Beperk het gebruik van verzadigd vet en transvet
- Eet minimaal 1 keer per week en bij voorkeur 2 keer per week (vette) vis
- Eet voldoende groente en fruit
- Beperk het gebruik van zout
Bij de wetenschappelijke onderbouwing van leefstijlinterventies draait het om de vraag of de gewenste gedragsveranderingen leiden tot een vermindering van het risico op nieuwe cardiovasculaire gebeurtenissen en overlijden. In de module Interventies wordt besproken wat de kenmerken zijn van effectieve interventies gericht op de beïnvloeding van risicogedrag.
Roken
De relatie tussen roken en het optreden van hart- en vaataandoeningen is consistent, biologisch plausibel, onafhankelijk van andere factoren en dosisafhankelijk (wat wil zeggen dat de kans op ziekte stijgt met het toenemen van het aantal gerookte sigaretten) (USDHHS 1990, Menotti 2001).
Een roker met een hart- of vaatziekte kan het risico van toekomstige complicaties met ongeveer de helft (Wilhelmsson1975) verminderen door alsnog met roken te stoppen (Sparrow1978, Salonen 1980, Sato 1992, Voors 1996, Van Berkel 1999). Een recente meta-analyse laat zien dat het relatieve risico voor totale sterfte voor de groep patiënten die stopt, daalt met ruim 35% (95% betrouwbaarheidinterval: 29-42%) (Critchley2003).
De manier waarop roken hart- en vaatziekten veroorzaakt, is nog niet volledig opgehelderd: zowel trombogene Bottcher1999 als atherogene Pech-Amsellem 1996, Powell 1998 factoren lijken een rol te spelen. Omdat het effect van stoppen met roken bij patiënten met manifeste hart- en vaatziekten al na enkele maanden optreedt, lijken de trombogene factoren de hoofdrol te spelen. Prescott 1998 Uit de EUROASPIRE-II-studie blijkt dat een half jaar na hun ziekenhuisopname 28% van de Nederlandse patiënten met coronaire hartziekten nog rookt. Dat is hoger dan het Europese gemiddelde van 21% (EuroaspireII 2001).
Lichamelijke activiteit
Epidemiologische studies tonen aan dat een lichamelijk inactieve leefstijl zowel de totale als de cardiovasculaire mortaliteit verhoogt (Berlin 1990). Naast het risico van hart- en vaatziekten verlaagt meer lichaamsbeweging ook de kans op andere chronische ziekten zoals diabetes, obesitas, osteoporose en sommige vormen van kanker (USDHHS 1990). Voor patiënten met coronaire hartziekten is het beschermende effect van meer lichaamsbeweging aangetoond in experimentele studies met bewegingsprogramma’s (Thompson 2003). Een recente meta-analyse toonde aan dat de mortaliteit voor degenen die na hun myocardinfarct een fysiek trainingsprogramma volgden en daarna een actieve leefstijl onderhielden, met 30% verminderde (Jolliffe2001).
De beschermende werking van lichaamsbeweging kan enerzijds toegeschreven worden aan het verbeteren van het risicoprofiel, waardoor de ontwikkeling van plaques vertraagt en het risico op trombose vermindert. Anderzijds is ook een rol weggelegd voor directe effecten, zoals een intensievere doorbloeding van de coronaria, een verbeterde metabole capaciteit en een verlaagde kans op ventrikelfibrilleren (Reincke2001).
Omdat bij meer dan de helft van de bevolking het niveau van lichamelijke activiteit te laag is, werd in 1998 de Nederlandse Norm Gezond Bewegen (NNGB) opgesteld. Kemper 2000 In navolging van internationale richtlijnen (Pate1995, USDHHS 1990, Kemper 2000, Jolliffe 2001, Reincke 2001, Thompson 2003) krijgen volwassenen hierin het advies om minimaal 30 minuten per dag matig intensief te bewegen, op minstens vijf maar bij voorkeur zeven dagen per week.
Deze algemene aanbeveling geldt ook voor patiënten met cardiovasculaire ziekten en hartfalen (Thompson 2003). Afhankelijk van de individuele testuitslagen kunnen echter adviezen op maat worden verstrekt met betrekking tot de intensiteit, de duur en de frequentie van de inspanning (Fletcher 1996) (Zie ook module Fysieke doelen).
Matig intensieve activiteit wordt gedefinieerd als inspanning die de hartslag verhoogt tot 60% à 75% (De Backer 2003) van iemands maximale hartslag of de zuurstofconsumptie tot 40% à 60% van het persoonlijke maximum (VO2max) (Thompson 2003). De aanbevolen hoeveelheid matige inspanning komt overeen met een extra energieverbruik van circa 200 kcal per dag of 1000 kcal per week. Voorbeelden van matig inspannende activiteit voor mensen van 18 tot 55 jaar zijn wandelen met een snelheid van 5 à 6 km per uur of fietsen met een snelheid van 15 km per uur. Voor ouderen is wandelen met een snelheid van 3 à 4 km per uur of een fietstempo van 10 km per uur al genoeg (Kemper 2000).
De NNGB moet gezien worden als een ondergrens. Met meer inspanning kan meer gezondheidswinst behaald worden. Voor veel patiënten is het echter al winst als ze de ondergrens halen. De verwachting is dat zij deze voorzichtige aanbeveling eerder opvolgen dan hogere inspanningsdoelen.
De aanbevelingen van de NNGB zijn onvoldoende voor het verliezen van lichaamsgewicht en het bereiken van een optimaal inspanningsvermogen (McKechnie 2003). Verondersteld wordt dat dagelijks 45 tot 60 minuten matig intensieve activiteit nodig is om overgewicht of obesitas te voorkomen, en 60 tot 90 minuten om gewichtstoename in voorheen obese patiënten te voorkomen (Saris 2003). Voor een optimaal inspanningsvermogen is een wekelijkse hoeveelheid van 3 maal 20 minuten intensieve activiteit nodig (Kemper 2000).
De beweeggewoonten van Nederlandse patiënten met coronaire hartziekten zijn onderzocht door van Elderen en collega’s (van Elderen 2001). Zij vonden dat 3 en 12 maanden na een ziekenhuisopname voor een acute coronaire gebeurtenis respectievelijk 42% en 47% van de patiënten minder dan 3 keer per week 20 minuten actief was. De EUROASPIRE-II-studie laat zien dat Nederlandse patiënten minder vaak een advies over lichaamsbeweging krijgen (48%) dan gemiddeld in Europa (67%) (Euroaspire II 2001).
Alcoholgebruik
Het effect van alcohol op het cardiovasculaire risico is afhankelijk van de gebruikte hoeveelheid (Corrao2000). Mogelijk speelt ook het drinkpatroon (bijvoorbeeld bij de maaltijden of tussendoor, vooral in het weekend of gespreid over alle dagen van de week) een rol (Poikolainen1998).
Overmatig alcoholgebruik, dat wil zeggen een langdurig gebruik van meer dan 3 alcoholconsumpties per dag, wordt in verband gebracht met hypertensie Xin 2001, verhoogde cardiovasculaire risico’s Criqui1998 en een verhoogde incidentie van levercirrhose, ongevallen, haemorragische herseninfarcten, slokdarmkanker Cleophas1999 en mogelijk ook borstkanker Smith-Warner 1998 en darmkanker. Meyer 1993 Daartegenover staat dat gematigd alcoholgebruik het cardiovasculair risico vermindert. Dit wordt gedeeltelijk verklaard door het verhogende effect van alcohol op het HDL-cholesterol en een gunstig effect op de stollingsfactoren (Rimm1999).
Data over het effect van matig alcoholgebruik op de recidiefkans en sterfte bij patiënten die een myocardinfarct hebben gehad zijn niet consistent, maar wijzen in de richting van een beschermend effect (Thun1997, Muntwyler 1998, Shaper 2000, De Lorgeril 2002).
Met het oog op de preventie van hart- en vaatziekten en de algemene gezondheid wordt aanbevolen om het alcoholgebruik te beperken tot maximaal 3 consumpties per dag voor mannen (21 per week) en maximaal 2 per dag (14 per week) voor vrouwen (ScottishIntercollegiate Guidelines Network 2000). Van de volwassenen in Nederland is 38% van de mannen en 17% van de vrouwen een matige drinker (CBS 2003).
Voedingsgewoonten
Voeding beïnvloedt het risico van hart- en vaatziekten via meerdere factoren, zoals de hoogte van de verschillende lipidenfracties in het bloed, overgewicht, insulineresistentie, de oxidatie van het LDL-cholesterol, de bloeddruk, de homocysteïnespiegel en de trombogenese. Daarom is het zinnig een aantal voedingsrichtlijnen voor hartpatiënten aan te houden. Hieronder een overzicht.
Zorg voor evenwicht tussen energie-inname en energieverbruik
Patiënten met overgewicht of obesitas – vooral abdominale obesitas – hebben een verhoogde kans op hart- en vaatziekten (NHLBI 1998, Gezondheidsraad 2003). De prevalentie van overgewicht en obesitas is hoog onder patiënten met hart- en vaatziekten (respectievelijk 79% en 28%), terwijl in de huidige praktijk slechts een klein deel van deze patiënten (36%) van hun arts daadwerkelijk het advies krijgt om af te vallen (Euroaspire II 2001). Gewichtsvermindering zal onder meer leiden tot een daling van de bloeddruk (TOHP 1997, He 2000, Stevens 2001), verbetering van het lipidenprofiel (Datillo 1992) en daling van het bloedglucosegehalte (Van Gaal 1997). Vooral bij patiënten met het metabool syndroom of diabetes mellitus is gewichtsafname van belang voor het verminderen van de insulineresistentie en het verbeteren van het risicoprofiel (NCEP 2001).
Volgens internationale richtlijnen (NHLBI 1998, WHO 2000) dienen alle patiënten onder de 70 jaar met een BMI>30 kg/m2 en patiënten met een BMI>25 kg/m2 in combinatie met andere risicofactoren voor hart- en vaatziekten voor behandeling in aanmerking te komen. Voor personen boven de 70 jaar en voor niet-kaukasische bevolkingsgroepen gelden andere criteria (Gezondheidsraad 2003). De middelomtrek is een goede maat voor het vaststellen van abdominale obesitas (WHO 2000). Bij een buikomvang van 80 cm voor vrouwen en 94 cm voor mannen is er sprake van een verhoogde kans op metabole complicaties. Bij een buikomtrek van 88 cm voor vrouwen en 102 cm voor mannen is de kans op hart- en vaatziekten ernstig verhoogd en behandeling noodzakelijk.
Bij de behandeling dient gestreefd te worden naar een geleidelijk gewichtsverlies van 10% van het begingewicht in circa 6 maanden, gevolgd door een minder intensieve behandeling van twee jaar gericht op het stabiliseren van het bereikte lichaamsgewicht en het voedings- en bewegingspatroon (Gezondheidsraad 2003). Naast het behandelen van overgewicht en obesitas verdient ook het voorkómen van gewichtstoename aandacht.
Gebruik minder dan 10 energieprocenten verzadigd vet en minder dan 1 energieprocent transvet
Verzadigde vetten verhogen de kans op coronaire hartziekten door onder meer een ongunstig effect op de verhouding tussen totaal- en HDL-cholesterol (Mensink 1992) en de trombogenese (Agren1997). Het verminderen van de inname van verzadigd vet leidt tot een afname in cardiovasculaire gebeurtenissen en sterfte (Truswell1994, Hooper 2001). Het is een misverstand te denken dat beperking van de inname van verzadigd vet alleen zinvol is bij een serumcholesterolspiegel van 5 mmol/l of meer. Ook bij lagere spiegels kan risicoreductie worden bereikt (Law2002). Vergeleken met het effect van statines (25% risicoreductie) is het effect van een verminderde inname van verzadigd vet op het LDL-cholesterol niet groot (10%). Beide effecten zijn echter wel additief (Law1994, Tang 1998).
De belangrijkste bronnen van verzadigd vet zijn roomboter, sommige margarines, vet vlees en vette vleeswaren, volvette kaas en volle melkproducten, koffiecreamer, snacks, gebak en koekjes. De gemiddelde inname van verzadigd vet is in Nederland gedaald van 16 naar 14 energieprocent (Voedingscentrum 1998). Aanbevolen wordt een inname van maximaal 10 energieprocenten.
Naast een beperking van de inname van verzadigd vet wordt ook een beperking van de transvetten geadviseerd. De transvetten verhogen het LDL-cholesterol, verlagen het HDL-cholesterol, verhogen de concentraties van lipoproteïne Lp(a) in nuchter bloed en zijn geassocieerd met een hogere incidentie van en sterfte aan coronaire hartziekten (Zock1998). Transvetten komen van nature in kleine hoeveelheden voor in melk en vlees van herkauwers. Ze ontstaan tijdens industriële processen door hydrogenatie van onverzadigde vetten. De belangrijkste bronnen zijn vetgrondstoffen voor bakkerijproducten (bijvoorbeeld koek en gebak) en horecaproducten (zoals frites). Door het aanpassen van de productieprocessen van margarines is de gemiddelde inname in Nederland de afgelopen 10 jaar gedaald van 5 naar 2 energieprocent. Aanbevolen wordt om de inname te beperken tot minder dan 1 energieprocent (Health Council of the Netherlands 2003). Om een nog grotere daling te bereiken, zijn vooral inspanningen van industrie en horeca vereist.
Ook het beperken van het cholesterolgehalte in de voeding (tot <33 mg/1000 kJ of <139 mg/1000 kcal) is nog actueel, omdat dit bijdraagt aan het verlagen van het LDL-cholesterol in serum (Clarke1997). In de voorlichting wordt hierop echter minder nadruk gelegd. Dit omdat de gemiddelde inname in Nederland met 22,6 mg per 1000 kJ ruim onder de aanbeveling ligt, en omdat men aanneemt dat een beperking van de inname van verzadigd vet automatisch leidt tot een lagere inname van cholesterol.
Het is ook mogelijk het serum-LDL-cholesterol te verlagen door het gebruik van margarines of andere producten verrijkt met stanolesters of plantenstanolen. Deze stoffen remmen de cholesterolresorptie in het maagdarmkanaal. Uit onderzoek blijkt dat deze stoffen het LDL-cholesterol met circa 10% kunnen verlagen (Law2000), maar dat ze niet werkzaam zijn bij gebruik van een vetarm dieet (Denke 1995, Van Heyningen 1999).
In de huidige voorlichting maakt men geen onderscheid tussen enkelvoudig en meervoudig onverzadigde vetten. Nieuwe onderzoeksresultaten tonen aan dat de effecten van enkelvoudig onverzadigde vetten op het lipidenprofiel nauwelijks verschillen van meervoudig onverzadigde vetten (Truswell1994).
Eet minstens 1 tot 2 maal per week (vette) vis (of plantaardige bronnen van n-3 vetzuren)
Een veelbelovende voedingsinterventie bij hartpatiënten lijkt een verhoging van de consumptie van de zogenaamde n-3 vetzuren uit vis of plantaardige bronnen. Een recente meta-analyse (Bucher2002) schatte dat interventies met n-3 vetzuren het percentage niet-fatale myocardinfarcten kan verminderen met 20, de cardiale sterfte met 30 en de acute hartsterfte met 30. Dit effect wordt niet verklaard door veranderingen in de klassieke risicofactoren. De n-3 vetzuren beïnvloeden het serumtriglyceridegehalte en hebben mogelijk anti-aritmische effecten. De aanbevolen hoeveelheid voor n-3 vetzuren uit vis is in Nederland 200 mg per dag. Afhankelijk van de soort vis komt dit overeen met een wekelijkse visconsumptie van 70 tot 280 gram per week (Gezondheidsraad 2003). De gemiddelde consumptie ligt in Nederland veel lager (Voedingscentrum 1998). Gegeven de positieve onderzoeksresultaten bij post-myocardinfarctpatiënten zijn er redenen om aan hartpatiënten te adviseren om de inname van n-3 vetzuren uit vis te verhogen (echter niet boven de 1000 mg per dag) en te streven naar 2 porties vette vis per week (Kris-Etherton 2002). Voorbeelden van vette vis zijn: zalm, heilbot, sprot, makreel en bokking. Omdat voor sommige patiënten het eenmaal per week eten van vis al een hele stap is, is het belangrijk te benadrukken dat zelfs bij een bescheiden visconsumptie al aanzienlijke risicoreducties zijn gevonden (Zock 2002). Voor wie echt niet van vis houdt, kan alfalinoleenzuur, een n-3 vetzuur uit plantaardige bron, een oplossing zijn. Hierover zijn echter veel minder onderzoeksresultaten beschikbaar dan over de n-3 vetzuren uit vis (De Lorgeril 1994, Singh 1997, Hu 1999). De omzetting van n-3 vetzuren uit plantaardige bron verloopt zeer inefficiënt. Mogelijk heeft alfalinoleenzuur een beschermend effect onafhankelijk van deze omzetting (Lemaitre 2003). De aanbevolen hoeveelheid voor alfalinoleenzuur is in Nederland 1 energieprocent (dit komt overeen met 2 gram alfalinoleenzuur per dag). De inname ligt waarschijnlijk rond de 0,5 energieprocent (Voskuil 1996, Bemelmans 2002). De inname kan verhoogd worden door te kiezen voor alfalinoleenzuurrijke oliën en margarines, volkorenproducten, noten, zaden en (groene) groente.
Eet per dag minstens 200 gram groente en 2 porties fruit
Het advies om per dag 200 gram groente en 2 porties fruit te eten is gebaseerd op de resultaten van cohortstudies waarin beschermende effecten van groenteen fruitconsumptie op cardiovasculaire ziekte en sterfte zijn aangetoond (Ness 1997, Law 1999, Joshipura 2001, Bazzano 2002).
Interventiestudies waarin de inname van groente en fruit werd verhoogd, laten effecten zien op onder meer de bloeddruk (Appel 1997, Sacks 2001, Appel 2003), de antioxidantcapaciteit van het serum (Miller 1998) en het serumhomocysteïnegehalte (Appel 2000). Uit studies bij patiënten die een myocardinfarct hadden gehad, blijkt dat een voedingsregime waarin onder meer de groente- en fruitconsumptie was verhoogd, leidt tot een aanzienlijke afname van de recidiefkans en de sterfte (Singh1992, De Lorgeril 1999).
Het beschermende effect kan gedeeltelijk verklaard worden door bekende voedingsstoffen uit groente en fruit, zoals kalium (He 2001), antioxidanten, foliumzuur (Law1999) en vezels (Truswell1999), maar mogelijk spelen ook minder bekende (KrisEtherton2002) en nog onbekende bioactieve stoffen een rol.
Door het verhogen van de huidige gemiddelde inname in Nederland van 250 gram naar de gewenste 400 gram kan de cardiovasculaire sterfte met 16% verminderen (Van ’t Veer 2000).
Ook tussen de inname van volkoren graanproducten en het optreden van hart- en vaatziekten is in cohortstudies een verband gevonden (Rimm1996, Mozaffarian 2003). Een positief effect op het cardiovasculaire risico is (nog) niet bevestigd in experimenteel onderzoek bij patiënten met hart- en vaatziekten (Burr1989, Truswell 2002).
Beperk het zoutgebruik
Er bestaat een sterk verband tussen bloeddruk en cardiovasculair risico. Al vanaf een bloeddruk van 115/75 mm Hg verdubbelt het risico met elke stijging van 20 mm Hg van de systolische bloeddruk. Leefstijladviezen ter verlaging van de bloeddruk moeten daarom worden aanbevolen zodra de systolische bloeddruk boven de 120 mm Hg komt (prehypertensie) (Chobanian2003). Een beperking van de zoutinname is een van deze leefstijladviezen (Midgley 1996).
Verschillende meta-analyses tonen aan dat het mogelijk is om door zoutbeperking de bloeddruk te laten dalen (Midgley1996, Cutler 1997, Graudal 1998). De schatting van het te verwachten effect op de systolische bloeddruk van natriumbeperking is kleiner (2-8 mm Hg) dan het effect van bijvoorbeeld gewichtsvermindering (5-20 mm Hg/10 kg), een dieet rijk aan groente en fruit en magere melkproducten (8-14 mm Hg) of meer lichaamsbeweging (4-9 mm Hg) (Chobanian2003). De grootte van het gecombineerde effect van de verschillende leefstijladviezen is vergelijkbaar met dat van medicamenteuze therapie en bovendien additief daaraan. Of het ook mogelijk is om door zoutbeperking de cardiovasculaire morbiditeit of mortaliteit te verlagen, is nog onduidelijk. In internationale richtlijnen wordt aanbevolen om met het oog op de cardiovasculaire gezondheid de zoutinname te beperken tot 5 gram (2000 mg natrium) WHO 2003 of 6 gram (2400 mg natrium) (Chobanian 2003).
De gemiddelde zoutinname van de Nederlandse bevolking is 9 gram keukenzout (3700 mg natrium). De Nederlandse Voedingsnormen geven geen aanbeveling voor maximale zoutinname. Voor individuen met een verhoogde bloeddruk wordt in Nederland een beperking van 2400 mg natrium aangehouden (NVD 2003). De natriuminname kan beperkt worden door geen zout toe te voegen bij het bereiden van maaltijden en beperkt gebruik te maken van industrieel bereide producten die veel zout bevatten, zoals soepen, sauzen, hartige snacks, kaas, vleeswaren en kant-en-klaarmaaltijden.
Samenvattend kunnen we stellen dat bovenstaande voedings- en leefstijladviezen belangrijk zijn voor alle coronaire hartpatiënten, ongeacht de hoogte van hun individuele risicofactoren (Truswell1994). Stoppen met roken heeft het grootste effect op het individuele cardiovasculaire risico. Daarna mag men het meest verwachten van een combinatie van interventies gericht op het veranderen in de voedingsgewoonten en leefstijl (Barzi 2003, Kromhout 2003). Grootschalige studies bij coronaire hartpatiënten naar effecten van gecombineerde voedings- en leefstijlinterventies op morbiditeit en mortaliteit zijn niet beschikbaar. Kleinschalige studies bij hartpatiënten (Ornish 1998) of andere hoog-risicogroepen (Hjermann1981) laten hoopvolle resultaten zien.
Goede voeding en leefstijlveranderingen
Informatie in groepsverband over goede voeding hoort, evenals fysieke trainingen, van oudsher tot de standaardinterventies van een poliklinisch hartrevalidatieprogramma. Naast voedingsvoorlichting maakt ook voorlichting over andere leefstijlfactoren zoals roken, beperkt alcoholgebruik en meer bewegen deel uit van het informatieprogramma (Nederlandse Hartstichting 2002). Dit informatieprogramma is bestemd voor alle patiënten en hun partners. Vaak is het geven van voorlichting echter onvoldoende om blijvende veranderingen in voedings- en leefstijlgewoonten te bewerkstelligen. Daarom maken ook individuele interventies, zoals een individueel behandeltraject bij de diëtist en leefstijlprogramma’s waarin (onder meer) gewerkt wordt aan gewichtsmanagement, deel uit van het hartrevalidatieprogramma. Deze programmaonderdelen onderscheiden zich van het informatieprogramma doordat ze gericht zijn op patiënten die al een bewuste keus gemaakt hebben om hun risico te verminderen door gedragsverandering. De organisatie van individuele interventies en leefstijlprogramma’s in groepsverband kan per centrum sterk verschillen. Het is mogelijk groepsgericht te werken aan één leefstijldoel (bijvoorbeeld stoppen met roken), maar ook zijn er gecombineerde programma's in gebruik waarbij de deelnemers elkaar tot steun zijn terwijl ze aan verschillende doelen werken. Wanneer leefstijlprogramma’s niet door de eigen instelling worden georganiseerd, kan er gebruik worden gemaakt van bijvoorbeeld cursussen voor stoppen met roken en gewichtsmanagementprogramma's van andere instanties en instellingen.
Voor voedings- en leefstijladviezen komen in aanmerking alle patiënten die risicogedrag vertonen. Verandering van gedrag kan aanzienlijke gezondheidswinst opleveren (Hauner1990, Chauhan 1994, Ley 1994, National Heart and Lung and Blood Institute 1998). De intensievere (groeps)interventies gericht op het veranderen van gedrag worden doorgaans gereserveerd voor patiënten voor wie het moeilijk is zonder begeleiding de gestelde doelen te bereiken. De indicatie voor voedingsen leefstijladviezen en intensievere gedragsinterventies is niet afhankelijk van de hoogte van de individuele risicofactoren (zie module Hulpmiddelen indicatiestelling: Intakegesprek) (Law 2002).
Therapietrouw aan medicamenten
Het is moeilijk om betrouwbare en exacte cijfers te krijgen over therapietrouw. Bij het gebruik van antihypertensiva en cholesterolverlagers ligt de therapietrouw respectievelijk rond de 60 en 80%. In het eerste jaar van behandeling staken tussen de 16 en 50% van de patiënten hun behandeling. Het niet trouw innemen van bètablokkers verviervoudigt de relatieve kans op chronische hartziekten.
Interventietechnieken, zoals regelmatige telefonische controles, kunnen de therapietrouw verbeteren met 18% (Burke 1997). Depressieve symptomen verminderen de therapietrouw (zie module Psychische doelen (slechtere cardiovasculaire prognose).
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 01-01-2011
Laatst geautoriseerd : 01-01-2011
Geplande herbeoordeling :
In oktober 2000 vroeg de Commissie Kwaliteit van de NVVC de revalidatiecommissie om de Richtlijnen Hartrevalidatie 1995/1996 te actualiseren. Immers, ervaring met hartrevalidatie en wetenschappelijk onderzoek hebben inmiddels geleid tot nieuwe inzichten. Uit het wetenschappelijk onderzoek blijkt dat ook patiënten met hartfalen, aangeboren hartafwijkingen en ritmestoornissen in aanmerking kunnen komen voor hartrevalidatie. Hetzelfde geldt voor patiënten die een harttransplantatie hebben ondergaan. De groep patiënten voor wie hartrevalidatie is bestemd, is daarmee vergroot. Ook de wetenschappelijke kennis over het belang van een gezonde leefstijl is toegenomen. Het veranderen van de leefstijl kan indien gecombineerd met medicamenteuze behandeling het atherosclerotische proces vertragen of zelfs terugdringen. Daarmee vermindert de kans op nieuwe vasculaire gebeurtenissen.
Begin 2008 initieerde de NVVC een subsidieaanvraag bij het Kennisbeleid Kwaliteit Curatieve Zorg (KKCZ)-programma van ZonMW om de Richtlijn Hartrevalidatie 2004 te herzien met betrekking tot psychische en sociale doelen. De richtlijn uit 2004 bood onvoldoende houvast om het verhoogde niveau van psychische symptomen, die voorkomen bij driekwart van de patiënten die voor hartrevalidatie in aanmerking komen, effectief te behandelen. Bovendien is de wetenschappelijke kennis over dergelijke psychische symptomen na een cardiaal incident en over de behandeling daarvan enorm toegenomen. Daarnaast waren er inmiddels richtlijnen met betrekking tot hartpatiënten voor bedrijfsartsen en voor verzekeringsartsen en was de wens ontstaan om de richtlijn voor de tweedelijns gezondheidszorg beter te laten aansluiten op deze nieuwe richtlijnen. Ook was er behoefte aan meer houvast met betrekking tot het bereiken van werkhervatting. Bij de herziening, die in oktober 2008 in het project Psychische en Arbeidsgerelateerde Aspecten van HartRevalidatie (PAAHR) van start ging, is besloten om de richtlijn niet alleen te herzien met betrekking tot werkhervatting maar ook met betrekking tot sociale steun. Uit de wetenschappelijke literatuur komt namelijk naar voren dat patiënten met weinig sociale steun een hogere cardiale morbiditeit en mortaliteit, een hogere kans op depressie en een lagere kwaliteit van leven hebben.
Algemene gegevens
De herzieningen uit 2011 zijn geautoriseerd / geaccepteerd door:
- De Hart&Vaatgroep
- NVHVV
- NVVA
Doel en doelgroep
Doel
De Richtlijn Hartrevalidatie is in 1996 voor het eerst verschenen. In 2004 werd het nut ervan als volgt omschreven:
Richtlijnen leveren op drie niveaus een belangrijke bijdrage aan het verbeteren van de zorg voor hartpatiënten:
- Ze bieden een onderbouwing van het nut van hartrevalidatie.
- Ze leiden tot standaardisatie van de zorg bij hartrevalidatie, naast een op het individu toegesneden aanpak.
- Ze benadrukken het belang van een multidisciplinaire aanpak voor hartrevalidatie, waarbij hartrevalidatie zich niet beperkt tot training, maar ook psychische counseling en secundaire preventie omvat.
Er is inmiddels overtuigend bewijs voor de positieve effecten van hartrevalidatie in termen van verminderde morbiditeit, mortaliteit, verbeterde kwaliteit van leven en kosteneffectiviteit. Ades 1997, Oldridge 1997, Lowensteyn 2000, Papdakis 2005, Lee 2007, Piepoli 2010 Richtlijnen bevorderen de implementatie van hartrevalidatie.
Recent heeft de Cardiac Rehabilitation Section van de European Association of Cardiovascular Prevention and Rehabilitationeen position paperopgesteld waarin zij praktische aanbevelingen geeft met betrekking tot de kerncomponenten van hartrevalidatie Piepoli 2010. De huidige richtlijn sluit aan bij deze aanbevelingen, maar is gebaseerd op nieuwe literatuurstudies.
Doelgroep
Het proces van hartrevalidatie is een bij uitstek multidisciplinaire aangelegenheid. Bij de hartrevalidatie zijn vele zorgverlenende deskundigen betrokken, zoals cardiologen, revalidatieartsen, huisartsen, bedrijfsartsen, inspanningsfysiologen, verpleegkundigen, diëtisten, psychologen, maatschappelijk werkers, fysiotherapeuten, bewegingsagogen, ergotherapeuten, psychiaters, verzekeringsartsen en arbeidsdeskundigen. Alle betrokkenen kunnen gebruik maken van deze richtlijn. Ook patiëntenverenigingen kunnen baat hebben bij de informatie in deze richtlijn, hoewel voor patiënten een specifieke patiëntenrichtlijn ontwikkeld zal worden (zie www.hartenvaatgroep.nl).
Samenstelling werkgroep
Auteurs herziening 2011 met betrekking tot psychische en sociale doelen (naast oorspronkelijke auteurs richtlijn 2004)
- Inleiding: Richtlijn 2004: drs. P.J. Senden; herziening 2011: mw. dr. A.E. de Rijk
- Kosteneffectiviteit herziening 2011: drs. A.M.W. van Stipdonk, mw. dr. S. Evers
- Doorverwijzing naar de cardioloog: Richtlijn 2004: dr. J. Brügemann, drs. H.J. van Exel; herziening 2011: drs. A.M.W. van Stipdonk, mw. dr. P.M.J.C. Kuijpers, mw. dr. A.E. de Rijk, prof. dr. A. Gorgels en projectgroep PAAHR
- Revalidatie op maat (de doelen): Richtlijn 2004: mw. dr. M. Chatrou, mw. J.A. Lestra, drs. M.W.A. Jongert,dhr. H. Koers, dhr. S. van der Voort; herziening 2011: mw. dr. A.E. de Rijk, drs. A.M.W. van Stipdonk en projectgroep PAAHR
- Revalidatie op maat (hulpmiddelen indicatiestelling): Richtlijn 2004: mw. dr. M. Chatrou, mw. prof. dr. Th. van Elderen, mw. J.A.Lestra, drs. M.W.A. Jongert, dhr. H. Koers, mw. drs. A.M. Strijbis, dhr. S. van der Voort; herziening 2011: mw. dr. A.E. de Rijk, drs. A.M.W. van Stipdonk, mw. dr. P.M.J.C. Kuijpers en projectgroep PAAHR
- Interventies: Richtlijn 2004: mw. dr. M. Chatrou, drs. J.L. van Dijk, dr. J.J. van Dixhoorn,mw. J.A. Lestra, dhr. H. Koers, drs. M.W.A. Jongert, dhr. S. van der Voort; herziening 2011: drs. A.M.W. van Stipdonk, mw. dr. A.E. de Rijk, mw. dr. P.M.J.C. Kuijpers, projectgroep PAAHR (par. 5.3); mw. dr. A.E. de Rijk, drs. A.M.W. van Stipdonk, mw. dr. P.M.J.C. Kuijpers, drs. J. van Dijk en overige leden projectgroep PAAHR (par. 5.4)
- Hartfalen: Richtlijn 2004: drs. P.J. Senden
- Bijzondere diagnosegroepen: Richtlijn 2004: dr. J. Brügemann; herziening 2011: drs. A.M.W. van Stipdonk,mw. dr. P.M.J.C. Kuijpers, prof. dr. A. Gorgels, mw. dr. A.E. de Rijk en projectgroep PAAHR
- Klinische hartrevalidatie: Richtlijn 2004: dr. J. Brügemann, drs. M.H. Oosterwijk
- Overgang naar nazorg: (in 2011 toegevoegd) mw. dr. A.E. de Rijk, drs. A.M.W. van Stipdonk, mw. dr.P.M.J.C. Kuijpers, mw. dr. M. Bouma en projectgroep PAAHR
- Implementatie: (in 2011 toegevoegd) mw. dr. A.E. de Rijk
Werkgroep PAAHR (Psychische en Arbeidsgerelateerde Aspecten van
HartRevalidatie) ten behoeve van de herziening 2011 met betrekking tot psychische en sociale doelen
- dhr. H. Koers, fysiotherapeut, KNGF-VHVL, Amersfoort (lid PAAHR vanaf 2008)
- drs. A.M.T.M. Derks, revalidatiearts, VRA, Utrecht (lid PAAHR vanaf 2008)
- dhr. dr. C.H.Z. Kuiper, lector participatie, ergotherapeut, Ergotherapie Nederland, Utrecht(lid PAAHR vanaf 2008)
- mw. drs. I. van den Broek, adviseur belangenbehartiging, De Hart&Vaatgroep,Soesterberg (lid PAAHR vanaf 2008)
- dhr. mr. J.A.M. Wijnekus, arbeidsdeskundige NVAA, Nijkerk (lid PAAHR vanaf 2008)
- mw. drs. G. Casteelen, psychiater, NVVP, Utrecht (lid PAAHR vanaf 2009)
- dhr. dr. R.A. Kraaijenhagen, cardioloog, NVVC, Utrecht (lid PAAHR vanaf 2008)
- mw. drs. E.H.N. Stoffers, adviseur, Huis voor de zorg, Sittard (lid PAAHR vanaf 2008)
- dhr. dr. P.R.J. Falger, GZ-psycholoog, Maastricht University, Maastricht (lid PAAHR vanaf2008)
- mw. ir. K.T. Idema, adviseur belangenbehartiging, De Hart&Vaatgroep, Soesterberg (lidPAAHR vanaf 2008 tot 2009)
- mw. E.R. Geleijnse, maatschappelijk werker Capri Hartrevalidatie Rotterdam, NVMW/LOMH, Utrecht (lid PAAHR vanaf 2008)
- mw. C.E. Muller-Grijzenhout, verpleegkundig coördinator hartrevalidatie, Sint FranciscusGasthuis, Rotterdam (lid PAAHR vanaf 2009)
- mw. J.J. Doornenbal, gedifferentieërd hart- en vaatverpleegkundige en verpleegkundig coördinator hartrevalidatie, Academisch Medisch Centrum, Amsterdam (lid PAAHR vanaf 2009)
Namens de revalidatiecommissie (richtlijn 2004):
- drs. P.J. Senden, cardioloog, Meander Medisch Centrum, Amersfoort (voorzitter revalidatiecommissie vanaf 1997)
- mw. drs. A.M. Strijbis, secretaris, Nederlandse Hartstichting, Den Haag (lid revalidatiecommissie vanaf 1998)
Werkgroep bijzondere diagnosegroepen (richtlijn 2004)
- dr. J. Brügemann, cardioloog, Academisch Ziekenhuis Groningen, Groningen (lid revalidatiecommissie vanaf 1997)
- drs. H.J. van Exel, cardioloog, Rijnlands Revalidatiecentrum, Leiden (lid revalidatiecommissie vanaf 2001)
- mw. E. Schück, verpleegkundige, Isala Klinieken locatie Weezenlanden, Zwolle (lid revalidatiecommissie van 1999 t/m 2002)
- Adviseurprof. dr. W.A. Helbing, kindercardioloog, Erasmus Medisch Centrum/ Sophia Kinderziekenhuis, Rotterdam
Werkgroep psychosociale ondersteuning en secundaire preventie (richtlijn 2004)
- drs. E.L.D. Angenot, revalidatiearts, Revalidatiecentrum Amsterdam, Amsterdam (lidrevalidatiecommissie van 1996 t/m 2002)
- mw. dr. M. Chatrou, psycholoog, Máxima Medisch Centrum, Eindhoven (lid revalidatiecommissie vanaf 2001)
- drs. J.L. van Dijk, bedrijfsarts, Achmea-Arbo, Amsterdam (lid revalidatiecommissie vanaf2001)
- mw. E.R. Geleijnse, maatschappelijk werkster, Rotterdamse Stichting voorCardiologische Revalidatie (lid revalidatiecommissie van 1994 t/m 2002)
- mw. dr. I.M. Hellemans, cardioloog, Alant Cardio, (lid revalidatiecommissie vanaf 1997)
- drs. J.A.M. Hoevenaar, huisarts, Elsendorp (lid revalidatiecommissie vanaf 2001)
- mw. J.A. Iestra, diëtist, Universitair Medisch Centrum, Utrecht (lid revalidatiecommissievanaf 1999)
- drs. H.C.A.M. Kruijssen, cardioloog, Academisch Ziekenhuis Rotterdam, Rotterdam (lidrevalidatiecommissie vanaf 1984)
- drs. E.C. de Melker, cardioloog, Sint Lucas Andreas ziekenhuis, Amsterdam (lid revalidatiecommissie vanaf 2001)
- mw. P.M. Muns, maatschappelijk werker, Universitair Medisch Centrum, Utrecht (lidrevalidatiecommissie vanaf 2003)
- Adviseurs
- mw. ir. S.J. van Dis, epidemioloog, Nederlandse Hartstichting, Den Haag drs. F. Duysens, psycholoog, Centrum voor Hart- en Longrevalidatie Rijnlands Revalidatiecentrum, Leiden
- mw. prof. dr. Th. van Elderen, psycholoog, Klinische en Gezondheidspsychologie, Universiteit Leiden (lid revalidatiecommissie van 1992 t/m 2000) mw. drs. I. Kersten, psycholoog, Sint Lucas Andreas Ziekenhuis, Amsterdam dhr. H. Koers, fysiotherapeut/ manueel therapeut, Groene Hart Ziekenhuis, Gouda (lid revalidatiecommissie van 1994 t/m 2000)
- mw. A.B. Nieuwveld, verpleegkundig consulent cardiologie, Isala Klinieken locatie Weezenlanden, Zwolle
Werkgroep lichamelijke activiteit en hartfalen (richtlijn 2004)
- drs. E.L.D. Angenot, revalidatiearts, Revalidatiecentrum Amsterdam (lid revalidatiecommissie van 1996 t/m 2002)
- dr. J. Brügemann, cardioloog, Academisch Ziekenhuis Groningen, Groningen (lid revalidatiecommissie vanaf 1997)
- drs. W.A.J. Bruggeling, cardioloog, Amphiaziekenhuis locatie Pasteurlaan, Oosterhout (lidrevalidatiecommissie vanaf 2001)
- drs. H.J. van Exel, cardioloog, Centrum voor Hart- en Longrevalidatie RijnlandsRevalidatiecentrum, Leiden (lid revalidatiecommissie vanaf 2001)
- drs. J.A.M. Hoevenaar, huisarts, Elsendorp (lid revalidatiecommissie vanaf 2001)
- drs. P.J. Senden, cardioloog, Meander Medisch Centrum, Amersfoort (voorzitter revalidatiecommissie vanaf 1997)
- drs. E.P. Viergever, cardioloog, Groene Hart Ziekenhuis, Gouda (lid revalidatiecommissievanaf 2001)
- dhr. S. van der Voort, fysiotherapeut, Hart-, Long-, Vaatrevalidatie Zonnestraal,Ziekenhuis Hilversum (lid revalidatiecommissie vanaf 2001)
- Adviseursmw. dr. H.J.G. van den Berg-Emons, bewegingswetenschapper, Erasmus Medisch Centrum, Rotterdam
- dr. J.J. van Dixhoorn, arts/ ontspanningstherapeut, Kennemer Gasthuis, locatie Deo, Haarlem
- drs. E. Hulzebos, fysiotherapeut/gezondheidswetenschapper, Universitair Medisch Centrum, Utrecht drs. M.W.A. Jongert, inspanningsfysioloog, TNO Preventie en Gezondheid, Leiden dhr. H. Koers, fysiotherapeut/ manueel therapeut, Gouda (lid revalidatiecommissie van
- 1994 t/m 2000) mw. P.M. Rijke-van Zeijl, diëtist, Leids Universitair Medisch Centrum mw. dr. M.L. Zonderland, medisch fysioloog, Universitair Medisch Centrum, Utrecht
Met dank voor hun deskundige advies (richtlijn 2004)
- drs. A.M.T.M. Derks, revalidatiearts, Stichting Revalidatie Limburg, RevalidatiecentrumHoensbroeck, Hoensbroek (lid revalidatiecommissie vanaf 2003)
- dr. J.W. Deckers, cardioloog, coördinator richtlijnen NVVC
- mw. dr. I.C. van Gelder, cardioloog, Academisch Ziekenhuis Groningen, Groningen
- drs. R. Goud, medisch informatiekundige, Academisch Medisch Centrum, Amsterdam
- prof. dr. D.E. Grobbee, klinisch epidemioloog, Julius Centrum voor Gezondheidsweten-schappen en Eerstelijns Geneeskunde, Universitair Medisch Centrum, Utrecht
- mw. C.J. Koppelaar, verpleegkundig onderzoeker, Erasmus Medisch Centrum,Rotterdam (lid revalidatiecommissie vanaf 2003)
- prof. dr. ir. D. Kromhout, directeur sector Voeding en Consumenten VeiligheidRijksinstituut voor Volksgezondheid en Milieu (RIVM), Bilthoven
- prof. dr. J. Perk, cardioloog, streekziekenhuis Oskarshamn, Zweden, lid van “3rd JointEuropean Societies Task Force on Preventive Cardiology”
- dr. A. Vermeulen, cardioloog, niet praktiserend (lid revalidatiecommissie vanaf 1984)
- mw. drs. M.H.L. van der Wal, verpleegkundige, onderzoeker COACH (lid revalidatiecommissie van 1995 t/m 1998)
Commentatoren herziening 2011
- drs. J. Brügemann, cardioloog, Thoraxcentrum / Cardiologie, Universitair MedischCentrum Groningen, Groningen
- drs. G.A.H.M Castermans, huisarts, vertegenwoordiger RHZ Hart en Vaatcentrum AZM,lid werkgroep Vasculair Risicomanagement, Stichting RHZ Heuvelland, Maastricht
- mw. Y.M.C.H. Curfs, ergotherapeut, Adelante zorggroep, Hoensbroek
- De Hart&Vaatgroep, Soesterberg
- Ergotherapie Nederland, Utrecht
- drs. A.H.M. van Erp, psycholoog en programmacoördinator ‘Hart voor Mensen’,Nederlandse Hartstichting, Den Haag
- drs. H.J. van Exel, cardioloog, centrum voor Hart- en Longrevalidatie, Rijnlands
- Revalidatie Centrum, Leiden (lid commissie Cardiovasculaire Preventie en Hartrevalidatie van de Nederlandse Vereniging voor Cardiologie)
- mw. dr. J. Fleer, psycholoog en onderzoeker, Universitair Medisch Centrum Groningen,afdeling Gezondheidswetenschappen, sectie Gezondheidspsychologie, Groningen
- mw. drs. M.M. van Engen-Verheul, gezondheidswetenschapper en promovenda, VakgroepKlinische Informatiekunde, Academisch Medische Centrum Amsterdam
- mw. dr. I.M. Hellemans, cardioloog (lid commissie Cardiovasculaire Preventie enHartrevalidatie van de Nederlandse Vereniging voor Cardiologie)
- Huis voor de Zorg, Sittard
- mw. dr. A. Huizing, gezondheidswetenschapper en cöordinator eerstelijnsketen DBC,stichting RHZ Heuvelland, Maastricht
- H.M.C. Kemps, cardioloog, Cardiologie, Maxima Medisch Centrum, Veldhoven (lid commissie Cardiovasculaire Preventie en Hartrevalidatie van de Nederlandse Vereniging voor Cardiologie)
- mw. drs. A.B.A. Klabbers, gezondheidswetenschapper en promovenda, vakgroep Sociale
- Geneeskunde / onderzoeksschool CAPHRI, Faculty of Health, Medicine & Life Sciences, Universiteit Maastricht, Maastricht
- mw. prof. mr. S. Klosse, jurist en hoogleraar Sociaal Recht, Faculteit der
- Rechtsgeleerdheid, Capaciteitsgroep Publiekrecht, Universiteit Maastricht, Maastricht
- Kwaliteitsbureau Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde, Utrecht
- prof. dr. C.M.J.G. Maes, psycholoog en hoogleraar Gezondheidspsychologie, InstituutPsychologie, Faculteit der Sociale wetenschappen, Universiteit Leiden
- Nederlands Huisarts Genootschap, Utrecht
- Nederlands Instituut van Psychologen, Amsterdam
- Nederlandse Vereniging van Revalidatie Artsen (VRA), Utrecht
- Nederlandse Vereniging voor Hart en Vaat Verpleegkundigen, Woerden
- dr. N.B. Peek, medisch informaticus en projectleider CARDSS, Vakgroep KlinischeInformatiekunde, Academisch Medische Centrum Amsterdam, Amsterdam
- drs. R.Y. Schouten, psycholoog en projectmanager ‘Hart voor Mensen’, NederlandseHartstichting, Den Haag
- prof. dr. A. Honig, psychiater, afdeling psychiatrie, Sint Lucas Andreas Ziekenhuis,Amsterdam
- prof. dr. P. de Jonge, vakgroep Medische psychologie en Neuropsychologie, Faculteit
- Sociale Wetenschappen, Tilburg University, Tilburg
- Nederlandse Vereniging van Maatschappelijk Werkers, Utrecht
- Nederlandse Vereniging voor Verzekeringsgeneeskunde, Utrecht
- Prof. dr. A.H. Schene, psychiater, afdeling Psychiatrie, Academisch Medisch CentrumAmsterdam
Met dank voor hun deelname aan interviews over hartrevalidatie (herziening 2011)
- Respondenten en hun partners die deelnamen aan de achterbanconsultatie in het kadervan PAAHR door de Hart&Vaatgroep
- Het hartrevalidatieteam van het Maastricht Universitair Medisch Centrum + (MUMC+)
Methode ontwikkeling
Evidence based
Implementatie
Ter bevordering van de implementatie van deze richtlijn, zijn de volgende implementatiehulpmiddelen ontwikkeld:
- Algoritmen, gebaseerd op algoritmen gepubliceerd bij de Europese richtlijn (aangepast na de update) (zie bijlagen “Flowchart”);
- Indicatoren (te vinden op de website van de NVU) (zie bijlage Indicatoren);
- Een vormgegeven samenvatting (aangepast na de update) (zie bijlage Samenvattingskaart);
- Een samenvatting voor patiënten (aangepast na de update) (zie bijlage Samenvatting voor Patiënten);
- Een artikel voor de Prostaatkankerstichting
Tevens is een artikel voor het Tijdschrift voor Urologie geschreven. Daarnaast adviseert de Werkgroep om lokale behandelprotocollen zoveel mogelijk te baseren op deze Richtlijn, rekening houdende met de lokale situatie.
Werkwijze
Wetenschappelijke onderbouwing
De conclusies en aanbevelingen in deze richtlijn zijn onderbouwd met wetenschappelijk onderzoek. Bij de herziening in 2004 heeft de revalidatiecommissie de onderzoeksresultaten gewogen en afhankelijk van de mate van bewijskracht is aan de conclusies en aanbevelingen een niveau van bewijskracht toegekend. Daarbij is een indeling in drie niveaus gehanteerd (A, B en C).
Daarnaast kan over een conclusie of aanbeveling meer of minder consensus bestaan over het nut/de effectiviteit van behandelen. Aan het niveau van bewijskracht is een indeling in twee klassen (I en II) toegevoegd over de mate van acceptatie van behandelen. Klasse II is onderverdeeld in a en b, hetgeen een extra aanduiding is voor de mate van acceptatie bij een verdeelde mening. Deze indeling in niveaus en klassen is in overeenstemming met de criteria van de European Society of Cardiology.
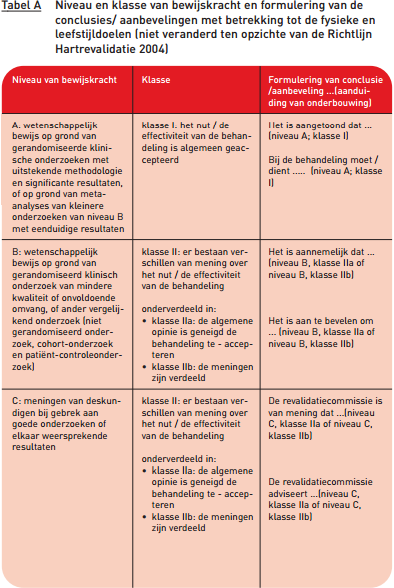

De formulering van de conclusies en aanbevelingen is aangepast aan het niveau van uit wetenschappelijk onderzoek verkregen bewijskracht (zie tabel A).
Voor de delen herzien in 2011 is uitgegaan van nieuwe standaarden voor richtlijnontwikkeling. CBO 2007 Eerst zijn knelpunten geformuleerd en geprioriteerd. Naar aanleiding daarvan zijn uitgangsvragen voor de literatuurstudies geformuleerd. In de literatuurstudies is de literatuur stapsgewijs geselecteerd (zie ‘Werkwijze project PAAHR’ op https://www.nvvc.nl/richtlijnen/bestaande-richtlijnen#risicomanagement). Aan de conclusies uit de wetenschappelijke literatuur is een niveau van bewijskracht toegekend, dat aangeeft hoe goed de conclusie door het wetenschappelijke onderzoek wordt onderbouwd. Als bijvoorbeeld de uitkomsten tegenstrijdig zijn, dan is een conclusie daaruit minder goed onderbouwd dan bij uitkomsten die overeenkomen. Hiertoe is eerst de methodologische kwaliteit van individuele kwantitatieve studies bepaald (A1, A2, B, C of D; waarbij A voor de hoogste kwaliteit staat en D voor de laagste kwaliteit) (zie bijlage Kwaliteitscriteria). Vervolgens zijn conclusies opgesteld op basis van meerdere studies en is daar een bepaald niveau van bewijskracht aan toegekend. Die niveaus van bewijskracht zijn weergegeven in tabel B. In vergelijking met de niveaus zoals gehanteerd in 2004, hebben de niveaus gehanteerd in 2011 dus alleen betrekking op de conclusies uit de literatuur en niet op de aanbevelingen die daaruit afgeleid zijn.
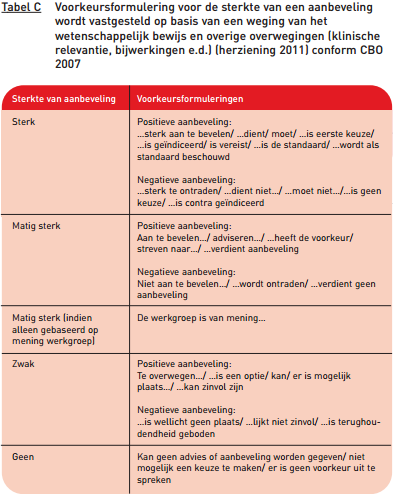
Aanbevelingen zijn gevormd op basis van 1) de conclusies uit de wetenschappelijke literatuur en 2) overige overwegingen van de projectgroep. Voorbeelden van overige overwegingen zijn: klinische relevantie, schade of bijwerkingen, de beschikbaarheid van voorzieningen, de kosten van zorg, de organisatie van zorg, patiëntenperspectief, professioneel perspectief, juridische aspecten, en ethische aspecten. De formulering van de aanbevelingen geeft de sterkte van de aanbeveling weer, dit is weergegeven in tabel C. CBO 2007
Kosteneffectiviteit hartrevalidatie
Al langere tijd is bekend dat de meeste economische evaluaties van hartrevalidatie laten zien dat hartrevalidatie een kosteneffectieve behandeling is. Oldridge 1998, Ades 2001, Piepoli 2010 In het kader van de vernieuwing van de richtlijn in
2011, is een literatuuronderzoek uitgevoerd naar de effecten van hartrevalidatie
en interventies met betrekking tot de psychische en sociale doelen in het bijzonder.
In totaal zijn 24 studies gevonden met betrekking tot kosteneffectiviteit van hartrevalidatie. Op basis van vijf systematische reviews Ades 1997, Oldridge 1997,
Lowensteyn 2000, Papdakis 2005, Lee 2007 en een meer recente studie Kruse 2006 van matige tot goede kwaliteit kan geconcludeerd worden dat zowel hartrevalidatie in multidisciplinaire vorm (met name secundaire preventie en bewegingsprogramma’s) als ook bewegingsprogramma’s kosteneffectief zijn voor patiënten met coronaire hartziekten. Dit wordt vooral verklaard door vermindering van het aantal cardiovasculaire opnames en een kortere opnameduur.
Er zitten echter beperkingen aan deze conclusie. De studies zijn erg divers met betrekking tot:
- onderzochte indicatoren voor kosteneffectiviteit (cardiovasculaire en andereheropnames; jaren tot overlijden; bezoek eerste hulp en polikliniek; behandelingen; functioneel herstel en kwaliteit van leven; stijging van levensverwachting in aantal jaren goede gezondheid (Quality Adjusted Life Years, QALYs))
- berekende kosten (directe, tijdgebonden kosten evaluatie van alle separatekostenposten, alleen kosten interventies en kosten specifieke uitkomstmaat).
Deze diversiteit vermindert de vergelijkbaarheid van de studies. Oldridge 1997, Papadakis 2005, Lee 2007 Voorts zijn in de bepaling van de kosteneffectiviteit maatschappelijke kosten (kosten door verminderde hervatting van betaald werk wanneer er geen revalidatie plaatsvond) niet meegenomen.
Voor de overige interventies en de meer uitgebreide multidisciplinaire interventies zijn onvoldoende kwalitatief goede studies gevonden om de kosteneffectiviteit goed te kunnen beoordelen. Begeleiding bij psychische symptomen en bij arbeidsre-integratie leiden tot matige kosteneffectiviteit, maar waarschijnlijk worden de effecten onderschat door een te korte follow-up en andere methodologische beperkingen Southard 2003, Yu 2004, Briffa 2005, Turner 2008
Hierover is wel meer bekend bij patiënten met hartfalen. Bij deze groep blijkt dat een uitgebreide multidisciplinaire aanpak met psychosociale begeleiding en ontslagbegeleiding kostenbesparend is, met name door vermindering van het aantal opnames, en verkorting van de opnameduur van nieuwe opnames. Rich 1995, Riegel 2000, O’Connell 2001, Kasper 2002, Capomolla 2002, Krumholz 2002, Turner 2008 Er zijn geen betrouwbare gegevens gevonden met betrekking tot patiënten die een omleidingsoperatie (Coronary Artery Bypass Grafting (CABG), ook wel genoemd: bypassoperatie) hebben ondergaan. Penque 1999 Bij de specifiekere groep van hartpatiënten met depressieve symptomen en/of angstsymptomen zijn er bemoedigende resultaten met betrekking tot kosteneffectiviteit van hartrevalidatie, zowel hartrevalidatie in het algemeen als hartrevalidatie met interventies specifiek gericht op deze symptomen. Oldridge 1993, O’Connor 2001, Lee 2007 Uit meerdere studies blijkt dat hartpatiënten (zowel patiënten met coronaire hartziekten als met hartfalen) met een hoog risico op complicaties (in termen van behandelingen en heropnames) meer baat hebben bij hartrevalidatie. Hierdoor is de kosteneffectiviteit bij hartpatiënten met een laag risico minder of niet kosteneffectief. Riegel 2000, O’Connell 2001, Hall 2002, Kaspar 2002 Dit onderstreept het belang van screening (zie ook Revalidatie op maat (hulpmiddelen indicatiestelling)).
Noord-Amerikaanse studies geven aanwijzingen voor de kosteneffectiviteit van poliklinische hartrevalidatie versus klinische hartrevalidatie Rich 1995, Robertson 2001, Naylor 2004, Lee 2007, Taylor 2007, Turner 2008. Hierbij moet opgemerkt worden dat de patiëntenpopulaties voor klinische hartrevalidatie verschillen van die in Nederland, waar klinische hartrevalidatie alleen voor complexe gevallen geïndiceerd is.
Concluderend zijn er voldoende aanwijzingen dat de in deze richtlijn beschreven hartrevalidatie kosteneffectief is, hoewel meer onderzoek wenselijk is.
Hoe is deze richtlijn opgebouwd?
Deze richtlijn volgt min of meer chronologisch het traject van zorg voor hartrevalidatie zoals dat grafisch is weergegeven in de figuurmodel voor Hartrevalidatie in de Inleiding.
De doorverwijzing door de cardioloog wordt in de module Doorverwijzing Cardioloog beschreven. Alle patiënten moeten door een cardioloog naar hartrevalidatie worden doorverwezen. In de module Doorverwijzing Cardioloog wordt beschreven welke patiënten voor hartrevalidatie in aanmerking komen.
Welke doelen kunnen worden vastgesteld bij een individuele patiënt, wordt in de module Revalidatie op maat (doelen) beschreven. Hartrevalidatie kent vier hoofddoelen: (1) fysieke doelen, (2) psychische doelen, (3) sociale doelen en (4) beïnvloeden van risicogedrag (leefstijldoelen). Hartrevalidatie wordt op maat aangeboden. Dat betekent dat per patiënt vastgesteld wordt wat de doelen voor die patiënt zijn, en welke interventies aangeboden worden.
Hoe de doelen bij een individuele patiënt vastgesteld worden, wordt in de module Revalidatie op maat (hulpmiddelen indicatiestelling) beschreven. Daarin komen de volgende hulpmiddelen bij de indicatiestelling aan bod: het intakegesprek, de beslisboom en het multidisciplinair overleg. De beslisboom is een hulpmiddel om aan de hand van screening vast te kunnen stellen welke interventies geïndiceerd zijn.
De interventies die binnen hartrevalidatie aangeboden kunnen worden, worden per hoofddoel beschreven in de module Interventies. Binnen hartrevalidatie worden groepsinterventies aangeboden, maar het is ook mogelijk om patiënten door te verwijzen voor individuele behandeling. Nadere diagnostiek kan onderdeel uitmaken van de individuele behandeling. Screening, zoals beschreven in de module Revalidatie op maat (doelen), geeft slechts aan of er een verhoogde kans is op bijvoorbeeld een depressieve stoornis. Met diagnostiek kan vastgesteld worden welke aandoening een patiënt heeft en hoe de individuele behandeling vorm moet krijgen. In de module Interventies wordt ook beschreven hoe de evaluatie van de interventies die zijn aangeboden binnen hartrevalidatie moet plaatsvinden.
De module Hartfalen is gewijd aan hartfalen. De module Bijzondere diagnosegroepen is gewijd aan bijzondere diagnosegroepen en de module Klinische Hartrevalidatie aan klinische hartrevalidatie.
Tenslotte wordt in de module 'Overgang naar zorg' de nazorg beschreven. Hierin staat, conform de transmurale afspraken, de overdracht naar de huisarts centraal.
De referenties zijn weergegeven in een digitale referentielijst die te vinden is op de website van de NVVC (https://www.nvvc.nl/richtlijnen/bestaande-richtlijnen#risicomanagement). De bijlage Afkortingen en begrippen bevat een lijst met afkortingen en begrippen.
Hoewel we ons ervan bewust zijn dat de vrouwelijke hartpatiënt meer aandacht behoeft, zullen patiënten in deze richtlijn als ‘hij’ worden aangeduid. Daar waar ‘hij’ of ‘zijn’ staat, kan met evenveel reden ‘zij’ of ‘haar’ gelezen worden, tenzij specifiek is aangegeven dat de gegevens alleen op mannen betrekking hebben.
Als de gegevens specifiek op vrouwen betrekking hebben, is dat ook aangegeven.
We volgen hiermee de keuze die in de Richtlijn Hartrevalidatie 2004 is gemaakt.
