Palliatieve zorg bij hartfalen NYHA-klasse III en IV - Advance care planning (ACP)
Uitgangsvraag
Leidt advance care planning [1] bij patiënten met hartfalen (NYHA-klasse III-IV) tot een betere kwaliteit van leven en/of hogere tevredenheid van de patiënt en de naasten?
P Patiënten met hartfalen NYHA klasse III-IV
I Advance care planning
C Geen advance care planning
O Tevredenheid van de patiënt, tevredenheid van de familieleden, kwaliteit van leven, kwaliteit van sterfte, heropname, percentage reanimatie in eindstadium
Methodiek: Evidence based (GRADE)
[1] In het Kwaliteitskader palliatieve zorg Nederland [IKNL/Palliactief 2017] en in de Algemene principes van palliatieve zorg [IKNL 2017, www.pallialine.nl wordt in plaats van over advance care planning over proactieve zorgplanning gesproken. Aangezien de basis van het literatuuronderzoek de term ‘advance care planning’ was, hanteren we dat begrip hier. Daarbij merken we op dat dit in de praktijk op hetzelfde neerkomt als proactieve zorgplanning.
Aanbeveling
Start tijdig gesprekken over advance care planning bij patiënten met hartfalen NYHA klasse III-IV.
Aanleidingen voor dergelijke gesprekken kunnen zijn:
- De ‘surprise question’ wordt negatief beantwoord (zie de module Organisatie van zorg);
- Ongeplande ziekenhuisopnames;
- Functionele status is laag of gaat achteruit, met beperkt herstelvermogen (WHO performance status 3: overdag 50% of meer in bed of op stoel);
- Afhankelijkheid van anderen voor zorgbehoeften, door fysieke en/of mentale problemen;
- De mantelzorger heeft meer hulp en ondersteuning nodig;
- Significant gewichtsverlies in de afgelopen maanden of aanhoudend ondergewicht of toename van gewicht, niet reagerend op ophogen van dosering van diuretica;
- Persisterende symptomen ondanks optimale behandeling van onderliggende aandoening(en);
- De patiënt (of naaste) vraagt om palliatieve zorg, kiest om verdere behandeling te verminderen, te staken of er vanaf te zien; of wenst een focus op kwaliteit van leven;
- De patiënt geeft aan niet lang meer te zullen leven.
Bespreek actuele en te verwachten symptomen in alle palliatieve domeinen en daarbij, indien relevant en door de patiënt gewenst, de volgende aspecten:
- individuele levensdoelen en doelen van zorg;
- levensbeschouwing en culturele achtergrond;
- mogelijkheden van palliatieve zorg;
- (niet)-behandelafspraken;
- ziekenhuisopnames / ic-opnames;
- plaats van zorg en sterven;
- crisissituaties (acute verstikking, refractaire symptomen);
- wilsverklaring;
- wettelijke vertegenwoordiging in de situatie van (acute) verslechtering en wilsonbekwaamheid;
- levenseindebeslissingen (onder meer vochttoediening, voeding, antibiotica, reanimatie, uitzetten van de ICD shockfunctie, morfine voor symptoomverlichting (zie richtlijn Dyspneu in de palliatieve fase), dialyse, palliatieve sedatie, euthanasie, weefseldonatie, bewust stoppen met eten en drinken);
- draaglast en draagkracht naasten en mantelzorgers;
- wensen met betrekking tot de uitvaart;
- nazorg.
Stem onderling af wie dit gesprek voert (mede afhankelijk waar de patiënt verblijft en behandeld wordt en wie de hoofdbehandelaar is): de cardioloog, de hartfalenverpleegkundige, de klinisch geriater, de huisarts, de praktijkondersteuner, de verpleegkundig specialist, de specialist ouderengeneeskunde, de consulent palliatieve zorg of de arts verstandelijk gehandicapten. Verwijs zo nodig door naar medebehandelaars, bijvoorbeeld psycholoog, maatschappelijk werken of geestelijk verzorger.
Documenteer de gemaakte afspraken in het individueel zorgplan en zorg dat de andere betrokken hulpverleners op de hoogte zijn van de gemaakte afspraken. Geef een kopie van de gemaakte afspraken mee aan de patiënt.
Herhaal deze gesprekken met enige regelmaat, check of de gemaakte afspraken nog steeds actueel zijn en pas deze zo nodig aan. Noteer de veranderde afspraken in het individueel zorgplan en zorg dat de andere betrokken hulpverleners op de hoogte zijn van de herziene afspraken.
Overwegingen
Bij het zoeken naar literatuur om de onderzoeksvraag ‘leidt ACP bij patiënten met hartfalen (NYHA-klasse III-IV) tot een betere kwaliteit van leven en/of een hogere tevredenheid van de patiënt en de naasten?’ te kunnen beantwoorden, hebben we slechts een gering aantal studies gevonden. De gevonden studies hadden een zeer lage kwaliteit van bewijs.
ACP lijkt een gunstig effect te hebben op de tevredenheid van zowel patiënt als naasten [Denvir 2016 (15)]. Hoewel er géén effect is aangetoond op kans op heropnames [Denvir 2016 (15); Dev 2012 (16)], zijn er aanwijzingen dat de kans op mechanische ventilatie vermindert. Er zijn geen studies gevonden die een effect van ACP bij patiënten met hartfalen op kwaliteit van leven of van sterven als uitkomstmaat hadden. Wel bleek in een vergelijkende, niet-gerandomiseerde studie dat 54% van de patiënten met een niet-reanimeerverklaring in een time-trade-off utility kozen voor kwaliteit van leven boven levensverlenging, terwijl dit percentage slechts 22% was bij mensen zonder niet-reanimeerverklaring (p=0,007) [Dev 2012 (16)]. In een multivariate analyse bleek de kans op het kiezen van kwaliteit van leven boven levensverlenging bij het hebben van een niet-reanimeerverklaring ruim 10 keer zo hoog te zijn als in de groep zonder niet-reanimeerverklaring. De patiënten in deze studie die een niet-reanimeerverklaring hadden, waren ouder, hadden vaker coronaire hartziektes, hypertensie en/of nierfunctiestoornissen en een slechtere inspanningstolerantie dan patiënten met een maximaal beleid. Verder waren ze langer opgenomen en was de mortaliteit binnen 6 maanden hoger. De groepen met en zonder niet-reanimeerverklaring waren dus niet vergelijkbaar.
Het Kwaliteitskader Palliatieve Zorg [IKNL/Palliactief 2017 (18)] geeft aan dat een negatief antwoord op de zogenaamde ‘surprise question’ (zie de module Organisatie van zorg) ook aanleiding kan zijn om een gesprek over ACP aan te gaan.
In het afgelopen decennium zijn er ook diverse tools ontwikkeld om zorgverleners te helpen patiënten te identificeren die een verhoogde kans op achteruitgang of overlijden hebben, en die dus baat zouden kunnen hebben bij ACP of palliatieve zorg [Maas et al 2013 (19); Walsh et al 2015 (20)].
Een van de eerste tools was de RADPAC [Thoonsen 2012 (21)]. Deze is ontwikkeld voor huisartsen, en bevat zeven identificatiecriteria bij hartfalen, die elk zouden kunnen triggeren om ACP te starten:
- De patiënt heeft ernstige functionele beperkingen en ervaart symptomen ook in rust. Het gaat meestal om bedlegerige patiënten (NYHA-klasse 4);
- Frequente ziekenhuisopnames (>3 per jaar);
- Frequente exacerbaties van hartfalen (>3 per jaar);
- Karnofsky Performance Status 50%: patiënt heeft veel hulp en frequente medische ondersteuning nodig;
- Toename van gewicht, niet reagerend op ophogen van dosering van diuretica;
- Algehele achteruitgang van de klinische toestand, gepaard gaande met oedeem, orthopnoe, nycturie en dyspneu;
- De patiënt geeft aan niet lang meer te zullen leven.
Rond dezelfde tijd werd in Edinburgh de SPICT ontwikkeld, welke jaarlijks geüpdatet wordt met commentaar vanuit zorgverleners, en ook jaarlijks in het Nederlands vertaald wordt [Highet 2014 (22)] (http://www.spict.org.uk/ en SPICT-NL) . De SPICT overlapt gedeeltelijk met de RADPAC, maar is voor alle bij palliatieve zorg betrokken professionals in eerste en tweede lijn ontwikkeld. De SPICT bevat een aantal generieke identificatiecriteria en daarnaast per ziektegroep nog een of meerdere specifieke criteria. De generieke criteria, zoals geformuleerd in versie 2017 zijn:
- Ongeplande ziekenhuisopnames;
- Functionele status is laag of gaat achteruit, met beperkt herstelvermogen (WHO performance status 3: overdag 50% of meer in bed of op stoel);
- Afhankelijk van anderen voor zorgbehoeften, door fysieke en/of mentale problemen;
- De mantelzorger heeft meer hulp en ondersteuning nodig;
- Significant gewichtsverlies in de afgelopen maanden, of aanhoudend ondergewicht;
- Persisterende symptomen ondanks optimale behandeling van onderliggende aandoening(en);
- De patiënt (of naaste) vraagt om palliatieve zorg, kiest om verdere behandeling te verminderen, te staken of er vanaf te zien; of wenst een focus op kwaliteit van leven.
Het ziektespecifieke criterium voor hartfalen betreft: hartfalen met dyspneu of pijn op de borst in rust of geringe inspanning.
Doordat de SPICT (http://www.spict.org.uk/ en SPICT-NL) jaarlijks geüpdatet wordt, gebruikt kan worden door alle professionals in zowel de eerste en de tweede lijn, en doordat de criteria tot vroegere identificatie uitnodigen dan de RADPAC hebben we in deze richtlijn voor de SPICT gekozen, aangevuld met twee criteria van Thoonsen die in de SPICT missen (RADPAC 5 en 7). Daarnaast merken we bij criterium 4 van de SPICT op dat niet als los criterium beschouwd kan worden, maar altijd als aanvulling op de aanwezigheid van één van de vorige criteria. Tenslotte hebben we het ziektespecifieke criterium van de SPICT niet meegenomen doordat dit overeenkomt met NIHA-klasse III en daardoor de overige criteria overbodig zouden worden.
Onderbouwing
In deze richtlijn wordt de volgende definitie van advance care planning (ACP) gehanteerd: ACP is het proces waarin de patiënt samen met de zorgverlener en de naasten beslissingen neemt over de toekomstige zorg en over toekomstige medische behandelingen [Singer 1996 (1)]. Andere gebruikte termen hiervoor zijn toekomstige zorgplanning, anticiperende zorgplanning of proactieve zorgplanning. Vooruit denken, plannen en organiseren zijn hierin essentiële elementen. Met gezamenlijke besluitvorming als leidraad is het een continu en dynamisch proces van gesprekken over huidige en toekomstige levensdoelen en keuzes en welke zorg daar nu en in de toekomst bij past.
Door deze definitie te hanteren beperken we ons met ACP niet tot het maken van afspraken over de stervensfase. Door dergelijke gesprekken tijdig, gestructureerd en regelmatig te voeren kunnen zowel de patiënt en naasten als de zorgverleners zich voorbereiden op de toekomst.
ACP leidt tot het vaker opstellen van een wilsbeschikking en het vaker bespreken van wensen en behoeften, maakt dat de geboden zorg en behandeling vaker in overeenstemming zijn met de voorkeuren van de patiënt, en lijkt de kwaliteit van de communicatie tussen patiënt, naasten en zorgverlener te verbeteren [Houben 2014 (2)].
Een gerandomiseerd onderzoek bij oudere patiënten liet zien dat advance care planning leidt tot betere bekendheid van wensen met betrekking tot het levenseinde, minder stress, angst en depressie bij de nabestaanden en meer tevredenheid bij patiënt en naasten [Detering 2010 (3)].
Prognose, ziekteprogressie, problemen, behoeften en wensen voor de toekomst en het levenseinde worden bij mensen met hartfalen weinig besproken, terwijl patiënten en naasten het waarderen wanneer het wel gebeurt [Allen 2008 (4), Janssen 2011 (5), Harding 2008 (6), Houben 2015 (7)]. Uit onderzoek blijkt dat veel patiënten in dit stadium van de ziekte kwaliteit van leven en goede zorg belangrijker vinden dan duur van het leven. Communicatie over reële behandeldoelen in overeenstemming met de wens en voorkeuren van patiënt, bij voorkeur vastgelegd in een schriftelijk zorgplan, ontbreekt vaak [Bakitas 2013 (8), Hanratty 2002 (9), Stewart 2002 (10)]. Een knelpunt daarbij is de onvoorspelbaarheid van het ziektetraject, waardoor een ‘prognostische paralyse’ bij de zorgverleners bestaat [Stewart 2002 (10), Kendall 2014 (11), Epiphaniou 2014 (12)]. Deze paralyse staat gezamenlijke bespreking van en besluitvorming over toekomstige zorgopties en -behoeften in de weg.
Bij deze uitgangsvraag wordt ingegaan op de rol van ACP bij patiënten met hartfalen.
Er is bewijs van zeer lage kwaliteit dat advance care planning geen effect heeft op de kwaliteit van leven in vergelijking met gewone zorg bij patiënten met hartfalen.
[Denvir 2016 (15)]
Er is bewijs van zeer lage kwaliteit dat de aanwezigheid van een wilsverklaring met behandelbeperkingen gepaard gaat met een significant lagere kans op mechanische ventilatie bij patiënten met hartfalen.
[Dunlay 2012 (17)]
Er is bewijs van zeer lage kwaliteit dat advance care planning een gunstig effect heeft op de tevredenheid van patiënten met hartfalen en hun naasten.
[Denvir 2016 (15)]
Er is bewijs van zeer lage kwaliteit dat advance care planning geen significant effect heeft op het aantal heropnames bij patiënten met hartfalen, en eveneens bewijs van zeer lage kwaliteit dat het wel tot een kortere opnameduur leidt.
[Denvir 2016 (15)]
Er is bewijs van zeer lage kwaliteit dat een niet-reanimeerverklaring geen significant effect heeft op heropnames bij patiënten met hartfalen.
[Dev 2012 (16)]
Algehele kwaliteit van bewijs = zeer laag
Literatuurbeschrijving
Beschrijving van de studies
Systematische reviews
De search identificeerde twee systematische reviews, één die het effect bestudeerde van interventies om verwijzing naar palliatieve zorg bij terminale patiënten te bevorderen [Kirolos 2014 (13)] en één brede review die het effect van palliatieve zorg interventies bestudeerde [Singer 2016 (14)].
Kirolos et al. vonden één observationele studie (Schellinger 2011) over ACP bij patiënten met hartfalen [Kirolos 2014 (13)]. De gerapporteerde uitkomsten zijn echter niet relevant voor de uitgangsvraag en de studie wordt dan ook verder niet besproken.
Singer et al. vonden geen gerandomiseerde studie over ACP bij patiënten met hartfalen [Singer 2016 (14)].
RCT’s
De search identificeerde aanvullend nog één RCT die niet in één van de eerder vermelde reviews geïncludeerd werd.
Denvir et al. randomiseerden 50 patiënten, die opgenomen waren met acuut hartfalen (68%) en/of een acuut coronair syndroom, naar advance care planning (future care planning) of gewone zorg [Denvir 2016 (15)]. In het advance care plan werden o.a. de volgende elementen opgenomen: bespreken om een wettelijk vertegenwoordiger te kiezen, voorkeursplaats van verzorging bij verdere verslechtering, staken van levensverlengende behandeling en cardiopulmonaire reanimatie.
Observationele studies
Eén observationele studie evalueerde het effect van een niet-reanimeerbeleid bij 375 patiënten met gevorderd hartfalen (26 patiënten met een niet-reanimeerverklaring en 349 patiënten met een maximaal beleid) [Dev 2012 (16)]. Een tweede observationele studie vergeleek 249 patiënten met hartfalen die een wilsverklaring (advance directive) hadden met 359 patiënten zonder een wilsverklaring [Dunlay 2012 (17)]. (In een wilsverklaring staat beschreven hoe iemand behandeld wenst te worden bij het levenseinde.)
Kwaliteit van het bewijs
De review van Kirolos et al. is van lage kwaliteit [Kirolos 2014 (13)]. Er wordt wel een behoorlijke beschrijving gegeven van de gebruikte methodologie, maar het is bijvoorbeeld onduidelijk of de selectie gebeurde door twee onafhankelijke onderzoekers. Bovendien was de literatuursearch beperkt tot Medline en tot Engelstalige literatuur.
De review van Singer et al. is van behoorlijke kwaliteit [Singer 2016 (14)]. Er is een goede beschrijving van de methodologie, die bovendien degelijk was. Er werd wel alleen gezocht in de Engelstalige literatuur.
De RCT van Denvir et al. heeft een hoog risico op bias door het onvermijdelijk ontbreken van blindering van de patiënten en behandelaars [Denvir 2016 (15)]. Bovendien was er geen duidelijke allocation concealment en was er geen intention-to-treat analyse voor sommige uitkomsten, zoals voor kwaliteit van leven. Vermoedelijk was er ook een selectiebias: van de 137 patiënten die in aanmerking kwamen voor inclusie, werden er 54 uiteindelijk niet geïncludeerd om onduidelijke redenen (en 33 met reden).
De observationele studie van Dev et al. was van degelijke kwaliteit [Dev 2012 (16)]. Ze deden een analyse van een gerandomiseerde studie, waarbij de uitkomsten blind beoordeeld werden door een onafhankelijke commissie. Er werd tevens gecorrigeerd voor een aantal prognostische factoren. Voor de time-trade-off utility was er wel selectieve loss-to-follow-up.
De studie van Dunlay et al. was een retrospectieve populatie-gebaseerde studie, waarbij de evaluatie niet geblindeerd was [Dunlay 2012 (17)]. Er werd wel een multivariate analyse verricht.
Effect op kwaliteit van leven: belangrijke uitkomstmaat
Advance care planning
Denvir et al. vonden geen significant effect van advance care planning op kwaliteit van leven, gemeten met de EQ-5D na 12 weken (gecorrigeerd gemiddeld verschil = -0,01; 95%BI -0,16 tot 0,13) of 24 weken (gecorrigeerd gemiddeld verschil = -0,07; 95%BI -0,25 tot 0,11) [Denvir 2016 (15)]. Dit gebrek van een positief resultaat wordt door de auteurs overigens als een relatief positieve bevinding gerapporteerd. Het spreekt namelijk tegen dat door het bespreken van de toekomst en het eindeleven de kwaliteit van leven van de patiënt zou dalen, wat vaak als argument wordt genoemd door zorgverleners om het gesprek over de toekomst niet aan te gaan.
Effect op kwaliteit van sterven: belangrijke uitkomstmaat
Advance care planning/wilsverklaring
Denvir et al. rapporteerden geen duidelijke resultaten over kwaliteit van sterven [Denvir 2016 (15)]. Er was geen verschil in de plaats van overlijden, maar de aantallen waren te klein om een statistische analyse uit te voeren.
Dunlay et al. rapporteerden (na correctie voor geslacht, leeftijd en comorbiditeit) een significant lagere kans op mechanische ventilatie bij patiënten met een wilsverklaring met behandelbeperkingen dan bij patiënten zonder een wilsverklaring of met een wilsverklaring zonder behandelbeperkingen (gecorrigeerde odds ratio = 0,26; 95%BI 0,06 tot 0,88) [Dunlay 2012 (17)]. De kans op opname op een intensive care was lager, maar niet statistisch significant (gecorrigeerde odds ratio = 0,45; 95%BI 0,16 tot 1,29).
Effect op tevredenheid van de patiënt: kritische uitkomstmaat
Advance care planning
Denvir et al. deden een kwalitatief onderzoek naar de tevredenheid van de patiënt [Denvir 2016 (15)]. Patiënten waardeerden het contact en de communicatie.
Effect op tevredenheid van de familie: kritische uitkomstmaat
Toekomstige zorgplanning
Denvir et al. deden een kwalitatief onderzoek naar de tevredenheid van de naasten [Denvir 2016 (15)]. Naasten waren zeer positief over de advance care planning, vooral door de openheid waarmee over een aantal moeilijke punten werd gesproken en door de gedetailleerde toekomstige zorgplanning.
Effect op heropname: kritische uitkomstmaat
Advance care planning/wilsverklaring
Denvir et al. vonden geen significant effect van een advance care plan op ongeplande heropnames binnen 12 weken (relatief risico = 1,25; 95%BI 0,54 tot 2,89) of 6 maanden (relatief risico = 1,23; 95%BI 0,64 tot 2,34), en ook niet specifiek op ongeplande cardiovasculaire heropnames (12 weken: relatief risico = 1,22; 95%BI 0,41 tot 3,62; 6 maanden: relatief risico = 0,83; 95%BI 0,33 tot 2,11) [Denvir 2016 (15)].
De opnameduur in de eerste 12 weken (relatief risico = 0,50; 95%BI 0,37 tot 0,67) en 6 maanden (relatief risico = 0,73; 95%BI 0,61 tot 0,88) was wel significant lager in de groep met een toekomstig zorgplan, hoewel de auteurs dit deels toeschreven aan een iets hogere sterfte in die groep.
Dunlay et al. rapporteerden geen significant verschil in het risico op ziekenhuisopname in de laatste levensmaand tussen patiënten met een wilsverklaring met behandelbeperkingen en patiënten zonder een wilsverklaring of met een wilsverklaring zonder behandelbeperkingen (gecorrigeerde odds ratio = 1,26; 95%BI 0,64 tot 2,48) [Dunlay 2012 (17)].
Niet-reanimeerbeleid
Dev et al. vonden geen significant verschil tussen patiënten met en zonder een niet-reanimeerverklaring in ziekenhuisopname binnen 6 maanden (41% vs. 52%, p = 0,79) [Dev 2012 (16)].
Reanimatie in eindfase:
Voor deze uitkomst werden geen studies gevonden.
Methodology report PICO 3 (ACP)
Key question
Uitgangsvraag 3: Leidt advance care planning bij patiënten met hartfalen (NYHA-klasse III-IV) tot een betere kwaliteit van leven en/of hogere tevredenheid van de patiënt en de familieleden?
P: Patiënten met hartfalen NYHA klasse III-IV
I: Advance care planning
C: Geen advance care planning
O: Tevredenheid van de patiënt, tevredenheid van de familieleden, kwaliteit van leven, kwaliteit van sterfte\, heropname, percentage reanimatie in eindstadium
Search strategy
Search date: November 23 and December 8, 2016.
Databases: OVID Medline, Pubmed, Embase and Cochrane Library (see appendix for search strings).
Search limits:
- Publication date: 2007-2016
- English, Dutch;
- Study design: systematic reviews, RCTs, comparative observational studies.
Search Results
Table 3. Overall search results.
|
Database |
|
Number of hits |
|
|
|
23-11-2016 |
8-12-2016 |
8-12-2016 |
|
OVID Medline |
542 |
180 |
|
|
Pubmed |
|
|
271 |
|
Embase |
1454 |
|
|
|
CENTRAL |
387 |
|
|
|
HTA |
0 |
|
|
|
DARE |
4 |
|
|
|
CDSR |
29 |
|
|
|
Total hits |
2416 |
180 |
271 |
|
N excluded (language, year, duplicates) |
710 |
33 |
8 |
|
Total unique eligible hits |
1706 |
147 |
263 |
a. Excluded studies
1706, 147 and 263 unique hits, respectively, were screened on title and abstract (Table 3). Of these, 2078 were excluded in a first phase. The most important reasons for exclusion were:
- Other population: patients without heart failure, no palliative population
- Wrong intervention
- Wrong study design: e.g. narrative reviews, case series, needs assessment, etc.
Of the remaining 38 papers, the full-text was retrieved. Based on the full-text, 33 papers were excluded.
Table 4 provides an overview of the excluded studies.
b. Included studies
The following five studies were included:
- Denvir MA, Cudmore S, Highet G, et al. Phase 2 Randomised Controlled Trial and Feasibility Study of Future Care Planning in Patients with Advanced Heart Disease. Sci Rep. 2016;6:24619 LID - 10.1038/srep [doi].
- Kirolos I, Tamariz L, Schultz EA, et al. Interventions to improve hospice and palliative care referral: a systematic review. J Palliat Med. 2014;17(8):957-64.
- Singer AE, Goebel JR, Kim YS, et al. Populations and Interventions for Palliative and End-of-Life Care: A Systematic Review. J. Palliative Med. 2016;19(9):995-1008.
- Dev S, Clare RM, Felker GM, et al. Link between decisions regarding resuscitation and preferences for quality over length of life with heart failure. Eur J Heart Fail. 2012;14(1):45-53.
- Dunlay SM, Swetz KM, Mueller PS, et al. Advance directives in community patients with heart failure. Circ Cardiovasc Qual Outcomes. 2012;Cardiovascular Quality & Outcomes. 5(3):283-9.
Table 4. Key question 3: overview of excluded studies based on full-text evaluation.
|
Reference |
Reason |
|
Adler ED, Goldfinger JZ, Kalman J, et al. Palliative care in the treatment of advanced heart failure. Circulation. 2009;120(25):2597-606. |
Narrative overview |
|
Brännström M, Boman K. A new model for integrated heart failure and palliative advanced homecare--rationale and design of a prospective randomized study. European journal of cardiovascular nursing : journal of the Working Group on Cardiovascular Nursing of the European Society of Cardiology. 2013;12(3):269-75. |
Protocol for RCT |
|
Brannstrom M, Boman K. Effects of person-centred and integrated chronic heart failure and palliative home care. PREFER: a randomized controlled study. Eur J Heart Fail. 2014;16(10):1142-51. |
ACP not clearly delineable |
|
Butler J, Binney Z, Kalogeropoulos A, et al. Advance directives among hospitalized patients with heart failure. JACC Heart Fail. 2015;3(2):112-21. |
No comparative study |
|
Chen CY, Thorsteinsdottir B, Cha SS, et al. Health care outcomes and advance care planning in older adults who receive home-based palliative care: A pilot cohort study. J. Palliative Med. 2015;18(1):38-44. |
ACP reported as outcome |
|
Chen JLT, Sosnov J, Lessard D, et al. Impact of do-not-resuscitation orders on quality of care performance measures in patients hospitalized with acute heart failure. Am Heart J. 2008;156(1):78-84. |
Wrong outcomes |
|
Denvir MA, Murray SA, Boyd KJ. Future care planning: a first step to palliative care for all patients with advanced heart disease. Heart. 2015;101(13):1002-7. |
Narrative overview |
|
Dionne-Odom JN, Kono A, Frost J, et al. Translating and testing the ENABLE: CHF-PC concurrent palliative care model for older adults with heart failure and their family caregivers. J. Palliative Med. 2014;17(9):995-1004. |
No comparative study |
|
El-Jawahri A, Paasche-Orlow MK, Matlock D, et al. Randomized, controlled trial of an advance care planning video decision support tool for patients with advanced heart failure. Circulation. 2016;134(1):52-60. |
ACP use as an outcome |
|
Evangelista LS, Liao S, Motie M, et al. Does the type and frequency of palliative care services received by patients with advanced heart failure impact symptom burden. J. Palliative Med. 2014;17(1):75-9. |
No comparative study |
|
Evangelista LS, Liao S, Motie M, et al. On-going palliative care enhances perceived control and patient activation and reduces symptom distress in patients with symptomatic heart failure: a pilot study. EUR J CARDIOVASC NURS. 2014;13(2):116-23. |
ACP not clearly delineable |
|
Evangelista LS, Lombardo D, Malik S, et al. Examining the effects of an outpatient palliative care consultation on symptom burden, depression, and quality of life in patients with symptomatic heart failure. J Card Fail. 2012;18(12):894-9. |
ACP not clearly delineable |
|
Gadoud A, Jenkins SMM, Hogg KJ. Palliative care for people with heart failure: summary of current evidence and future direction. Palliat Med. 2013;27(9):822-8. |
Narrative overview |
|
Gomes B, Calanzani N, Curiale V, et al. Effectiveness and cost-effectiveness of home palliative care services for adults with advanced illness and their caregivers. Cochrane Database Syst. Rev. 2013;2016(3). |
ACP not clearly delineable |
|
Hayek S, Nieva R, Corrigan F, et al. End-of-life care planning: improving documentation of advance directives in the outpatient clinic using electronic medical records. J Palliat Med. 2014;17(12):1348-52. |
ACP use as an outcome |
|
Irving G, Holden J, Edwards J, et al. Chronic heart failure guidelines: do they adequately address patient need at the end-of-life? Int J Cardiol. 2013;168(3):2304-9. |
Overview of guidelines; useful for other considerations |
|
Jaarsma T, Beattie JM, Ryder M, et al. Palliative care in heart failure: A position statement from the palliative care workshop of the Heart Failure Association of the European Society of Cardiology. Eur. J. Heart Fail. 2009;11(5):433-43. |
Position statement; no methods reported for searching; useful for other considerations |
|
Johnson M, Nunn A, Hawkes T, et al. Planning for end-of-life care in heart failure: Experience of two integrated cardiology-palliative care teams. Br. J. Cardiol. 2012;19(2):71-5. |
Descriptive study |
|
Lemond L, Allen LA. Palliative Care and Hospice in Advanced Heart Failure. Prog. Cardiovasc. Dis. 2011;54(2):168-78. |
Narrative overview |
|
Low J, Pattenden J, Candy B, Beattie JM, Jones L. Palliative care in advanced heart failure: An international review of the perspectives of recipients and health professionals on care provision. J. Card. Fail. 2011;17(3):231-52. |
Not on ACP as such |
|
Malhotra C, Sim DKL, Jaufeerally F, et al. Impact of advance care planning on the care of patients with heart failure: Study protocol for a randomized controlled trial. Trials. 2016;17(1). |
Protocol for RCT |
|
McIlvennan CK, Allen LA. Palliative care in patients with heart failure. Bmj. 2016;353. |
Is in fact a narrative overview |
|
McKelvie RS, Moe GW, Cheung A, et al. The 2011 Canadian cardiovascular society heart failure management guidelines update: Focus on sleep apnea, renal dysfunction, mechanical circulatory support, and palliative care. Can. J. Cardiol. 2011;27(3):319-38. |
Consensus guidelines; useful for other considerations |
|
Mentz RJ, Tulsky JA, Granger BB, Anstrom KJ, Adams PA, Dodson GC, et al. The palliative care in heart failure trial: rationale and design. Am Heart J. 2014;168(5):645-51.e1. |
Protocol for RCT |
|
Pattenden JF, Mason AR, Lewin RJP. Collaborative palliative care for advanced heart failure: outcomes and costs from the 'Better Together' pilot study. BMJ support. 2013;3(1):69-76. |
No clear ACP as part of intervention |
|
Sadeghi B, Walling AM, Romano PS, et al. A Hospital-Based Advance Care Planning Intervention for Patients with Heart Failure: A Feasibility Study. J. Palliative Med. 2016;19(4):451-5. |
Study on implementation of ACP intervention |
|
Schwarz ER, Baraghoush A, Morrissey RP, et al. Pilot study of palliative care consultation in patients with advanced heart failure referred for cardiac transplantation. J. Palliative Med. 2012;15(1):12-5. |
No comparative study |
|
Shah AB, Morrissey RP, Baraghoush A, et al. Failing the failing heart: a review of palliative care in heart failure. Reviews in Cardiovascular Medicine. 2013;14(1):41-8. |
Narrative overview |
|
Siouta N, van Beek K, Preston N, et al. Towards integration of palliative care in patients with chronic heart failure and chronic obstructive pulmonary disease: a systematic literature review of European guidelines and pathways. BMC Palliative Care. 2016;15(18). |
Overview of guidelines; useful for other considerations |
|
Stevenson LW, O'Donnell A. Advanced care planning: care to plan in advance. JACC Heart Fail. 2015;3(2):122-6. |
Editorial |
|
Van Scoy LJ, Green MJ, Dimmock AEF, et al. High satisfaction and low decisional conflict with advance care planning among chronically ill patients with advanced chronic obstructive pulmonary disease or heart failure using an online decision aid: A pilot study. Chronic Illn. 2016;12(3):227-35. |
No comparative study |
|
Ventura MdM. Effectiveness and cost-effectiveness of home palliative care services for adults with advanced illness and their caregivers. Sao Paulo Med J. 2016;134(1):93-4. |
Comment on Gomes 2013 |
|
Xu J, Abshire M, Han HR. Decision Making Among Persons Living With Heart Failure. J Cardiovasc Nurs. 2016;31(5):E1-9 LID - 10.1097/JCN.0000000000000312 [doi]. |
Not on ACP as such |
Search strings Question 3 (ACP)
1. medline (ovid): 23-11-2016
1 exp Heart Failure/ (108062)
2 (heart adj2 failure*).tw. (127967)
3 (cardiac adj2 failure*).tw. (13178)
4 (myocardial adj2 failure*).tw. (2750)
5 (heart adj2 decompensat*).tw. (2859)
6 heart failure.tw. (127362)
7 cardiac failure.tw. (10677)
8 or/1-7 (171860)
9 NYHA III.mp. (599)
10 NYHA IV.mp. (239)
11 NYHA 3.mp. (26)
12 NYHA 4.mp. (6)
13 or/1-12 (172070)
14 exp Advance Care Planning/ (8406)
15 (advance care adj (plan or plans or planning)).tw. (1332)
16 (advance adj (directive* or decision*)).tw. (3044)
17 living will*.tw. (1173)
18 Right to Die/ (5120)
19 right to die.tw. (925)
20 ((patient or patients) adj5 (advocat* or advocacy)).tw. (4859)
21 power of attorney.tw. (353)
22 ((end of life or EOL) adj5 (care or discuss* or decision* or plan or plans or planning or preference*)).tw. (10117)
23 Terminal Care/ (25238)
24 Treatment Refusal/ (11915)
25 exp Withholding Treatment/ (14673)
26 (treatment adj5 (refus* or withhold* or withdraw*)).tw. (14155)
27 future care planning.mp. (22)
28 anticipating care.mp. (1)
29 early palliative care.mp. (120)
30 timely palliative care.mp. (11)
31 or/14-30 (74433)
32 13 and 31 (926)
33 limit 32 to yr="2007 -Current" (542)
2. medline (ovid): 8-12-2016
1 exp Heart Failure/ (108079)
2 (heart adj2 failure*).tw. (127990)
3 (cardiac adj2 failure*).tw. (13182)
4 (myocardial adj2 failure*).tw. (2752)
5 (heart adj2 decompensat*).tw. (2859)
6 heart failure.tw. (127385)
7 cardiac failure.tw. (10681)
8 or/1-7 (171889)
9 NYHA III.mp. (601)
10 NYHA IV.mp. (239)
11 NYHA 3.mp. (26)
12 NYHA 4.mp. (6)
13 or/1-12 (172099)
14 exp Advance Care Planning/ (8409)
15 (advance care adj (plan or plans or planning)).tw. (1336)
16 (advance adj (directive* or decision*)).tw. (3046)
17 living will*.tw. (1173)
18 Right to Die/ (5120)
19 right to die.tw. (925)
20 ((patient or patients) adj5 (advocat* or advocacy)).tw. (4861)
21 power of attorney.tw. (353)
22 ((end of life or EOL) adj5 (care or discuss* or decision* or plan or plans or planning or preference*)).tw. (10126)
23 Terminal Care/ (25250)
24 Treatment Refusal/ (11917)
25 exp Withholding Treatment/ (14678)
26 (treatment adj5 (refus* or withhold* or withdraw*)).tw. (14160)
27 future care planning.mp. (22)
28 anticipating care.mp. (1)
29 early palliative care.mp. (120)
30 timely palliative care.mp. (11)
31 or/14-30 (74459)
32 13 and 31 (929)
33 limit 32 to yr="2007 -Current" (545)
34 *"Palliative Care"/ (26669)
35 31 or 34 (94797)
36 13 and 35 (1214)
37 limit 36 to yr="2007 -Current" (725)
38 37 not 33 (180)
3. PubMed: 8-12-2016
#20,"Search #5 and #18 Filters: Publication date from 2016/01/01 to 2016/12/31",271,09:06:18
#19,"Search #5 and #18",4418,09:05:40
#18,"Search #6 or #7 or #8 or #9 or #10 or #11 or #12 or #13 or #14 or #15 or #16 or #17",211534,09:05:22
#17,"Search timely palliative care",445,09:04:26
#16,"Search early palliative care",3881,09:04:17
#15,"Search anticipating care",852,09:04:10
#14,"Search future care planning",9633,09:04:02
#13,"Search (treatment and (refus* or withhold* or withdraw*))",115848,09:03:53
#12,"Search ((end of life or EOL) and (care or discuss* or decision* or plan or plans or planning or preference*))",27503,09:03:38
#11,"Search power of attorney",423,09:03:22
#10,"Search ((patient or patients) and (advocat* or advocacy))",49439,09:03:11
#9,"Search right to die",5804,09:02:57
#8,"Search living will*",2209,09:02:49
#7,"Search (advance and (directive* or decision*))",9587,09:02:42
#6,"Search (advance care and (plan or plans or planning))",3943,09:02:27
#5,"Search #1 or #2 or #3 or #4",229234,09:02:09
#4,"Search NYHA",10804,09:01:46
#3,"Search myocardial and failure",64853,09:01:38
#2,"Search cardiac and failure",221219,09:01:30
#1,"Search heart and failure",204795,09:01:22
4. Embase
|
#1 |
'heart failure'/exp |
389502 |
|
#2 |
(heart NEAR/2 failure*):ab,ti |
202388 |
|
#3 |
(myocardial NEAR/2 failure*):ab,ti |
3791 |
|
#4 |
(cardiac NEAR/2 failure*):ab,ti |
18833 |
|
#5 |
(heart NEAR/2 decompensat*):ab,ti |
5732 |
|
#6 |
nyha:ab,ti AND 3:ab,ti OR nyha:ab,ti AND 4:ab,ti OR nyha:ab,ti AND iii:ab,ti OR nyha:ab,ti AND iv:ab,ti |
9721 |
|
#7 |
#1 or #2 or #3 or #4 or #5 or #6 |
429594 |
|
#8 |
'living will'/exp OR 'right to die'/exp OR 'patient advocacy'/exp OR 'power of attorney'/exp OR 'terminal care'/exp OR 'treatment refusal'/exp OR 'treatment withdrawal'/exp |
100146 |
|
#9 |
(living NEAR/1 will*):ab,ti |
1370 |
|
#10 |
('advance care' NEAR/1 (plan OR plans OR planning)):ab,ti |
2050 |
|
#11 |
'right to die':ab,ti |
920 |
|
#12 |
((patient OR patients) NEAR/5 (advocat* OR advocacy)):ab,ti |
6796 |
|
#13 |
'power of attorney':ab,ti |
469 |
|
#14 |
(('end of life' OR eol) NEAR/5 (care OR discuss* OR decision* OR plan OR plans OR planning OR preference*)):ab,ti |
14104 |
|
#15 |
'terminal care':ab,ti |
1687 |
|
#16 |
(treatment NEAR/2 (refus* OR withhold* OR withdraw*)):ab,ti |
10163 |
|
#17 |
#8 OR #9 OR #10 OR #11 OR #12 OR #13 OR #14 OR #15 OR #16 |
117925 |
|
#18 |
#7 AND #17 |
3203 |
|
#19 |
#18 AND ([article]/lim OR [article in press]/lim OR [review]/lim) AND ([dutch]/lim OR [english]/lim) AND ([embase]/lim OR [medline]/lim) AND [2007-2016]/py |
1454 |
5. Cochrane Library
#1 MeSH descriptor: [Advance Care Planning] explode all trees
#2 MeSH descriptor: [Right to Die] 1 tree(s) exploded
#3 MeSH descriptor: [Terminal Care] 1 tree(s) exploded
#4 MeSH descriptor: [Treatment Refusal] 1 tree(s) exploded
#5 MeSH descriptor: [Withholding Treatment] 1 tree(s) exploded
#6 MeSH descriptor: [Patient Advocacy] 1 tree(s) exploded
#7 ("advance care" and (plan or plans or planning)):ti,ab
#8 (advance and (directive* or decision*)):ti,ab
#9 living will*:ti,ab
#10 "right to die":ti,ab
#11 ((patient or patients) and (advocat* or advocacy)):ti,ab
#12 "power of attorney":ti,ab
#13 (("end of life" or EOL) and (care or discuss* or decision* or plan or plans or planning or preference*)):ti,ab
#14 (treatment and (refus* or withhold* or withdraw*)):ti,ab
#15 "terminal care":ti,ab
#16 "palliative approach":ti,ab
#17 #1 or #2 or #3 or #4 or #5 or #6 or #7 or #8 or #9 or #10 or #11 or #12 or #13 or #14 or #15 or #16
#18 MeSH descriptor: [Heart Failure] 1 tree(s) exploded
#19 (heart and failure*):ti,ab
#20 (cardiac and failure*):ti,ab
#21 (myocardial and failure*):ti,ab
#22 (heart and decompensat*):ti,ab
#23 "NYHA III":ti,ab
#24 "NYHA IV":ti,ab
#25 "NYHA 3":ti,ab
#26 "NYHA 4":ti,ab
#27 #18 or #19 or #20 or #21 or #22 or #23 or #24 or #25 or #26
#28 #17 and #27
- 18 - Kwaliteitskader palliatieve zorg Nederland, IKNL/Palliactief 2017
Beoordelingsdatum en geldigheid
Publicatiedatum : 07-02-2018
Beoordeeld op geldigheid :
Actualisatie
Deze richtlijn(module) is goedgekeurd op 28 november 2017. IKNL en PAZORI bewaken samen met betrokken verenigingen de houdbaarheid van deze en andere onderdelen van de richtlijn. Zo nodig wordt de richtlijn tussentijds op onderdelen bijgesteld. De geldigheidstermijn van de richtlijn is maximaal 5 jaar na vaststelling. Indien de richtlijn dan nog actueel wordt bevonden, wordt de geldigheidsduur van de richtlijn verlengd.
Houderschap richtlijn
De houder van de richtlijn moet kunnen aantonen dat de richtlijn zorgvuldig en met de vereiste deskundigheid tot stand is gekomen. Onder houder wordt verstaan de verenigingen van beroepsbeoefenaren die de richtlijn autoriseren.
IKNL draagt zorg voor het beheer en de ontsluiting van de richtlijn.
Juridische betekenis van richtlijnen
De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. Er kunnen zich feiten of omstandigheden voordoen waardoor het wenselijk is dat in het belang van de patiënt van de richtlijn wordt afgeweken. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd gedocumenteerd te worden. De toepassing van de richtlijnen in de praktijk is de verantwoordelijkheid van de behandelende arts.
Algemene gegevens
Initiatief
Platform PAZORI (Palliatieve Zorg Richtlijnen)
IKNL (Integraal Kankercentrum Nederland)
Autoriserende en betrokken verenigingen
Patiëntenfederatie Nederland (voorheen Nederlandse Patiënten en Consumenten Federatie NPCF)*
De Hart&Vaatgroep/Hartstichting*
Nederlandse Vereniging voor Cardiologie (NVVC)
Nederlandse Vereniging voor Klinische Geriatrie (NVKG)
Nederlands Huisartsen Genootschap (NHG)*
Nederlandse Vereniging van Ziekenhuisapothekers (NVZA)
Palliactief
Specialisten ouderengeneeskunde (Verenso)
Nederlandse Vereniging voor Hart- en Vaat Verpleegkundigen (NVHVV)
Verpleegkundigen & Verzorgenden Nederland (V&VN)
Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie (KNMP)*
*Deze verenigingen autoriseren niet, maar stemmen in met de inhoud.
Financiering
Deze richtlijn c.q. module is gefinancierd door IKNL. De inhoud van de richtlijn c.q. module is niet beïnvloed door de financierende instantie.
Een richtlijn is een kwaliteitsstandaard. Een kwaliteitsstandaard beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een kwaliteitsstandaard in het Register betekent dus niet noodzakelijkerwijs dat de in de kwaliteitsstandaard beschreven zorg verzekerde zorg is.
Procesbegeleiding en verantwoording
IKNL (Integraal Kankercentrum Nederland) is het kennis- en kwaliteitsinstituut voor professionals en bestuurders in de oncologische en palliatieve zorg dat zich richt op het continu verbeteren van de oncologische en palliatieve zorg.
IKNL benadert preventie, diagnose, behandeling, nazorg en palliatieve zorg als een keten waarin de patiënt centraal staat. Om kwalitatief goede zorg te waarborgen ontwikkelt IKNL producten en diensten ter verbetering van de oncologische zorg, de nazorg en de palliatieve zorg, zowel voor de inhoud als de organisatie van de zorg binnen en tussen instellingen. Daarnaast draagt IKNL nationaal en internationaal bij aan de beleidsvorming op het gebied van oncologische en palliatieve zorg.
IKNL rekent het (begeleiden van) ontwikkelen, implementeren en evalueren van multidisciplinaire, evidence based richtlijnen voor de oncologische en palliatieve zorg tot een van haar primaire taken. IKNL werkt hierbij conform de daarvoor geldende (inter)nationale kwaliteitscriteria. Bij ontwikkeling gaat het in toenemende mate om onderhoud (modulaire revisies) van reeds bestaande richtlijnen.
Doel en doelgroep
Doel
Een richtlijn is een aanbeveling ter ondersteuning van de belangrijkste knelpunten uit de dagelijkse praktijk. Deze richtlijn is zoveel mogelijk gebaseerd op wetenschappelijk onderzoek en consensus. De richtlijn palliatieve zorg bij hartfalen geeft aanbevelingen over begeleiding en behandeling van patiënten met hartfalen NYHA-klasse III en IV en beoogt hiermee de kwaliteit van de zorgverlening te verbeteren.
Doelpopulatie
Deze richtlijn heeft betrekking op volwassen patiënten met hartfalen met NYHA (New York Heart Association)-klasse III en IV, d.w.z. patiënten met een:
- belangrijke beperking in de dagelijkse activiteit door symptomen die zich al voordoen bij beperkte inspanning, zoals vermoeidheid en kortademigheid bij lopen van 20-100 meter. Alleen rust geeft comfort en in rust zijn er geen klachten (klasse III);
- ernstige beperking in activiteit door symptomen die al in rust ontstaan. Bij zeer geringe inspanning nemen de klachten in ernst toe (klasse IV).
Doelgroep
Deze richtlijn is bestemd voor alle professionals die betrokken zijn bij de zorg voor patiënten met hartfalen NYHA-klasse III en IV zoals huisartsen, specialisten ouderengeneeskunde, medisch specialisten (vooral cardiologen, internisten en klinisch geriaters), apothekers, verpleegkundigen, verpleegkundig specialisten, physician assistants, POHs (Praktijkondersteuners Huisarts), fysiotherapeuten, psychologen, maatschappelijke werkers, geestelijk verzorgers en andere bij de patiënt betrokken professionals.
Indien in de richtlijn wordt gesproken over zorgverleners rondom de patiënt met hartfalen, kunnen afhankelijk van de specifieke situatie van de patiënt alle bovengenoemde professionals bedoeld worden.
Samenstelling werkgroep
Alle werkgroepleden zijn afgevaardigd namens wetenschappelijke en beroepsverenigingen en hebben daarmee het mandaat voor hun inbreng. Bij de samenstelling van de werkgroep is geprobeerd rekening te houden met landelijke spreiding, inbreng van betrokkenen uit zowel academische als algemene ziekenhuizen/instellingen en vertegenwoordiging van de verschillende verenigingen/ disciplines. Het patiëntenperspectief is vertegenwoordigd door middel van afvaardiging van een ervaringsdeskundige (hartpatiënt) en een beleidsmedewerker van de Hart&Vaatgroep/Hartstichting. Bij de uitvoer van het literatuuronderzoek is een methodoloog/epidemioloog/literatuuronderzoeker betrokken.
Werkgroepleden
mw. dr. L. Bellersen, voorzitter, cardioloog, NVVC
mw. M.S.A. Aertsen, lid, verpleegkundig specialist, NVHVV en V&VN
mw. dr. Y.M.P. Engels, lid, universitair hoofddocent, Palliactief
dhr. J. van Erp, lid, Beleidsadviseur/patiëntvertegenwoordiger, Hart&Vaatgroep
dr. A. de Graeff, lid, internist-oncoloog, Palliactief
dr. M. van Leen, lid, specialist ouderengeneeskunde, Verenso
mw. dr. C.M.H.B. Lucas, lid, cardioloog, NVVC
mw. drs. C.W. Middeljans-Tijssen, lid, klinisch geriater, NVKG
dr. R.J.J.E.T. Starmans, lid, kaderhuisarts palliatieve zorg, NHG
drs. P.E. Polak, klankbordlid, cardioloog, NVVC
dhr. R. Tabak, klankbordlid, voorzitter PAR Radboud Health Academy, patiëntvertegenwoordiger Hart&Vaatgroep
Ondersteuning
mw. drs. M.G. Gilsing, adviseur (richtlijnen) palliatieve zorg, IKNL
mw. dr. O.L. van der Hel, literatuuronderzoeker, IKNL
dr. J. Vlayen, literatuuronderzoeker, ME-TA
mw. drs. A. van der Mei, secretaresse, IKNL
Belangenverklaringen
Om de beïnvloeding van de richtlijnontwikkeling of formulering van de aanbevelingen door conflicterende belangen te minimaliseren zijn de leden van de werkgroep gemandateerd door de wetenschappelijke en beroepsverenigingen.
Alle leden van de richtlijnwerkgroep hebben verklaard onafhankelijk gehandeld te hebben bij het opstellen van de richtlijn. Een onafhankelijkheidsverklaring ‘Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling' zoals vastgesteld door onder meer de KNAW, KNMG, Gezondheidsraad, CBO, NHG en Orde van Medisch Specialisten is door de werkgroepleden bij aanvang en bij afronding van het traject ingevuld. De bevindingen zijn schriftelijk vastgelegd in de belangenverklaring en opvraagbaar via info@iknl.nl.
Inbreng patiëntenperspectief
Twee patiëntvertegenwoordigers namen (via de Nederlandse Patiëntenfederatie en Hart&Vaatgroep) zitting in de richtlijnwerkgroep/klankbordgroep: een ervaringsdeskundige (hartpatiënt) en een beleidsmedewerker van de Hart&Vaatgroep/Hartstichting. De input van patiëntvertegenwoordigers is nodig voor de ontwikkeling van kwalitatief goede richtlijnen. Goede zorg voldoet immers aan de wensen en eisen van zowel zorgverlener als patiënt.
Door middel van onderstaande werkwijze is informatie verkregen en zijn de belangen van de patiënt meegenomen:
- Bij aanvang van het richtlijntraject hebben de patiëntvertegenwoordigers knelpunten aangeleverd.
- Via de Nederlandse Patiëntenfederatie en haar organisatielid de Hart&Vaatgroep is een enquête gehouden voor het inventariseren van de knelpunten.
- De patiëntvertegenwoordigers waren aanwezig bij de vergaderingen van de richtlijnwerkgroep.
- De patiëntvertegenwoordigers hebben de conceptteksten beoordeeld om het patiëntenperspectief in de formulering van de definitieve tekst te optimaliseren.
- De Nederlandse Patiëntenfederatie (met organisatielid de Hart&Vaatgroep) is geconsulteerd in de externe commentaarronde.
-
De Nederlandse Patiëntenfederatie (en daarmee de Hart&Vaatgroep) heeft ingestemd met de inhoud van de richtlijn.
Patiënteninformatie/een patiëntensamenvatting wordt opgesteld en gepubliceerd op de daarvoor relevante sites.
Methode ontwikkeling
Evidence based
Implementatie
Bevorderen van het toepassen van de richtlijn in de praktijk begint met een brede bekendmaking en verspreiding van de richtlijn. Bij verdere implementatie gaat het om gerichte interventies om te bevorderen dat professionals de nieuwe kennis en kunde opnemen in hun routines van de palliatieve zorgpraktijk, inclusief borging daarvan. Als onderdeel van elke richtlijn stelt IKNL samen met de richtlijnwerkgroep een implementatieplan op. Activiteiten en interventies voor verspreiding en implementatie vinden zowel op landelijk als regionaal niveau plaats. Deze kunnen eventueel ook op maat gemaakt worden per instelling of specialisme. Informatie hierover is te vinden op http://www.iknl.nl/. Het implementatieplan bij deze richtlijn is een belangrijk hulpmiddel om effectief de aanbevelingen uit deze richtlijn te implementeren voor de verschillende disciplines.
Werkwijze
Werkwijze
De werkgroep is op 5 juli 2016 voor de eerste maal bijeengekomen. Op basis van een door de werkgroepleden opgestelde enquête heeft een knelpuntenanalyse plaatsgevonden onder professionals en patiënten(vertegenwoordigers). Na het versturen van de enquête hebben 121 professionals en 3 patiënten gereageerd en knelpunten geprioriteerd en/of ingebracht. De meest relevante knelpunten zijn uitgewerkt tot 6 uitgangsvragen (bijlage 9).
Voor iedere uitgangsvraag werd uit de richtlijnwerkgroep een subgroep geformeerd.
Op basis van de uitkomsten van de enquête zijn de onderwerpen inschatten van de levensverwachting, advance care planning (ACP) en invloed van het starten en staken van medicatie (diuretica, ACE-remmers, ARB’s en bèta-blokkers) in de laatste levensfase uitgewerkt volgens de evidence based methodiek GRADE. Bij de beantwoording van deze uitgangsvragen verzorgde een (IKNL en externe) methodoloog het literatuuronderzoek. Dit betrof het uitvoeren van een systematische literatuursearch, het kritisch beoordelen van de literatuur en het verwerken van de literatuur in evidence tabellen. Daarnaast werd door de methodoloog een concept literatuurbespreking met bijbehorende conclusies aangeleverd voor deze uitgangsvragen. Vervolgens pasten de subgroepleden, na interne discussie met de methodoloog, de conceptliteratuurbespreking en conclusies aan en stelden overwegingen en aanbevelingen op.
De werkgroepleden raadpleegden voor de uitgangsvragen over palliatieve zorg en organisatie van zorg en communicatie de door hen zelf verzamelde relevante literatuur. Op basis hiervan hebben de werkgroepleden de literatuurbespreking, conclusies, overwegingen en aanbevelingen opgesteld.
De werkgroep heeft gedurende circa 7 maanden gewerkt aan de tekst van de conceptrichtlijn. Alle teksten zijn tijdens plenaire vergaderingen besproken en na verwerking van de commentaren door de werkgroep geaccordeerd. De conceptrichtlijn is op 20 juni 2017 ter becommentariëring aangeboden aan alle voor de knelpuntenanalyse benaderde wetenschappelijke, beroeps- en patiëntenverenigingen en de landelijke en regionale werkgroepen. Het commentaar geeft input vanuit het veld om de kwaliteit en de toepasbaarheid van de conceptrichtlijn te optimaliseren en landelijk draagvlak voor de richtlijn te genereren. Alle commentaren werden vervolgens beoordeeld en verwerkt door de richtlijnwerkgroep. Aan de commentatoren is teruggekoppeld wat met de reacties is gedaan.
De richtlijn is inhoudelijk vastgesteld op 28 november 2017. Tenslotte is de richtlijn ter autorisatie/accordering gestuurd naar de betrokken verenigingen/instanties.
Knelpunteninventarisatie
De uitkomsten van de knelpunteninventarisatie ziet u via onderstaande hyperlink:
Gegevens enquête professionals Richtlijn Palliatieve zorg bij hartfalen
Methode ontwikkeling
Elke module van de richtlijn bestaat uit een richtlijntekst. De teksten naar aanleiding van de uitgangsvragen zijn opgebouwd volgens het volgende vaste stramien: uitgangsvraag en aanbevelingen, literatuurbespreking, conclusies en overwegingen. De referenties zijn aangeleverd per module (of paragraaf) en de evidence tabellen staan in bijlage 11. De antwoorden op de uitgangsvragen (derhalve de aanbevelingen in deze richtlijn) zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek.
De uitgangsvragen 1, 3 en 6 zijn via de evidence based systematische methodiek uitgewerkt. Uitgangsvragen 2, 4 en 5 zijn zonder systematisch literatuuronderzoek uitgewerkt omdat de werkgroep verwachtte geen studies te vinden die antwoord geven op de vraag, specifiek voor de Nederlandse situatie.
De GRADE-methodiek
Uitgangsvragen 1, 3 en 6 zijn via de evidence based GRADE methodiek uitgewerkt.
Selectie
Naast de selectie op relevantie werd tevens geselecteerd op bewijskracht. Hiervoor werd gebruik gemaakt van de volgende hiërarchische indeling van studiedesigns gebaseerd op bewijskracht:
- Gerandomiseerde gecontroleerde studies (RCT's)
- Niet gerandomiseerde gecontroleerde studies (CCT's)
Waar deze niet voorhanden waren werd verder gezocht naar vergelijkend cohortonderzoek.
Critical appraisal
De kwaliteit van bewijs wordt weergegeven in vier categorieën: hoog, matig, laag en zeer laag. RCT's starten hoog en observationele studies starten laag. Vijf factoren verlagen de kwaliteit van de evidentie (beperkingen in onderzoeksopzet, inconsistentie, indirectheid, imprecisie, publicatie bias) en drie factoren kunnen de kwaliteit van de evidentie verhogen (sterke associatie, dosis-respons relatie, plausibele (residuele) confounding) (zie tabel 1).
Tabel 1. GRADE-methodiek voor het graderen van bewijs
|
Quality of evidence |
Study design |
Lower if * |
Higher if * |
|
High (4) |
Randomized trial |
Study limitations -1 Serious -2 Very serious Inconsistency -1 Serious -2 Very serious Indirectness -1 Serious -2 Very serious Imprecision -1 Serious -2 Very serious Publication bias -1 Likely -2 Very likely |
Large effect + 1 Large + 2 Very large Dose response + 1 Evidence of a gradient All plausible confounding + 1 Would reduce a demonstrated effect, or + 1 Would suggest a spurious effect when results show no effect |
|
Moderate (3) |
|
||
|
Low (2)
|
Observational study |
||
|
Very low (1) |
|
Algehele kwaliteit van bewijs
Omdat het beoordelen van de kwaliteit van bewijs in de GRADE-benadering per uitkomstmaat geschiedt, is er behoefte aan het bepalen van de algehele kwaliteit van bewijs. Zowel voor als na het literatuuronderzoek wordt door de richtlijnwerkgroep bepaald welke uitkomstmaten cruciaal, belangrijk en niet belangrijk zijn.
Het niveau van de algehele kwaliteit van bewijs wordt in principe bepaald door de cruciale uitkomstmaat met de laagste kwaliteit van bewijs. Als echter de kwaliteit van het bewijs verschilt tussen de verschillende cruciale uitkomstmaten zijn er twee opties:
- De uitkomstmaten wijzen in verschillende richtingen (zowel gewenst als ongewenste effecten) of de balans tussen gewenste en ongewenste effecten is onduidelijk, dan bepaalt de laagste kwaliteit van bewijs van de cruciale uitkomstmaten de algehele kwaliteit van bewijs;
- De uitkomstmaten wijzen in dezelfde richting (richting gewenst of richting ongewenst effecten), dan bepaalt de hoogste kwaliteit van bewijs van de cruciale uitkomstmaat dat op zichzelf voldoende is om de interventie aan te bevelen van de algehele kwaliteit van bewijs.
Tabel 2. Formulering conclusies op basis van kwaliteit van bewijs per uitkomstmaat
|
Kwaliteit van bewijs |
Interpretatie |
Formulering conclusie |
|
Hoog |
Er is veel vertrouwen dat het werkelijk effect dicht in de buurt ligt van de schatting van het effect. |
Er is bewijs van hoge kwaliteit dat... (Referenties) |
|
Matig |
Er is matig vertrouwen in de schatting van het effect: het werkelijk effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt. |
Er is bewijs van matige kwaliteit dat...
(Referenties) |
|
Laag |
Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
Er is bewijs van lage kwaliteit dat....
(Referenties) |
|
Zeer laag |
Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect. |
Er is bewijs van zeer lage kwaliteit dat.... (Referenties) |
|
Formulering algehele kwaliteit van bewijs: hoog/matig/laag/zeer laag |
||
Overwegingen en aanbevelingen
Aanbevelingen in richtlijnen geven een antwoord op de uitgangsvraag. De GRADE methodiek kent twee soorten aanbevelingen: sterke aanbevelingen of conditionele (zwakke) aanbevelingen. De sterkte van de aanbevelingen reflecteert de mate van vertrouwen waarin - voor de groep patiënten waarvoor de aanbevelingen zijn bedoeld - de gewenste effecten opwegen tegen de ongewenste effecten.
Formulering:
- Sterkte aanbeveling: Doe/geef/etc. (gebiedende wijs)
- Zwakke/conditionele aanbeveling: Overweeg te doen/te geven/etc.
Naast de evidence uit de literatuur (conclusies) zijn er andere overwegingen die meespelen bij het formuleren van de aanbeveling. Deze aspecten worden besproken onder het kopje ‘Overwegingen' in de richtlijntekst. Hierin worden de conclusies (op basis van de literatuur) geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van de conclusie(s) in combinatie met deze overwegingen.
Figuur 1. Van bewijs naar aanbeveling
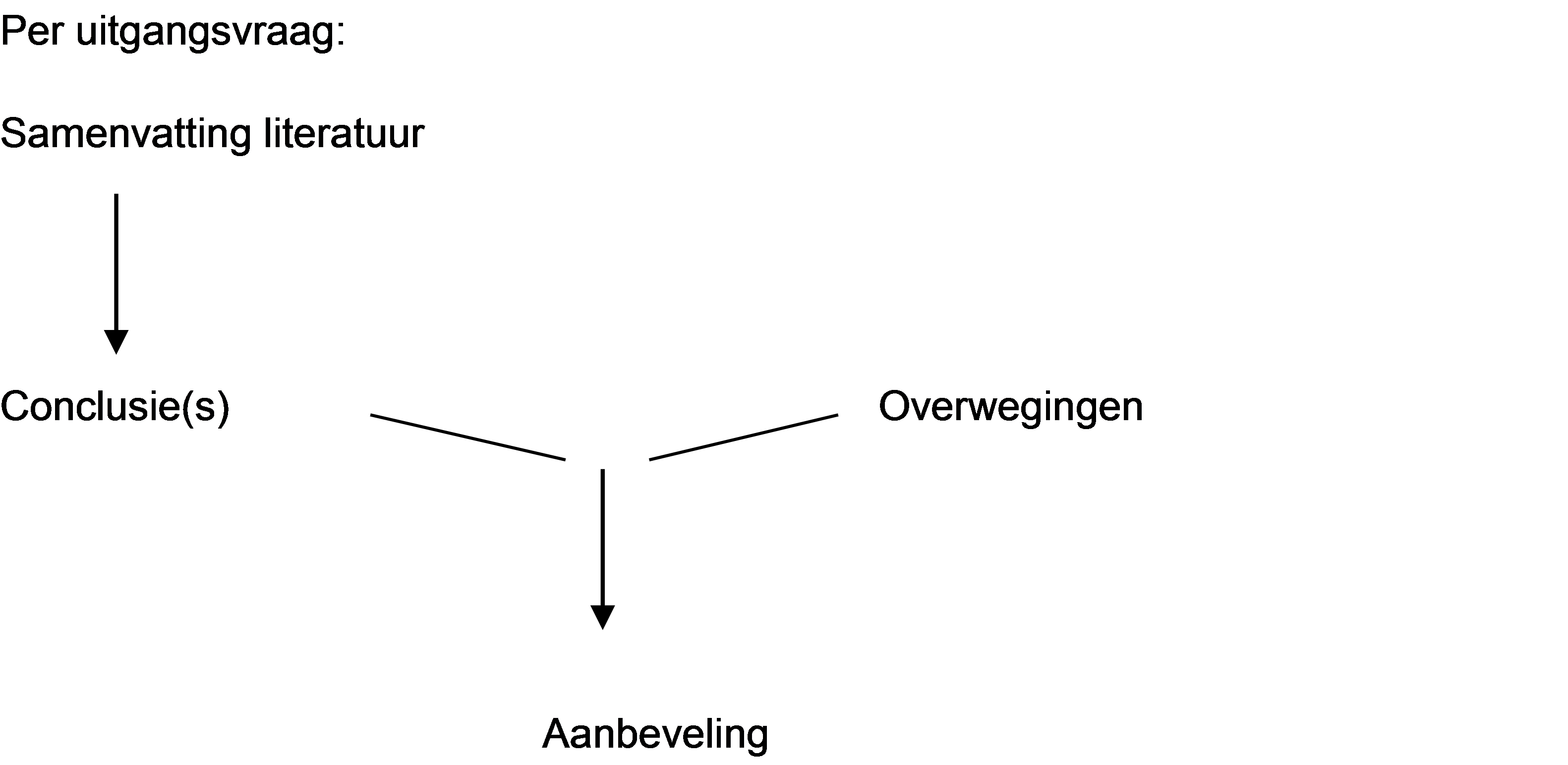
Bij de overwegingen kan men informatie kwijt over:
- veiligheid (bijvoorbeeld bijwerkingen, risico’s en complicaties);
- patiëntenperspectief (waarden en voorkeuren van de patiënt);
- professioneel perspectief (bijvoorbeeld tijdsbesparing);
- beschikbaarheid, werkbaarheid en wenselijkheid van organisatie van zorg aspecten: kosten, voorzieningen, coördinatie, communicatie, gegevensverwerking, taakverdeling, verantwoordelijkheden, etc.
- kosteneffectiviteit, besteed hierbij aandacht aan het perspectief (maatschappelijk perspectief versus gezondheidszorgperspectief).
Bij overwegingen kan men denken aan alle aspecten die niet vallen onder de systematische literatuuranalyse bij de uitgangsvraag maar wel van belang zijn bij het formuleren van de aanbeveling.
Methodiek bij de uitgangsvragen zonder systematisch literatuuronderzoek
Bij uitgangsvragen 2 (Wat is palliatieve zorg bij hartfalen?), 4 (Communicatie) en 5 (Organisatie van zorg) is geen systematisch literatuuronderzoek verricht omdat de werkgroep verwachtte geen studies te vinden die antwoord geven op de vraag, specifiek voor de Nederlandse situatie.
De aanbevelingen zijn uitsluitend gebaseerd op overwegingen die zijn opgesteld door de werkgroepleden op basis van kennis uit de praktijk en waar mogelijk onderbouwd door (niet systematisch) literatuuronderzoek.
De teksten zijn gebaseerd op evidence, maar de artikelen zijn niet methodologisch beoordeeld.
De overwegingen staan onder een apart kopje in de richtlijntekst. Hierin wordt de context van de dagelijkse praktijk beschreven en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties.
